Ytkemi (föreläsningar/bok)
1/105
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
106 Terms
Hur stor är en kolloid?
10 nm- 1µm
Olika dispersioner
Skum
Gas i vätska
Olika dispersioner
Fast skum
Gas i solid
Olika dispersioner
Aerosol
Vätska i gas
Olika dispersioner
Emulsion
Vätska i vätska
Olika dispersioner
Gel
Vätska i solid
Olika dispersioner
Fast aerosol
Fast fas i gas
Olika dispersioner:
Suspension
Fast fas i vätska
Olika dispersioner
Fast sol
Fast fas i fast fas
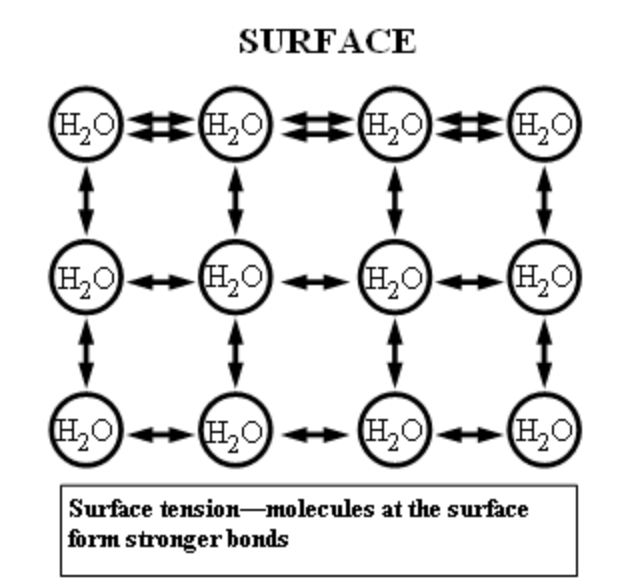
Vad är ytspänning?
Molekylerna i t.ex vatten binder till varandra med vätebindningar, vilket är starka intermolekylära krafter. Vid gränsytan med luft blir dessa molekyler påverkade av asymmetriska krafter som drar hårdare ned mot de andra vattenmolekylerna och varandra. Detta skapar som ett “skinn” mellan vattnet och luften.
Vad påverkas ytspänningen av?
Molekylstrukturen: hur starka intermolekylära krafterna är mellan molekylerna
Temperaturen: när den minskar, ökar ytspänningen
Addering av tillsatser: tvål (tensider) sänker ytspänningen
Varför har bensen lägre ytspänning än vatten?
Pga intermolekylära bindningar
Vatten har starkare sådana eftersom vatten är polär och skapar starka vätebindningar
Bensen är gjort av kol och väte och binder därför med svaga van der Waals bindningar istället. Dessa bindningar håller inte lika hårt i varandra vilket ger lägre ytspänning.
Varför har hexan lägre ytspänning än oktan?
Oktan är en längre molekyl och har därför chans till fler van der Waals bindningar mellan molekylerna än hexan.
Varför har kvicksilver så hög ytspänning?
Kvicksilver är en metall och binder därför med metallbindning vilket är mycket starkare krafter än vätebindningar.
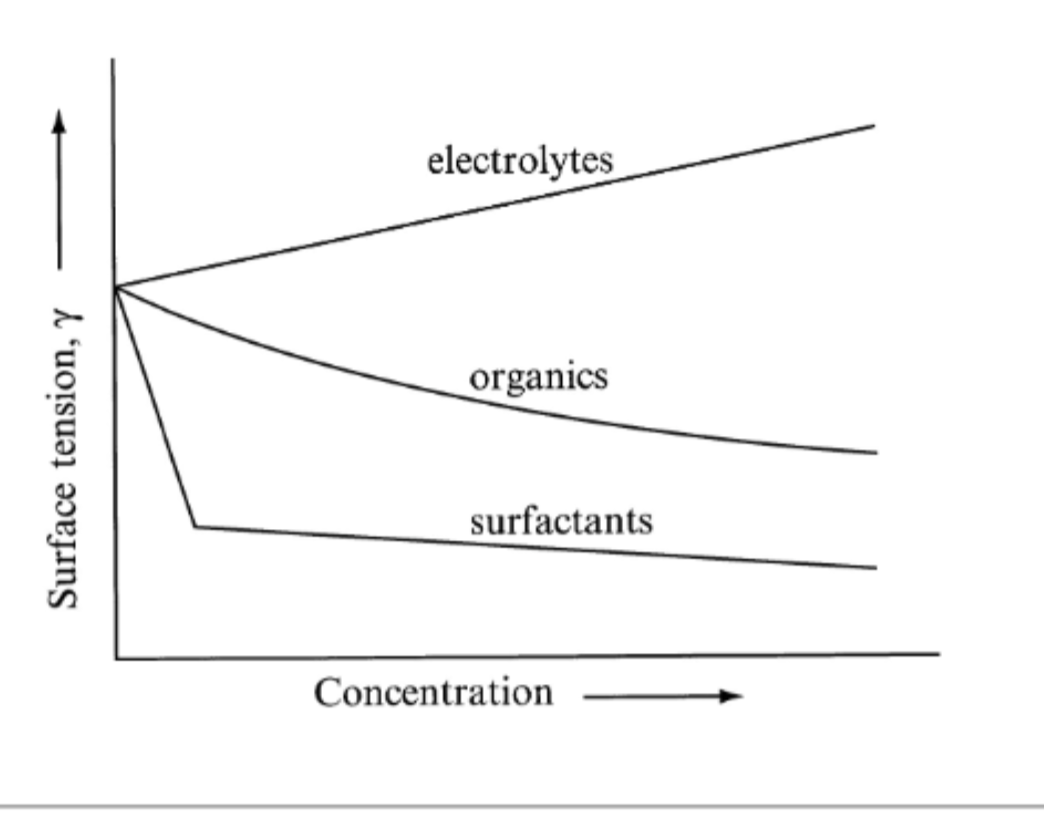
Hur påverkas ytspänningen av tillsatser
Det är olika för olika tillsatser
Elektrolyter: ytspänningen ökar
Organiska medel: minskar något
Tensider: minskar mycket
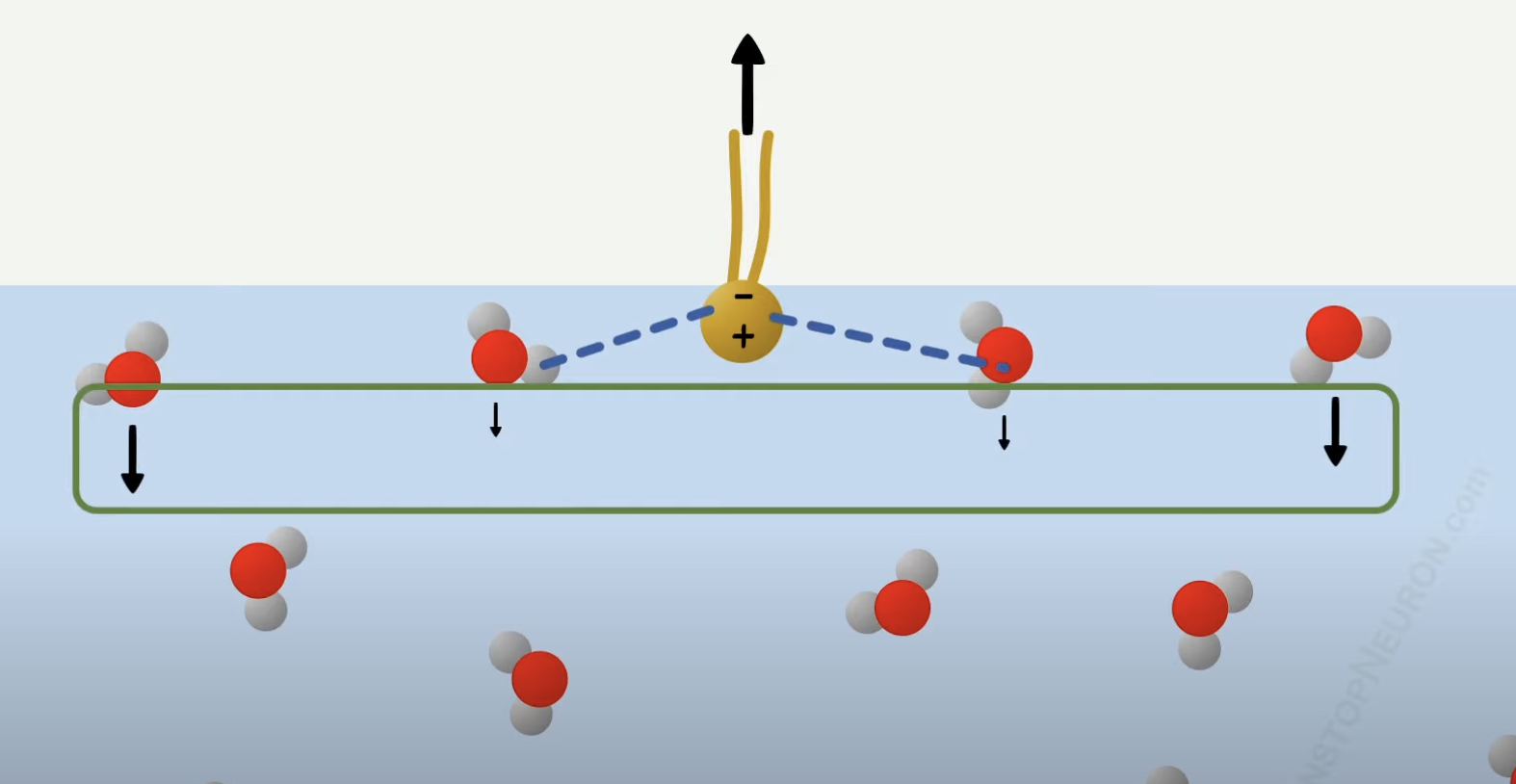
Varför minskar ytspänningen mycket av tensider?
Tensiderna som har ett polär huvud lägger sig på ytan av vätskan (t.ex vatten). Vid ytan minskar då densiteten av vattenmolekyler och ökar med tensider. Med färre vattenmolekyler minskar ytspänningen.
Tensiderna binder också till vattenmolekylerna vilket gör att deras resulterande kraft nedåt bli mindre. Fler tensider - mindre kraft.
Varför ökar ytspänningen med elektrolyter?
Elektrolyter, så som NaCl, är laddade och kan binda med vatten med jon-dipolbindningar vilka är starkare än vätebindningar.
Vad är gränsskiksspänning?
Det är som ytspänning fast mellan olika vätskor istället för vätska-luft.
Hur är en tensid uppbyggd?
Hydrofilt huvud (polär, vattenlösligt)
Hydrofob svans (opolär, oljelöslig)
Vad finns det för typer av tensider?
Anjonisk (SDS)
Katjonisk (CTAB)
Zwitterjonisk (CAPD)
Nonjonisk (C12E3)
Annat ord för tensid
ytaktiva ämnen
Vad står CMC för och vad händer då?
Kritisk micell koncentration, unimererna minskar och miceller bildas då det varit överskott av unimerer
Vad kan miceller ha för struktur?
Sfäriska
Stavformade
Polymerliknande
Dubbellager
Vesiklar
Reversed miceller
Vad bestämmer formen på micellerna?
Strukturen på tensiden
Koncentrationen av tensider; vid låga koncentrationer är de oftast sfäriska, sedan mer komplexa som dubbellager och stavformade
Tillsatser i vätskan kan påverka
Vad händer när tensider blandas?
??
Vad har ytaktiva polymerer för egenskaper?
associerar i lösning
ökad viskositet
komponent av färgskikt
skjuvtunnande
Vad är en suspension?
Vätska i vätska
Oftast vatten och organiskt ämne (W/O eller O/W)
Vad är en emulgator och vad gör den?
Det är ett ytaktivt ämne som säker gränsskiktsspänningen och underlättar sönderdelning.
Hur sker en emulsifikation?
Genom homogenisering - från fas till emulsion
Behövs mekanisk energi då emulsionen inte är termodynamiskt stabil.
Förklara Marangoni effekten
Masstransport som sker då det finns en gradient av ytspänning mellan två faser. En vätskemolekyl kommer då gå från låg ytspänning till hög ytspänning.
Exempel: om man tillsätter tvål till en vattenyta med peppar i kommer vattnet att dra med pepparkornen mot sidorna då tvålen rör sig mot den höga ytspänningen.
Nämn några olika stabiliseringar av emulsioner
Elektrostatisk
Sterisk
Tensid
Ytaktiv polymer
Osmos/entropi
Hur stabiliseras en emulsion av elektrostatiska krafter?
Tensider med laddningar kan finnas i emulsionen - anjoniska t.ex. Dessa fördelar sig vid gränsskiktet (olja-vatten) i ett dubbellager. Till exempel, i en vatten-i-olja-emulsion stabiliserad av anjoniska tensider skulle de negativt laddade tensidernas huvudgrupper bilda det inre lagret. Katjoner från vattenfasen skulle då utgöra det yttre lagret.
(Med katjoniska tensider blir det tvärtom)
Effekt av osmotiskt tryck- vatten strömmar till området för att jämna ut koncentrationen
Styrs även av entropi
Hur stabiliseras en emulsion av steriska hinder?
Genom att antigen tillsätta tensider eller polymerer till emulsionen. Svårt för dropparna att komma nära varandra då.
Effekt av osmotiskt tryck- vatten strömmar till området för att jämna ut koncentrationen
Styrs även av entropi
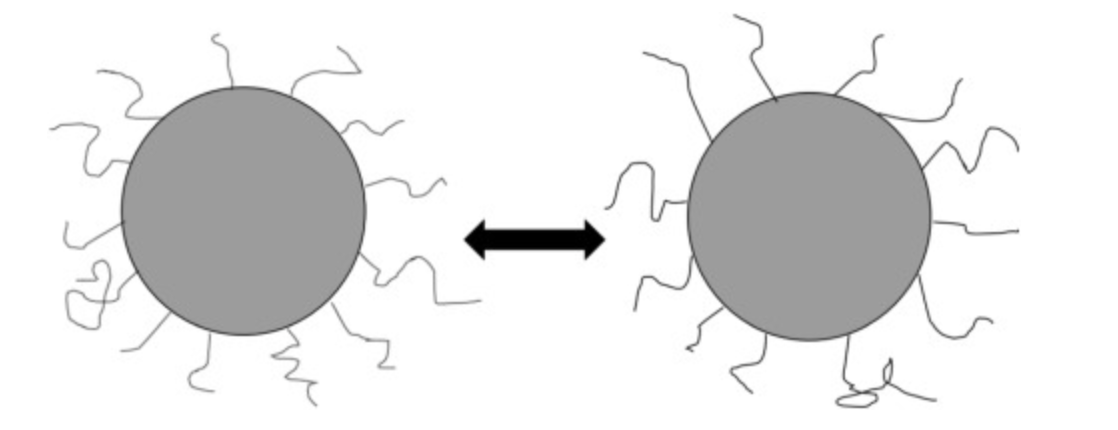
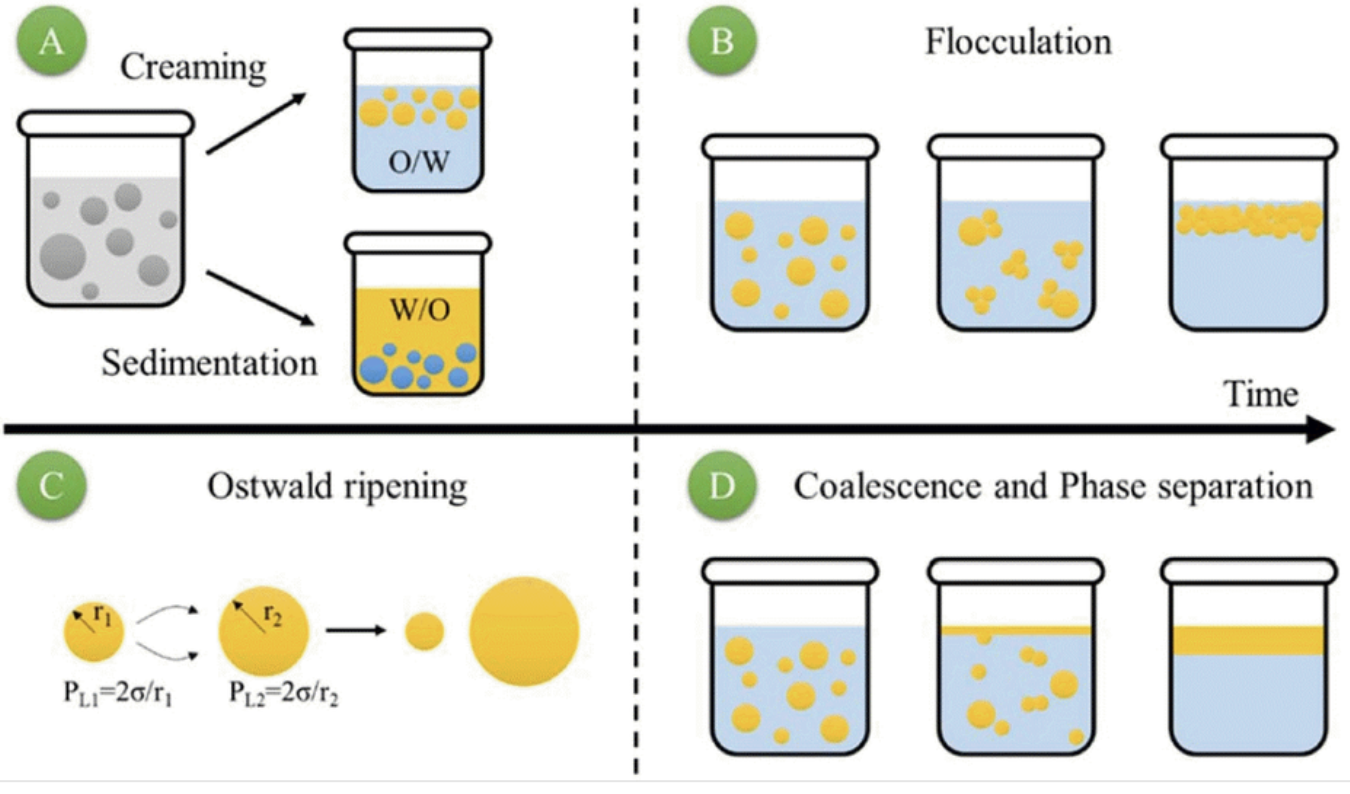
Beskriv flockuering.
Små partiklar i en dispersion eller suspension aggregerar eller klumpar ihop sig för att bilda större och tyngre partiklar. Sker vanligtvis när partiklarna kolliderar och bindningarna övervinner de avstötande krafterna.
Det är en reversibel process vid omrörning.
Beskriv koagulering.
Droppar i emulsionen flyter samman till större droppar - efter flockulering. Irreversibelt.
Beskriv gräddbildning/sedimentation.
Dropparna i emulsionen har lägre densitet än den kontinuerliga fasen - dropparna flyter på ytan. Om man ökar viskositeten (tillsätt polymer) på den kontinuerliga fasen med en polymer kan detta undvikas.
Beskriv Ostwaldmogning.
Beskriver en process där större droppar i en dispersion eller emulsion växer i storlek på bekostnad av de små dropparna. Det är molekyler på droppens yta som löses ut.
Vad är DLVO-teorin?
Beskriver den elektrostatiska stabiliteten för en emulsion.
Behandlar interaktionskrafterna mellan kolloidala partiklar i en dispersionsvätska
Attraktiva krafter: van der Waals
Repulsiva: Elektrostatiska krafter
Växelverkansenergin kan illustreras i ett diagram, se sidan 31. Över 0: repulsion (stabilisering), under 0: attraktion (instabilitet).
En emulsion med nonjoniska tensider. Temperaturberoende?
Ja,
Hög temp - W/O
Låg temp- O/W
Hur bryter man en emulsion? (stabiliserad av joniska tensider)
Addera salt som avskärmar laddningarna
Hur bryter man en emulsion? (stabiliserad av nonjoniska tensider)
Ändra temperatur och rör inte om.
Hur framställs en suspension?
Top-down: sönderdelning genom malning av stora partiklar
Bottom-up: kondensation - nödvändigt för små partiklar (nm) så som silkia
Storlek på mikroemulsion
Nanometer
Skillnad mellan mikroemulsion och emulsion?
Mikroemulsion:
Olja, vatten och tensid
Termodynamiskt stabil
Enfassystem
Spontanformation
Hög dynamik
Små aggregat
3-100 nm
Stor gränsyta
Hög kurvatur
Emulsion:
Olja, vatten och tensid
Termodynamiskt instabil (kommer separera)
Tvåfassystem
Kräver homogenisering (mekanisk kraft)
Låg dynamik
Stora aggregat
0,1 - 1 mikrometer
Liten gränsyta
Låg kurvatur
Varför är mikroemulsioner bra för tillämpningar?
Löser både polära och opolära substanser
reaktanter som normalt inte är lösliga i samma lösningsmedel kan komma i kontakt och reagera.
Har en stor och aktiv yta för reaktioner
Kan styra storleken och formen
Tar sig igenom porösa material
Obegränsad lagringsstabilitet
Tillämningar för mikroemulsioner
Organisk syntes
Hantera inkompabilitetsproblem mellan reaktanterna
Katalysera reaktioner
Åstadkomma regioselektivitet
Nanopartikelsyntes
Reverse system
Städning
Hur ser en vesikel ut? Är den större än en micell?
En vesikel är gjord av ett bilager av tensider i en sfär.
Större än miceller.
Olika typer av skum.
Instabila
T.ex. sparkling drycker, bara vätska när gasen försvinner
Metastabila, ultrastabila
T.ex. grädde, raklödder
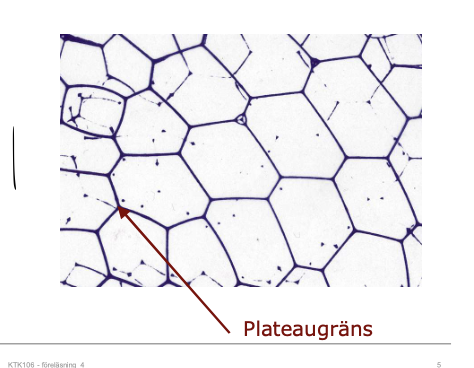
Hur ser ett koncentrerat skum ut?
Sfärerna försvinner då de är energikrävande
Plateaugränsen har lägre Laplace tryck än de tunna (blå) lamellerna.
Vad är det för krafter som agerar på skum? Vilka är bra och vilka är dåliga för skummets stabilitet?
Bra
Marangonieffekten
Laddningsrepulsion vid gränsytor
Dåligt
Tryckskillnaden inom kontinuerlig fas (lameller och Plateau)
Tryckskillnad mellan bubblor av olika storlek
Gravitationen
Varför är “Tryckskillnaden inom kontinuerlig fas (lameller och Plateau)” en destabiliserande kraft för skummet?
När tryckskillnaden inom den kontinuerliga fasen är för hög kan det leda till en snabbare dränering av vätska från filmerna, vilket gör att skummet destabiliseras och kollapsar. Omvänt, om tryckskillnaden är för låg, kan vätskefilmerna bli för tjocka och skummet kan bli instabilt.
Varför är “Maragonieffekten” bra för skummet?
Reglerar hastigheten på vätskedränering från de tunna vätskefilmerna som separerar gasbubblorna i skummet. De är oftast tjockare vid Plateau-gränserna och tunnare vid lamellerna.
Skillnaden i ytspänning mellan dessa regioner skapar en ytspänningsgradient.
Denna gradient inducerar konvektionsflöde, vilket i sin tur påverkar dräneringen av vätska.
Ytaktiva ämnen kan sänka vätskans ytspänning. När ytaktiva molekyler förflyttas från områden med hög ytspänning till områden med lägre ytspänning kan Marangonieffekten få tensiderna att ackumuleras vid Plateau-gränserna.
Detta stärker effektivt de tunna filmerna vid dessa gränser och gör dem mer motståndskraftiga mot dränering.
Varför är “laddningsrepulsion mellan gränsytorna” bra för skummets stabilisering?
De gör att bubblorna repellerar från varandra.
Minskar tendensen för dränering
Tensiderna, eller andra molekyler som hittas i gränsytorna, kommer närmare varandra när lamellerna krymper vid dränage. Det leder till mer repulsion mellan molekylerna och hindrar ytterligare dränage
(Uppnås genom att tillsätta laddade joner eller ytaktiva polymerer/tensider)
Varför är “tryckskillnaden mellan bubblor av olika storlek” dåligt för skummets stabilitet?
Bubblorna blir färre, större och mer jämnstora
Laplace-trycket är direkt beroende av bubbelstorleken. Små bubblor har högre Laplace-tryck än stora bubblor med samma vätska och ytspänning. Detta beror på att ytan hos små bubblor är böjd i en högre grad jämfört med stora bubblor.
- Om Laplace-trycket är positivt, kommer det att motverka dränering och behålla filmens tjocklek.
En stor bubbla har en tendens att skapa ett positivt Laplace-tryck på en mindre bubbla, vilket resulterar i en tryckskillnad som driver gas från den större bubblan till den mindre. Detta kan leda till att stora droppar växer på små droppars bekostnad. - Ostwaldmogning
Skumdämpare (defoamers), hur fungerar de och ge exempel.
De stör tensidpackningen.
Alkohol t.ex oktanol
Hydrofoba oljor skapar tunn film
Vad kan skum användas till?
Brandskum
Skum för isolering
Mineralflotation
Vad innebär vätning?
Processen då en vätska sprider sig över
en annan vätska eller över en fast yta
Förklara vad kontaktvinkeln är? (vätning)
Vinkeln mellan vätskan, ytan och gasen (luft oftast)
om vinkeln är 0: fullständig vätning
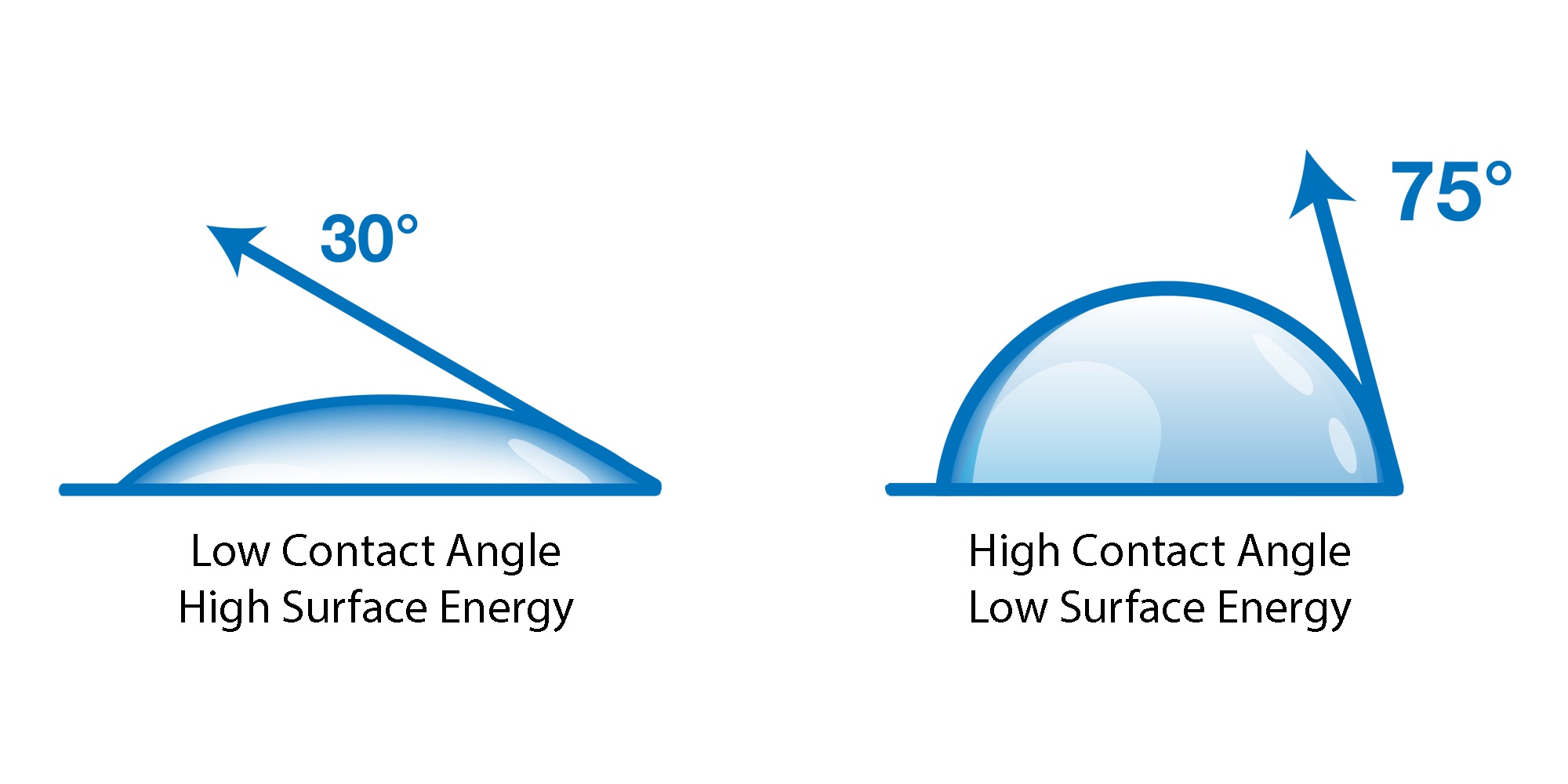
Spontan vätning sker när ..
γ(solid-air)>γ(solid-water)+γ(water-air)
Vad är kohesion?
Attraktiva krafter mellan molekyler av samma ämne
Vad är adhesion?
Attraktiva krafter mellan molekyler av olika ämnen
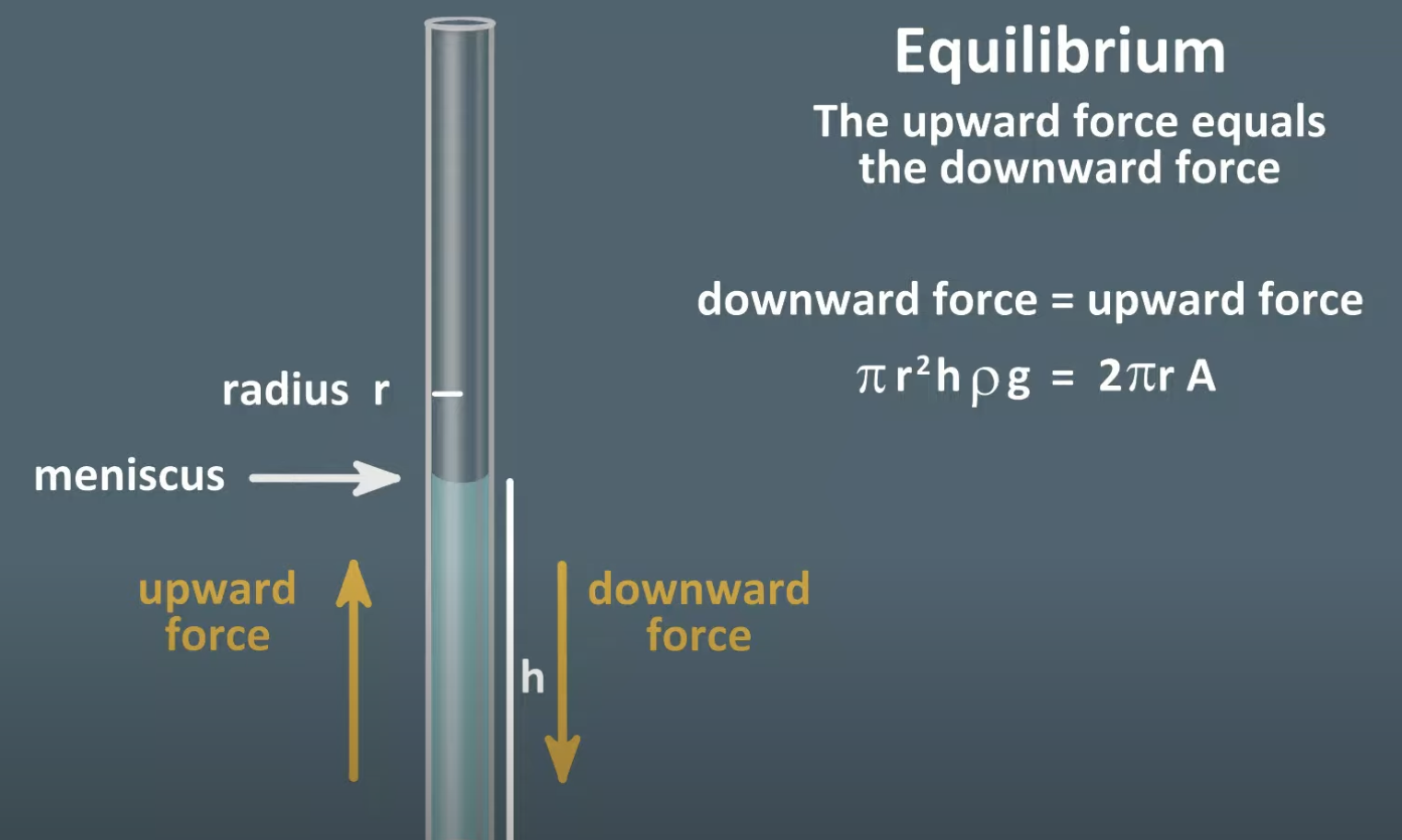
Hur fungerar kapilläreffekten?
En vätska är i en bägare, om en liten tub sätts i vätskan kommer vätskan att åka upp något i tuben.
De adhesiva krafterna gör att vätskan åker upp och skapar en menisk då vätskan attraheras av väggarna. De kohesiva krafterna drar ned vätskan med gravitationen.
När radien på tuben ökar, ökar de kohesiva krafterna enligt ekvationen.
Varför blir en menisk konvex eller konkav
Konvex (vatten): adhesiva krafter finns och är relativt starka
Konkav (kvicksilver): har inga adhesiva krafter
Tillämpningar för kapilläreffekten
Tunnlagers-kromatografi
små blod vessles
blodanalys
vattentransport i växter och jord
Servetter, blöjor
Kapillär effekt i porösa material: Kapillaritet är viktigt i material som pappershanddukar, svampar och jord, där det hjälper till att fördela och absorbera vätskor effektivt.
Bläckpennor: Kapilläreffekten drar bläck från reservoaren till pennans spets.
Blodflöde i kapillärer: Kapillärer i det cirkulatoriska systemet använder kapillär effekt för att underlätta utbyte av syre, näringsämnen och avfallsprodukter mellan blod och omgivande vävnad.
Ytmätning: Kapillär stigning kan användas för att mäta ytförspänning i en vätska.
Lite förtydlingar
Coating
Paint
Color
Ytbeklädnad (kan vara färglöst)
Färg som i målarfärg
Färgen på målarfärgen
Vad används färg för?
Skydda ett material
Ändra egenskaperna på ytor
Estetik
Vilka 4 grejer består färg av?
Pigment
Bindemedel
Lösningsmedel
Tillsatser
Typer av pigment
Organisk eller oorganiskt
Typer av bindemedel
Solubiliserat eller dispersed
Typer av lösningsmedel (färg)
Organisk eller vatten
Typer av tillsatser i färg och vad de gör
De ger egenskaper
Förtjockningsmedel (polymer)
Shear thinner (polymer)
Vätmedel (tensid)
Skumdämpare (tensid)
Dispergeringsmedel (tensid)
Biocider (Antibateriell substans)
Konserveringsmedel
Behöver fillers (Kalciumkarbonat) blir så dyrt annars
Vad är bindemedel gjort av. Ge några exempel.
Polymerfilm och pigment
Låg MW: behöver cross-linking
Hög MW: behöver inte cross-linking
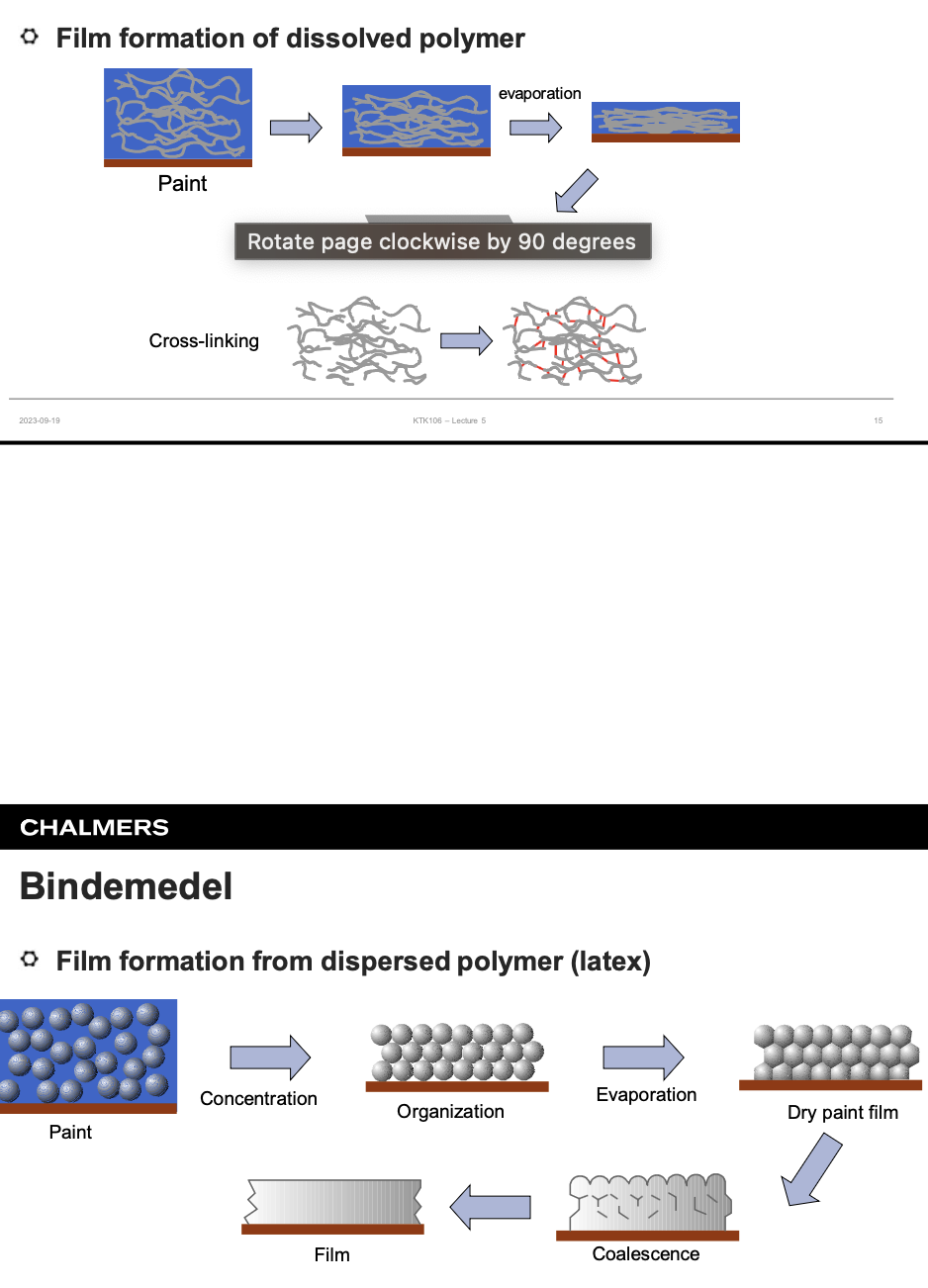
Hur ser utvecklingen ut för vattenbaserad färg då det målas till att det torkat
Det är först polymerer i vatten och polymererna organiserar sig och vattnet avdunstat, polymererna koagulerar och en film har skapats.
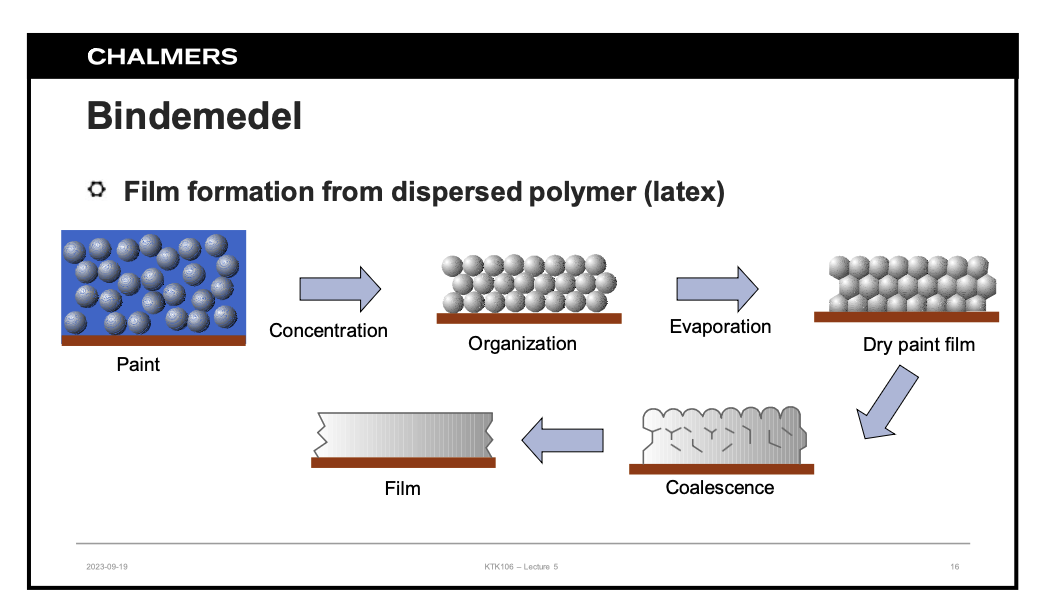
Hur bildas bindemedlet (binder)?
Via emulsionspolymerisation
Manomerer polymeriseras mha initiator - skapar miceller
Tensider stabiliserar
Varför är inte “vattenlöslig färg” korrekt?
oftast är både bindemedel och pigment dispergerade, inte upplösta
Vad är den hydrofoba effekten
Den hydrofoba effekten uppträder när hydrofoba ämnen i en vattenlösning försöker minimera sin kontakt med vattenmolekyler. (formning av miceller t.ex.)
Drivkraften för separation och adsorption.
Ett viktigt exempel är hur proteiner veckar sig i rätt struktur.
när bildar tensiderna dubbellager miceller?
När huvudet lika stort som svansen. Svansarna mot varandra och huvudet mot vattnet.
När bildar tensiderna vesiklar?
Låga tensidkoncentrationer → tvåfassystem där lamellär flytande kristallin fas står i jämvikt med vatten.
De innehåller vatten i sitt inre.
Dubbelskikt av tensider i en sfär.
När bildar tensider omvända miceller?
Mycket bulkig svans och litet huvud.
Är miceller ytaktiva?
Nej
vilka tensider har en större strävan att bilda miceller och varför?
Nonjoniska vill bilda miceller mer. Drivkraften för bildandet av miceller: strävan att avlägsna tensidens hydrofoba svans från vattnet OCH strävan att motjonerna ska vara så utspridda som möjligt.
nonjoniska tensider har inga motjoner
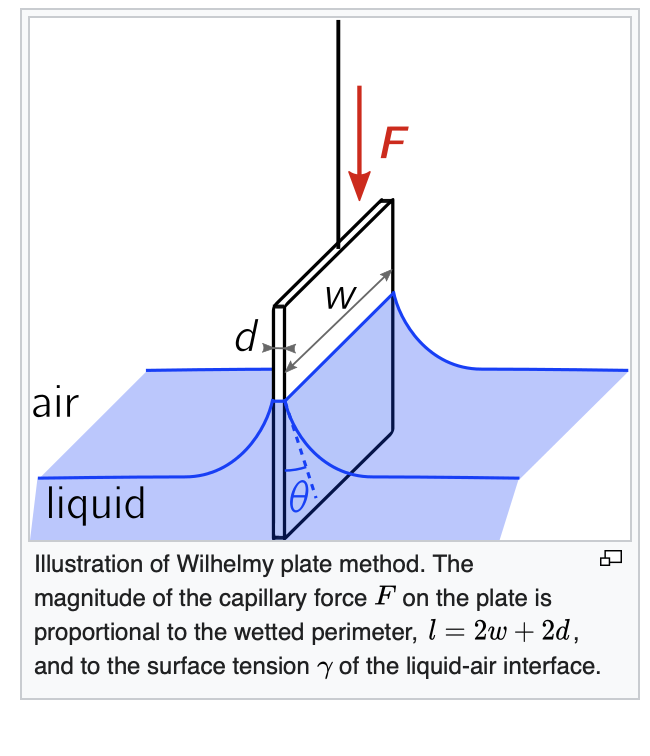
Metoder för att mäta ytspänningen!!
Wilhelmy plate: Denna metod innebär att man sänker ner en tunn platta (oftast en glasplatta) i en vätska och mäter kraften som krävs för att dra upp plattan ur vätskan. Skillnaden i kraft före och efter doppning i vätskan ger information om ytspänningen. Mer kraft → mer ytspänning
DuNouy ring: Här används en Du Nouy-ring (platinaring), som sänks ner i vätskan och sedan lyfts upp igen. Den kraft som krävs för att lyfta ringen ur vätskan mäts, och detta ger information om ytspänningen.
Varför har anjoniska och katjoniska tensider höga värden på CMC? hur kan detta kringgås?
Det är entropimässigt ogynnsamt att ha en hög koncentration av motioner samlade runt micellen.
Om man blandar anjoniska och katjoniska tensider kommer miceller bildas med båda motjonerna →kontakten mellan två laddningar av samma slag undviks.
Beskriv filmbildning för oljebaserad färg respektive vattenbaserad färg
Oljebaserd: Polymererna ordnar sig och sen avdunstar för att härda på ytan. Kan vara ett crosslinking steg också
Vattenbaserad: organiserar sig, vattnet avdunstar, de coaliserar och sen färg
Varför är mikroemulsioner nästan klara lösningar?
En mikroemulsion består av domäner med storlekar långt under ljusets våglängd - 5-10nm
Hur används mikroemulsioner i bildning av nanopartiklar
Blandar två mikroemulsioner av W/O-typ. Den ena innehåller Reaktant 1 (platinasalt i dropparna) och den andra har Reaktant 2 (reduktionsmedel, NaBH4) i dropparna. Den snabba dynamiken i mikroemulsionerna gör att reaktanterna kommer mötas. Platinajonerna reduceras till metalliskt platina.
Men vilken hastighet sker gräddbildning? Hur undviks gräddbildning
V= delta densitet d^2 g/ 18 * viskositet
minska densitetsskillanden
minska droppens diameter
öka viskositet (tillsätt polymer)
När är den kolloidiala kraften dominerande för systemets uppförande och när tar gravitationskraften över allt mer i dispersioner?
Då diametern på den dispersa fasen är < 1 *10^(-6)m = kolloidiala krafterna. Större --> gravitationskraften tar över allt mer.
Vad innebär en hög ytaktivitet?
Om en tensid har en hög ytaktivitet innebär det att den har en hög drivkraft att dras till gränsytor. Dvs den har ett lågt CMC, tensiden fungerar i låga koncentrationer.
Vad är motjonskoncentration? Och varför kan man inte uppnå en 100%-ig motjonskoncentration?
Motjonskoncentrationer beror på mängden motjoner runt micellen, ligger ofta på 60-80%. Antalet motjoner runt micellen är alltså mindre än antalet sulfatgrupper på ytan. Resten finns ute i bulkfasen. Det är överskottet av negativa laddningar som utgör micellens verkliga laddning. Anledningen till att man inte får en 100%-ig koncentration beror på att det är entropimässigt ogynnsamt att ha alla motjoner liggande runt micellens yta, alltså en balans mellan strävan att avlägsna tensidens hydrofoba svansar från vattnet, vilket gynnar micellbildningen, och strävan efter att ha motjonerna skall vara så utspridda som möjligt.
Varför sänks CMC i en blandning med två typer av tensider?
Då en lösning innehåller två typer av tensider så kommer dessa miceller att innehålla båda typer av tensider. Dessa kommer att lägga sig alternerande så att kontakten mellan två laddningar av samma slag undviks. Genom att micellens yta består av ungefär lika mycket negativa som positiva laddningar så kommer antalet motjoner, den entropimässigt ogynnsamma ansamlingen, att bli litet och inget problem. Det resulterar i att CMC för blandningen sänks kraftigt.
Vad innebär "konceptet" pseudoplastiskt eller skjuvförtunnande?
Då man rör om i en lösning med ytaktiva polymerer och bryter nätverket av hydroba svansar --> viskositeten sjunker. Detta reologiska beteende kallas pseudoplastiskt eller skjuvförtunnande.
Vad händer om man blandar en ytaktiv polymer med en tensid?
Kan bildas aggregat, vilka i viss mån påminner om de blandmiceller som bildas av olika typer av tensider. Dessa kan leda till en utpräglad viskositetsuppgång. Tensiden förstärker den växelverkan mellan polymerkedjorna som uppstår då polymerens hydrofoba svansar kommer samman.
Varför är det fördelaktigt med en tensid som har ett lågt CMC?
Om en tensid har ett lågt CMC innebär det att den ogärna befinner sig som fria unimerer i en lösning, detta i sig gör att den drar sig till gränsytor redan vid låga koncentrationer. Att en tensid då har ett lågt CMC indikerar på att den uppvisar hög ytaktivitet, vilket är önskvärt.
Beskriv polymer- tensidväxelverkan:
Inledningsvis kommer tensiden att gå till gränsytorna för att sänka spänningen. Vid en viss koncentration, CAC, kommer tensiden att börja att växelverka med polymeren och bilda aggregat. Ytspänningen ligger då vid en konstant nivå. När polymeren är mättad så kommer tensiderna att fortsätta att gå till gränsytorna.
Vad finns det för olika typer av stabiliseringar när det gäller emulgatorer?
Om tensiden är jonisk --> elektrostatisk stabilisering: en positivt eller negativt laddad tensid sätter sig runt dropparna (drar sig till gränsytan). Då kommer motjoner att dra sig mot dropparna. Då dropparna närmar sig varandra kommer man att få en hög koncentration av motjoner --> vatten strömmar till för att utjämna koncentrationen (drivkraften bakom det osmotiska trycket är att utjämna koncentrationen).
Nonjonisk tensid --> sterisk stabilisering: dropparna stabiliseras av polymerkedjor som fäster på ytan. Likaså här så bildas en hög koncentration av polymerkedjor, entropimässigt ogynnsamt --> osmotiska trycket gör att vatten strömmar till. Även partiklar kan användas.
Ofta används en blandning av joniska och nonjoniska tensider --> mer stabil.
Varför tillsätts en emulsionsstabilisator till en emulsion då den redan innehåller en emulgator?
En emulgator "stabiliserar" (ej termodiynamisk stabilisering) via elektrostatisk eller steriskt och gör att det inte sker koalescens, men stabiliteten räcker ofta inte till. Därför tillsätts en emulsionsstabilisator. Här är polymerer lämpade. De anrikas i gränsytan, de vänder hydrofob del in i oljan och den hydrofila ut i vattnet. De stora polymersegmenten gör det svårt för dropparna att komma nära varandra. Mer effektiva än tensider då de inte är dynamiska utan sitter där de sitter (trots att de är långsammare).
Vad innebär det primära och sekundära minimumet i DLVO-kurvan och vad innebär Born-repulsionen?
Det primära minimat är då man har stor attraktion, sker på kort avstånd, det sekundära minimat kommer vid längre avstånd. Där emellan finns ofta en höjning --> repulsion. Born-repulsionen är den nästintill vertikala delen vid kort avstånd som uppstår då det kommer en stor repulsiv kraft. Elektronmolnen hos atomerna i partiklarna kommer nära varandra.
Vad sker vid fasomvandling av en mikroemulsion, i jämförelse med en emulsion?
Den sker gradvis, det finns alltså periodvis en blandning av O/W och W/O. För emulsioner sker det abrupt. Med nonjonisk tensid kan gasomvandling ske genom temperaturhöjning.
Hur går en emulsionspolymerisation till?
Latex är den produkt som tillverkas genom emulsionspolymerisation.
Man har en emulsion, dropparna innehåller monomerer, dropparna är stabiliserade av en blandning av anjoniska och nonjoniska tensider, överskott av tensider --> tensidmiceller.
Monomeren är vattenlöslig vilket gör att en liten del befinner sig i vattenfasen.
En initiator tillsätts och polymerisationen sätts igång i vattenfasen.
När oligomerena är tillräckligt stora kan de senare hamna i monomerdropparna eller i micellerna. De hamnar i micellerna --> sväller. Man kan säga att man har en emulsion av monomerer i vatten. Alltså monomerer vandrar från emulsionsdroppar genom den kontinuerliga fasen till de svullna micellerna. Reaktionen slutar sedan och produkten som bildats är en dispersion av polymerpartiklar i vatten, latex. Är stabiliserad av elektrostatisk och sterisk stabilisering.