P-C
1/35
Earn XP
Description and Tags
Chap.7: De la structure à la polarité de la molécule
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
36 Terms
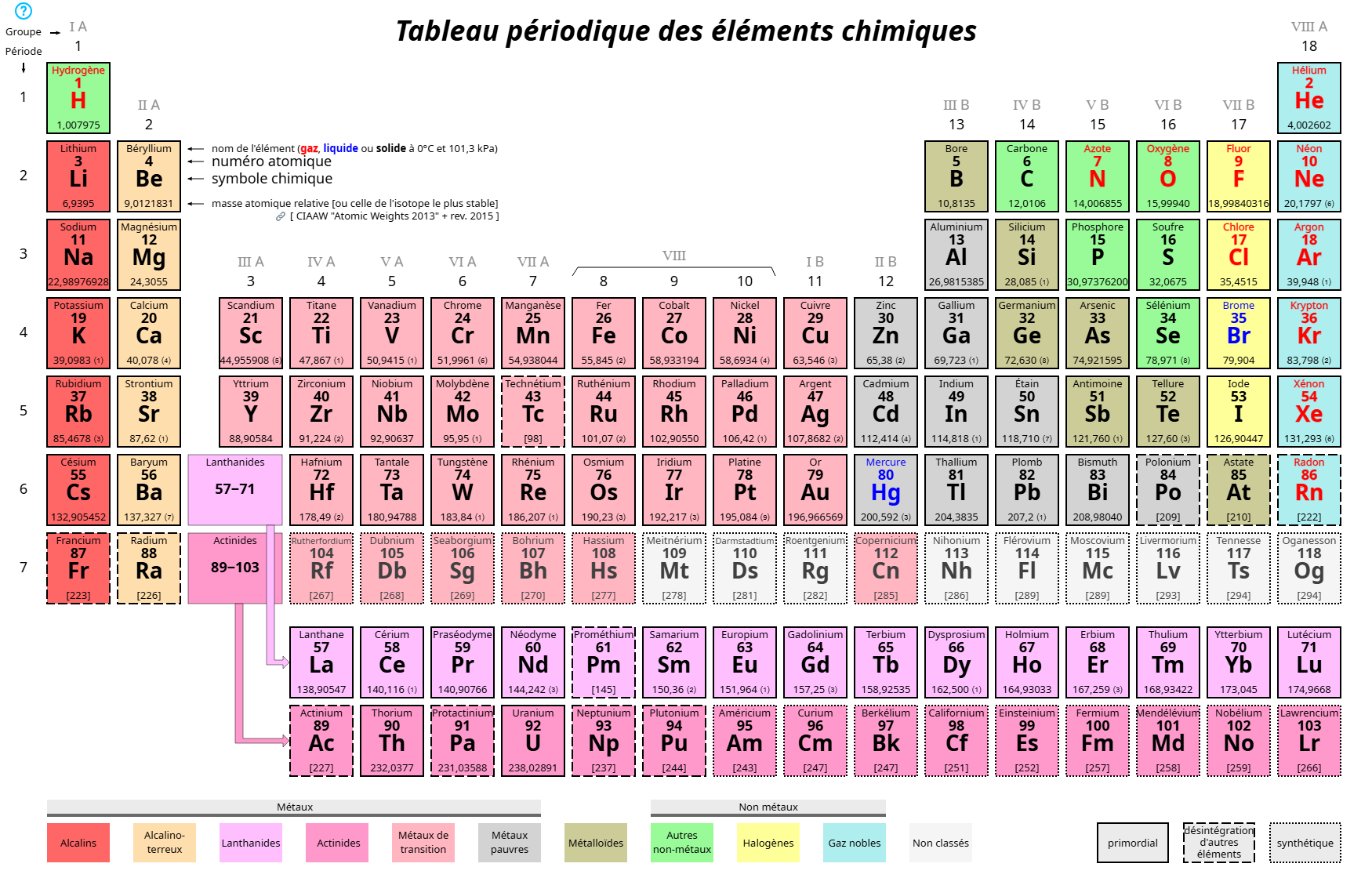
Nom des 2 1ers et dernières colonnes
2 1ers: Alcalins et alcalino terreux
2 derniers: Halogènes et gaz nobles
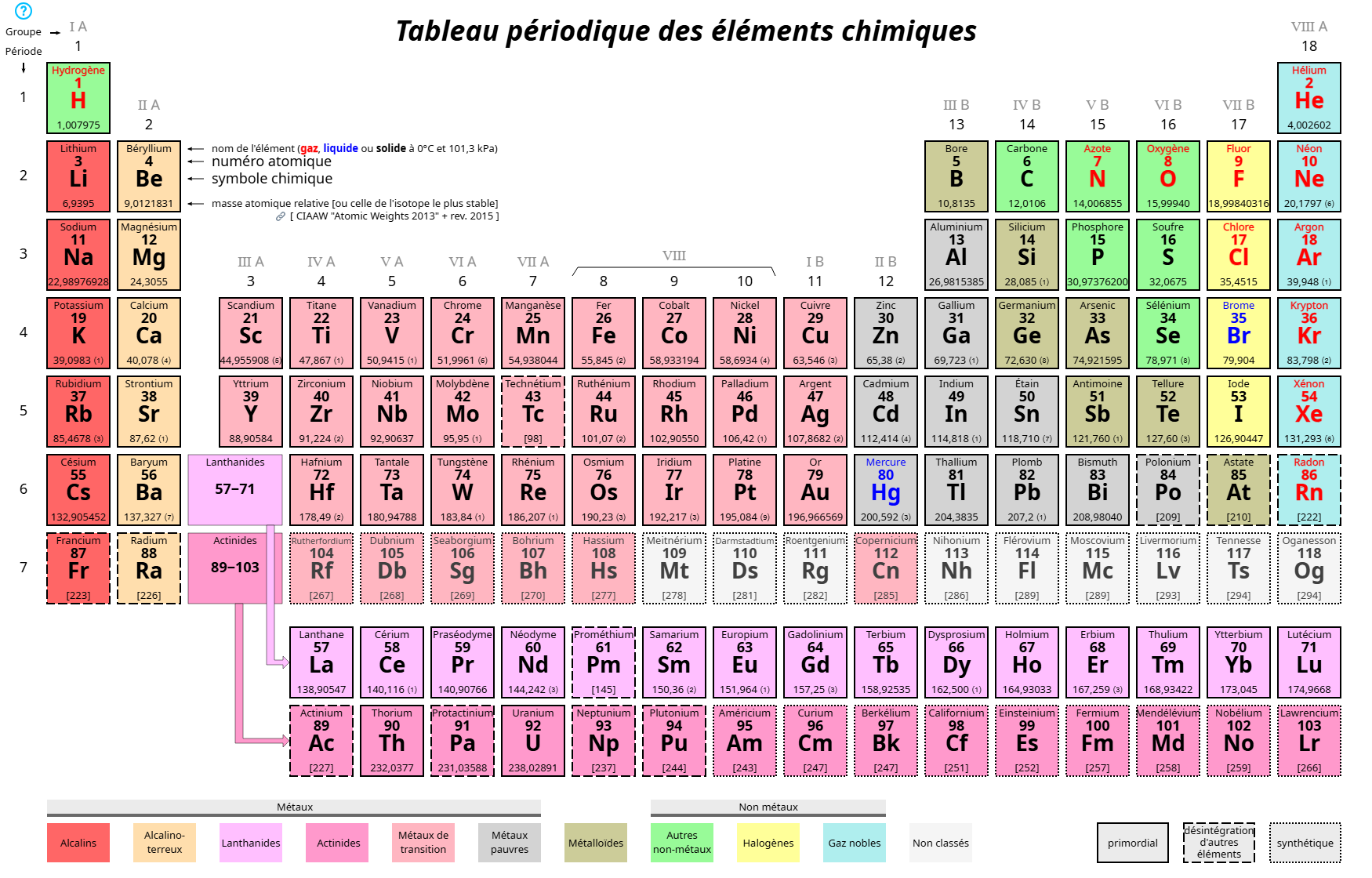
Propriété de chaque colonne concernant électrons de valence
Gaz nobles 8 electrons de valence (sauf Hélium = 2) et diminue en avancant
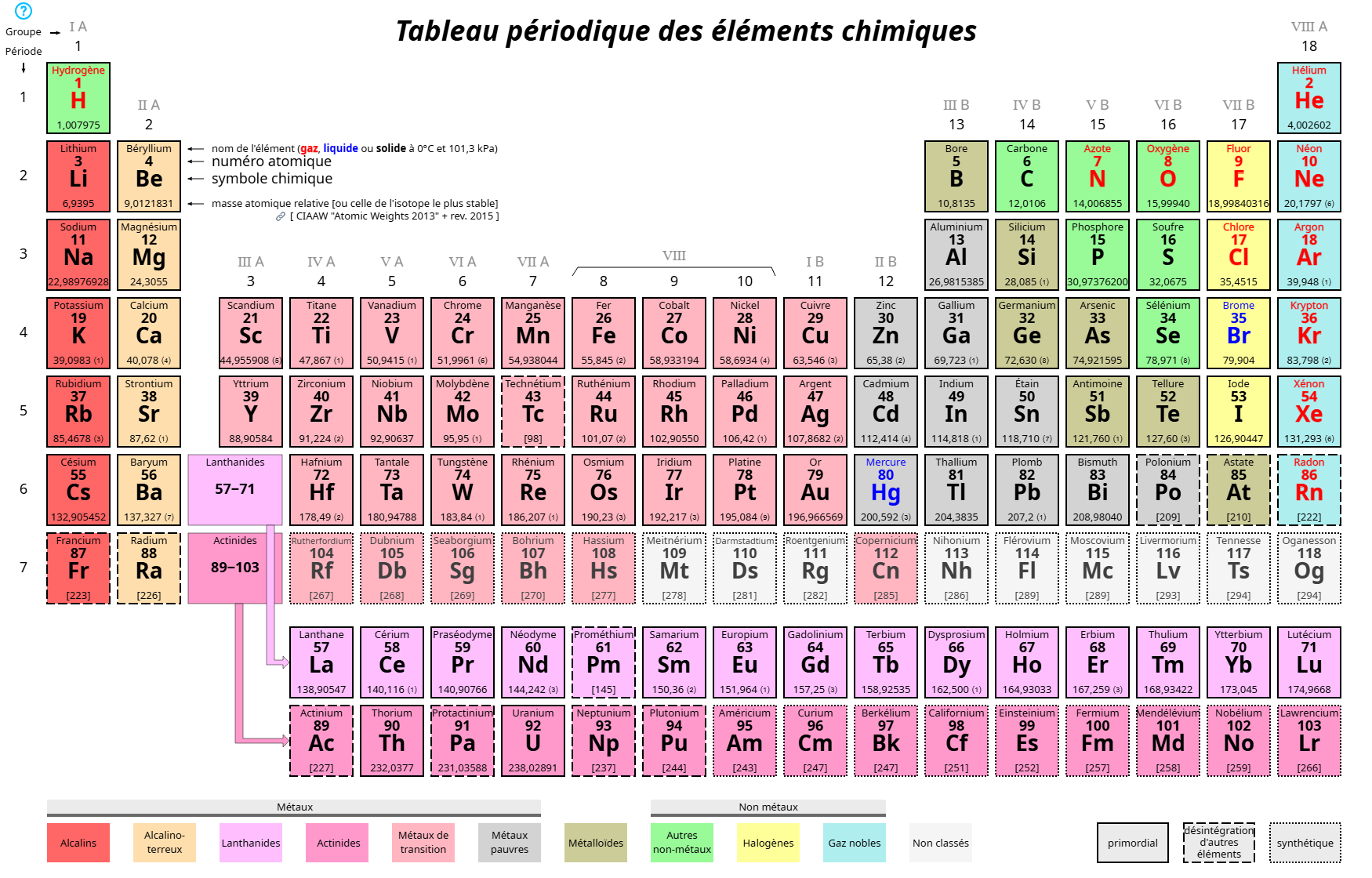
Pour gagner en stabilité, comment les atomes ils font
se transformer en ion(+/- e)
ou
liaisons valence ds moléc
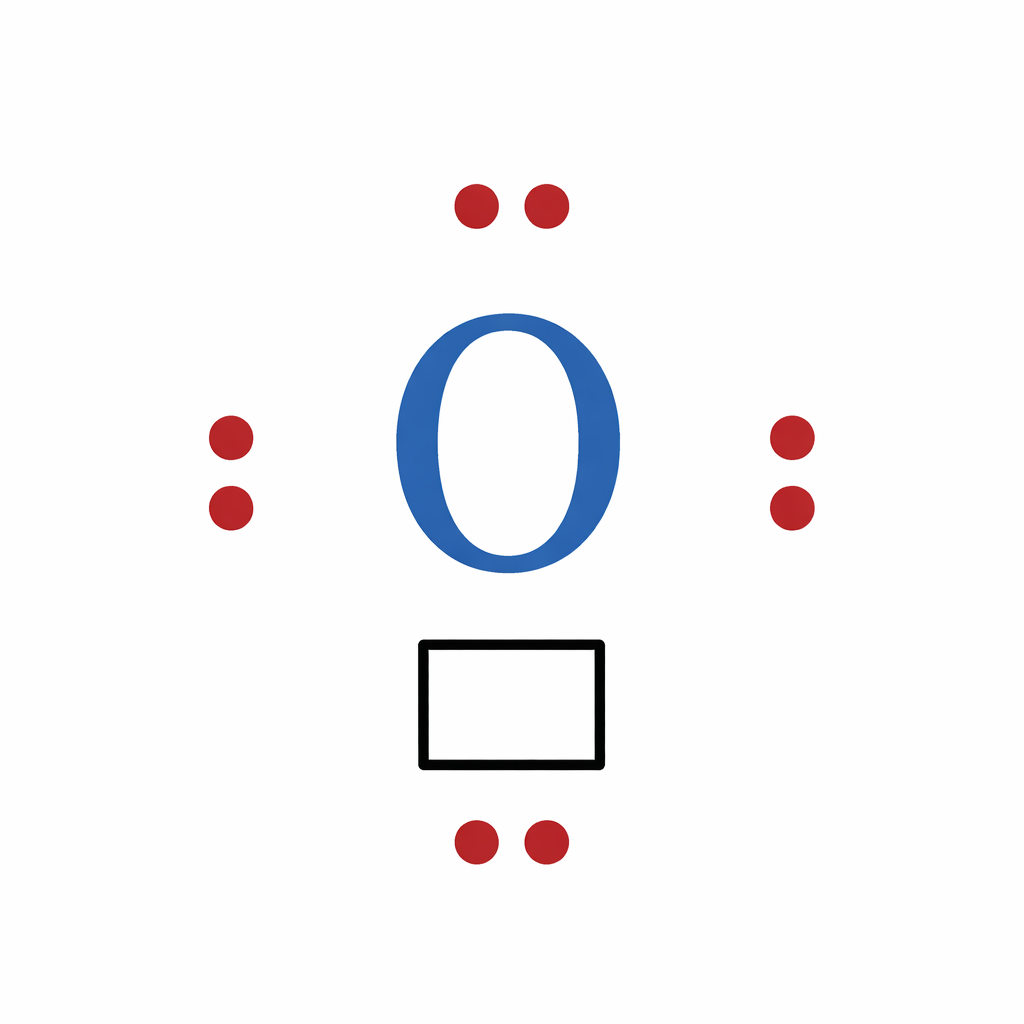
C quoi ce rectangle
lacune eléctronique → quand atome n’a pas 8 electrons de valence
Def cation/anion
Cation: charge électrique positive (perd electron)
Anion: charge électrique négative (gagne electron)
Entre modèle de Lewis et logiciel ChemSketch, quel est plus riche en info
Lewis car il représente doublets nn liants
Quelle info apporte un modèle moléculaire (ex: Chemsketch) par rapport à Lewis ?
La géométrie de molécule
Molécule tétraédrique def
4 liaisons simples : forme molécule ?
4 liaisons simples : forme molécule ?
Molécule tétraédrique / tétragonal def
3 liaisons simples 1 doublet nn liant: forme molécule ?
Molécule pyramidale
Molécule pyramidale
3 liaisons simples 1 doublet nn liant: forme molécule ?
Molécule plane coudée def
2 liaisons simples et 2 doublets nn liants
2 liaisons simples et 2 doublets nn liants, forme molécule ?
Molécule plane coudée def
Molécule triangulaire plane def
2 liaisons simples et 1 double liaison, quelle forme
2 liaisons simples et 1 double liaison, quelle forme
Molécule triangulaire plane def
Molécule linéaire def
2 liaisons doubles, forme ?
2 liaisons doubles, forme ?
Molécule linéaire def
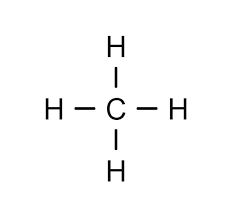
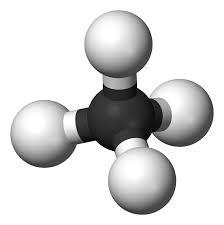
Forme du méthane
Tétraédrique
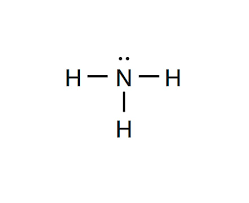
Forme de l’ammoniac
Pyramidale
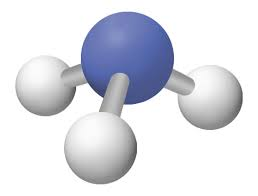
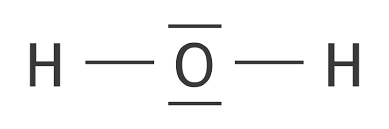
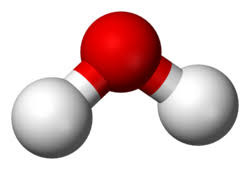
Forme de l’eau
Plane coudée
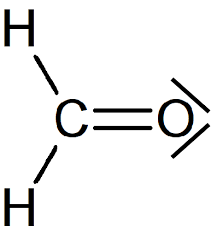
Forme du méthanal
Molécule trinagulaire plane
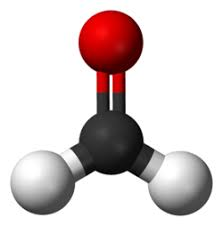
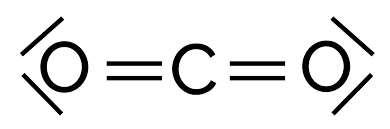
Forme CO2
Linéaire
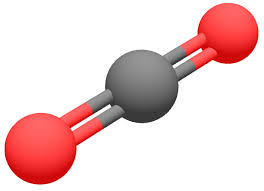
Formes géométriques où ts les atomes sont ds le même plan
Molécule plane coudée
Molécule plane triangulaire
Que peut on dire sur l’atome d’oxygène est sa forme géométrique
L’atome d’oxygène aura tjrs 2 doublets nn liants (coudées) sauf si ya 2 liaisons doubles (linéaire)
Digonal synonyme
Linéaire synonyme
Trigonal synonyme
Triangulaire plane synonyme
Digonal synonyme
Linéaire synonyme
Forme géométrique pour laquelle les doublets d’électrons s’écartent le plus
Forme tétraédrique
L’électronégativité
Traduit l’aptitude d’un atome à attirer à lui les électrons d’une liaison dans laquelle il est engagé
Est ce que l’électronégativité a une unité, si oui laquelle ?
Non
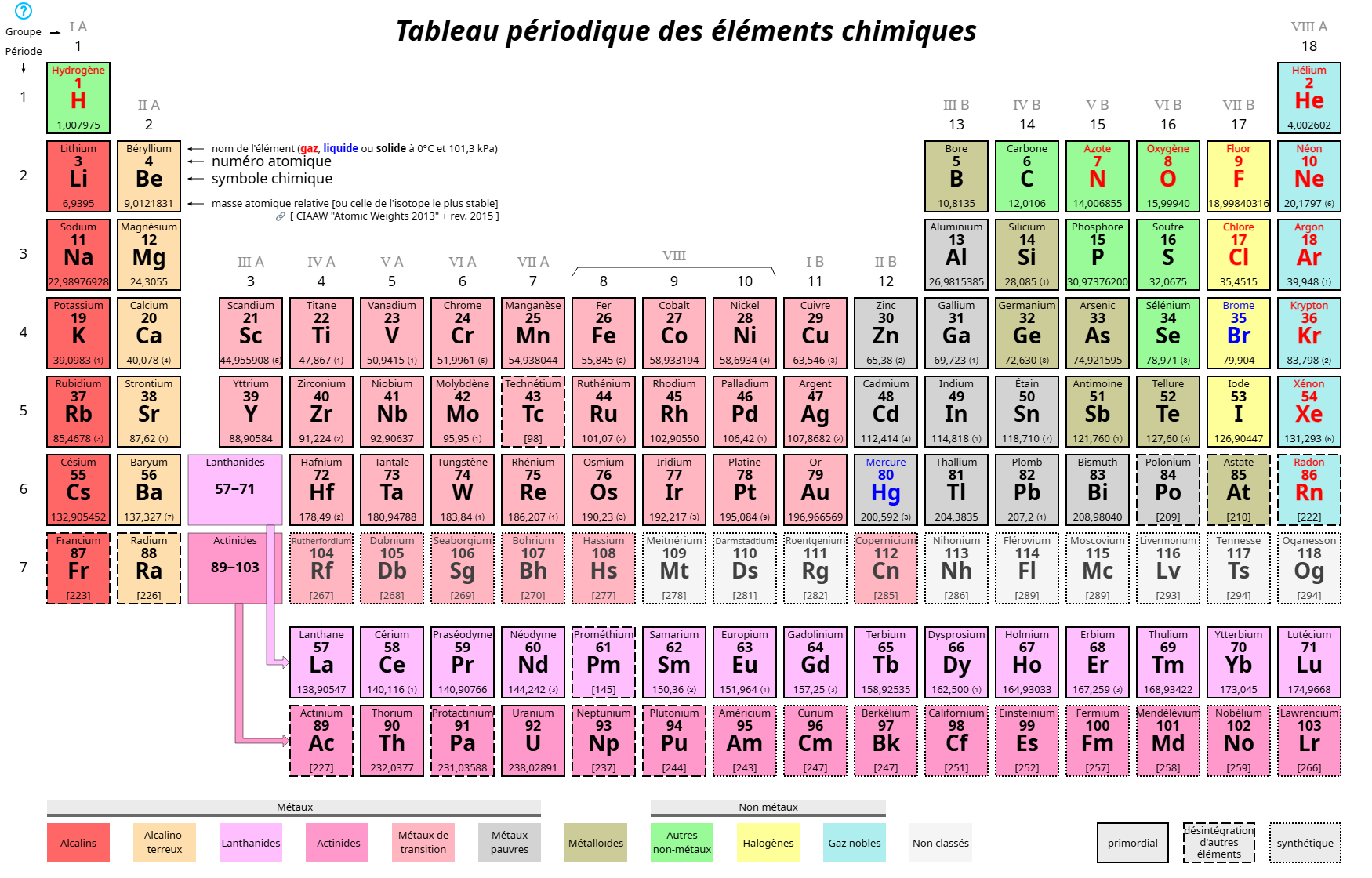
Comment varie l’électronégativité ?
Varie en fonction de la place de l’élément chimique dans le tableau périodique:
De bas en haut = électronégativité augmente
De gauche à droite = électronégativité augmente
Liaison polarisée def
Lorsque dans une liaison covalente, atome A est plus polarisée que l’atome B
Molécule polaire def (Savoir mot par mot)
Centres géométriques des charges partielles négatives et posistives sont nn confondus. Comment est la molécule ?
Centres géométriques des charges partielles négatives et posistives sont nn confondus.
Molécule polaire
Centres géométriques des charges partielles négatives et posistives sont confondus.
Molécule apolaire
Molécule apolaire
Centres géométriques des charges partielles négatives et positives sont confondus.