attività elettrica del cuore
1/28
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
29 Terms
Quali sono i gruppi cellulari del miocardio, come è strutturato il cardiomiocita e la membrana?
• Gruppi Cellulari: Si dividono in cardiomiociti di lavoro (atriali più piccoli dei ventricolari), cellule della conduzione/dei nodi (dettano il passo e trasmettono velocemente il PdA tramite il sistema ventricolare) e cellule di transizione. Diversità strutturale = diversità funzionale ed elettrofisiologica.
Il Cardiomiocita
Il miocardio di lavoro è formato da cellule allungate (cardiomiociti, 80-100 x 20 micron nel ventricolo, più piccole negli atri). Sono intimamente connesse da gap junctions che uniscono i citoplasmi creando un sincizio funzionale. Il 60-70% del citoplasma è occupato dall'apparato contrattile, circondato da mitocondri e reticolo sarcoplasmatico (che fornisce il Calcio).
Il Sistema dei Tubuli T (Trasversi)
La membrana cellulare (sarcolemma) presenta compartimentazioni. I canali ionici non sono distribuiti uniformemente. Per portare lo stimolo elettrico in profondità, il sarcolemma si invagina creando i tubuli T:
• Sono invaginazioni digitiformi a fondo cieco (circa 300 nm di diametro).
• Vengono studiati tramite microscopia a fluorescenza (molecole lipidiche), immunoistochimica (anticorpi per canali) o traccianti extracellulari impermeabili.
• Le ricostruzioni 3D (anni '90) hanno svelato una rete complessa e anastomizzata.
• La quantità di tubuli T varia in base alla specie e alla frequenza cardiaca (frequenza maggiore = più tubuli). Nelle patologie (cardiomiopatie, scompenso, post-infarto) si assiste a una grave perdita dei tubuli T.
Quali sono le 4 caratteristiche funzionali principali, con particolare attenzione all'eccitabilità e alla refrattarietà?
Le 4 Caratteristiche Funzionali:
1. Eccitabilità (Batmotropismo): Proprietà elettrofisiologica; capacità di generare un PdA in risposta a uno stimolo adeguato.
2. Automatismo-Ritmiicità (Cronotropismo): Proprietà elettrofisiologica.
3. Conduzione del PdA (Dromotropismo): Proprietà elettrofisiologica.
4. Contrattilità (Ionotropismo): Proprietà meccanica.
Potenziale di azione cardiomiocita ventricolare
Il profilo elettrico di un cardiomiocita di lavoro ventricolare è molto diverso da quello di un assone: dopo la depolarizzazione, permane per lungo tempo a un potenziale positivo e lontano da quello di riposo (fase di plateau). Il potenziale cambia in base alla tipologia cellulare (es. miocardio di lavoro vs. sistema di conduzione).
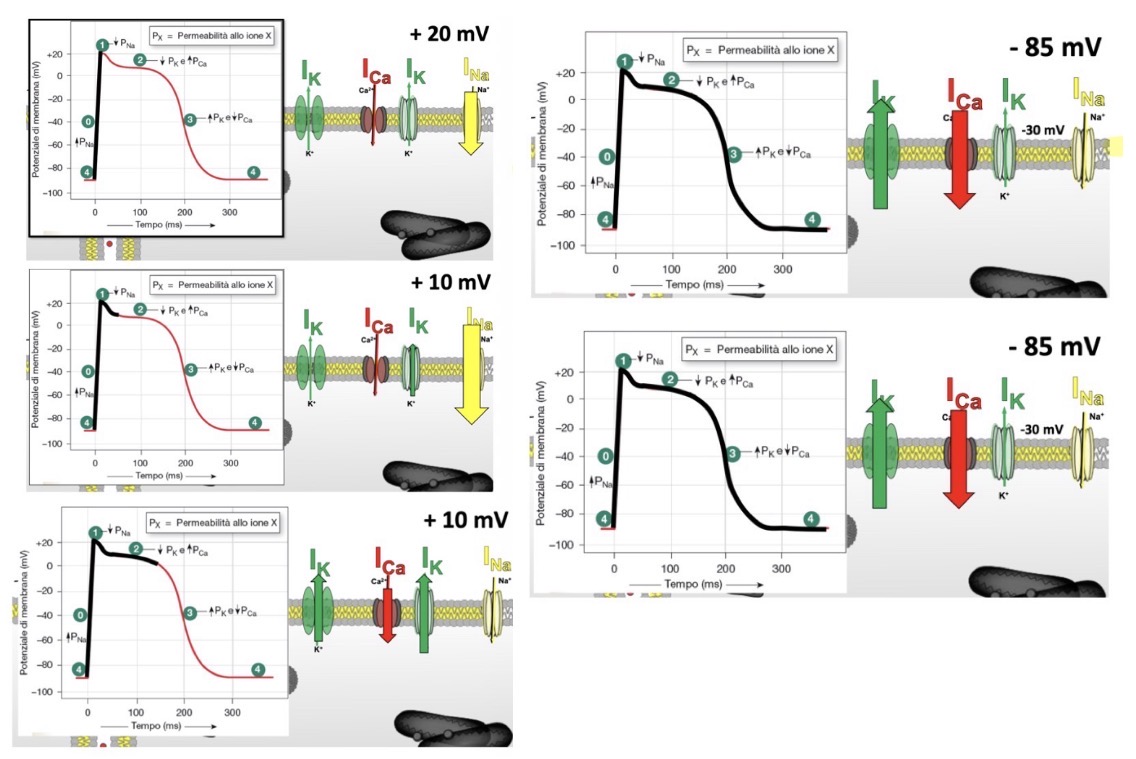
Le 5 Fasi del Potenziale Ventricolare
Le correnti dipendono dallo stato dei canali e dal gradiente elettrochimico:
• Fase 0 (Salita rapida / Upstroke): Apertura rapida dei canali del Sodio (Na^+) che entra nella cellula. Il potenziale schizza verso valori positivi (picco di +20 mV). Dura circa 0.5 ms.
• Fase 1 (Ripolarizzazione parziale): Chiusura dei canali del sodio e apertura di canali rapidi per il Potassio (K^+) in uscita, ovvero la Corrente transitoria Ito che abbassa il potenziale a +10mV.
• Fase 2 (Plateau): Elemento distintivo cardiaco. Si ha l'apertura ritardata dei canali del Calcio (per ICa-L). La corrente in entrata di calcio bilancia perfettamente le correnti in uscita di potassio, mantenendo il PdM attorno a 0mV. Iniziano ad attivarsi le correnti K+ lente (I_{Kr} rapida e I_{Ks} lenta). Serve per il rilascio di calcio dal reticolo.
• Fase 3 (Ripolarizzazione rapida): I canali del calcio si chiudono, prevalgono i canali lenti del Potassio (I_{Kr}, I_{Ks}, I_{K1}) in uscita, riportando la cellula al potenziale di riposo.
• Fase 4 (Potenziale di riposo): Coinvolti I_{K1} (elevata conduttanza al K+), pompa Na+/K+ e scambiatore Na+/Ca2+.
Scoperta del plateau
Esperimenti di Hodgkin applicati al cuore
Per studiare le correnti, si manipolano gli ioni extracellulari.
• Bloccando i canali del sodio (es. con tetrodotossina - TTX) nell'assone gigante di calamaro, l'attività elettrica si azzera.
• Ripetendo l'esperimento sul cardiomiocita, bloccando il sodio si perde la "salita rapida" (Fase 0), ma la cellula riesce comunque a depolarizzarsi grazie a una seconda corrente indipendente dal sodio. Questa corrente, caratterizzata da attivazione più lenta ma durata e ampiezza simili, è proprio quella del Calcio. Solo eliminando anche il calcio si ottiene un'attività elettrica nulla.
La tecnica del voltage clamp e la misurazione delle correnti
Il Voltage Clamp permette di studiare le correnti ioniche mantenendo costante il potenziale di membrana.
• Funzionamento: Si impone alla cellula il voltaggio (voltaggio comandato, Vc). Dopo che la cellula raggiunge il voltaggio viene "clampata" (bloccata), al potenziale desiderato. In questo modo la driving force (forza spingente) per ciascun ione è costante.
• Significato delle misurazioni: L'equazione fondamentale è I = G x (Em - E_{ion}). Essendo la driving force (Em - E_{ion}) mantenuta costante dallo sperimentatore, qualsiasi variazione di corrente misurata (I) corrisponde direttamente a una variazione della conduttanza (G), ovvero all'apertura o chiusura dei canali ionici.
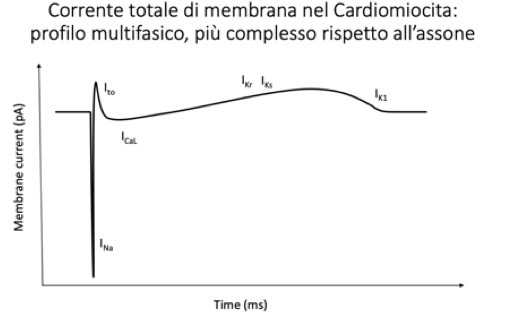
• Profilo delle correnti: Nel cardiomiocita, il tracciato della corrente totale è multifasico e complesso: presenta due deflessioni verso il basso (correnti entranti depolarizzanti: prima il sodio, poi il calcio con un certo ritardo) seguite da correnti uscenti (potassio, ripolarizzanti). Nel neurone il profilo è più semplice (sodio entrante, potassio uscente). Per isolare e misurare una specifica corrente (es. solo quella del sodio), si utilizzano bloccanti selettivi per gli altri ioni (es. bloccanti del potassio e del calcio).
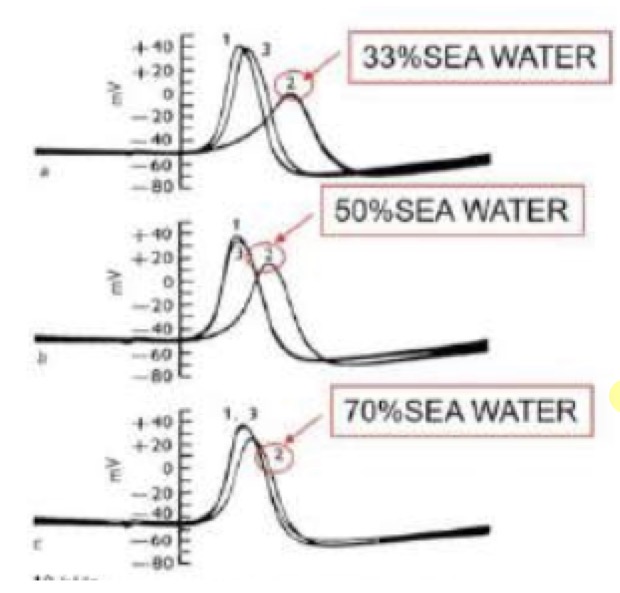
Caratteristiche della corrente di sodio
La corrente del sodio è presente in tutte le cellule eccitabili (muscolo, neurone, cuore) e possiede caratteristiche costanti:
• È un potenziale molto ampio ma di brevissima durata.
• Ha un picco che declina rapidamente. Nei cardiomiociti ventricolari umani a 37°C, il picco si raggiunge in frazioni di millisecondo (es. 500 microsecondi) e tende a inattivarsi e scomparire completamente entro 5-10 ms.
• Dimostrazione tramite sostituzione ionica: Se si sostituisce l'acqua di mare (ricca di sodio) con una soluzione isotonica priva di sodio (es. contenente colina), la corrente entrante scompare del tutto (quindi no depolarizzazione). Ripristinando il sodio, la corrente ricompare, confermando che è il sodio il portatore di questa carica.
Isolamento dei cardiomiociti e tecnica del Patch Clamp
Per studiare l'elettrofisiologia cellulare, è necessario ottenere singoli cardiomiociti isolati.
• La difficoltà di preparazione: A differenza della fibra muscolare scheletrica (lunga e facilmente dissecabile manualmente), i cardiomiociti sono piccoli, fragili, interconnessi da gap junctions e immersi in una fitta matrice extracellulare.
• Isolamento enzimatico: Si utilizza una tecnica di digestione enzimatica (es. collagenasi) per distruggere la matrice. Nel modello animale si perfonde il cuore intero; per i tessuti umani (provenienti da scarti chirurgici o cuori non trapiantabili), il tessuto viene sminuzzato, agitato meccanicamente e digerito. Tramite successive centrifughe si scarta la matrice digerita e si isola il singolo cardiomiocita a forma di bastoncello.
• Patch Clamp: Questa tecnica è l'evoluzione del Voltage Clamp. Si utilizza una micropipetta di vetro con punta di circa 1 micron che entra in contatto con la cellula. Applicando una suzione si crea un sigillo ad altissima resistenza (gigaseal). Nella modalità "whole cell", si frammenta la membrana all'interno della pipetta, mettendo in comunicazione il citoplasma con la soluzione della pipetta, permettendo di registrare l'attività elettrica di tutta la membrana.
• Single Channel Recordings: Lo studio del singolo canale nel cardiomiocita adulto è ostacolato dall'alta densità di canali e dalla struttura complessa (tubuli T). Spesso si utilizzano linee cellulari immortalizzate (es. cellule HEK) in cui viene indotta l'espressione di un singolo canale d'interesse tramite ingegneria genetica. Le registrazioni a singolo canale mostrano un tipico aspetto a gradino (aperto/chiuso). La corrente registrata dipende dal potenziale di membrana in maniera lineare.
Struttura, stadi funzioni e isoforme dei canali sodio
Il canale del sodio fa da capostipite per lo studio di altri canali (calcio, potassio) per via della sua struttura modulare.
• Struttura: È costituito da una subunità alpha (più eventuali subunità beta regolatrici). La subunità alpha è formata da 4 domini omologhi. Ogni dominio è costituito da 6 regioni transmembrana (S1-S6). L'ansa tra S5 ed S6 costituisce il poro.
• Sensore del voltaggio: Il segmento S4 di ogni dominio contiene residui di aminoacidi con cariche positive. Questa zona cambia conformazione in risposta alle variazioni del potenziale di membrana, fungendo da sensore.
I 3 stadi funzionali: I canali non sono semplicemente aperti o chiusi, ma transitano tra 3 stati: Chiuso (fase 4 del potenziale d'azione), Aperto (fase 0, in cui la permeabilità diventa massimale) e Inattivato (fine fase 0 e fase di plateau). Quando il canale è inattivato, l'eccitabilità della membrana crolla a zero.
• Isoforme e Farmacologia: Esistono almeno 9 isoforme diverse del canale del sodio, codificate da geni diversi su cromosomi diversi. Sono tessuto-specifiche (es. 1.1, 1.2, 1.3 nel SNC; 1.4 nel muscolo scheletrico; 1.7, 1.8, 1.9 nei neuroni sensitivi del dolore). Nel cuore l'isoforma prevalente è la Nav 1.5.
• Sebbene il meccanismo molecolare di funzionamento non cambi tra le isoforme, cambia drasticamente la capacità di legare i farmaci. Ad esempio, un anestetico locale blocca le isoforme dei neuroni del dolore ma non ha effetto a livello cardiaco; un farmaco selettivo per Nav 1.5 agirà come antiaritmico.
Driving force
Si calcola come la differenza tra il potenziale di membrana attuale (E_m) e il potenziale di equilibrio dello ione (E_{ion}): Driving force= Em - Eion
1. Il Gradiente di Concentrazione (Chimico)
Gli ioni tendono a spostarsi da dove sono più concentrati a dove lo sono meno (diffusione). Ad esempio, il Sodio (Na^+) è molto più concentrato fuori dalla cellula e "spinge" per entrare.
2. Il Gradiente Elettrico
Le cariche opposte si attraggono. Se l'interno della cellula è negativo, attirerà ioni positivi (cationi) come il Sodio o il Potassio, indipendentemente dalla loro concentrazione.
Come interpretare il valore
Il segno e la grandezza della driving force determinano la direzione e l'intensità del flusso ionico:
• Driving Force Positiva (> 0): Se lo ione è positivo (come il K^+), tenderà a uscire dalla cellula.
• Driving Force Negativa (< 0): Se lo ione è positivo (come il Na^+), tenderà a entrare nella cellula.
• Driving Force Zero (= 0): Lo ione è in equilibrio. Non c'è movimento netto, anche se i canali sono aperti.
Un esempio pratico: Il Sodio nel cuore
All'inizio del battito cardiaco, il potenziale di membrana (Em) è circa -90mV, mentre il potenziale di equilibrio del Sodio (ENa) è circa +60mV. Quindi la driving force sarà -90-(+60)= -150mV
Il valore è enormemente negativo, il che spiega perché, non appena i canali del sodio si aprono, il sodio "si precipita" dentro la cellula con una forza incredibile, causando la fase di salita rapida del potenziale d'azione di cui parlavamo prima.
Meccanismi di gating
Il meccanismo di gating (apertura/chiusura) del canale del sodio è duplice, controllato da due zone distinte ma entrambe sensibili al voltaggio.
1. Attivazione (Porta di apertura - m): Il cambiamento conformazionale del segmento S4 (che si sposta verso l'esterno in risposta alla depolarizzazione) rende il poro accessibile al sodio.
2. Inattivazione: È regolata da una regione intracellulare situata tra il dominio D3 e D4. Contiene 3 aminoacidi idrofobici (IFM) che, al variare del voltaggio, si muovono verso la parte interna del canale ostruendolo. Porta di inattivazione (dominio IFM) è più lenta.
• Il meccanismo di gating fa sì che esista una finestra temporale ristretta in cui il canale è accessibile detta finestra di accessibilità (incrocio delle curve). Questo significa che il meccanismo di inattivazione non influenza il processo opposto (meccanismi indipendenti).
• Uscita dallo stato inattivato: Dipende da tempo e voltaggio. Se il potenziale di membrana rimane a valori positivi, il canale rimane inattivato. Se invece torna al potenziale di riposo per un tempo sufficiente, transita di nuovo a "chiuso" (pronto ad aprirsi). Stadi: chiuso, aperto, inattivato.
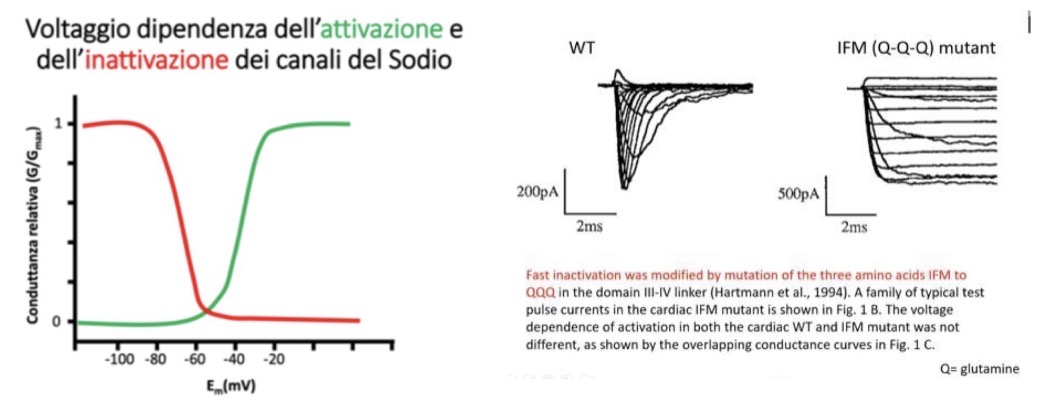
• Prova sperimentale (Mutante QQQ): Sostituendo la sequenza IFM con tre molecole di glutammina (QQQ), il canale mutante si attiva ma non si inattiva più, mantenendo una corrente sostenuta nel tempo.
• Analisi dei grafici: Un tracciato con un picco rapido che poi declina (profilo multifasico) indica la presenza di un doppio meccanismo (attivazione + inattivazione). Un tracciato a gradino (sostenuto) indica un semplice meccanismo di apertura senza inattivazione.
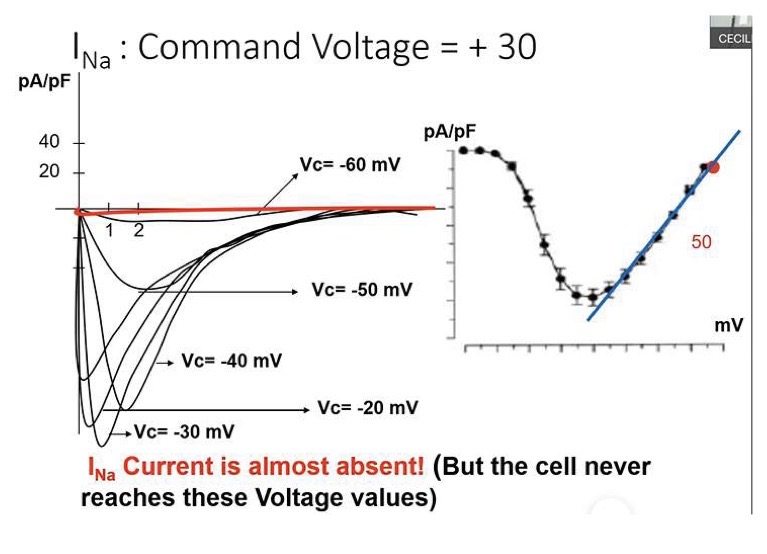
Relazione corrente voltaggio per il canale del sodio
Sottoponendo la cellula a salti di voltaggio (step) via via più positivi, si osserva un comportamento specifico dettato dall'interazione tra apertura dei canali e driving force.
• A -90 mV: La maggioranza dei canali è chiusa. Non c'è corrente.
• Verso -65 mV (Soglia): Si osserva una piccola corrente. Un certo numero di canali passa allo stato aperto. La driving force favorisce massicciamente l'ingresso del sodio, causando un'ulteriore depolarizzazione che porta all'apertura di altri canali (feedback positivo).
• Tra -40 mV e -20 mV (Il Picco): Il numero di canali aperti è il massimo possibile (massima permeabilità). Imponendo un voltaggio di -30 mV la depolarizzazione aumenta la conduttanza (G_{Na}), aprendo più canali → Aumento della corrente. Quindi intorno a -30mV si registra tipicamente la corrente di ampiezza massima (il picco più basso nel tracciato, o deflessione massima verso il basso).
• Verso valori più positivi (0, +20, +60 mV): Sebbene i canali siano già tutti aperti al massimo (GNa costante e massima), la corrente in ingresso diminuisce. Questo accade perché ciò che cambia è il gradiente elettrochimico (la driving force). Man mano che il potenziale di membrana (Em) diventa positivo (avvicinandosi al potenziale di equilibrio del Na+, ENa), la forza elettrica inizia a spingere il sodio verso l'esterno, opponendosi al gradiente chimico. La corrente diminuisce linearmente.
• A +60 mV (Potenziale di equilibrio): Il gradiente elettrochimico si dissipa completamente. Le forze si equivalgono e la corrente netta si azzera.
Curva I/V (Intensità/Voltaggio) della Corrente del Sodio
Costruendo una curva I/V (variabile indipendente: voltaggio imposto; variabile dipendente: corrente normalizzata sulla capacità cellulare), si osserva una proporzionalità diretta tra intensità e voltaggio al di sopra dei -20 mV.
In questa porzione lineare del grafico, la conduttanza al sodio è già massimale (tutti i canali disponibili sono aperti). Pertanto, applicando la legge I = G x (Em - ENa), l'unico fattore che determina il cambiamento dell'intensità di corrente è la variazione del gradiente elettrochimico (la driving force).
Voltaggio dipendenza dell’inattivazione e stadi funzionali
Anche l'inattivazione del canale del sodio è voltaggio-dipendente. La soglia di inattivazione è simile a quella di attivazione (circa -60 mV).
• Il meccanismo a feedback positivo: Nel modello di Hodgkin e Huxley, la depolarizzazione apre il canale, il sodio entra e depolarizza ulteriormente la cellula, aprendo altri canali.
• La finestra temporale: Questo feedback positivo dura per una finestra temporale brevissima (1 o 2 millisecondi). Dopodiché, la porta di inattivazione si chiude, bloccando l'ingresso dello ione.
• Uscita dall'inattivazione: Finché il potenziale di membrana resta su valori positivi, il canale rimane inattivato. Per tornare allo stato chiuso (e quindi di nuovo apribile), il potenziale deve tornare ai valori di riposo e deve trascorrere un tempo sufficiente.
• Corrente finestra: Esiste un piccolo intervallo di voltaggio in cui le curve di attivazione e inattivazione si sovrappongono. In questa "finestra":
• Alcuni canali sono attivati (aperti).
• Ma non tutti sono ancora inattivati.
Questo significa che a determinati voltaggi (vicini alla soglia), esiste una piccolissima corrente continua di sodio che non si spegne mai del tutto, perché c'è un equilibrio dinamico tra canali che si aprono e canali che si inattivano.
Indipendenza dei meccanismi di attivazione e inattivazione
Dallo studio delle registrazioni a singolo canale, si evince che l'apertura avviene con tempistiche stocastiche (alcuni senza latenza, altri in ritardo), ma la corrente totale è la sommatoria di questi eventi.
L'utilizzo del mutante QQQ (privo di inattivazione) dimostra che la curva di attivazione rimane identica a quella del canale normale (WT). Questo prova che attivazione e inattivazione dipendono da meccanismi molecolari diversi e sono completamente indipendenti.
Regolazione canali
Le caratteristiche dei canali possono essere modificate tramite meccanismi di adattamento fisiologico, come le modificazioni post-trascrizionali operate dalle chinasi (es. fosforilazione).
• Un esempio è la risposta beta-adrenergica mediata dalla PKA (chinasi che risponde ai livelli di calcio).
• La fosforilazione sposta la curva voltaggio-dipendenza dell'inattivazione verso valori più negativi: questo restringe la finestra temporale di apertura, diminuendo la durata complessiva della corrente di sodio (perché si inattiva prima).
Le fosforilazioni nel canale del sodio avvengono sulla subunità principale (alpha), a differenza di altri canali dove avvengono sulle subunità accessorie.
Alterazioni del gating
Le proprietà di gating possono essere alterate da farmaci, da adattamenti patologici prolungati o da mutazioni genetiche (Canalopatie).
• Sindrome di Brugada: È un'aritmia (tachicardia ventricolare) causata da una mutazione del canale del sodio (Nav1.5) in un dominio strutturale che lega l'anchirina. Questa proteina serve a localizzare correttamente il canale sui tubuli trasversi. La mutazione causa:
1. Un problema di localizzazione spaziale.
2. Uno spostamento della curva di attivazione verso sinistra (il canale si apre troppo facilmente).
3. Un'inattivazione prematura e un recupero più rapido (periodo refrattario più breve, propensione all'aritmia).
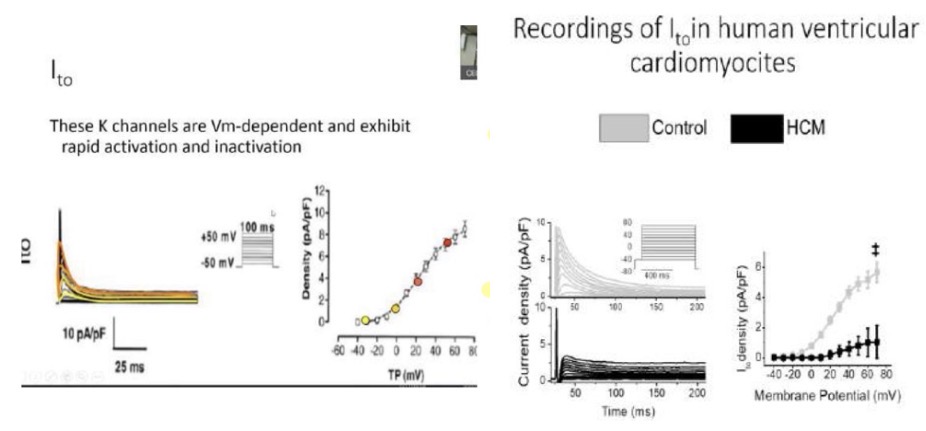
Corrente di potassio transiente uscente I_{to} (caratteristiche, componenti e patologie)
La corrente I_{to} è la prima corrente di potassio ripolarizzante ed è responsabile della Fase 1.
• Caratteristiche: Ha un comportamento molto simile al canale del sodio, presentando un'attivazione e un'inattivazione voltaggio-dipendenti ed estremamente rapide. La sua soglia di attivazione è intorno a -35 mV. Genera una corrente di densità modesta (circa 10 pA/pF).
• Componenti:
• Componente rapida: inattiva in 5 ms, sensibile alle 4-aminopiridine, non modulata dal calcio.
• Componente lenta: tipica dell'atrio o di condizioni patologiche ventricolari. Ha un'inattivazione nell'ordine dei 100 ms (si estende fino al plateau). È modulata dai livelli di calcio citosolico (aumenta all'aumentare del calcio per controbilanciarne l'ingresso).
• Variabilità Regionale e Patologia: La I_{to} è più marcata nell'epicardio rispetto all'endocardio, determinando durate diverse del potenziale d'azione nei vari strati del cuore. Nella cardiomiopatia ipertrofica, i cardiomiociti malati presentano un picco della corrente I_{to} drasticamente ridotto (es. 1 pA/pF contro i 6 pA/pF sani).
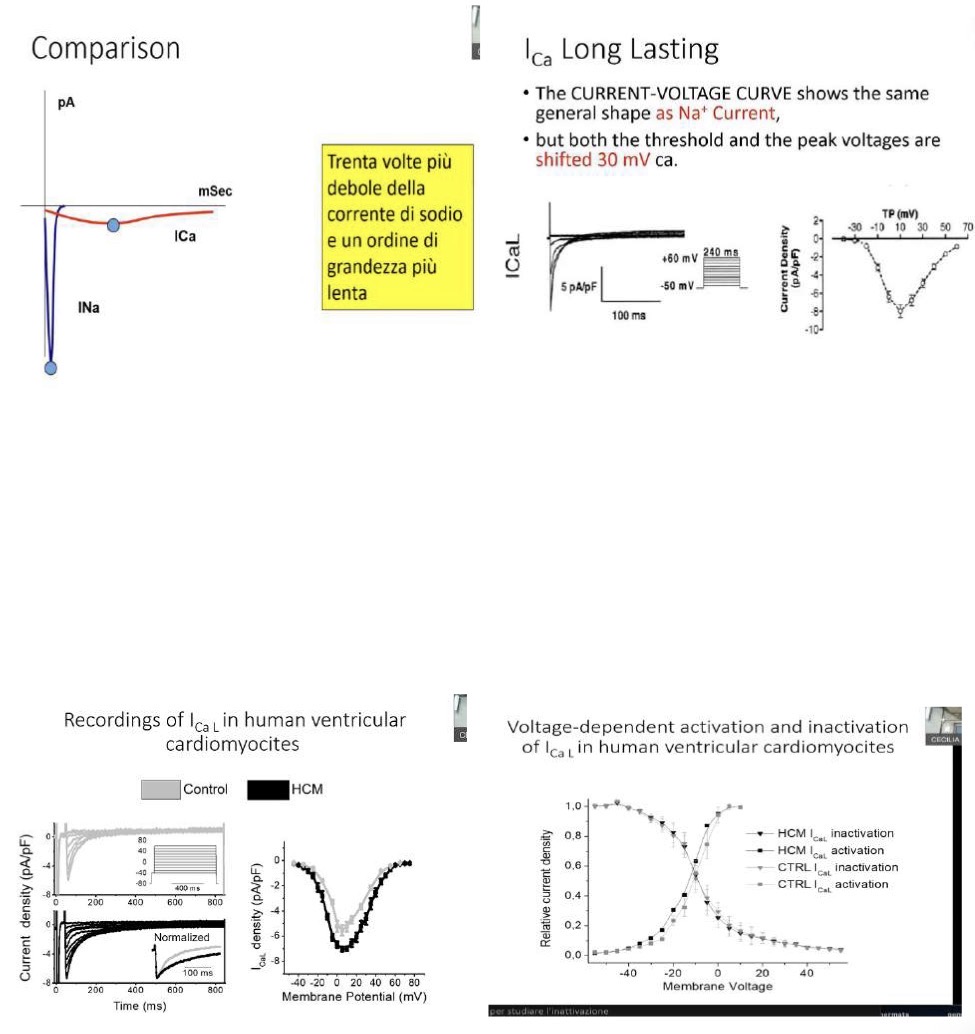
Fase 2 plateau: corrente principale, confronto con il sodio e patologie
Il plateau (Fase 2) è la caratteristica che differenzia il miocardio da muscolo scheletrico e nervi. È il risultato di un bilanciamento tra correnti entranti (depolarizzanti) e correnti uscenti (ripolarizzanti).
• La Corrente I_{Ca,L} (Long Lasting): È la principale corrente entrante che sostiene il plateau.
• Confronto con il Sodio: La curva I/V ha una forma a campana simile a quella del sodio, e anche i meccanismi di gating (apertura/inattivazione) sono analoghi. Tuttavia, ci sono profonde differenze:
1. L'intensità è circa 30 volte più piccola.
2. I tempi sono un ordine di grandezza più lenti (l'inattivazione dura circa 100-200 ms).
3. Soglia e picco sono shiftati (spostati) di circa +30 mV verso valori più positivi (la soglia del calcio è a -30/-40 mV).
• Patologia: Nella cardiomiopatia ipertrofica, la curva del calcio non è shiftata (il gating è uguale), ma l'intensità della corrente aumenta perché c'è una maggiore densità (maggiore espressione) di proteine canale sulla membrana.
Protocollo per studiare l’inattivazione del calcio
Poiché l'inattivazione del calcio è più lenta di quella del sodio, si presta meglio a essere studiata con un protocollo a doppio impulso (o due stimoli quadrati):
1. Primo stimolo (Prepuls): Impone vari livelli di potenziale di membrana per indurre l'apertura di un certo numero di canali.
2. Secondo stimolo (Test step): Applicato dopo un breve intervallo, è uno stimolo a valori molto positivi (zona di massima permeabilità).
L'ampiezza della corrente generata dal test step dipende da quanti canali si sono aperti (e poi inattivati) durante il prepuls. Se il prepuls era vicino alla soglia (pochi canali aperti), il test step ne aprirà moltissimi. Se il prepuls era già a valori massimali (molti canali aperti), il test step ne troverà pochi disponibili. Questo metodo permette la costruzione accurata della curva di inattivazione.
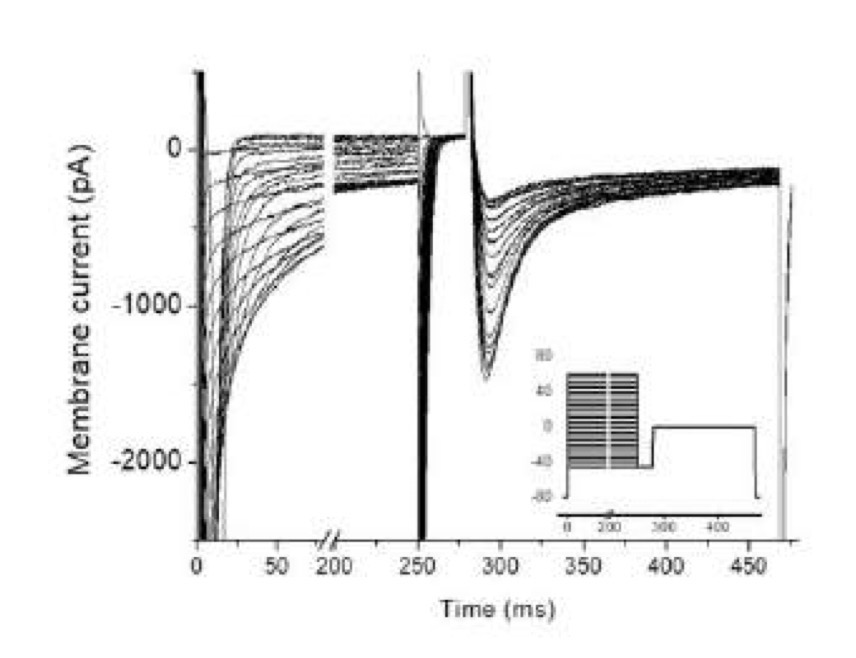
Separazione delle correnti I(Na) e I(CaL)
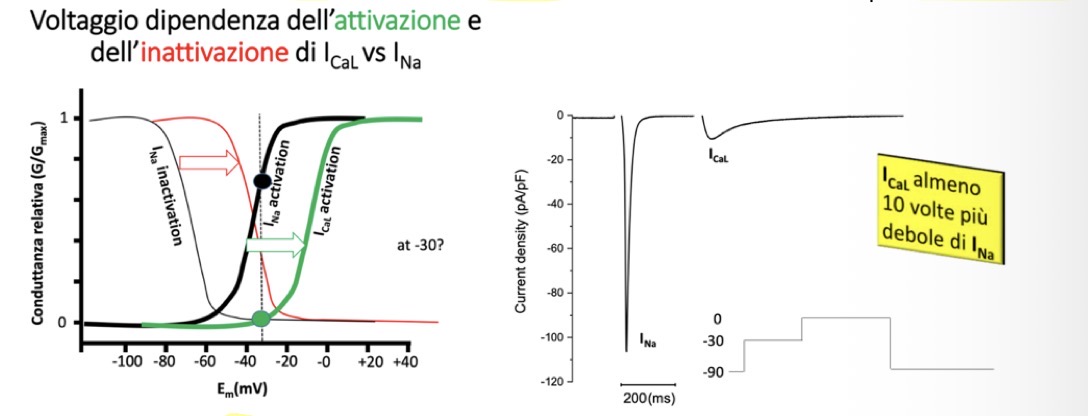
Per studiare le correnti responsabili della ripolarizzazione, è necessario prima isolare le singole correnti. È possibile separare la corrente del sodio I(Na) dalla corrente del calcio I(CaL) senza l'uso di farmaci bloccanti, sfruttando lo shift (spostamento) di circa 30 mV delle loro curve di inattivazione.
• Impostando un voltaggio di mantenimento a -30 mV, la quasi totalità dei canali del Na+ viene inattivata ("fatta fuori"), mentre i canali del Ca2+ si trovano ancora sotto la loro soglia di inattivazione.
• Applicando un secondo stimolo di voltaggio, si registra una corrente entrante dovuta esclusivamente al calcio.
• Questo esperimento dimostra anche una differenza di ampiezza: infatti guardando i pA/pf delle correnti, la corrente I(CaL) è almeno 10 volte più piccola rispetto alla I(Na) (sebbene ci sia variabilità in base alla specie e allo stato dei canali). A -30 mV, la I(Na) è vicina alla permeabilità massima, ma il picco assoluto si raggiunge a circa -20 mV.
Distribuzione dei canali sul sarcolemma e ruolo dei Tubuli a T
La distribuzione spaziale dei canali ionici non è omogenea e influenza profondamente il Potenziale d'Azione (PA). Questo è stato dimostrato tramite una procedura di shock osmotico controllato:
• Le cellule vengono poste in un ambiente iperosmolare (si rimpiccioliscono) e poi riportate in un ambiente normoosmolare (si rigonfiano). Questa variazione di volume genera una trazione che fa staccare i tubuli trasversi (tubuli T) dalla superficie, lasciandoli intrappolati all'interno e rendendoli funzionalmente silenti.
• Confronto (Controllo vs. Detubulate): Misurando il potenziale d'azione, l'ampiezza rimane simile, ma la durata si riduce nelle cellule detubulate. La capacità di membrana diminuisce in proporzione alla perdita di superficie.
• Distribuzione delle correnti:
• La I(Na) resta uguale (distribuzione omogenea sul sarcolemma superficiale e nei tubuli T).
• La I(CaL) diminuisce drasticamente perché è quasi completamente localizzata nei tubuli T. La perdita di questa corrente causa l'accorciamento della fase di plateau e la riduzione della durata del potenziale d'azione.
• La localizzazione di I(CaL) nei tubuli T è fondamentale: funge da trigger per l'accoppiamento eccito-contrattile.
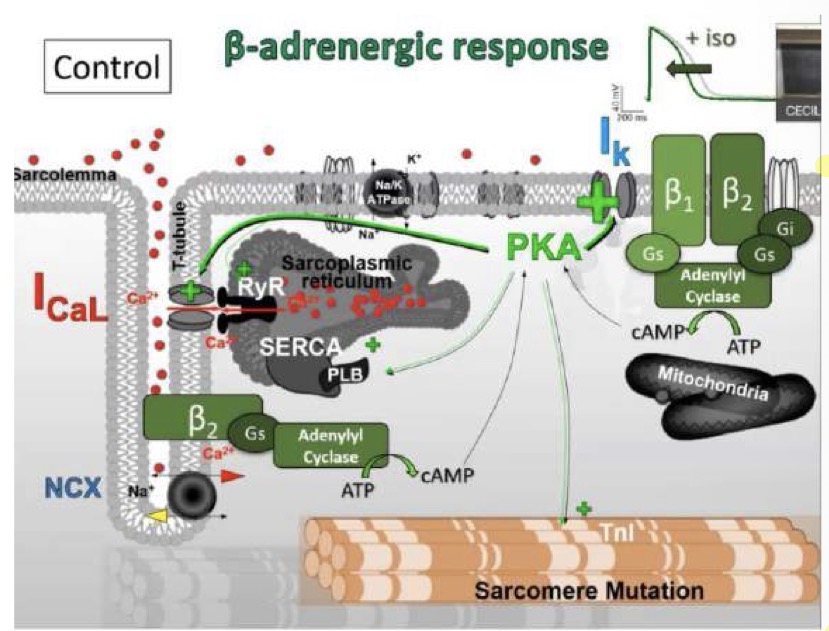
Accoppiamento eccito-contrattile e regolazione beta-adrenergica
Il calcio che entra attraverso i canali I(CaL) (canali DHPR) nello spazio diadico attiva i recettori per la rianodina (RyR) sul reticolo sarcoplasmatico.
• Questo innesca una massiccia liberazione di Ca2+ nel citoplasma (da decine a circa 600 nanomoli), fondamentale per innescare la contrazione muscolare. Successivamente, la pompa SERCA e lo scambiatore Na-Ca ripristinano i livelli basali di calcio.
• Stimolazione Beta-Adrenergica: L'adrenalina/noradrenalina agisce sui recettori beta1 e beta2, attivando la cascata dell'adenilato ciclasi → cAMP → PKA.
• La PKA fosforila diversi bersagli, tra cui i canali L del calcio. La I(CaL) (depolarizzante) viene potenziata, il che teoricamente dovrebbe prolungare il potenziale d'azione.
• Tuttavia, la PKA fosforila e potenzia anche la corrente uscente I(Ks) (ripolarizzante). Questo effetto ripolarizzante è dominante e antagonizza il prolungamento, portando a un effetto netto di riduzione della durata del potenziale d'azione sotto stimolo beta-adrenergico.
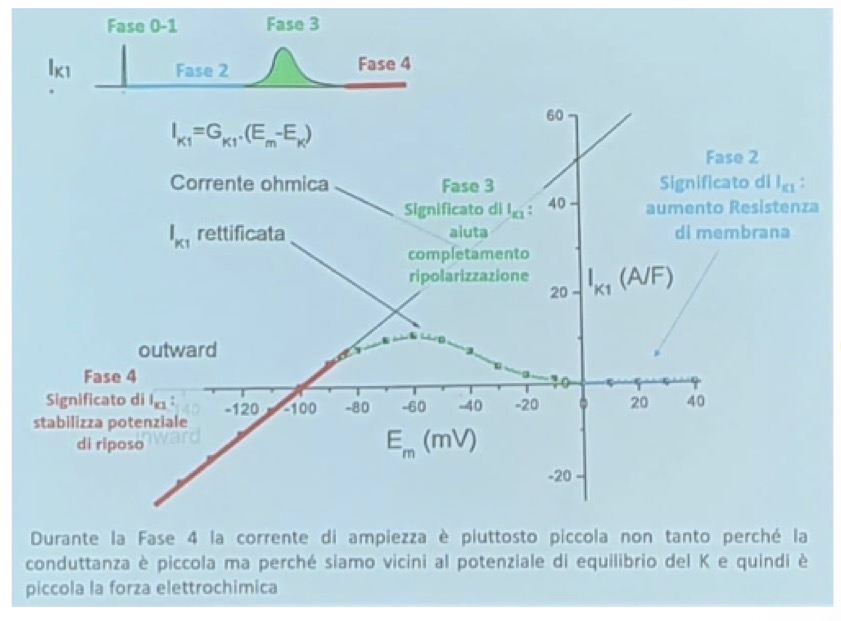
La corrente K1 I(K1)
La corrente I(K1) ha il ruolo cruciale di mantenere il plateau, bilanciare la I(Ca) e stabilizzare il potenziale di membrana sui valori di riposo (fase 3 e 4).
• Comportamento "sempre aperto": A differenza di altri canali, la famiglia responsabile della I(K1) non ha classiche porte di gating voltaggio-dipendenti.
• Rettificazione in ingresso (Inward Rectification): Per valori iperpolarizzati (sotto i -90 mV), la corrente si comporta in modo ohmico (relazione lineare intensità-voltaggio, favorisce l'ingresso di K+). Salendo sopra i -90 mV, si perde il comportamento ohmico e la curva si appiattisce.
• Meccanismo: A potenziali superiori a quello di riposo, ioni Mg2+ e poliammine citoplasmatiche vengono spinti verso il poro del canale, occupandolo e bloccando fisicamente l'uscita del K+. La corrente uscente è quindi ostacolata.
• Impatto sulla resistenza di membrana: Durante la fase di upstroke e la ripolarizzazione finale, la conduttanza della membrana è elevata (bassa resistenza). Durante il plateau, la conduttanza crolla e la resistenza è molto alta (grazie al blocco della I(K1) dato dal Mg2+). Questa alta resistenza permette a una corrente piccola come la I(CaL) di produrre e mantenere uno scostamento di voltaggio significativo per un tempo prolungato (centinaia di ms). Se I(K1) non si chiudesse, il cuore dovrebbe far entrare una quantità enorme di Calcio per mantenere il plateau.
• Curva intensità-voltaggio I(K1): Sotto -100 mV la corrente entrante aumenta linearmente. Salendo verso il range fisiologico, devia dal comportamento ohmico, diminuisce fino a stabilizzarsi a 0 mV, rimanendo assente per valori positivi. Durante la ripolarizzazione (fase 3), scendendo di voltaggio, la corrente uscente si riattiva prepotentemente, antagonizzando la depolarizzazione e riportando la cellula a riposo (proteggendo da aritmie).
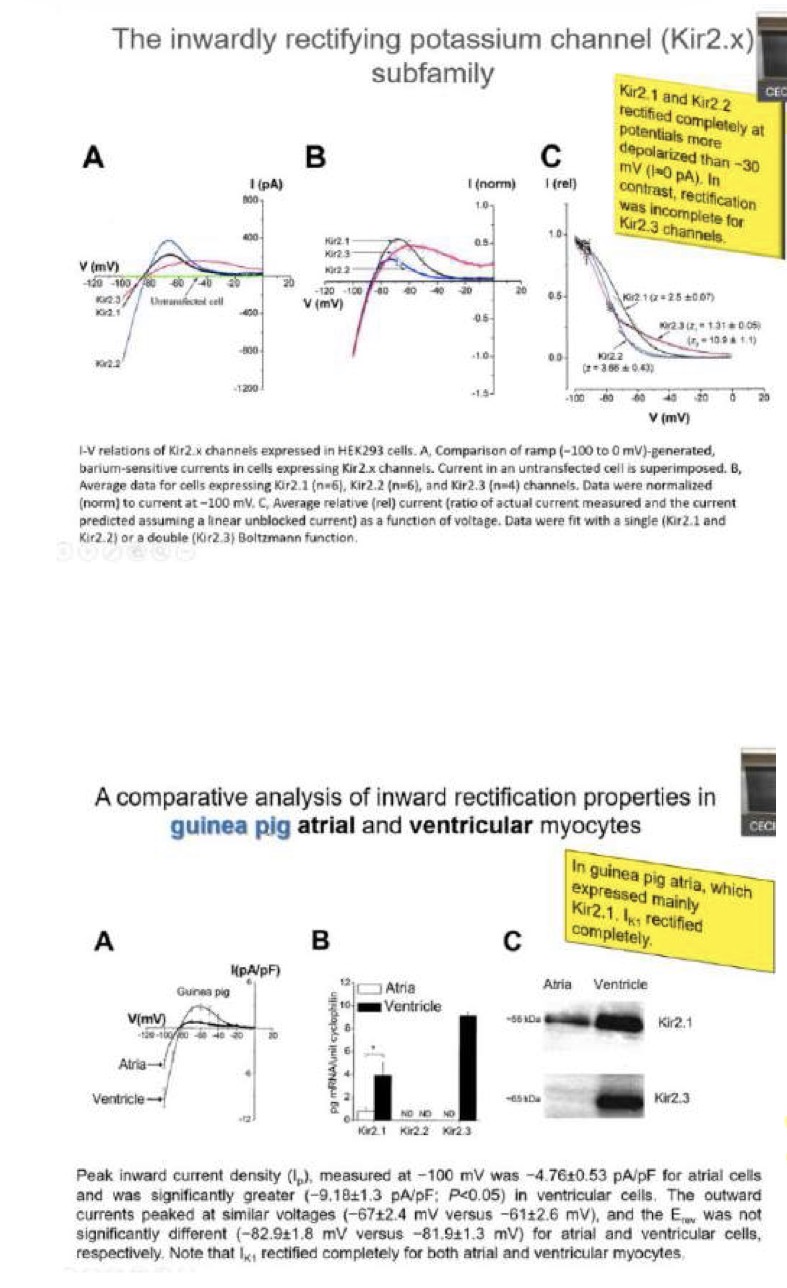
Isoforme della famiglia Kir e differenze regionali
La corrente I(K1) è trasportata dai canali della famiglia Kir (inwardly rectifying), che presenta 3 isoforme: Kir2.1, Kir2.2 e Kir2.3.
• Kir2.1 e Kir2.2: Raggiungono un picco uscente intorno a -70 mV, poi declinano mostrando una rettificazione completa (scompaiono per valori superiori a -20 mV).
• Kir2.3: Ha un picco a -60 mV, ma la rettificazione è incompleta (la corrente diminuisce ma non scompare del tutto vicino allo 0).
• Differenze Atrio-Ventricolo:
• Il ventricolo esprime un mix di isoforme (Kir2.1 e Kir2.3) e mostra una rettificazione completa.
• Nell'atrio, il livello di espressione è diverso (es. nelle pecore prevale Kir2.3, nelle cavie Kir2.1). In generale, nell'atrio è presente una quota di corrente uscente anche vicino allo 0 mV (rettificazione incompleta). Questo contribuisce a posizionare il plateau più in basso e a rendere la durata del potenziale d'azione atriale molto più breve (150 ms) rispetto a quello ventricolare (300/350 ms).
Sensibilità al potassio extracellulare della I(K1) e correnti ligando dipendenti
• Potassio Extracellulare: La I(K1) è sensibile ai livelli di K+ extracellulare. Un aumento del K+ esterno (che modifica il potenziale di equilibrio) porta a un aumento paradossale della corrente uscente e della conduttanza (soprattutto per l'isoforma Kir2.1, a causa di modifiche conformazionali). Questo principio è usato nella cardioplegia (es. durante i trapianti): soluzioni ad alto K+ inattivano i canali del Na+ e fermano il cuore reversibilmente.
• Correnti ligando-dipendenti: Esistono altre correnti con rettificazione in ingresso, come la I(K(ATP)). Si attiva quando i livelli di ATP scendono (es. durante un'ischemia), rinforzando l'effetto della I(K1) per spegnere la cellula, accorciare il potenziale e proteggerla mettendola in stato di quiescenza metabolica.
Le correnti ripolarizzanti
La famiglia delle correnti Delayed Rectifier è composta da tre componenti (correnti di potassio K+) responsabili della ripolarizzazione (escono dalla cellula riportando il potenziale di membrana verso valori negativi):
1. I(Ks) (Slow):
• Si attiva molto lentamente e non presenta inattivazione tempo-dipendente.
• Mostra una relazione intensità-voltaggio lineare (comportamento ohmico) al di sopra di -20/-30 mV.
• Al di sotto dei -20 mV, la corrente è assente (rettificazione perfetta).
• Il gating è semplice: transizione da chiuso ad aperto (lenta, non raggiunge il picco massimo in un battito normale) e da aperto a chiuso (deattivazione causata dall'iperpolarizzazione).
• È altamente sensibile alla stimolazione beta-adrenergica, che la potenzia, riducendo la durata del plateau.
2. I(Kur) (Ultra-rapid):
• Ha caratteristiche analoghe alla I(Ks) (gating semplice, rettificazione in uscita), ma si differenzia per la cinetica molto più veloce (ordine di decine di ms, contro le centinaia della I(Ks)).
• È poco espressa nel ventricolo ma molto espressa nell'atrio, contribuendo ulteriormente alla differenza di durata del potenziale d'azione tra le due camere.
3. I(Kr) (Rapid):
• Portata dal canale hERG, differisce notevolmente dalle altre.
• Possiede due porte: una di attivazione (cinetica lenta) e una di inattivazione (cinetica rapidissima, circa 1 ms). Questo determina una "delayed rectification" (rettificazione ritardata).
• Meccanismo: Durante l'inizio del potenziale d'azione, il canale si apre ma si inattiva quasi istantaneamente, permettendo il passaggio di pochissima corrente. Durante la ripolarizzazione, scendendo verso i -60 mV, l'inattivazione viene rimossa velocemente, mentre la porta di attivazione è ancora aperta. Questo crea una "finestra temporale" (window current) che permette un grosso flusso uscente di K+, fondamentale per la ripolarizzazione finale. Non è regolata da stimoli beta-adrenergici.
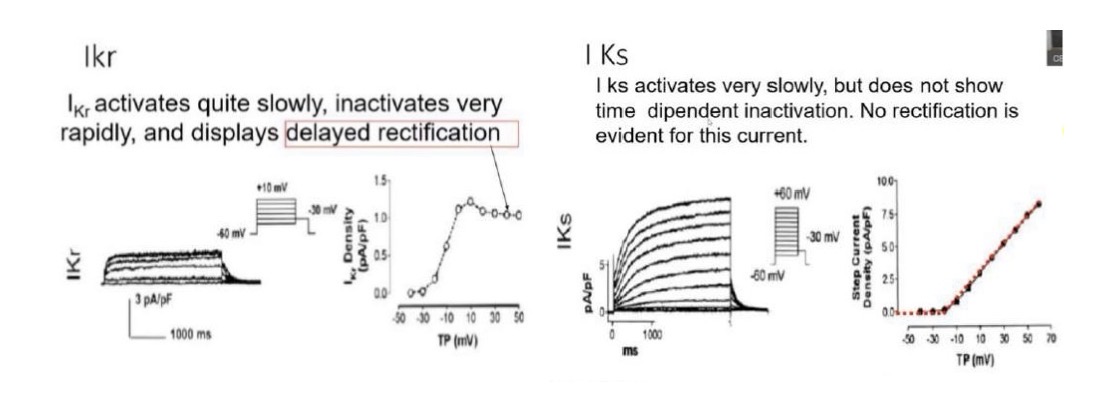
Correnti I(Kur)
La corrente I(Kur) ha un comportamento analogo alla I(Ks) ma si differenzia per una cinetica molto più rapida: raggiunge il picco in qualche decina di millisecondo.
• Distribuzione: La densità di questa corrente varia fortemente in base alla sede. È tipica del miocardio atriale, mentre nel ventricolo è quasi assente.
• Ruolo fisiologico: Questa distribuzione fa sì che il potenziale d'azione atriale duri meno di quello ventricolare. Nell'atrio, il bilanciamento delle correnti di calcio durante il plateau è affidato a questi canali con cinetica di apertura e chiusura più rapida.
• Farmacologia: Questi canali rendono l'atrio sensibile a farmaci diversi. Ad esempio, bloccanti specifici della corrente I(Kur) sono stati testati per la cura della fibrillazione atriale.
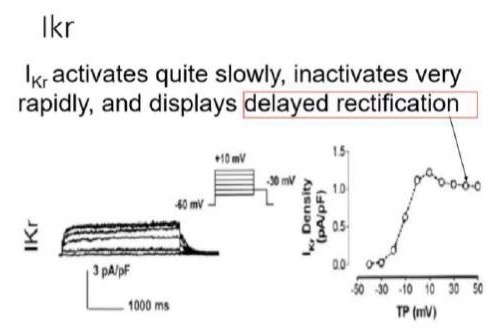
Correnti I(Kr)
La corrente I(Kr) è caratterizzata da un'attivazione lenta, un'inattivazione molto rapida e mostra una rettificazione su valori di potenziale positivi. Il canale responsabile di questa corrente è il canale hERG (espresso anche in altri tessuti, come il sistema nervoso).
• Meccanismo a due porte: Presenta una voltaggio-dipendenza sia in apertura che in chiusura, governata da due porte con velocità diverse:
1. Un cancello di apertura/chiusura che si muove lentamente.
2. Una porta di inattivazione molto rapida.
• Comportamento durante il potenziale d'azione:
• Depolarizzazione: Innesca entrambe le porte. Il cancello si apre lentamente, ma la porta di inattivazione si chiude quasi subito. Il frangente di tempo in cui il canale è permeabile (aperto e non inattivato) è brevissimo.
• Ripolarizzazione: La porta di apertura/chiusura si chiude lentamente, mentre l'inattivazione viene rimossa velocemente. Questo crea un lungo intervallo di permeabilità elevata e possibilità di transito per il potassio.
• Protocollo sperimentale: Se si impone uno step da -80 mV a +30 mV, si registra una corrente piccolissima (il canale si inattiva subito). Se poi si porta il potenziale da +30 mV a -60 mV (sotto la soglia di inattivazione), la corrente registrata è molto grande perché la porta di apertura non si è ancora chiusa, ma il canale è già uscito dall'inattivazione.
• Ruolo funzionale: Questo meccanismo contribuisce alla fase 3 (completamento della ripolarizzazione). Quando la corrente del calcio si spegne e la I(Ks) riporta il potenziale verso lo zero o valori negativi, la corrente portata da hERG inizia ad avere un significato cruciale grazie alla sua "finestra di conduttanza".
Patologie associate al canale hERG
Il canale hERG è fondamentale per una corretta ripolarizzazione, e le sue alterazioni portano a conseguenze cliniche:
• Sindrome del QT lungo congenita: Mutazioni del canale hERG sono associate a questa sindrome (l'intervallo QT sull'elettrocardiogramma descrive la fase di ripolarizzazione). La mutazione allunga questo intervallo, causando un prolungamento del potenziale d'azione (la perdita di correnti di potassio ha sempre questo effetto).
• Sindrome del QT lungo acquisita: Molti farmaci possono influenzare negativamente l'attività di hERG, creando una condizione simile a quella genetica.
• Rischio di Aritmie: Il prolungarsi della durata del potenziale d'azione espone la cellula al rischio di depolarizzazioni anomale che, se raggiungono la soglia, possono innescare un potenziale d'azione "immaturo", portando ad aritmie.
Adattamento alla frequenza (memoria del canale I(Ks))
Sotto stimolo beta-adrenergico (es. esercizio fisico), la frequenza cardiaca aumenta.
• I canali I(Ks) hanno una chiusura molto lenta. Quando i battiti sono ravvicinati, questi canali non fanno in tempo a richiudersi completamente tra un potenziale d'azione e l'altro.
• Di conseguenza, all'inizio del battito successivo, è già presente una quota di canali aperta e disponibile dal battito precedente. Questo meccanismo permette al miocardio di lavorare efficientemente ad alta frequenza.