Aula 0- QOF
1/34
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
35 Terms
Quais as características do modelo de Bohr ?
núcleo denso no centro
Núcleo = prótons e nêutrons
Elétrons dispostos em órbitas no espaço do volume
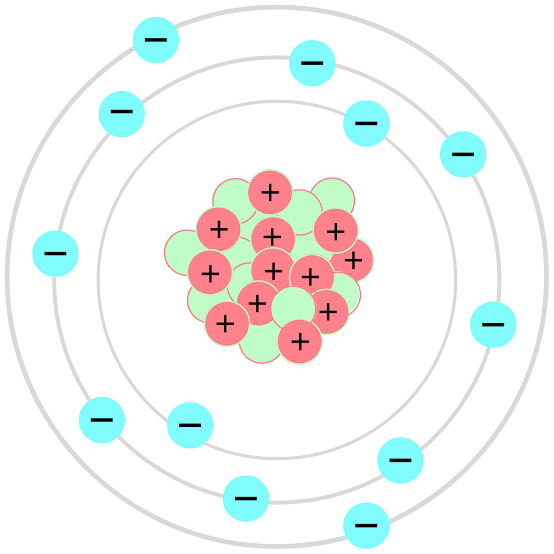
Como os elementos se movem de acordo com o modelo de bohr ?
orbitais circulares - camadas
Relações do elétron com a camada energética segundo o modelo de bohr
atração com os prótons no núcleo os mantém no lugar
Elétrons em diferentes camadas se repelem
Mais perto do núcleo = menos energia
Como elétrons mudam de camada no modelo de bohr?
Absorvendo energia saltam para uma camada mais energética
Liberando energia voltam a camada original
Quais os níveis energéticos (em ordem crescente) no modelo de bohr?
K , L , M, N, O, P, Q
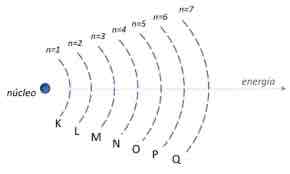
O que é a camada de valência de um átomo
Camada mais externa que os elétrons chegam no átomo ( mais próximo de Q é número mais)
Como a camada de valência influência a realidade dos elementos?
Os elétrons na camada de valência são mais fáceis de serem usados/ roubados - interação com outros átomos
O que é ter uma camada de valência completa e como isso influencia o átomo?
Uma camada completa tem 8 elétrons, isso estabiliza e diminui a reatividade do átomo
Como identificar o número de elétrons na camada de valência?
distribuição eletrônica em o modelo de Linus Pauling- tendo a última camada preenchida é só contar os elétrons nesta horizontal
Família na tabela periódica
Oq são subniveis de energia ?
Camadas menores entre os níveis de energia
Quais os subniveis de energia em ordem crescente de energia?
S, P, D, F, (G, H - teóricos)
Qual a relação entre o número do nível energético e a quantidade de subniveis presente ?
Número do nível energético é a quantidade de subniveis presentes nesse
Quantos subniveis tem cada nível?
diagrama de linus pauling
K=1 , L=2, M=3, N= 4, O= 4, P= 3, Q= 2
Oq são orbital em um átomo?
Regiões nas camadas com maior probabilidade de encontrar um elétrons
Quantos elétrons cabe em um orbital?
No máximo 2 elétrons
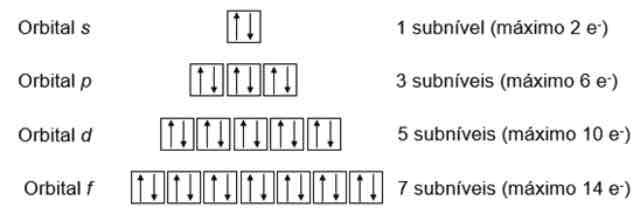
Qual a relação dos orbitais nos subniveis ?
S= 1 orbital
P= 3 orbitais
D= 5 orbitais
F= 7 orbitais
Como os elementos estão organizando-se na tabela periódica?
Os elementos são organizados em ordem crescente de número atômico e propriedades químicas/físicas semelhantes
Oq são as famílias na tabela periódica?
Colunas verticais- elementos de propriedade químicas semelhantes por conta da camada de valência
Como são distribuídas as camadas de valência nas famílias?
Número da família = número de elétrons na camada de valência
Importância da tabela periódica
Ajuda a prever o comportamento dos elementos e entender suas propriedades
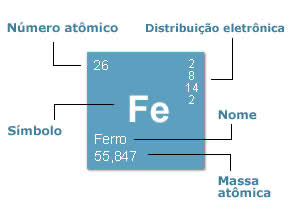
Quais as informações fornecidas pela tabela periódica?
Número atômico = número de prótons = número de elétrons
Massa atômica
Símbolo do átomo
Características dos halogênios
família 17
Alta eletronegatividade = alta reatividade
Forma compostos iônicos
Substitui elementos ou grupos em uma reação molecular
Forma grupos funcionais
Funciona como catalisadores de reagentes
Quais os elementos da família Halogênio
Flúor (F), cloro (C), bromo (Br), iodo (I), astato (At)
Como os halogênio fazem ligações iônicas
Transferência de elétrons, a alta eletronegatividade mantém os elétrons mais próximo dos halogenios os deixando com uma carga negativa
Qual a importância do oxigênio na química?
Está presente em muitas moléculas orgânicas- fundamental para reações biológicas
Sobre o oxigênio: Qual é o número atômico, número de elétrons de valência e a distribuição eletrônica?
O(8)= 6e - 1S2, 2S2, 2P2
Sobre o nitrogênio : Qual é o número atômico, número de elétrons de valência e a distribuição eletrônica?
N(7)= 5e - 1S2, 2S2, 2P1
Sobre o carbono : Qual é o número atômico, número de elétrons de valência e a distribuição eletrônica?
C(6)=4e - 1S2, 2S2
Sobre o hidrogênio : Qual é o número atômico, número de elétrons de valência e a distribuição eletrônica?
H(1)=1e - 1S1
No que as propriedades periódicas se baseiam ?
Número atômico- aumenta ou diminui dentro da família e do período
O que é o raio atômico e como está na tabela?
Distância do núcleo a camada de valência
Aumenta de cima pra baixo e direita para a esquerda
O que é a eletronegatividade e como está na tabela ?
Capacidade de um átomo de atrair elétrons de outros átomos fazendo uma ligação, nesta ficando negativo
Aumenta de baixo para cima e da esquerda para a direita
Por que gases nobres não são classificados na eletronegatividade?
Gases nobres são perfeitos na regra do octeto = tem 8e na camada de valência, sendo pouquíssimo atraentes de elétrons
Qual a relação da eletronegatividade com o raio atômico ?
Quanto mais próximo o elétron estiver do núcleo (menor o raio) = maior a atração dos portos sobre os elétrons
Por que os halogênio são tão eletronegativos?
Por precisar de apenas um elétron para o equilíbrio e a forte atração dos prótons