Hele pensum i kjemi 2
1/262
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
263 Terms
Massevirkningsloven
Forholdet mellom produkter og reaktanter opphøyd i hver sin tilhørende koeffisient.
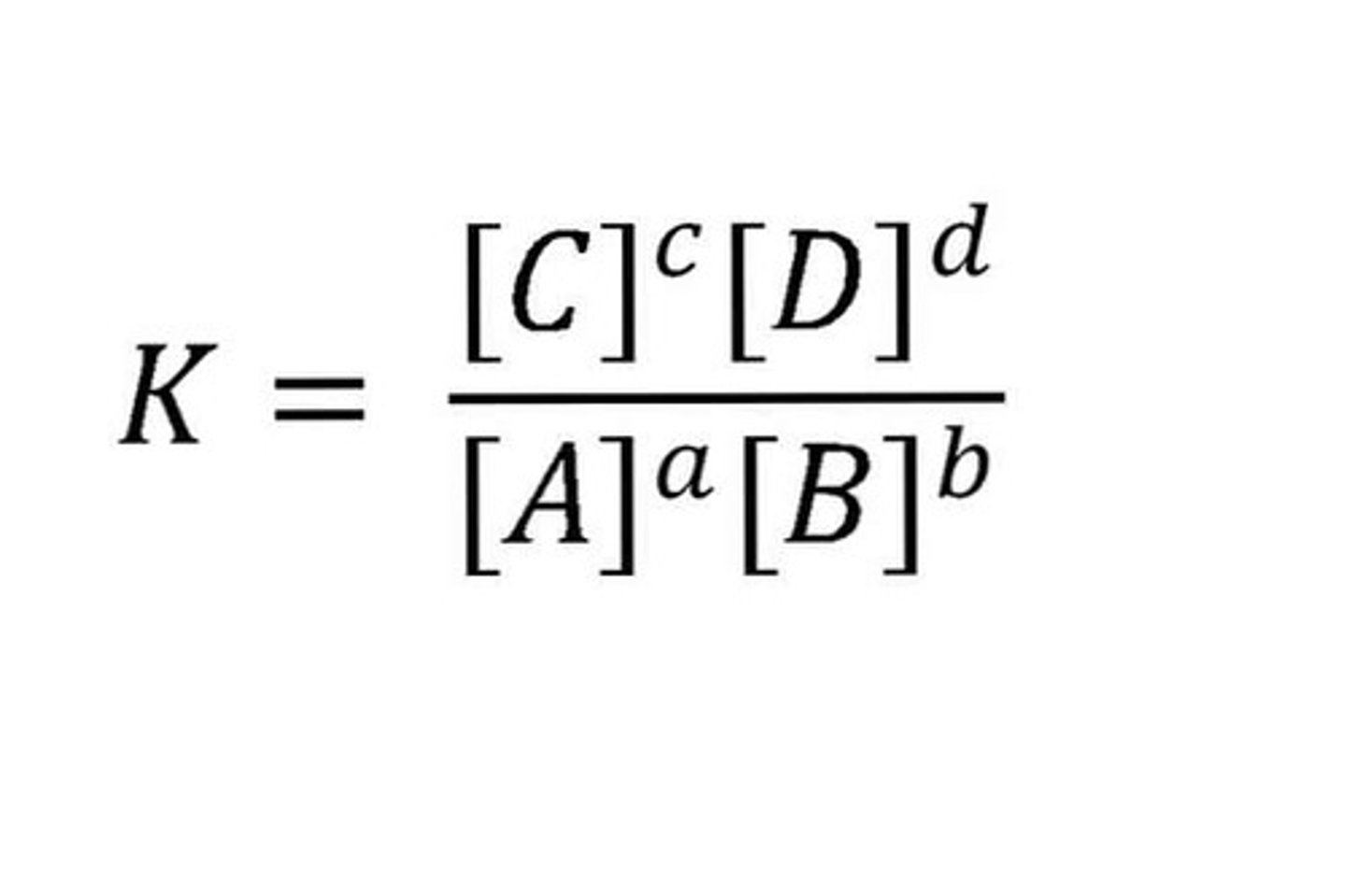
Likevektskonstanten
Forholdstall mellom produkter og reaktanter ved likevekt. Den har symbolet K.
Størrelsen av likevektskonstanten
Størrelsen forteller om det er flest reaktanter eller flest produkter i en reaksjonsblanding med likevekt. K > 1000 betyr at det er mange flere produkter enn reaktanter. K < 0,001 betyr at det er mange flere reaktanter enn produkter. 0,001 < K < 1000 betyr at det er omtrent like mange produkter og reaktanter.
Le Châteliers prinsipp
Enhver ytre endring som påvirker likevekten i et system, vil medføre at systemet justerer likevekten slik at endringen motvirkes.
Reaksjonskvotienten Q
Forholdstall ved enhver sammensetning av reaktanter og produkter i en reaksjonsblanding. Beregnes på samme måte som K.
Q < K
Reaksjonen vil gå mot høyre for at det skal bli likevekt. Dvs. at det dannes flere produkter.
Q > K
Reaksjonen vil gå mot venstre for at det skal bli likevekt. Dvs. at det dannes flere reaktanter.
Q = K
Reaksjonen er i likevekt.
Løsning
En homogen blanding av to eller flere stoffer. Molekylene eller ionene av de løste stoffene er jevnt fordelt i løsemidlet.
Coulombs lov
Kreftene mellom to elektrisk ladde partikler øker med økende ladning og minker med økende avstand mellom partiklene.
Generell regel for løselighet
Alle salter av alkalimetaller, salter med ammoniumioner og salter med nitrationer er lettløselige, fordi disse er relativt store og har liten ladning, slik at ionebindingene er lettere å bryte.
Løselighet til et fast stoff i en væske
Den stoffmengden som maksimalt kan bli løst opp i løsemidlet ved en bestemt temperatur.
Mettet løsning
Når det ikke kan løses mer av det faste stoffet i løsningen. Da er det en heterogen likevekt mellom det løste og det faste stoffet.
Heterogen likevekt
En likevekt der ulike faser inngår.
Overmettet løsning
En løsning der det er løst mer stoff enn i en mettet løsning. Dette kan gjøres ved å øke temperaturen, og deretter nedkjøle den sakte slik at det ikke utfelles faste krystaller. Den er ustabil, og det skal lite til før det skjer utkrystallisering av fast stoff.
Løsningsreaksjon
Når et salt løser seg i vann, brytes ionebindingene mellom ionene i saltkrystallene. Ionene binder seg til vannmolekyler med ion-dipolbindinger (de hydratiseres).
Fellingsreaksjon
Reaksjon der to saltløsninger med ioner blandes, og vi får en utfelling av faste saltkrystaller.
Tilskuerioner
Ionene som er til stede i en fellingsreaksjon, men som ikke danner bunnfall.
Løselighetsproduktet Ksp
Produktet av ionekonsentrasjonene i løsningen (der eksponenten til hver ionekonsentrasjon er lik koeffisienten til ionet i reaksjonslikningen). Jo mindre verdien er, desto lavere er løseligheten til et stoff.
Fellesioneffekten
Når vi løser et salt i et løsemiddel som på forhånd inneholder et av ioneslagene i saltet, blir løseligheten til saltet mindre enn om det var blitt løst i rent vann.
Ioneproduktet Q
Ved å regne ut ioneproduktet og sammenlikne med løselighetsproduktet kan vi finne ut om det blir utfelling av et lite løselig salt når vi blander saltløsninger. Finner det ved å ta produktet av ionekonsentrasjonene (opphøyd i koeffisienten).
Q = Ksp
Løsningen er mettet. Vi har likevekt og får ingen utfelling.
Q > Ksp
Løsningen kan betraktes som overmettet, og vi får utfelling.
Q < Ksp
Alt stoff er oppløst. Løsningen er umettet og vi får ingen utfelling.
Redoksreaksjon
Kjemisk reaksjon der et stoff tar opp elektroner, mens et annet stoff gir fra seg elektroner.
Reduksjon
Hvis oksidasjonstallet til et atom minker. Det vil si at et stoff helt eller delvis tar opp elektroner.
Oksidasjon
Hvis oksidasjonstallet til et atom øker. Det vil si at et stoff helt eller delvis gir fra seg elektroner.
Reduksjonsmiddel
Et stoff som reduserer noe annet, og selv blir oksidert.
Oksidasjonsmiddel
Et stoff som oksiderer et annet, og selv blir redusert.
Oksidasjonstall
En tenkt ladning som et atom ville hatt hvis bindingselektronene var blitt helt overført til det mest elektronegative atomet i en kjemisk binding. Hjelper oss å holde orden på elektronoverføringen i redoksreaksjoner. Oppgis som romertall med ladninger.
Regler for oksidasjonstall
1. Okstallet til et grunnstoff i fri tilstand er 0.
2. Okstallet til et ion skal være lik ioneladningen.
3. Summen av okstallene til atomene i et molekyl eller i en nøytral formelenhet av en ioneforbindelse skal være 0.
4. Summen av okstallene i et sammensatt ion er lik ioneladningen.
5. Okstallet til fluor i kjemiske forbindelser er -I.
6. Okstallet til alkalimetaller i kjemiske forbindelser er +I.
7. Okstallet til jordalkalimetaller i kjemiske forbindelser er +II.
8. Okstallet til hydrogen i kjemiske forbindelser er vanligvis +I.
9. Okstallet til oksygen i kjemiske forbindelser er vanligvis -II.
Oksidasjonstall og unntak
Det finnes tilfeller der oksidasjonstallene avviker fra det som er vanlig. Det gjelder blant annet hydrogen i hydrider, oksygen i peroksider og halogener i forbindelser med hverandre eller med oksygen. For halogener i forbindelse med hverandre, vil halogenet med høyest elektronegativitet ha oksidasjonstall -I og det med lavest elektronegativitet vil ha +I. I stoffer mellom halogener og oksygen har oksygen okstall -II.
Frie radikaler
Forbindelser som inneholder et uparet elektron. Er veldig reaktive og reagerer med mange stoffer rundt seg.
Oksidativ
God til å ta elektroner fra andre stoffer.
Antioksidant
Et stoff som selv lett lar seg oksidere, og som kan hindre at frie radikaler gjør skade på celler eller viktige molekyler i kroppen.
Balansering av redoksreaksjoner
Vi deler reaksjonen opp i oksidasjon og reduksjon, balanserer de to halvreaksjonene for seg, og slår dem så sammen.
Redokstitrering
Titrering der standardløsningen oksiderer eller reduserer stoffet i prøveløsningen. Brukes for å finne stoffmengden og konsentrasjonen av et stoff.
Galvanisk element
Et system der kjemisk energi blir overført til elektrisk energi i en spontan redoksreaksjon. Består av to kamre med løsninger, med en elektrode i hver løsning. Mellom kamrene er det en saltbro.
Spontan reaksjon
En reaksjon som går av seg selv uten at vi trenger å tilføre noe ekstra energi.
Elektrode
Metallstaver som er ledere der det foregår en redoksreaksjon.
Saltbro
Inneholder en saltløsning av et lettløselig salt, som er i kontakt med stoffene i kamrene i en galvanisk celle. Ionene utlikner ulikheten i ladning som oppstår, og danner en lukket krets. Ionene må ikke reagere med noen av de andre stoffene i elementet.
Anode
Elektroden der det skjer en oksidasjon.
Katode
Elektroden der det skjer en reduksjon.
Cellediagram
Måte å representere en galvanisk celle på. Anoden står til venstre, katoden til høyre. Faseskiller markeres med en loddrett strek, mens saltbroen markeres med to streker.
Reduksjonspotensial
Sier noe om hvor lett et stoff blir redusert.
Spenningsrekka
Oversikt over reduksjonspotensialet til ulike halvceller, målt mot standard hydrogenelektrode.
Standard hydrogenelektrode
Referanseelektrode som vi bruker til å sammenlikne elektroder, slik at vi kan rangere reduksjonspotensialet.
Spontanitet
E_celle > 0
E_celle = E_katode + E_anode
Uedle metaller
Metaller som er under standardelektroden i spenningsreakka, og har reduksjonspotensial mindre enn 0. De oksideres spontant med saltsyre. Reagerer ofte med oksygen og vann.
Edle metaller
Metaller som har reduksjonspotensiale høyere enn 0, og befinner seg over standardelektroden i spenningsrekka. Oksideres ikke med saltsyre. Lar seg ikke korrodere.
Korrosjon
Oksidasjon av uedle metaller.
Rust
Korrosjonsprodukt. Er en blanding av jernoksider og hydroksider og dannes ved at jern blir oksidert og oksygengass redusert når det er vann til stede.
Rustbeskyttelse
Å dekke jernmetallet med lakk eller maling, eller å galvanisere jernet.
Galvanisering
Bruker et metall som blir lettere oksidert enn jern. Det virker som offeranode.
Irr
Kobber reagerer med fuktig luft og danner dobbeltsalter. Disse er grønnfarget.
Beskyttende oksidlag
Aluminium reagerer spontant med oksygen, og det dannes et tynt lag med aluminiumoksid som beskytter aluminium mot videre oksidasjon. Andre metaller som danner oksidlag, er krom og magnesium.
Batteri
Ett eller flere galvaniske elementer som omdanner kjemisk energi til elektrisk energi. Anoden fungerer som negativ pol, siden den leverer elektroner til kretsen. Katoden er den positive polen. Hvilke typer halvceller som benyttes, er avhengig av batteritypen.
Primærbatteri
Engansbatteri, siden omdanningen fra kjemisk til elektrisk energi er irreversibel.
Sekundærbatteri
Oppladbart batteri, siden det er mulig å omdanne elektrisk energi til kjemisk energi for å lade batteriet. Når redoksreaksjonen går spontant, frigjøres det elektroner, og batteriet leverer elektrisk strøm. Når batteriet er tomt, kan elektrisk strøm brukes til å gjendanne utgangsstoffene.
Batterikapasitet
Et mål for hvor mye ladning et fulladet batteri maksimalt kan levere. Måles i Ah eller mAh.
Q = I * t
Ladning = strøm * tid
1 Ah = 3600 As = 3600 C
Elektrisk strøm
Et mål for antallet ladninger som passerer et visst sted per tidsenhet. Måles i A.
I = Q/t
Batterienergi
Den totale energien i joule som et batteri kan levere, er avhengig av kapasiteten (i coulomb) og spenningen (i volt):
E = Q * U
Batterienergi = kapasitet * spenning
Elektrolyse
En ikke-spontan redoksreaksjon som skjer ved hjelp av elektrisk strøm. Elektrisk energi omdannes til kjemisk energi. Anoden er positiv pol, og katoden er negativ pol (motsatt av galvaniske elementer). Oksidasjonen skjer på anoden, og reduksjonen på katoden.
Elektrolyse av vann
Vann spaltes til hydrogengass og oksygengass ved bruk av strøm.
Elektrolytt
En løsning med ioner som leder elektrisk strøm. Kan lages ved å tilsette salter eller andre stoffer som danner ioner i vann, slik at ledningsevnen til vannet blir bedre. Da kan en elektrolyse skje mer effektivt. Tilsetter man elektrolytter som inneholder stoffer med høyere reduksjonspotensial enn vann, vil disse stoffene reduseres i stedet for vann ved katoden ved elektrolyse.
Smelteelektrolyse
Vannfri elektrolyse. Kan brukes for å framstille metaller med lavt reduksjonspotensial, som aluminium, kalium natrium og litium.
Inerte elektroder
Elektrodene reagerer ikke selv under elektrolysen, og de tåler høye temperaturer.
Utbytte i en elektrolyse
Ut fra antallet elektroner som blir overført kan vi finne stoffmengden av stoffet som blir framstilt ved hjelp av reaksjonslikningen. n_(elektroner) = (I * t)/F.

Reaksjonstyper i organisk kjemi
Substitusjon
Addisjon
Eliminasjon
Kondensasjon
Hydrolyse
Oksidasjon
Reduksjon
Substitusjon
Et atom eller en atomgruppe i et organisk molekyl byttes ut med et annet atom eller en annen atomgruppe.
En vanlig stoffgruppe som ofte reagerer eller blir dannet, er halogenerte hydrokarboner.
Halogenerte hydrokarboner
Hydrokarboner som har ett eller flere halogenatomer bundet til seg.
Addisjon
Et lite molekyl binder seg til en dobbelt- eller trippelbinding i et annet molekyl, og det blir dannet et nytt molekyl. Omvendt av eliminasjon.
Det er vanlig at alkener inngår.
Det er mulig å addere ulike molekyler til en karbon-karbon-dobbeltbinding:
1. Halogener, som Cl2 og Br2. Danner dihalogenerte hydrokarboner.
2. Syrer. Danner halogenerte hydrokarboner.
3. Vann. Danner alkoholer. En syre er katalysator i reaksjonen.
Eliminasjon
Et (lite) molekyl blir spaltet av fra et større molekyl slik at det blir dannet en dobbelt- eller trippelbinding mellom karbonatomer i det nye molekylet. Omvendt av addisjon.
Kondensasjon
To molekyler binder seg sammen til et større molekyl ved at det spaltes av et vannmolekyl. Omvendt av hydrolyse.
Sentralt i dannelse av de funksjonelle gruppene til estere, etere og amider.
Dannelse av ester
Når en karboksylsyre reagerer med en alkohol, går de sammen i en kondensasjonsreaksjon. Produktene blir en ester og et vannmolekyl.
Dannelse av amid
En karbonylgruppe (C=O) er bundet til et nitrogenatom, generelt CONR2. Dannes gjennom kondensasjon når en karboksylsyre og et amin reagerer, og det spaltes av vann.
Dannelse av eter
Dannes gjennom kondensasjon når to alkoholer reagerer og det spaltes av vann.
Hydrolyse
Et større molekyl tar opp et vannmolekyl som spaltes til to mindre molekyler. Omvendt av kondensasjon.
Oksidasjon
Et karbonatom får bindinger til oksygenatomer og/eller mister bindinger til hydrogenatomer. Da overføres elektrontetthet fra karbonatomet til oksygenatomet, som er mer elektronegativt. Motsatt av reduksjon.
Viktig for alkoholer.
Reduksjon
Et karbonatom mister bindinger til oksygenatomer og/eller får bindinger til hydrogenatomer. Da overføres elektrontetthet til karbonatomet. Motsatt av oksidasjon.
Primære alkoholer
Alkoholer der OH-gruppa er bundet til et karbonatom, som igjen er bundet til bare ett karbonatom.
Kan bli oksidert i to steg. Først til aldehyd, og så til karboksylsyre.
Sekundære alkoholer
Alkoholer der OH-gruppa sitter på et karbonatom som er bundet til to karbonatomer.
Kan bli oksidert til ketoner.
Tertiære alkoholer
Alkoholer der OH-gruppa er bundet til et karbonatom som igjen er bundet til tre karbonatomer.
Kan ikke bli oksidert, fordi karbonatomet ikke kan ha flere enn fire kovalente bindinger.
Skal vi oksidere en tertiær alkohol, må vi bryte en C-C-binding for å få plass til flere C-O-bindinger. Dette krever kraftige reagenser eller høy temperatur.
Vanlige oksidasjonsmidler
Stoffer med overgangsmetaller som har et høyt oksidasjonstall, som KMnO_4 eller K_2CrO_4.
Oksidasjonstall på organiske forbindelser
Vi ser kun på oksidasjonstallet til det karbonatomet som er involvert i redoksreaksjonen.
1. Andre karbonatomer har oksidasjonstall 0.
2. Oksygenatomer har oksidasjonstallet -II. Hydrogenatomer har oksidasjonstall +I.
Summen av oksidasjonstallene må være 0.
Reaksjonsmekanisme
Modell som viser hvordan en reaktant blir gjort om til et produkt, steg for steg. Vi bruker piler for å vise hvordan elektronpar vandrer.
Vandring av elektroner
Kjemiske bindinger brytes eller dannes. Vi bruker piler for å markere at elektroner vandrer.
Nukleofil
Elektronrik. Et stoff eller et ion med høy elektrontetthet. De kan være nøytrale eller ladde. Mange inneholder et elektronegativt atom med ett eller flere frie elektronpar eller en negativ ladning. Angriper elektrofiler pga. elektrostatisk tiltrekning og danner nye kovalente bindinger.
Elektrofil
Elektronfattig forbindelse. Et stoff eller et ion med lav elektrontetthet. Mange har positiv ladning. Blir angrepet av nukleofiler pga. elektrostatisk tiltrekning.
Vi finner også elektrofile karbonatomer, som ofte er bundet til et halogen, som gjør at karbon-halogen-bindingen blir polarisert. Siden halogenene er mer elektronegative enn karbon, vil det bli en liten positiv ladning på karbonatomet.
Noen positive ioner er også elektrofiler. F.eks. protoner og karbokationer.
Karbokation
Karbonatomer med positiv ladning. De har tre kjemiske bindinger, ikke fire. De blir ofte dannet som et mellomprodukt i addisjonsreaksjoner. De er veldig reaktive og reagerer raskt videre (med nukleofile stoffer).
Reaksjonsmekanisme for substitusjon
Nukleofilen angriper elektrofilen. Siden karbonatomer ikke kan ha fem bindinger, må en av bindingene brytes ved at et stoff går ut av molekylet. Det mest elektronegative tar med seg bindingselektronene. Deretter dannes binding mellom nukleofilen og elektrofilen.
Reaksjonsmekanisme for addisjon
Den elektronrike dobbeltbindingen angriper et elektrofilt atom. Da vil det ene karbonatomet være et karbokation. Karbokationet angripes av det andre ionet, slik at produktet blir dannet. Husk på Markovnikovs regel.
Markovnikovs regel
I addisjonsreaksjoner bindes hydrogenatomet til det karbonatomet som har flest hydrogenatomer fra før.
Reaksjonsmekanisme for eliminasjon
Alkoholer kan elimineres til alkener ved bruk av en syrekatalysator (ofte svovelsyre eller fosforsyre). Mekanismen skjer i tre steg. Først tar OH-gruppa opp et hydrogenion. Deretter går vann ut, slik at det blir dannet et karbokation. Til slutt blir en C-H-binding i naboposisjon til karbokationet brutt og danner en dobbeltbinding mellom de to karbonatomene. Da mister H-atomet et elektronpar og blir omdannet til et hydrogenion.
Zaitsevs regel
I eliminasjonsreaksjoner fjernes et H+-ion fra det karbonatomet som er nabo med karbokationet og har færrest hydrogenatomer fra før. Det blir dannet en dobbeltbinding.
Syntese
Prosess der vi lager et stoff fra et annet stoff ved å gjennomføre ulike reaksjoner.
Målmolekyl
Stoffer vi ønsker å lage i en syntese.
Utbytte i en syntese
Sier noe om stoffmengden som lages, sammenliknet med stoffmengden av begrensende reaktant som ble brukt. Vanligvis i prosent.
u (%) = n_(produkt) / n_(begrensende reaktant) * 100%
Syntese i mikroskala
I liten skala. Godt egnet til forsøk. Fordeler er at vi forbruker mindre mengder av kjemikalier, får mindre avfall og reduserer risikoen og farene ved eksperimentet.
Syntese i makroskala
Syntese i større skala. Godt egnet når man må ha tilgang på store mengder stoff, f.eks. i industrien.