6 Vodne raztopine kislin in baz
1/12
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
13 Terms
Arrheniusova definicija kislin in baz
kisline - snovi, ki v vodni razt. disociirajo na vodikove ione (npr. HCl →← H+ + Cl-)
baze - snovi, ki v vodi disociirajo na hidroksidne ione (npr. NaOH → Na+ + OH-)
ni popolna → baze omejene le na snovi, ki vsebujejo OH- ione
velja le za vodne razt.
Kaj je nevtralizacija?
ionska reakcija, protoni reagirajo s hidroksidnimi ioni, nastanejo molekule vode (slabo disociirana snov)
med kislinami in bazami, nastane sol
lažje poteče v vodni razt.
Brønstedova definicija kislin in baz
kisline - snovi, ki oddajo protone
baze - snovi, ki sprejemajo protone
protoliza - reakcija prehoda protona od kisline na bazo
kislina in baza sodelujeta z njunima konjugiranima oblikama (v ravnotežju)
Pojem kislina-baza ni vezan na snov, ampak …
… na lastnost, da neka snov odda oz. sprejme H+
amfolit - snov, ki se v kombinaciji z različnimi drugimi snovmi obnaša kot kislina ali kot baza (npr. voda)
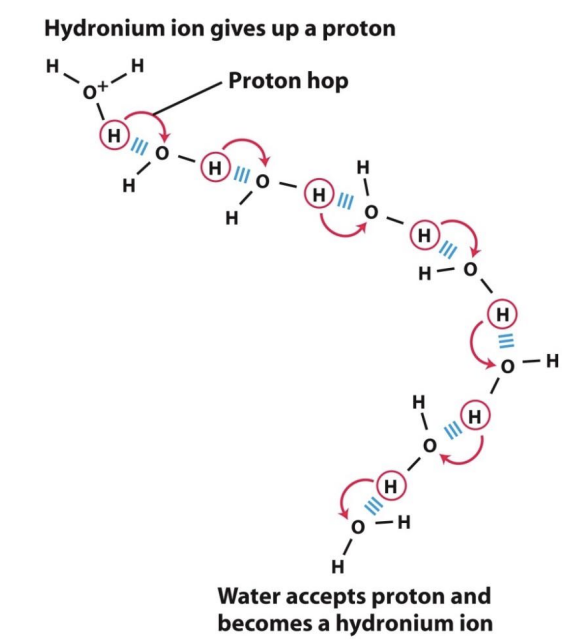
Zakaj rečemo, da je voda rahlo ionizirana?
oksonijev ion je v vodnih razt. nosilec kislih lastnosti → kratkoživ (10-13 s)
molekule vode si protone neprestano podajajo (štafetni mehanizem, bistveno hitrejši od difuzije)
biološki pomen: prenost protonov skozi tilakoidno membrano
Kaj opisuje pH? Kako izgleda pH lestvica?
koncentracijo oksonijevih ionov
Kw = [H3O+][OH-] = 1×10-14 M2 (pri T = 25 °C)
pKw = pH + pOH = 14
pH = -log[H3O+]
pOH = -log[OH-]
nevtralno: [H3O+] = [OH-]
NI NUJNO pH = 7 (npr. povišamo T, s tem spremenimo Kw)
S čim opišemo jakost kislin?
Ka … konstanta disociacije kisline (Ka = [H3O+][A- ]/[HA])
pKa … negativni dekadični log konstante disociacije kisline
močnejše kisline → manjša vrednost (analogno s pH)
močnejše kisline: slaba afiniteta do protonov, dobra disociacija (α = 1)
šibke kisline: dobra afiniteta do protonov, slaba disociacija (α < < 1)
Kako dobro mora kislina disociirati, da je ‘‘močna’’?
dogovor: pri c = 1M naj kislina vsaj 10% disociira (α = 0,1)!
močne: Ka > 10-2; pKa < 2
šibke: 10-7 < Ka < 10-2; 2 < pKa < 7
zelo šibke: Ka < 10-7; pKa > 7
Kako izračunamo pH raztopin močnih kislin? Zakaj? Kaj moramo še upoštevati pri računanju?
pH = - log [H3O+] = - log [ca ]
ker kislina popolno disociira, je [H3O+] enaka začetni koncentraciji močne kisline
upoštevati moramo protičnost kislin (koliko H+ odda močna kislina → monoprotična, diprotična, triprotična …)
S čim opišemo jakost baz?
Kb … konstanta disociacije baze (Kb =[BH+][OH- ]/[B])
pKb … negativni dekadični log konstante disociacije baze
močnejše baze → manjša vrednost pKb (analogno pOH)
Kdaj sta Ka in Kb povezani?
pri konjugiranih parih (šibka kis. - konjugirana baza; šibka baza - konjugirana kis.)
Ka · Kb = [H3O+]·[OH- ] = K
pKa + pKb = pKw
Kateri so elektronski in strukturni vplivi na kislinsko-bazne lastnosti spojin?
konjugacija in delokalizacija (energijsko ugodno, da se naboj razmaže po večji površini, če je to le mogoče)
induktivni efekt (več in bolj elekrtonegativni elementi v strukturi povečajo kislost)
vodikove vezi
Kako izračunamo pH šibkih kislin (in šibkih baz)?
HF + H2O →← H3O+ + F-
pH = 1/2 pKa – 1/2 log ca
šibke kisline ne disociirajo popolnoma → ca ni enaka [H3O+]
Ka = [H3O+][A- ]/[HA]
zanemarimo avtoprotolizo vode → protone lahko odda le kislina → [H3O+] = [A- ]
šibka kis. slabo disociira → α zelo nizka
[HA] = c
zgornja enačba preide v Ka = [H3O+]2/c
[H3O+] = √ Kac enačbo logaritmiramo in pomnožimo z -1
-log[H3O+] = -1/2 logKa – 1/2 log ca
pH = 1/2 pKa – 1/2 log ca
za šibke baze enaka izpeljava
pOH = 1/2 pKb – 1/2 log cb