Organismes modèles, chromosomes et chromatine
1/18
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No study sessions yet.
19 Terms
% de gènes codant consrvés par rapport à l’humain chez levure
20-30%
% de gènes codant consrvés par rapport à l’humain chez nématode
30-40%
% de gènes codant consrvés par rapport à l’humain chez drosophile
50-60%
% de gènes codant consrvés par rapport à l’humain chez zebrafish
60-70%
% de gènes codant consrvés par rapport à l’humain chez souris
80-90%
levure en tant qu’organisme modèle
étudier le fonctionnement de la cellule sans la complexité de la multicellularité
Peut croître de façon végétative ou sexuée
Peut subir une mitose ou méiose
aspects principaux du cycle cellulaire ont été conservés lors de l’évolution eucaryote
bcp de ses composants peuvent fonctionner de façon interchangeable dans cellules humaines
Peut subir une différenciation
nématode en tant qu’organisme modèle
modèle d’étude important du vieillissement
modèle de choix pour étudier les maladies neurodégénératives
drosophile en tant qu’organisme modèle
Organisme expérimental approprié pr la génétique, la
cytologie et la biochimie
Offre des caractères spécifiques (ex. les chromosomes polytènes)
Mécanismes de dvlp conservés entre la mouche et les vertébrés
zebrafish en tant qu’organisme modèle
embryons transparents, dvlp rapide, observation en direct
Criblage pharmacologique : larves adaptées aux tests à haut
débit, évaluation toxicité/efficacité
génome proche de l’humain, facile à
manipuler (CRISPR), modèles de maladies
régénère cœur, nageoires, rétine → étude mécanismes de réparation
Comportement et neurosciences, fonction musculaire analyse
mémoire, stress, troubles psy, réponses mesurables
Fonction musculaire : étude du dvlpt musculaire, myopathies, régénération et tests fonctionnels
souris en tant qu’organisme modèle
offre un sys génétique puissant, permettant l’inactivation ou surexpression ciblée de gènes
modèle de choix pour l’étude des maladies humaines, qu’il s’agisse de pathologies rares, métaboliques, neurodégénératives ou encore du cancer
caryotype
image des chromosomes d’une cellule au cours de la prométaphase ou métaphase de la mitose
3 séquences d’ADN principales pr le fonctionnement d’un chromosome eucaryote
télomère, origine de réplication et centromère
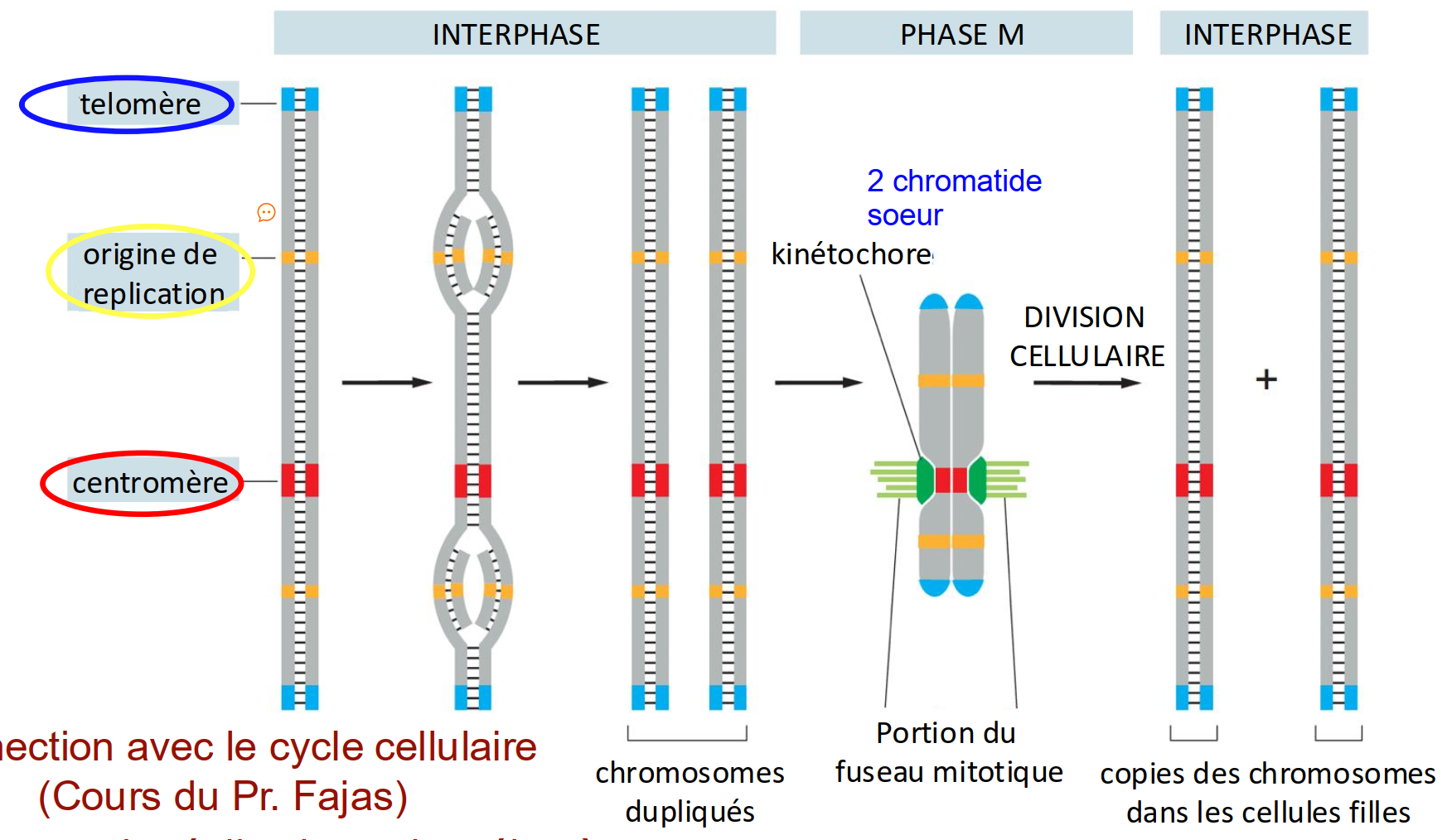
chromatine
composé d’ADN lié à des protéines histones et des protéines “non-histones"
extrémité N-terminale des histones est « libre » de la structure nucléosomale et se projettte vers l’extérieur
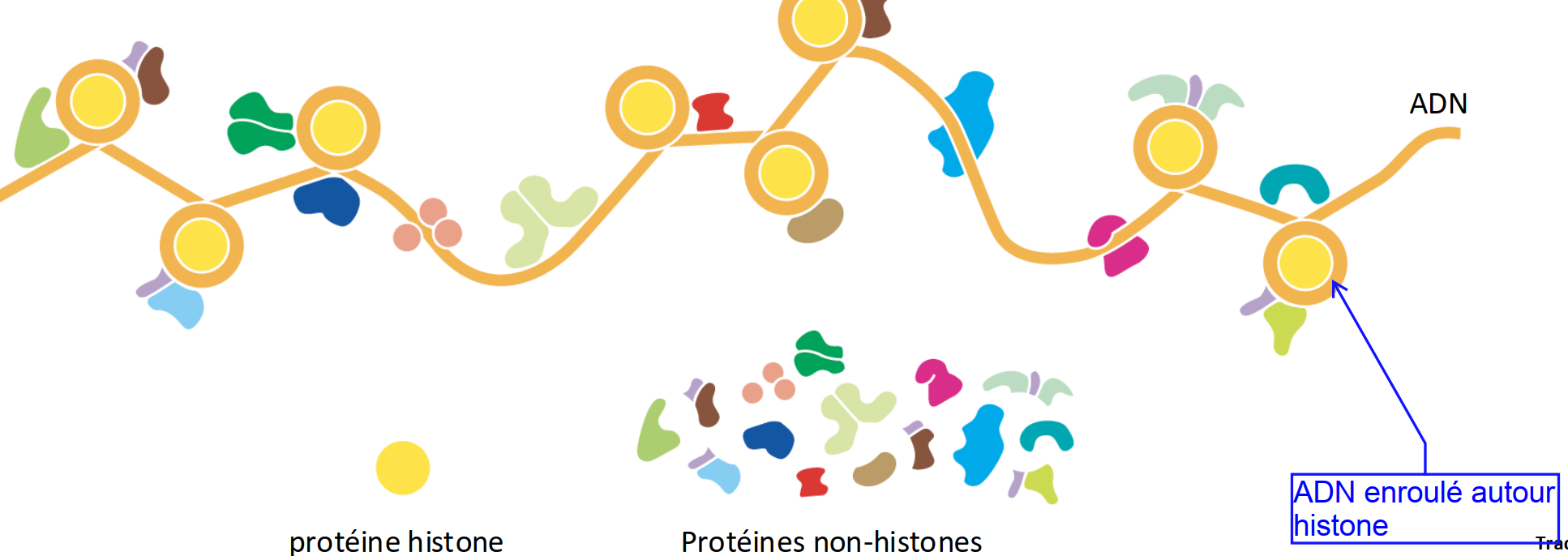
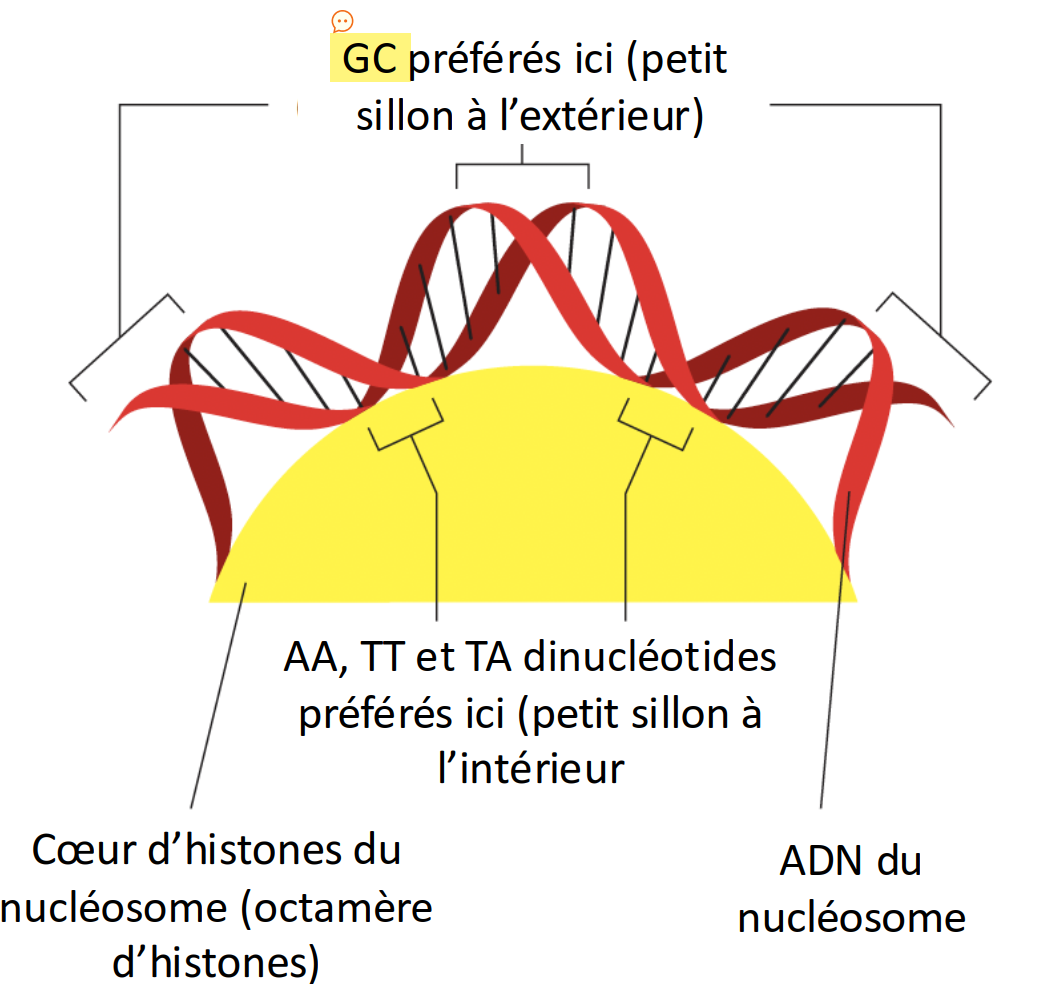
nucléosomes
unités de structure de base des chromosomes eucaryotes
repliement de l’ADN autour de l’octamère
d’histones est faiblement séquence-dépendant
dinucléotides AA, TT et TA, peuvent
diriger le positionnement d’un nucléosome,
car ils sont plus faciles à replier
repli d’histone pour
structurer la chromatine
« queue » N-terminale non-structurée pour
régulation de la chromatine
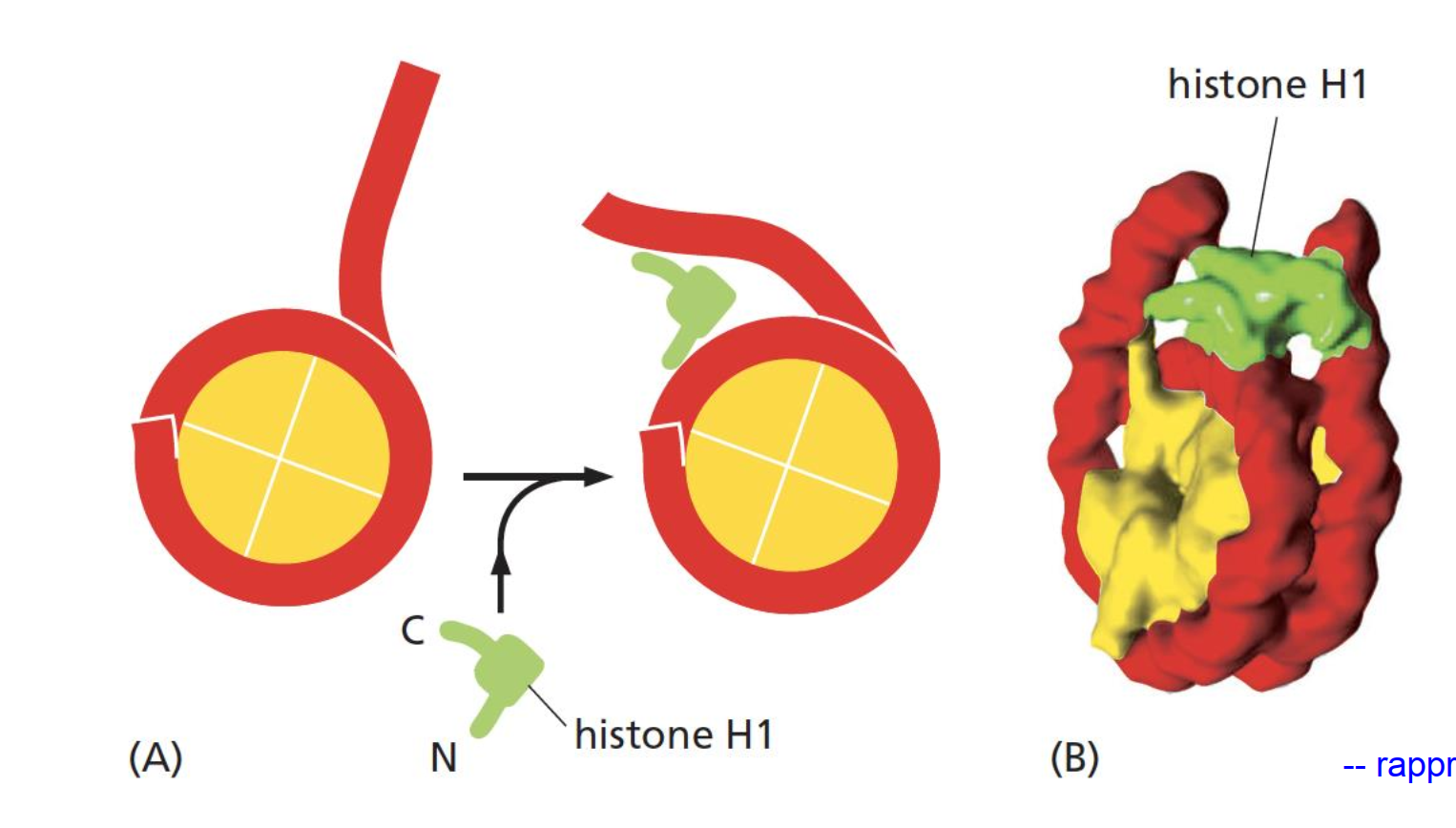
5ème histone H1
participe à la compaction des nucléosomes
rassemble nucléosomes en fibres de 30nm, joue un role de histone de « liaison »
rapproche 2 bras d’ADN
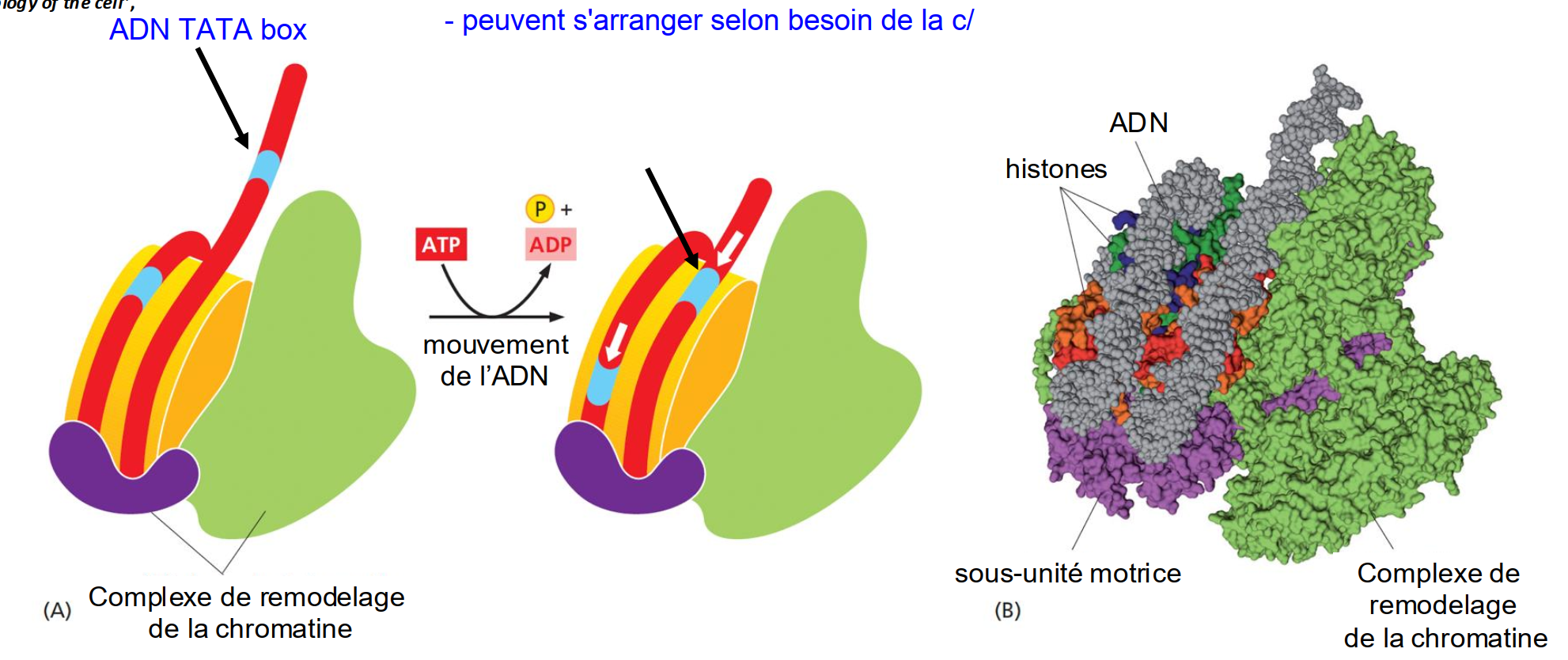
nucléosomes sont dynamiques
leur glissement est catalysé par des cplx de remodelage de la chromatine dépendants de l’ATP
processus rapides permettant d’adapter l’organisation de la chromatine
nucléosomes peuvent être
enlevés ou échangés, des
variants de histones peuvent
être introduits