Aldeídos e cetonas I e II
1/5
Earn XP
Description and Tags
Estrutura e nomenclatura. Propriedades físicas. Espetroscopia. Síntese de aldeídos e cetonas. Oxidação de álcoois. Ozonólise: clivagem oxidativa de alcenos. Hidratação de alcinos. Acilação de Friedel-Crafts. Adição nucleofílica ao grupo carbonilo. Fatores que afetam a reatividade dos aldeídos e cetonas. Reações reversíveis e irreversíveis. Nucleófilos de oxigénio. Formação de hidratos
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
6 Terms
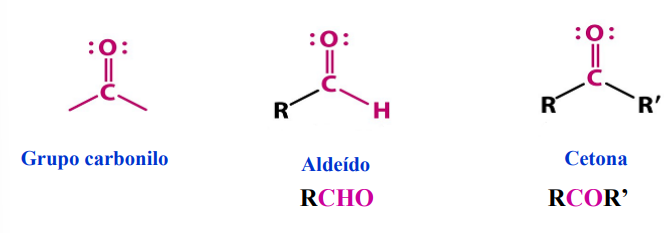
Estrutura de um grupo carbonilo
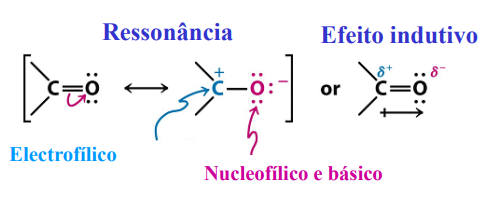
O átomo de oxigénio é mais eletronegativo que o carbono, por isso esta ligação está polarizada. O carbono tem uma carga parcial positiva e o oxigénio uma carga parcial negativa.
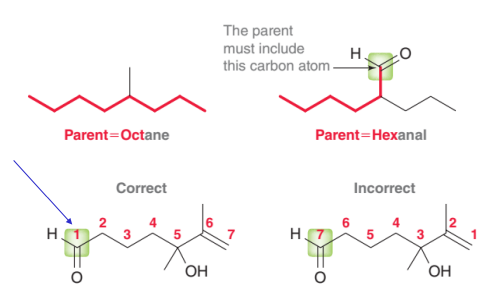
Nomenclatura de aldeídos
Identificar e nomear a cadeia principal.
Identificar e nomear os substituintes.
Atribuir a localização a cada substituinte.
Colocar os substituintes por ordem alfabética.
O grupo carbonilo está sempre no carbono 1
O pent”ano” substitui-se por pentan”al”
Quando o aldeído está ligado a um anel cíclico: é um carbaldeído (ex. ciclopentanocarbaldeído
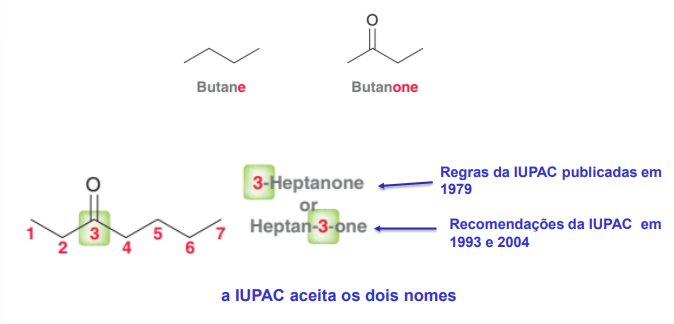
Nomenclatura de cetonas
Substituição da terminação o dos alcanos correspondentes por ona
As cetonas aromáticas são nomeadas alcanonas. O anel aromático considera-se como substituinte.
As cetonas cíclicas são nomeadas ciclo-alcanonas. O carbono carbonílico é o C1.
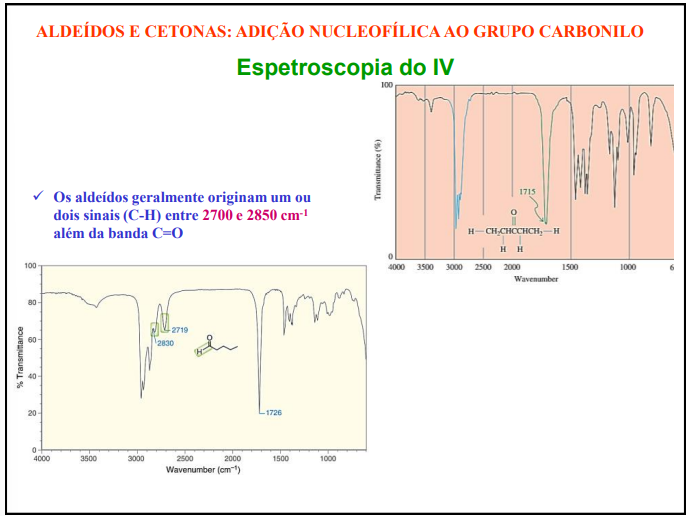
Espetroscopia IV
O grupo C=O origina um sinal intenso no espectro IV, geralmente a 1715-1720cm1
O grupo C=O conjugado origina um sinal com número de onda mais baixo devido ao efeito de ressonância
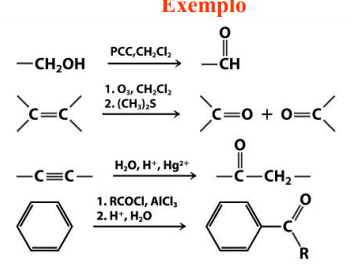
Técnicas de síntese de aldeídos e cetonas:
Oxidação de alcoois
Ozonólise de alcenos
Hidratação de alcinos
Acilação de Friedel-Crafts
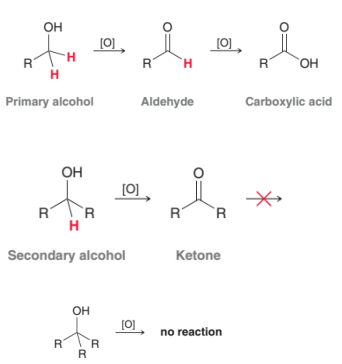
Oxidação de alcoois
Alcoois primários dão origem a aldeídos pelo oxidante fraco PCC
Alcóis secundários dão origem a cetona pelo oxidante forte Na2Cr2O7 ou pelo PCC (fraco).