AP. BLOC 7
1/11
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
12 Terms
Define los conceptos de diferenciación, displasia i anaplasia
DIFERENCIACIÓN: Magnitud que es basa en la semblança en funció i forma que tenen les cèl·lules canceroses amb les cèl·lules normals. De manera que una elevada diferenciació vol dir que les cèl·lules neoplàsiques s’assemblen força a les del teixit sa (benignitat) i poca diferenciació, que les cèl·lules gairebé no s’assemblen (malignitat).
DISPLASIA: Es refereix al creixement desordenat de les cèl·lules depenent de factors externs. Aquest és un procés reversible i pot ser precursor d’una neoplàsia (sovint maligne). Ho serà quan aquest creixement desordenat deixi de dependre de factors externs i esdevingui autònom.
ANAPLASIA: Se refiere a la falta de diferenciació. Les cèl·lules anaplàsiques no s’assemblen en forma ni en funció a la original, i això indicarà sempre malignitat.
Identifica los factores que determinan el ritmo de crecimiento de un tumor
Hi ha quatre factors principals que determinen la velocitat de creixement d’un tumor:
Temps de duplicació de les cèl·lules tumoral.
Alteració dels checkpoints del cicle cel·lular
S’accelera el pas d’una fase a una altra del CC
Velocitat de duplicació cel·lular = velocitat de creixement
Fracció de cèl·lules tumorals al fons comú replicatiu: la fracció del creixement és la proporció de cèl·lules tumorals que estan en el fons comú proliferatiu. Com més diferenciades siguin les cèl·lules, més quantitat de cèl·lules estaran en repòs. En canvi, quantes més estiguin en diferenciació seran perquè encara estan indiferenciades, aleshores això fa que augmenti la velocitat de creixement.
Velocitat d’eliminació o mort de cèl·lules: creixement i velocitat venen determinats per la relació entre la producció cel·lular i la pèrdua. Velocitat de progressió cel·lular > velocitat d’eliminació cel·lular à augmenta la velocitat.
Factores externos, com l’estimulació hormonal, irrigació sanguinea i altres influencias.
Descriure les principals característiques macroscòpiques, microscòpiques i evolutives dels tumors benignes i dels malignes, fent un èmfasi especial en les característiques diferencials generals.
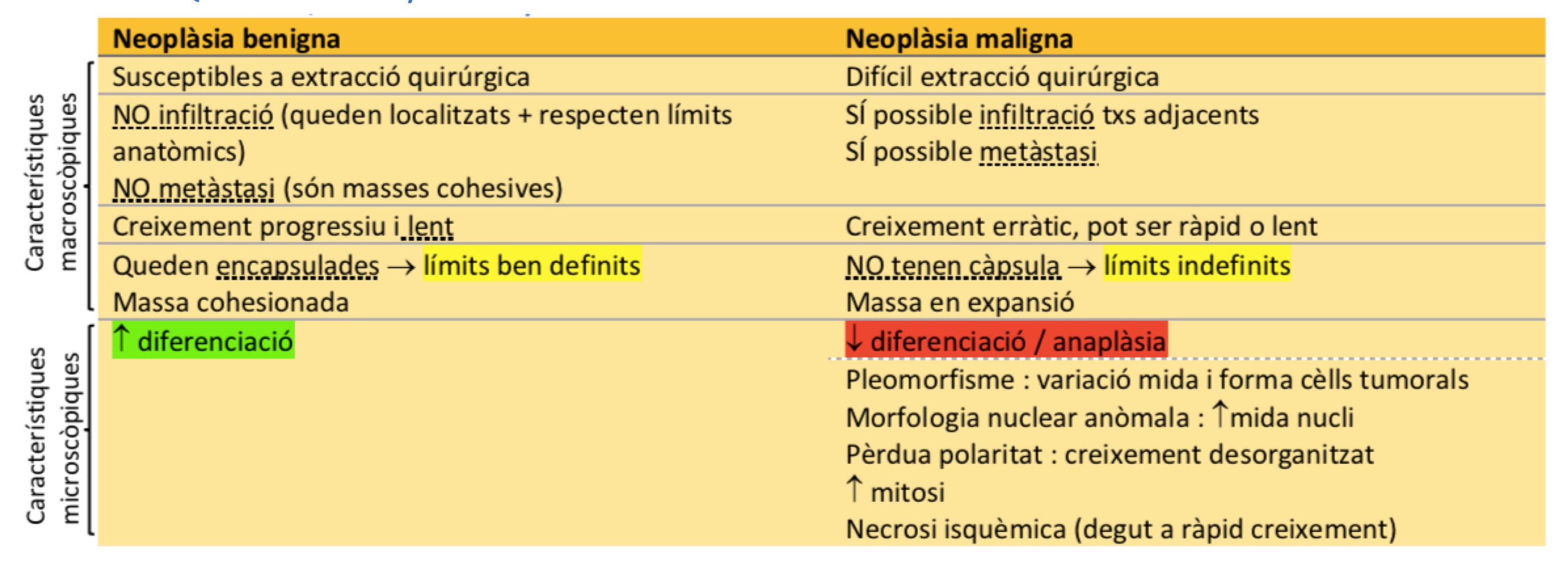
Definir els conceptes de carcinoma in situ i de carcinoma microinvasor.
Carcinoma in situ: alteració displàsica intensa que afecta a tot l’espessor de l’epiteli, però no penetra la membrana basal (benigne)
Carcinoma microinvasor: envaeix estroma no més de 5 mm (bon pronòstic)
Explicar el mecanismes biològics de la invasió tumoral i de la metàstasi.
imagen

Distingir i descriure les diferents vies de disseminació metastàtica dels tumors malignes.
Descriure les característiques generals de les metàstasis per via hematògena. Descriure les característiques generals de les metàstasis per via limfàtica, el significat biològic i les característiques anatomopatològiques.
imagen

Diferenciar entre factors pronòstics i factors predictius.
FACTORS PRONOSTICS: Es tracta de qualsevol característica que proporcioni informació sobre la possible evolució del pacient i que ens permeti guiar les decisions terapèutiques i determinar la probabilitat de sobreviure o recidiva.
Caracteristicas demograficas (edad, etnia, edad menopausica)
Caracteristicas tumorals histologicas (mida i estadi tumor)
Marcadors tumorals (oncogens alerats, factors creixement o gens tumoral supressors)
FACTORS PREDICTIUS: Ens volen indicar la probabilitat de resposta del tumor a un determinat agent terapèutic o una combinació.
Explicar en que es basa l’estadiatge d’un tumor i descriure els diferents mètodes de classificació de l’extensió dels tumors: sistema TNM i estadis d’extensió tumoral.
L’estadiatge estableix agressivitat segons la mida de la lesió primària, grau de disseminació a ganglis limfàtics regionals i presència o absència de metàstasi. Basat en exploració clínica, radiològica i a vegades quirúrgica.
El mètode d’estadiatge emparat actualment és el TNM on les sigles signifiquen:
T: TUMOR. El significat concret variarà segons el tipus de tumor que vulguem estadificar, en alguns serà la mida, en altres la profunditat...
T0: no es localitza el tumor primari
T1: tumor in situ
T1, T2, T3, T4
Tx: no podem medir el tumor
N: NODULE (gangli). Indica si els ganglis limfàtics regionals estan afectats
N0: ganglis no infectats
N1, N2...
M: METASTASI. Descriu metàstasi
M0: no hi ha metàstasi
M1, M2
Segons la TNM classificarem el tumor en els estadis I, II, III, IV i segons el valor obtingut de l’estadiatge recorrerem a una opció terapèutica o a una altra.
Definir els termes d’adenoma, papil·loma, cistadenoma, pòlip, tumor mixt, teratoma i hamartoma.
ADENOMA: Se emplea para la mayor parte de neoplasias epiteliales benignas, incluidas las que producen estructuras de tipo glandular y las que no.
PAPILOMA: Alude a una neoplasia epitelial benigna que forma frondas digitiformes macro o microscopica
CISTADENOMA: Masa quistica hueca, que se encuentra sobre todo en el ovario.
POLIPO: Masa que se proyecta por encima de una superficie mucosa y genera una estructura visible macroscopica. Se suele emplear para los tumores benignos, algunos malignos tienen un crecimiento polipoideoy existen polipos de origen inflamatorios.
TUMOR MIXTO: S’origina per diferenciació divergent d’un sol clon neoplàsic. Solen estar formats per components epitelials dispersos al si d’un estroma mucoide el qual pot contenir illots de cartílag o os. Ejemplo: tumor mixto de la glandula salival, que se suele llamar adenoma pleomorfo
TERATOMA: Tipo especial de tumor mixto que contiene celulas o tejidos maduros o inmaduros que pertenencen a mas de una capa de cel germinales y a veces las tres.
HAMARTOMA: Masa de tejido desorganizado que recuerda al tejido afectado. La mayoria tienen alteraciones cromosomicas clonales, y se interpreta como neoplasias benignas infecuentes
Definir els termes de carcinoma, carcinoma escamós, adenocarcinoma, sarcoma, limfoma i melanoma.
CARCINOMA: Las neoplasias malignas de origen epitelial se denominan carcinoma sea cual sea el tejido en el que se originan.
CARCINOMA ESCAMOSO: Carcinomas que estan conformados por celulas escamosas
ADENOCARCINOMA: Carcinomas que adoptan un patrón de crecimiento glandular
SARCOMA: Neoplasias malignas derivadas de los tejidos mesenquimatosos o sus derivados
LIMFOMA: Neoplasias malignas derivadas de las celulas sanguineas
MELANOMA: Neoplasia maligna y agresiva, que se origina de los melanocitos.
Definir el terme marcador tumoral i les seves aplicacions i limitacions y enumerar els marcadors tumorals més utilitzats a la pràctica clínica.
Els marcadors tumorals són substàncies biològiques associades a l’activitat tumoral que és usada en detecció, pronòstic, seguimiento, prevenció i recerca del càncer. No serveix pel diagnòstic definitiu però ajuda en la detecció.
Són marcadors sensibles i poc específics ja que es poden elevar també amb malalties que no siguin neoplàsiques. Són especialment útils per detectar recidives després d’excitació. Els troben en sang en concentracions més elevades que els valors de referència. Els més importants són: (tabla)

Descriure els diferents mètodes anatomopatològics en l’estudi de les neoplàsies (diagnòstic citològic, biòpsia diagnòstica i estudi de peces quirúrgiques, microscopia electrònica, immunohistoquímica i biologia molecular) i avaluar-ne la importància i utilitat en el diagnòstic i en la valoració de l’agressivitat.
DIAGNOSTIC CITOLOGIC: Consisteix en l’estudi de cèl·lules aïllades obtingudes per exfoliació (p. ex. citologia cervical), aspiració amb agulla fina (PAAF) o líquids corporals.
Utilitat en agressivitat: Limitada; pot suggerir atípia o alt grau, però no permet una valoració completa.
BIOPSIA DIAGNOSTICA: Obtenció d’un fragment de teixit (biòpsia incisional, excisional o amb agulla gruixuda). Utilitat en agressivitat:
• Permet valorar: Grau histològic, Índex mitòtic, Necrosi
• Important per orientar el pronòstic inicial.
ESTUDIO DE PIEZAS QUIRURGICAS: Anàlisi completa del tumor extirpat.
Utilitat en agressivitat:
• Fonamental per a l’estadiatge (TNM)
• Determina el pronòstic i la necessitat de tractaments addicionals
MICROSCOPIA ELECTRONICA: Estudi ultraestructural de les cèl·lules.
Valor global
• Baix en la pràctica actual
• Útil només en casos seleccionats de diagnòstic difícil
INMUNOHISTOQUIMICA: Tècnica basada en l’ús d’anticossos per detectar proteïnes específiques en el teixit tumoral.
Valor
• Molt alt. Permet valorar: Índex proliferatiu (Ki-67) y Alteracions associades a mal pronòstic
• Fonamental en diagnòstic i classificació tumoral
BIOLOGIA MOLECULAR: Estudi de les alteracions genètiques i moleculars del tumor.
Valor
• Molt alt. Permet: Predir evolució del tumor, Identificar tumors més agressius y Seleccionar tractament específic
• Essencial en oncologia moderna