elementet e bllokut d
1/79
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
80 Terms
elementet e bllokut d
elementet kimike të cilat elektronet e fundit i kanë të vendosura në orbitalin d quhen elemente kalimtare (transite)
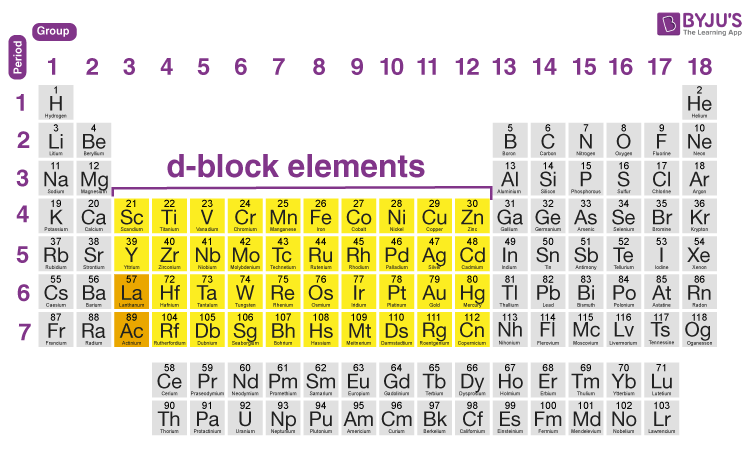
çka janë elementet e bllokut d?
çka i dallon elementet e bllokut d nga elementet e bllokut s dhe p?
elementet e bllokut d, përveç në kuadër të grupit, mund të kenë veçori të ngjajshme edhe në kuadër të periodës (siç kemi grupet 8,9 dhe 10 ku renditen Fe, Co dhe Ni të cilat kanë veti të ngjajshme)
prej cilës periodë fillon renditja e elementeve të bllokut d?
konfiguracioni elektronik i elementeve të bllokut d
ns2 (n-1)dx
ku n mund të jetë nga 4 - 7
ku x mund të jetë nga 1 - 10 (sepse orbitali d zë 10 elektrone maksimalisht)
anomalitë e konfiguracionit
ns2(n-1)d4 X
ns1(n-1)d5 e saktë
ns2(n-1)d9 X
ns1(n-1)d10 e saktë
elementet me numër të lartë oksidues
V, Cr dhe Mn mund të paraqiten me numra të lartë oksidues (+5, +6, +7), janë mjete të forta oksiduese, pra i oksidojnë metalet kurse vetë reduktohen
përdorimi i metaleve kalimtare
përdoren si katalizatorë (Fe, Ni, Pt) dhe formojnë jone komplekse
vetitë e metaleve kalimtare
kanë dendësi të madhe, janë të fortë, janë të ngurta dhe kanë ngjyrë argjend në blu përveç arit dhe bakrit. Janë përcjellës të mirë të elektricitetit dhe nxehtësisë, posaçërisht grupi IB dhe kanë pika të larta të shkrirjes dhe vlimit
cilat elektrone marrin pjesë në formimin e lidhjeve kimike të elementeve kalimtare?
elektronet s dhe elektronet d të shtresës së fundit
lidhja metalike
forcat tërheqëse që krijohen mes elektroneve të delokalizuara të shtresës së fundit
si rritet fortësia e lidhjes metalike?
rritja e ngarkesës pozitivet ë joneve në rrjetën metalike
zvogëlimi i përmasave të joneve të metalit në rrjetë
rritja e numrit të elektroneve lëvizëse për atom
aliazhet
përzierje e dy apo më shumë metaleve ose një metali me jo metal.
Atomet e metalit të pastër janë të vendosura në radhë të rregullta dhe kur përplasen me një metal tjetër të pastër do të kemi rrëshkitje të radhëve me njëra-tjetrën. Kur metali formon aliazh me një metal tjetër, prishet rrjeta kristalore dhe kemi përzierje të atomeve me madhësi të ndryshme gjë që e bën të pamundur rrëshkitjen e radhëve me njëra-tjetrën.
Prandaj, alizathet janë me të forta se metalet.
tunxhi
përbëhet nga bakri dhe zinku (Cu + Zn). Është më i fortë se bakri, por akoma i farkueshëm. Përdoret për instrumentet muzikore
bronzi
aliazh i bakrit dhe kallajit (Cu + Sn). Është shumë i fortë dhe përdoret për pjesë të automjeteve, këmbana dhe statuja
çeliku
aliazh i hekurit, kromit dhe nikelit (Fe+Cr+Ni). Nuk ndryshket si hekuri dhe përdoret për pjesë makinash, mjete prerëse, intrumente kirurgjikale
aliazhet me veti memorizuese
nitinoli (nikel + titan)
Nëse një copë teli nitinol derdhet në formën S ai e mban atë formë. Nëse forma drejtohet, teli do të bëhet i drejtë. Por nëse teli vendoset në ujë të nxehtë, ai do të rikthehet në formën e parë S, dhe kjo quhet kujtesë e formës së aliazhit.
amalgamet
aliazhe të merkurit (Hg) me elemente të tjera
ndarja e metalurgjisë
metalurgjia e zezë që është metalurgjia e hekurit dhe aliazheve të tij (gizë, çelik, ferrokrom)
metalurgjia e metaleve me ngjyrë (Cu, Ni, Al, Pb, Sn, Cr, Co) dhe e metaleve të rralla
grupi 8 - familja e hekurit
Fe, Co, Ni
konfiguracioni i hekurit
hekuri (Fe) me 26 elektrone, përfundon me konfiguracion 4s23d6 por jonet e hekurit do të krijojnë një anomali ku do të marrin të gjitha elektronet e orbitalit s dhe do të vendosen në orbitalin d, duke rezultuar në ns0
numrat oksidues të hekurit
+2 dhe +3
xehet e hekurit
magnetiti
hematiti
piriti
sideriti
limoniti
përfitimi i hekurit
në furrnaltë, qzmzri koks reagon me oksigjen dhe përfitojmë monoskidin e karbonit. Ky i fundit reagon me një mineral të hekurit dhe përfitohet hekuri elementar. Në furrnaltë shtohet edhe guri gëlqror, i cili vepron me papastërtitë që ndodhen në mineralin e hekurit duke krijuar skorjet, të cilat notojnë mbi sipërfaqen e hekurit të shkrirë dhe largohet nga furrnalta. Hekuri i shkrirë (giza) që prodhohet përmban deri në 4% karbon dhe sasi të vogla elementesh të tjera.
veprimi i hekurit me oksigjen
oksidi magnetik
veprimi i hekurit me ujin
oksidi magnetikk
veprimi i hekurit me acidet
zhvendos hidrogjenin duke krijuar kripëra dhe liron hidrogjen
çfarë karakteri kanë oksidet dhe hidroksidet e hekurit (ll)
karakter bazik
oksidimi i komponimeve të hekurit
oksidi ferror oksidohet dhe përfitojmë oksidin ferrik
hidroksidi ferror oksidohet dhe përfitojm hidroksidin ferrik
karakteri i oksidit ferrik (lll)
karakter amfotern, është pluhur i kuq dhe përdoret si pigment
kripërat e hekurit
sulfati i hekurit (ll)
kloruri ihekurit (ll)
kloruri i hekurit (lll)
përdorimi i klorurit të hekurit të hidratuar FeCl3 x H2O
ka medikamente që përdoren për koagulimin e gjakut si dhe në trajtimin e anemisë
aliazhet e hekurit
çeliku - përmban karbon, mangan dhe kallaj. Sasia e karbonit në çelik kontrollohet përmes sasisë së oksigjenit që futet në konvertitor. Sa më e madhe të jetë sasia e oksigjenit, aq më e madhe është sasia e karbonit të larguar. Shtimi i kromit dhe nikelit e bën çelikun të fortë dhe rezistent ndaj korrozionit e nehtësisë, kurse mangani i jep fortësi dhe qëndrueshmëri të lartë.
giza - përmban karbon, silic, mangan ose papastërti si fosfori dhe sulfuri
korrozioni i metaleve
ndryshku është oksid i hidratuar i hekurit (lll) me formulë Fe2O3 x H2O (kur mbi hekur bie një pikë ujë, ai priret të oksidohet):
Fe = Fe2+ + 2e-
grupi i 11-të
bakri
xehet e bakrit
kalkozina
kalkopiriti
kupriti
numrat oksidues të bakrit
+1 (kupror) dhe +2 (kuprik)
karbonati bazik i bakrit
bakri është më i qendrueshëm se hekuri ndaj brejtjes atmosferike, në ajër të thatë nuk oksidohet, kurse në prani të lagështisë e të gazit karbonik në ajër formon karbonatin bazik të bakrit me ngjyrë të gjelbër.
Ky formohet në materialet e ndërtuara nga bakri me qëndrim të gjatë në atmosferë dhe i mbron ato nga oksidimi i mëtejmë. Statuja e lirisë në New Zork është ndërtuar nga bakri, me oksidimin e Cu është fituar karbonati bazik i tij dhe statuja ka marrë ngjyrë të gjelbër

përdorimi i gurkalit CuSO4 x H2O
fungicid / insekticid
xehet e plumbit
galena
ceruziti
angleziti
karbonati bazik i plumbit
në atmosferë me lagështi dhe në prani të dioksidit të karbonit, plumbi mbulohet shpejt me një shtresë të hollë të oksidimit të plumbit e cila gradualisht shndërrohet në karbonat bazik të plumbit, që e mbron plumbin nga oksidimi i mëtejshëm
përfitimi i plumbit
me fërgimin e xeheve sulfure (galenës) formohet PbO e cila reduktohet në CO dhe formohet plumbi Pb
numrat oksidues të plumbit
+2 dhe +4
monoksidi i plumbit PbO
ka ngjyrë të verdhë dhe përdoret për pikturim me emrin masikot
përdorimi i karbonatit bazik të plumbit (ll)
njihet me emrin bardha e plumbit dhe përdoret si ngjyrë e bardhë për pikturim
dioksidi i plumbit PbO2
përdoret për përfitimin e akumulatorëve
miniumi Pb3O4
është oksid i përzier; pluhur me ngjyrë të kuqe, i tretur në tretës organik, përdoret për lyerje të sipërfaqeve të hekurit dhe çelikut si mjet antikorrodiv
mineralet e zinkut
sfaleriti
zinkiti
smitsoniti
silikati i zinkut
frankliniti
grupi i 12-të
zinku
numri oksidues i zinkut
+2
përfitimi i zinkut
metoda pirometalurgjike - me fërkimin e ZnS formohet ZnO, i cili reagon me karbon elementar ose monoksid karboni dhe lirohet zinku + dioksidi i karbonit
metoda elektrolitike
çfarë karakteri kanë oksidi dhe hidroksidi i zinkut?
karakter amfotern
grupi i 10-të
Nikeli
mineralet e nikelit
limoniti
nikel-hekur
garnieriti
silikati nikel-magnez
pentlanditi
lateritet
me këtë emërtim njihen dy nga mineralet e nikelit, limoniti dhe pentlanditi
përdorimi i nikelit
bën hidrogjenizimin e yndyrnave në procesin e prodhimit të yndyrnave të ngurta (gjalpi, margarina)
aliazhet “argjendi i ri” dhe alpaka
aliazhe të bakrit, nikelit dhe zinkut, të cilat përdoren për prodhimin e monedhave
nitinoli
aliazh nikel-titan; nëse një tel të këtij aliazhi e ngrohim në 500oC mund t’i japim çdo formë që e dëshirojmë, por kur ftohet ai rikthehet në formën fillestare, ashtu siç ka qenë para ngrohjes . Ky njihet si aliazh intelegjent
grupi i 6-të
kromi
mineralet e kromit
kromiti
krokoiti
përfitimet e kromit
përfitohet përmes oksdit të kromit me metodën e aluminotermisë (metodë ku alumini përdoret si mjet reduktues për përfitimin e metaleve)
kromimi
proces elektrolitik i veshjes së hekurit për mbrojtje ndaj korrozionit
ferrokromet
aliazhe të hekurit dhe kromit
me cilin acid nuk vepron kromi?
me acid nitrik
numrat oksidues të kromit
paraqitet me numra oksidues të ndryshëm, por më të zakonshëm janë +2, +3 dhe +6. Oksideve të kromit, me rritjen e numrit oksdues, iu rritet karakteri acidik
acidet e kromit
oksidi i kromit CrO3 formon acidet kromike dhe acidet dikromike
kripërat e kromit
kripërat e acidit kromik - kromate ( oksidues të fortë dhe në tretësirë ujore kanë ngjyrë të verdhë)
kripërat e acidit dikromik - dikromate (në tretësirë ujore kanë ngjyrë portokalli)
grupi i 7-të
mangani
mineralet e manganit
piroluziti
brauniti
hauzmaniti
manganiti
përfitimi i manganit
përfitohet me metodën e aluminotermisë
numrat oksidues të manganit
+2, +3, +4, +6 dhe +7
me cilin numër oksidues formon përbërës të tretshëm?
në gjendje +2
karakteri i oksideve të manganit
me rritjene numrit oksidues, rritet karakteri acidik
acidi permanganik HMnO4
përbëhet nga tretja në ujë e oksidit Mn2O7
permanganati i kaliumit
kripë e cila shërben si mjet i fortë oksidues dhe tretësira ujore e saj ka ngjyrë të vjollcë
metalet e rënda të domosdoshme
Co
Cr
Cu
Fe
Mn
Zn
metalet e rënda jo- të domosdoshme
Ba
Zr
metalet e rënda pak toksike
Sn
Al
metalet e rënda me toksicitet të lartë
Pb
Hg
Cd
metalet fisnike
janë argjendi (Ag), ari (Au) dhe platina (Pt). Janë shumë pak reaktive