CM6: DECARBOXYLATION OXYDATIVE / RESPIRATION
1/10
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
11 Terms
🔹 Cycle de Krebs et chaîne respiratoire 1. Caractéristiques générales
Q1. Quelles sont les caractéristiques essentielles du cycle de Krebs et de la chaîne respiratoire, et quel est leur rôle global ?
2. Substrats d’entrée
Q2. Quels substrats principaux alimentent le cycle de Krebs et par quelles voies métaboliques ?

1. Caractéristiques générales
Q1. Quelles sont les caractéristiques essentielles du cycle de Krebs et de la chaîne respiratoire, et quel est leur rôle global ?
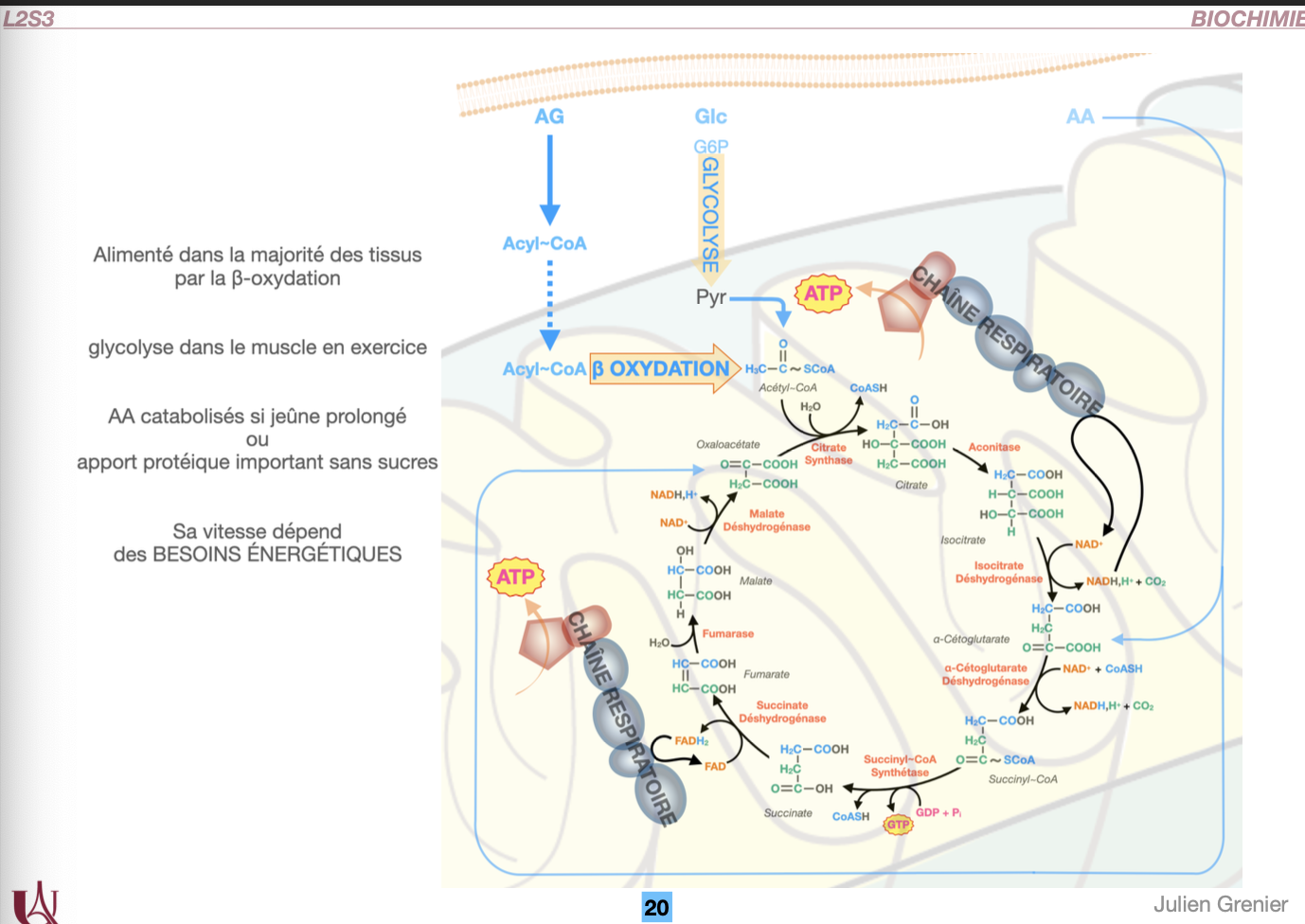
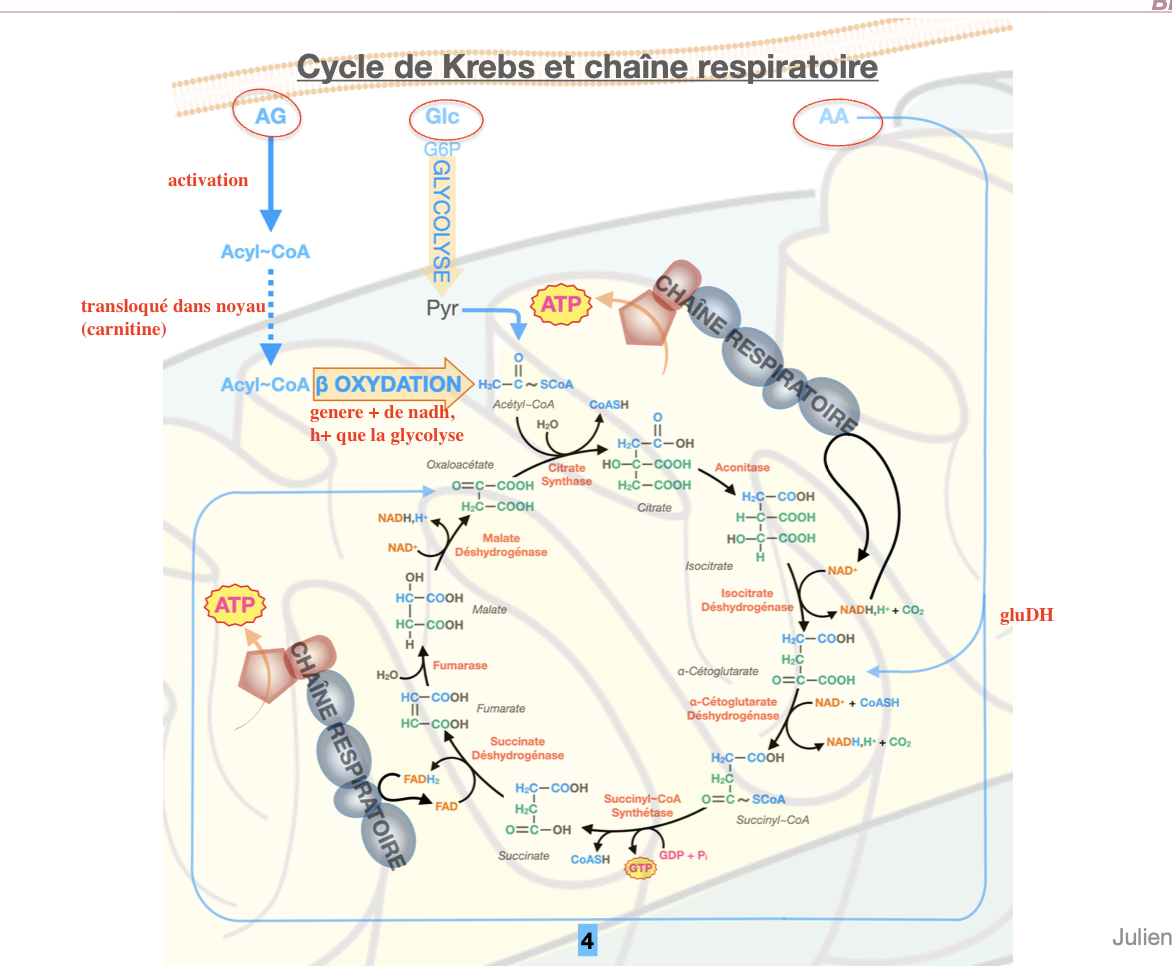
R1. Le cycle de Krebs et la chaîne respiratoire sont des voies ubiquitaires, permanentes et indispensables (sauf dans les hématies qui n’ont pas de mitochondries). Elles se déroulent strictement dans la mitochondrie et nécessitent un environnement aérobie.
Le cycle de Krebs assure l’oxydation complète de l’acétyl-CoA, produisant du CO₂, du NADH, H⁺ et du FADH₂. Ces coenzymes réduits alimentent la chaîne respiratoire, qui consomme de l’O₂ et génère de l’ATP par phosphorylation oxydative.
Les deux voies sont reliées par la succinate déshydrogénase, à la fois enzyme du cycle et Complexe II de la chaîne respiratoire.
2. Substrats d’entrée
Q2. Quels substrats principaux alimentent le cycle de Krebs et par quelles voies métaboliques ?
R2.
Glucose : subit la glycolyse → formation de pyruvate → conversion en acétyl-CoA (substrat direct du cycle) par le complexe pyruvate déshydrogénase (PDH).
Acides gras (AG) : activés en acyl-CoA, transportés par la carnitine dans la mitochondrie → β-oxydation → production d’acétyl-CoA, de NADH et de FADH₂.
Acides aminés (AA) : désaminés → squelettes carbonés transformés en intermédiaires du cycle (α-cétoglutarate, oxaloacétate, succinyl-CoA), participant ainsi à l’alimentation de Krebs.
Le carrefour du pyruvate
1. Génération du pyruvate
Q1. Quels sont les principaux moyens métaboliques permettant de générer du pyruvate ?
2. Issues principales du pyruvate
Q2. Quelles sont les trois grandes voies métaboliques à partir du pyruvate, et dans quelles conditions elles se produisent ?
1. Génération du pyruvate
Q1. Quels sont les principaux moyens métaboliques permettant de générer du pyruvate ?
R1.
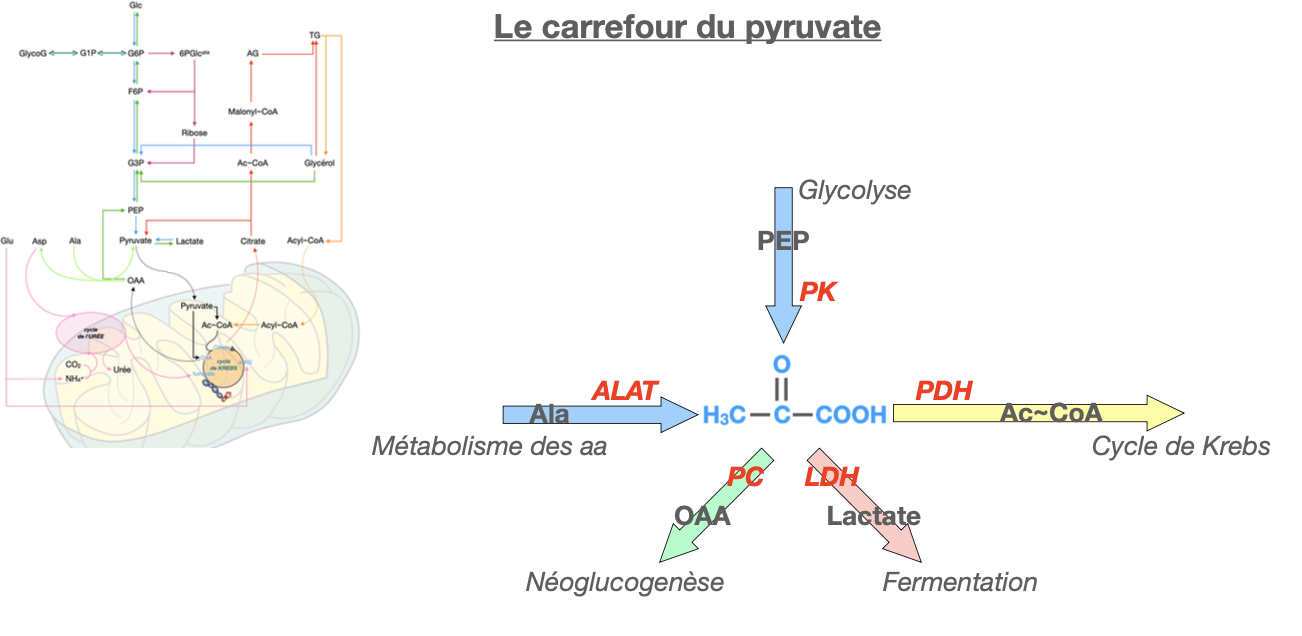
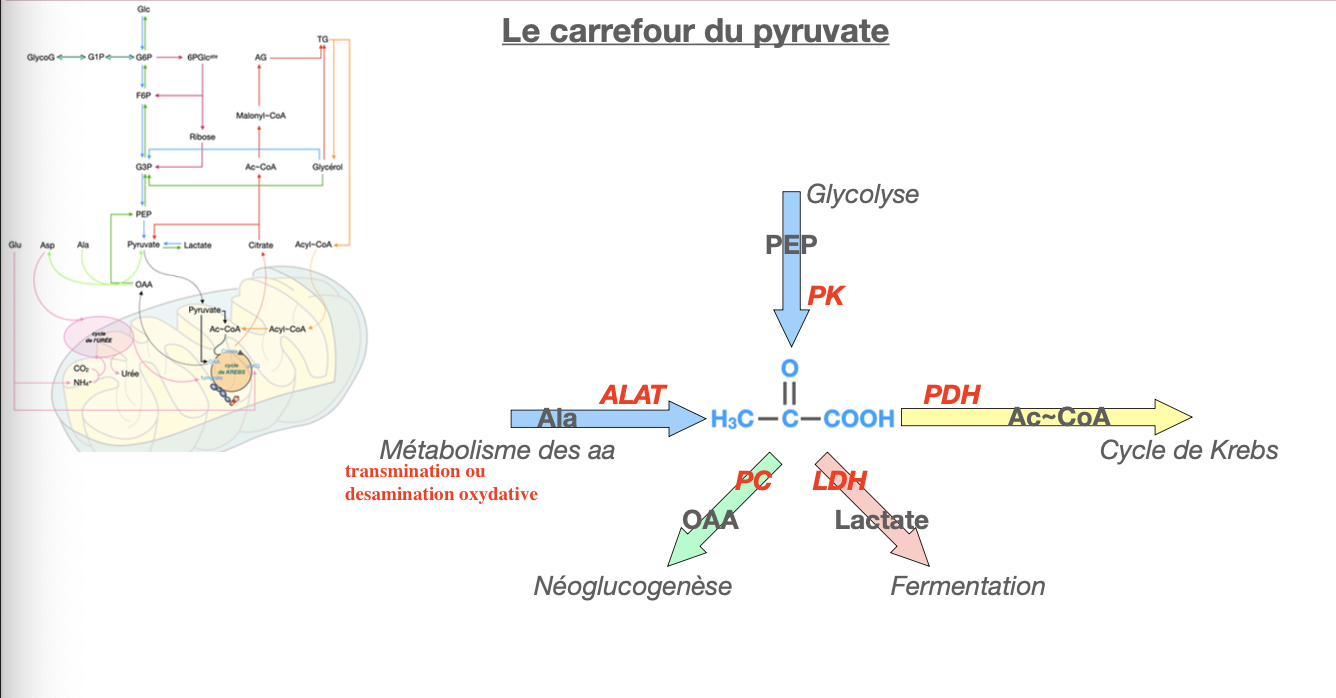
Glycolyse : transformation du phosphoénolpyruvate (PEP) en pyruvate par la pyruvate kinase (PK).
Métabolisme des acides aminés : par transamination (alanine ↔ pyruvate via l’alanine aminotransférase, ALAT) ou par désamination oxydative.
Autres voies : certaines réactions de catabolisme des glucides (ex. galactose, fructose) convergent vers la glycolyse et génèrent du pyruvate indirectement.
2. Issues principales du pyruvate
Q2. Quelles sont les trois grandes voies métaboliques à partir du pyruvate, et dans quelles conditions elles se produisent ?
R2.
Cycle de Krebs (voie oxydative)
Conversion en acétyl-CoA par la pyruvate déshydrogénase (PDH).
Se produit en conditions aérobies.
Permet l’entrée dans le cycle de Krebs, production de NADH/FADH₂ et ATP via la chaîne respiratoire.
Néoglucogenèse (voie anabolique)
Conversion en oxaloacétate (OAA) par la pyruvate carboxylase (PC).
Active lorsque l’organisme est en excès de pyruvate ou en jeûne prolongé.
Sert à reformer du glucose pour maintenir la glycémie.
Fermentation lactique (voie anaérobie)
Conversion en lactate par la lactate déshydrogénase (LDH).
Occurs when O₂ is limiting (ex. effort musculaire intense).
Régénère du NAD⁺ nécessaire à la glycolyse pour produire de l’ATP rapidement.
🔹 Transport du pyruvate dans la mitochondrie 1. Entrée du pyruvate
Q1. Comment le pyruvate traverse-t-il la double membrane mitochondriale ?
2. Destins possibles du pyruvate
Q2. Quels sont les deux grands destins métaboliques du pyruvate une fois dans la mitochondrie ?
1. Entrée du pyruvate
Q1. Comment le pyruvate traverse-t-il la double membrane mitochondriale ?
R1.
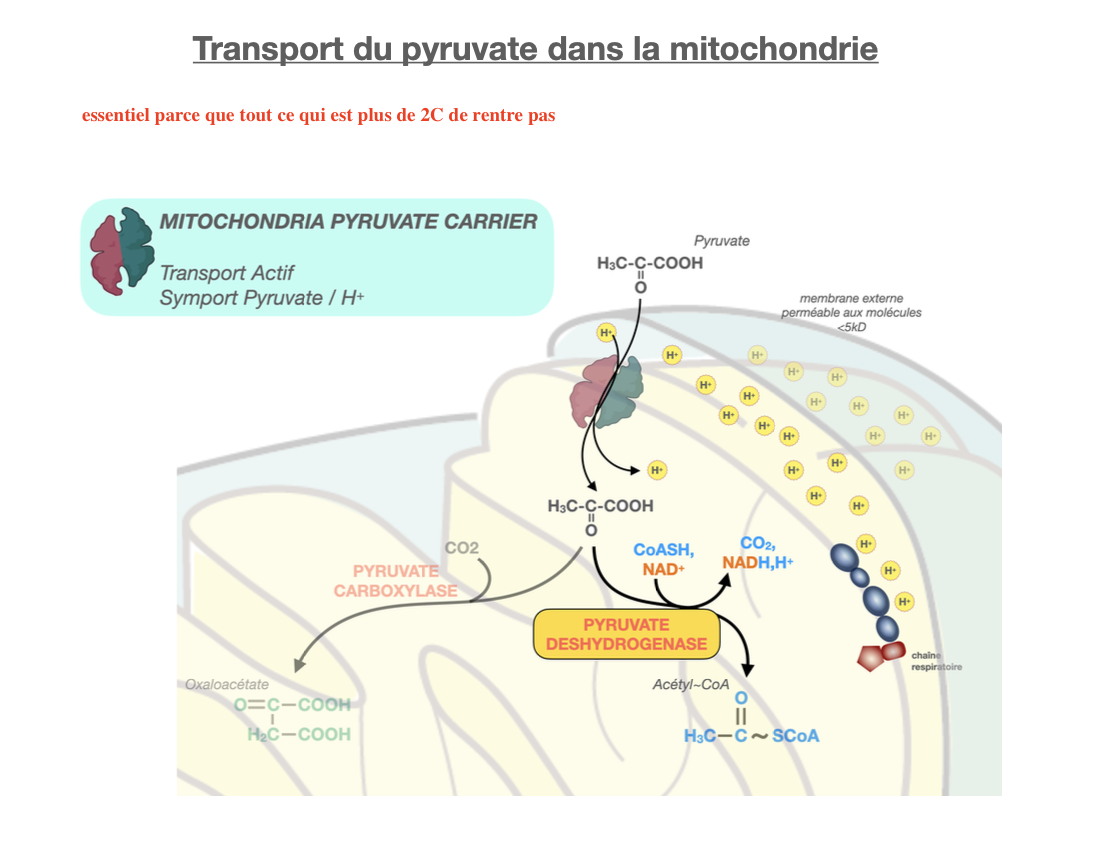
La membrane externe est perméable aux petites molécules (< 5 kDa).
La membrane interne est imperméable : le passage du pyruvate nécessite un transporteur spécifique, le Mitochondrial Pyruvate Carrier (MPC).
Le transport se fait par symport Pyruvate/H⁺, actif et couplé au gradient protonique.
Seules les petites molécules à 2 carbones (comme le pyruvate) peuvent franchir directement, d’où l’importance de cette étape.
2. Destins possibles du pyruvate
Q2. Quels sont les deux grands destins métaboliques du pyruvate une fois dans la mitochondrie ?
R2.
Décarboxylation oxydative par le complexe pyruvate déshydrogénase (PDH)
Pyruvate → Acétyl-CoA
Production de NADH, H⁺ et CO₂
Acétyl-CoA entre ensuite dans le cycle de Krebs pour l’oxydation complète et la production d’ATP.
Carboxylation par la pyruvate carboxylase (PC)
Pyruvate → Oxaloacétate (OAA)
Réaction anaplérotique (réapprovisionnement du cycle de Krebs) ou point de départ de la néoglucogenèse.
🔹 Pyruvate Déshydrogénase 1. Sous-unités
Q1. Quels sont les trois types de sous-unités du complexe pyruvate déshydrogénase et leur rôle ?
2. Coenzymes et co-substrats
Q2. Quels sont les coenzymes et co-substrats associés aux sous-unités de la PDH ?
3. Réaction globale
Q3. Quelle est la réaction catalysée par la pyruvate déshydrogénase ?
🔹 Pyruvate Déshydrogénase 1. Sous-unités
Q1. Quels sont les trois types de sous-unités du complexe pyruvate déshydrogénase et leur rôle ?
R1.
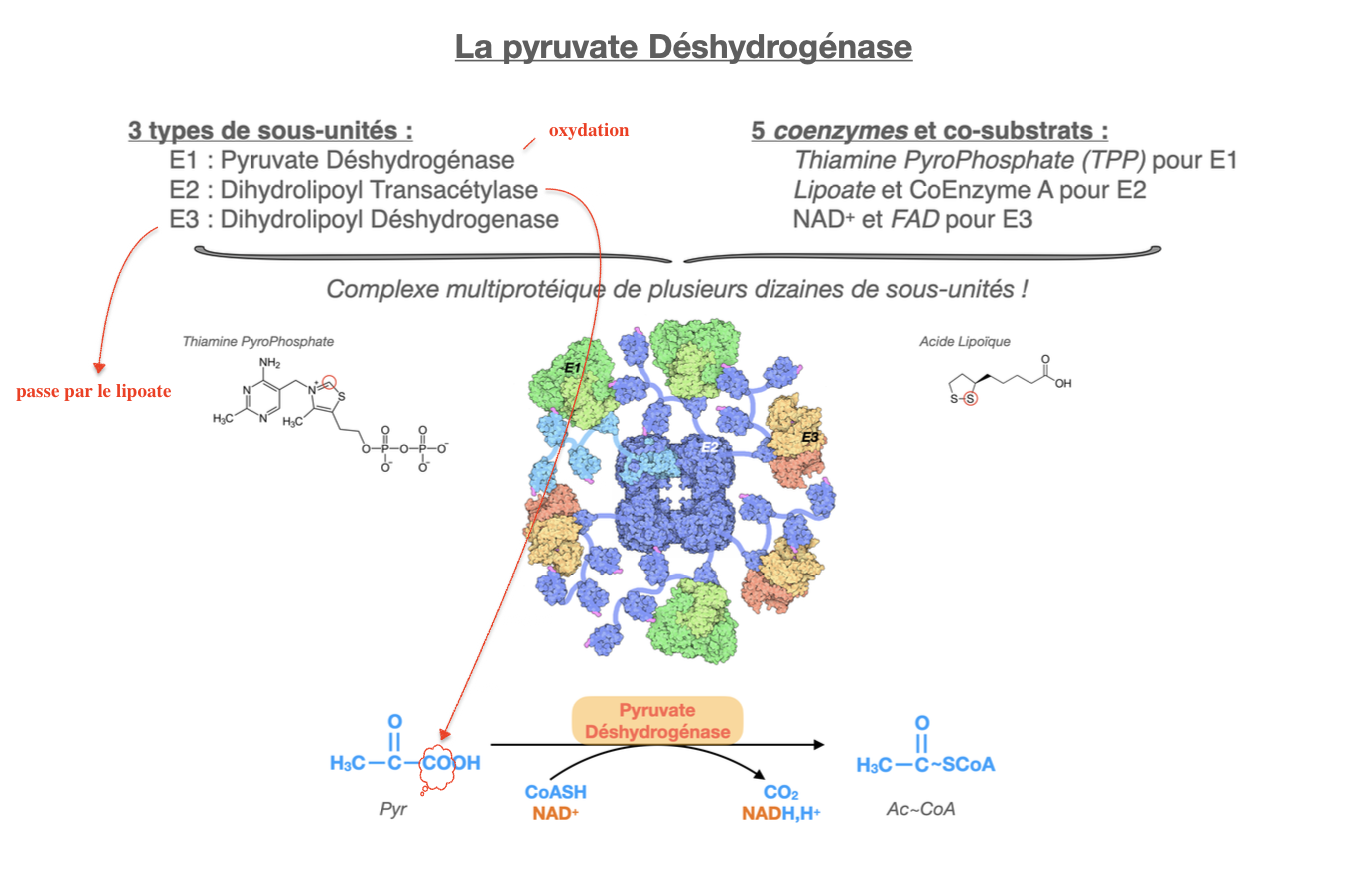
E1 : Pyruvate déshydrogénase → décarboxylation oxydative du pyruvate, transfert du fragment hydroxyéthyle sur le TPP.
E2 : Dihydrolipoyl transacétylase → transfert du groupement acétyle sur le lipoate puis sur le Coenzyme A pour former l’acétyl-CoA.
E3 : Dihydrolipoyl déshydrogénase → régénération du lipoate oxydé grâce au FAD et transfert des électrons sur le NAD⁺.
2. Coenzymes et co-substrats
Q2. Quels sont les coenzymes et co-substrats associés aux sous-unités de la PDH ?
R2.
E1 → Thiamine pyrophosphate (TPP).
E2 → Lipoate et Coenzyme A (CoA-SH).
E3 → FAD et NAD⁺.
3. Réaction globale
Q3. Quelle est la réaction catalysée par la pyruvate déshydrogénase ?
R3.
Pyruvate+CoA-SH+NAD+ ⟶ Aceˊtyl-CoA+CO2+NADH+H+
🔹 Régulation de la Pyruvate Déshydrogénase (PDH) 1. Mécanisme de régulation
Q1. Comment la PDH est-elle régulée par phosphorylation et déphosphorylation ?
Q2. Quelle est la forme active (R) et la forme inactive (T) de la PDH ?
2. Contrôles allostériques et rétroinhibition
Q3. Quels sont les effecteurs allostériques de la PDH Kinase (PDK) et de la PDH Phosphatase (PDP) ?
Q4. Quels sont les rétrocontrôles négatifs de la PDH ?
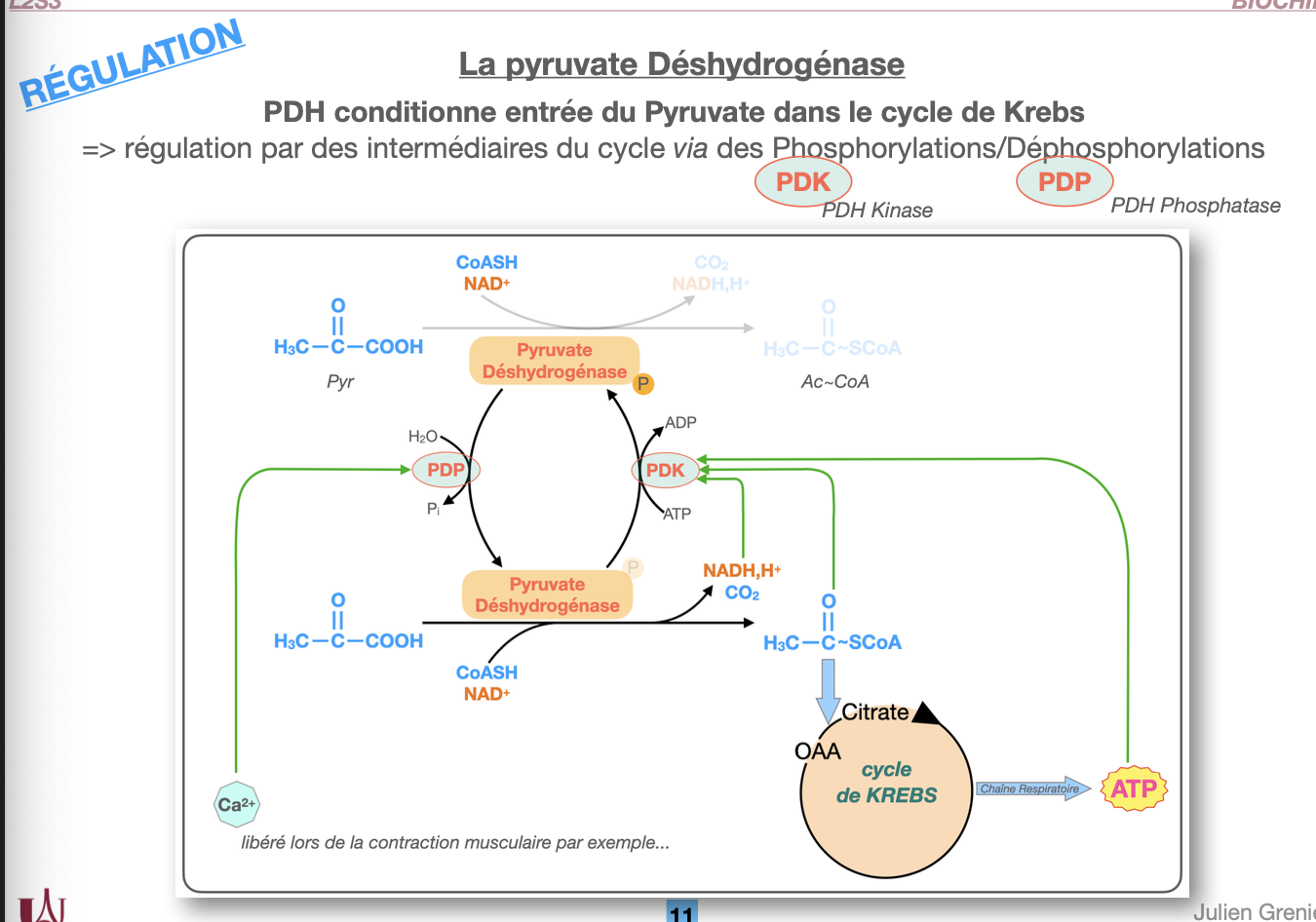
1. Mécanisme de régulation
Q1. Comment la PDH est-elle régulée par phosphorylation et déphosphorylation ?
Q2. Quelle est la forme active (R) et la forme inactive (T) de la PDH ?
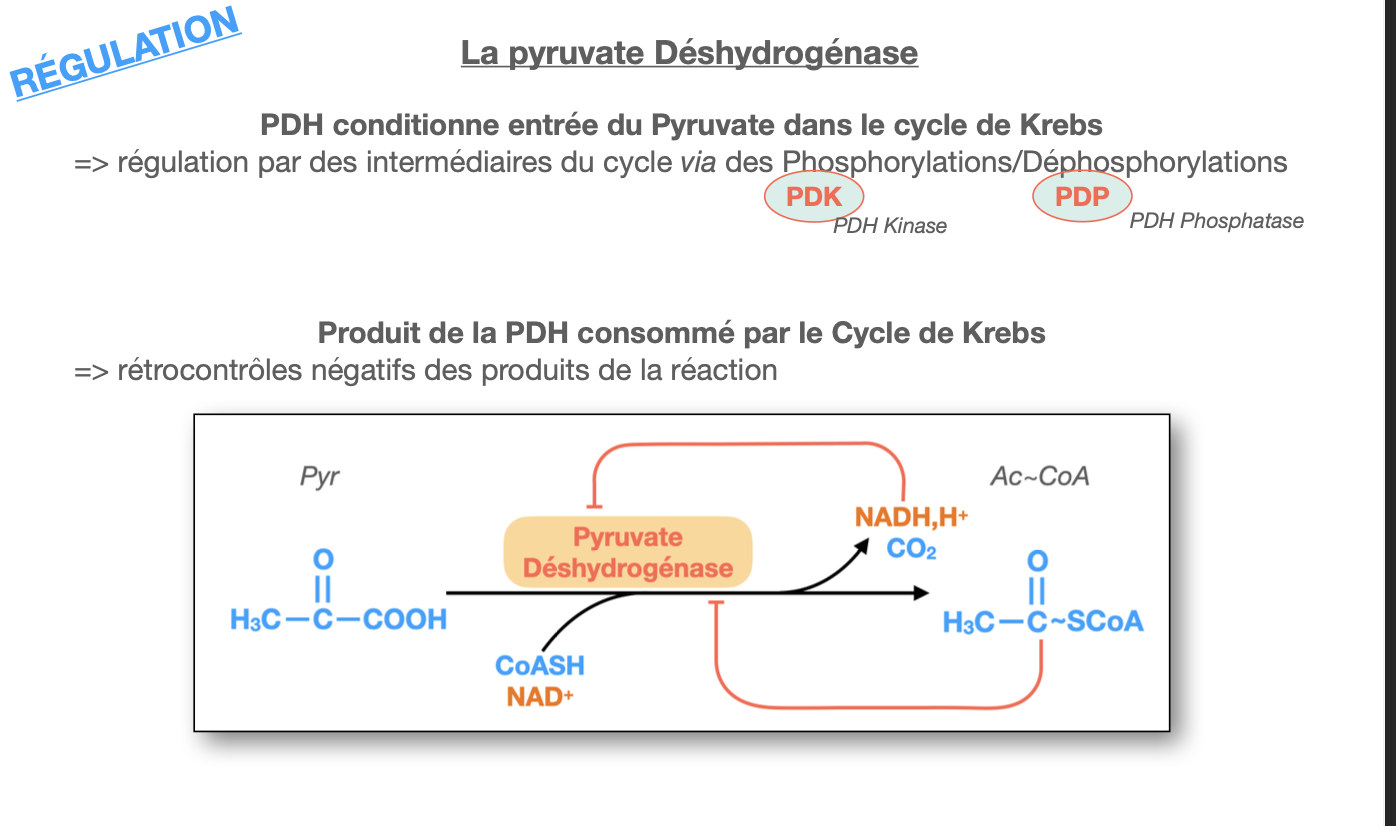
R1. La régulation repose sur un cycle de phosphorylation/déphosphorylation :
PDH Kinase (PDK) → phosphoryle la PDH → inactivation.
PDH Phosphatase (PDP) → déphosphoryle la PDH → activation.
R2.
Forme déphosphorylée = active (R).
Forme phosphorylée = inactive (T).
Le Ca²⁺ (libéré notamment lors de la contraction musculaire) active la PDP, favorisant donc la forme R pour stimuler la production d’ATP.
2. Contrôles allostériques et rétroinhibition
Q3. Quels sont les effecteurs allostériques de la PDH Kinase (PDK) et de la PDH Phosphatase (PDP) ?
Q4. Quels sont les rétrocontrôles négatifs de la PDH ?
R3.
Activation de la PDK (favorise l’inactivation de PDH) : ATP, NADH, Acétyl-CoA (témoins d’un état énergétique élevé).
Inhibition de la PDK (favorise l’activation de PDH) : ADP, pyruvate, Ca²⁺ (témoins d’un besoin énergétique).
Activation de la PDP : Ca²⁺ (notamment dans le muscle).
R4. Les produits directs de la réaction catalysée par la PDH, à savoir NADH et Acétyl-CoA, exercent un rétrocontrôle négatif sur l’enzyme pour éviter une surproduction.
bilan pour un tour de cycle de krebs

1. Production de CO₂
Q1. Quelles étapes du cycle produisent les 2 molécules de CO₂ ?
2. Production de NADH,H⁺
Q2. Quelles étapes produisent les 3 molécules de NADH,H⁺ ?
3. Production de FADH₂
Q3. Quelle étape produit le FADH₂ ?
4. Production de GTP
Q4. Quelle étape produit le GTP (équivalent ATP) ?

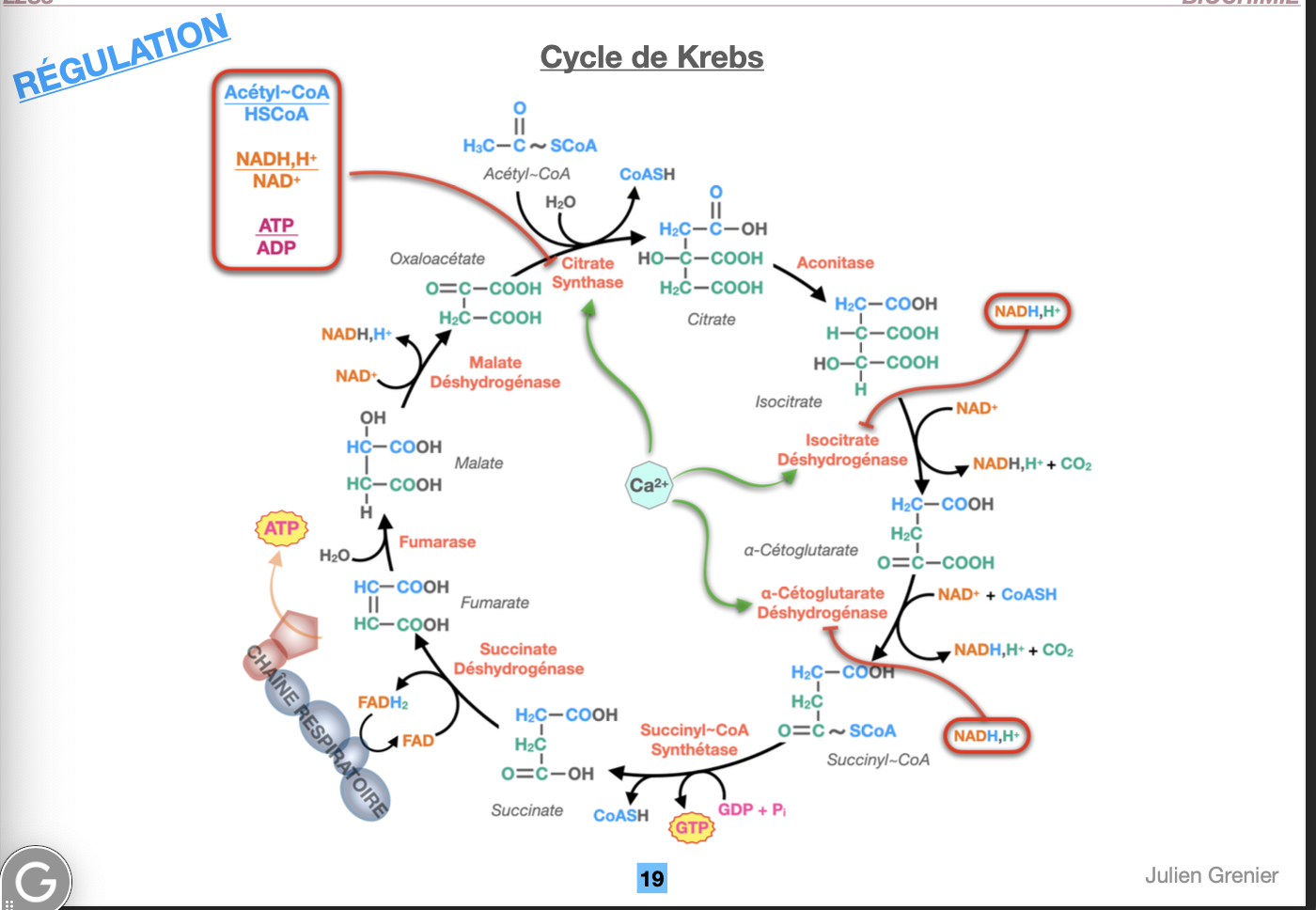
1. Production de CO₂
Q1. Quelles étapes du cycle produisent les 2 molécules de CO₂ ?
R1.
Isocitrate déshydrogénase : conversion de l’isocitrate en α-cétoglutarate → libération d’1 CO₂.
α-cétoglutarate déshydrogénase : conversion de l’α-cétoglutarate en succinyl-CoA → libération d’1 CO₂.
2. Production de NADH,H⁺
Q2. Quelles étapes produisent les 3 molécules de NADH,H⁺ ?
R2.
Isocitrate déshydrogénase (isocitrate → α-cétoglutarate).
α-cétoglutarate déshydrogénase (α-cétoglutarate → succinyl-CoA).
Malate déshydrogénase (malate → oxaloacétate).
3. Production de FADH₂
Q3. Quelle étape produit le FADH₂ ?
R3.
Succinate déshydrogénase : transformation du succinate en fumarate → réduction du FAD en FADH₂.
4. Production de GTP
Q4. Quelle étape produit le GTP (équivalent ATP) ?
R4.
Succinyl-CoA synthétase : conversion du succinyl-CoA en succinate → production d’1 GTP par phosphorylation au niveau du substrat.

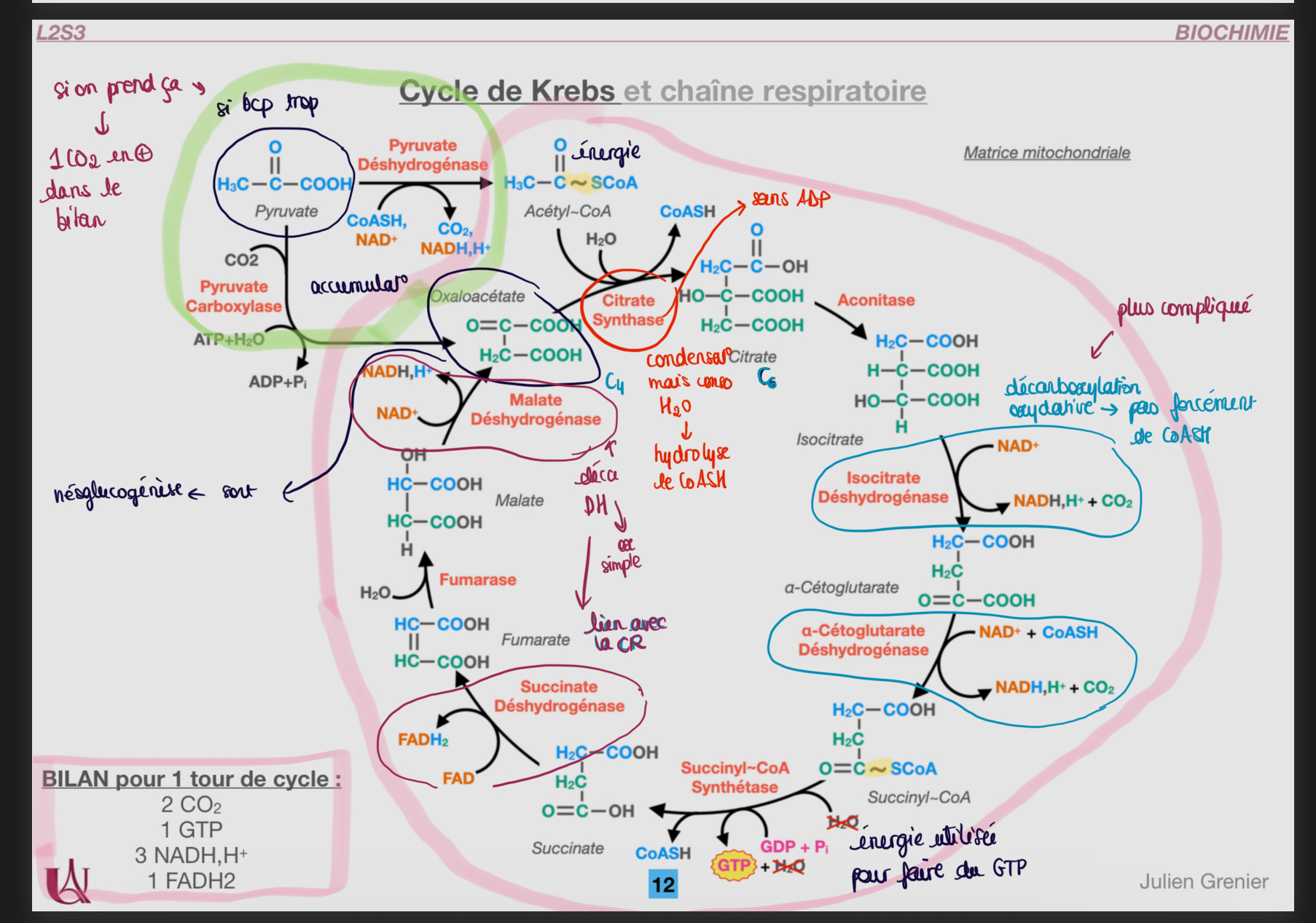
🔹 Chaîne respiratoire et recyclage des coenzymes
1. Importance du pouvoir oxydant
Q1. Pourquoi le recyclage des coenzymes réduits (NADH, FADH₂) est-il indispensable au métabolisme cellulaire ?
2. Complexes de la chaîne
Q2. Quels sont les 5 grands complexes de la chaîne respiratoire et leurs rôles ?
3. Transporteurs mobiles
Q3. Quels sont les transporteurs mobiles d’électrons de la chaîne ?
4. Bilan énergétique
Q4. Quel est le rendement en ATP de la réoxydation des coenzymes réduits par la chaîne respiratoire ?
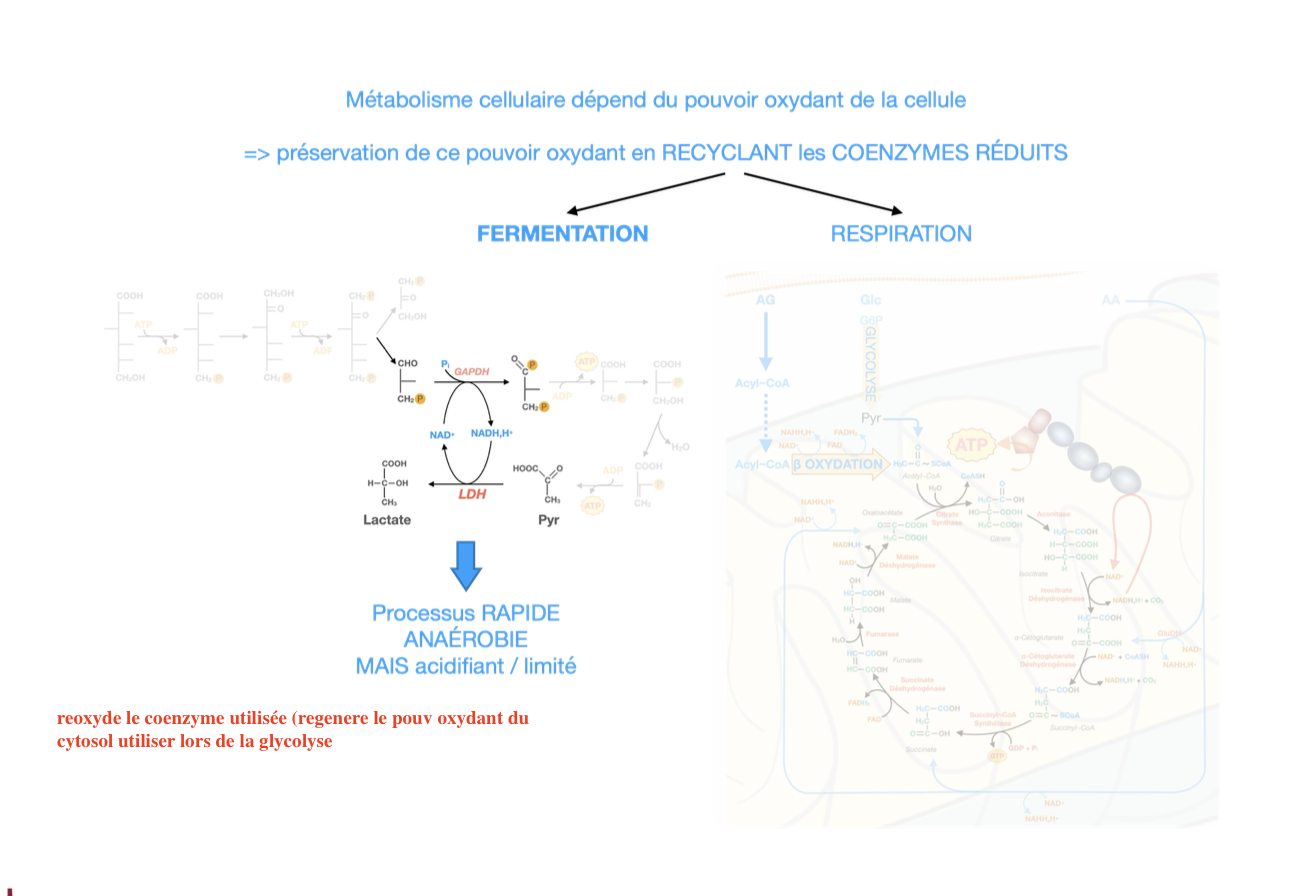
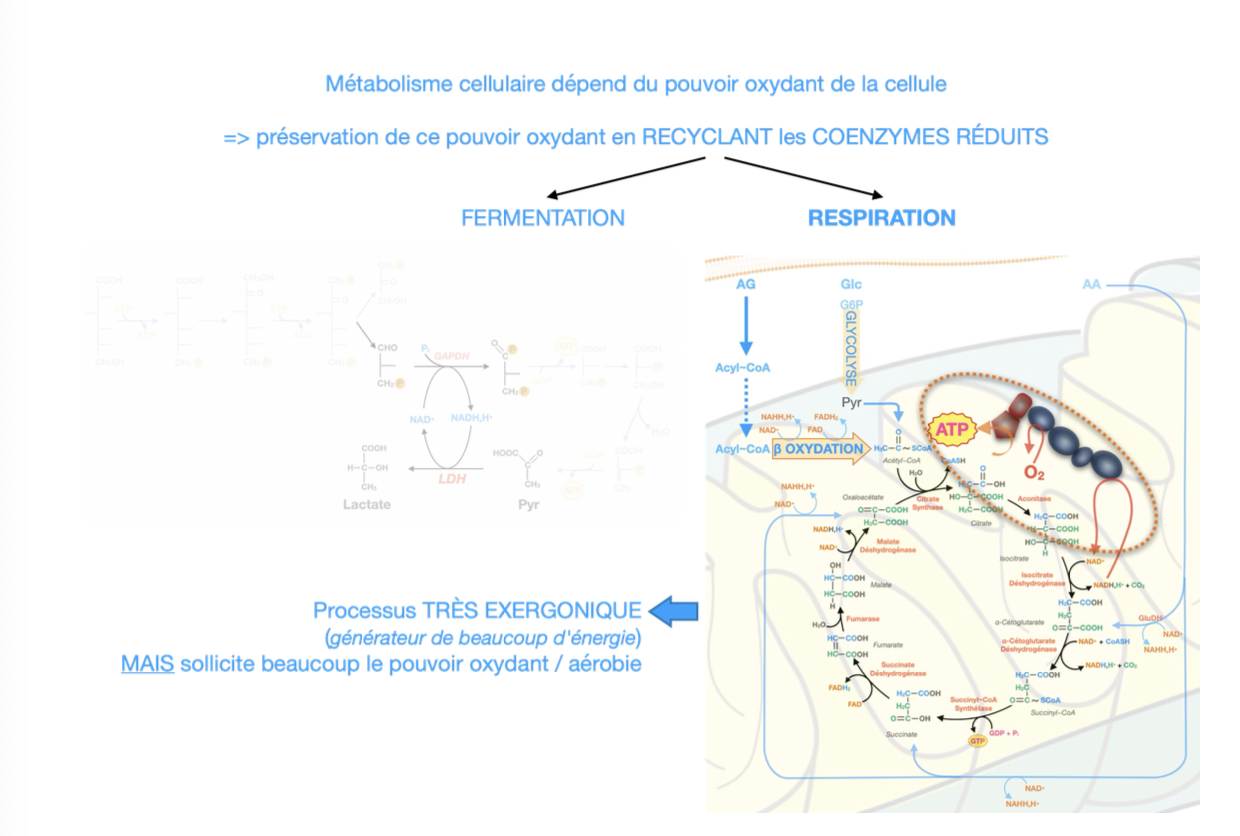

1. Importance du pouvoir oxydant
Q1. Pourquoi le recyclage des coenzymes réduits (NADH, FADH₂) est-il indispensable au métabolisme cellulaire ?
R1. Parce que le métabolisme dépend du pouvoir oxydant (NAD⁺, FAD) nécessaire aux réactions d’oxydation (ex. glycolyse, β-oxydation). Sans régénération, les voies cataboliques s’arrêtent.
Le recyclage se fait par :
Fermentation (anaérobie) → régénération rapide mais limitée de NAD⁺, production de lactate, acidification.
Respiration mitochondriale (aérobie) → réoxydation massive des coenzymes réduits via la chaîne respiratoire, avec production d’ATP.
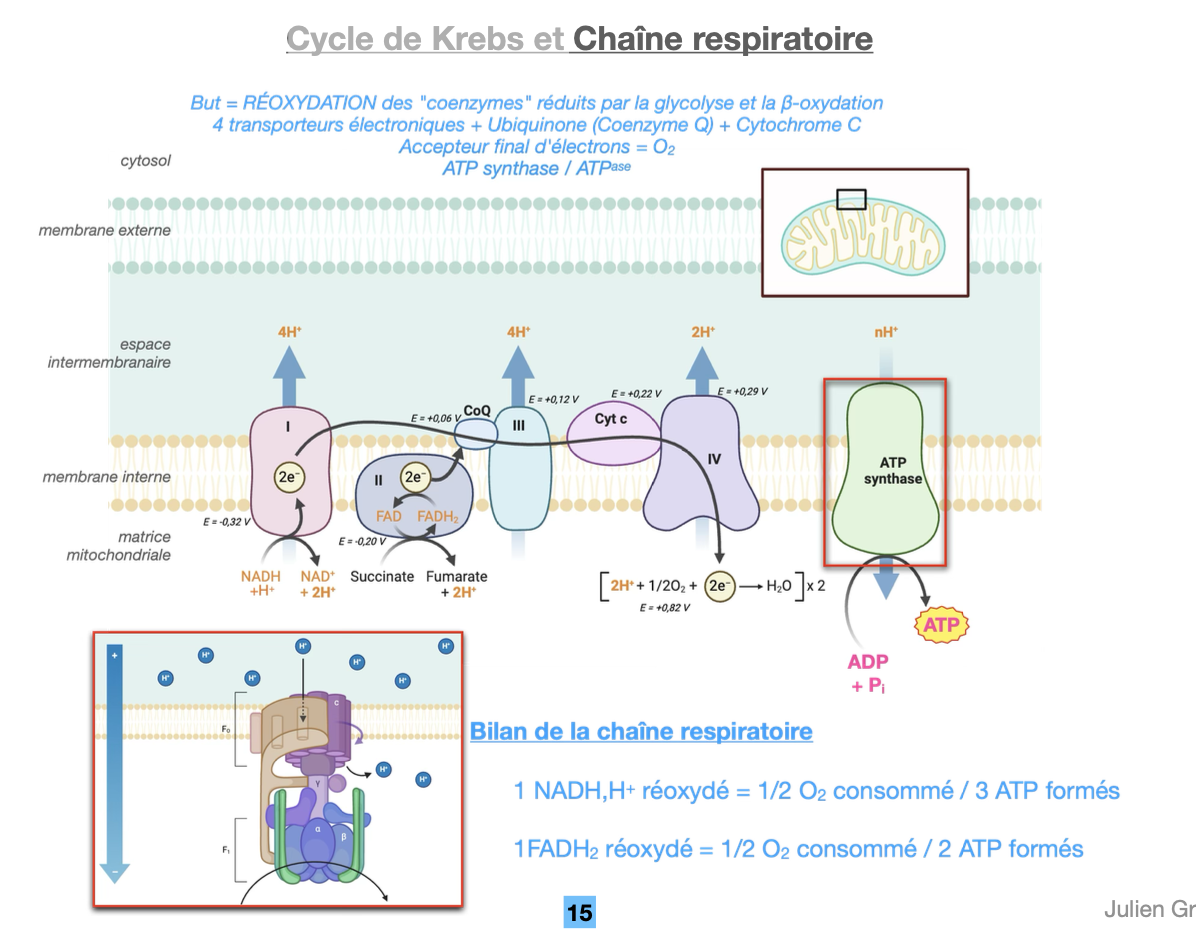
2. Complexes de la chaîne
Q2. Quels sont les 5 grands complexes de la chaîne respiratoire et leurs rôles ?
R2.
Complexe I (NADH déshydrogénase / NADH-Q réductase) → oxyde NADH, transfère électrons au coenzyme Q, pompe 4 H⁺.
Complexe II (Succinate déshydrogénase) → oxyde FADH₂, transfère électrons au Q, pas de pompage.
Complexe III (Ubiquinol-cytochrome c réductase) → transfère électrons de QH₂ au cytochrome c, pompe 4 H⁺.
Complexe IV (Cytochrome c oxydase) → transfère électrons du cyt c à O₂ (accepteur final) → H₂O, pompe 2 H⁺.
Complexe V (ATP synthase) → utilise le gradient de protons pour produire l’ATP par rotation mécanique.
3. Transporteurs mobiles
Q3. Quels sont les transporteurs mobiles d’électrons de la chaîne ?
R3.
Ubiquinone (Q) : liposoluble, transporte électrons entre complexes I/II et III.
Cytochrome c : protéine soluble, transporte électrons entre complexe III et IV.
4. Bilan énergétique
Q4. Quel est le rendement en ATP de la réoxydation des coenzymes réduits par la chaîne respiratoire ?
R4.
1 NADH,H⁺ → ½ O₂ consommé → environ 2,5–3 ATP.
1 FADH₂ → ½ O₂ consommé → environ 1,5–2 ATP.

role du calcium