RECETTORI MUSCARINICI e farmaci che agiscono su di loro
1/30
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
31 Terms
Caratteristiche generali dei recettori muscarinici e localizzazione
Sono GPCR dispari (Gq quindi scindono il PIP2 in IP3 e DAG) e pari (Gi o Go quindi inibiscono l’adenilato ciclasi riducendo il cAMP).
Il riconoscimento avviene a livello extracellulare ma il sito ortosterico si trova vicino allo strato lipidico, presenta anche dei siti allosterici. Le regioni ortosteriche sono molto conservate in tutte le classi di recettori —> difficiele la selettività d’azione: non esistono agonisti recettoriali selettivi (al massimo agonisti funzionali ossia preferiscono una via trasduzionale) mentre esistono antagonisti selettivi perchè agiscono sui siti allosterici meno conservati.
Periferici: a livello post-sinaptico
Cuore (M2)—> bradicardia
Ghiandole esocrine (M3)—> aumento dell’escrezione
Muscolatura liscia—> contrazione
Vasi sanguigni —> vasodilatazione
Centrali : corteccia ed ippocampo
Funzioni vegetative, sensoriali, motorie (sonno e T corsporea) e cognitive superiori (memoria e apprendimento)
Risposte più lente dei recettori nicotinici e possono influenzare anche l’attività di alcuni canali ionici.
Interazioni dell’acetilcolina sui recettori muscarinici
L’Ach si inserisce nel sito di riconoscimento ortosterico del recettore interagendo con aminoacidi omologhi presenti in tutti i recettori nicotinici:
interazione ionica con l’aspartato —> gruppo amminico carico +
Legami H con tirosina e treonina —> gruppo estereo
Requisiti strutturali essenziali che deve possedere una molecola per interagire con il recettore muscarinico
Testa ammonica quaternaria
Quando i sostituenti di N sono dei metili = massima attività
Presenza di un O estereo per la formazione di legami H
Regola dei 5 atomi: distanza tra N e C acilico deve essere di 5 atomi
Agonisti muscarinici elenco
Metacolina
Carbacolo
Metanecolo
Policarpina
Arecolina
Ossotremorina
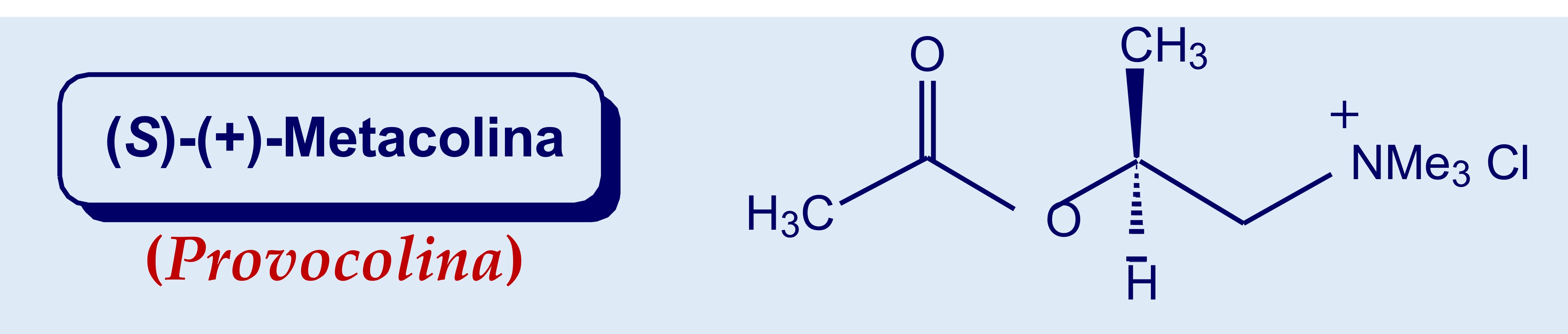
Metacolina (struttura, stereochimica e caratteristiche)
Aggiunta di un metile in beta all’Ach= selettività d’azione sui recettori muscarinici
Nuovo centro chirale = 2 stereoisomeri possibili—> attivo enantiomero S
Attività d’azione breve per idrolisi dell’estere ma maggiore dell’Ach
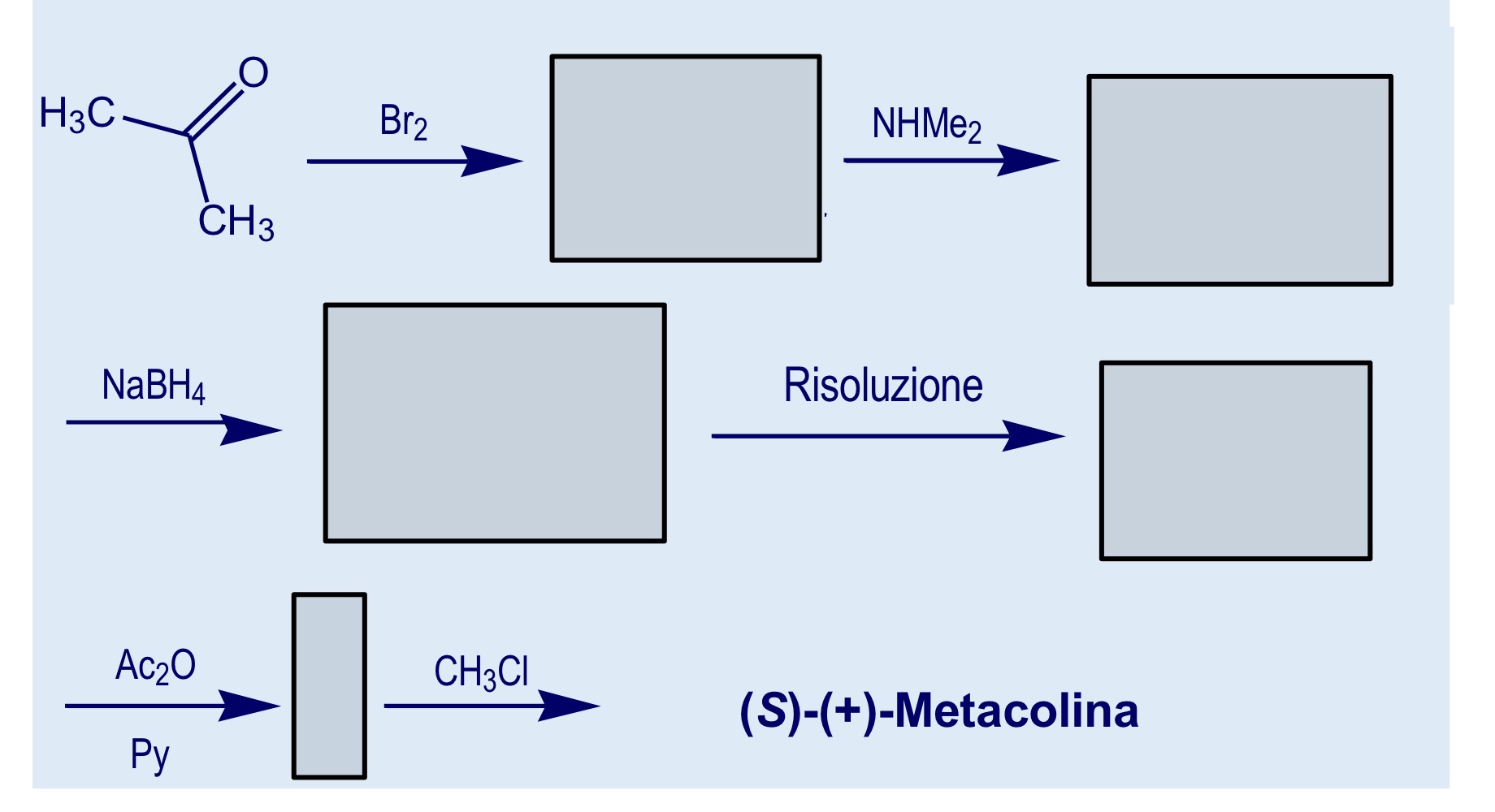
Sintesi metacolina
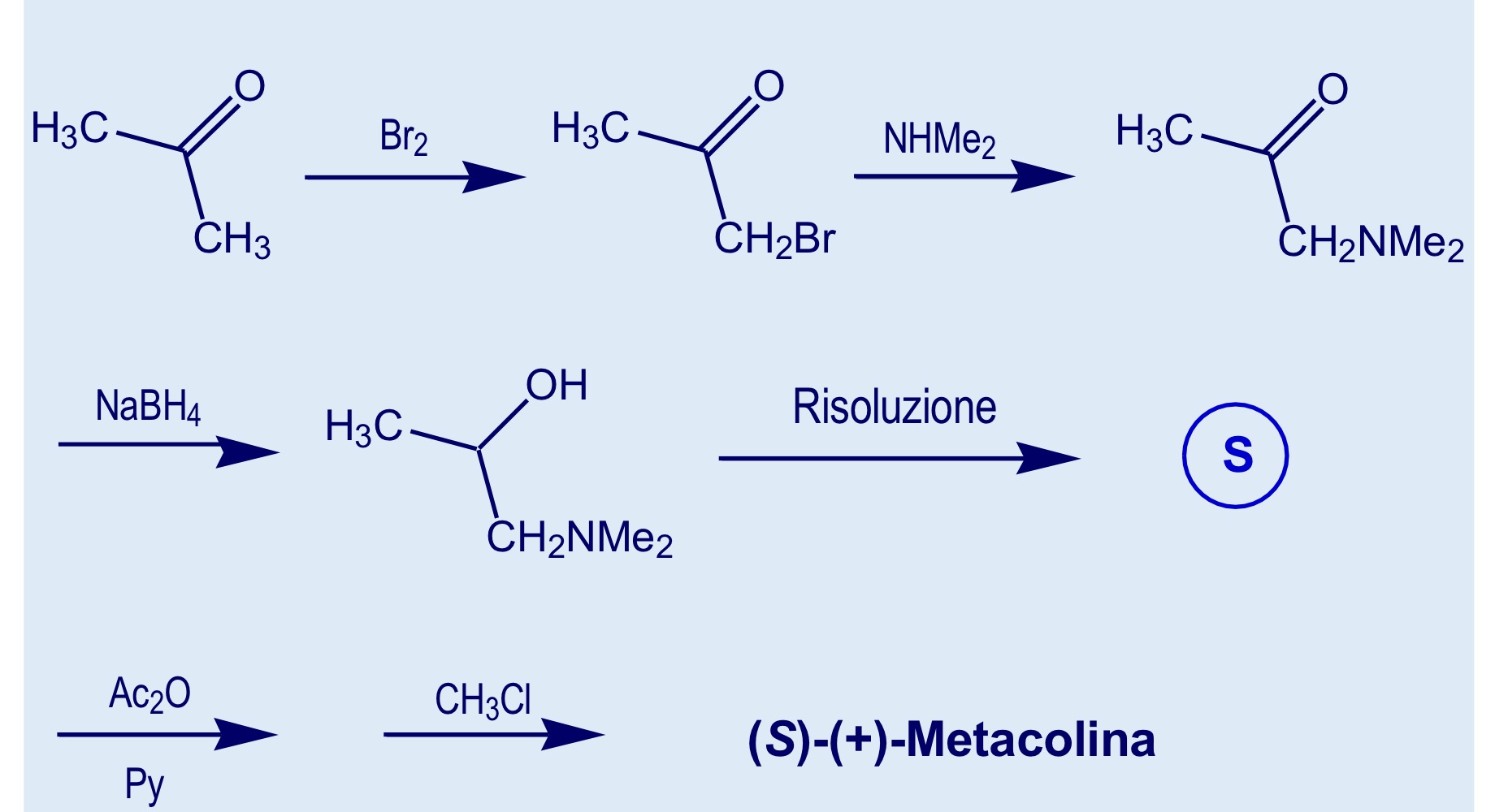
Carbacolo
Carbammato dell’Ach resistente all’idrolisi
Più attivo dell’Ach—> carbammato probabilmente forma dei legami maggiori con il recettore
Ha azione sia nicotinica che muscarinica
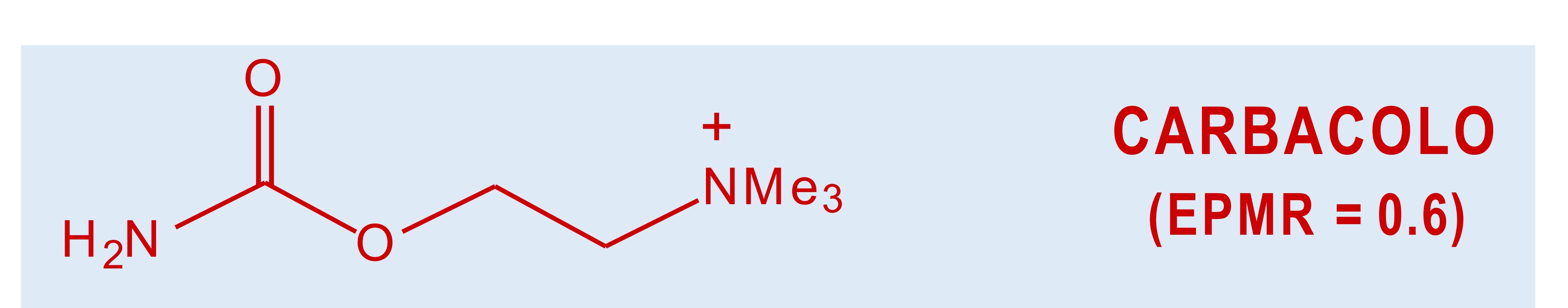
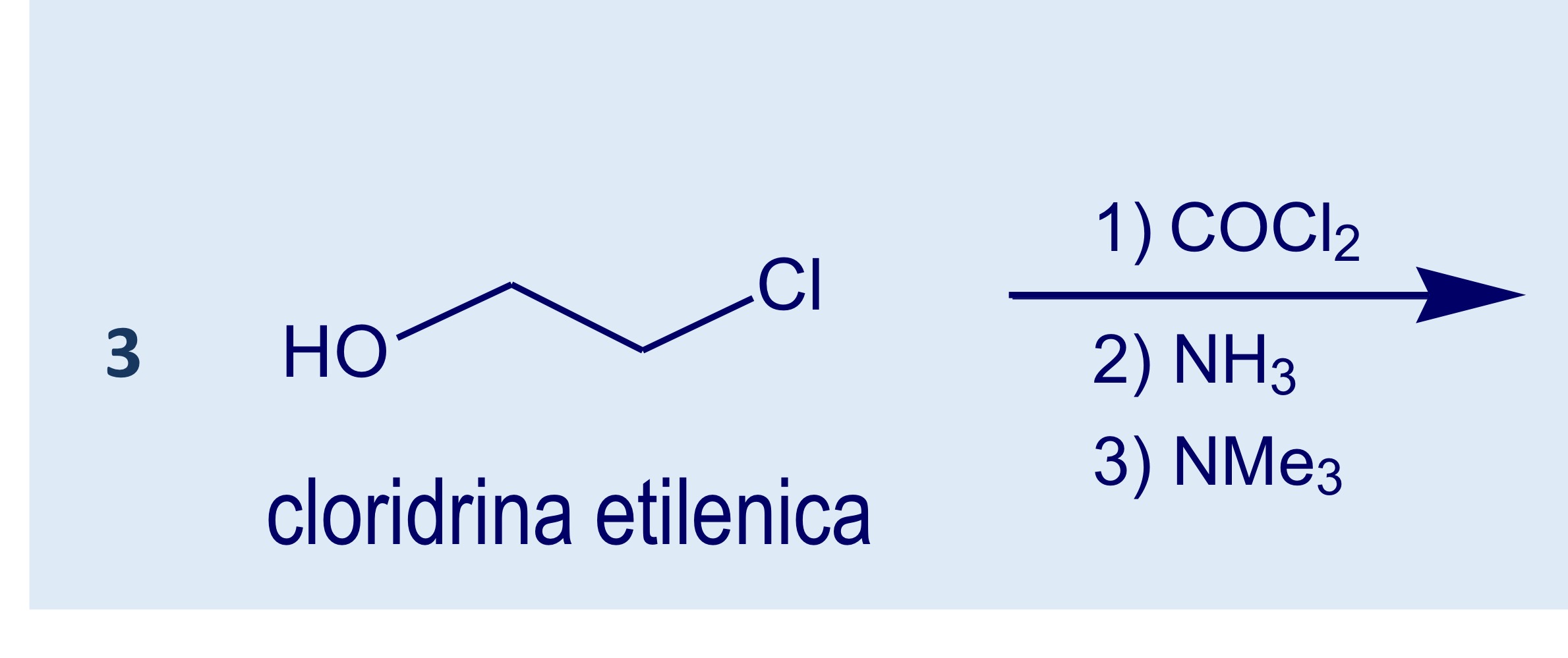
Sintesi carbacolo
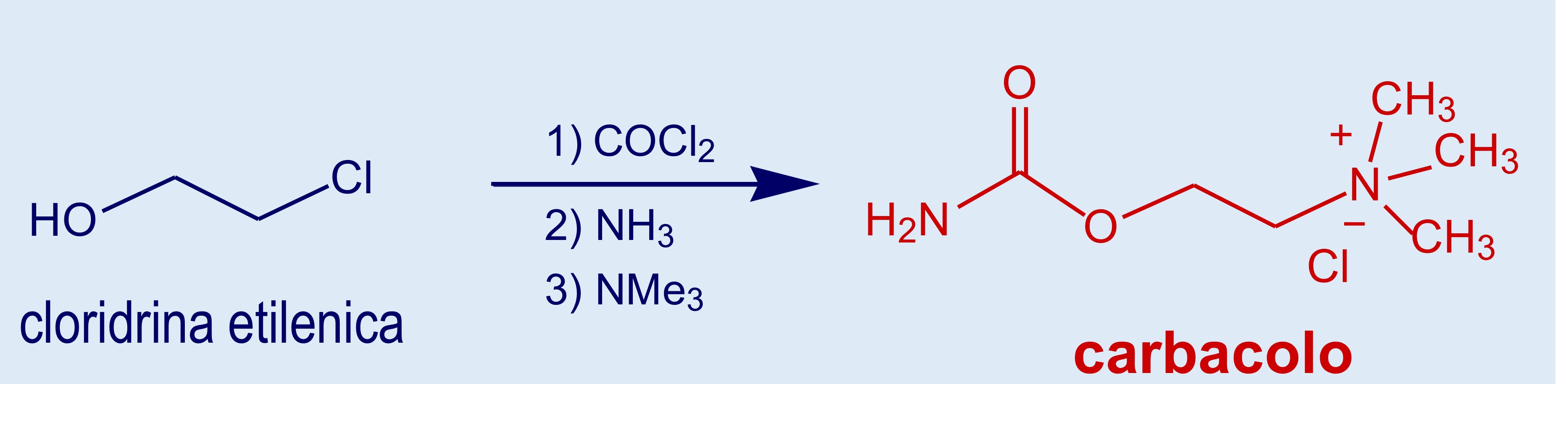
Betanecolo
Carbammato della metacolina resistente all’idrolisi
Attività simile all’Ach —> attivo solo l’enantiomero S (stereoselettività come il metanecolo)
Selettivo sui recettori muscarinici
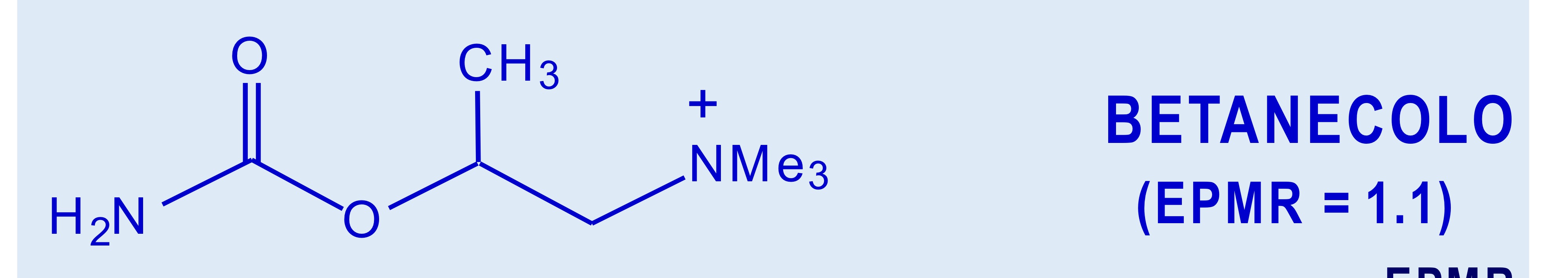
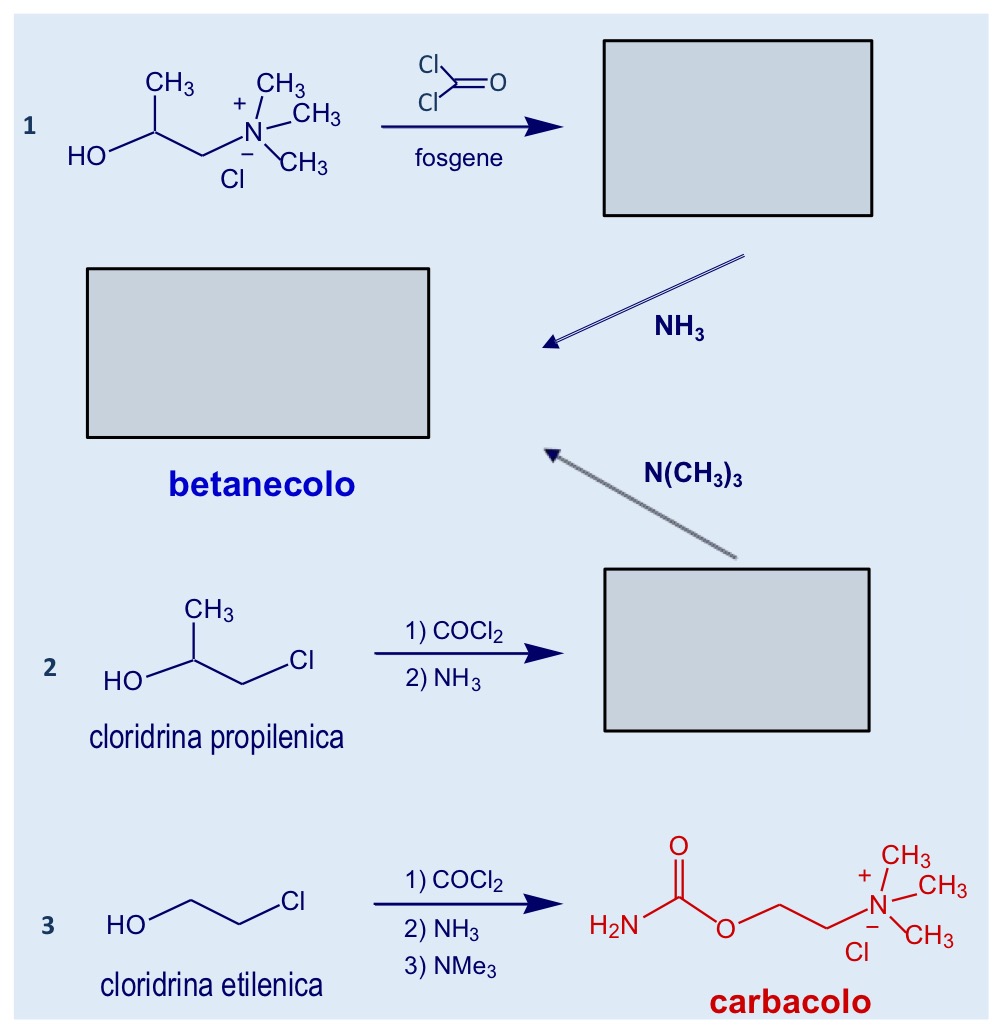
Sintesi betanecolo e risoluzione del racemo
Per isolare l’enantiomero S faccio reagire la miscela racemica con acidi e genero i sali diastereomeri che possono poi essere separati
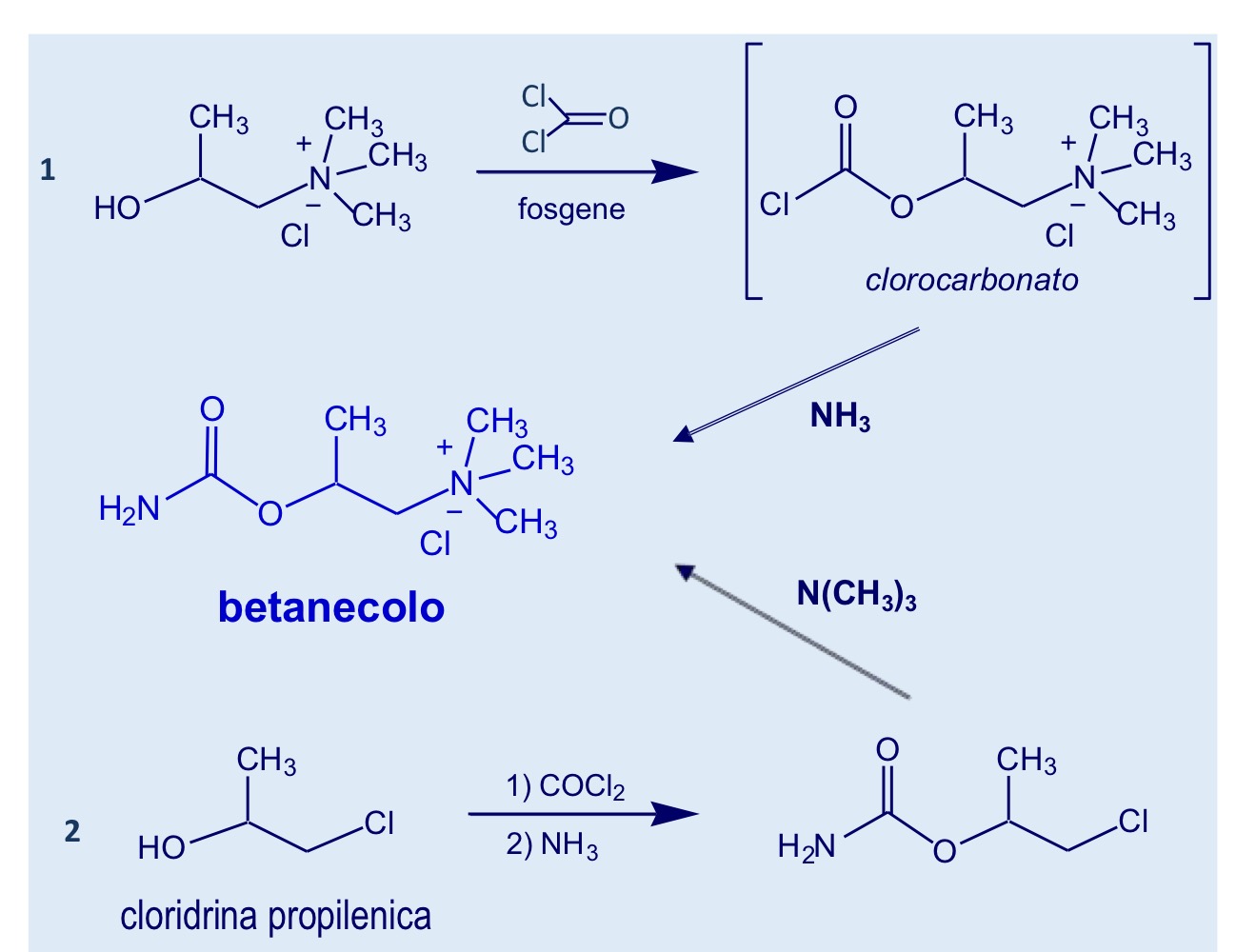
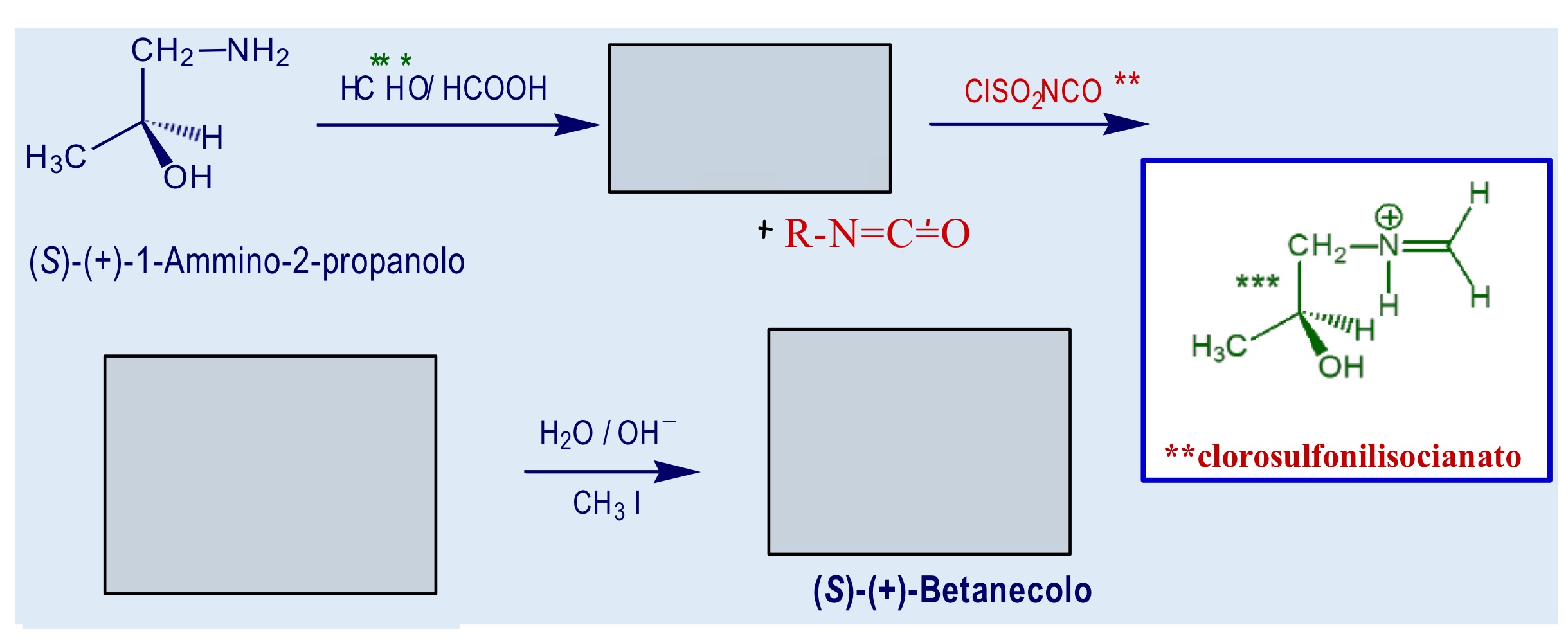
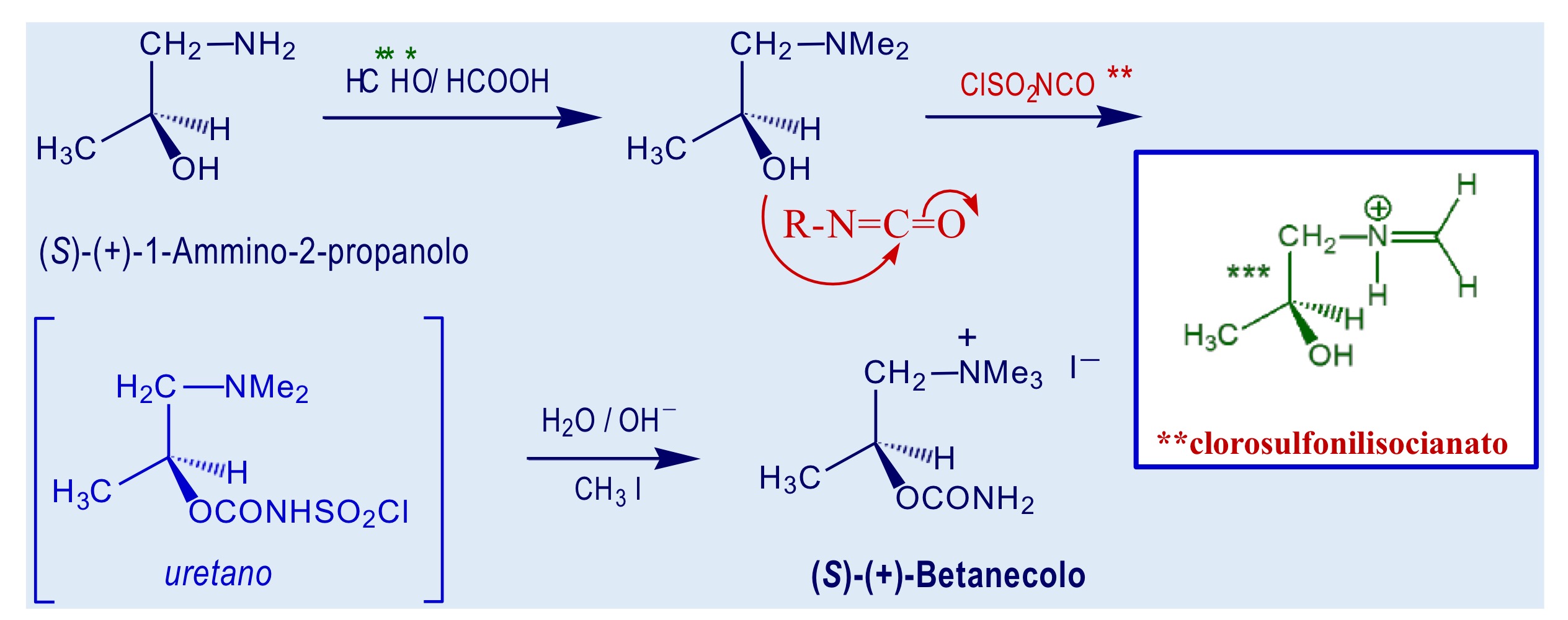
Sintesi enantiomerica del betanecolo
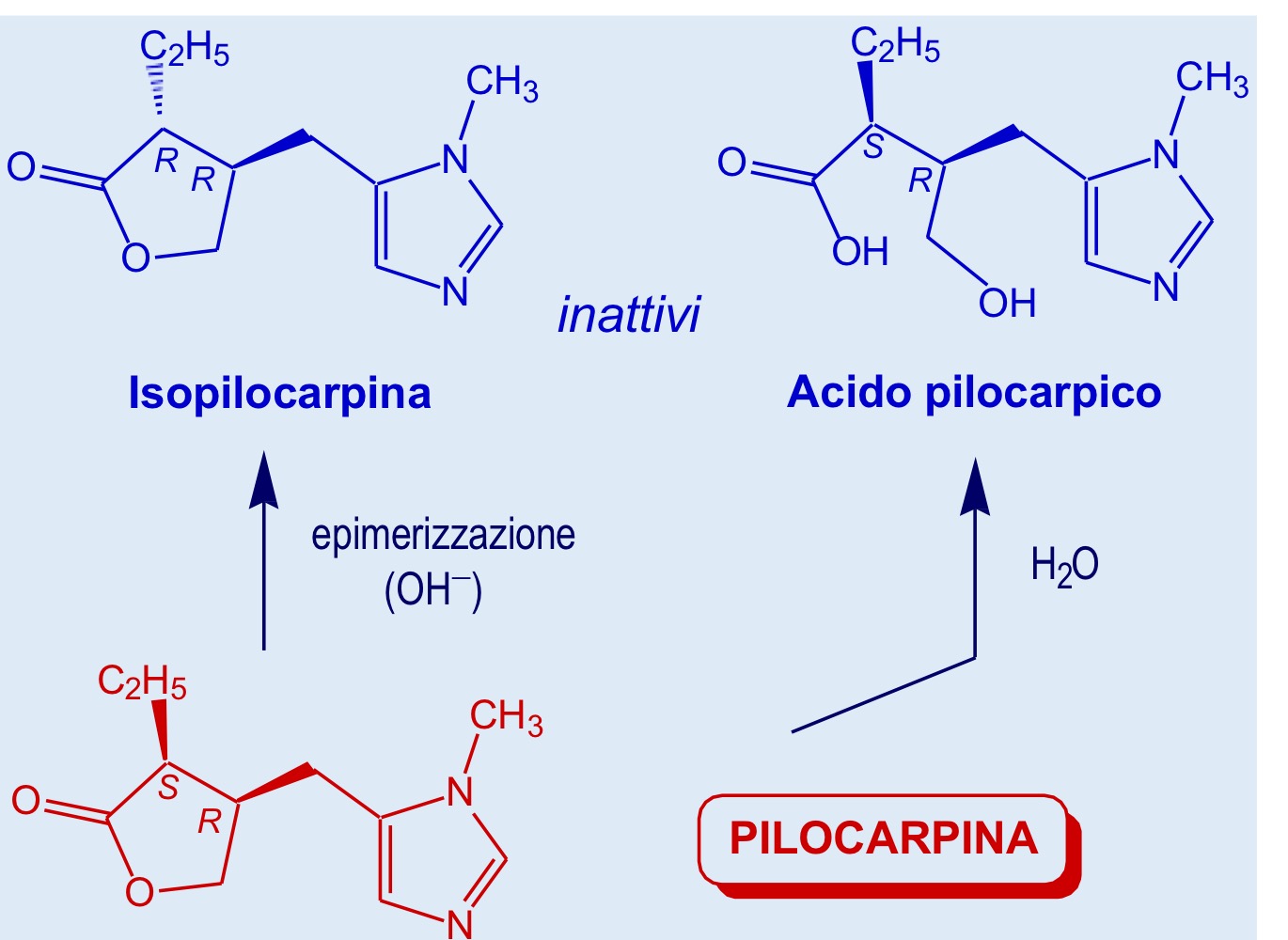
Pilocarpina (struttura e caratteristiche)
P.52
Alcaloide naturale
Bassa biodisponibilità ma non ha cariche permanenti quindi può andare anche a livello centrale
Non è selettiva, è un’agonista parziale di M1 ed ha un’attività indiretta perchè blocca l’acetilcolinesterasi
In ambiente indrolitico può aprire il lattone dando acido pilorico, mentre in condizione basiche può andare incontro ad epimerizzazione dando l’isomero trans più stabile di quello cis
Arecolina (struttura e caratteristiche)
P.53
Molecola di origine naturale
Molecola basica pka=7,8 una piccola percentuale a pH fisiologico non è protonata quindi può andare a livello centrale dove si protona completamente e quindi rimane “bloccata” e svolge la sua azione.
per renderla meno basica quindi più lipofila e più attiva si è creato un suo bioisostero ossia è stato aggiunto un gruppo isossazolico.
Il derivato propargilico, invece, è più attivo di ACh ed è selettivo per gli M2
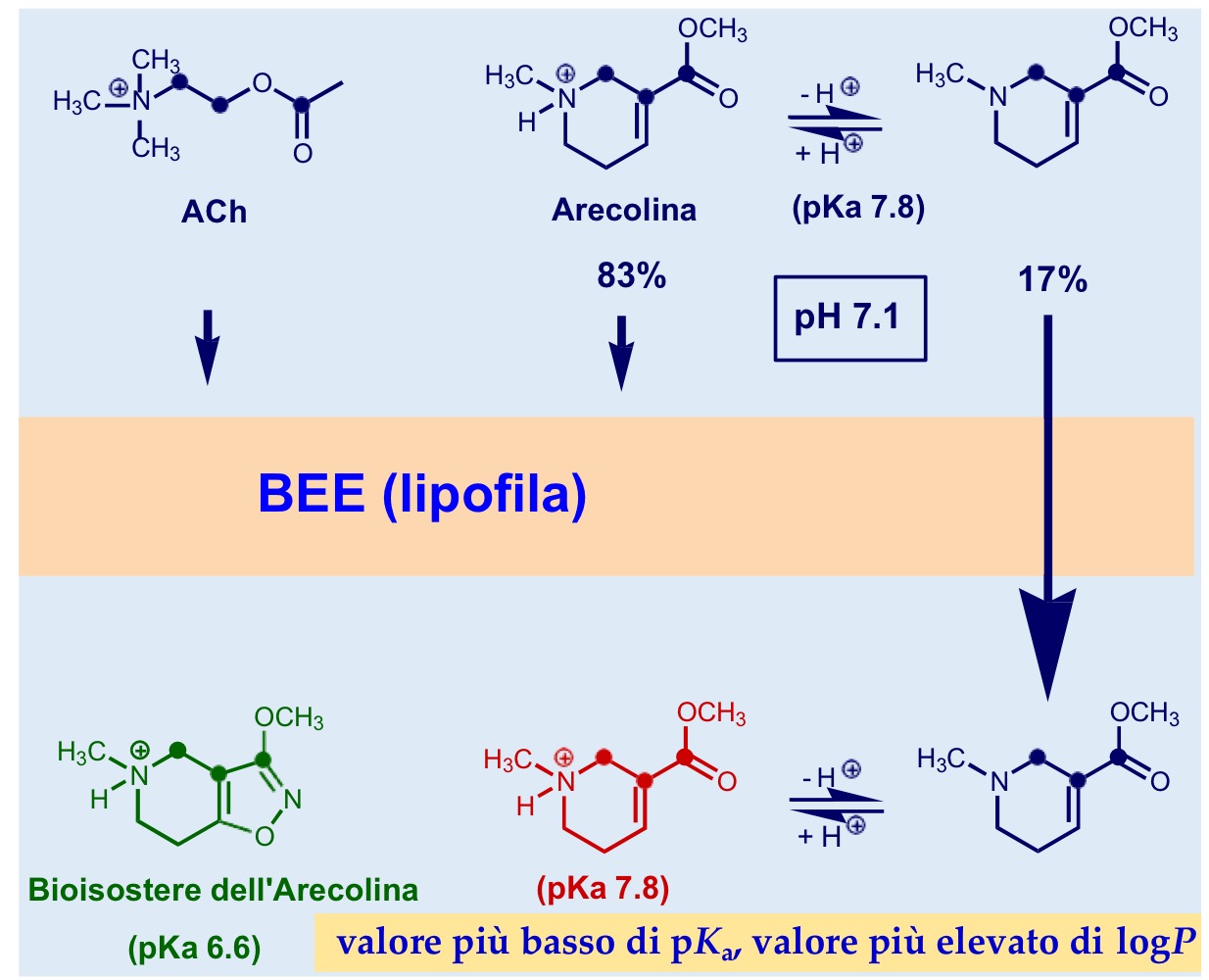
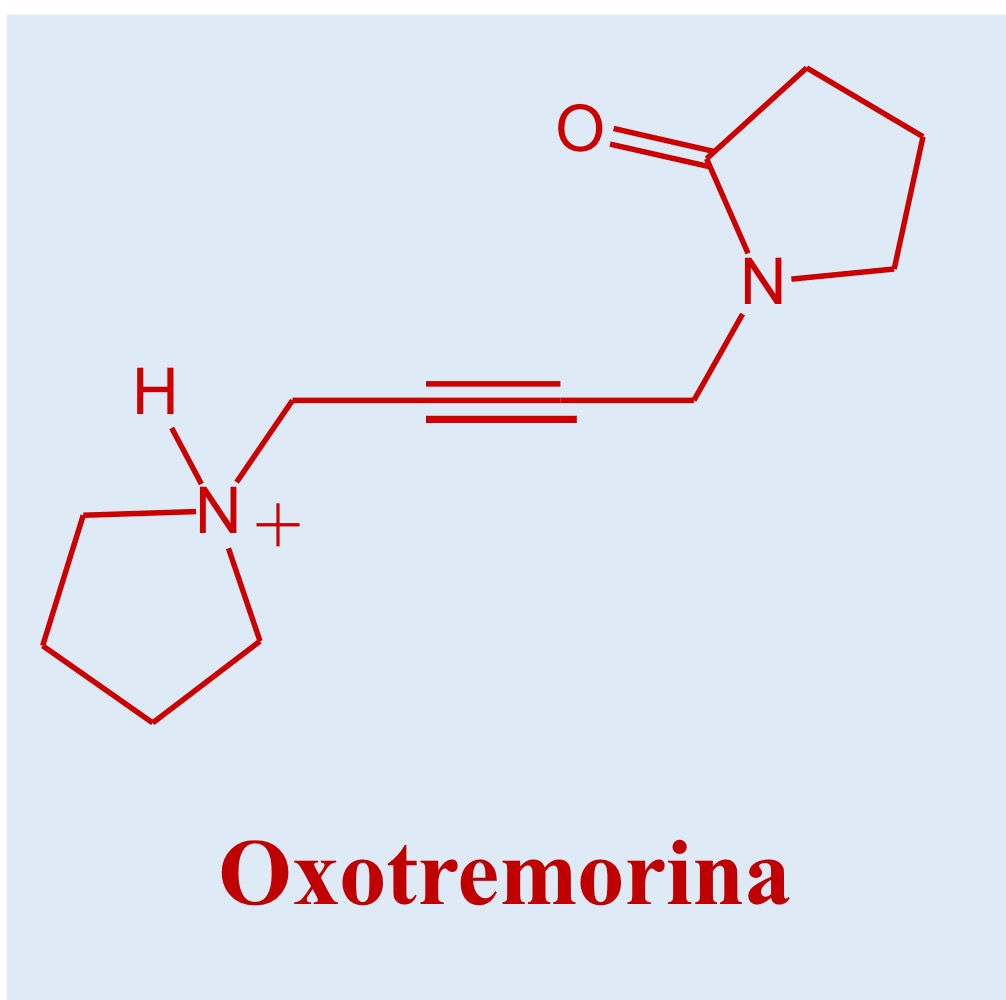
Riconosci la molecola e descrivila
Ossotremorina P.56
Molecola di sintesi che presenta un lattame ed una pirrolidina basica. È molto potente con selettività per gli M2, attiva sia su SNC che su SNP.
Effetti collaterali: provoca tremori che ricordano il Parkinson
Antagonisti muscarinici elenco
Antiulcera (pirenzepina)
Spasmolitici (tolterodina per incontinenza urinaria)
Midriatici (atropina e scopolamina)
Antiparkinsoniani : propanolammine sostituite (es. prociclidina) e benzatropina
Antibradicardici—> molecole selettive per M2: otenzepad, metoctramina, tripitramina
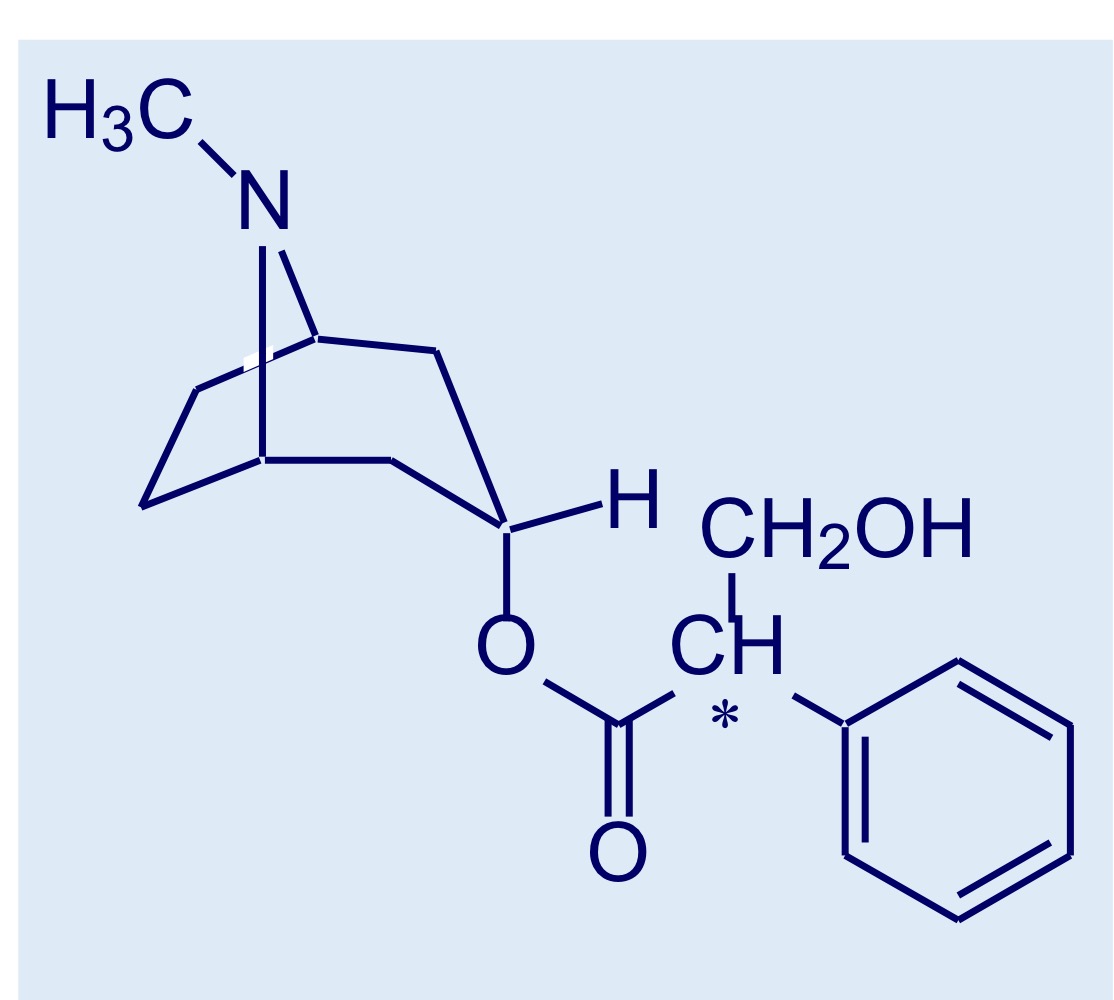
Riconosci la molecola caratteristiche
Atropina P.68
Molecola di origine naturale costituita da acido tropico ed 3-tropanolo (o tropina). Presenta un centro chirale con stereochimica S (più potente) ma viene persa durante la fase di estrazione, si somministra come racemo
Antagonista muscarinico non selettivo e senza componenti nicotiniche.
Presenta un gruppo amminico protonabile ed ha effetti sia periferici che centrali; esistono dei derivati 4° per solo uso periferico.
Viene usato come “prototipo” per la progettazione di antimuscarinici di sintesi. Usi terapeutici: midriatico e cicloplecico.
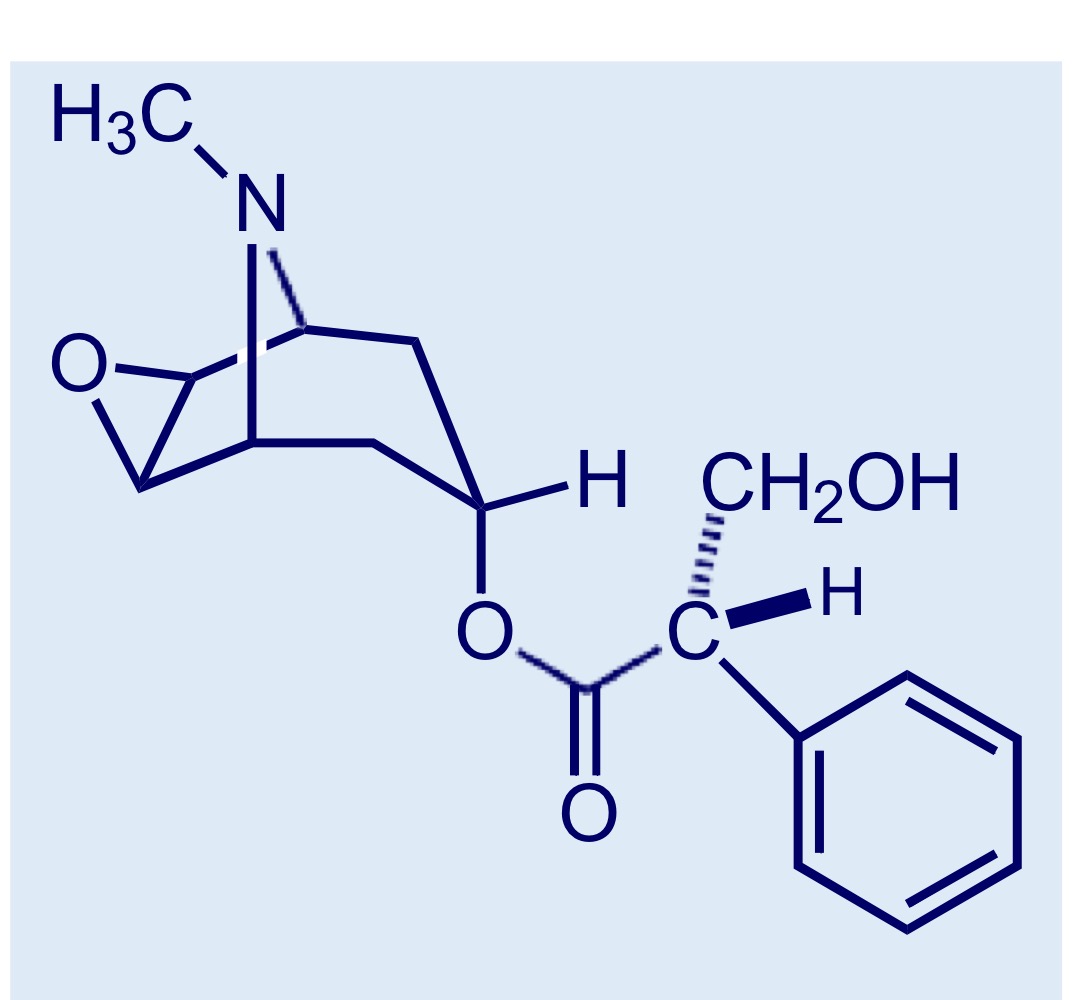
Riconosci la molecola + descrizione
Scopolamina P.69
Molecola di origine naturale costituita da acido tropico ed scopina. Presenta un centro chirale con stereochimica S (più potente) ma si somministra come racemo.
Antagonista muscarinico non selettivo e senza componenti nicotiniche.
Presenta un gruppo amminico protonabile ed ha effetti sia periferici che centrali; esistono dei derivati 4° per solo uso periferico (es. buscopan).
Viene usato come “prototipo” per la progettazione di antimuscarinici di sintesi. Usi terapeutici: midriatico e cicloplecico.
Riconosci la molecola + descrizione
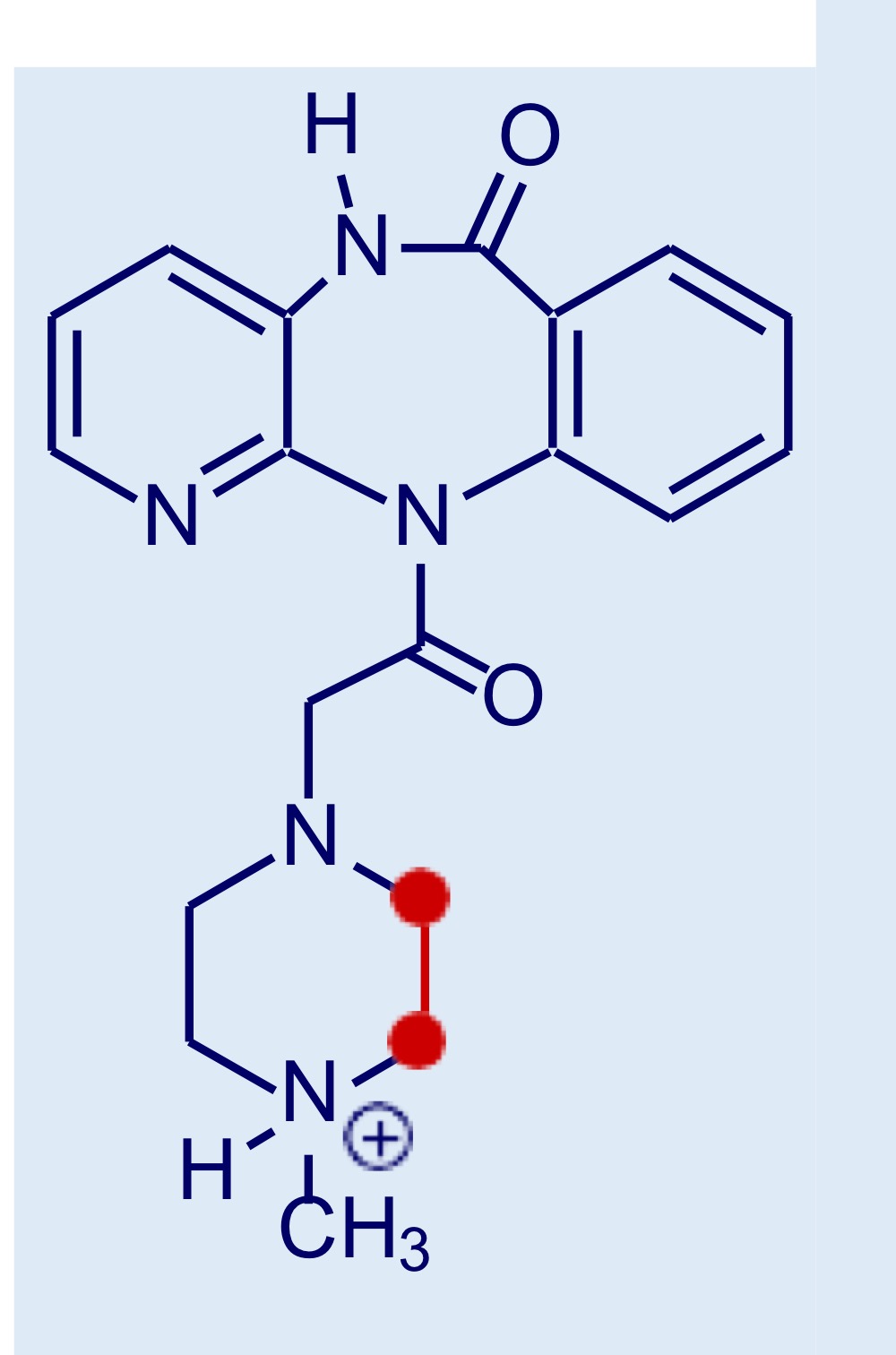
Pirenzepina P.71
Derivato dell’imipramina. Struttura:
ammide endociclica + ammide esociclica—> conferisco affinità ai recettori muscarinici e perdità attività per i recettori dell’imipramina
Piridina—> aumenta l’idrofilia della molecola
Molecola idrofila con azione periferica e selettiva per i recettori M1–>ANTIULCERA (azione inibitoria della secrezione gastrica e citoprotettiva). Per la selettività è importante la posizione del centro basico (derivato otenzepad selettivo per M2)
Possiede una conformazione a farfalla in quanto la porzione triciclica non è planare—>enantiomeri conformazionali (per convertirli è necessario superare una barriera energetica)
Riconosci la molecola + descrizione
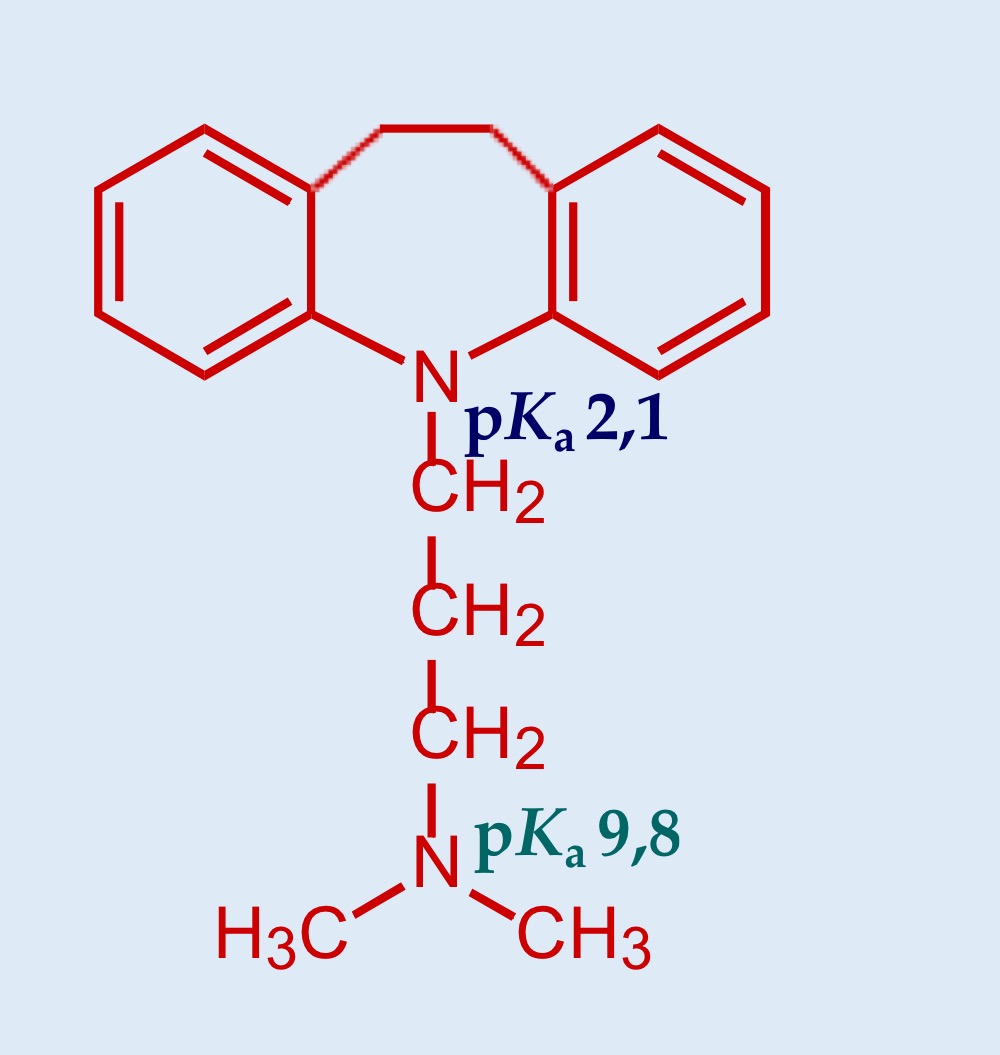
Imipramina P.71
Antidepressivo che ha anche un’attività antimuscarinica grazie ad un recettore imipraminico
Riconosci la molecola
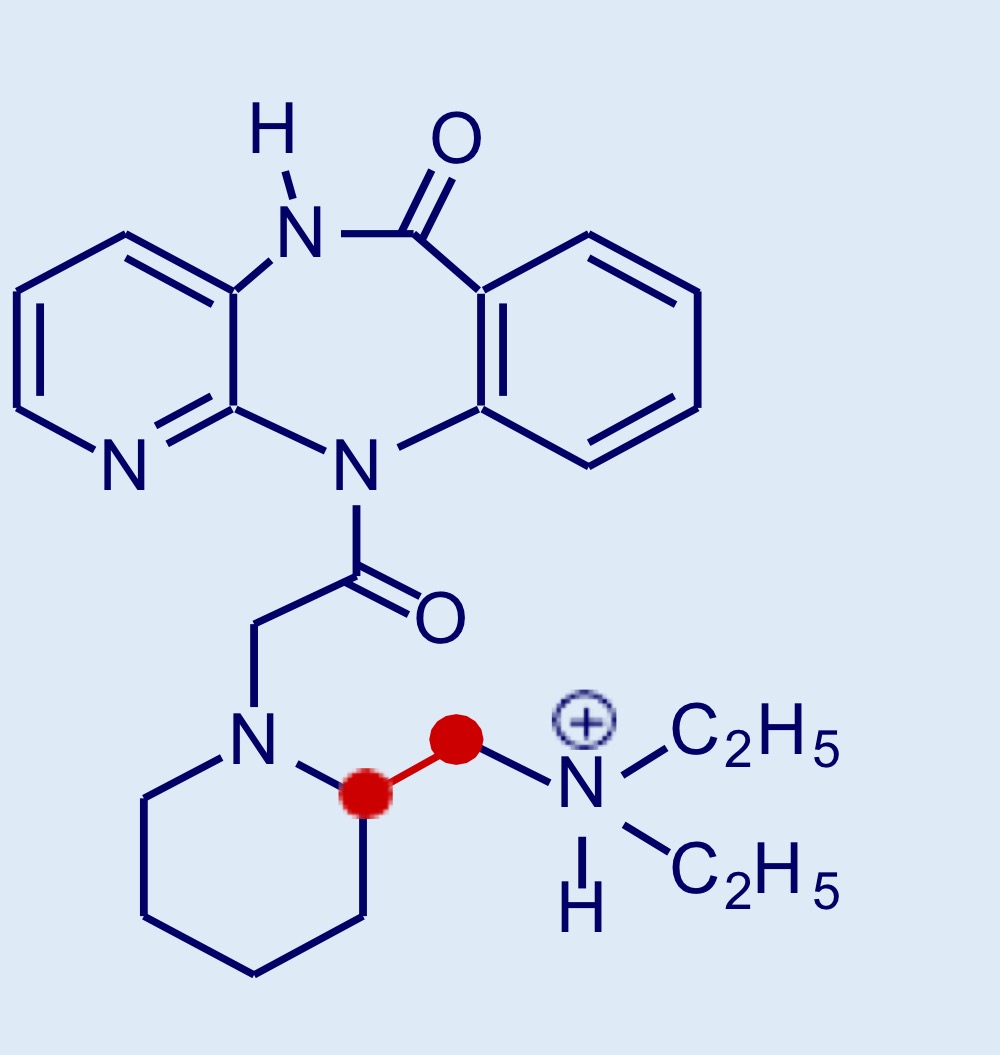
Otenzepad
Derivato della pirenzepina con attività periferica antimuscarinica selettiva M2 dovuta alla posizione del gruppo NH2 protonabile–> ANTIBRADICARDICO
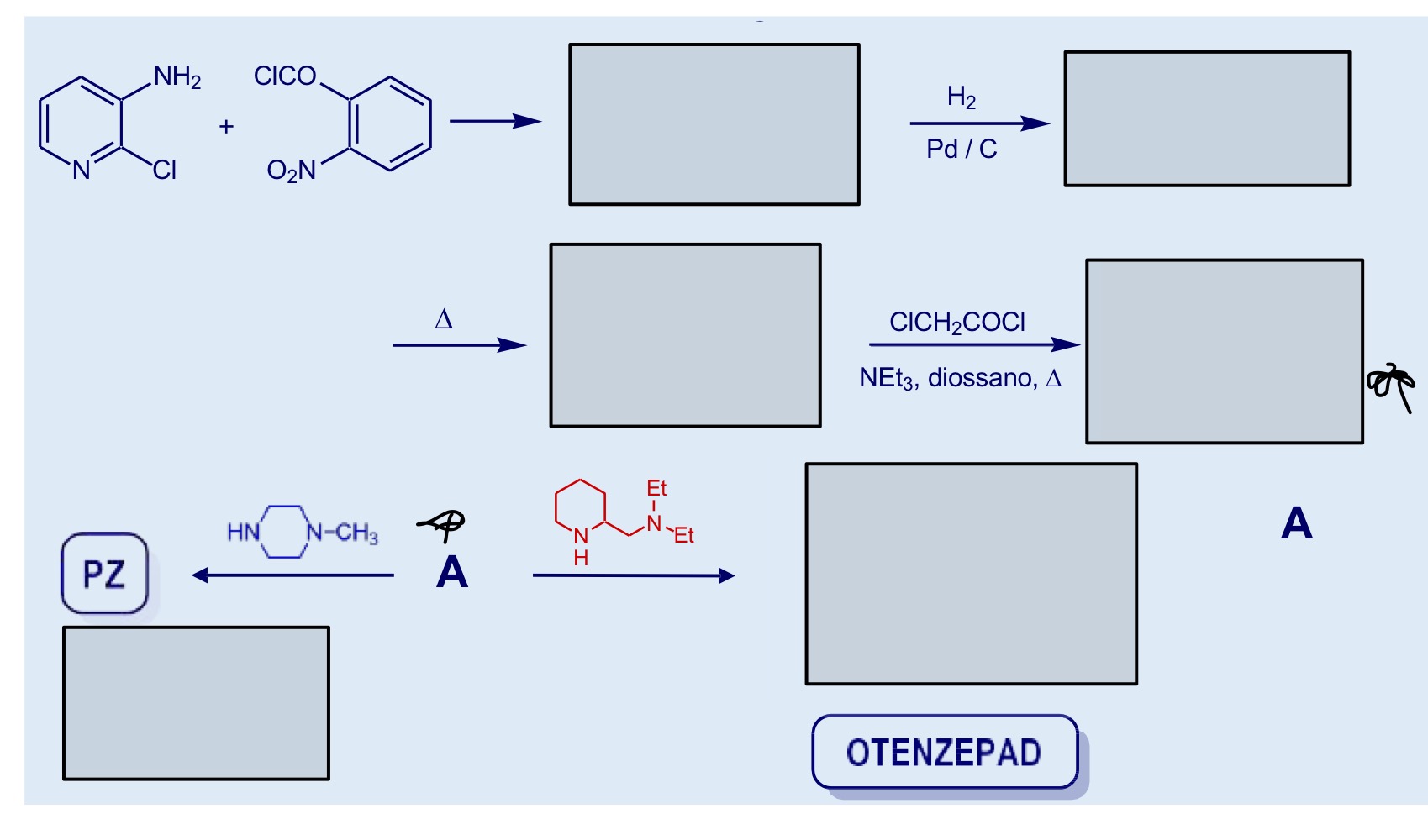
Sintesi pirenzepina
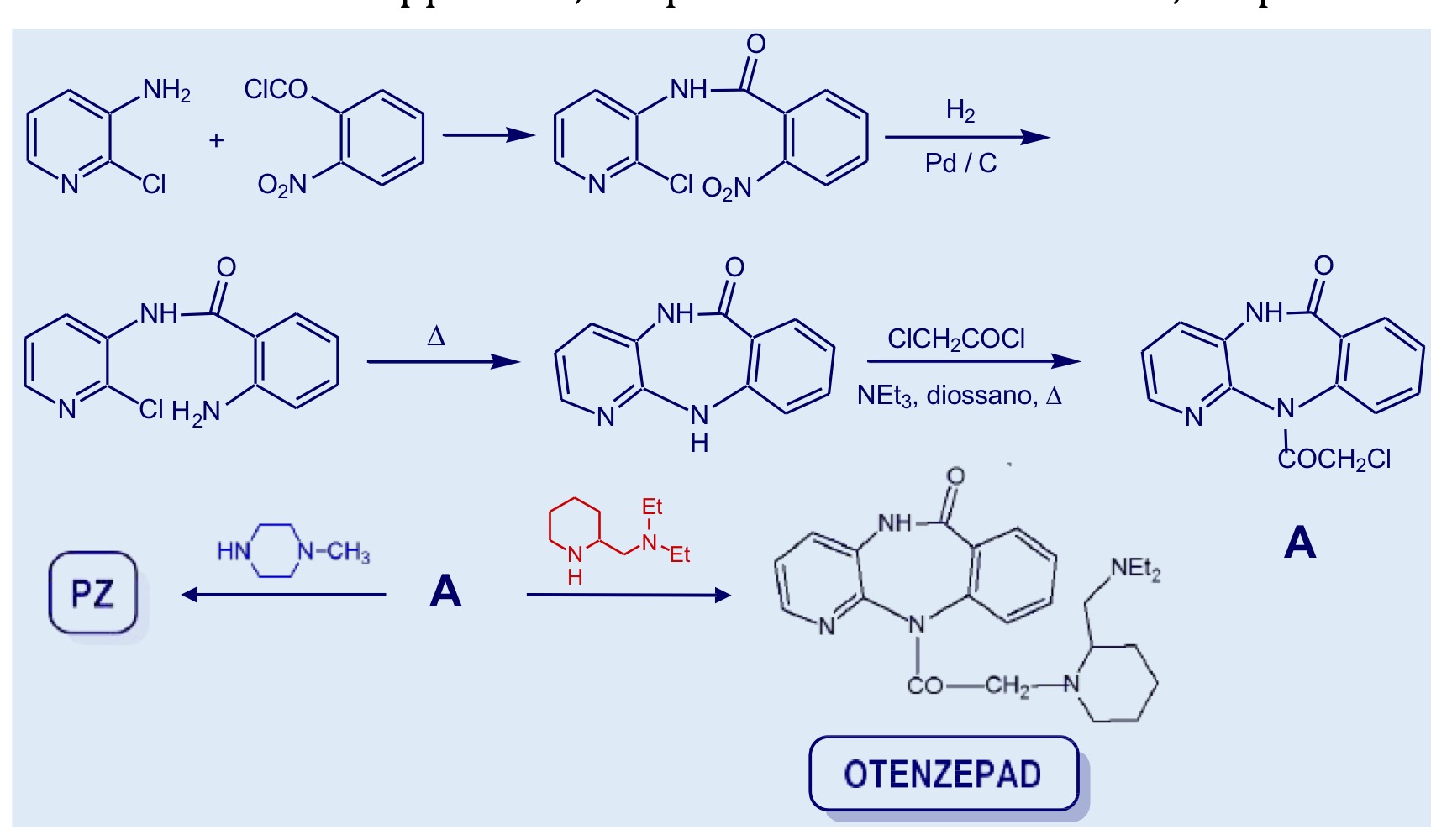
Riconosci la molecola+ descrizione
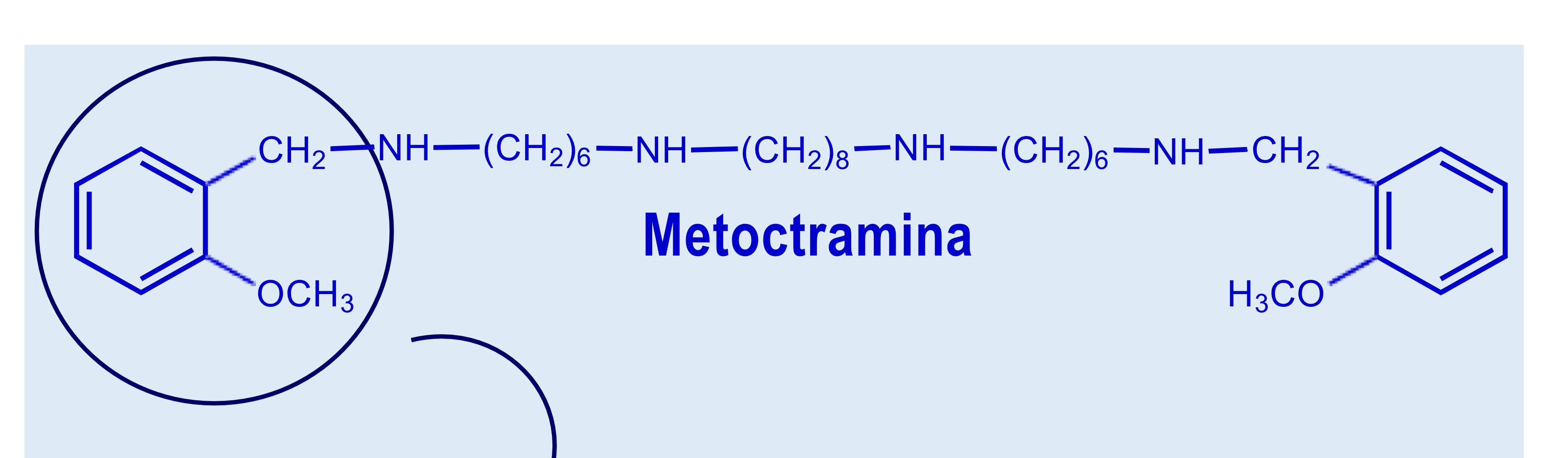
Metoctramina P.74
Molecola M2 selettiva che fa parte della classe delle polietilentetramine
Vantaggi delle molecole M2 selettive

Riconosci la molecola
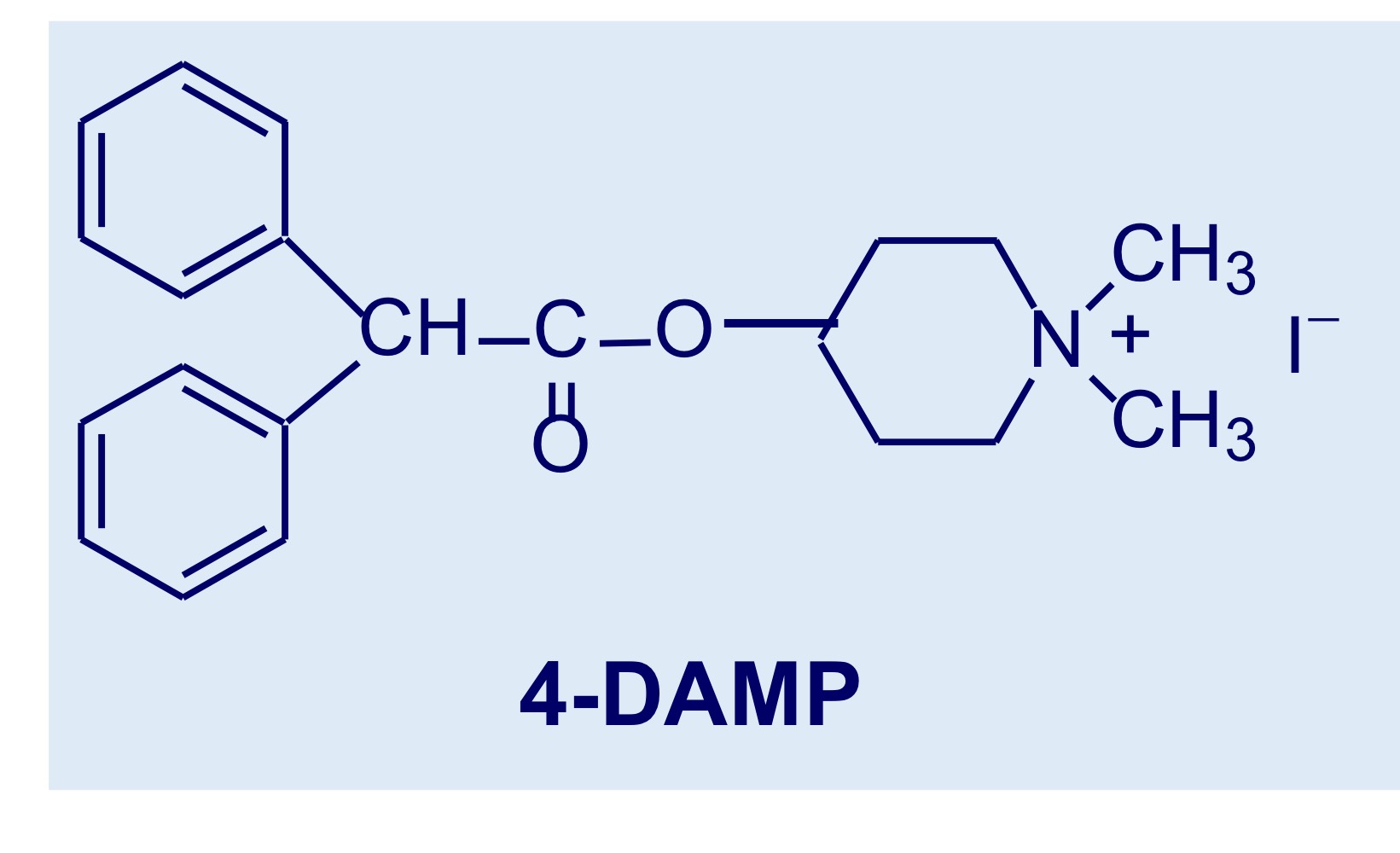
4-DAMP P.76
Sale d’ammonio quaternario su un nucleo piperidinico—> selettiva per M3
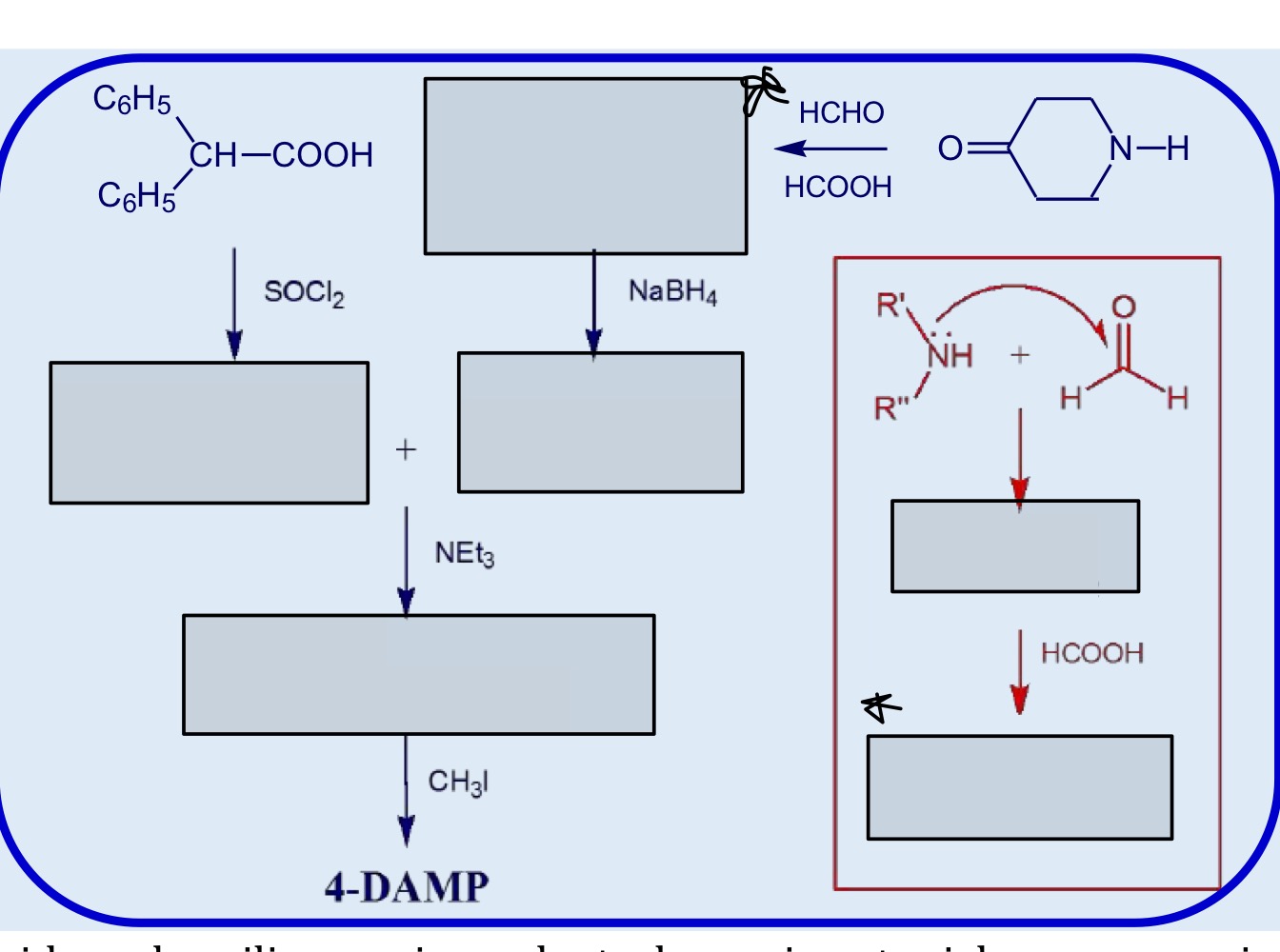
Sintesi del 4-DAMP
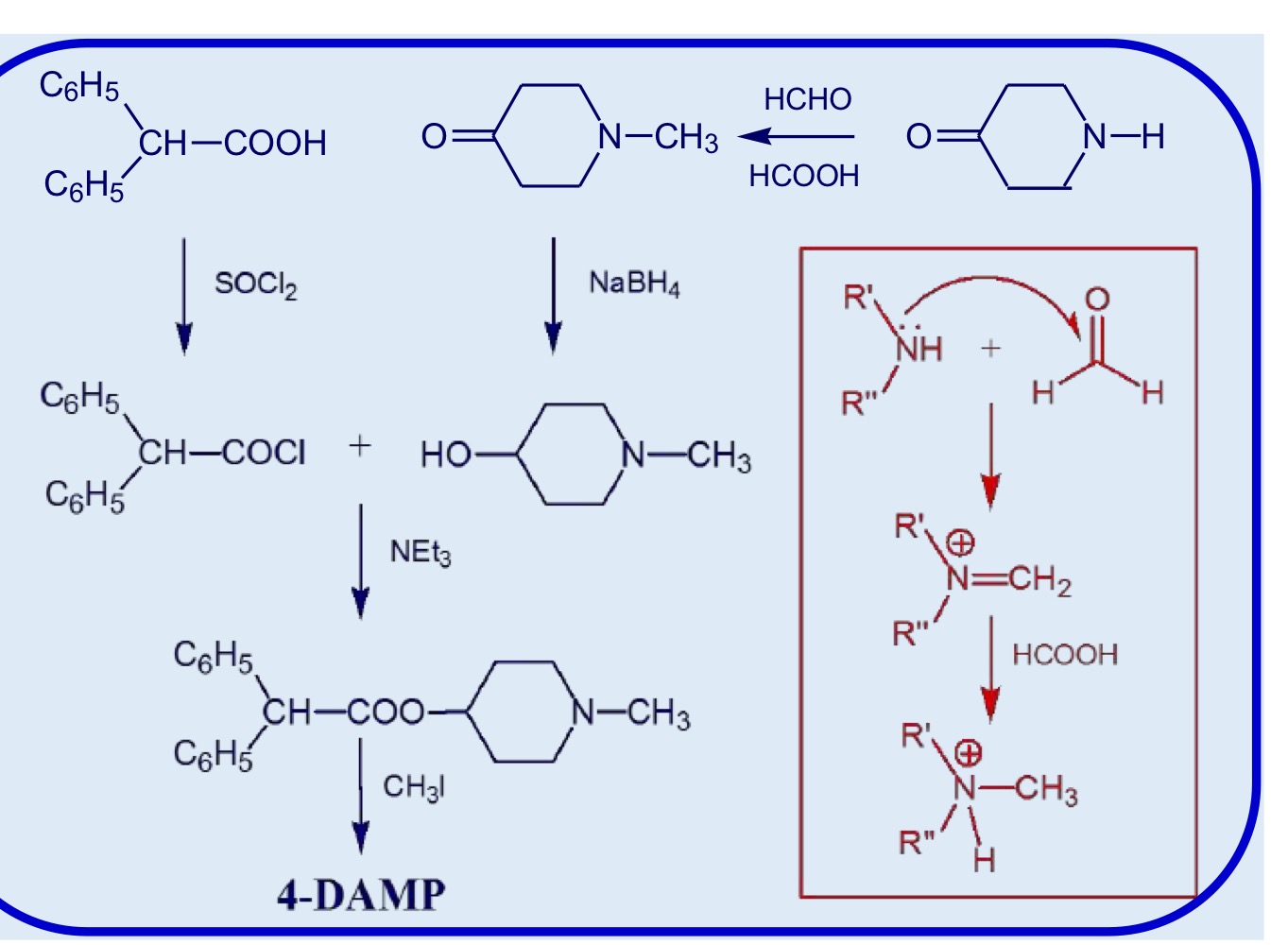
Riconosci la molecola + descrizione
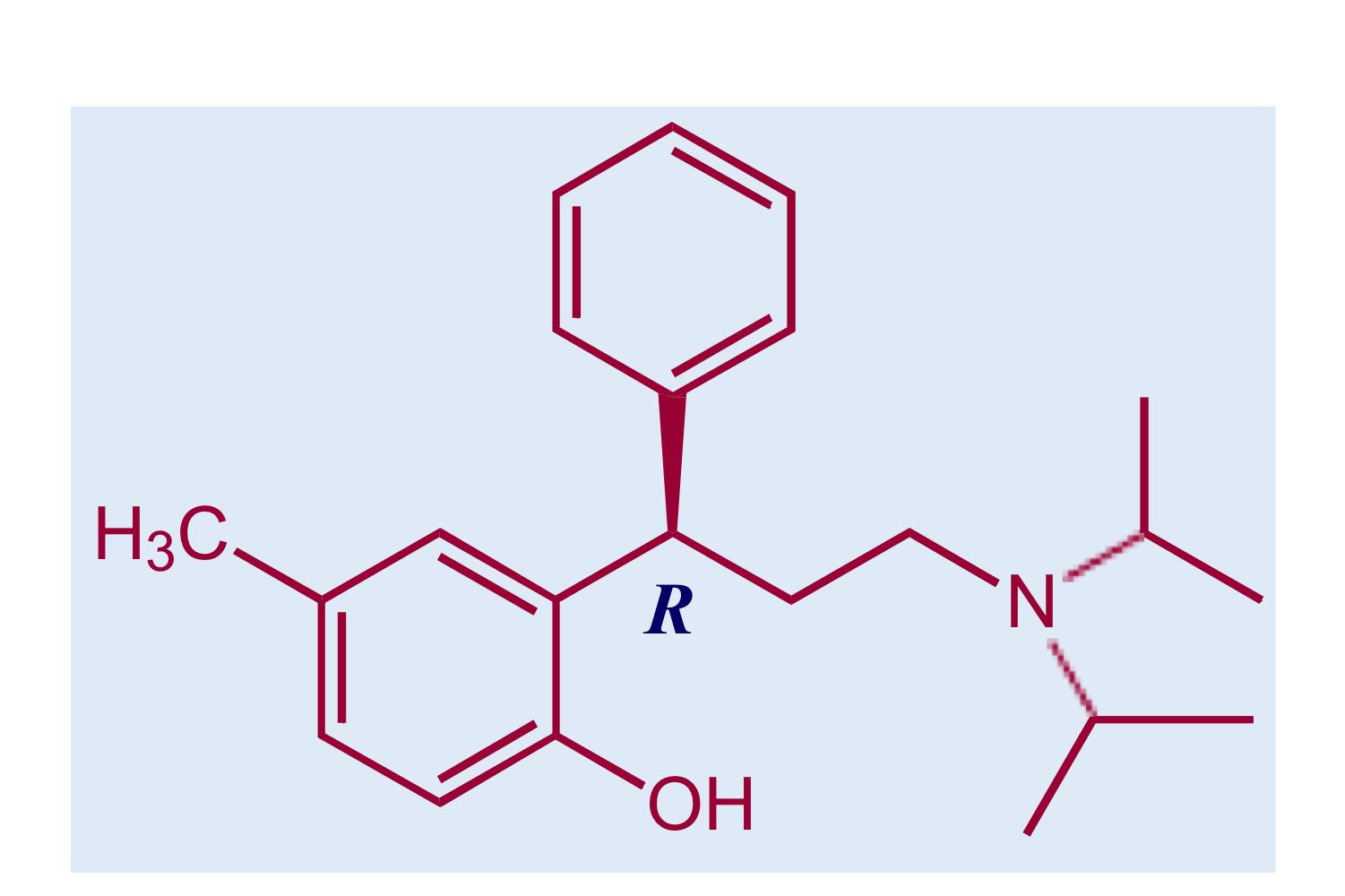
Tolterodina P.78
Molecola che è stata introdotta sul mercato come singolo enantiomero per l’incontinenza urinaria
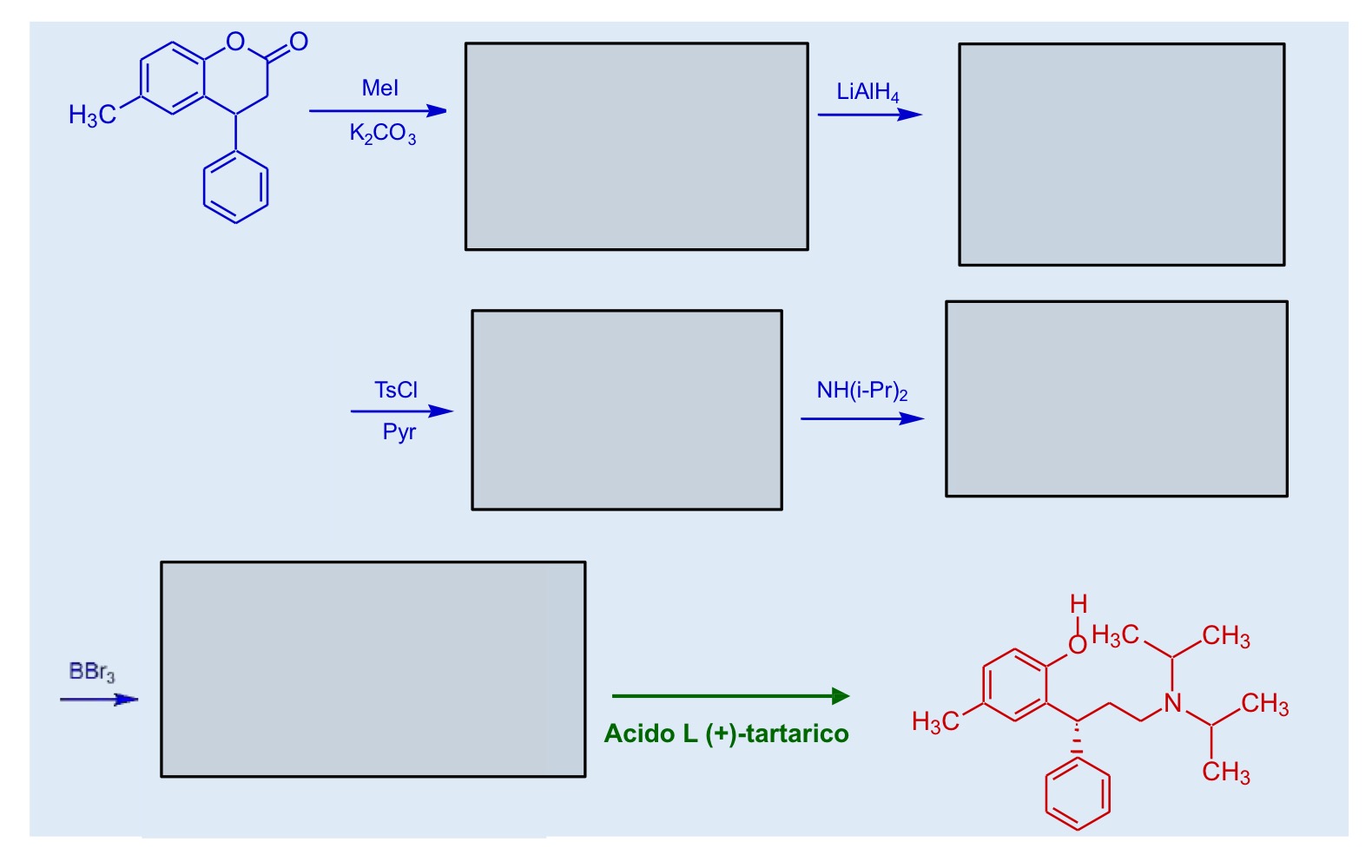
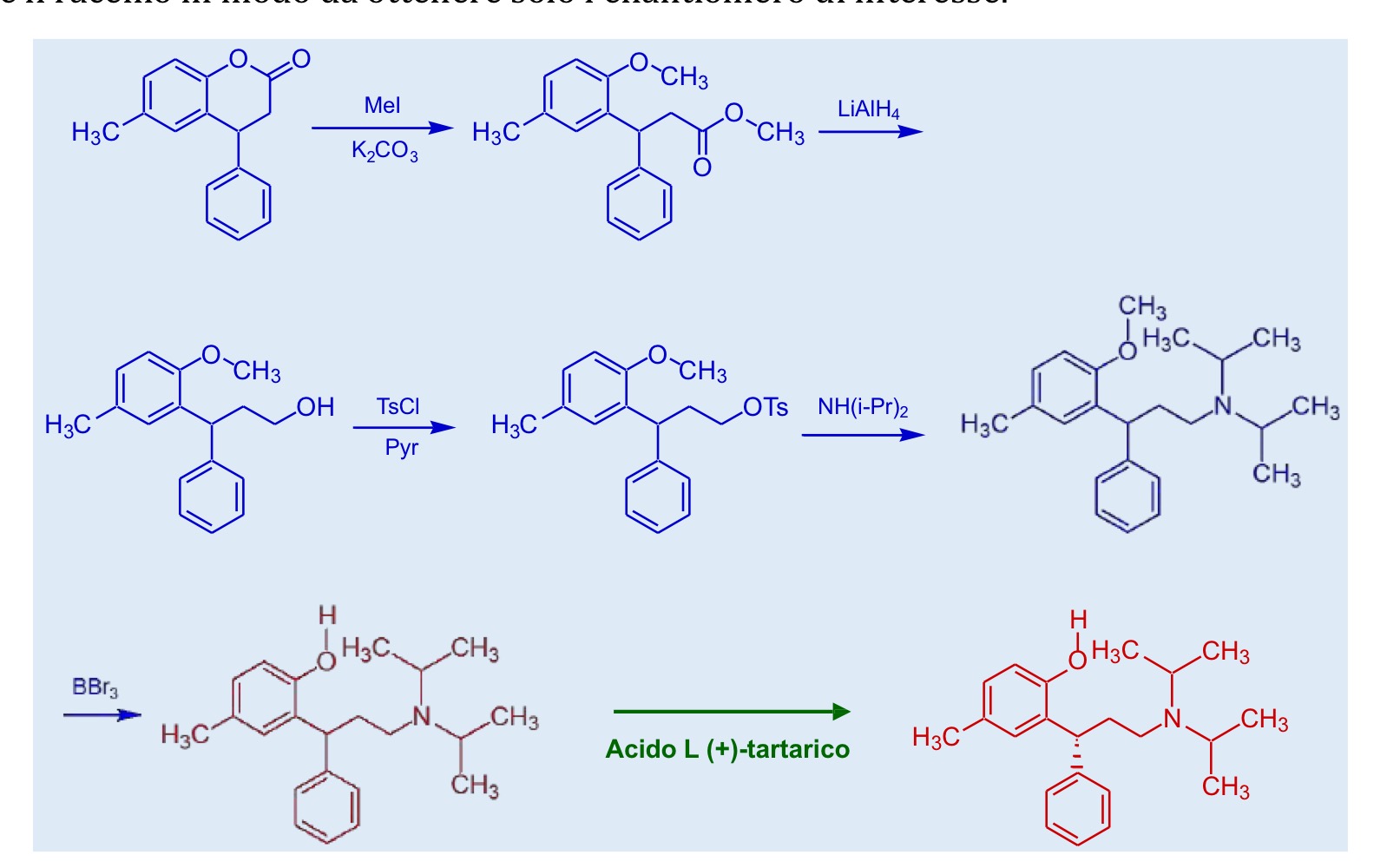
Sintesi tolterodina
Propanolammine sostituite (descrizione e struttura generale)
P.81
Gruppo di molecole usate in co-somministrazione con la Levodopa nelle fasi avanzate del parkinson
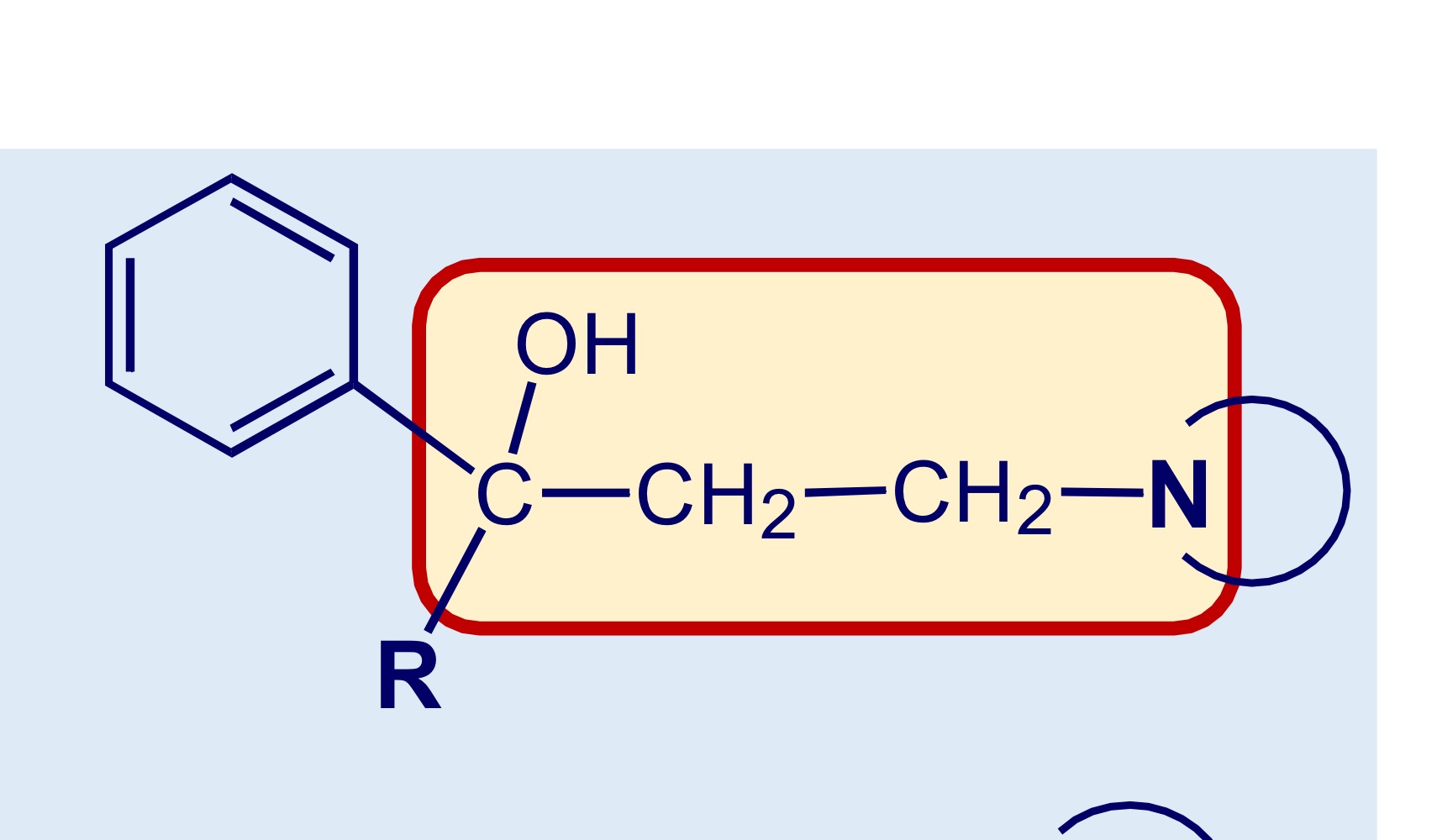
Riconosci la molecola
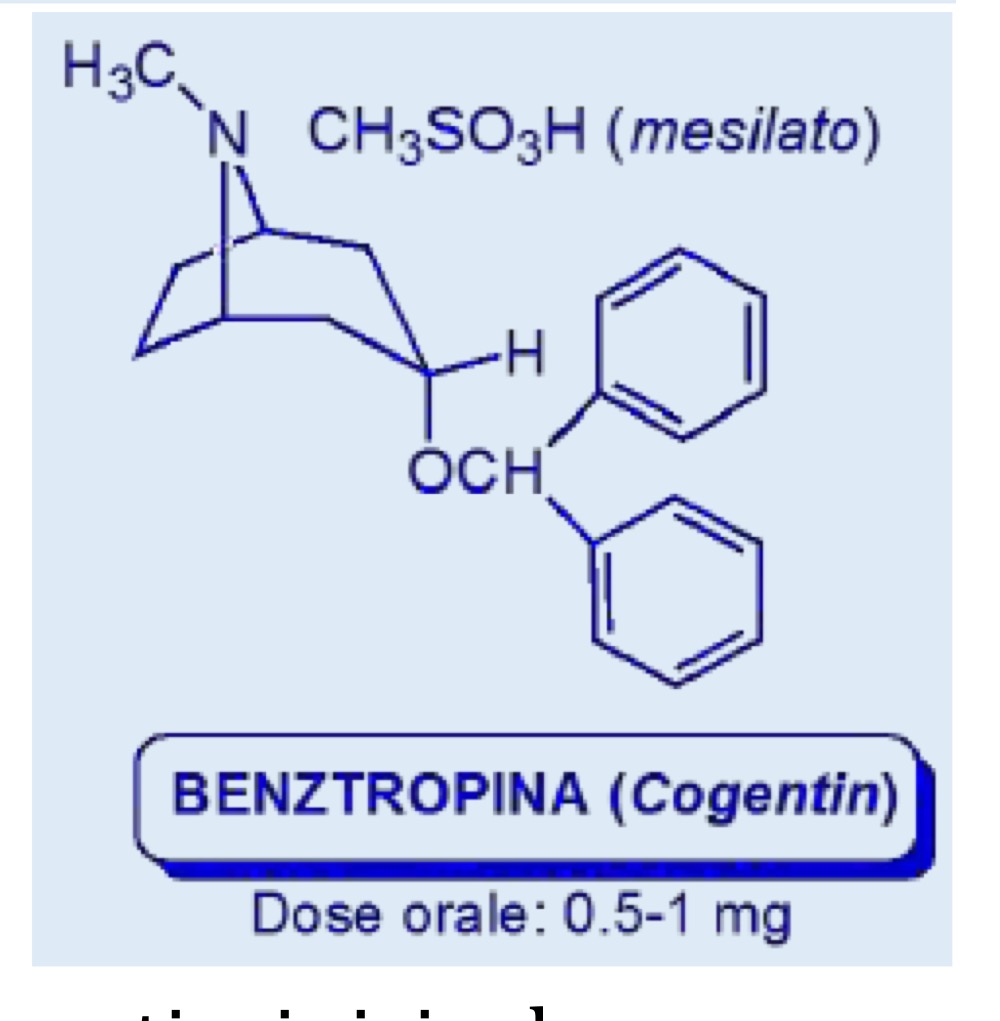
Benzatropina P.81
molecola usata in co-somministrazione con la Levodopa nelle fasi avanzate del parkinson
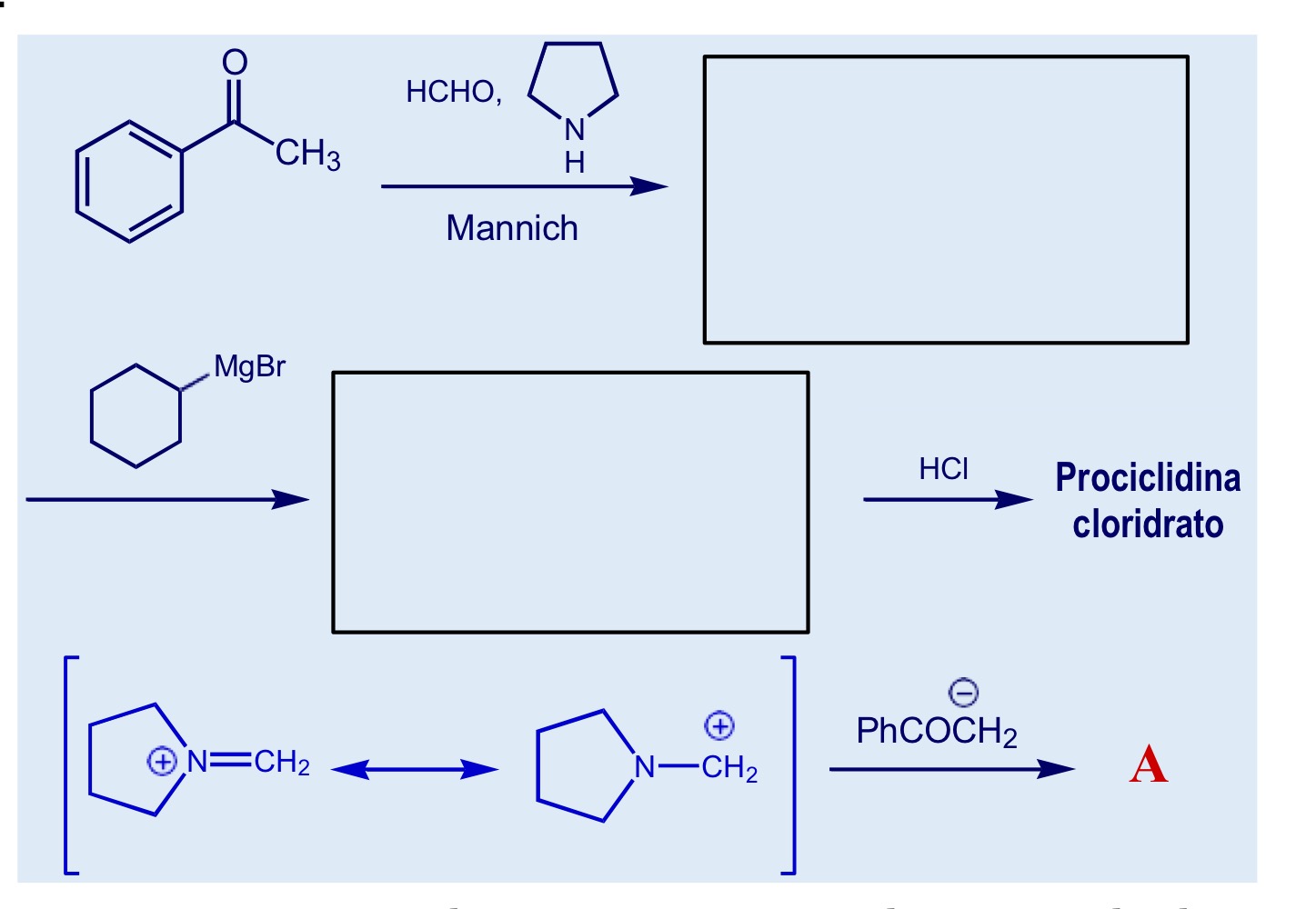
Sintesi prociclidina
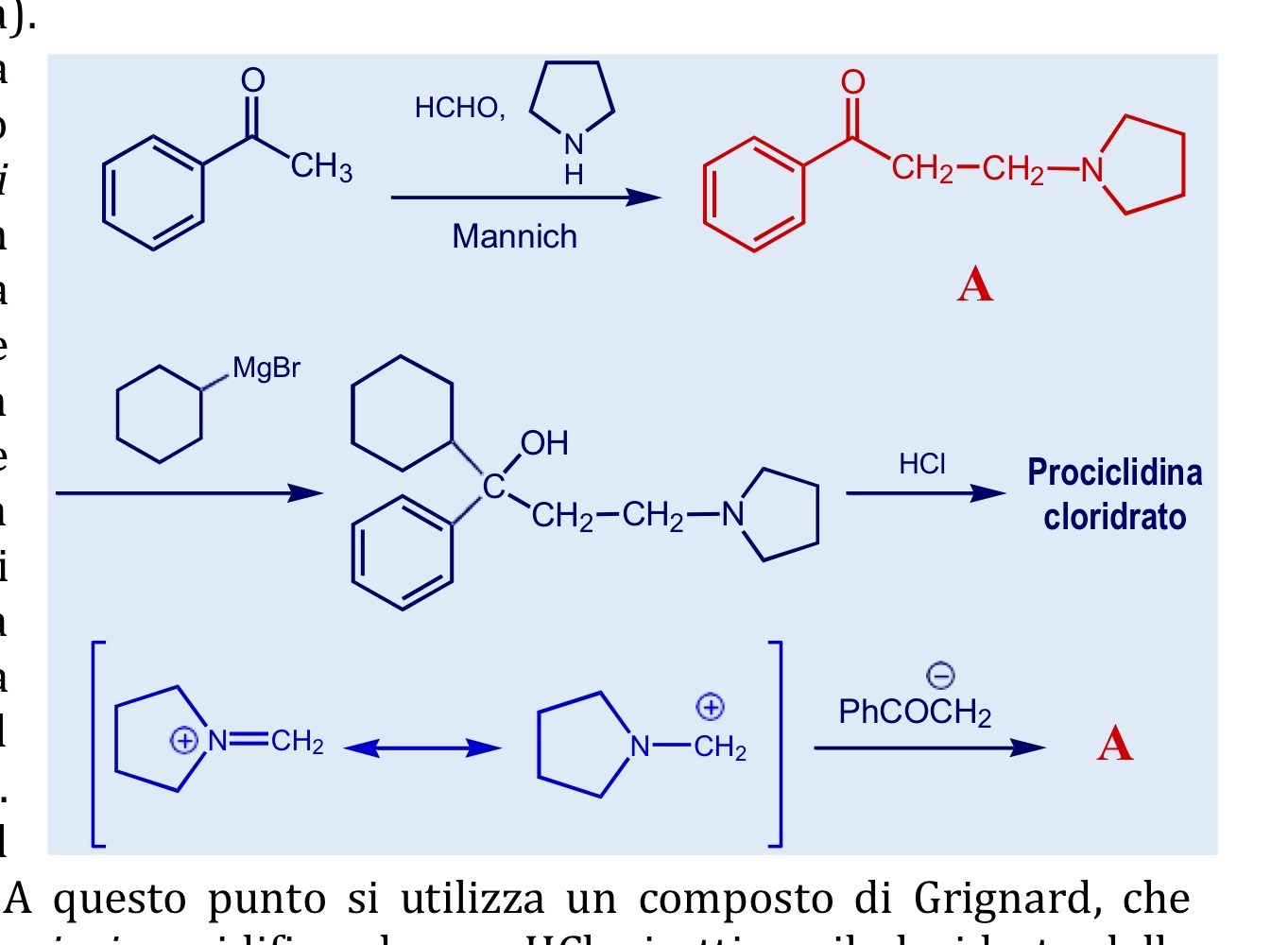
Caratteristiche delle molecole antimuscariniche contro il parkinson
