SEGUNDO EXÁMEN DEPARTAMENTAL- BIOQUÍMICA (copy)
0.0(0)
Studied by 8 peopleCard Sorting
1/167
Earn XP
Description and Tags
Last updated 1:59 AM on 2/2/23
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
168 Terms
1
New cards
¿Qué son las proteínas?
Las proteínas son polímeros lineales de aminoácidos unidos entre sí mediante enlaces peptídicos
2
New cards
¿Cuántos aminoácidos se usan para la síntesis de proteinas de todos los seres vivos?
Solo 20 aminoácidos
3
New cards
¿Cuál es la estructura general de los aminoácidos?
Todos los aminoácidos contienen grupos ionizables
\-Un carbono alfa “Ca” unido a 3 sustituyentes comunes
\+Un grupo CARBOXILO: -COOH (pKa cercano a 2)
\+Un grupo AMINO: -NH2 (pKa cercano a 9.5)
\+Un ÁTOMO DE HIDRÓGENO: H+
\+Una cadena lateral: R (determina la identidad del aminoácido)
\-Un carbono alfa “Ca” unido a 3 sustituyentes comunes
\+Un grupo CARBOXILO: -COOH (pKa cercano a 2)
\+Un grupo AMINO: -NH2 (pKa cercano a 9.5)
\+Un ÁTOMO DE HIDRÓGENO: H+
\+Una cadena lateral: R (determina la identidad del aminoácido)
4
New cards
¿Qué son los aminoácidos?
Los aminoácidos son iones dipolares o zwitteriones, ya que en una especie iónica dada coexisten cargas positivas y negativas
5
New cards
Es un valor particular de pH en el que la carga neta del aminoácido es cero:
Punto isoelectrico
6
New cards
¿Por que se dice que el Carbono alfa (Ca) de los aminoácidos es quiral?
Ya que sus 4 constituyentes pueden adoptar 2 configuraciones espaciales diferentes llamadas enantiómeros
7
New cards
Cada par de enantiómeros presenta características químicas iguales, sin embargo, ¿Qué pasa al colocarlas frente a un haz de luz polarizada?
Las dos configuraciones desvían la luz en sentidos opuestos
8
New cards
¿Mediante que enlaces los L-aminoácidos se encuentran unidos en las proteínas?
Mediante el enlace covalente del grupo carboxilo de un aminoácido con el grupo amino de otro.
En esta reacción de condensación se forma una AMIDA, que une los dos aminoácidos para formar el ENLACE PEPTÍDICO
En esta reacción de condensación se forma una AMIDA, que une los dos aminoácidos para formar el ENLACE PEPTÍDICO
9
New cards
¿En cuántas regiones se divide la cadena polipeptídica para su estudio?
Se divide en 2 regiones:
\-El esqueleto polipeptídico
\-Las cadenas laterales
\-El esqueleto polipeptídico
\-Las cadenas laterales
10
New cards
¿Por qué está formado el esqueleto polipeptídico?
Esta formado por unidades repetitivas que constan de 3 átomos:
%%-El nitrógeno de la amida:%% Antes de la condensación peptídica formaba parte del grupo amino
\
\-El carbono alfa (Ca)
\
\-El carbono del carboxilo (C’): proveniente del carboxilo en el aminoácido original
%%-El nitrógeno de la amida:%% Antes de la condensación peptídica formaba parte del grupo amino
\
\-El carbono alfa (Ca)
\
\-El carbono del carboxilo (C’): proveniente del carboxilo en el aminoácido original
11
New cards
¿Cómo puede considerarse el esqueleto polipéptidico?
Puede considerarse una secuencia de enlaces peptídicos separados por carbonos alfa
12
New cards
En el esqueleto polipeptídico ¿A qué está unido el carbono del carbonilo (C’)?
Esta unido a 2 átomos muy electronegativos:
\-El oxígeno del carbonilo
\-El nitrógeno de la amida
\-El oxígeno del carbonilo
\-El nitrógeno de la amida
13
New cards
Debido a la unión del C’ con esos 2 átomos ¿Qué se genera?
Se genera un doble enlace parcial entre el C’ y el N, este doble enlace restringe la rotación entre el carbono y el nitrógeno a las 2 conformaciones posibles CIS y TRANS
14
New cards
¿Qué son las conformaciones TRANS y CIS del enlace peptídico?
CIS: El isómero que tiene los carbonos alfa al mismo lado
\
TRANS: El isómero que tiene los carbonos alfa a lados opuestos
\
TRANS: El isómero que tiene los carbonos alfa a lados opuestos
15
New cards
¿Qué proporciona cada amida del esqueleto polipetídico?
Cada amida del esqueleto polipeptídico proporciona:
\-Un donador de puentes de hidrógeno (-NH)
\-Un receptor (-C’O)
\-Un donador de puentes de hidrógeno (-NH)
\-Un receptor (-C’O)
16
New cards
¿Cuál es la función de las cadenas laterales?
Son también llamadas residuos, y determinan la identidad y propiedades de la proteína al ser incorporadas a la cadena polipeptídica
17
New cards
La conformación que adoptan las cadenas polipeptídicas en el espacio es determinada por:
El volumen y la solubilidad de las cadenas laterales
18
New cards
Menciona los 20 aminoácidos esenciales:
1\.-Glicina
2\.-Alanina
3\.-Leucina
4\.-Isoleucina
5\.-Valina
6\.-Prolina
7\.-Fenilalanina
8\.-Tirosina
9\.-Triptófano
10\.-Serina
11\.-Treonina
12\.-Histidina
13\.-Glutamato
14\.-Aspartato
15\.-Lisina
16\.-Arginina
17\.-Asparagina
18\.-Glutamina
19\.-Cisteína
20\.-Metionina
2\.-Alanina
3\.-Leucina
4\.-Isoleucina
5\.-Valina
6\.-Prolina
7\.-Fenilalanina
8\.-Tirosina
9\.-Triptófano
10\.-Serina
11\.-Treonina
12\.-Histidina
13\.-Glutamato
14\.-Aspartato
15\.-Lisina
16\.-Arginina
17\.-Asparagina
18\.-Glutamina
19\.-Cisteína
20\.-Metionina
19
New cards
¿Cuál es el aminoácido más simple y porqué?
La glicina, ya que su cadena lateral o radical es un átomo de hidrógeno y como el Carbono alfa tiene dos sustituyentes iguales, este aminoácido no es quiral
20
New cards
De acuerdo a sus cadenas laterales o regiones radicales ¿Cómo se clasifican los aminoácidos?
\-No polares o apolares
\-Polares
\-De cadenas laterales cargadas
\-Polares
\-De cadenas laterales cargadas
21
New cards
¿Cómo se dividen los aminoácidos apolares?
\-De cadena alifática o creciente: Glicina, Alanina, Valina, Isoleucina, Leucina
\
\-Aromáticos: Fenilalanina, Triptófano
\
\-Azufrados: Metionina, Cisteina
\
\-1 IMINOÁCIDO: la prolina
\
\-Aromáticos: Fenilalanina, Triptófano
\
\-Azufrados: Metionina, Cisteina
\
\-1 IMINOÁCIDO: la prolina
22
New cards
¿Cuáles son los aminoácidos polares?
1\.- Serina
2\.- Treonina
3\.- Asparagina
4\.- Glutamina
5\.- Tirosina
2\.- Treonina
3\.- Asparagina
4\.- Glutamina
5\.- Tirosina
23
New cards
¿Cómo se dividen los aminoácidos de cadenas laterales cargadas?
Se dividen en 2 categorias:
\-ÁCIDOS: -Ácido glutámico
-Ácido aspártico
\
\-BÁSICOS: -Lisina
-Arginina
-Histidina
\-ÁCIDOS: -Ácido glutámico
-Ácido aspártico
\
\-BÁSICOS: -Lisina
-Arginina
-Histidina
24
New cards
¿De qué depende la solubilidad de las proteinas?
Depende de la concentración de sales, pH, temperatura y polaridad del solvente
25
New cards
¿Cómo afecta la solubilidad de las proteinas las concentraciones bajas de sal?
\-A concentraciones BAJAS de sal AUMENTA LA SOLUBILIDAD de las proteínas
\
\-A concentraciones ALTAS de sal DISMINUYE LA SOLUBILIDAD de las proteínas
\
\-A concentraciones ALTAS de sal DISMINUYE LA SOLUBILIDAD de las proteínas
26
New cards
¿Qué es la conformación nativa de las proteínas?
\-Es la estructura funcional y tridimensional de una proteína, que tiene las características estructurales y dinámicas que permiten a la proteína llevar a cabo una función biológica.
\
\-Se considera la estructura más estable de todas las estructuras posibles.
\
\-Se considera la estructura más estable de todas las estructuras posibles.
27
New cards
¿Generalmente a que suele asociarse el estado nativo de las proteínas?
Suele asociarse a una conformación GLOBULAR que posee una estructura rígida y ordenada
28
New cards
¿Qué es el estado nativo desordenado de las proteínas?
Es cuando las proteínas no adoptan una conformación globular ordenada, si no que se encuentran en parte o por completo desestructuradas
29
New cards
¿En dónde abundan las proteínas en estado nativo desordenado o intrínsecamente desordenadas?
Abundan en particular en eucariontes ya que se estima que en mamiferos 20 a 30% de las proteínas corresponden a esta categoría
30
New cards
¿Qué les permite el estado nativo a las proteínas?
El estado nativo ordenado o desordenado otorga a la proteina la capacidad de reconocer, unir o transformar algunas moléculas, de las miles que circulan en la célula.
31
New cards
¿De qué depende la carga neta de las proteínas?
Depende del pH del medio, ya que algunas cadenas laterales, así como los grupos amino y carboxilo terminales, presentan grupos ionizables
32
New cards
¿Qué producen el oxígeno y el nitrógeno del esqueleto polipeptídico?
El oxígeno y el nitrógeno del esqueleto polipeptídico son muy electronegativos, por lo que producen un MOMENTO DIPOLAR en el enlace peptídico, en el cual:
\
\-El grupo AMINO presenta carga parcial POSITIVA y es donador potencial de puentes de hidrógeno
\
\-El oxígeno del grupo CARBONILO presenta carga parcial NEGATIVA y es aceptor potencial de puentes de hidrógeno
\
\-El grupo AMINO presenta carga parcial POSITIVA y es donador potencial de puentes de hidrógeno
\
\-El oxígeno del grupo CARBONILO presenta carga parcial NEGATIVA y es aceptor potencial de puentes de hidrógeno
33
New cards
Mediante que técnicas se puede determinar la estructura tridimensional de las proteinas:
\-Mediante la difracción de rayos X por cristales de proteína
\-Mediante Resonancia Magnética Nuclear
\-Mediante criomicroscopia electrónica
\-
\-Mediante Resonancia Magnética Nuclear
\-Mediante criomicroscopia electrónica
\-
34
New cards
¿Cuántos niveles de organización se distinguen al analizar la información contenida en la estructura de las proteinas?
Se distinguen 4 niveles de organización:
\-Estructura primaria
\-Estructura secundaria
\-Estructura terciaria
\-Estructura cuaternaria
\-Estructura primaria
\-Estructura secundaria
\-Estructura terciaria
\-Estructura cuaternaria
35
New cards
¿Por qué esta determinada la estructura PRIMARIA o COVALENTE de la molécula?
Esta determinada por:
\-la secuencia de aminoácidos de la cadena polipeptídica
\-la posición de los puentes disulfuro
\-la secuencia de aminoácidos de la cadena polipeptídica
\-la posición de los puentes disulfuro
36
New cards
En la estructura primaria ¿Cómo puede obtenerse la secuencia de aminoácidos de la proteína?
Puede obtenerse a partir de la secuencia de nucleótidos del gen que la codifica
37
New cards
¿Qué es la estructura secundaria?
Especifica la conformación local de segmentos de la proteína, en los que la cadena adopta conformaciones regulares repetitivas, como:
\-Las hélices a
\-Las hojas o láminas B
\
o no repeitivas como vueltas y giros de conformación definida llamados
\-Asas o loops
\-Las hélices a
\-Las hojas o láminas B
\
o no repeitivas como vueltas y giros de conformación definida llamados
\-Asas o loops
38
New cards
¿Por qué está definida la conformación local o estructura secundaria?
Esta definida por el patrón de puentes de hidrógeno de la estructura polipeptídica y el valor de los angulos O y Y
39
New cards
A partir de consideraciones geométricas, ¿Quiénes predijeron dos conformaciones regulares repetitivas, la hélice a y la lámina B?
Pauling y Corey
40
New cards
¿Cuándo se presentan las hélices a?
Se presentan cuando un grupo de aminoácidos, contiguos en la secuencia, adopta ángulos de torsión que corresponden al cuadrante inferior izquierdo en el mapa de Ramachandran, estos residuos generan una estructura helicoidal repetitiva, en la que se forma un PUENTE DE HIDRÓGENO entre el H unido al N del aminoácido n y el oxígeno del carbonilo distante 4 aminoácidos hacia el extremo amino
41
New cards
¿Por qué están formadas las hojas o láminas B?
Están formadas por 2 o más hebras:
\-B paralelas (O=-119°, Y=113°)
\-B antiparalelas (O=-139°, Y=\*135°)
\-B paralelas (O=-119°, Y=113°)
\-B antiparalelas (O=-139°, Y=\*135°)
42
New cards
¿Qué son las asas o loops?
Son ciertas conformaciones locales no repetitivas donde la cadena cambia de manera abrupta de dirección y se encuentran con frecuencia en las superficies de las moléculas conectando láminas B y hélices a
43
New cards
¿Qué es la estructura terciaria?
Determina el arreglo espacial de la estructura secundaria en dominios compactos, la estructura terciaria contiene la posición relativa de todos los átomos de la molécula en proteínas monoméricas
44
New cards
¿Qué fuerzas estabilizan la estructura terciaria de la proteina?
\-Puentes disulfuro
\-Atracción electrostática
\-Puentes de hidrógeno
\-Interacciones hidrófobas
\-Atracción electrostática
\-Puentes de hidrógeno
\-Interacciones hidrófobas
45
New cards
¿Qué es la estructura cuaternaria?
Especifica la estequiometría y la orientación espacial relativa de las diferentes cadenas, en proteinas formadas por varias cadenas polipeptídicas
46
New cards
¿Por qué esta dada la estructura cuaternaria?
\-La estructura cuaternaria esta dada por el número y la orientación relativa de las subunidades que posee la proteína, ya se dímerica, trimérica, tetramérica, etc.
47
New cards
¿Qué es la desnaturalización?
Es el despliegue o la ruptura de una ***proteína***, modificando su estructura tridimensional estándar, es decir su estructura nativa, conservandose solo la estructura primaria, y perdiendo así su función.
48
New cards
¿Qué factores pueden desnaturalizar una proteína?
\-Calor excesivo
\-Sustancias que modifican el pH
\-Alteraciones en la concentración
\-Alta salinidad
\-Agitación molecular
\-Sustancias que modifican el pH
\-Alteraciones en la concentración
\-Alta salinidad
\-Agitación molecular
49
New cards
¿Cuáles son las funciones de las proteinas a nivel molecular?
A nivel molecular las proteinas llevan a cabo labores biológicas como:
\-la catálisis
\-El soporte
\-El transporte
\-La señalización
\-la catálisis
\-El soporte
\-El transporte
\-La señalización
50
New cards
¿Qué se requiere para que las proteínas lleven a cabo su función?
Se requiere que las proteínas tengan una estructura tridimensional precisa
51
New cards
¿Qué es el plegamiento de las proteinas?
Es el proceso en el cual la cadena de aminoácidos sintetizada en el ribosoma, al salir de este, debe adquirir su conformación funcional o nativa
52
New cards
¿Cómo se clasifican las proteínas con base a su estructura?
Se claisifican en:
\
\-FIBROSAS: -Tienen funciones de soporte
-Están formadas por la repetición de elementos de estructura secundaria (hélices a y láminas B en formas de fibras)
\
\-GLOBULARES: Están formadas por elementos de estructura secundaria que adoptan una conformación compacta
\
\-FIBROSAS: -Tienen funciones de soporte
-Están formadas por la repetición de elementos de estructura secundaria (hélices a y láminas B en formas de fibras)
\
\-GLOBULARES: Están formadas por elementos de estructura secundaria que adoptan una conformación compacta
53
New cards
¿De qué otra manera se pueden clasificar las proteinas?
\-HOLOPROTEINAS: Todo es proteína, y además son fibrosas
\
\-HETEROPROTEINAS: Hay una parte de proteína + algo diferente (carbohidratos, grupo prostético, grupo fosfato, grupo peptil, etc.) y además son globulares
\
\-HETEROPROTEINAS: Hay una parte de proteína + algo diferente (carbohidratos, grupo prostético, grupo fosfato, grupo peptil, etc.) y además son globulares
54
New cards
Características de las proteínas fibrosas u holoproteínas:
\-Distribución unidimensional
\-Poseen estructura 1aria, 2aria, 3aria, 4naria
\-Función estructural (forman bases de sosten)
\-Son insolubles en agua
\-Poseen estructura 1aria, 2aria, 3aria, 4naria
\-Función estructural (forman bases de sosten)
\-Son insolubles en agua
55
New cards
Ejemplos de proteínas fibrosas u holoproteínas:
\-Fibrina
\-Elastina
\-Miosina
\-Colágeno
\-Queratina
\-Elastina
\-Miosina
\-Colágeno
\-Queratina
56
New cards
Características de las proteínas globulares o heteroproteínas:
\-Función variada y compleja
\-Estructura 3aria o 4naria
\-Solubles en agua
\-Estructura 3aria o 4naria
\-Solubles en agua
57
New cards
Ejemplos de proteínas globulares o heteroproteínas:
\-ACTINA: ensamblaje, contracción muscular
\-ALBUMINA: transporte, almacén de aminoácidos
\-GLOBULINAS: anticuerpos, transporte de oxígeno
\-HISTONAS y PROTAMINAS: unión al ADN, compactación
\-ALBUMINA: transporte, almacén de aminoácidos
\-GLOBULINAS: anticuerpos, transporte de oxígeno
\-HISTONAS y PROTAMINAS: unión al ADN, compactación
58
New cards
¿Cómo se clasifican las proteínas según su función?
@@-ESTRUCTURALES:@@ +a-queratina
+Colágeno
\
%%-DE TRANSPORTE:%% +Hemoglobina
+Mioglobina
\
-CATALÍTICAS: +Enzimas
\
==-DE RECONOCIMIENTO:== +Inmunoglobulinas
\
^^-MOTORAS:^^ +Actina
+Miosina
\
@@-DE SEÑALIZACIÓN:@@ +Hormonas como la insulina, FSH, etc.
+Colágeno
\
%%-DE TRANSPORTE:%% +Hemoglobina
+Mioglobina
\
-CATALÍTICAS: +Enzimas
\
==-DE RECONOCIMIENTO:== +Inmunoglobulinas
\
^^-MOTORAS:^^ +Actina
+Miosina
\
@@-DE SEÑALIZACIÓN:@@ +Hormonas como la insulina, FSH, etc.
59
New cards
Características de la ALBUMINA:
\-Representa el 10% de la presión osmótica plasmática
\-Representa el 80% de la presión coloidosmótica en el plasma
\-Representa el 50% de contenido de proteínas en el plasma
\-Algunos la llaman la esponja molecular porque puede absorber y adsorber
\-Representa el 80% de la presión coloidosmótica en el plasma
\-Representa el 50% de contenido de proteínas en el plasma
\-Algunos la llaman la esponja molecular porque puede absorber y adsorber
60
New cards
¿Cuál es la función de la albumina?
\-Es TRANSPORTADORA de sustancias y elementos, tales como, pigmentos, ácidos grasos, metales, iones, hormonas, etc.
\-Evita que el líquido del torrente sanguíneo se filtre a otros tejidos.
\-Es amortiguadora ácido-base extracelular
\-Evita que el líquido del torrente sanguíneo se filtre a otros tejidos.
\-Es amortiguadora ácido-base extracelular
61
New cards
¿Qué cantidad de albumina
tenemos y producimos los seres humanos ?
tenemos y producimos los seres humanos ?
\-Concentración fisiológica: 3.5-4.5 g/dl
\-Síntesis hepática: 15 gr/día
\-Vida media:21 días
\-Síntesis hepática: 15 gr/día
\-Vida media:21 días
62
New cards
Características de la HEMOGLOBINA:
\-Es una proteína tetramérica con 4 subunidades: 2 alfa y 2 beta
\-Es una HETEROPROTEINA por lo tanto es una proteina globular
\-Es la proteina responsable de la captación de O2 en los pulmones y de su transporte hacia el resto del organismo
\-Transporta CO2 desde los tejidos hasta los pulmones
\-Representa el 35% del peso del eritrocito
\-Amortiguadora ácido- base intracelular
\-Es una HETEROPROTEINA por lo tanto es una proteina globular
\-Es la proteina responsable de la captación de O2 en los pulmones y de su transporte hacia el resto del organismo
\-Transporta CO2 desde los tejidos hasta los pulmones
\-Representa el 35% del peso del eritrocito
\-Amortiguadora ácido- base intracelular
63
New cards
¿Qué cantidad de hemoglobina hay en nuestro organismo?
Concentración fisiológica: 12-16 g/dl
Por eritrocito: cerca de 600 millones de Hb
Por eritrocito: cerca de 600 millones de Hb
64
New cards
Características del colágeno:
\-Es la proteína más abundante en los vertebrados y representa el 25% de las proteínas totales del cuerpo
\-Es una proteína fibrosa, extracelular, insoluble en agua y resistente a todo tipo de tensiones
\-Es una proteína de sostén y unión de los tejidos conectivos
\-Forma tendones, cartílagos y es además el componente orgánico de la matriz de los hueso
\-Tiene 3 cadenas alfa (1 alfa, 2 alfa, 3 alfa)
\-Promotor de procesos de cicatrización( a través de prolina)
\-Síntesis en fibroblastos
\-Vida media 200 días
\-Es una proteína fibrosa, extracelular, insoluble en agua y resistente a todo tipo de tensiones
\-Es una proteína de sostén y unión de los tejidos conectivos
\-Forma tendones, cartílagos y es además el componente orgánico de la matriz de los hueso
\-Tiene 3 cadenas alfa (1 alfa, 2 alfa, 3 alfa)
\-Promotor de procesos de cicatrización( a través de prolina)
\-Síntesis en fibroblastos
\-Vida media 200 días
65
New cards
¿Para qué sirve el efecto higroscópico tisular del colágeno?
Es lo que le da al colágeno la turgencia, elasticidad y resistencia en los tejidos
66
New cards
¿Qué indica la presencia de prolina?
Indica que debe haber reemplazo de células de colágeno
67
New cards
Características de la miosina:
\-Es la proteína más abundante del músculo esquelético 60-70%
\-Transforma la energía química contenida en el ATP en movimiento (es decir que es una ATPasa)
\-Es una complejo olimérico formada por 2 cadenas PESADAS y 4 cadenas LIGERAS
\-Actúa en la contracción de las fibras musuculares
\-Se biosintetiza en el MIOCITO
\-Su vida media es de 180 días
\-Transforma la energía química contenida en el ATP en movimiento (es decir que es una ATPasa)
\-Es una complejo olimérico formada por 2 cadenas PESADAS y 4 cadenas LIGERAS
\-Actúa en la contracción de las fibras musuculares
\-Se biosintetiza en el MIOCITO
\-Su vida media es de 180 días
68
New cards
¿Cuántas moléculas de miosina se asocian mediante sus colas para formar un filamento?
\-Se asocian cerca de 300 moléculas de miosina
69
New cards
Características de las porinas:
\-Están presentes en todas las membranas celulares animales principalmente en células excitables
\-Se dividen en nerviosas y musculares
\-Su función es meter y sacar de la célula
\-Se dividen en nerviosas y musculares
\-Su función es meter y sacar de la célula
70
New cards
¿Cuál es la función de la porina ATPasa Na+ K+?
Su función es sacar 3Na y METER 2K+
71
New cards
¿Cuál es la importancia de estudiar las proteínas plasmáticas en medicina?
Es muy importante estudiarlas ya que las proteínas plasmáticas ayudan a determinar la distribución de líquido entre sangre y tejidos. La concentración agregada de las proteínas presentes en el plasma típicamente cae dentro del rango de 7.0 a 7.5 g/dL para humanos.
\
Por lo tanto un deficit o aumento de proteínas plamáticas podria causar enfermedades.
\
Por lo tanto un deficit o aumento de proteínas plamáticas podria causar enfermedades.
72
New cards
¿Qué pasa con las proteínas ante reacciones febriles?
Si la temperatura sigue aumentando, las proteínas pierden su estructura y pueden producir daños irreversibles, ocasionando una DESNATURALIZACIÓN irreversible y perdiendo la función de las proteínas, es por eso, que es muy importante no dejar que el paciente alcance elevadas temperaturas
73
New cards
¿Qué mide el exámen de proteínas totales en sangre?
Mide la cantidad total de albúmina y globulina en sangre:
* La albúmina ayuda a impedir que se escape líquido de los vasos sanguíneos. También transporta químicos a través de su sangre.
* Las globulinas son una parte importante del sistema inmunitario.
* La albúmina ayuda a impedir que se escape líquido de los vasos sanguíneos. También transporta químicos a través de su sangre.
* Las globulinas son una parte importante del sistema inmunitario.
74
New cards
¿Qué significa tener niveles de proteínas altos o bajos en sangre?
Significa que probablemente la persona padece una enfermedad como:
\
BAJOS: Enfermedades de hígado, riñón, desnutrición
\
ALTOS: Hepatitis viral, VIH, mieloma multiple (un tipo de cáncer en la sangre)
\
BAJOS: Enfermedades de hígado, riñón, desnutrición
\
ALTOS: Hepatitis viral, VIH, mieloma multiple (un tipo de cáncer en la sangre)
75
New cards
¿Cuál es la importancia de tener lipoproteínas plasmáticas?
La función de las lipoproteínas plasmáticas es transportar moléculas lipídicas de unos órganos a otros en el medio acuoso del plasma, principalmente colesterol
76
New cards
¿Cuántos tipos de lipoproteínas existen?
Existen 2 tipos:
\-lipoproteínas de alta densidad o colesterol "bueno"
\
\-lipoproteínas de baja densidad o colesterol "malo"
\-lipoproteínas de alta densidad o colesterol "bueno"
\
\-lipoproteínas de baja densidad o colesterol "malo"
77
New cards
¿Qué pasa si tenemos un aumento de lipoproteínas de baja densidad o colesterol malo en el plasma?
El colesterol puede acumularse en las arterias y formar bloqueos llamados placas, además puede provocar otro tipo de enfermedades como ataque cardiaco, enfermedades cerebrovasculares, etc.
78
New cards
¿Qué es la termodinámica?
Es la parte de la física que estudia los cambios de energía en la naturaleza
79
New cards
Para la termodinámica ¿Qué es el sistema?
Para la termodinámica el sistema es la parte del universo que es objeto de estudio y puede ser una célula, un organismo o una mezcla de reacción en un tubo de ensayo
80
New cards
¿Con base a qué se clasifican los sistemas?
Se clasifican con base en las fronteras o límites que los separan de los alrededores
81
New cards
¿Cómo se clasifican los sistemas?
Se clasifican en:
\-Sistemas abiertos
\-Sistemas cerrados
\-Sistemas aislados
\-Sistemas abiertos
\-Sistemas cerrados
\-Sistemas aislados
82
New cards
¿Qué es un sistema abierto?
\-Es aquel cuyas fronteras permiten el intercambio de calor y de masa
\
\-Un ejemplo es el ser humano, ya que a través de sus epitelios hay un flujo constante de calor, agua, glucosa, CO2 con el ambiente
\
\-Un ejemplo es el ser humano, ya que a través de sus epitelios hay un flujo constante de calor, agua, glucosa, CO2 con el ambiente
83
New cards
¿Qué es un sistema cerrado?
\-Es aquel que permite el flujo de calor pero NO de masa
\
\-Un ejemplo es una lata de conservas, ya que se puede calentar o enfriar pero no admite el intercambio de masa, a menos que se rompa el recipiente
\
\-Un ejemplo es una lata de conservas, ya que se puede calentar o enfriar pero no admite el intercambio de masa, a menos que se rompa el recipiente
84
New cards
¿Qué es un sistema aislado?
\-Es aquel en el que no hay flujo de calor ni flujo de materia
\
\-Un ejemplo es un termo, que se usa para guardar líquidos calientes o fríos que mantienen su temperatura debido a que no hay intercambio de calor
\
\-Un ejemplo es un termo, que se usa para guardar líquidos calientes o fríos que mantienen su temperatura debido a que no hay intercambio de calor
85
New cards
¿Cuáles son los componentes de una reaccióm química?
\-Los componentes a la izquierda se denominan REACTANTES o sustratos
\
\-Los componentes a la derecha se denominan PRODUCTOS
\
Además se considera un SISTEMA CERRADO por lo que se permite el flujo de calor pero no de masa
\
\-Los componentes a la derecha se denominan PRODUCTOS
\
Además se considera un SISTEMA CERRADO por lo que se permite el flujo de calor pero no de masa
86
New cards
¿A qué se le denominan condiciones estándar de una reacción?
Se denominan condiciones estándar de una reacción cuando:
CONCENTRACIÓN de reactantes y productos es: 1M
la PRESIÓN: 1 atm
Temperatura: 25°c (298k)
pH: 7
\
CONCENTRACIÓN de reactantes y productos es: 1M
la PRESIÓN: 1 atm
Temperatura: 25°c (298k)
pH: 7
\
87
New cards
¿Cuál es la primera ley de la termodinámica?
Es la LEY DE LA CONSERVACIÓN DE LA ENERGÍA:
\-Un proceso del mundo real involucra la @@transformación@@ de la energía y la @@cantidad@@ total de la energía, siempre se conserva en una simetría tiempo dirección y dice:
\
“Le energía no se crea ni se destruye solo se transforma”
\-Un proceso del mundo real involucra la @@transformación@@ de la energía y la @@cantidad@@ total de la energía, siempre se conserva en una simetría tiempo dirección y dice:
\
“Le energía no se crea ni se destruye solo se transforma”
88
New cards
¿Qué nos dice la segunda ley de la termodinámica?
\-Dice que la energía en forma de CALOR solo fluye espontáneamente desde regiones de MAYOR temperatura a regiones de MENOR temperatura
\-Describe la irreversibilidad de los sistemas termodinámicos
\-Describe la irreversibilidad de los sistemas termodinámicos
89
New cards
¿Cuál es la definición de ENTROPÍA?
Es una propiedad relacionada con el orden del sistema:
\-a MAYOR ORDEN, el contenido de entropía es menor
\-a MENOR ORDEN, el contenido de entropía es mayor
\-a MAYOR ORDEN, el contenido de entropía es menor
\-a MENOR ORDEN, el contenido de entropía es mayor
90
New cards
¿Qué relación tiene la entropía conforme a la segunda ley de la termodinámica?
Conforme a la segunda ley de la termodinámica, la entropía del universo crece con cada proceso que se lleva acabo en forma irreversible. Esto implica que el cambio de energía del universo siempre es positivo
\
\-Por lo tanto la entropía se define como el caos que busca el orden, pero que invariablemente va a caer en desorden
\
\-Por lo tanto la entropía se define como el caos que busca el orden, pero que invariablemente va a caer en desorden
91
New cards
¿Cuál es la definición de ENTALPÍA?
Es una magnitud termodinámica que expresa la cantidad de energía que un sistema puede intercambiar con su entorno
92
New cards
¿Qué representa el cambio de entalpía?
Representa la cantidad de calor que se libera o se absorbe en una reacción a presión constante
93
New cards
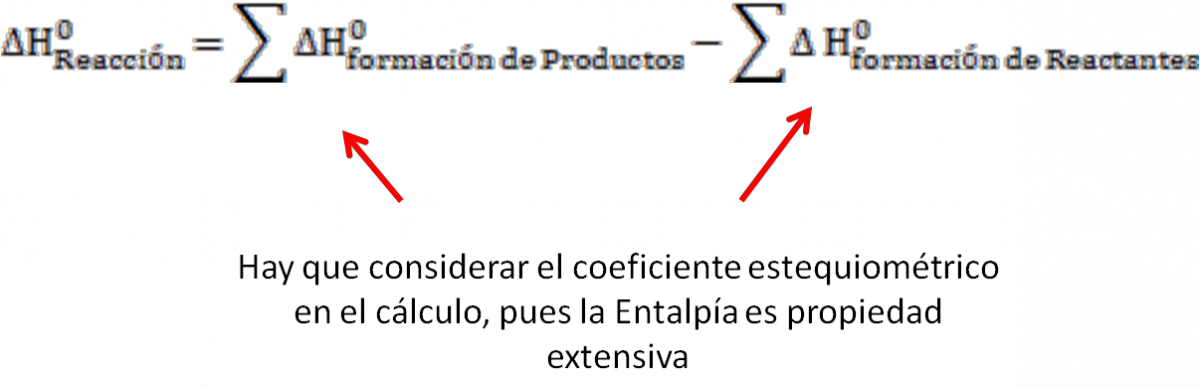
¿Por qué ecuación estada dada el cambio de entapía?
94
New cards
¿Qué es la energía libre de Gibbs?
\-Es una propiedad de las reacciones termodinámicas que solo toma en cuenta los cambios de entalpia y entropía del sistema y que representa un criterio medible de la espontaneidad de las reacciones
\
\-Esto quiere decir que la energía libre de GIBBS es la energía que está a disposición y quieta para usarse
\
\-Esto quiere decir que la energía libre de GIBBS es la energía que está a disposición y quieta para usarse
95
New cards
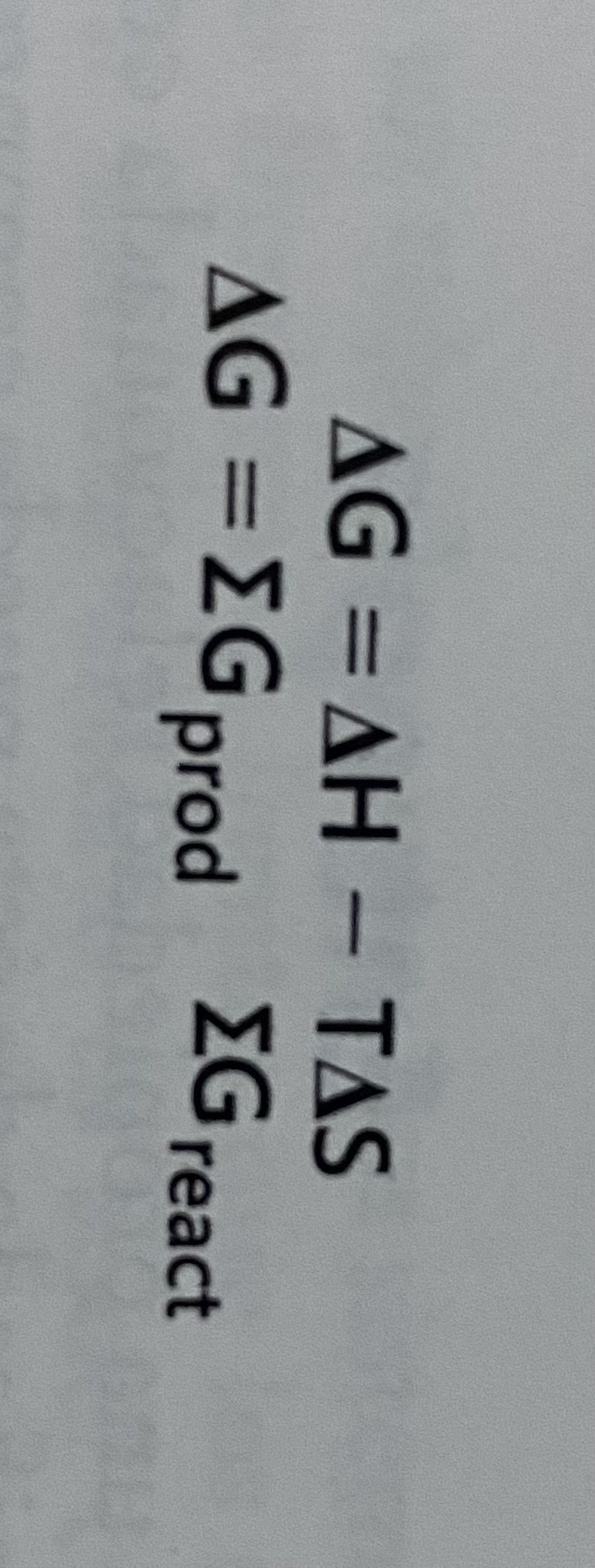
¿Por qué ecuación está dado el cambio de energía libre de Gibbs de cualquier reacción?
AG: valor de energía libre
AH: cambio de entalpía de la reacción
T: temperatura absoluta en kelvins
AS: el cambio de entropía
Eprod: la suma de las energías libres de los productos
Ereact: la suma de las energía libres de los reactantes
AH: cambio de entalpía de la reacción
T: temperatura absoluta en kelvins
AS: el cambio de entropía
Eprod: la suma de las energías libres de los productos
Ereact: la suma de las energía libres de los reactantes
96
New cards
¿Qué se necesita para que una reacción sea espontánea?
\-Para que una reacción sea espontánea habrá de liberarse energía libre, lo cual se indica con un AG (valor de energía libre) negativo
\
\-Por lo tanto una reacción es espontánea cuando la energía libre de los reactantes es mayor que la de los productos
\
\-A estas reacciones se les llama EXERGÓNICAS
\
\-Por lo tanto una reacción es espontánea cuando la energía libre de los reactantes es mayor que la de los productos
\
\-A estas reacciones se les llama EXERGÓNICAS
97
New cards
¿Cuándo se dice que una reacción no es espontánea?
\-Cuándo el AG de la reacción es positivo
\-Cuando la energía libre de los reactantes es menor que la de los productos
\-A estas reacciones se les llama ENDERGÓNICAS
\-En estas reacciones se debe aportar energía libre al sistema para lograr la transformación de reactantes en productos
\-Cuando la energía libre de los reactantes es menor que la de los productos
\-A estas reacciones se les llama ENDERGÓNICAS
\-En estas reacciones se debe aportar energía libre al sistema para lograr la transformación de reactantes en productos
98
New cards
¿Cuándo una reacción es exotérmica o endotérmica?
EXOTÉRMICA: -Cuando libera calor
-Cuando su AH (cambio de entalpía de la reacción) es negativo
\
ENDOTÉRMICA:-Cuando absorbe calor de los alrededores
-Cuando su AH (cambio de entalpía de la reacción) es positivo
-Cuando su AH (cambio de entalpía de la reacción) es negativo
\
ENDOTÉRMICA:-Cuando absorbe calor de los alrededores
-Cuando su AH (cambio de entalpía de la reacción) es positivo
99
New cards
¿Cuándo una reacción es exergónica o endergónica?
EXERGÓNICA: -Cuando libera energía libre
(Espontánea) -Cuando su AG (valor de energía libre) es negativo
\
ENDERGÓNICA:-Cuando no se lleva acabo en el sentido propuesto
-Cuando su AG (valor de energía libre) es positivo
(Espontánea) -Cuando su AG (valor de energía libre) es negativo
\
ENDERGÓNICA:-Cuando no se lleva acabo en el sentido propuesto
-Cuando su AG (valor de energía libre) es positivo
100
New cards
¿Cuál es la definición de la “ENERGÍA DE ACTIVACIÓN” de una reacción?
**-La energía de activación, representada por Ea, es la energía mínima requerida para que una reacción química se pueda llevar a cabo**, es decir, es la barrera energética se debe superar para que los reactivos puedan convertirse en productos.