microbio med virologie
1/44
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
45 Terms
INFECTIONS RESPIRATOIRES VIRALES
genres concernés ? (5)
Orthomyxoviridae (virus influenza)
Paramyxoviridae
Coronavirus (SARS)
Picornaviridae (Rhinovirus)
Adénovirus
Virus Influenza / Influenzavirus
ORTHOMYXOVIRIDAE
= le virus de la grippe
Virus à ARN monocaténaire de polarité négative, Huit segments d’ARN, Capside hélicoïdale, enveloppé
Réplication intranucléaire, amorce = 5’ARNm cellulaire, RNA polymérase RNA dépendante
Protéines d’enveloppe =
Hémagglutinine =
Hémagglutinine: trimère de 2 gp
Impliquée dans la fixation du virus sur le récepteur cellulaire:
Ac. sialique ou ac. N-acétylneuraminique
Neuraminidase =
Neuraminidase: tétramère
Impliquée dans la libération des virions
Inhibiteurs = Zanamivir (Relenza™) et Oseltamivir (Tamiflu™)
Protéines M1 =
Rôle dans le recruttement protéique “d’emballage”
Protéine M2 =
Canaux ionique de proton important pour la décapsidation quand changement de pH dans le lysosome
Trois types: A, B et C → Selon la nature de la nucléocapside
A chez l’homme et les animaux à l’origine de pandémies (car risque de co-infection chez les animaux)
→ 16 sous-types H(émagglutinine) (1-16) et 9 sous-types N(euraminidase) (1-9)
B et C chez l’homme (B aussi chez phoque), C peu pathogène
Les virus A et B évoluent sans cesse et le type C est assez stable (d’où, il est peu pathogène)
Variations antigéniques de HA et NA par mutations et réassortiments
Conséquence des variations →
Cas sporadiques
Épidémies (annuelles 5 à 10% de la population, hivernales)
Pandémies (→ si assez de gènes de virus humain dans le nouveau virus → transmissible → pandémie)
→ Modifications annuelles du vaccin !
Physiopathologie =
Transmission par voie aérienne jusqu’à 2 jours après signes cliniques, (selles et eau contaminées par oiseaux pour H5N1)
Localisation au tractus respiratoire, Nécrose des cellules ciliées et des cellules à mucus (→ forte atteinte du système respiratoire)
2 jours d’incubation, début brutal → Frissons, fièvre, courbatures, Céphalées, Atteintes respiratoires (sévérité dépend de la susceptibilité des patients)
Surinfections possibles.
Formes graves = ( ! âge, grossesse, immunodéprimés, insuf. resp. chron, obésité)
Œdème aigu et Symptômes neurologiques (syndrome de Reye)
décès (taux de léthalité dépend de la souche)
Traitement =
Inhibiteur de M2 (décapsidation: amantadine et rimantadine ): beaucoup de résistances
Inhibiteur de neuraminidase virale (Zanamivir, oseltamivir): aussi en chimioprophylaxie
→ ! Développement rapide de souches mutées résistantes aux antiviraux !
Prévention =
Vaccins inactivés sans adjuvants (produits sur œufs embryonnés), Antigènes de surface (N et H)
Induisent IgG mais mais pas IgA (IgA seront produit pdt réponse naturelle)
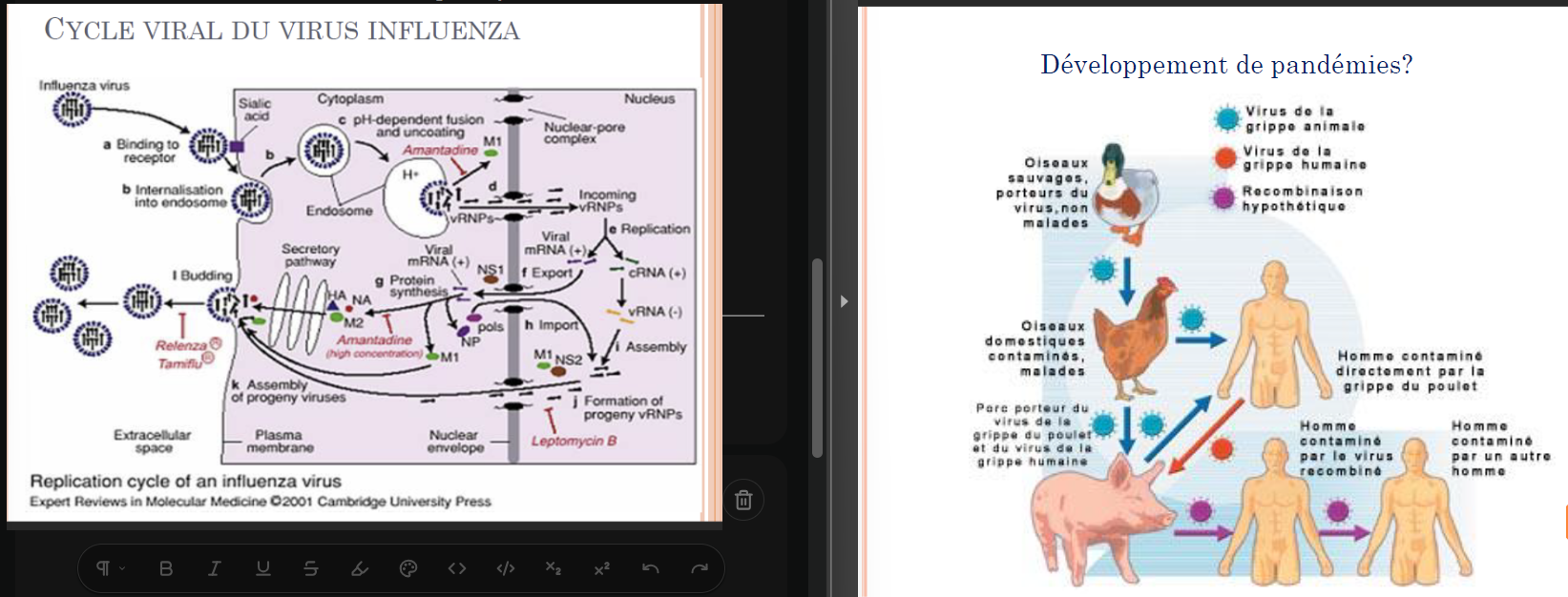
intérêt vaccination ? (3)
Protection individuelle (personnes vulnérables et à risque) Dans le cas de la vaccination antigrippe , la recommandation est pour le personnel de santé ou travaillant en institution, les personnes avec des maladies chroniques sous-jacentes, les femmes enceintes, les personnes en institution et les personnes de plus de 65 ans.
Protection collective (d’où propsition au personnel soignant de se faire vacciner)
Maîtrise d’une épidémie
PARAMYXOVIRIDAE (famille)
3 genres ?
infection système … ?
généralité ?
Paramyxovirus
Morbillivirus
Pneumovirus
Système respiratoire
Virus à ARN monocaténaire, non segmenté, de polarité (-), Capside hélicoïdale, enveloppée
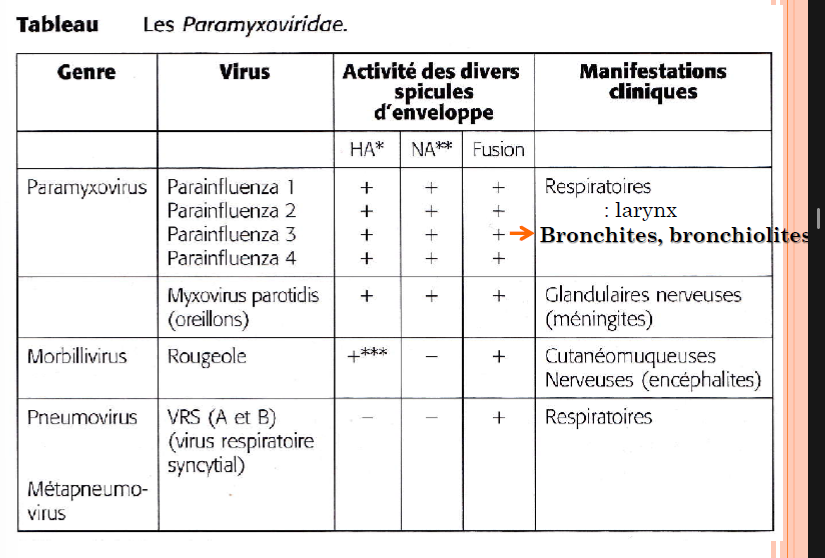
VIRUS PARAINFLUENZA
famille PARAMYXOVIRIDAE
Virus à ARN monocaténaire, non segmenté, de polarité (-), Capside hélicoïdale, enveloppée
propriétés de fusion → sortie par bourgeonnement
épidémiologie =
Parainfluenza de type 3 : avant l’âge de 2 ans (!!!)
Parainfluenza de type 1 et 2: avant l’âge de 6 ans
Epidémies (saisonnière, surtout printemps (avril mai juin))
! Réinfection possible
→ bronchites et bronchiolites
Peut donner des épidémies (plutôt au printemps) et réinfections possible
Pas de traitement particulier (→ plutôt symptomatique)
MYXOVIRUS PAROTIDIS
= Virus des OREILLONS
famille PARAMYXOVIRIDAE, genre paramyxovirus
Virus à ARN monocaténaire, non segmenté, de polarité (-), Capside hélicoïdale, enveloppée
Clinique et épidémiologie =
Incubation de 14 à 21 jours
Tuméfaction des glandes salivaires, parotidite
Complications glandulaires: orchite (= atteintes des testicules et risque d’infertilité, 20-30%), pancréatite, thyroïdite, … ou méningite (1/400)
Personnes à risques pour complications → les adultes (si primo-infection)
L’homme est le seul réservoir, transmission par voie aérienne
Immunité acquise durable
Prévention = Vaccins vivants atténués ou inactivés
(avec vaccin contre rubéole et rougeole, produits sur œufs embryonnés pour les atténués)
virus des oreillons ?
MYXOVIRUS PAROTIDIS
famille PARAMYXOVIRIDAE, genre paramyxovirus
Virus à ARN monocaténaire, non segmenté, de polarité (-), Capside hélicoïdale, enveloppée
Clinique et épidémiologie =
Incubation de 14 à 21 jours
Tuméfaction des glandes salivaires, parotidite
Complications glandulaires: orchite (= atteintes des testicules et risque d’infertilité, 20-30%), pancréatite, thyroïdite, … ou méningite (1/400)
Personnes à risques pour complications → les adultes (si primo-infection)
L’homme est le seul réservoir, transmission par voie aérienne
Immunité acquise durable
Prévention = Vaccins vivants atténués ou inactivés
(avec vaccin contre rubéole et rougeole, produits sur œufs embryonnés pour les atténués)
virus de la ROUGEOLE
famille PARAMYXOVIRIDAE, genre MORBILLIVIRUS
Virus à ARN monocaténaire, non segmenté, de polarité (-), Capside hélicoïdale, enveloppée (présence hémagglutinine, neuraminidase et prot de fusion), infecte les lymphocytes
Clinique =
L’homme est le seul réservoir
Transmission par aéroportée (95% infectés ont 5 9 ans), 10 jours d’incubation
→ Endéans les 5 jours: macules avec centre blanchâtre dans joues internes (=taches de Koplik) puis, Exanthème maculopapuleux rétro auriculaire
→ Guérison en 8 jours (=> pour les enfants = bénin)
Complications importantes =
pour enfants en malnutrition ou personnes immuno-déprimés: infections respiratoires importantes
Pour personnes âgées: encéphalites postéruptives (1/1000 à 1/2000)
Panencéphalité sclérosante subaiguë (1/100.000): paralysie et dégradation neurologique après plusieurs années. (serait une réaction immunitaire auto-immune)
Prévention = vaccin vivant atténué (RRO)
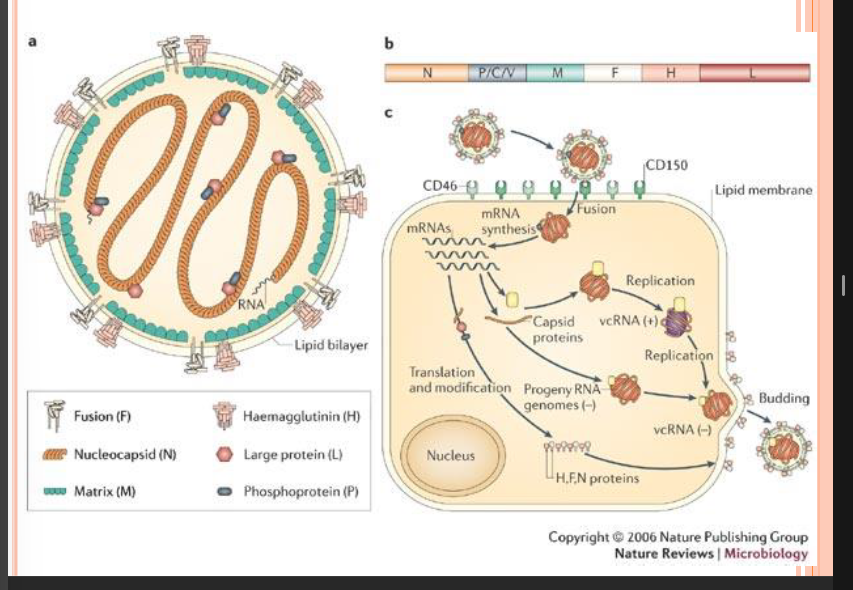
VIRUS RESPIRATOIRE SYNCYTIAL = VRS
famille PARAMYXOVIRIDAE, genre Pneumovirus
Virus à ARN monocaténaire, non segmenté, de polarité (-), Capside hélicoïdale, enveloppée, protéine de fusion
(Syncytia = 1 cellule multi-nuclée car obtenue par fusions de plusieurs cellules, principe qui existe naturellement au niveau du placenta mais certains virus sont capable de fusionner plusieurs cellules aussi)
Clinique, épidémiologie =
plutôt en hiver
4 5 jours d’incubation
Personnes à risque = les tous petits (surtout dans premières semaines de vie)
Rhinopharyngite chez adulte
Bronchite ou pneumopathie chez les nouveaux-nés
Endéans l’âge de 5 ans: > 90% des primo-infections
Réinfection possible chez les adultes →
complication chez les personnes âgées et immunodéprimés
(Remarque: Clinique et épidémiologie similaire à un nouveau virus:, le métapneumovirus humain)
Traitement =
Ribavirine
Immunoglobulines anti VRS
Existe un vaccin (de type recombinant) (proposé aux femmes enceintes et au adultes à risque)
Coronaviridae, Coronavirus, virus SARS
2 à 10% des rhumes, épidémies et réinfections
= Syndrome respiratoire aigu sévère (SRAS) = Severe acute respiratory syndrome (SARS)
Virus enveloppé (avec protéines SPIKE), ARN de 30.000 pb, polarité positive
! Résiste > 24h sur surface externe (contre-intuitif car enveloppé, mais du coup ne résiste pas au gel hydroalcoolique)
Réservoir animal (civettes, chauves souris)
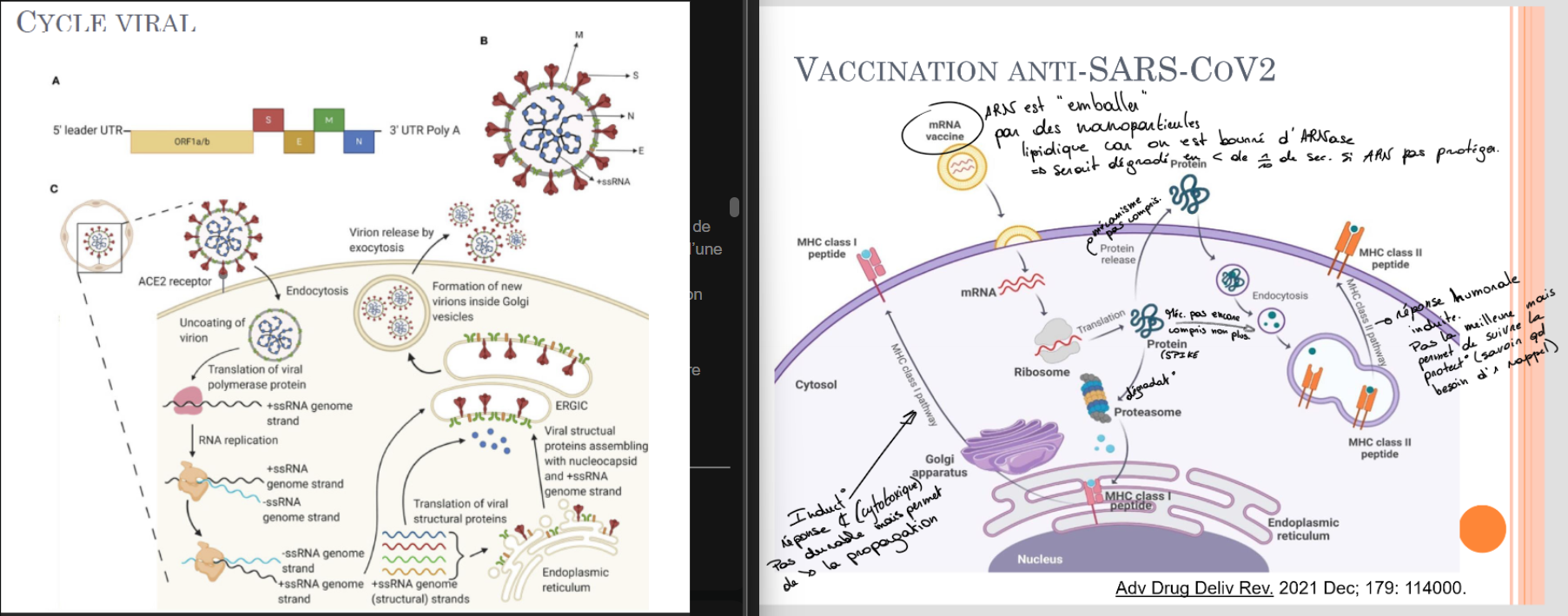
Cycle viral (image)
Clinique =
Signe radiologique de pneumonie, fièvre, …
Incubation de 3-10j, mortalité de 10%
Prophylaxie =
Masques
Lavage des mains, poignées de portes, boutons d’ascenseurs, …
traitement =
Recommandations de l’OMS: administration (par voie intraveineuse ou orale) de corticostéroïdes systémiques pendant 7 à 10 jours chez les patients atteints d’une forme grave ou critique de la COVID 19 (les systèmes immunitaires ont une réaction trop forte, donc forte production de cytokines), et une recommandation conditionnelle de ne pas recourir à une corticothérapie pour le traitement des patients atteints d’une forme non sévère de la COVID 19.
Existe des Ac → Ac contre les cytokines “c’est une valeur sûre” (on a eu contre prot. SPIKE mais ces prot. mutent donc…) par contre c’est très cher
+vaccin à ARNm (qui code pour une protéine SPIKE), ! ARNm est TRES fragile (donc on le protège par des nanoparticules lipidiques (enveloppe les ARNm) qui va se faire phagocyter par une cellule dendritique et présentation par CMH de classe 1 (image 2)) → pas de protection très longue (surtout réponse cellulaire, un peu réponse humorale (permet de suivre l’immunité mais pas de protection contre l’infection, surtout protection contre les complications/la sévérité de l’infection), existe aussi vaccin avec vecteur viral (= virus non viral pour l’Homme à qui on fait exprimer des facteurs de virulence pour induire une réponse immunitaire visant le virus pathogène visé, → permet induire une réponse humorale plus durable mais plus de risque de complications,), vaccin virus inactivé
Picornaviridae
2 genres ?
généralités ?
entérovirus (poliovirus, Coxsackie, Echovirus et entérovirus)
Rhinovirus
Petits virus , ARN polarité (+), capside icosaédrique, non enveloppé, résistant dans le milieu extérieur
ADÉNOVIRUS
42 types
Virus ADN bicaténaire , capside icosaédrique, non enveloppé, possède une activité hémaglutinine
Hôte des tissus lymphoïdes, provoquent adénopathies,
atteintes voies aériennes (5-10% des infections resp. virales) et conjonctives
→ sont responsables de bcp de types d’infections différentes
Clinique et épidémiologie =
Transmission par voie aérienne
Infections respiratoires : rhinopharyngites, adénopathies, pneumopathies
Conjonctivites épidémiques
Adénites mésentériques
Gastroentérites
Exanthèmes maculopapuleux
Cystites hémorragiques
(méningo-encéphalites)
Touche surtout les “tous petits”
Virus des gastroentérites
4 genres ?
Picornaviridae : Entérovirus (avec Poliovirus et Coxsackie)
Calicivirus (→ Norovirus/virus de type Norwalk)
Rotavirus
Adénovirus
PICORNAVIRIDAE , ENTÉROVIRUS
généralité + les virus ?
Petits virus ARN de polarité (+) (donc la réplicase est importante !), capside icosaédrique non enveloppée (donc résistante dans le monde extérieur, à la dessication, à certains désinfectant) → virus particulièrement résistant
Entérovirus avec tropisme pour le tractus digestif et souvent aussi le système nerveux
Transmission =
Réservoir strictement humain
Transmission par voie oro-fécale, aliments souillés et aérienne
Directe ou indirecte
Poliovirus: Rare depuis la vaccination
Incubation 10-14 jours
(normalement) Asymptomatique, fièvre, douleurs musculaires
Multiplication virale dans amygdales, dans les plaques de Peyer (au niveau de l’intestin) → porte d’entrée du virus pour atteinte nerveuse
(si patient plus sensible) Virémie secondaire: atteintes de neurones de la moelle épinière → paralysie (1/100 à 1/1000)
Coxsackie, echovirus et autres entérovirus
Asymptomatique
Méningite lymphocytaire aigue, encéphalite
Myocardite et péricardite
Diarrhée?
Éruption maculopapuleuse
Paralysie (généralement sans séquelles)
VACCINS anti-poliovirus contre les 3 types de poliovirus
Inactivé: innocuité, Ac sérique protecteur, protège contre les complications MAIS besoin de rappels
existe vivant atténué mais n’est plus utilisé (car !!! aux réversions de virulence)
CALICIVIRUS
+les virus “les plus communs”
Petits virus à ARN linéaire de polarité (+), Capsides non enveloppées en forme d’étoile
Norovirus/virus de type Norwalk
Hautement contagieux, transmis par voie oro-fécale/aérienne par contact direct ou indirect
Responsable de la majorité des gastroentérites non bactériennes
Incubation courte et symptômes entre 24 et 60h
Responsable de gastroentérites dans les collectivités (surtout les crèches), non saisonnières!
Pas de vaccins, pas de traitement → !!! réhydrater le patient
prophylaxie = mesures d’hygiène
ROTAVIRUS
Famille Reoviridae
ARN génomique bicaténaire en 11 segments
Capside icosaédrique double!
ARN polymérase dans le virion
Très résistant dans le monde extérieur
Transmission par voie oro-fécale directe ou indirecte
Ubiquitaire, épidémies hivernales (donc, est un peu moins résistant à la dessiccation que Norovirus)
physiopathologie =
Multiplication virale dans les entérocytes
Perturbation de l’activité électrolytique (=> réhydratation)
Rôle des IgA dans la neutralisation du virus AVANT qu’il infecte les entérocytes
Clinique =
Souvent chez les enfants < 3 ans
Diarrhée
Vomissement
Déshydratation
Décès dans les pays démunis
Traitement = symptomatique
Prévention = vaccin vivant atténué (permet d’obtenir une réponse avec des IgA), par voie orale (gouttes de vaccin → facilité d’administration pour les enfants)
VIRUS DES HÉPATITES
virémie ?
clinique ?
transmission ?
Virémie secondaire
→ Herpesviridae, arbovirus (fièvre jaune), arenavirus (fièvre de Lassa), Filovirus (Ebola, …)
Virémie primaire
Virus d’ Hépatite A , B , C , D , E (et G)
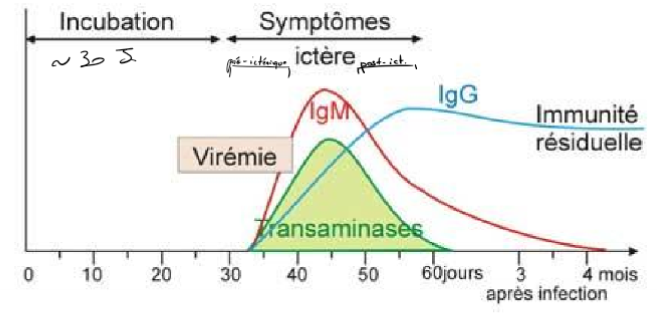
Clinique =
Variabilité du temps d’incubation
Même tableau clinique =
Forme majeure (fulminante) ou mineure (abortive, voire inapparente)
3 phases:
pré-ictérique (4-7 jours): troubles digestifs, asthénie, rash et arthralgies
Ictériques (8-30 jours): ictère, oligurie, décoloration des selles
Convalescence : crise urinaire et fatigabilité
DEUX VOIES DE TRANSMISSION:
Voie oro-fécale → Hépatites A et E => non enveloppés
Voie parentérale → Hépatites B, C, D, G => enveloppés
Physiopathologie =
Lésions nécrotiques de cellules hépatiques (par une lyse nécrotique lié au cycle virale OU par réponse immunitaire)
Infiltration lymphomonocytaire

VHA
Picornaviridae (entérovirus)
petit virus à ARN (+), capside icosaédrique, sans enveloppe (un des virus les plus résistant au monde extérieur)
Epidémiologie
Réservoir humain
Infection orofécale directe ou indirecte (eau, coquillages, ..)
Hépatite épidémique en zone tempérée
Prévention =
Règles d’hygiène
Ig en intramusculaire: protection pendant 3 mois (→ intéressant si l’entourage est non vacciné)
Vaccin inactivé: Havrix (forme adulte ou enfant)
Vaccin mixte Twinrix anti-VHA et anti-VHB
Vaccin inactivé anti-hépatite A + Antigène de surface (biotechnologie) hépatite B
VHE
Ressemble aux Caliciviridae, genre Hepevirus
Virus ARN (+), monocaténaire, capside en forme d’étoile, fragile (forte dose de virus nécessaire à la transmission ET pour sa survie dans le tractus intestinal)
Transmission orofécale indirecte (eau), responsable d’épidémie en Asie, Afrique et Amérique du sud
Réservoir humain et animal
Souvent asymptomatique sauf chez la femme enceinte où l’infection peut être fulminante
Pas de vaccination
VHB
Hepadnaviridae
Virus ADN bicaténaire à ¾, brin long à polarité (-)
Capside icosaédrique enveloppée
Différents génotypes
Transcriptase inverse !
Epidémiologie =
Réservoir humain
Transmission par le sang et ses dérivés ou matériel injectable mal stérilisé
Attention au sperme, sécrétions vaginales, (la salive)
→ transmission sexuelles et périnatales
→ Groupes à risque: Drogués, enfants nés de mères porteuses de l’infection, transfusés, personnel soignant
Physiopathologie =
Multiplication dans les hépatocytes
Cellules NK induisent la lyse des cellules infectées
Complications (périartérite noueuse, glomérulonéphrite, polynévrite) dues dépôt complexes immuns circulants
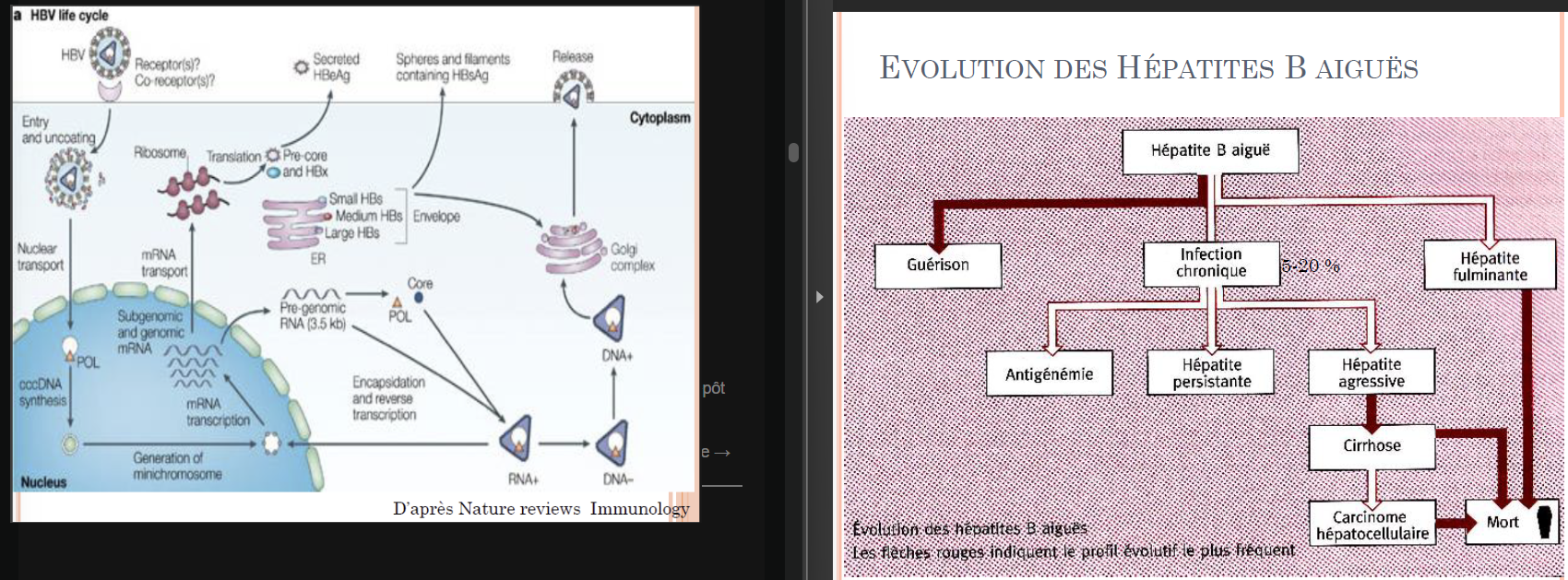
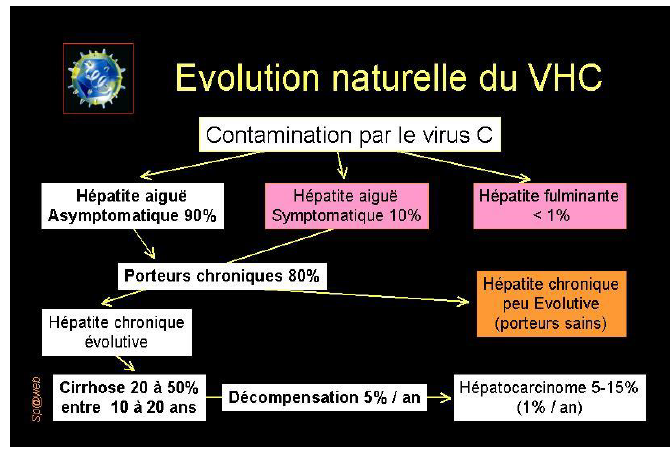
Infection chronique fréquente (5-10%), rôle du système immunitaire → fibrose → cirrhose → hépatocarcinome
Traitement =
Portage chronique? = Ag HBs persistant plus de 6 mois
IFN alpha (vu cours cpb) (pas mal de résistance => mtn est donner AVEC un inhibiteur de réverse transcriptase)
Lamivudine : inhibiteur de la transcriptase inverse, analogue de la cytidine
Adéfovir dipivoxil (Hepsera TM ), analogue nt inhibiteur de la transcriptase inverse
Et autres ( entécavir , ténofovir, …)
Vaccination avec AgHBs recombinant
VHD
Virus défectif
Co-infection avec VHB → infection fulminante? (risque augmente quand présence du VHD en plus du VHB)
Virus ARN (-), capside (Ag Delta) et enveloppe de VHB (HBs)
VHC
Flaviviridae, virus ARN de polarité (+), enveloppé
→ 6 génotypes (sévérité des lésions et difficulté de traitement dépend du génotype)
Présence séquence IRES → Liaison des ribosomes préférentiellement à cette amorce → synthèses des protéines virales devient “prioritaire”)
Epidémiologie =
Transmission sanguine
Transmission sexuelle? (oui mais facteur moins important que sanguin)
Transmission materno-foetale réduite (existe mais rare)
Transmission néonatale: hépatite bénigne
Physiopathologie =
Multiplication dans le foie et libération dans le sang (cible = monocyte)
Forme asymptomatique fréquente (problème car…), Chronicité élevée → cirrhose (après >10 ans) → hépatocarcinome
Traitement =
Portage chronique? Fibrose?
Anciennement: IFN alpha + ribavirine (analogue nucléosidique)
Meilleure chance de réponse si faible charge virale, si fibrose peu sévère et si génotype 2 ou 3
Bi- Trithérapie → avec un inhibiteur de la protéase NS3: Bocéprévir ,
siméprevir , télaprévir , paritaprévir
Plus récemment, développement d’inhibiteurs de la RNA polymerase , exemples :
Daclat asvir (NS5A ): inhibiteur non nucléosidique pangénomique du complexe de réplication
Sofosbuvir NS5B) : inhibiteur nucléotidique pangénomique
→ bithérapie avec ou sans ribavirine (si génotype 2)
VIRUS À INFECTIONS DE LA PEAU ET DES MUQUEUSES GÉNITALES
virus classés selon type ADN/ARN ?
1. Les virus à ADN bicaténaire
Virus enveloppés:
Herpesviridae
Poxviridae
Virus non enveloppés:
Papillomavirus
2. Virus à ARN
Virus de la rubéole
3. Virus à ADN monocaténaire
Parvovirus (on en parle pas)
Herpesviridae 3 grandes “classes” ? + les virus
α Herpesvirinae →
Herpes simplex virus type 1 et 2 (HSV1 et HSV2)
Varicella zoster virus (VZV)
β Herpesvirinae →
Cytomegalovirus (CMV)
Human herpes virus 6 et 7
γ Herpesvirinae →
Epstein Barr virus (EBV)
Human herpes virus type 8
HSV
= Herpes simplex virus
Caractéristiques =
ADN linéaire, de grande taille (>125 kpb) et avec des séquences répétitives
Virus enveloppés de grande taille avec tégument et capside hélicoïdale.
Région de protéines proches et tardive (prot. impliquée dans structure pour sortie des virions)
Répartition mondiale (67 % HSV-1)
Cytopathogène
Primo-infection (dans l’enfance)
Maladies récidivantes avec persistance du virus dans les cellules
Caractère oncogène de certains virus herpétiques
Affection vésiculaire de territoires muqueux
• Primo infections généralement inapparentes
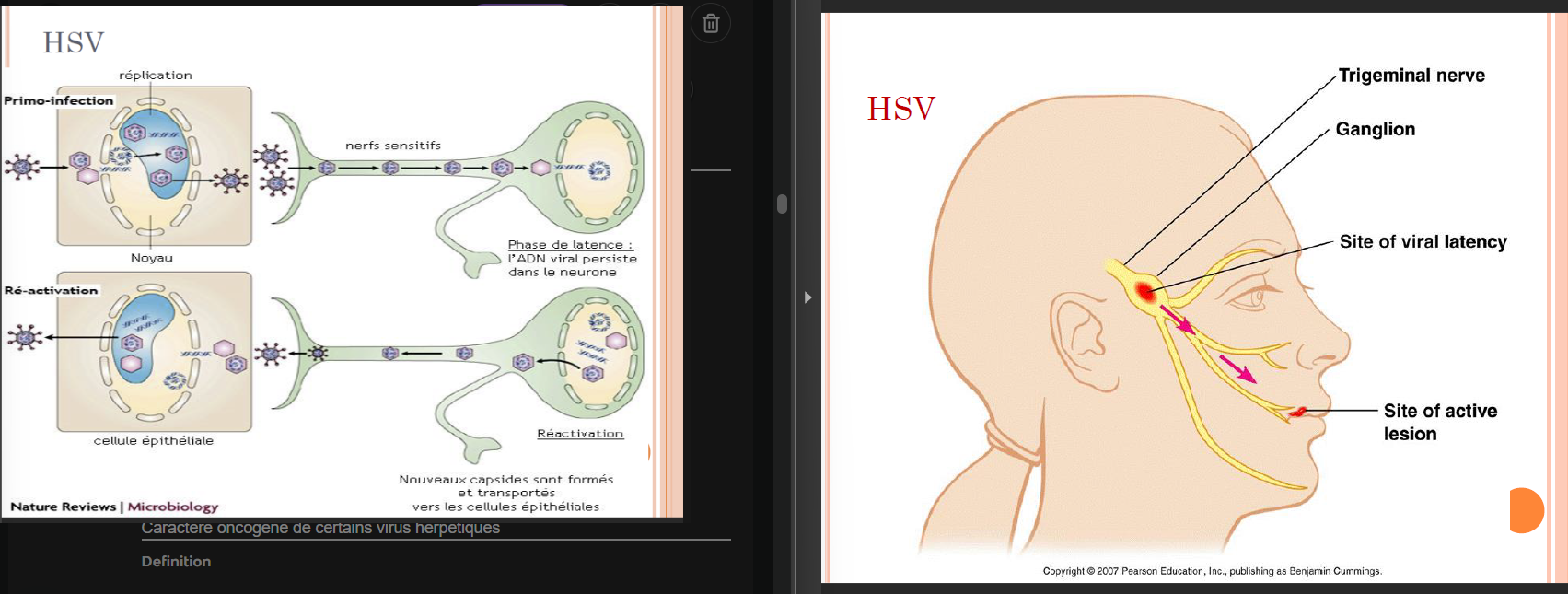
• Latence dans les neurones (ganglions sensitifs, sous forme d’épisome = cyclique et désactivé)
• Réactivation de virus latents quand affaiblissement du syst. immun.)
• Facteurs favorisants = Fièvre, UV, contrariétés, Infections, menstruations, immunité
Vésicule herpétique = Nécrose cellulaire intra-épithéliale
Contagion via Salive ou rapports sexuels
! Porteurs sains
HSV 1 et 2 →
Les deux types peuvent infecter les muqueuses orales et génitales mais en général
Dépend du contact:
HSV 1 transmission plutôt orale, directe (ou par ustensiles souillés)
Mains → plaies et yeux
HSV 2 transmission sexuelle, ! Mère vers enfant À l’accouchement (ou in utéro)
HSV1:
Complications =
Gingivo-stomatite, infection oculaire kératite herpétique → Entraîne la cécité, Eczéma herpétique chez des enfants atteints d’eczéma actif et Encéphalite herpétique (patients âgés, HIV+, etc..) → souvent mortelle
Récidive = herpès labial
HSV2:
Primo-infection asymptomatique mais lésions graves possibles
Récidives =
Pénis, col utérin, vagin et région ano-rectale
Forme sévère → Herpès néonatal (risque: éruption vésiculeuse généralisée, encéphalite, hépatite, cécité)
Traitement =
5 iodo déoxyuridine (IdU) et trifluorothymidine (TFT) en traitement local → contre HSV
Cytosine arabinoside et adénine arabinoside → contre HSV et VZV
→ Acycloguanosine (Acyclovir, Zovirax ) et valaciclovir
ACG → ACG-P par thymidine kinase virale (svt pro-drogue → permet diminuer toxicité car sera toxique uniquement pour les cellules infercté)
Penciclovir, Famciclovir
Foscarnet (Foscavir): analogue du pyrophosphate → contre CMV, HSV, VZV
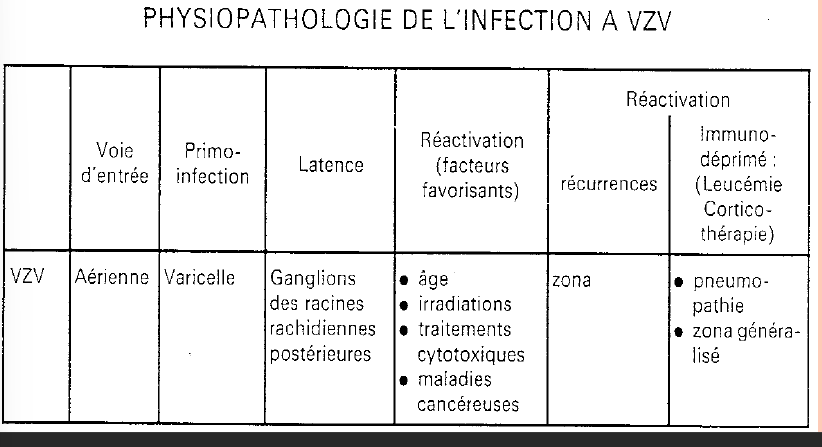
VZV
= virus de la varicelle et du zona
virus enveloppé
Varicelle
Infection vésiculeuse, Transmise par voie aérienne ou contact
Incubation de 12 à 14 jours
Rash avec papules sur tout le corps mais surtout tronc, face et cuir chevelu
Plus sévère chez enfants plus âgés et adultes
Complications rares = Pneumonies (15% des adultes) et Encéphalite
Zona
Récidive à partir d’un nerf sensitif avec zona intercostal ou ophtalmique
Douleurs importantes et brûlures même après disparition des papules (Atteint surtout les personnes âgées)
Traitement varicelle:
Essentiellement symptomatique (assèchement, désinfection, coupure des ongles)
Traitement zona:
→ Acycloguanosine (Acyclovir, Zovirax )
→ Vaccin atténué pour personne travaillant dans les centre de santé ou avant traitement immunosuppresseur ou grossesse
→ Ig pour femmes enceintes
CMV
= Le virus cytomégalovirus (CMV)
Infecte macrophages, cellules endothéliales, lymphocytes, cellules épithéliales et cellules souches moelle osseuse
Virus enveloppé à ADN linéaire, double brin 230 000 bp
Réservoir exclusivement humain, latence dans l’organisme avec sites multiples → Excrétion: Sang, salive, larmes, urines, selles…
Épidémiologie =
mondiale, ubiquitaire, permanente (prévalence pays industrialisé → 50-75%)
Primo infection ou Secondaire à Réactivation ou Réinfection par une souche exogène
Transmission =
Le plus fréquent = contact direct, contact étroit: salive, tissus, rapports sexuels, lait maternel…,
Contamination précoce en rapport avec le statut socio-économique
Intra-utérine, périnatale
Objets souillés, greffe d’organes
Clinique =
Chez sujets immunocompétent: Asymptomatique ou Syndrome mononucléosique
Fœtus ou immunodépression: Atteintes d’organes !!
Infection durant la grossesse:
Mère primo-infectée → Asymptomatique ou mononucléose.
Infection du Fœtus → Infection généralisée = Affection du foie, des poumons et de la rate Ou problèmes neurologiques: perte d’audition, de la vue ou retard mental (! dépend également de la période de grossesse pdt laquelle le fœtus va être infecté)
Infection à la naissance: Souvent peu grave
Infection chez les immunodéprimés, transplantés, SIDA: Pneumonies, rétinites, problèmes gastro-intestinaux et Mortalité (liste non exhaustive, dépend de la susceptibilité du patient)
PRÉVENTION =
Pas de vaccins (on essaye mais on y arrive pas)
Eviter les contact avec la salive et les urines des enfants et se laver les mains
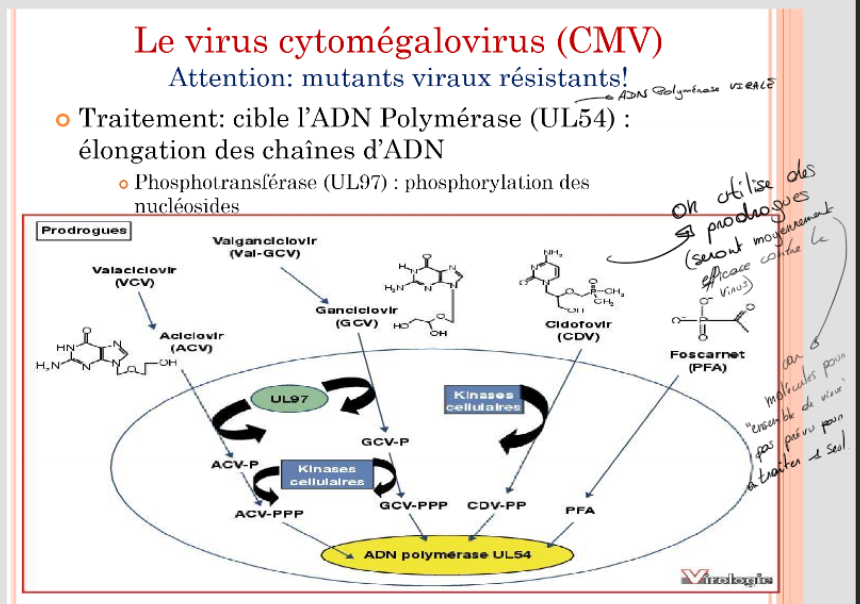
Traitement = (cf. imgae)
cible l’ADN Polymérase (UL54) : élongation des chaînes d’ADN
Le virus d’Epstein et Barr = EBV
Herpesviridae, long ADN, virus transformant (ADN s’insère)
Mononucléose infectieuse (90 à 95% de séropositif dans le monde)
Pénétration par oropharynx, “Maladie du premier baiser”, Contact étroit nécessaire
Souvent asymptomatique (et sévérité dépend de chacun, bcp plus important chez adulte)
Incubation 1 mois → Fièvre, fatigue, angine ou rhinopharyngite, Adénopathies (= ganglions gonflés), parfois rash
Guérison après 2 à 3 semaines → Parfois chronique 3 à 4 mois
Carcinome du nasopharynx
Prédisposition génétique Et cofacteur de l’environnement
Lymphome immunoblastique: HIV+
Virus du Sarcome de Kaposi (HHV-8)
ANNECDOTIQUE, PAS INTERROGE
cancer des tissus sous la peau ou des muqueuses:
paroi de la bouche, du nez et de l'anus.
Les organes internes peuvent aussi être atteints.
Transmission?
sexuelle MTM ou mère-enfant et enfant enfant par salive
→Touchait les patient atteint du SIDA avant qu’on ai des traitements
POXVIRIDAE
2 genres ?
Orthopoxvirus (mortalité: 50% variole à l’époque)
Molluscipoxvirus
Smallpox: virus de la variole
Eradiquée par vaccination
Maculeux → crouteux, forme hémorragique
Transmission aérienne et cutanée
Variole du singe
Orthopoxvirus
Fièvre, éruptions cutanées, adénopathie
Transmission par contact étroit ou indirect (literie)
Taux de létalité 3-6%
2-4 semaines de symptômes, guérison spontanée
LES PAPILLOMAVIRUS (HPV)
Famille des Papillomaviridae, non enveloppé
Infecte les épithélia de la peau et des muqueuses,
2 genres (alpha et beta) avec des tropismes différents
Plus de 100 papillomavirus (HPV) ont été identifiés
Genre beta : tropisme cutané → verrues pour certains types (bcp font parties de notre microbiome)
Genre alpha : tropisme pour muqueuses → orales, anales ou génitales (15 types donnent des cancers, surtout 16 et 18)
Transmission= beta → contact indirect, alpha → contact direct
Génome à ADN double brin circulaire de 8000 pb
Divisé en deux régions:
une région précoce: maintenance du génome (certaines prot ont des propriétés transformantes)
une région tardive: protéines de la capside (L1 et L2, une prot majeure et une prot mineure)
épidémiologie des HPV du genre alpha =
Infection sexuellement transmissible (toutes les muqueuses)
Risque de faire un jour une infection HPV : 80-85 %
Généralement infection asymptomatique (jusqu’à ce qu’on arrive au stade de lésion cancéreuse)
Relation cause à effet entre infection à HPV de haut risque et cancer du col utérin et est un facteur de risque pour d’autres types de cancers au niveau génital ou oropharynx
(image 2) Papillome juvénile laryngé → dure TOUTE SA VIE (doit être opérer tous les 6 mois pour retirer le virus qui aura bloquer le larynx) quand maman infectée et bébé prend du HPV à la naissance.
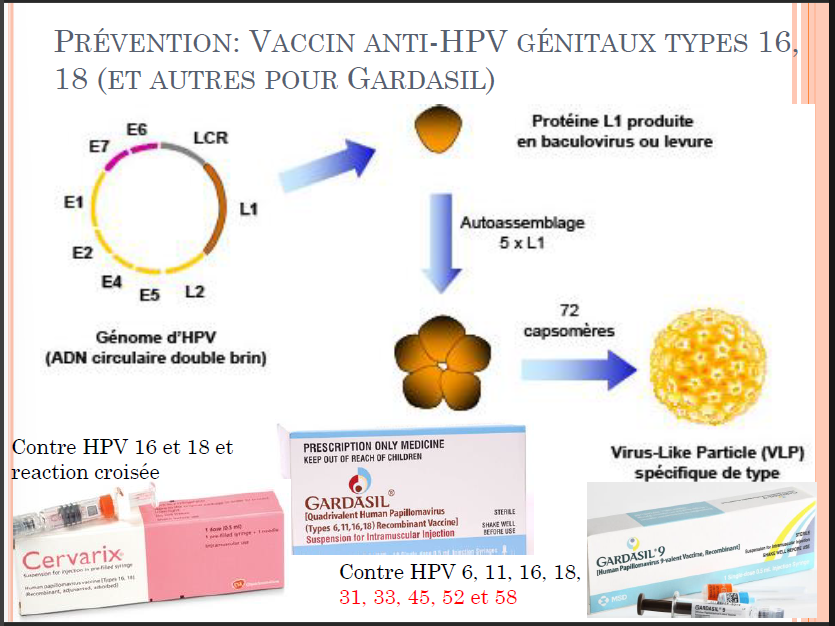
Vaccin → contre HPV 16 et 18, capsomère de prot. L1 → composé de Virus-Like Particle (existe un nonavalent)
Dépistage cancer du col → frottis (si détecter et traiter rapidement, 100% de guérison)

Vaccin anti-HPV ?
vaccin AVANT le 1er rapport des jeunes filles (si après → protection seulement ~50%)
VIRUS DE LA RUBÉOLE
genre rubivirus
Virus à ARN de polarité (+), capside icosaédrique, enveloppé, spicules hémagglutinants
Réservoir strictement humain
Transmission par contact direct ou aéroportée
Clinique et Epidémiologie =
Enfants (5-9 ans) et Adultes →
Transmission par voie aérienne, interhumaine
Incubation de 14-21 jours
Fièvre modérée, adénopathie, écoulement nasal, exanthème maculopapuleux (débute sur le visage)
Souvent asymptomatique
Maladie bénigne, rares complications (encéphalite et alors plutôt chez personnes âgées)
Rubéole congénitale →
Atteinte du fœtus lors d’une primo-infection maternelle dans les 20ères sem. de grossesse → Malformations du cœur, oreille, œil
Prévention =
vaccin vivant atténué, RRO
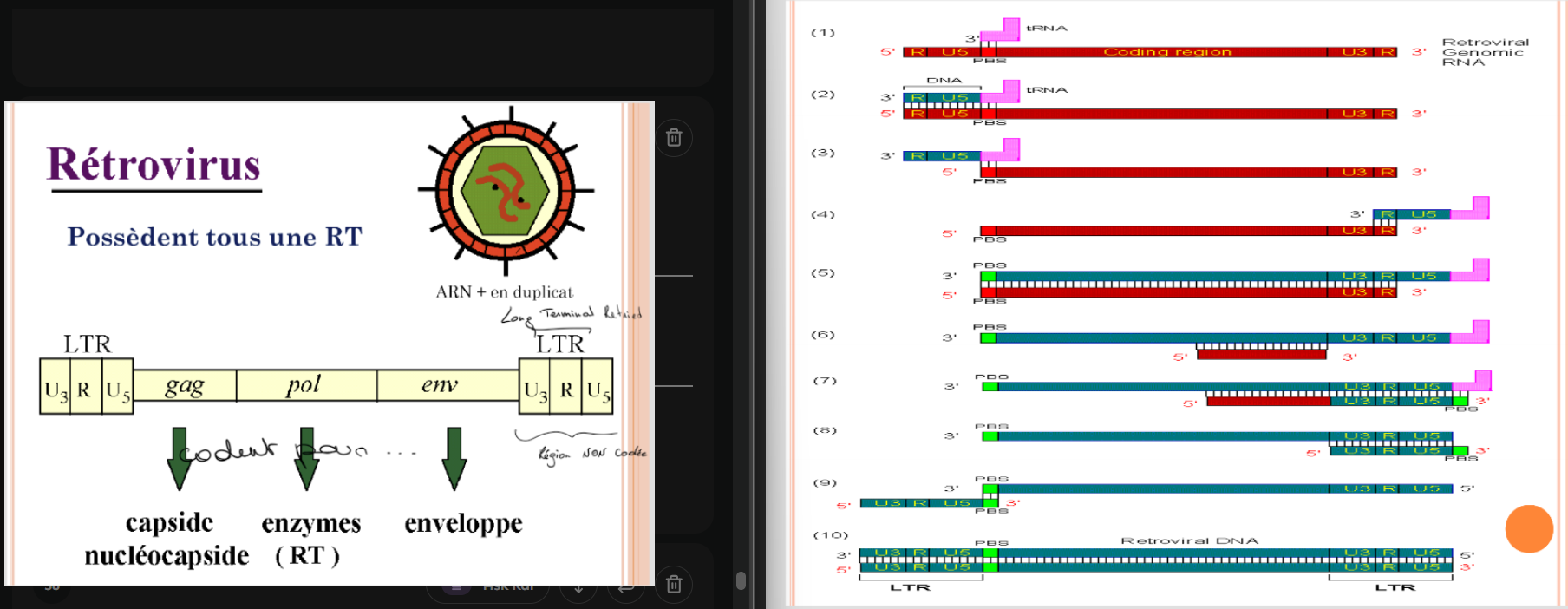
LES RETROVIRIDAE
citer
Les oncovirus (HTLV I)
Les lentivirus (HIV 1 et 2)
rétrotranscriptase des rétrovirus ?
→ “zones” répétitives sont plus longues que pour le génome “normal”
→ Quand on a les doubles brins → insertion dans le génome de nos T4
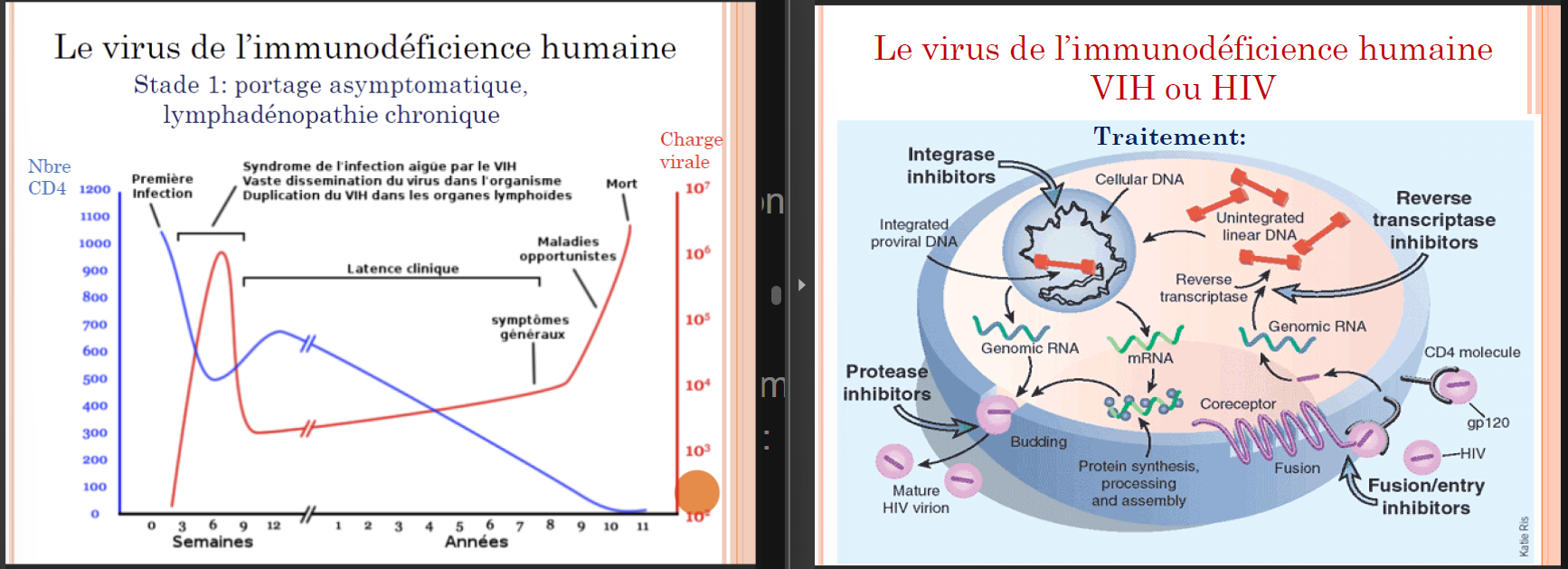
VIH ou HIV
= Le virus de l’immunodéficience humaine = Acquired Immune Deficiency Syndrome (SIDA)
transmission sanguine, le lait et le sperme
destruction des lymphocytes T CD4
Pathologie =
Stade 1 : primo infection
souvent inaperçue (~ mononucléose infectieuse), parfois symptôme neurologique (méningite lymphocytaire aiguë) mais pour personnes déjà immuno-déprimés
Stade 2:
La réponse immunitaire diminue la charge virale, Dure deux jours à 20 ans. Grande quantité de virus capturé dans les cellules dendritiques, augmentation du nombre de cellules CD4 infectées et augmentation lente de la charge virale (virus en mode “proviral” dans les cellules avec ADN double brin dans le génome)
Stade 3 - 4 = SIDA
Remontée de la charge virale → Fièvre, amaigrissement, diarrhée et Syndrome de démence, Diminution des lymphocytes T CD4, Infections «opportunistes»: Zona, Candidose, Tuberculose, pneumocystose, toxoplasmose cérébrale, cancer HPV+, Mycobactériose à Mycobactéries atypiques,…
Prévalence HIV-1 > HIV-2 (HIV-2 moins contagieux, surtout Afrique de l’ouest)
mais bcp de mutant de nos jours
Variabilité:
Problème pour élaborer un vaccin
Due aux mutations (fréquentes et multiplication virale élevée) et recombinaison
Traitement =
Inhibiteurs de la transcriptase réverse: Analogues nucléosidiques (ex = Emtricitabine, Ténofovir) OU analogue non nucléosidique (inhibiteur allostérique)
Inhibiteur de protéase (ex = Ritonavir)
inhibiteur de l’intégrase (ex = Raltégravir)
inhibiteur de CCR5 (ex= Maraviroc)
Inhibiteurs de la fusion → Peptide se liant à gp41 après interaction gp120/CD4 (ex = Enfuvirtide)
→ généralement une trithérapie (pour l’instant, traitement ad vitam aeternam, ajd on essaye de se débarrasser avec du virus, il faut booster le virus pour le sortir de sa dormance ET traiter en même temps (travaux ont actuellement lieu))
Prophylaxie =
capote
Chimioprophylaxie =
Pré-exposition → Traitement antiviral préventif chez les personnes à risque (ex. Les hommes qui ont des rapports sexuels avec des hommes)
→ Médicament = TRUVADA (tenofovir + emtricitabine) avec prise continue ou ponctuelle avant et après le rapport sexuel non protégé; efficacité entre 86 et 97%
Post-exposition → Tri-thérapie (tenofovir + emtricitabine + raltégravir) à prendre le plus rapidement possible (endéans les 72h et pendant 28 jours)
Existe des test immunochromatographique (auto-test dans les officines)
ARBOVIRUS
Arbovirus: Arthropod Borne virus, virus de vertébrés transmis par des arthropodes hématophages
Clinique =
Infections inapparentes
Etats fébriles pseudogrippaux
Fièvres hémorragiques (ex. fièvre jaune, dengue)
Atteintes du SNC (encéphalites japonaises, à tiques, West Nile, …)
(Avec les chgmts climatique, on observe une “migration” des vecteurs de ces maladies)

West Nile virus:
ARBOVIRUS , FLAVIVIRIDAE ARN (+), CAPSIDE ICOSAÉDRIQUE ENVELOPPÉE
Présent en Asie, Afrique, Inde, Amérique du Nord, Europe de l’Est et Camargue par l’arrivée d’oiseaux migrateurs sauvages infectés (réservoirs) et de moustiques (Culex) → touche plus les chevaux
Symptômes = fièvre, éruption et 1% atteinte SNC = encéphalite (→ mortalité élevée quand atteinte SN à virus)
Virus de la fièvre jaune
ARBOVIRUS , FLAVIVIRIDAE ARN (+), CAPSIDE ICOSAÉDRIQUE ENVELOPPÉE
Réservoir= singe et moustique (Aedes)
présent en Afrique et Amérique du sud (serait éradicable)
Symptômes =fièvre, hépatonéphrite → syndrome hémorragique et rénal (mortalité jusqu’à 50%)
Prévention = vaccin vivant atténué (protection à vie), démoustification
Dengue
ARBOVIRUS , FLAVIVIRIDAE ARN (+), CAPSIDE ICOSAÉDRIQUE ENVELOPPÉE
4 types
Réservoir = (singe) homme (principalement) et moustique (Aedes)
présents en Afrique, Asie et Amérique (s’étend de plus en plus mais Europe pas encore touchée)
Par an: 70 à 500 millions de personnes sont infectées, 2,1 millions font des formes graves nécessitant une hospitalisation et plus de 20 000 morts
Symptômes = après le paludisme, 2de cause d’états fébriles
Fièvre hémorragique (rare mais grave du coup)
Vaccin = vaccin Dengvaxia = vivant atténué, Indication → personnes âgées de 6 à 45 ans qui ont été infectées par le virus de la dengue dans le passé et qui vivent dans des régions où cette infection est endémique (pas parler cette année car pas optimum)
ZIKA VIRUS
Structure = Flaviviridae
Transmission = via les piqures de moustiques Aedes, mais aussi par transmission sexuelle
Pathologies =
asymptomatiques généralement (fièvre, exanthème, fatigue musculaire et articulaire, …)
Infection congénitale grave entrainant une microencéphalie chez le nouveau né, retard mentaux,…
Complication neurologique post-infectieuse: syndromes de Guillain Barré (paralysie), observé lors d’épidémies.
Prévention et traitement =
Pas de vaccins, ni de traitement spécifique →
Eviter les piqures de moustiques, Abstinence sexuelle pour les personnes vivants dans les zones endémiques lorsque la partenaire a une grossesse.
Virus Hantaan ou de Fièvre hémorragique de Corée
BUNYAVIRIDAE (juste qlqs cas par an mais arrive chez nous aussi)
Virus enveloppé, à ARN de polarité négative
Réservoirs = rongeurs (mulots, campagnols)
Symptômes = néphropathie (insuffisance rénale), fièvre hémorragique
Transmission par voie aérienne (ex urine sur les feuille, quand on “déplace” les feuilles) et contact direct
Virus Ebola
Filoviridae
Réservoirs = chauve-souris, présence en Afrique de l’ouest
Virus ARN (-), enveloppé, « double » capside hélicoïdale (très long virus)
Transmission par les sécrétions corporelles (sécrétion par TOUT le corps)
Incubation de 3 jours à 3 semaine
Maladie de 6-10 jours si létal
Signe majeur: fièvre, douleur abdominale avec diarrhées
VIRUS DE LA RAGE
Famille = Rhabdoviridae
Genre = Lyssavirus
Description: (“forme de suppo”)
Virus enveloppé
Grande sensibilité aux agents physico chimiques de désinfection
Faible résistance dans le milieu extérieur
Génome:
ARN de polarité (-), capside hélicoïdale enveloppée
6 génotypes, génotype 1 = rage classique
Espèces infectées = Tous les mammifères et l’Homme
Vecteurs = chauves souris, renard,…
Tropisme = Nerveux et en particulier le système nerveux central
Transmission = par la salive de l’animal infecté (parfois non symptomatique, surveillance de l’animal pendant 15 jours)
Multiplications: dans les neurones
Symptômes =
Chez les animaux :
Hypersalivation , forme furieuse ou paralytique, l’animal cherche à mordre
Chez l’Homme :
Incubation de 40 jours
Fièvre, fatigue, anxiété, confusion, tremblement
Troubles des fonctions cérébrales supérieures
Atteinte des systèmes respiratoire et gastro intestinal
Agitation, troubles du comportement, hallucinations,
Hyperactivité (rage furieuse) ou une paralysie (rage paralytique flasque), hydrophobie et aérophobie
La mort, inévitable, survient 2 à 10 jours après les premiers symptômes.
Traitements =
Traitement préventif :
Vaccination avec vaccin recombinant ou inactivé (personnes dont l’activité est un facteur de risque d’infection)
Traitement curatif :
Vaccin inactivé pendant la période d’incubation et Ig antirabbiques humaines