BCM 12º
1/187
Earn XP
Description and Tags
mezcla de términos importantes de qca gral (de 10º), biología celular molecular y qca orgánica (de 12º)
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
188 Terms
Configuración electrónica
La manera en la que los electrones están ordenados y distribuidos en los distintos orbitales atómicos

Niveles de energía
representan que tan cerca al núcleo se encuentran los electrones (periodos en la tabla periódica) 1 = más cerca 7 = más lejos
Subniveles de energía
Representan los orbitales que tienen las mismas características dentro de un nivel de energía. (El número de subniveles corresponde al nivel de energía) S P D F
Electrón
una partícula sub-atómica con carga negativa. Crean compuestos (reacciones químicas)
Protón
una partícula sub-atómica con carga positiva. Define que elemento es (da la identidad)
Neutrón
una partícula sub-atómica con carga neutra (igual positivo que negativo) que se encuentra en el núcleo del átomo. Define el tipo de átomo, si es un isótopo.
Átomo
Es la partícula más pequeña de materia que no se puede descomponer químicamente (carga neutra)
Isótopos
Es una variante de un elemento químico en el cual el número de neutrones cambia —sin que cambie el elemento químico—
Electrones de valencia
Los electrones que se encuentran en la capa más externa (la última)
Propiedades químicas
Son las características que se hacen evidentes durante una reacción química
Modelo de Thompson
Los átomos están compuestos por una esfera de carga positiva con electrones (carga negativa) están incrustados en ella
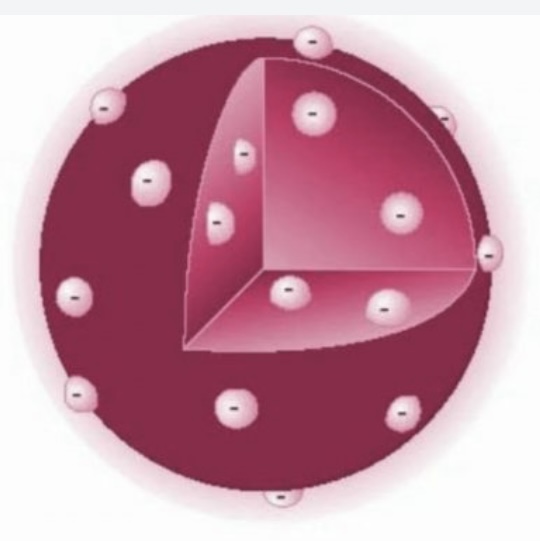
Modelo de Rutherford
Los átomos tienen una zona nuclear con carga positiva con electrones circulando alrededor
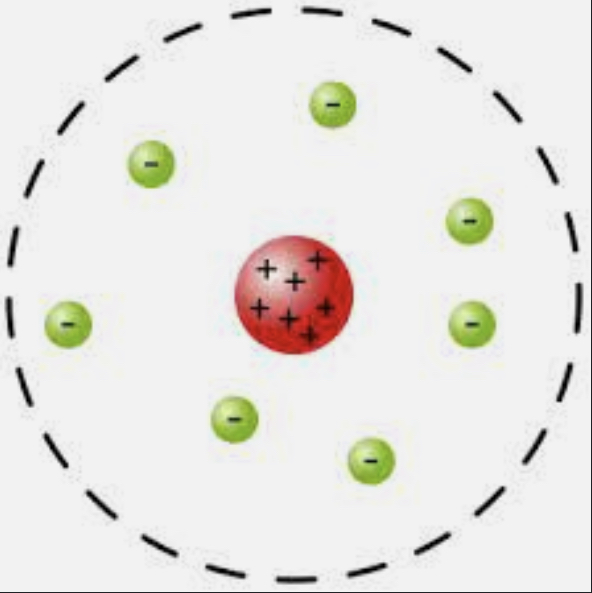
Modelo de Bohr
El átomo tiene un núcleo que continene protones y neutrones mientras que los electrones se encuentran en orbitales y niveles establecidos alrededor del núcleo
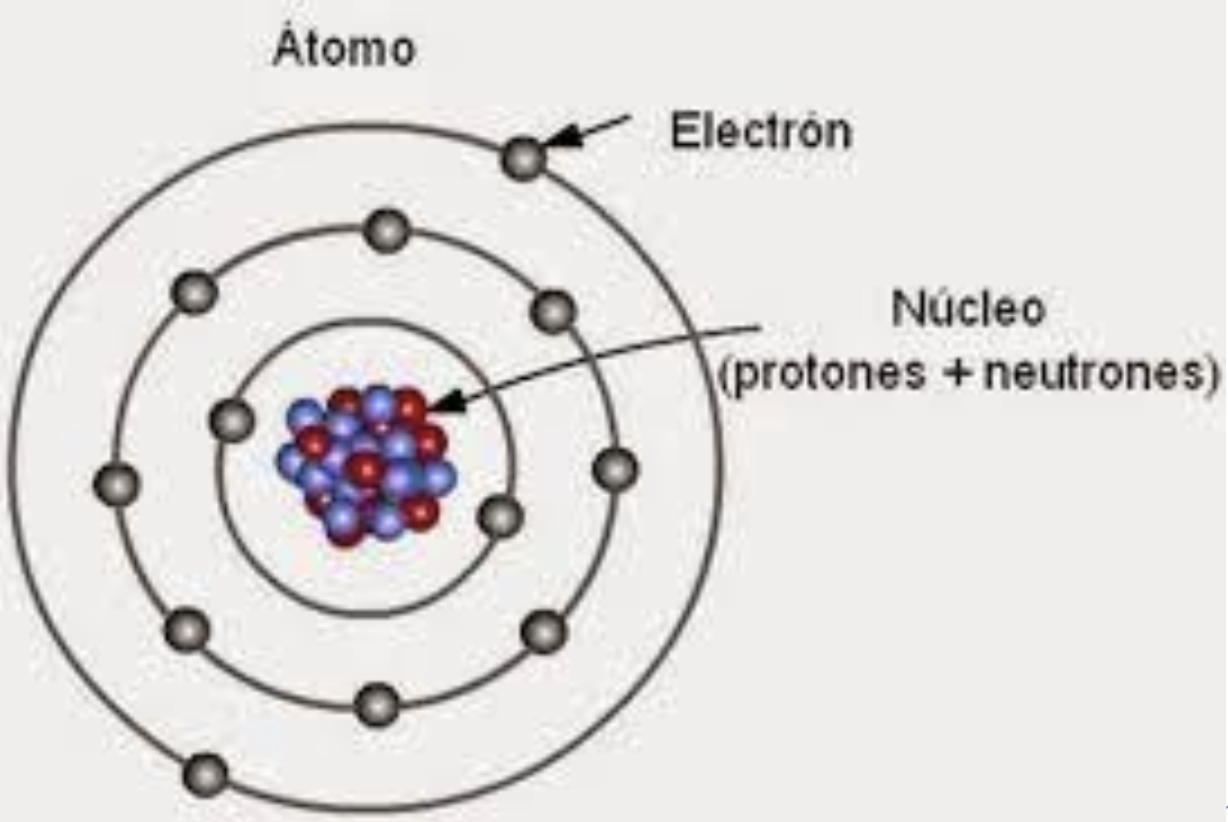
Iones
Son átomos cargados positiva o negativamente
Cationes
Son iones con carga positiva (menos electrones)
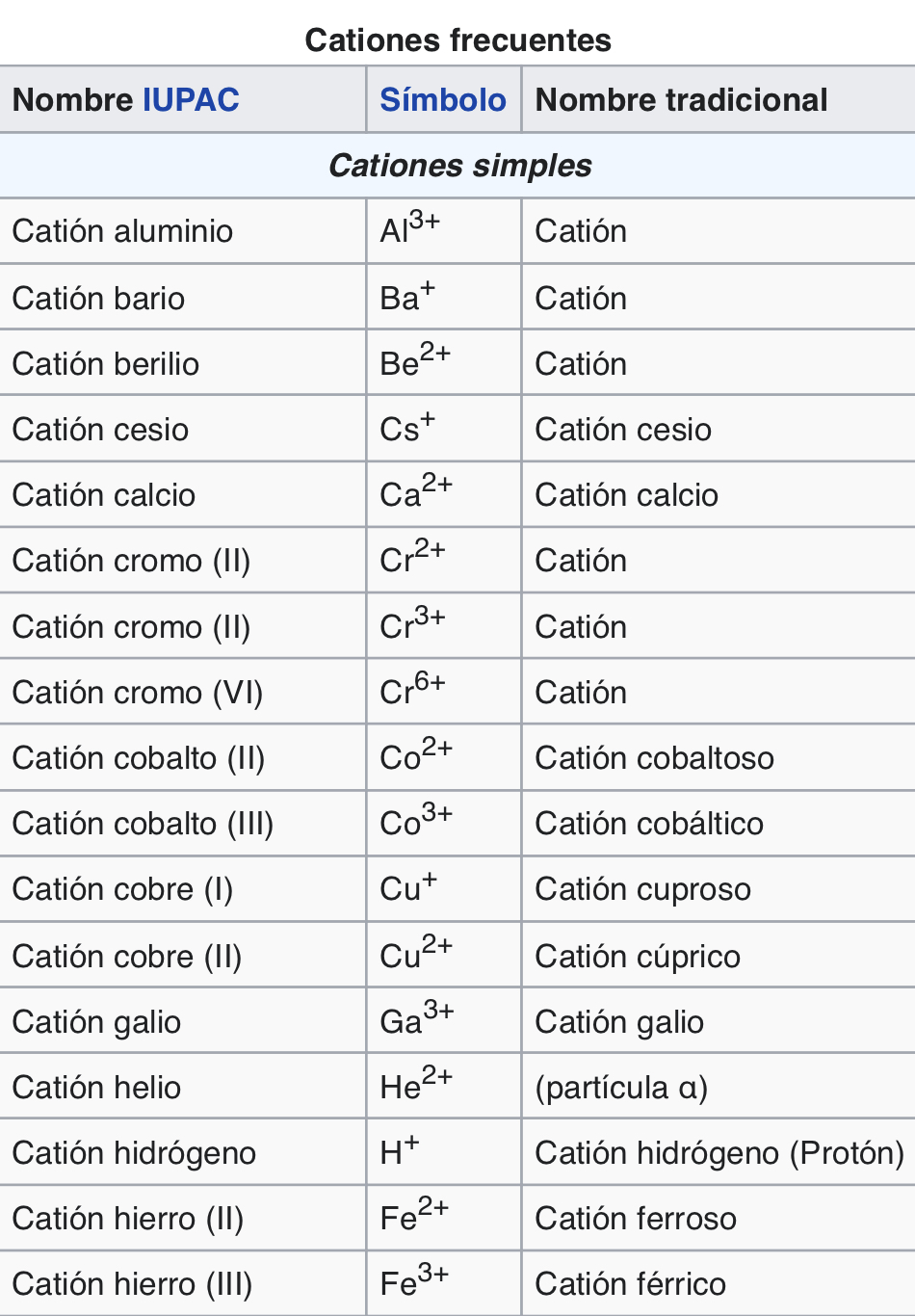
Aniones
Son iones con carga negativa (más electrones)
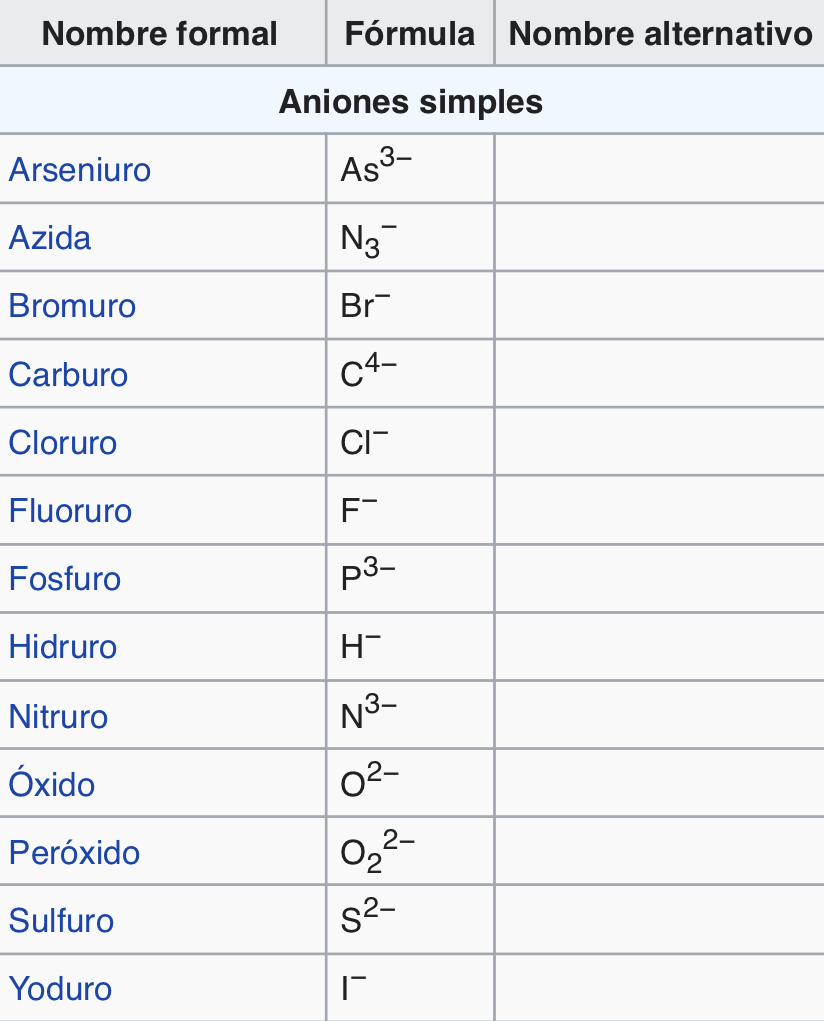
Elementos químicos
sustancias puras ya que la materia está compuesta de un mismo tipo de átomo
Números cuánticos
Definen el comportamiento de los electrones en un átomo. Son 4: N, L, M, Ms
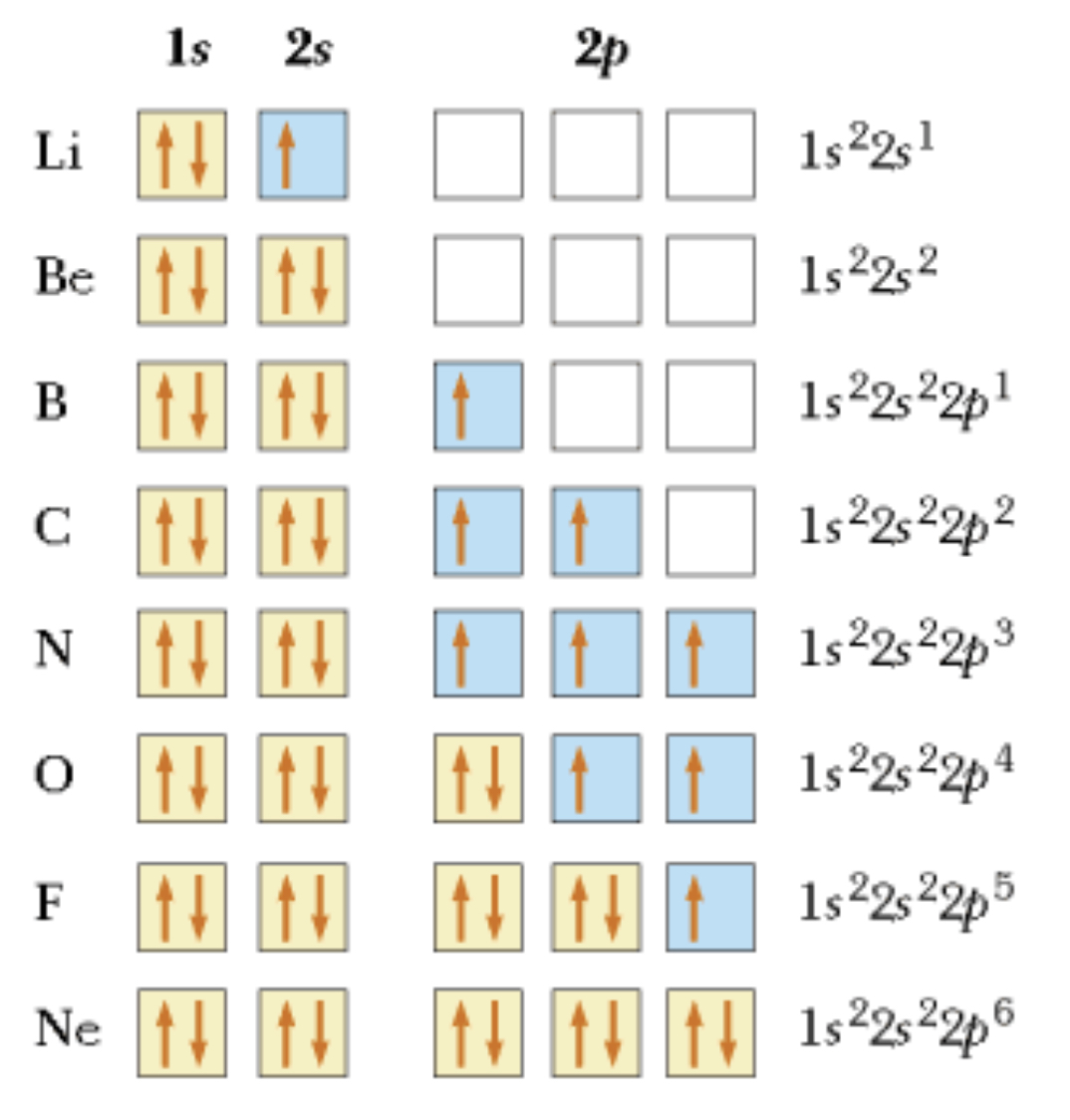
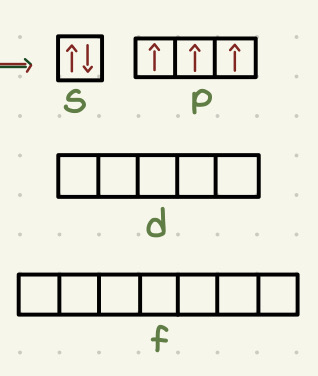
Principio de Aufbau
Un principio que sigue la regla de Hund y representa los orbitales como cajitas (los subniveles se llenan en orden (1s después 2s y so on)
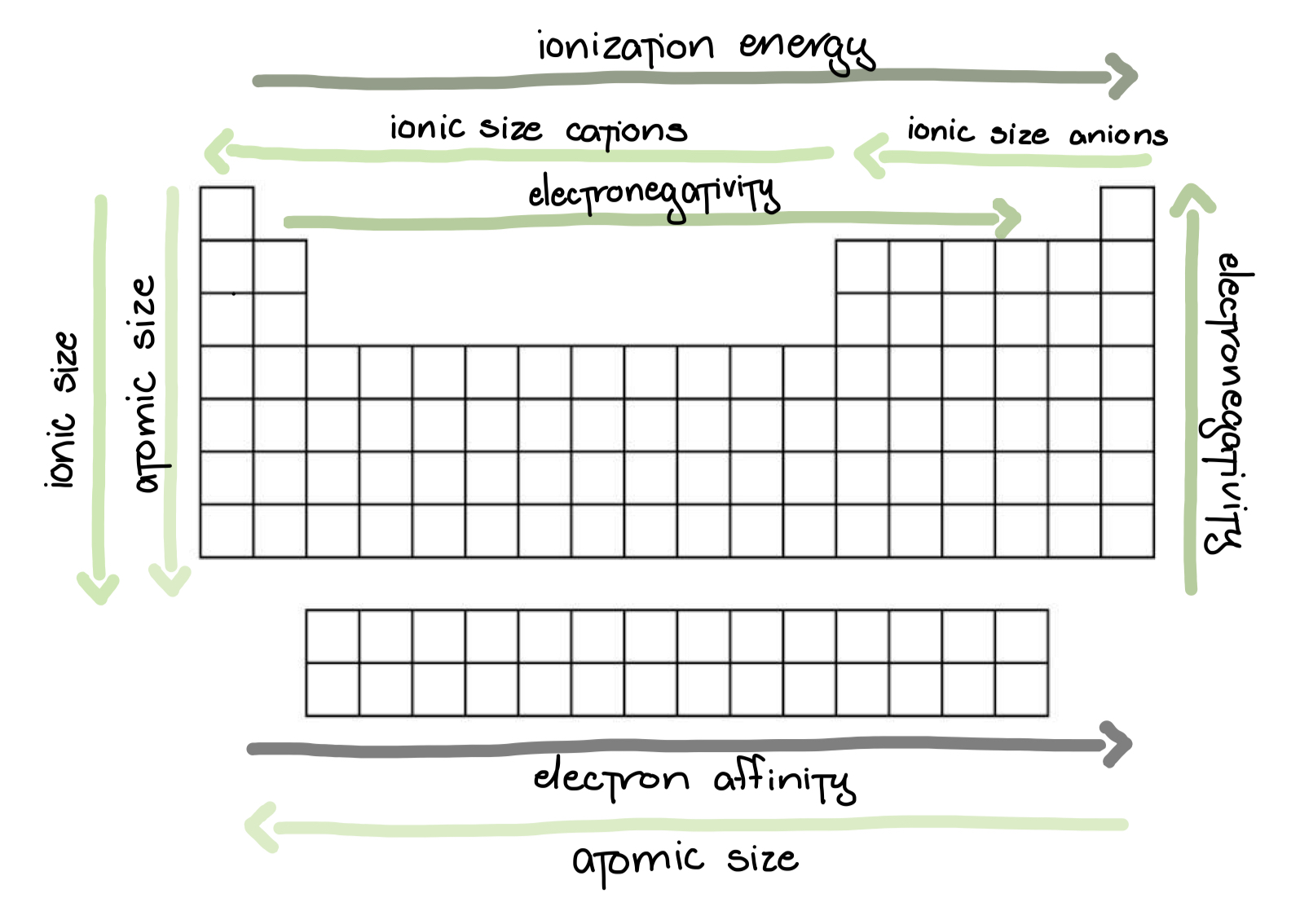
Electronegatividad
La habilidad/la fuerza de un átomo para atraer electrones de otro átomo • Decrease from top to bottom in a group • Increase from left to right in a period
Clases de elementos
• Metales (alkalinos, alkalino-terreos, metales de transición, tierras raras) • Metaloides • No-metales (halogenos (A7), anfígenos (A6), gases nobles)
Periodos/Series
Las líneas horizontales en la tabla periódica. Hay ciertas propiedades que los elementos en cada periodo tienen en común (representan el nivel de energía)

Grupos/Familias
Las líneas verticales en la tabla periódica. Hay ciertas propiedades que los elementos en cada grupo tienen en común (Grupos A & B)

Propiedades físicas
Las propiedades de la materia que se pueden ver y medir sin alterar la estructura atómica, la composición
N (número cuántico)
Representa el nivel de energía (1-7) y se encuentra en la tabla periódica
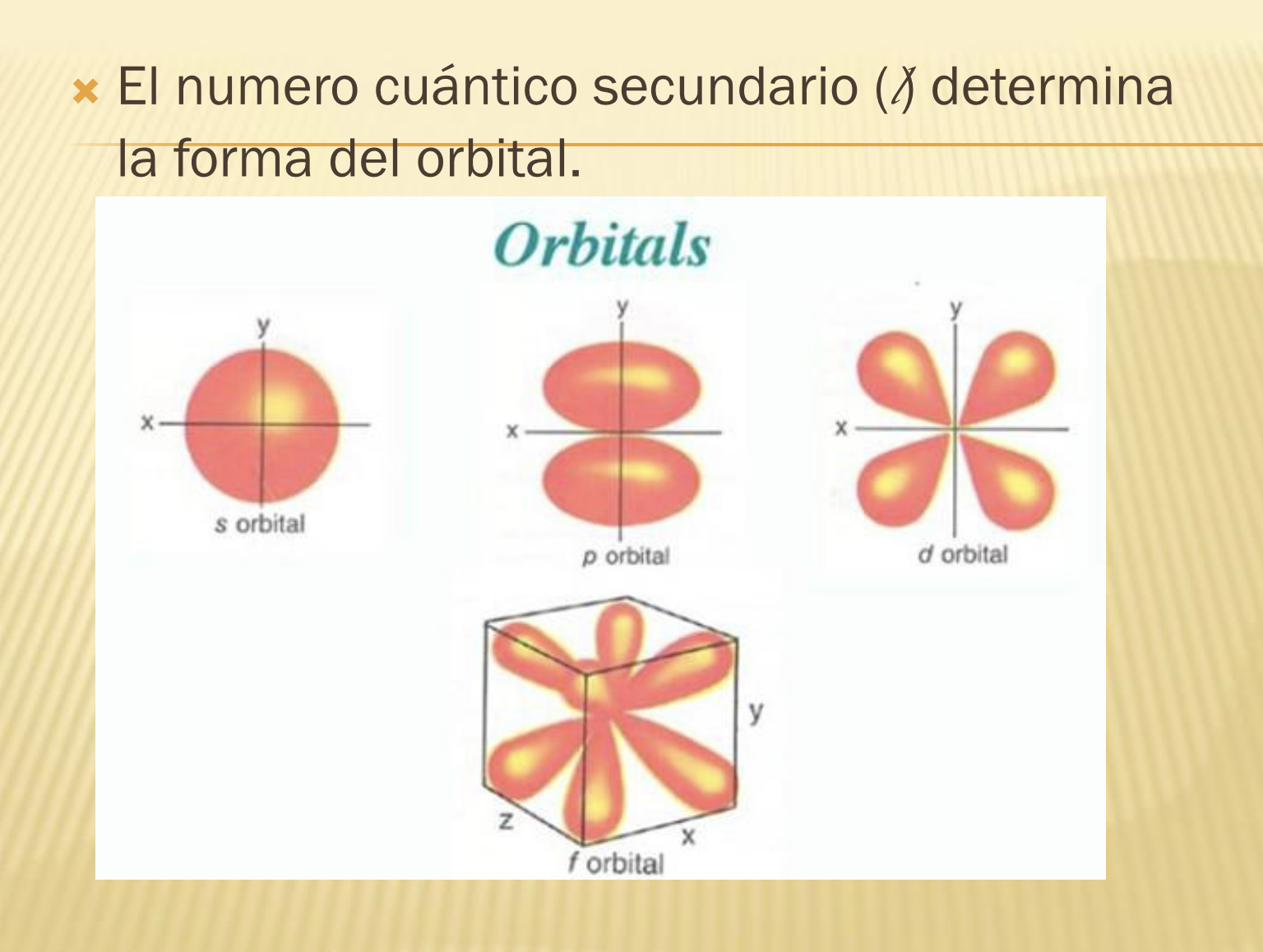
L (número cuántico)
Determina la forma del área en la que estarán los electrones (orbitales)
M (número cuántico)
Determina el sentido/la dirección en la cual están los electrones (X, Y o Z)
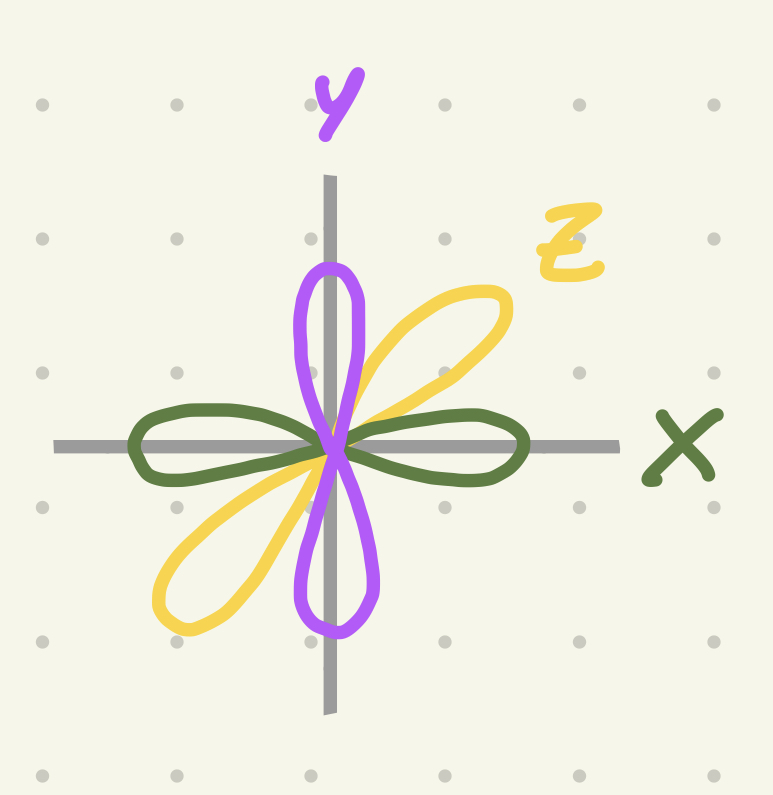
Ms (número cuántico)
Determina el spin/la rotación de los electrones. Si van hacia arriba o hacia abajo

Cómo pueden 2 electrones estar juntos?
Por ser 2 partículas con carga negativa se repelen, pero, al tener spins opuestos pueden convivir relativamente cerca sin crear una explosión
Metaloides
Elementos que tienen características de metales y no-metales
Subnivel S
Tiene 2 electrones = 1 orbital. Forma esférica
Subnivel P
Tiene 6 electrones = 3 orbitales. Forma lobular
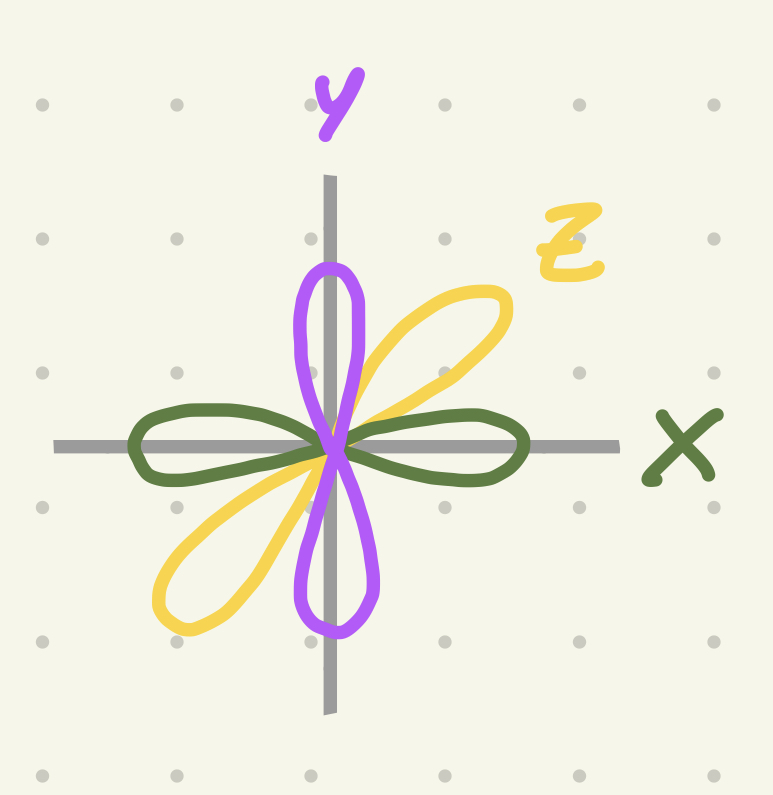
Subnivel D
Tiene 10 electrones = 5 orbitales
Subnivel F
Tiene 14 electrones = 7 orbitales
Enlaces iónicos
Es un enlace químico entre cationes (metales) y aniones (no metales) en los cuales el cation le entrega electrones al anion
Enlaces covalentes
Un enlace químico entre no-metales en los cuales los 2 átomos compartment electrones (formando pares de electrones)
Polaridad
La cantidad de electronegativad ejercida por los átomos en un enlace covalente (electronegatividades iguales = apolaridad) (electronegatvidades distintas = polaridad)
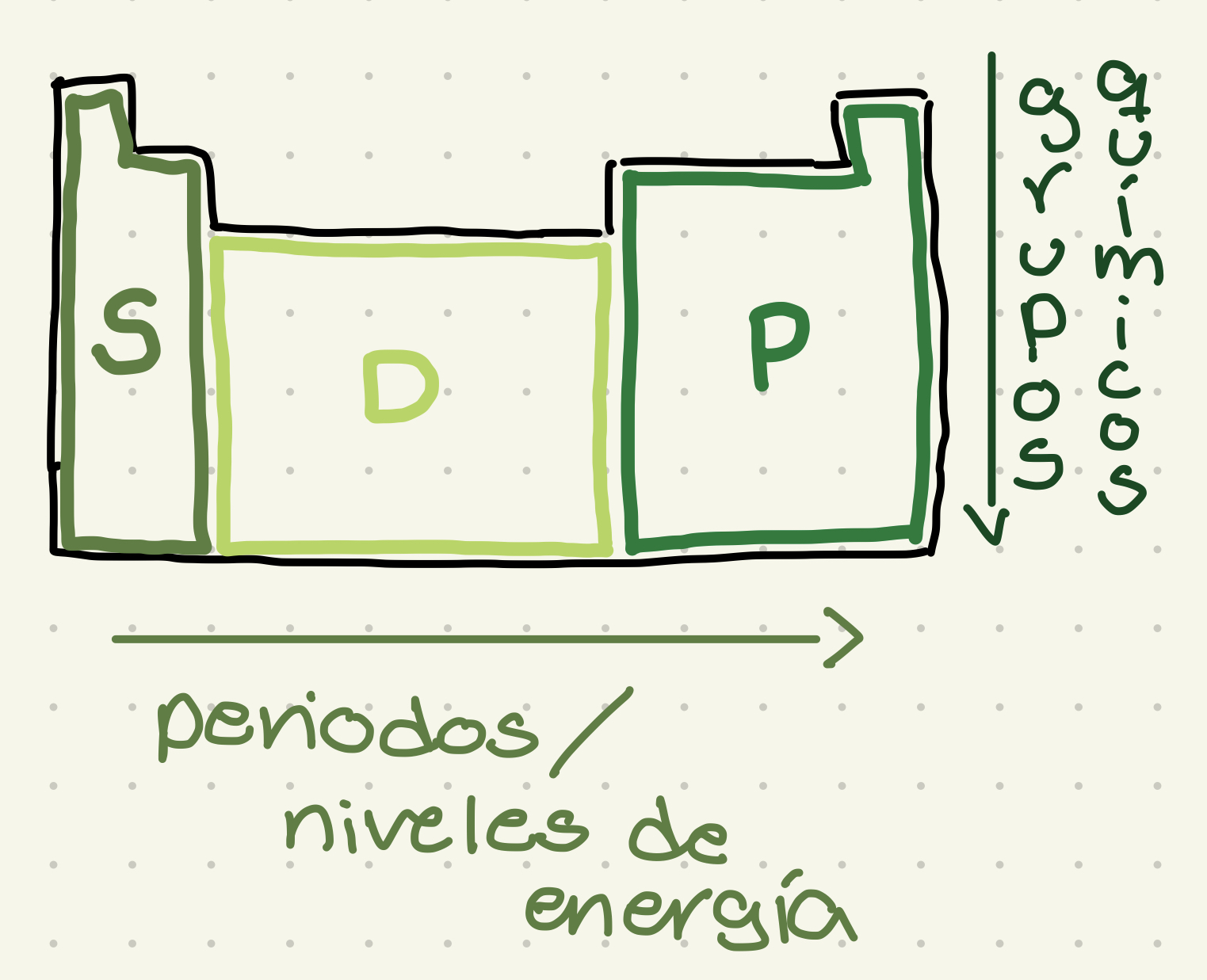
División en la tabla periódica
La tabla periódica se divide en periodos, grupos y el último orbital de la configuración electrónica de los elementos.
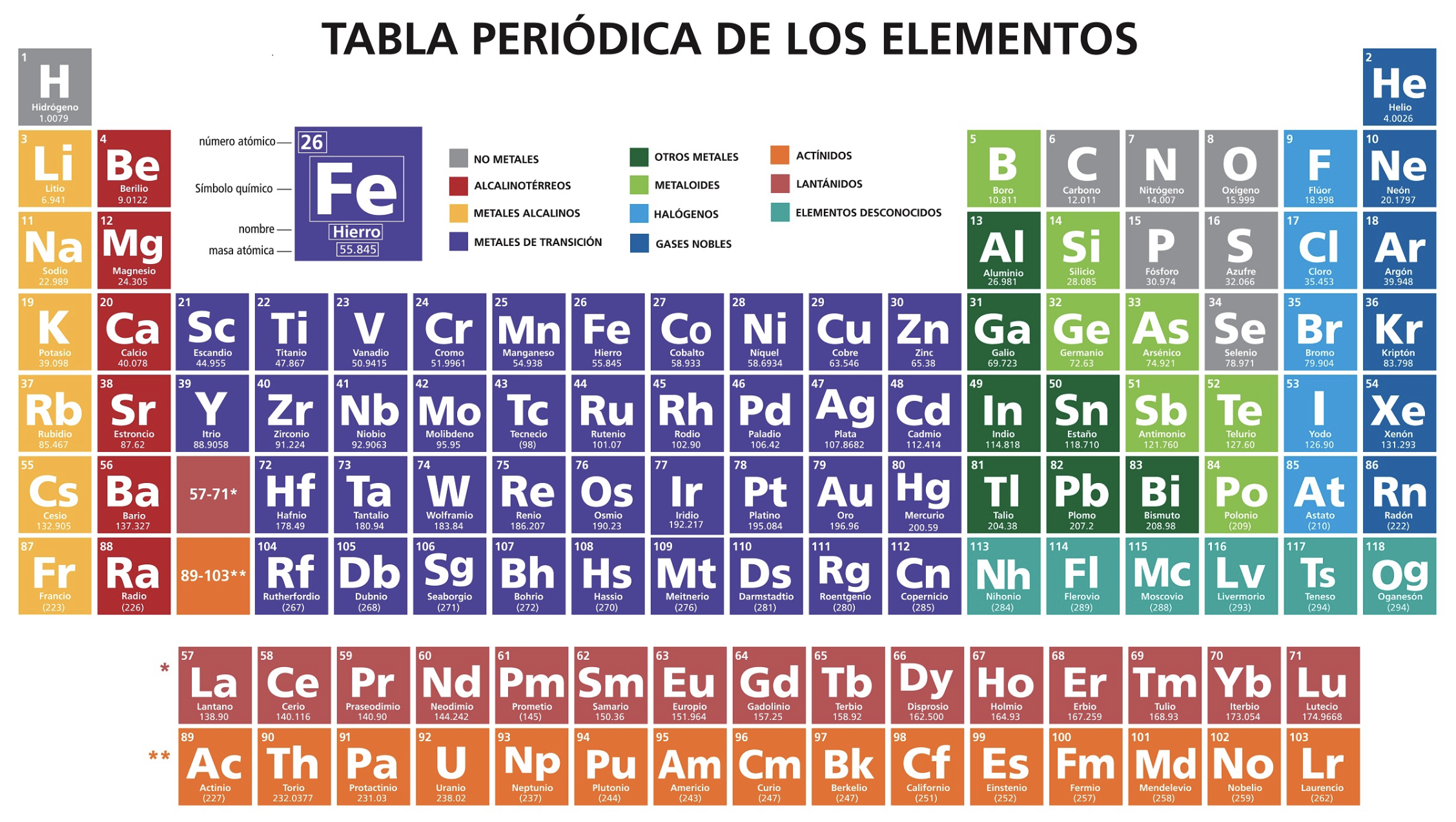
Element squares
The squares in the periodic table. They display: • names • symbols • Atomic number • Atomic mass

Halógenos
Son una clasificación de elementos no metales encontrados en la tabla periódica (del flúor al astato)
Espectro electromagnético
Es un área/región en el cosmos en la cual se encuentra concentrada la radiación electromagnética
Rayos X
Uno de los subniveles de la radiación electromagnética.
Estructura de Lewis
Es una manera visual de representar los electrones de valencia (últimos electrones) de un átomo y los enlaces iónicos y covalentes
Principio de Heisenberg (incertidumbre)
Si lo sabemos todo sobre dónde se encuentra una partícula (la incertidumbre de posición es pequeña), no sabemos nada sobre su momento (la incertidumbre de momento es grande), y viceversa. (Se puede tener cierto conocimiento del recorrido de las partículas en una onda pero no conocimiento exacto de la posición en un momento indicado)
Teoría Cuántica
la teoría que describe el comportamiento de la materia, la radiación y todas sus interacciones a nivel microscópico. Describe la dualidad onda-partícula de los electrones
Fotones
Las partículas encontradas en ondas de radiación de luz visible
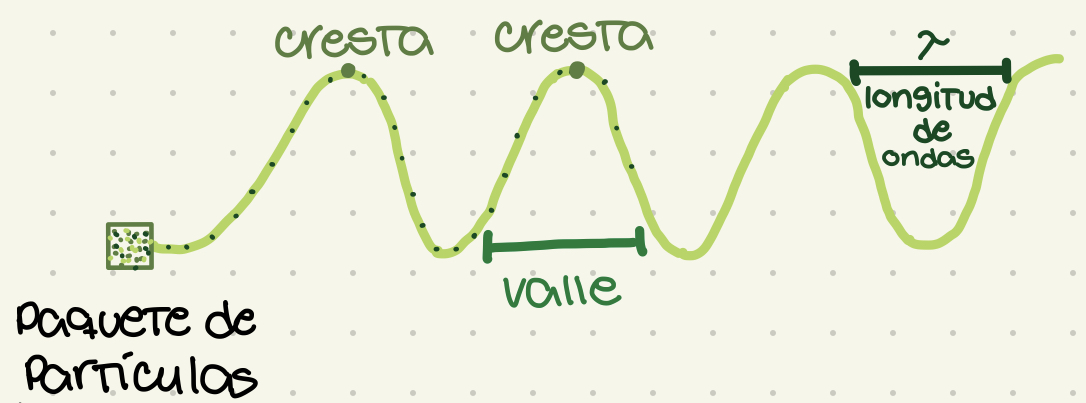
Longitud de onda
Distancia entre cresta y cresta. Representado por lambda (letra griega: λ). Define la violencia y el sub-tipo de radiación.

Hibridación
Es la acción entre átomos que se solapan (montan) y se deslizan entre ellos creando enlaces por medio de sus electrones (crean fricción para crear enlaces)
Salto electrónico
Cuando los electrones absorben tanta energía (radiación electromagnética) que necesitan saltar a un orbital con mayor capacidad de energía y viceversa. (De nivel a nivel)
Radiación electromagnética
Tipo de energía que carga a los electrones y causa o disminuye la excitación de los electrones (lo que causa el salto electrónico)(se absorbe y se emite) (cada elemento puede absorber más o menos dependiendo de las propiedades químicas)

Aleación
Enlace entre elementos metálicos. Ningún elemento acepta la electrones creando así el modelo del mar electrónico.
1ra ley de termodinámica
Conservación de la energía: no se crea ni se destruye, simplemente se transforma o transita
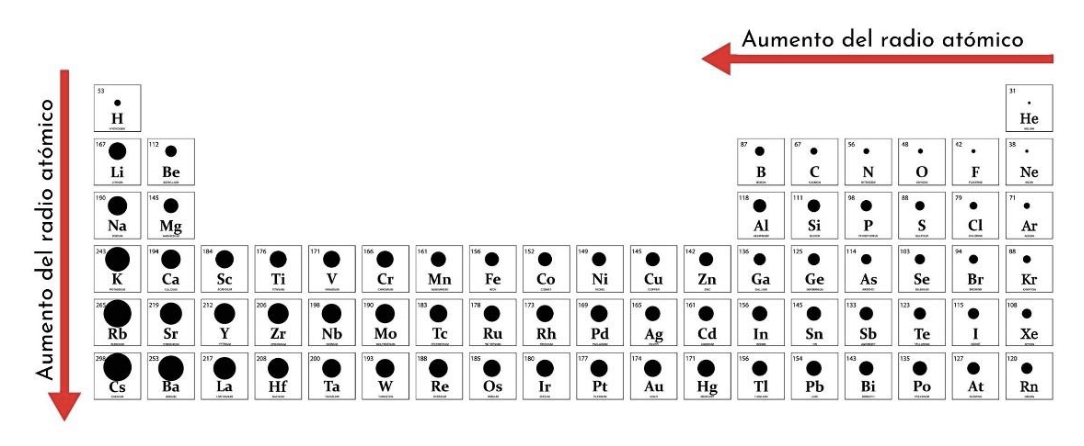
Tendencia de radio atómico
Aumenta de derecha a izquierda y de arriba hacia abajo
Radio atómico
Distancia que existe entre el núcleo y la capa de valencia (la más externa). El tamaño del átomo.

Zonas del espectro electromagnético
7 zonas que van de izquierda a derecha, de menor a mayor intensidad (de menos a más violencia) en el sub-tipo de radiación
Hormesis
alta exposición a un tratamiento (puede ser con radiación) por un instante para curar/eliminar cualquier enfermedad (debe tenerbalance)
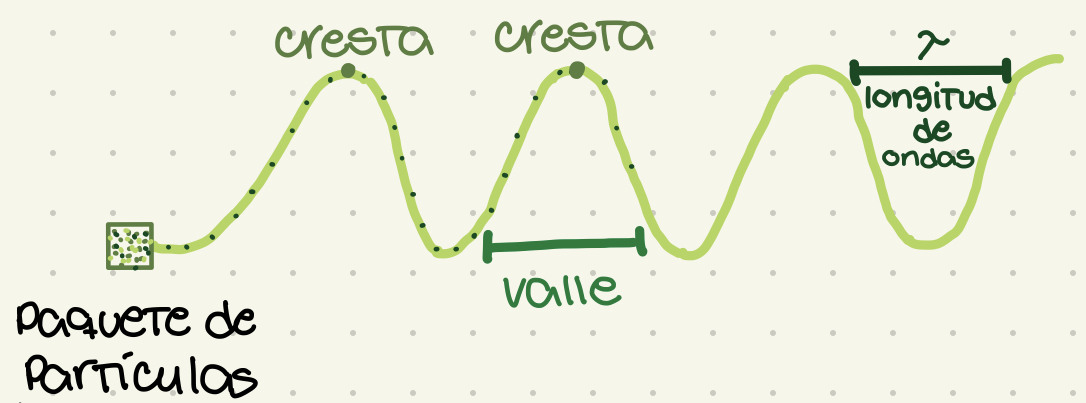
Ondas
La manifestación de la radiación electromagnética. Un paquete de partículas moviéndose en trayectoria de ondas.
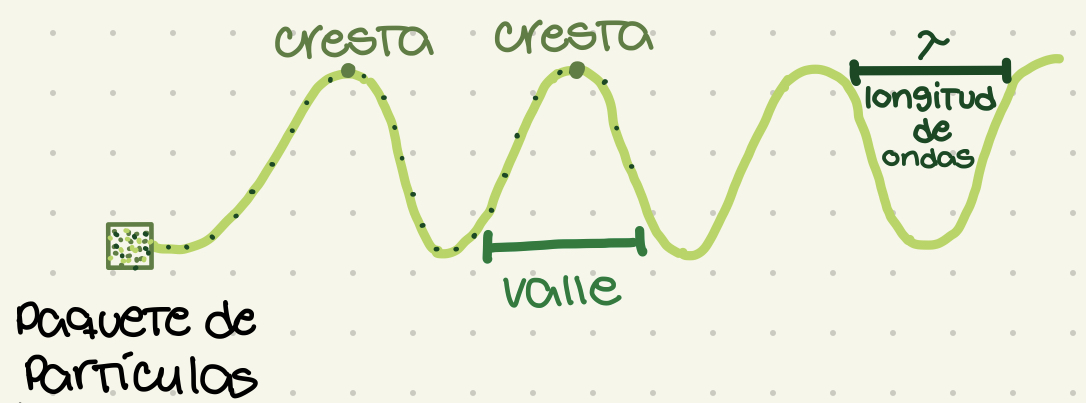
Cresta
El punto más alto de la onda
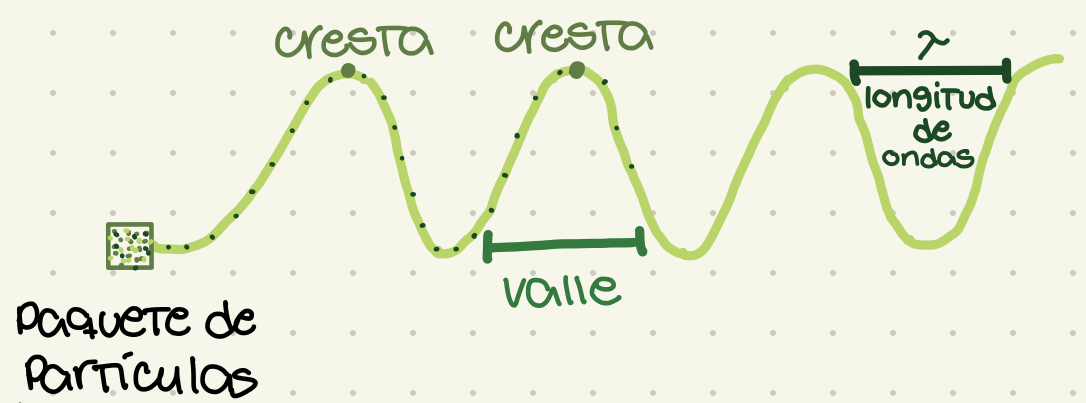
Valle
El punto más bajo de la onda. La base de la onda

Mayor longitud de onda
Menos intensidad en la radiación

Menor longitud de onda
Mayor intensidad en la radiación
Fotones
Las partículas que se encuentran en las ondas de luz visible
Efecto fotoeléctrico
También conocido como fotoemisión. La expulsión de electrones cuando la luz brilla en un metal
Conexión entre modelo de Bohr y modelo de Schrodinger
La dualidad onda-partícula.
Dualidad onda-partícula
Base de la teoría cuántica. Los electrones se pueden mover como ondas
Modelo de mar electrónico
El rebote/flujo continuo de los electrones de átomo en átomo en una aleación
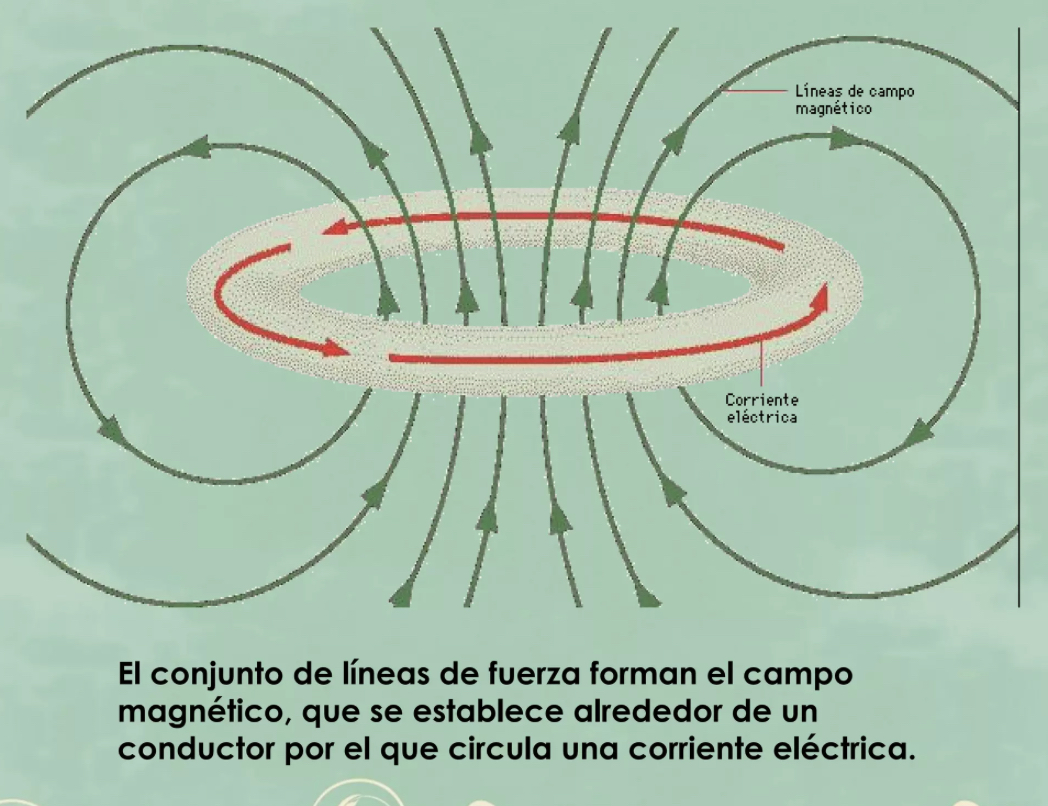
Campo electromagnético
una combinación de campos de fuerza eléctricos y magnéticos invisibles. (Cuando hay corriente en un campo eléctrico la magnitud del campo magnético cambia con el consumo de poder, la fuerza del campo eléctrico quedará igual)
Conductividad eléctrica
Habilidad de la materia para permitir el flujo de la corriente eléctrica a través de sus partículas.
Aniones poliatómicos
una molécula que ha sido ionizada al ganar o perder electrones. (e.g. OH-)
Números cuánticos
Indican las características del comportamiento de e- en los átomos.
Óxidos metálicos
Enlace entre un metal + oxígeno (Solo se usa el # de átomos del oxígeno) 1- mono, 2- bi/di, 3- tri, 4- tetra, 5- penta, 6- hexa, 7- hepta, 8- octa
Campo magnético
tienen su origen en las corrientes eléctricas: una corriente más fuerte resulta en un campo más fuerte.
Campo eléctrico
tiene su origen en diferencias de voltaje: entre más elevado sea el voltaje, más fuerte será el campo que resulta. (Existe aunque no hay corriente)
Cómo se lee una fórmula química?
Derecha a izquierda
Hidróxidos/Bases/Álcalis
Enlace entre metal + OH (hidróxido) OH siempre tendrá valencia de -1 2- bi/di, 3- tri, 4- tetra, 5- penta, 6- hexa, 7- hepta, 8- octa
Anidridos
Enlace entre no metales + oxígeno (Se mencionan ambos # de átomos) 1- mono, 2- bi/di, 3- tri, 4- tetra, 5- penta, 6- hexa, 7- hepta, 8- octa
Ácidos hidrácidos
H + no metal (grupo A6/A7) “Ácido” + raíz del no metal + “hídrico”
Sales binarias
Metal + no metal Raíz no metal + “uro” + de metal
Raíz del redox
Reducir (red), oxidar (ox)
¿A qué se debe la raíz del redox?
Porque en toda reacción química hay un elemento que se reduce y otro que se oxida, el redox mide la estabilidad y por ende el balance entre la reducción y la oxidación
¿Qué mide el redox?
mide la estabilidad de un enlace qxco
¿Cuál es la fórmula del redox?
Nivel 1 • Nivel 2 (left) - Nivel 1 • Nivel 2 (right) = 0 (should be)
¿ Cuántos niveles son al calcular redox?
3
Nivel 1 (redox)
El número de átomos en la fórmula qxca
Nivel 2 (redox)
Números de valencia
¿Cómo se determina el signo de la valencia?
Los metales son “+“ y los no metales “-” (el que está más a la derecha es “-”)
Nivel 3 (redox)
La fórmula en la que se determina la estabilidad
Maneras de encontrar la valencia
Cruce de valencia
Con la tabla periódica
Ácidos oxácidos
H + no metal + O Valencia 1 = acido + (“hipo” + raíz no metal + “oso”) Valencia 2 = acido + (raíz no metal + “oso”) Valencia 3 = acido + (raíz no metal + “ico”) Valencia 4+ = acido + (“hiper” + raíz no metal + “ico”)
Valencia de H
+1
Valencia de Oxígeno
-2 (almost always)
uma
(Unidad de masa atómica) promedio de isótopos de un elemento
Configuración geométrica espacial
Disposición tridimensional de una molécula (define si es polar o no polar)
Regla de Hund
Los orbitales se llenan de manera estable (tienen que tener todos 1 electrón (hacia arriba) antes de tener un segundo electrón (hacia abajo)
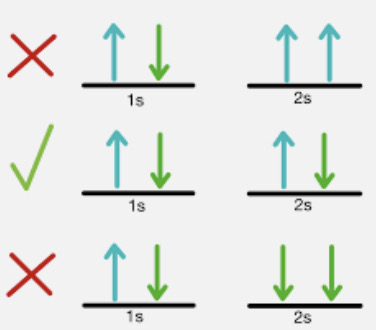
Regla de Pauli
Electrones deben tener spins opuestos, si tienen spins iguales no pueden ocupar el mismo estado cuántico
Ion poliatómico
Iones que tienen más de 1 átomo (se usa nomenclatura de las sales ternarias)
Fuerzas intermoleculares
Interacciones de carácter electroestático por las cuales se mantienen unidas las moléculas de enlaces covalentes
Fuerzas de Van der Waals
• Fuerzas Keesom (dipolo-dipolo)
• Fuerzas Debye (dipolo-inducido)
• Fuerzas de dispersión de London (dipolo instantáneo-inducido)
Fuerzas Keesom
Las fuerzas que unen 2+ moléculas polares
Fuerzas Debye
Las fuerzas que unen 2+ moléculas no-polares