Bioquimica I - Marks (Cap 19) y Meisenberg (Cap 27) Digestion y transporte de lipidos
1/93
Earn XP
Description and Tags
funciones
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
94 Terms
Triacilgliceroles
-Son las grasas más importantes de la dieta
-De almacenamiento
Estructura:Tres ácidos grasos esterificados (enlace éster con diferentes alcoholes) con un glicerol (alcohol)
Distincion entre lipidos
En los triacilgliceroles, las diferencias vienen dadas por los tipos de ácidos grasos que contiene la molécula.
En cambio los fosfolípidos difieren, tanto por los ácidos grasos como por la fracción polar de la molécula.
Los ácidos grasos se distinguen unos de otros por el número de carbonos de la cadena y por la presencia o no de dobles ligaduras entre ellos. Los ácidos grasos que no contienen dobles ligaduras (saturados) son flexibles y poco fluidos, por el contrario, los insaturados, son rígidos y más fluidos.
Acidos grasos cis y trans
La mayoria de los acidso grasos naturales estan en configuracion cis
Los dobles enlaces con configuracion cis producen desviacion de la cadena
Los acidos grasos trans estan relacionados con niveles altos de LDL (el que hace mas daños)
Característica común de lípidos
Insolubles en agua y solubles en solventes organicos
Acidos Grasos
Saturados: Enlaces simples,
Insaturados: Enlaces dobles
Lipidos de membrana
Fosfolípidos:
Glicerofosfolipidos (Glicerol, 2 Acido Graso, PO4 y alcohol): Anfipáticas
Esfingolipidos (Esfingolisina. 1 Acido graso, PO4 y Colina)
Glycolipidos
Esfingolipidos (Espingolisina, Acido graso y Mono o oligosacarido)
Lecitina (fosfatidilcolina)
Es el más común de los fosfolípidos
Contiene sal de amonio cuaternaria que le confiere su carácter polar, unida a un residuo fosfórico mediante un enlace éster.
Tiene un esqueleto de colesterol y ácidos grasos que forman su porción polar (tienen una base nitrogenada: la colina)
Lipidos estructurales
Fosfolipidos
Esfingolipidos
Colesterol
Glicerofosfolípidos
Derivados del acido fosfatidico = diacil glicerol-3-fosfato
En los glucerofosfolipidos se esterifica el grupo fosfato con el grupo hidroxilo en diferentes alcoholes
Ej: Serina - > Fosfatidilserina, Colina → fosfatidil colina
Esteroides
Derivados del colesterol:
-Cortisol
-Testosterona
-Ácido taurocótico: es un ácido biliar conjugado que se forma al unir ácido cólico con taurina. Es un componente principal de la bilis de animales carnívoros y mamíferos, donde actúa como un detergente natural para ayudar a la emulsificación y absorción de las grasas.
Colesterol
Principal esterol de los tejidos animales
Lipido estructural de la membrana plasmatica de las celulas eucariotas,, modula su fluidez
Precursos de acidos biliares y hormonas esteroides
Estructura 4 anillos, 3 con 6 C y 1 con 5C, Nucleo plano y rigido
Anfipatico: Cabeza polar (OH del c3) y un cuerpo hidrocarburano apolar
Esfingolipidos
Característica distintiva: Esfingosina
Estructura: Esqueleto de esfingosina unido por un enlace amida con un acido graso largo
Funciones de Lipidos
•Almacenamiento de energía alterna: Triacilgliceroles en tejido adiposo
•Componentes estructural de membranas celulares: Fosfolípidos, esfingolípidos, colesterol
•Agentes emulsionantes
Control: Hormonal, Mensajeros intracelulares, esteroides, prostaglandinas
Tranpsorte: Forman estructuras como lipoproteína de transporte de colesterol y triacilglicéridos
Defensa: Aislante térmico y amortiguador mecánico.
Nutricional: Fuente de ácidos grasos esenciales y proteínas liposolubles
Los lipidos forman polimeros?
Los lípidos no forman polímeros. Sin embargo, están estructurados por dos tipos de moléculas simples: ácidos grasos, que prácticamente son las moléculas de lípidos más sencillas, y un alcohol, unidos por enlaces éster.
Donde ocurre la digestión de los lípidos
Cadena corta
Boca (lipasa lingual, detras de la lengua)
Estómago (lipasa gástrica)
Cadena larga?
Intestino (emulsionadas por sales biliares) ← Principal
La ruta principal para la digestión de los triacilgliceroles involucra la:
Hidrólisis a ácidos grasos y 2 monoacilgliceroles en el lumen intestinal
La ruta de la digestión de los triacilgliceroles depende de:
Longitud de la cadena de ácido grasos
Los principales lípidos plasmáticos:
Triglicéridos, colesterol, fosfolípidos y ácidos grasos libres.
V o F: Los tejidos no dependen exclusivamente de los lípidos como fuente de energía, a diferencia de la glucosa
V
Cómo los ácidos grasos no esterificados (libres) son transportados?
Son transportados unidos covalentemente a albúmina serica
Los triglicéridos, los fosfolípidos y los ésteres de colesterol forman agregados no covalentes con proteínas llamados:
Lipoproteinas
Las cuatro vías principales de transporte de los lípidos en el cuerpo son:
Ácidos grasos libres → desde el tejido adiposo hacia otros tejidos, unidos a la albúmina sérica.
Lípidos de los alimentos → desde el intestino a otros tejidos (quilomicrones).
Lípidos de síntesis endógena → desde el hígado (VLDL). hasta otros tejidos
Transporte inverso de colesterol → desde tejidos extrahepáticos hacia el hígado (HDL).
El transporte inverso de colesterol es necesario porque:
El colesterol no se puede degradar a nivel local y de ser transportado hasta el higado para su excresion biliar.
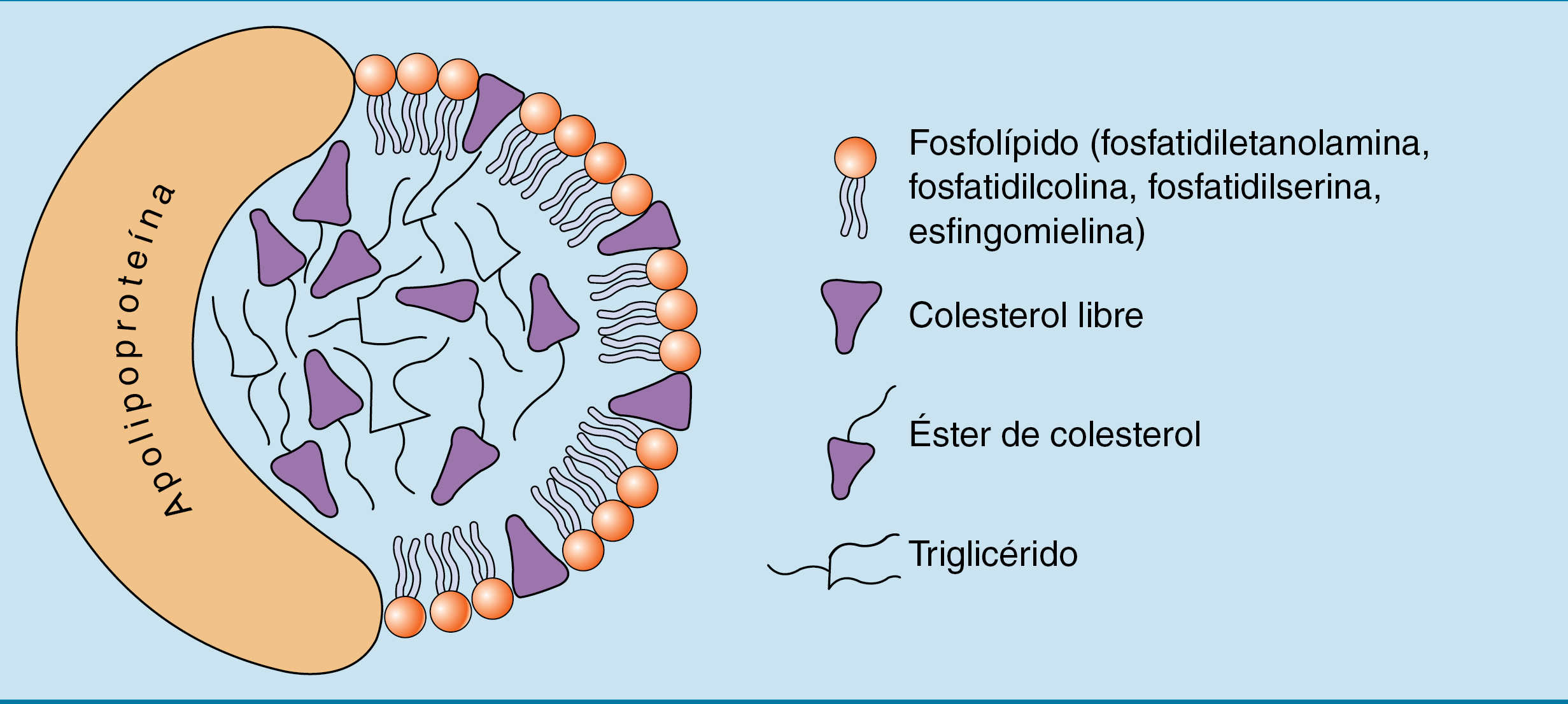
Lipoproteínas plasmáticas (estructura)
Núcleo hidrofóbico (triglicéridos y ésteres de colesterol).
Superficie anfipática (fosfolípidos y apolipoproteínas).
Modificación de las lipoproteínas en la circulación
Las lipoproteínas son estructuras dinámicas cuya composición no permanece constante mientras circulan por el torrente sanguíneo.
En su tránsito, intercambian lípidos y apolipoproteínas entre sí, lo que permite la adaptación a las necesidades metabólicas de los tejidos.
Además, pueden captar lípidos desde las células o entregarles parte de su contenido lipídico.
Las enzimas plasmáticas, como la lipoproteína lipasa (LPL) o la lecitina-colesterol aciltransferasa (LCAT), procesan los lípidos directamente sobre la superficie de las lipoproteínas, modificando su tamaño y densidad.
Finalmente, muchas lipoproteínas son destruidas y captadas por endocitosis mediada por receptores, ingresando a las células donde sus componentes son hidrolizados en los lisosomas, liberando ácidos grasos, colesterol y aminoácidos que el organismo reutiliza.
Electroforesis
Permite separarlas por su movilidad eléctrica, junto con otras proteínas plasmáticas.
En condiciones de ayuno se observan tres fracciones principales:
α (alfa) → corresponde a las HDL.
β (beta) → corresponde a las LDL.
pre-β (pre-beta) → corresponde a las VLDL.
Los quilomicrones, grandes y menos densos, no migran en este método, ya que están presentes solo tras una comida grasa.
Centrifugación por gradiente de densidad
Separa las lipoproteínas según su relación proteínas/lípidos.
Cuanto mayor es el contenido proteico, mayor es la densidad de la partícula.
En orden creciente de densidad:
Quilomicrones → VLDL → IDL → LDL → HDL.
Quilomicrones
Origen: Intestino
Función: Transporte de triglicéridos dietarios
Lipoproteínas de muy baja densidad (VLDL)
Origen: Higado
Función: Transporte de triglicéridos endógenos
-Las VLDL se sintetizan en el retículo endoplásmico (RE) y el aparato de Golgi con ayuda de una proteína microsomal de transferencia de triglicéridos, y se liberan mediante exocitosis. Los sinusoides hepáticos tienen un endotelio fenestrado que permite el paso de lipoproteínas hacia la sangre de los sinusoides.
Proteínas de densidad intermedia (IDL)
Origen: Degradación de VLDL
Función: Intermediarias en el metabolismo de VLDL
Lipoproteínas de baja densidad (LDL)
Origen: Derivadas de IDL
Función: Transporte de colesterol a tejidos
Lipoproteínas de alta densidad (HDL)
Origen: Hígado, intestino
Función: Transporte reverso del colesterol
Procentaje de trigliceridos en condiciones de ayuno:
Los triglicéridos plasmáticos provienen principalmente de VLDL.
Aproximadamente el 70% del colesterol total se encuentra en LDL.
Por ello, un aumento en los triglicéridos suele reflejar un exceso de VLDL, mientras que un aumento en el colesterol indica un exceso de LDL.
Cada lipoproteína contiene apolipoproteínas específicas que determinan su función y destino metabólico:
ApoB-48 → exclusiva de los quilomicrones.
ApoB-100 → presente en VLDL y LDL.
Apolipoproteínas A (ApoA-I, ApoA-II) → características de las HDL.
Solo las ApoB son componentes estructurales fijos. Las demás pueden transferirse entre partículas lipoproteicas.
Ordena las lipoproteínas según su densidad de menor a mayor.
Quilomicrones → VLDL → IDL → LDL → HDL.
¿Cuál es la relación entre la densidad y el contenido de proteínas en las lipoproteínas?
: A mayor contenido proteico, mayor densidad.
¿Qué apolipoproteína caracteriza a las VLDL y LDL?
ApoB-48.
¿Qué apolipoproteínas predominan en las HDL?
Apolipoproteínas A (A-I, A-II).
¿Qué funciones cumplen las apolipoproteínas?
Regulan enzimas que metabolizan lípidos.
Facilitan el intercambio de lípidos entre lipoproteínas.
Se unen a receptores celulares para endocitosis o intercambio lipídico.
Metabolismo de los quilomicrones
Se forman en el intestino tras una comida grasa y transportan los triglicéridos exógenos.
Contienen apoB-48, colesterol y fosfolipidos y algunas apolipoproteínas A, pero en la sangre adquieren de las HDL las apoC y apoE.
La LPL, activada por apoC-II e inhibida por apoC-III, hidroliza el 80–90% de los triglicéridos en músculo y tejido adiposo.
Durante este proceso, parte de los fosfolípidos y apolipoproteínas de superficie se transfieren a las HDL mediante una proteína de transferencia especializada.
El resultado es un remanente de quilomicrón, más pequeño y denso, que es reconocido por los receptores hepáticos (apoE-dependientes) y posteriormente degradado en el hígado.
El ciclo completo, desde la secreción intestinal hasta la captación hepática, dura menos de una hora
¿Cuál es la principal función de la LPL (lipoproteína lipasa)?
Hidrolizar los triglicéridos de los quilomicrones y las VLDL, liberando ácidos grasos y glicerol.
-Posiblemente facilita la captación hepática de los restos de quilomicrones y la transferencia de ésteres de colesterol desde las HDL hasta el hígado
¿Qué apolipoproteína activa la LPL y cuál la inhibe?
ApoC-II la activa y ApoC-III la inhibe.
¿Qué sucede con los restos de quilomicrones?
Son captados por el hígado mediante receptores que reconocen la ApoE, y degradados en los lisosomas.
¿Qué lipoproteína transporta la mayor parte de los triglicéridos plasmáticos en ayunas?
Las VLDL.
¿Qué lipoproteína transporta la mayor parte del colesterol total plasmático?
Las LDL (aproximadamente el 70%).
¿Qué efecto tienen las mutaciones que reducen la ApoC-III?
Disminuyen triglicéridos y LDL, aumentan HDL y reducen el riesgo de aterosclerosis.
Apoliproteinas
Las apolipoproteínas son proteínas especializadas que se encuentran unidas a los lípidos dentro de las lipoproteínas plasmáticas (como los quilomicrones, VLDL, LDL y HDL).
Desempeñan funciones estructurales, enzimáticas y reguladoras esenciales para el transporte y metabolismo de los lípidos en el organismo.
Síntesis y liberación de VLDL
El hígado sintetiza diariamente entre 25 y 50 g de triglicéridos, junto con pequeñas cantidades de colesterol y fosfolípidos.
Estos lípidos se empaquetan en forma de lipoproteínas de muy baja densidad (VLDL) en el retículo endoplásmico (RE) y el aparato de Golgi, mediante la acción de la proteína microsomal de transferencia de triglicéridos (MTP).
Las VLDL se secretan por exocitosis hacia los sinusoides hepáticos, que presentan un endotelio fenestrado que permite su paso a la sangre.
Las VLDL recién secretadas a la linfa y que luego se van para el torrente sanguíneo contienen principalmente:
ApoB-100 (principal apolipoproteína estructural).
Pequeñas cantidades de ApoE y ApoC.
Triglicéridos y algunos ésteres de colesterol.
En la circulación, las HDL transfieren más ApoC y ApoE a las VLDL y, mediante la CETP (proteína de transferencia de ésteres de colesterol), les ceden ésteres de colesterol.
¿Dónde y cómo se sintetizan las VLDL?
En el hígado, en el retículo endoplásmico y aparato de Golgi, mediante la acción de la proteína microsomal de transferencia de triglicéridos (MTP). Contienen triglicéridos, colesterol y ApoB-100 y se secretan por exocitosis hacia la sangre.
Es precursor de las LDL
a. VLDL
b. IDL
c. HDL
VLDL
¿Cuál es la función de la ApoC-II en las VLDL?
Activa la lipoproteína lipasa (LPL), que hidroliza los triglicéridos de las VLDL, liberando ácidos grasos y glicerol.
De VLDL a LDL: transformación metabólica
La Lipoproteína lipasa (LPL), activada por la ApoC-II, hidroliza los triglicéridos de las VLDL, liberando ácidos grasos y glicerol.
A medida que las VLDL pierden triglicéridos:
Parte de ellas es captada por el hígado (por tener varias ApoE).
El resto se convierte en IDL (lipoproteínas de densidad intermedia).
Posteriormente, la Lipasa hepática (HL) actúa sobre las IDL, eliminando más triglicéridos y fosfolípidos y transfiriendo las apolipoproteínas sobrantes a las HDL.
Así, las IDL se transforman en LDL (lipoproteínas de baja densidad).
Función y destino de las LDL
Las LDL contienen una sola molécula de ApoB-100 y una alta proporción de colesterol y ésteres de colesterol.
Su función principal es transportar colesterol a los tejidos periféricos para la síntesis de membranas celulares y hormonas esteroideas.
La captación de LDL ocurre por endocitosis mediada por el receptor de LDL, que reconoce la ApoB-100.
Este proceso culmina en los lisosomas, donde se degradan las apolipoproteínas y se libera el colesterol.
Aproximadamente dos tercios de las LDL son eliminadas por el hígado; el resto se utiliza en tejidos como las glándulas suprarrenales, ovarios, pulmones y riñones.
5. Receptores scavenger y aterogénesis
Cuando las LDL se oxidan o modifican químicamente, pierden afinidad por el receptor clásico de LDL que las elimina, en cambio, son captadas por los receptores scavenger (basurero) de los macrófagos.
Esta captación no está regulada por el colesterol intracelular, lo que favorece la acumulación de colesterol en macrófagos, formando células espumosas, una base del desarrollo de la aterosclerosis.
Porcentaje de la captacion de LDL en distintos organos
Más del 90% de la captación de las LDL se realiza a través del receptor de LDL en el hígado, los ovarios, las glándulas suprarrenales, los pulmones y los riñones.
Sin embargo, el 44% de la captación de las LDL es independiente del receptor de LDL en el intestino y el 72% en el bazo. Estos órganos contienen muchos macrófagos, que eliminan las LDL con sus receptores scavenger .
El colesterol intracelular regula su propio metabolismo a través de tres mecanismos principales:
Induce la acil-CoA-colesterol aciltransferasa (ACAT). Esta enzima convierte el exceso de colesterol en ésteres de colesterol muy insolubles que se almacenan en la célula:
Inhibe la HMG-CoA reductasa, reduciendo la síntesis endógena de colesterol.
Reprime la síntesis del receptor de LDL, disminuyendo la captación de colesterol desde la sangre
Transporte inverso de colesterol
Es un proceso biológico fundamental mediante el cual el exceso de colesterol presente en los tejidos periféricos es transportado de vuelta al hígado para su eliminación o reutilización, evitando su acumulación en las paredes de los vasos sanguíneos y, por tanto, reduciendo el riesgo de aterosclerosis.
¿Qué lipoproteína está principalmente involucrada en el transporte inverso de colesterol?
Las lipoproteínas de alta densidad (HDL).
Qué enzima convierte el colesterol libre en ésteres de colesterol durante este proceso?
La enzima LCAT (lecitin-colesterol aciltransferasa).
Cómo llega el colesterol de las HDL al hígado?
Directamente a través del receptor SR-BI o indirectamente mediante intercambio con otras lipoproteínas (VLDL, LDL).
¿Qué cambio estructural ocurre en la partícula de HDL durante la esterificación del colesterol?
: La HDL, inicialmente plana, se transforma en una partícula esférica con un núcleo hidrófobo de ésteres de colesterol; la lisofosfatidilcolina se transfiere a la albúmina.
¿Qué proteína se convierte en el principal suministrador de colesterol libre a HDL durante la fase esférica?
a: La proteína ABCG1, en lugar de ABCA1.
¿Qué mecanismos permiten que el colesterol libre llegue a las HDL?
Por exportadores ABCA1 y ABCG1, difusión pasiva y el transportador bidireccional SR-BI.
¿Qué proteína facilita la transferencia de ésteres de colesterol de HDL a otras lipoproteínas?
La CETP (proteína de transferencia de ésteres de colesterol), especialmente durante la lipólisis de quilomicrones y VLDL por la LPL.
¿Qué ocurre con las HDL en el hígado?
Sus triglicéridos y fosfolípidos son hidrolizados por la lipasa hepática (HL), convirtiendo HDL2 en HDL3; los ésteres de colesterol se transfieren a hepatocitos vía SR-BI.
¿Cuál es la diferencia clave entre la transferencia de colesterol por LDL y HDL?
Las LDL son endocitadas enteras, mientras que las HDL permanecen intactas y solo liberan ésteres de colesterol hacia las células.
: ¿Cuáles son las tres vías por las que el colesterol procedente de tejidos extrahepáticos llega al hígado?
1) Endocitosis mediada por apoE de partículas residuales,
2) Transferencia directa de ésteres desde HDL vía SR-BI,
3) Endocitosis de grandes HDL recubiertas de apoE.
HDL y transporte inverso de colesterol
Captación de colesterol: Las HDL recién formadas, ricas en apoA-I, extraen colesterol libre y fosfolípidos de las células mediante ABCA1.
Esterificación: La LCAT convierte el colesterol libre en ésteres, formando el núcleo hidrófobo y transformando la HDL de discoide a esférica.
Transferencia entre lipoproteínas: La CETP intercambia ésteres de colesterol con VLDL o LDL, facilitando su transporte al hígado.
Entrega hepática: El colesterol retorna al hígado por vía directa (SR-BI), endocitosis de HDL con apoE o transferencia indirecta mediante restos de VLDL y quilomicrones.
2. LDL y aterogénesis
Las LDL transportan colesterol hacia los tejidos y, cuando se acumula en exceso en la pared arterial, puede generar estrías grasas y progresar a placas ateroscleróticas.
Las células espumosas derivadas de macrófagos subendoteliales captan LDL oxidadas mediante receptores scavenger, liberando citocinas y factores de crecimiento que inducen inflamación, proliferación de fibroblastos y células musculares lisas, y depósito de matriz extracelular.
El exceso de LDL, especialmente en la hipercolesterolemia familiar, provoca aterosclerosis prematura y formación de xantomas.
Factores de riesgo y alimentación
La aterosclerosis se relaciona con edad, sexo, tabaquismo, diabetes, hipertensión e hipercolesterolemia.
La dieta influye en las concentraciones de lipoproteínas:
Grasas saturadas (excepto ácido esteárico) → ↑ LDL y ↑ HDL.
Grasas monoinsaturadas → ↓ LDL, ↑ HDL.
Grasas poliinsaturadas → ↓ LDL, efecto variable sobre HDL.
Alcohol, ejercicio y hormonas también modulan los niveles de HDL y LDL.
La sustitución de grasas saturadas por insaturadas es más eficaz para la salud cardiovascular que una dieta baja en grasas total.
Formación de estria grasa
Las LDL sean malas porque llevan el colesterol hasta el interior de la pared arterial y que las HDL sean buenas porque eliminan el exceso de colesterol.
Se produce una estría grasa cuando la cantidad de colesterol que aportan las LDL supera a la cantidad de colesterol que eliminan las HDL
Hiperlipoproteinemias
Son un grupo de trastornos metabólicos caracterizados por niveles anormales de lipoproteínas en la sangre, ya sea por exceso de colesterol, triglicéridos o ambos.
Consecuencias clínicas: Aumenta el riesgo de aterosclerosis, enfermedad cardiovascular y pancreatitis, según el tipo y nivel de lipoproteínas alteradas.
Tipo I- Hiperquilomicronemia
↑↑↑ triglicéridos, LDL bajas; asociada a deficiencia de LPL o apoC-II.
Tipo II – Hipercolesterolemia
↑ LDL, riesgo elevado de aterosclerosis; incluye hipercolesterolemia familiar.
Tipo III – Disbetalipoproteinemia:
↑ restos de VLDL y quilomicrones; relacionada con apoE-2 homocigota.
Tipo IV – Hipertrigliceridemia:
↑ VLDL; asociada a obesidad, diabetes tipo 2 y alcoholismo.
Tipo V:
↑ combinada de quilomicrones y VLDL; factores genéticos y metabólicos.
Lipoproteína(a)
Variante de LDL que contiene apo(a) unida a apoB-100.
Concentraciones elevadas → riesgo independiente de aterosclerosis.
Determinadas genéticamente; no responden significativamente a dieta.
¿Dónde comienza la digestión y absorción de los lípidos?
En el intestino delgado, donde triglicéridos, fosfolípidos y colesterol son emulsificados por sales biliares para facilitar la acción de las lipasas pancreáticas.
¿Qué son las micelas mixtas y su función?
Estructuras solubles de sales biliares, colesterol, fosfolípidos y lípidos hidrolizados (productos de la digestion enzimatica) que transportan lípidos hasta el borde en cepillo de los enterocitos para su absorción.
¿Qué ocurre con los ácidos grasos y monoacilglicéridos dentro del enterocito?
Se reesterifican en triglicéridos en el retículo endoplásmico y se ensamblan con apolipoproteínas (Apo B-48) formando quilomicrones.
¿Cuál es la ruta de los quilomicrones tras su formación?
Se liberan al sistema linfático y luego a la circulación sistémica, donde entregan ácidos grasos libres a tejidos mediante la lipoproteína lipasa (LPL).
¿Cuál es la función de las VLDL y su transformación en circulación?
Transportan triglicéridos endógenos a tejidos periféricos; tras la acción de LPL se convierten en IDL y luego en LDL, que transporta colesterol a las células.
¿Qué función cumplen las HDL?
Participan en el transporte reverso del colesterol, captando el exceso de tejidos periféricos y llevándolo al hígado para excreción biliar o reutilización, protegiendo frente a la aterosclerosis.
Accion sales biliares
Son compuestos anfipaticos sintetizadas en el higado y secretados por la vesicula biliar al lumen intestinal.
-Actúan como detergentes, se unen a gotas de grasa dietetica a medida que estas se fragmentan por la accion peristaltica del musculo intestinal → EMULSIONAN para AUMENTAR área superficial y facilitar el ataque por enzimas digestivas pancreaticas
La contraccion de la vesicula biliar y la secrecion de las enzimas pancreaticas son estimuladas por la hormona intestinal
Colecistocininca, secretada por las celulas intestinales cuando el contenido gastrico entra al intestino
Acción de la lipasa pancreatica
Enzima mas importante que digiere los triacilgliceroles
Actua junto la colipasa
Hidroliza los acidos grasos de cualquier longitud de cadena, que se situen en posición 1 y 3, produciendo acidos grasos libres y 2-monocilglicerol (glicerol con un acido grasos esterificado en posicion 2)
Accion de colesterol esterasa y fosfolipasa
Colesterol esterasa: Hidroliza éster colesterol en colesterol
Fosfolipasa A2: Hidroliza fosfolipido en lisofosfopido
Micelas
Pequeñas microgotas de productos de digestion enzimatica (AG, lisofosfolipdos y colesterol) y 2-MG que son emulsionadas por sales biliares,
Viajan hacia las superficie de celulas epiteliales intestinales: AG y 2 MG y otros lipidos son absorbidos, mientras que las sales biliares se quedan en el lumen instestinal y son absorbidas por el ileon para reciclarse
Quilomicrones maduros
A medida que los quilomicrones nacientes salen a la linfa por exocitosis, estas aceptan proteinas HDL. Las HDL transfieren:
a. apoE - permiten que lipoporteinas ingresen a las celulas por endocitosis para su posterior digestion en lisosomas
b. apoCII - actua como un activador de LPL, hidroliza Tg de los quilomicrones y VLDL en sangre
Destino principal de los acidos grasos
Almacenamiento como triacilgliceroles en el tejido adiposo y oxidados para generar energía en el músculo.
Destino de glicerol
Síntesis de triacilgliceroles en el hígado durante el estado posprandial
V o F: La LPL en los capilares tiene un menor Km que la LPL en el tejido adiposo
V