C1 Géologie
1/31
Earn XP
Description and Tags
cosmologie et formation de la terre
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
32 Terms
Naissance de l’univers
Avant Big bang à difficile à déterminer, imp à voir
A l’origine : milieu très chaud (> 1032K), très dense, concentré en un point !
Aucun atome, particule stable au temps zéro
Big bang :
· 13.7 M d’années
· E très forte en 1 pt
· Apparition 4 forces physique
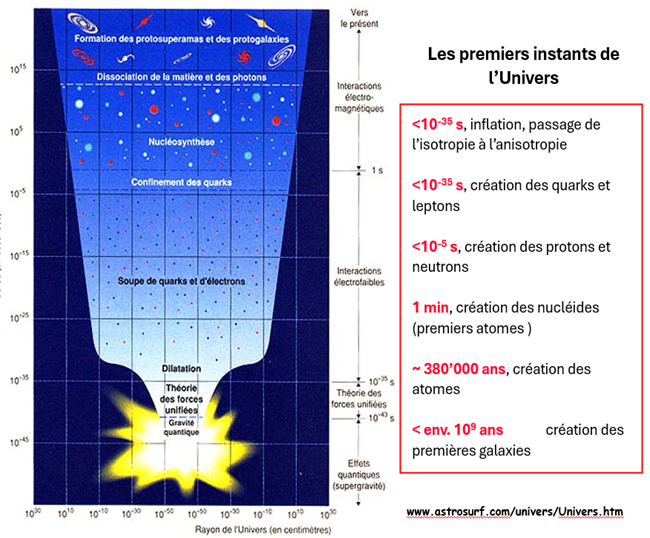
Théorie forces unifiés
gravité, électromagnétisme, force forte (noyau atomique) /faible (désintégration radiocative)
10-45 -10-35 = Formation des premiers atomes
Univers est en expansion, sa densité est très faible (10-30g/cm3)
Atomes
· protons, neutrons, électrons (mécanique quantique = complexe à atome met en jeu diverses particules (leptons, quarks, bosons))
· Un atome est une sphère quasiment vide ! Le volume du noyau = 1/1’000’000’000’000’000e du vol total
Isotopes
Deux nucléides d'un même élément chimique = isotopes ssi partagent mm nbr protons, Z, mais nbr de neutrons diff, N.
+ ou – stable, instable = radioactif (ils se décomposent + ou – vite en modifiant leur nombre de proton et/ou de neutrons)
Si nbr de protons Z change à isotopes change d’identité
Nucléosynthèse primordiale
T baisse de 1 milliard à 1000K pdt ˜1 million d’années
La force électromagnétique entre en jeu
Synthèse des premiers éléments (H, He, Be, Li) -> début de l’ère stellaire
· À très haute temp neutron est récupéré par un autre H, et ainsi de suit pour former un He
· H= 90%, He=10%, reste = trace par fusion
· Li et Be très rare car atomes complexe difficile à produire
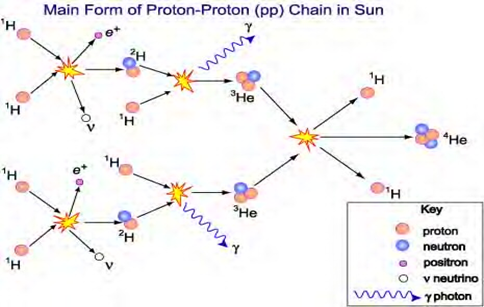
Usine thermonucléaire
1. Fusion nucléaire dans le cœur de l’étoile jusqu’au fer
2. Absorption de neutrons lents après le fer jusqu’au bismuth
3. Absorption de neutrons rapides pour les éléments + lourd et radioactifs
Création d’atomes résulte de la condensation de matière stellaire sous l’effet de la force de gravitation
Fusion nucléaire stellaire et étapes de la création des éléments
1. Chauffe (15m °C jusqu’à 3M) -> éléments se créent jusqu’au fer
2. Devient dense au centre -> s’effondre sur elle mm
3. Explose (radioactivité) -> nucléosynthèse àSupernova
Si étoile petite (Soleil) -> protoétoile àétoile jaune (soleil aujourd’hui ? H->He) → géante rouge (couche externe peu attiré par cœur =vent stellaire qui disperse He) → naine blanche(cœur dénudé à O et C, se refroidit très lentement) → naine noire (dead soleil dans 15M d’années)
Si étoile grosse (25x le soleil) -> protoétoile → supergéante rouge → supernova bleue
Vie et mort d’une supernova
Se forme en qlq dizième de seconde, disparaissent en qlq mois
Cycle ! -> à la mort de l’étoile, matière recyclée !
Composition actuelle de l’univers
· Divers objets célestes ont pratiquement la mm composition chimique à déterminée par mesure de spectrométrique optique
· Univers consitué en nbr d’atomes à 93%H + 7 %He + traces
· 1Ma après BigBang à NP a produit H et He essentielleemnt + traces Be et Li

Soleil
→ même repartition des éléments que dans le reste de l’univers -> recyclage
→ Pas étoile primaire car pas seulement H et He
• T coeur: 14 x 106 K • T atmosphère 2 x 106 K • Perte de masse par combustion de H en He: 600 Mégatonnes/s • Diamètre: 1.4 x 106 km • Masse: 2 x 1027 tonnes • Densité: 1.41 !!
| • 90 at-% H + 10% He • Seul He est synthétisé • Le reste est recyclé • Vent solaire >800km/s formé de particules • Cellules de convexion interne → taches solaires • Rotation en 27 jours
|
Formation planète
-> condensation de gaz dans le disque périsolaire
-> formation de poussières qui s’agglomèrent (100m d’années) -> sous forme de roche près du centre du disque et glace en périphérie
-> collision entre planetésimaux, accrétion de matériaux (météorite encore présente dans le désert = sources d'infos) -> + ils deviennent grand + ils attirent des météorites (chondrites ˜4560Ma ans)
-> proto-planète (due à l’accrétion)
à qlq dizaines d’années
Différenciation au sein du disque planétaire
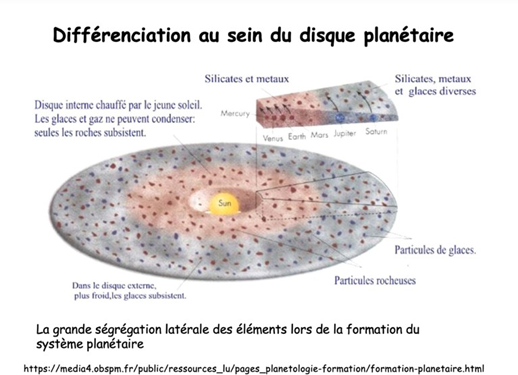
Condensation de la matière en fonction du temps
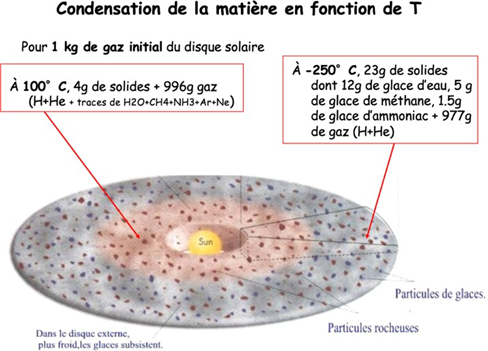
Propriétés planètes d’un système solaire
- Toutes orbitent sur le mm plan écliptique
- Toutes orbitent dans le mm sens autour du soleil
- Toutes formées dans la mm nébuleuse solaire
Pq différentes planètes ?
- Température pas a même proche ou loin du soleil
- Vent solaires pareil
Planète Tellurique
Proche du soleil (jusqu’à mars)-> trop chaud + vent solaire (pas de gaz/glace) = silicates + métaux = planètes telluriques (rocheuse) à petite, faible masse, haute densité
À 100°C, 4g de solides + 996g gaz (H+He + traces de H2O+CH4+NH3+Ar+Ne)
Planète gazeuse/géante
Loin du soleil (Jupiter,etc.) -> + froid donc encore des gaz = silicates, métaux et glaces diverses= planètes gazeuse/géante (encore H et He autour donc + de diamètre) àgrande, grande masse, peu dense (structure : H-> He-> métaux-> glace-> roche)
À -250°C, 23g de solides dont 12g de glace d’eau, 5 g de glace de méthane, 1.5g de glace d’ammoniac (NH3)+ 977g de gaz (H+He)
Origine de la lune
Impact de Théia (chondrite) avec la Terre (il y a 4.51 M d’années) → Lune même éléments que la terre
→ Conséquence : impact = effet thermique
-> + temperature
-> E = fonte de la masse terrestre
-> les éléments lourds (Fe) tombent au centre, élém. léger flottent (minéraux silicatés et eau)
-> refroidissement
-> structure en deux couches (noyau et manteau terrestre) = différentiation
différence verre/minéral
Verre = chaotique (amorphe)
Minéral = régulière (cristalline)
Composition globale de la Terre
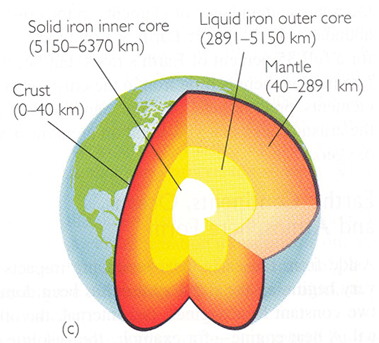
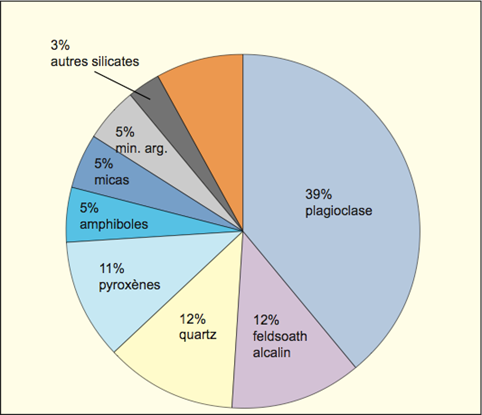
Composition de la croûte terrestre
• La croûte terrestre = composée de minéraux silicatés.
• Les minéraux carbonatés, les évaporites, les sulfures, etc., = très présents en surface, mais qu’environ 8 % de la croûte terrestre.
• La composition minéralogique et chimique moyenne de la croûte continentale est proche de celle d’un granite.
Importance des silicats dans la croûte terrestre
Différence minéral cristal et roche
Minéral =
→ Substance naturelle, inorganique, composition chimique définie et solides (cristaux) de forme géométrique
→ Formé d’une association d’éléments chimiques dans des proportions définies (=compo chimique du minéral)
→ Association ou non association régis par prop électrique et taille (association anion cation à ions)
→ Électriquement neutre
→ Associe suvent + de 2 éléments (exp : carbonates)
Cristal = un individu d’une espèce minérale
Roche = agrégat solide de cristaux représentant un minéral ou pls minéraux d’espèces diff
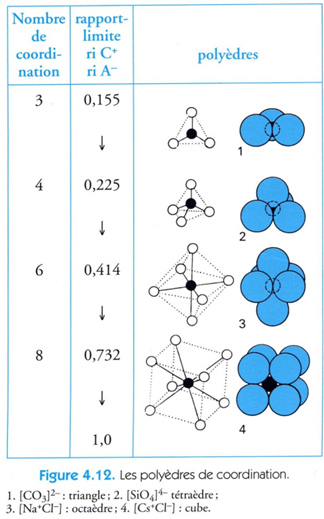
Polyèdre de coordinence
forme géométrique définie par les anions entourant un cation dans une lacune
· Moins assemblage compact, plus les lacunes sont grandes, plus gros seront les cations incorporés et plus élevé le nbr de coordinence (anions voisins directs)
· Il y a des limites dans le rapport possible entre taille cation et taille anion à détermine l’existence ou non d’un minéral (facteur de taille)
Taille des ions principaux
· Les anions Cl et S + grands que O à forment des assemblage compactes dont lacune comblé par des petits cations
· K va avoir de la peine à entre dans les structures cristallopgraphiques

Liaison atomique minéraux
· Cohésion entre atome grâce à forces électromagnétique
· 4 types de liaisons :
o Liaison de Van der Waals, très faible (ex. cristaux d’argon, fond à -189°C)
o Liaison ionique par échange d’électrons, forte, minéraux rel. durs et cassants (ex. NaCl, halite, fond à 801°C)
o Liaison covalente par mise en commun d’électrons, très forte, minéraux très durs (ex. C, diamant, fond à 3’546°C)
o Liaison métallique par mise en commun de nombreux électrons, faible, minéraux rel. moux (ex. or, cuivre, T de fusion env. 1000°C)
· Dureté et stabilité thermique dépend de la liaison
La maille élémentiare
· État cristallin = arrangement tridimensionnel périodique d’atomes à polymérsation dans 3 directions de l’espace d’un motif particulier)
· Arrangement 3D résulte d’un équilibre entre forces attractives cation-anion et force répulsives cation-cation / anion-anion
· Maille résultante = forme géométrique simple
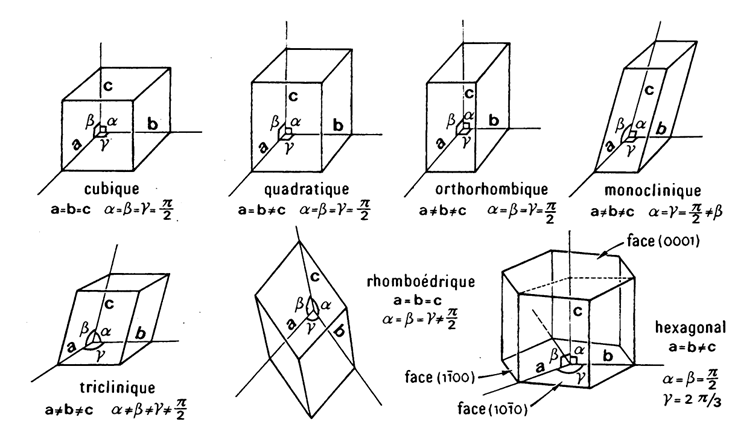
Les 7 systèmes cristallins
→ Baisse de niveau de symétrie de gauche à droite haut bas
→ Certains cristaux développent des formes géométriques plus complexes à mais tjrs à partir de l’une des 7 mailles élémentaires
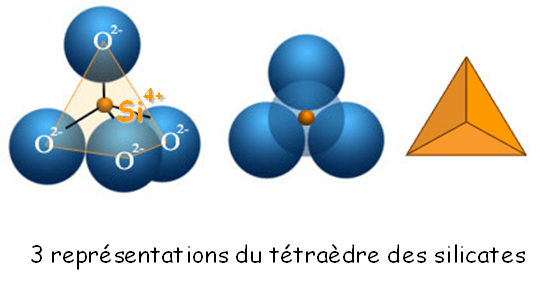
Les silicates
- second éléement le plus abondant dans la croûte terrestre à silicium cation Si4+ à il s’inscrit parfaitement dans le lacune du tétraèdre oxygène et donne le SiO44-
EXP : olivine
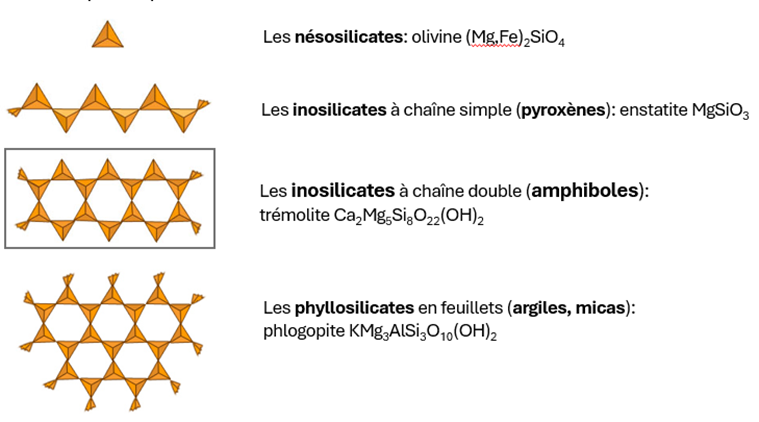
Architecture des silicates
Famille imp des silicates
+ la structure complexe, + compo chimique contient d’élément (sauf quartz)
Stabilité des minéraux (polymorphisme)
- Minéraux = sensibles à la température (T augmente, liaison interatomique se romp = déstabilisation du minéral)
- Sensible à la pression à taille des lacunes diminue = déstabilisation dans sa structure cristallographique (polymorphisme à mm compo chimique mais pas mm structure)
- Minéraux ont des domaines de stabilité bien définis, mais survivent souvent en conditions métastable (exp : diamant)
Exp de polymorphisme : graphite(formé à basse pression)/diamant (formé à haute pression)
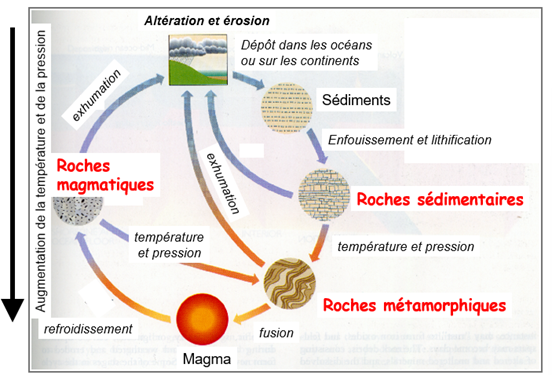
3 grandes catégories de roches et cycle des roches
1. Roches magmatiques (cristallisation de magma)
2. Roches sédimentaires (consolidation de dépôts de matériaux divers ou de précipitation chimique)
3. Roches métamorphiques (recristallisation en profondeur de roches préexistantes de toute nature)