Kaarten: biochemie H9: Chemotroof Energie Metabolisme: Glycolyse en Fermentatie | Quizlet
1/50
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
51 Terms
herhaling middelbaar voor de komende 4 kaartjes (quizlet: Biologie 6 celademhaling)
wat is celademhaling?
de oxidatie van organische moleculen (suikers, vetten en eiwitten) met als doel energie uit die stoffen op te slaan in de vorm van ATP. De celademhaling noemt men ook de dissimilatie van glucose of de aerobe verbranding van glucose
wat gebeurt er tijdens de oxidatie van voedingsstoffen
Tijdens de oxidatie van voedingsstoffen worden deze stoffen ‘verbrand’ door binding aan zuurstof. Dit is een reactie waarbij de voedingsstoffen H-atomen afstaan. NAD+ en FAD werken als waterstofdragers (houden H+ en e- in balans).
hoe verloopt de spijsvertering, en waar vindt de celademhaling plaats?
De voedingstoffen die we eten, grote moleculen (zetmeel,...) worden verkleind tot hun bouwstenen (glucose) door de hydrolyse in de maag bijvoorbeeld. Pas in de dunne darm worden de voedingsstoffen getransporteerd naar alle lichaamscellen. In die lichaamscellen vindt de celademhaling plaats.
uit welke drie processen bestaat de celademhaling?
-glycolyse (in het cytosol) ->H9 deze quizlet
-citroenzuurcyclus (matrix van de mitochondrien) -> H10
-eindoxidaties (innermembraan mitochondrien) -> H10
9.1 Metabole paden
Wat is metabolisme en in welke 2 soorten wordt het opgedeeld?
Metabolisme = een netwerk van reactiewegen (energiewinning, synthese van biomoleculen …) die bestaan uit geordende enzym-gekatalyseerde reacties en die met elkaar communiceren (allostere regulatoren, hormonen …)
Anabolisme = verhoging van orde (lokale daling in entropie), endergonisch vb. synthese van zetmeel en glycogeen vanuit glucose
Katabolisme = verlaging van orde (verhoging van entropie), exergonisch vb. oxidatie van glucose
->er ontstaan kleine organische moleculen (metabolieten) die de bouwsteen zijn voor biosynthese
9.2 ATP: een universele energie-drager
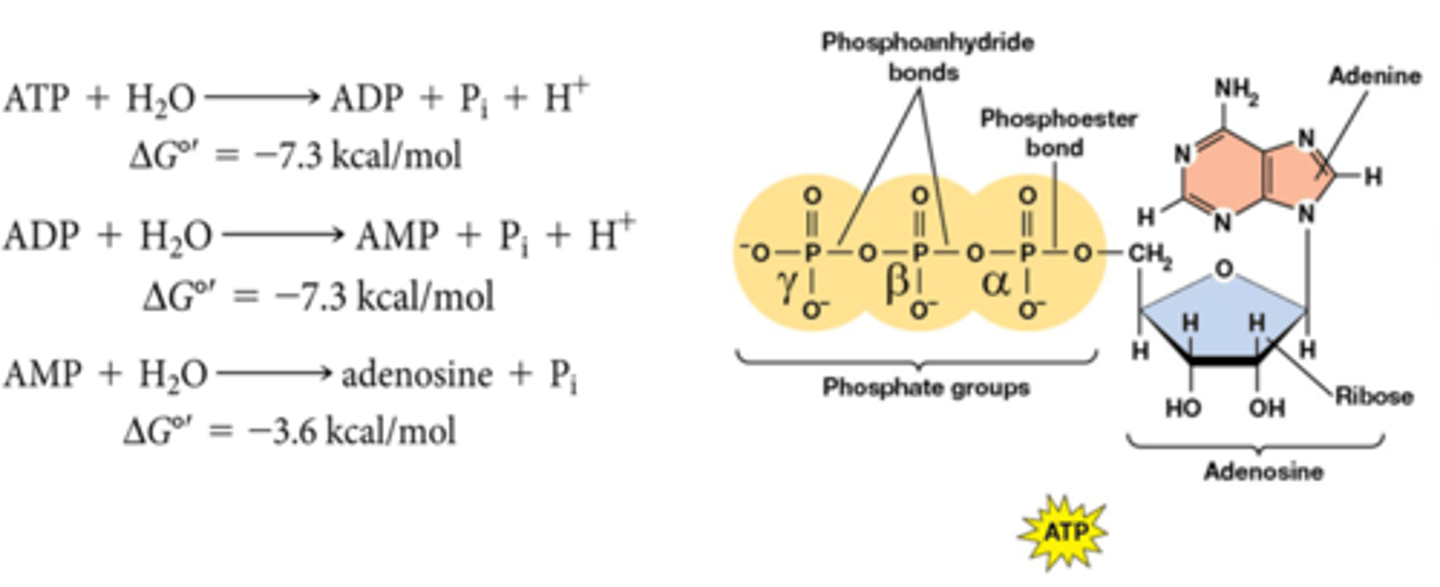
Wat is ATP?
adenosine (adenine en ribose)
3 fosfaatgroepen (PO₄³⁻)
->het is een nucleotide
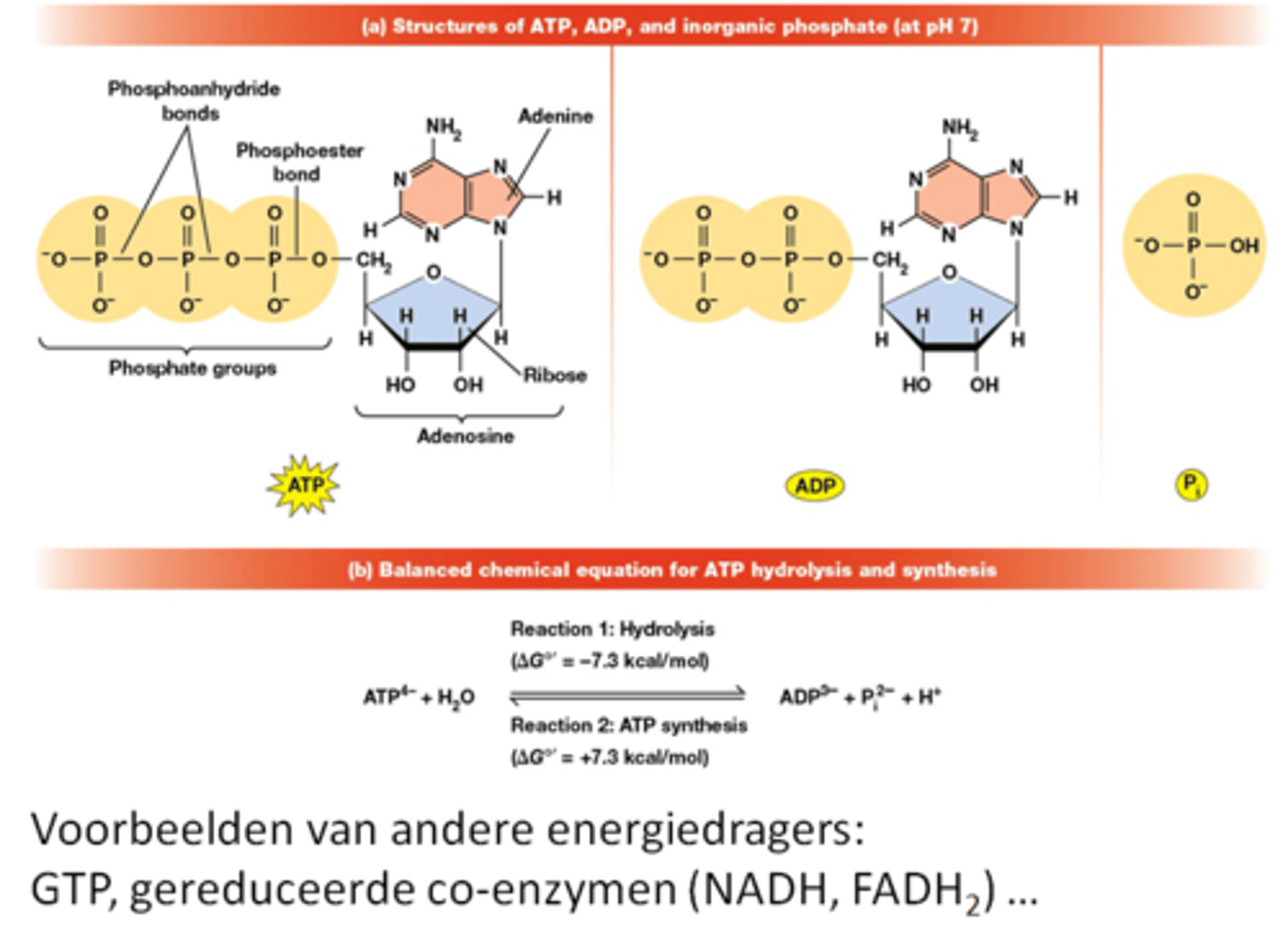
Wat is er speciaal aan Pi?
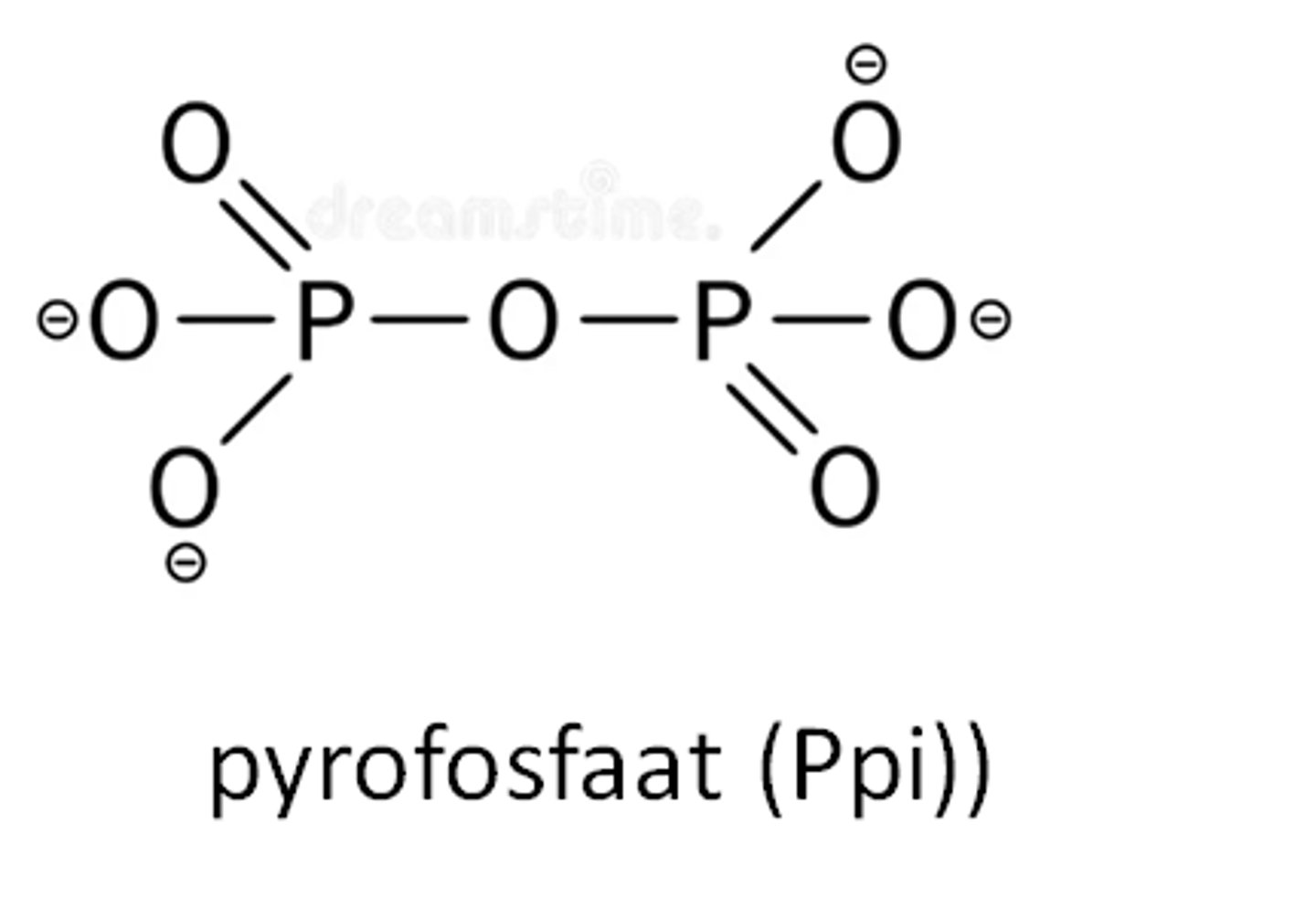
Orthofosfaat (meestal wordt gewoon fosfaat (PO₄³⁻) gezegd idk) =Pi heeft 4 resonantie structuren
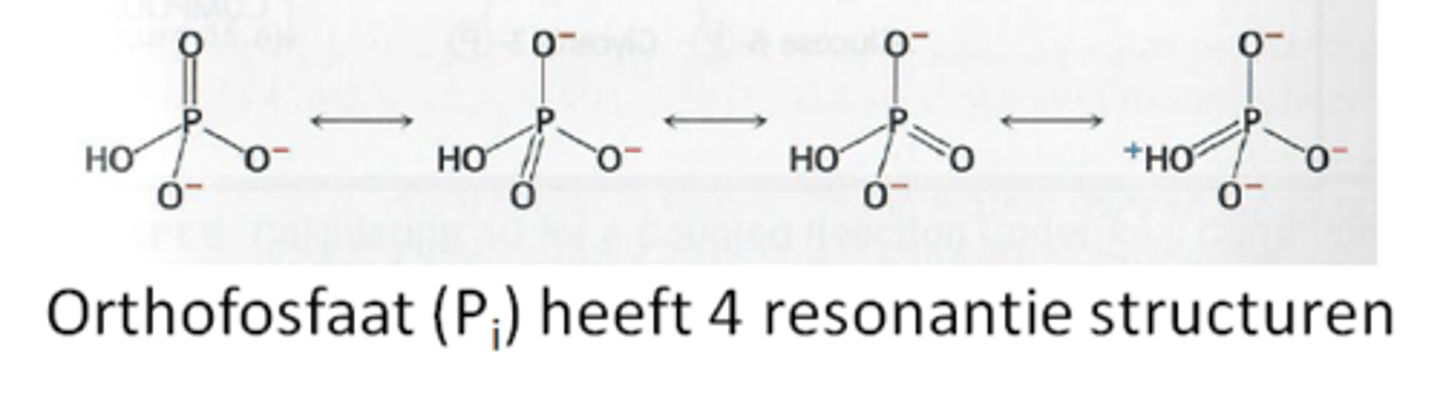
Wat is Ppi en wanneer wordt het vrijgesteld?
pyrofosfaat of difosfaat en het wordt vrijgesteld bij het incorporeren van een nucleotide in een DNA- of RNA-streng
We hebben in hoofdstuk 3 gezien dat er energie vrijkomt bij het maken van covalente bindingen, dit geldt echter alleen voor stoffen die elkaar leuk vinden, bv H-H, O-O NaCl...
Hoe komt het dat er energie vrijkomt bij de breking van ATP?
Breking van ATP: er komt 7,3kcal per mol vrij
De energie komt niet uit de klieving zelf (daar is energie voor nodig)
-in de klievingsproducten ontstaan er nieuwe covalente bindingen
- nieuwe niet covalente interacties met water
-verhoogde entropie van de producten
->Er komt meer energie vrij dan dat er geïnvesteerd moet worden in de hydrolyse
->zie hydrolyse van ATP, foto door chatgpt laten maken en -30,5kJ=-7,3kcal
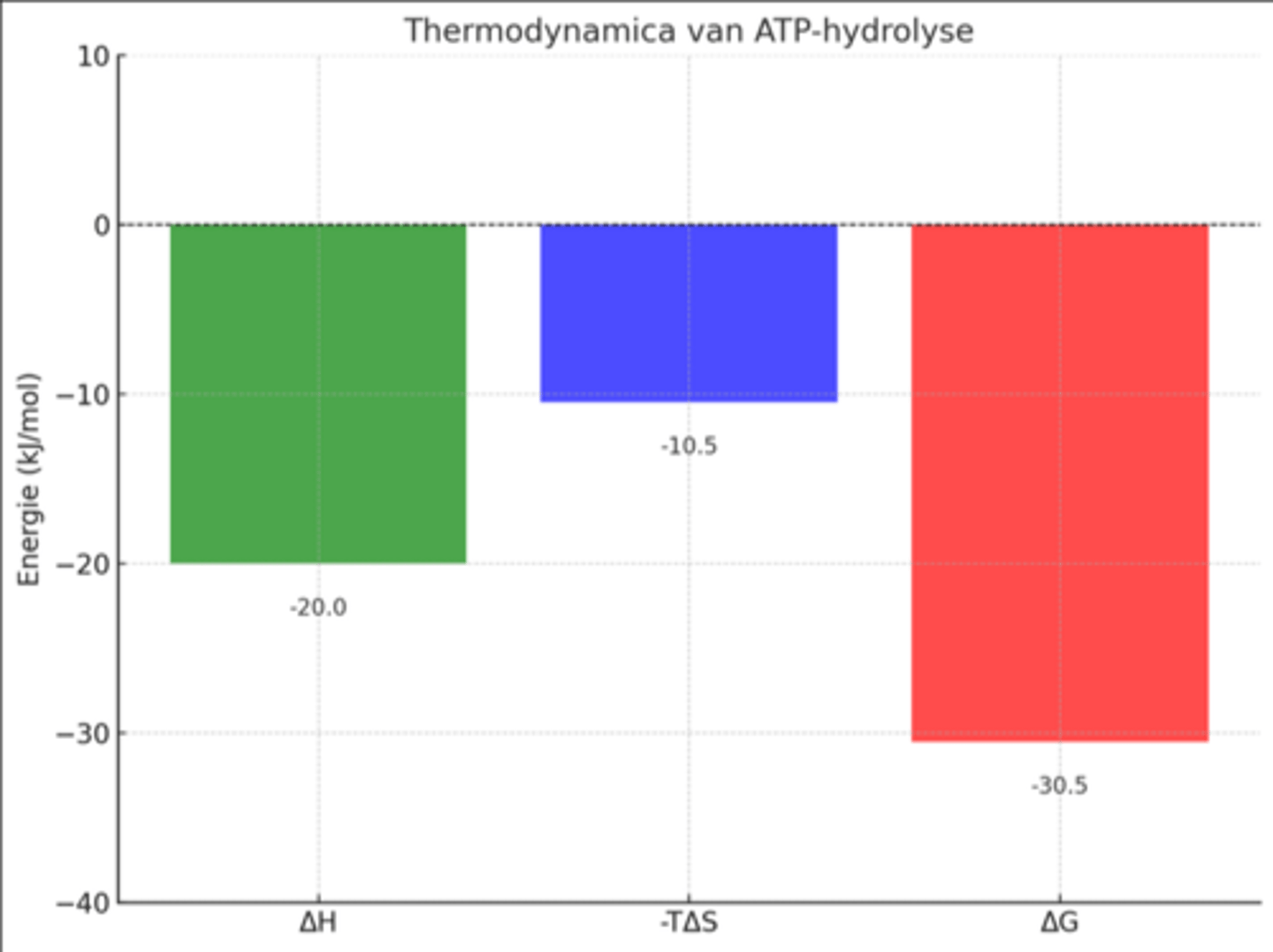
Waarom is ATP zo energierijk en waarom is de hydrolyse een exergonisch proces?
omdat er 2 fosfoanhybride bindingen zijn, bij het breken van die bindingen komt er veel energie vrij
hydrolyse van ATP is energierijk:
-Afstoting tussen 3 negatief geladen fosfaatgroepen (PO₄³⁻)
-het vrijgekomen inorganische fosfaat (Pi) gaat in een resonantievorm die energetisch gunstiger en stabieler is dan de fosfaatgroepen in het ATP-molecuul (ΔH is negatief)
-Niet-covalente interacties van producten met water
-Verhoogde entropie van producten tov reagentia (concentratie van water wordt als onveranderd beschouwd) (ΔS is positief)
Samenvatting:
Breken van fosfoanhybridebindingen kost 20kJ/mol
Vorming van nieuwe bindingen levert ongeveer -40kJ/mol
Toename van entropie levert extra vrije energie op
Hoe komt het dat de fosforylering van glucose verloopt als het een energetisch ongunstische reactie is?
het wordt gekoppeld aan de hydrolyse van ATP
glucose + Pi -> glucose-6-fosfaat + H2O (1)
ΔG°’ = + 3,3 kcal/mol
ATP + H2O -> ADP + Pi (2)
ΔG°’ = - 7,3 kcal/mol
_________________________________________________________________________________
ΔG°’ = + 3,3 kcal/mol – 7,3 kcal/mol = - 4 kcal/mol (1) + (2)
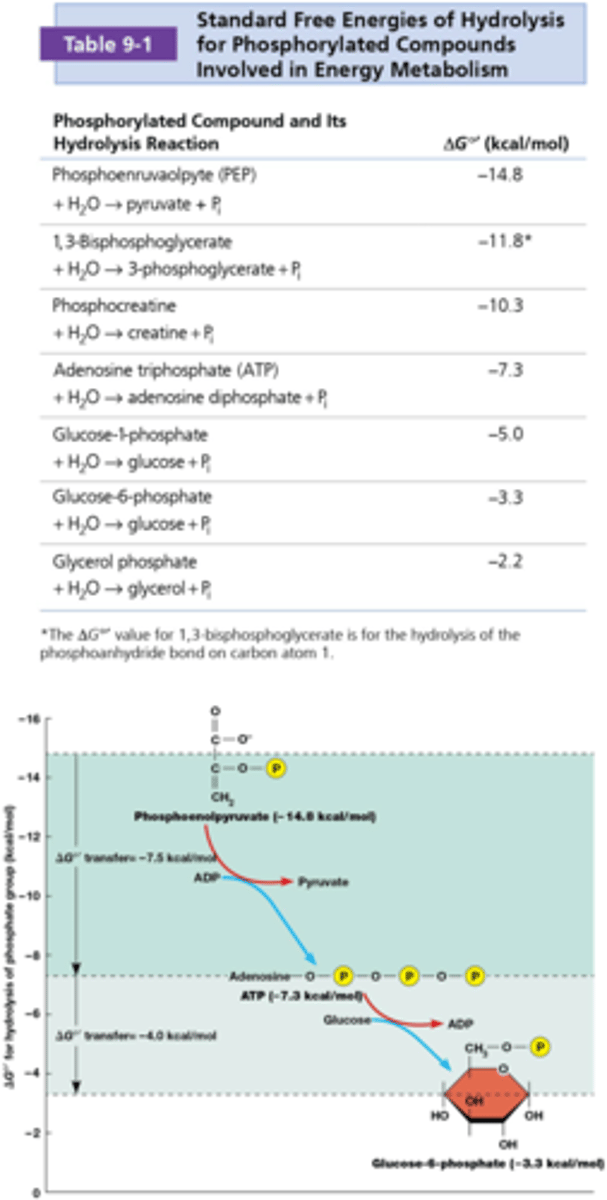
komt er altijd evenveel energie vrij als je een fosfaatgroep loskoppelt?
nee, op de y-as en in de tabel zie je hoeveel energie vrijkomt wanneer bepaalde stoffen hun fosfaatgroep breken = fosfotransferpotentiaal
Alle processen in het diagram zijn exergonisch, je ziet dat ATP in het midden staat, die kan dus zowel donor als acceptor (ADP) zijn van fosfaatgroepen!
9.3 Chemotroof energiemetabolisme
Welke en hoeveel energie komt vrij bij de verbranding van glucose?
het is sterk exergonisch ∆G°'=-686kcal/mol
->zal altijd vrijkomen, als dit ongecontroleerd gebeurt, is dit gewoon warmte
Als de mens dit gecontroleerd doet dan krijg je ongeveer 2/3 warmte en 1/3 ATP* (afhankelijk van partiele of volledige oxidatie)
*38mol ATP en 7,3kcal/mol ATP= 277kcal= ongeveer 1/3 van 686
wat is de volledige en onvolledige verbranding?
Aerobe ademhaling: O2 is elektronen acceptor
volledige oxidatie van glucose
=glycolyse + citroenzuurcyclus + oxidatieve fosforylering
(Bacteriën: S, H+, Fe3+ als elektronen acceptor)
In afwezigheid van O2: organische elektronen acceptor
partiële oxidatie van glucose
=glycolyse + fermentatie
3 soorten organismen:
-obligaat aeroob
-obligaat anaeroob
-facultatief aeroob/anaeroob (zoals spiercellen die beide processen kunnen doen)
Wat betekent oxidatie in de biologie?
In biologische chemie worden meestal niet alleen elektronen (e-), maar ook protonen (H+) uitgewisseld => [H] => meestal ‘dehydrogenatie’ (gekatalyseerd door dehydrogenasen).
de 2H tussen haakjes omdat die niet vrij in de oplossing zitten want ze worden opgenomen door coenzymen*
*kleine organische moleculen, vaak afgeleid van vitaminen, worden gerecycleerd in de cel, meestal zwakke associatie met het enzyme (cosubstraten)
![<p>In biologische chemie worden meestal niet alleen elektronen (e-), maar ook protonen (H+) uitgewisseld => [H] => meestal ‘dehydrogenatie’ (gekatalyseerd door dehydrogenasen).</p><p>de 2H tussen haakjes omdat die niet vrij in de oplossing zitten want ze worden opgenomen door coenzymen*</p><p>*kleine organische moleculen, vaak afgeleid van vitaminen, worden gerecycleerd in de cel, meestal zwakke associatie met het enzyme (cosubstraten)</p>](https://knowt-user-attachments.s3.amazonaws.com/09b9f461-19fe-4c08-9657-880b68b16daa.png)
Welke coenzymen nemen H+ op tijdens de celademhaling?
NAD+ vangt 2 elektronen en 1 proton op (= hydride ion H-) in dehydrogenatie reacties van volgend type: zie bovenste foto
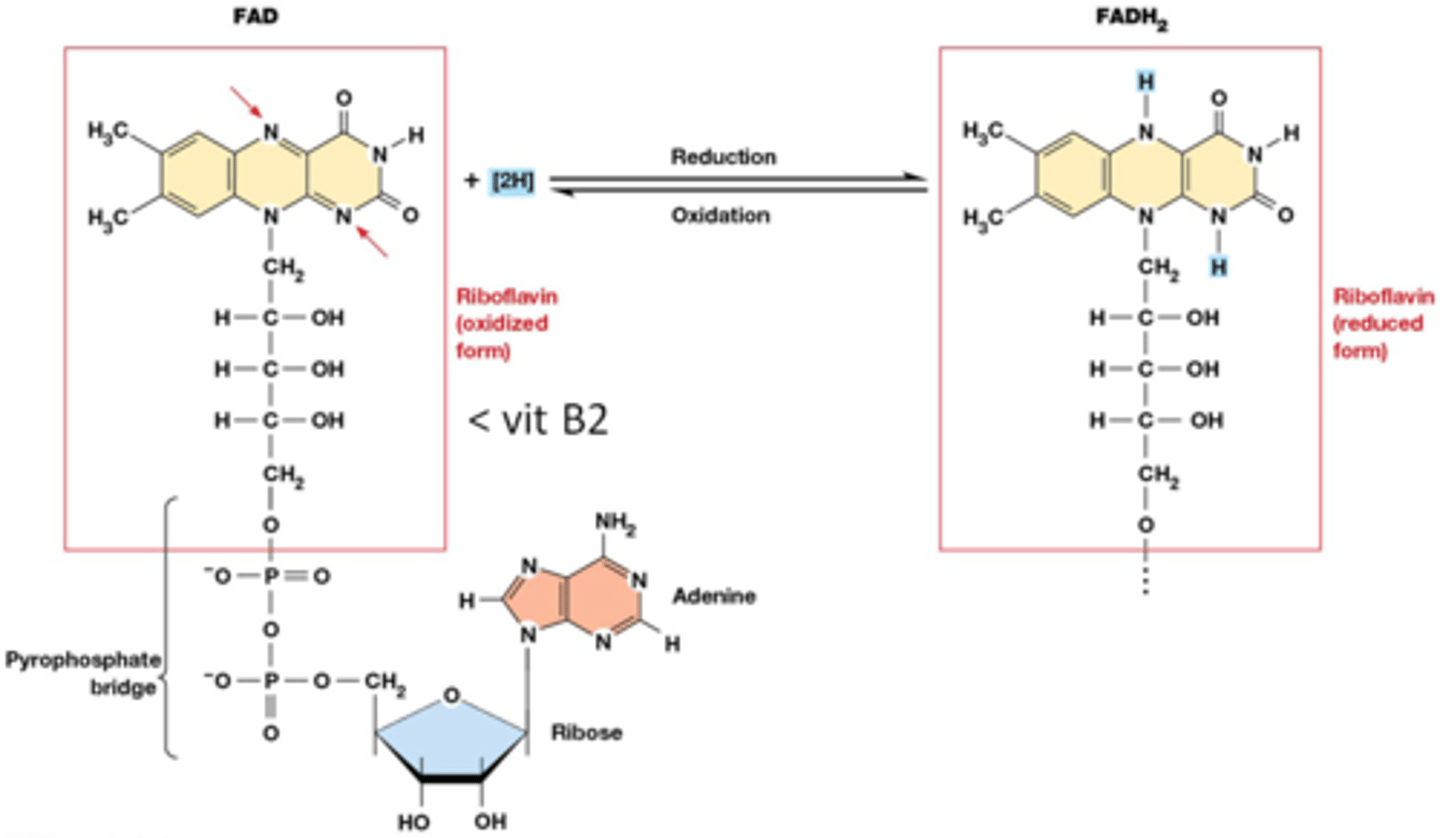
FAD vangt 2 elektronen en 2 protonen op in dehydrogenatie reacties van volgend type: zie onderste foto
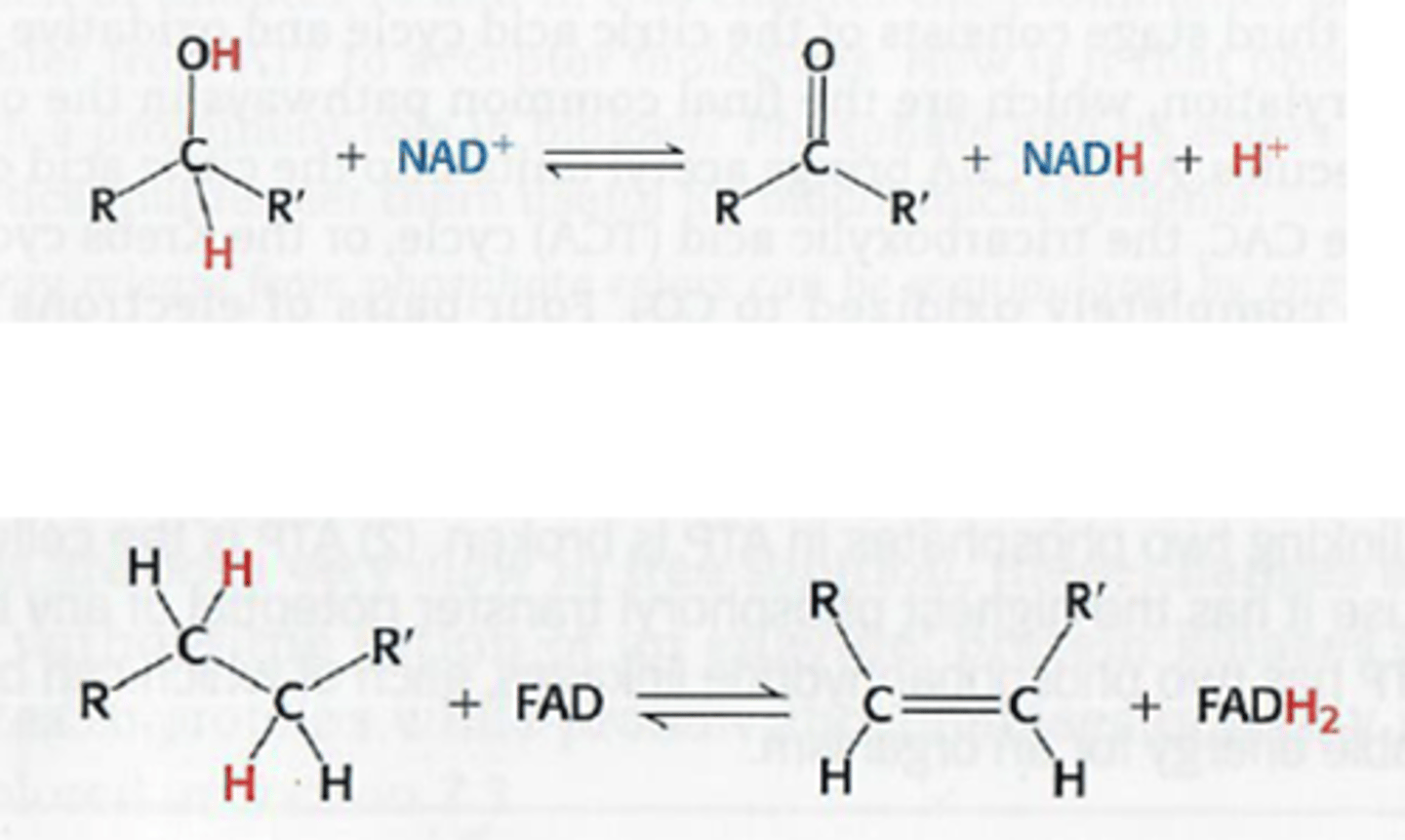
foto structuur NAD+
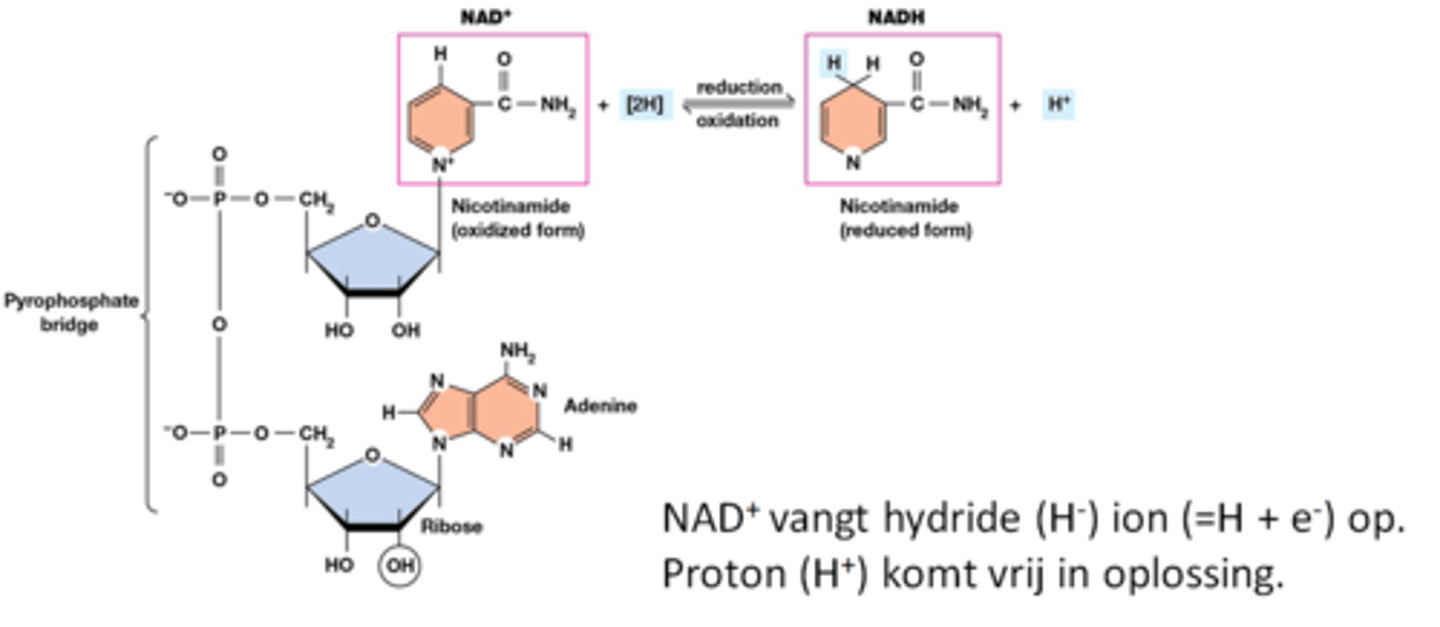
foto structuur FAD en FADH2
Wat zijn geactiveerde dragers? (niet in Beckers dus belangrijk)
kleine moleculen die drager zijn van een chemische groep of elektronen, die (exergonisch) kunnen overgedragen worden naar een ander molecule. Het zijn vaak co-enzymen of cosubstraten in enzym-gekatalyseerde reacties.
Voorbeelden:
-ATP is een geactiveerde drager van fosfaat groepen.
-NAD+ en FAD zijn dragers van hoge energie elektronen ontstaan bij de oxidatie van brandstofmoleculen.
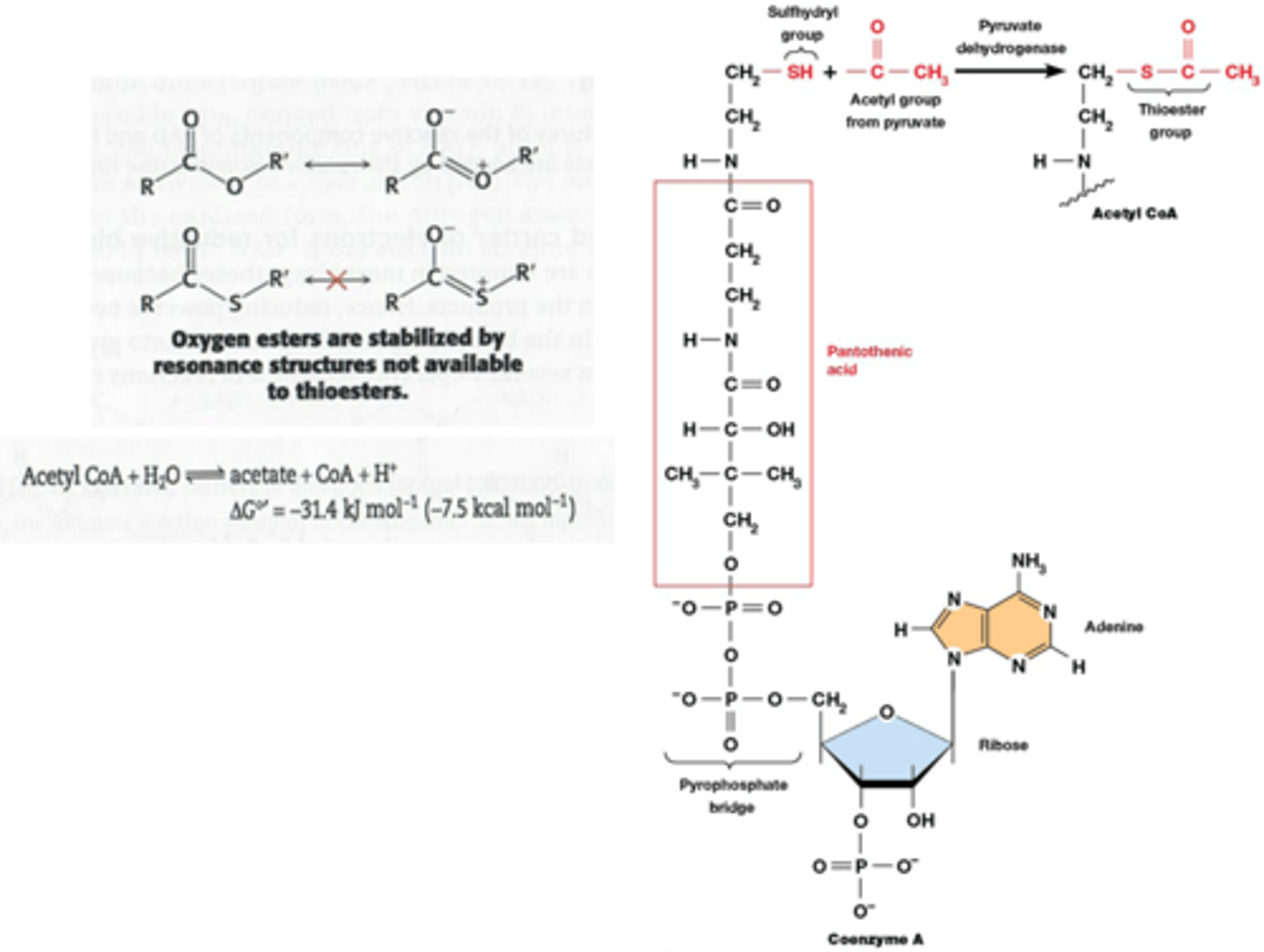
-Co-enzyme A (CoA-SH) is een geactiveerde drager van acyl groepen (vb. acetyl CoA, drager van C2). (zie foto)
extra info: in Co-enzyme A is er een thioester binding: energetisch hoger dan een zuurstofester binding omdat er minder energie geinvesteerd moet worden om ze te breken (onstabielere dubbele binding met zwavel)
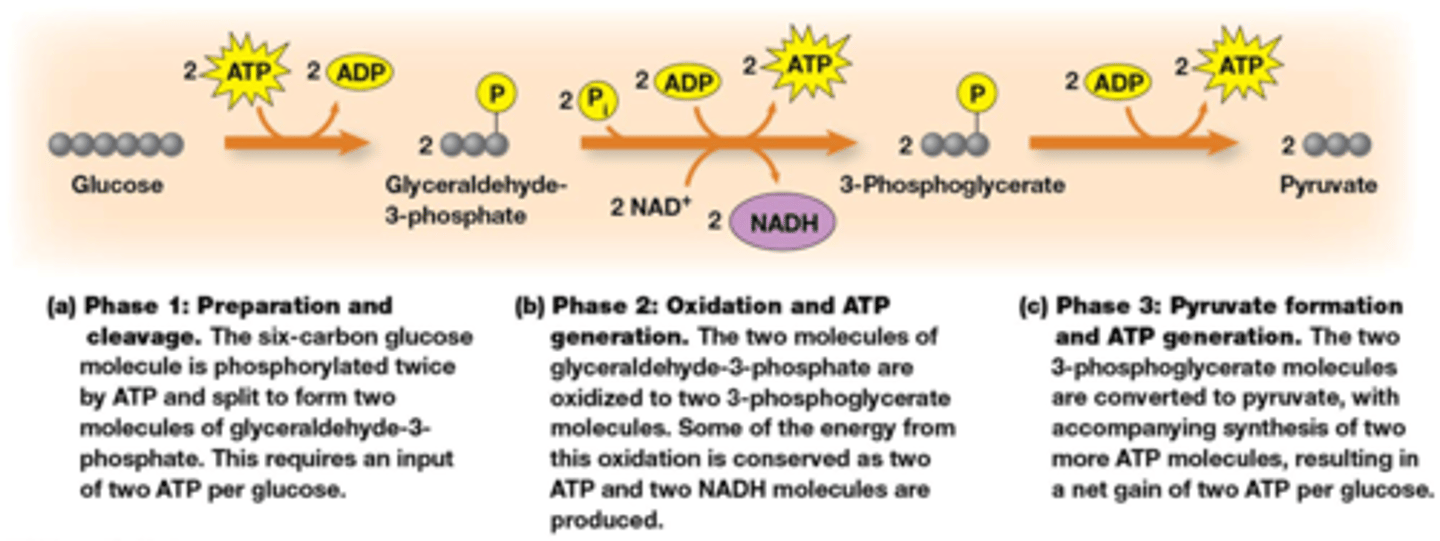
Wat is de reactievergelijking van de glycolyse?
C6H12O6 + 2NAD+ +2ADP +2Pi -> 2 pyruvaat + 2NADH+ 2ATP
er worden 2 ATP geïnvesteerd en er komen 4 ATP vrij
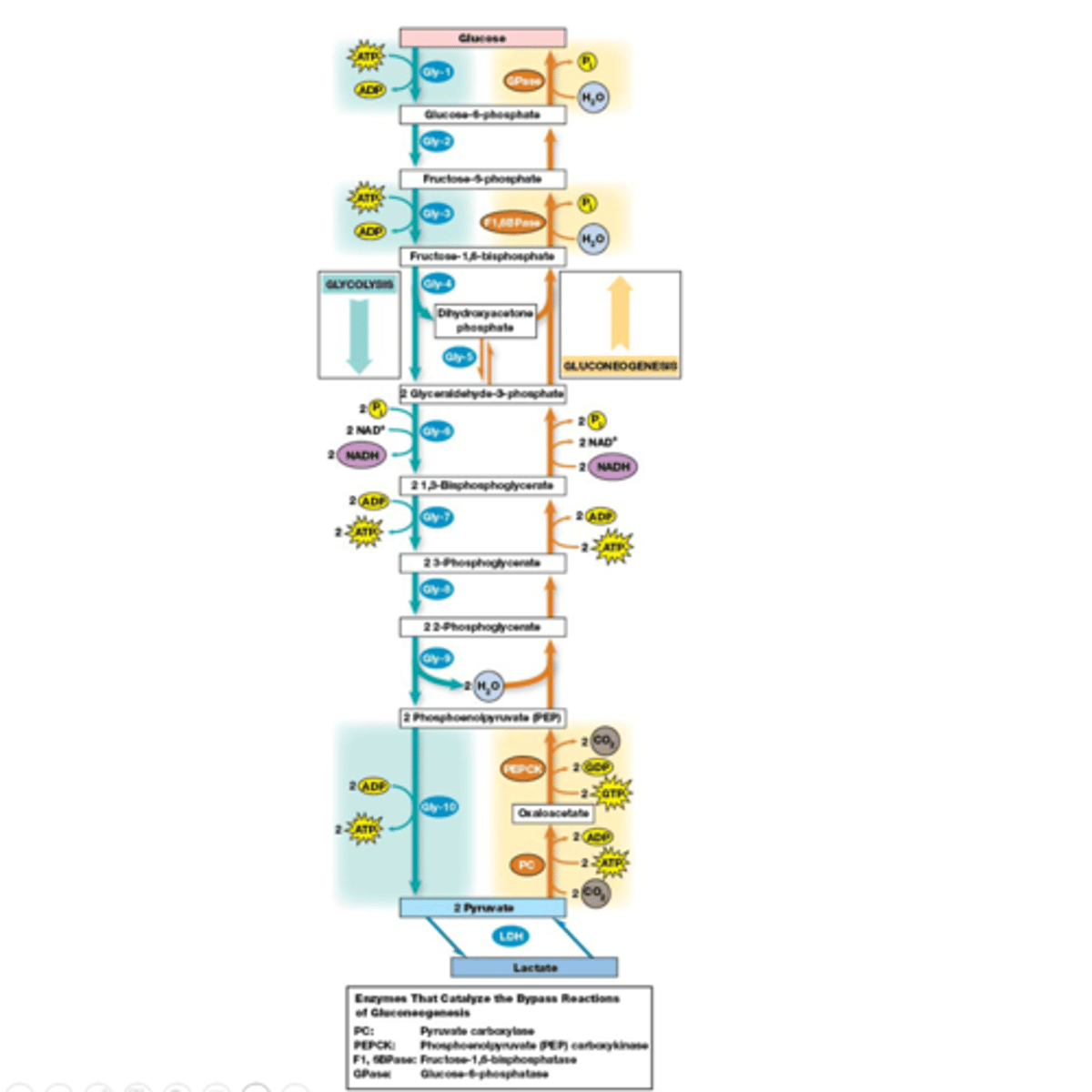
Grote schema van de hydrolyse
pijlen met enkele richting: zo exergonisch dat de prevailing concentrations er nooit in slagen om die in de andere richting te doen ->onomkeerbare reactie
belangrijk: na stap 5 komt elk molecule dubbel voor, die NADH die je ziet zijn er dus eigenlijk 2 en en die 2 ATP's zijn er dus eigenlijk 4 ;)
Wat moet je kennen van deze afbeelding?
-Alle namen in de kadertjes (uitgeschreven binnen 2 kaartjes)
-weten wat er gebeurt tussen de verschillende namen
-structuren herkennen
-namen van de enzymen die we besproken hebben (volgend kaartje)
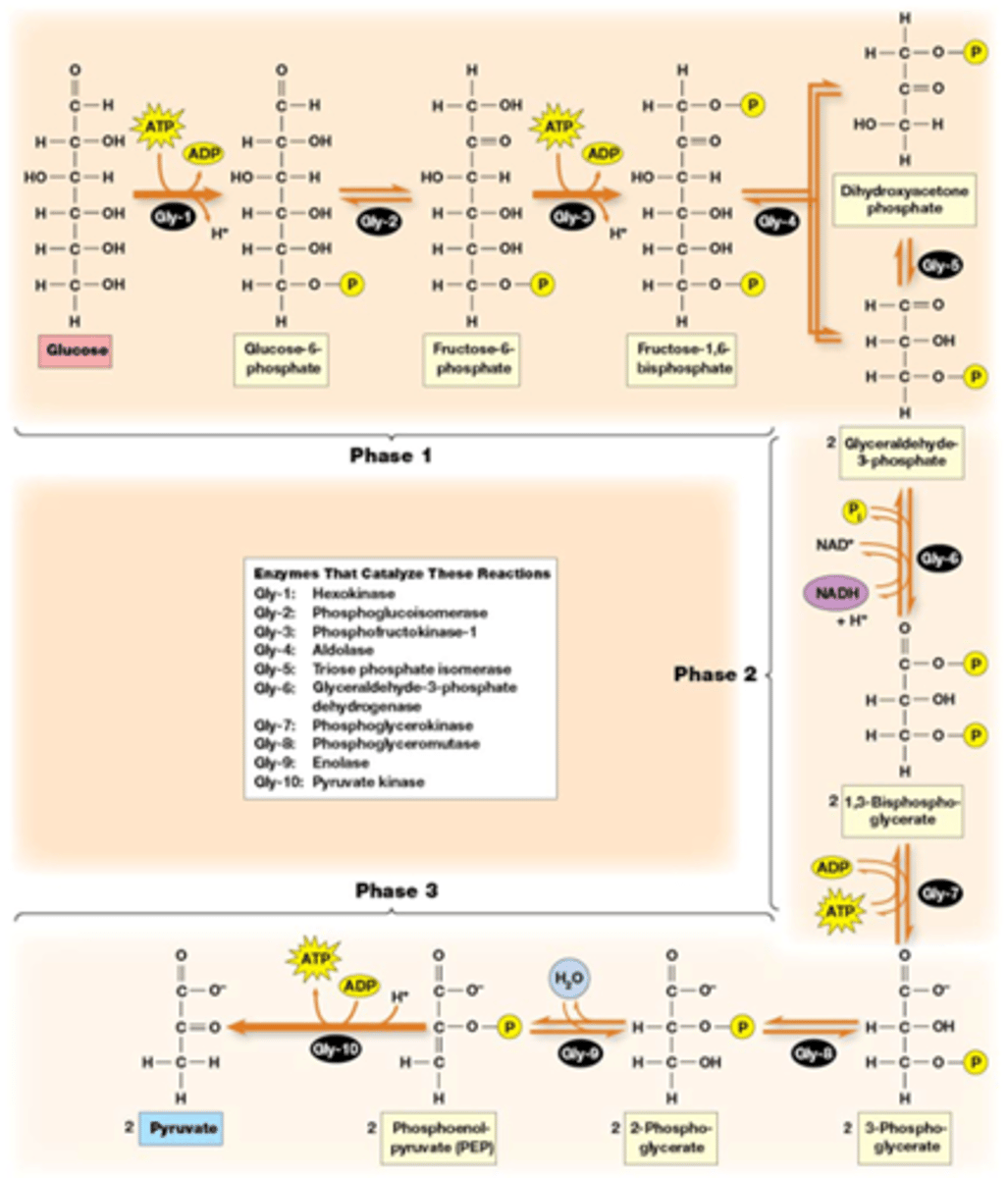
Welke namen van enzymen hebben we besproken? (we hebben gly-2 niet besproken maar het is phosphoglucoisomerase voor de geintresseerden)
Gly-1= Hexokinase
Gly-3=PFK-1 (fosfofructokinase-1)
Gly-4=aldolase
Gly-5= triose fosfaat isomerase
Gly-6= GAPDH (glyceraldehyde 3-fosfaat dehydrogenase)
gly-7= fosfoglyceraatkinase
Gly-8 = fosfoglyceraat mutase
Gly-9= enolase
Gly-10 = pyruvaat kinase
Geef de stappen van de glycolyse, geef de begin en eindstoffen, de enzymen en welke reactie ze uitvoeren (isomerisatie, dehydrogenatie, ...)
1. Glucose: fosforylatie door hexokinase, ATP wordt verbruikt → Glucose-6-fosfaat (kan niet meer uit de cel)
2. Glucose-6-fosfaat: isomerisatie door gly-2 we gaan van een aldose naar een ketose suiker→ Fructose-6-fosfaat
3. Fructose-6-fosfaat: fosforylatie door fosfofructokinase-1, ATP wordt verbruikt.→ Fructose-1,6-bisfosfaat
4. Fructose-1,6-bisfosfaat: klieving door aldolase → Dihydroxyacetonfosfaat (ketose C3 suiker)en Glyceraldehyde-3-fosfaat (aldose C3 suiker)
5. Dihydroxyacetonfosfaat: isomerisatie door triosefosfaatisomerase → Glyceraldehyde-3-fosfaat (evenwicht ligt heel sterk naar rechts door de prevailing concentrations)
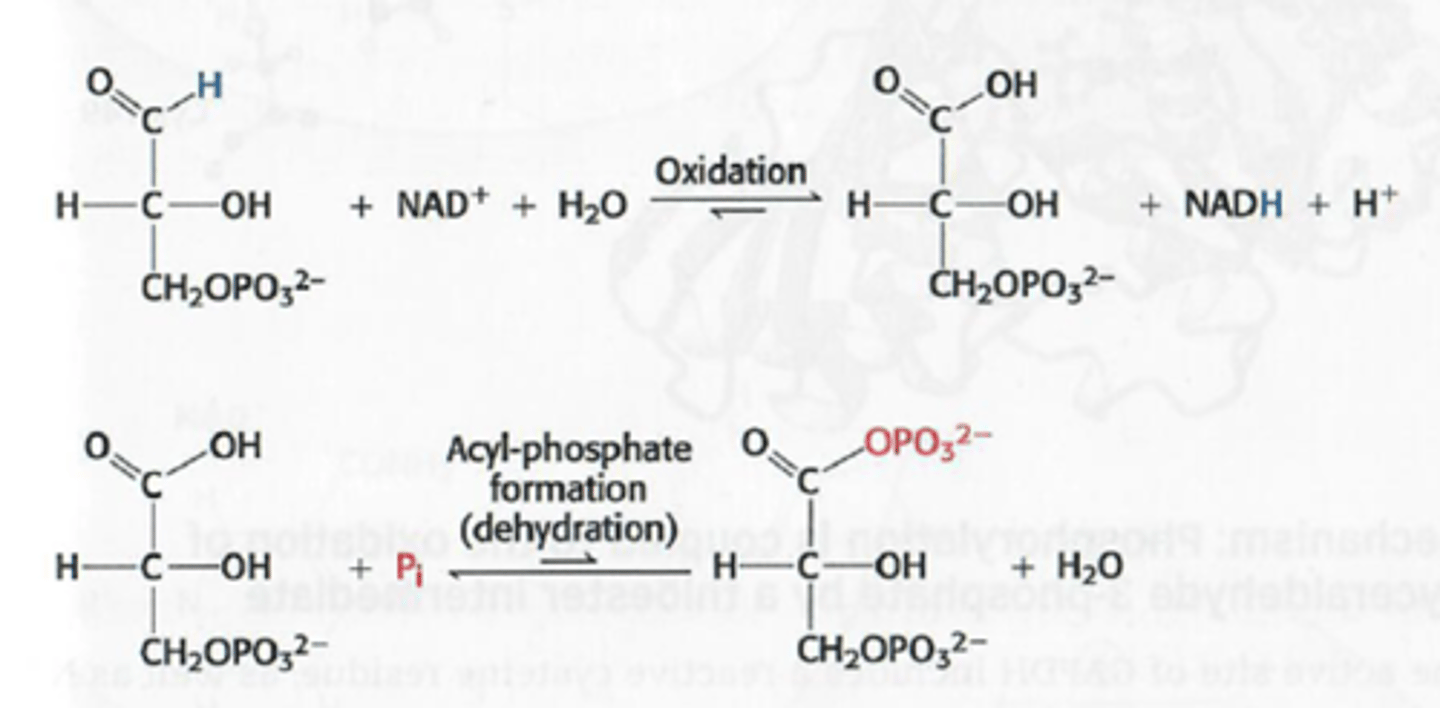
6. Glyceraldehyde-3-fosfaat: dehydrogenatie=oxidatie van aldehyde tot caborxylzuur (NADH vorming) en fosforylering (vorming van acyl-fosfaat) door glyceraldehyde-3-fosfaatdehydrogenase (GAPDH), → 1,3-Bisfosfoglyceraat (een gemengd anhydride)
7. 1,3-Bisfosfoglyceraat: substrate-level phosporylation door 3-fosfoglyceraatkinase, ATP wordt geproduceerd → 3-Fosfoglyceraat
8. 3-Fosfoglyceraat: herschikking door fosfoglyceraatmutase → 2-Fosfoglyceraat
9. 2-Fosfoglyceraat: dehydratie door enolase, H₂O wordt verwijderd (interne redox reactie)→ Fosfoenolpyruvaat (PEP) (hoge fosfotransferpotentiaal (zie kaartje 13))
10. Fosfoenolpyruvaat (PEP): substrate-level phosphorylation door pyruvaatkinase, ATP wordt geproduceerd → Pyruvaat (in stabiele keto vorm)
extra foto om stap 6 duidelijker te maken
Glyceraldehyde wordt geoxideerd
Aldehyde wordt een zuur
NAD+ wordt gereduceerd tot NADH
Bij de tweede reactie wordt een fosfaat ingebouwd: dehydrogenatie en vorming van acyl-fosfaat
energie komt van een binding niet van ATP
9.5 Fermentatie
Wanneer doen we aan fermentatie, waarom?
Wanneer er geen zuurstof is!
als je glycolyse blijft doen gaat de NAD+ op een gegeven moment op geraken -> regeneratie van NAD+.
Fermentatie is een redox neutraal proces: NADH gevormd tijdens glycolyse wordt opnieuw geoxideerd. ‘Glucose’ is donor en acceptor van elektronen. (elektronen zijn vrijgekomen van glucose en nu worden ze terug opgenomen door pyruvaat)
er wordt geen extra ATP gewonnen (buiten de 2ATP van de hydrolyse dan)
de energie blijft vast in lactaat, bij de fermentatie komt 47kcal/mol vrij
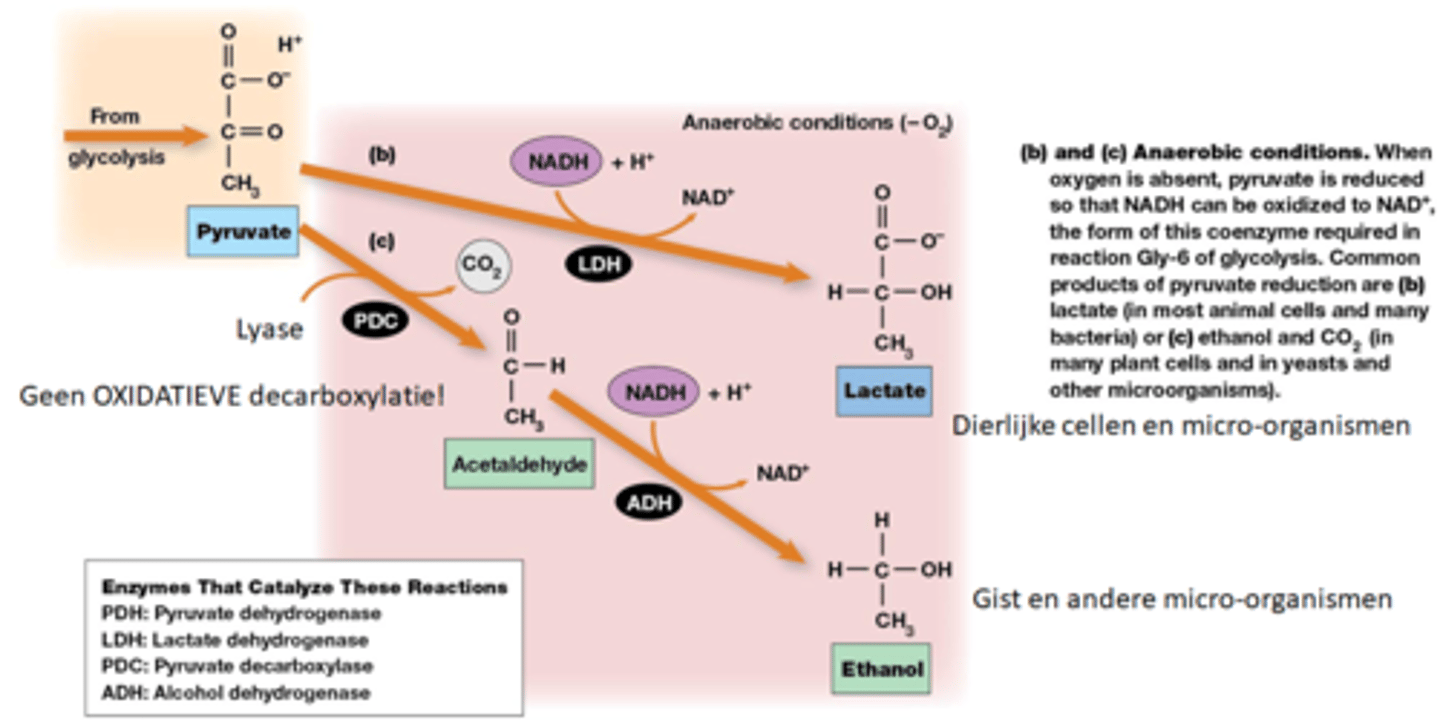
Wat is de lactaatfermentatie?
pyruvaat wordt gereduceerd, NADH wordt geoxideerd. Pyruvaat neemt de elektronen op ter vorming van lactaat
dit gebeurt ook soms in aerobe omstandigheden trouwens, bv bij kankercellen
Waar wordt lactaat gevormd?
•Spier (zware inspanning; fermentatie)
•Rode bloedcellen (geen mitochondriën)
•Huid (anaeroob)
bij gistcellen gebeurt er alcholische gisting, wat is dat?
-anaerobe decarboxylatie van pyruvaat door lyase
-acetaldehyde wordt gereduceerd ter vorming van ethanol
-NADH wordt geoxideerd

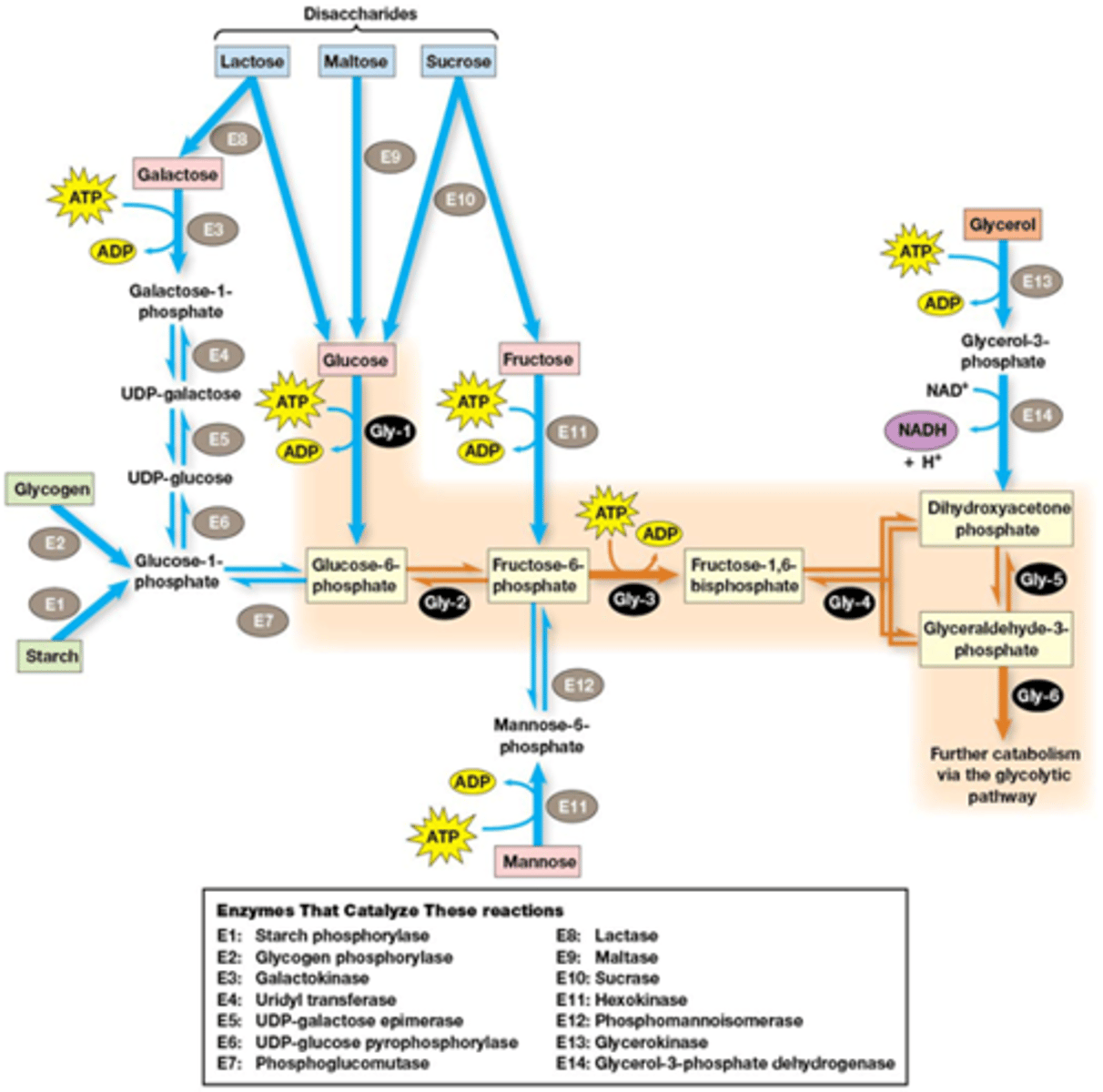
9.6 Alternatieve substraten van de glycolyse
foto om duidelijk te maken dat je ook kan vertrekken van andere stoffen voor aan de glycolyse te beginnen, enzymen moet je niet kennen
bij glycogeen en zetmeel lijkt het alsof er 1 ATP minder nodig is.
uitleg* is confusing maar komt er gewoon op neer dat er altijd 2 ATP geinvesteerd moet worden in de glycolyse en er altijd 4 vrijkomt!
*Bij die opslagsachariden is die 1 ATP gewoon al verbruikt bij de opbouw van die suikers
9.7 Gluconeogenese
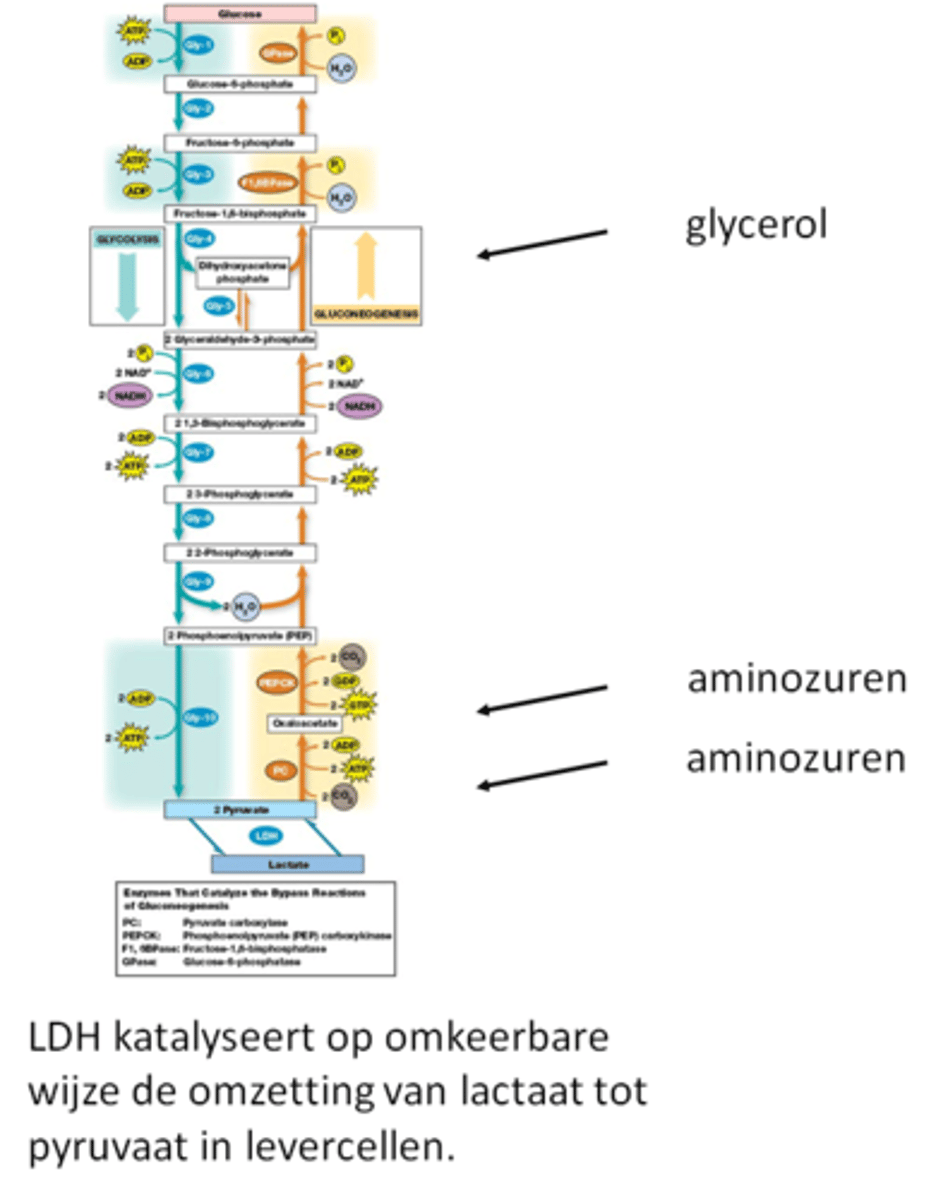
Wat is de gluconeogenese?
=het omgekeerde van de glycolyse (alleen zijn er stappen onomkeerbaar dus eigenlijk ook niet)
=synthese van glucose vanuit niet-koolhydraat precursoren, hoofdzakelijk in de lever en een beetje in de nieren
Niet-koolhydraat precursoren:
•pyruvaat
•lactaat (eerst omgezet naar pyruvaat)
•aminozuren (eerst omgezet naar pyruvaat of oxaloacetaat)
•glycerol (eerst omgezet naar dihydroxyaceton fosfaat) (vetzuurcompoment kunnen we niets doen)
Wat is de functie van de gluconeogenese?
-recyclage van lactaat
-als je lang niets eet (vasten) dan moeten je (hersen)cellen toch op een manier aan glucose geraken
Hoe bypassen we stap 10 van de glycolyse tijdens de gluconeogenese
2 stappen nodig om stap 10 van de glycolyse om te keren
1) Carboxylatie (consumptie van ATP)
2) Decarboxylatie + fosforylatie (fosfaat donor = GTP)
-gebeurt in cytoplasma
-decarboxylatie drijft een reactie die anders sterk endergonisch zou zijn (zie ook CAC).
verbruik van 4 energierijke bindingen!
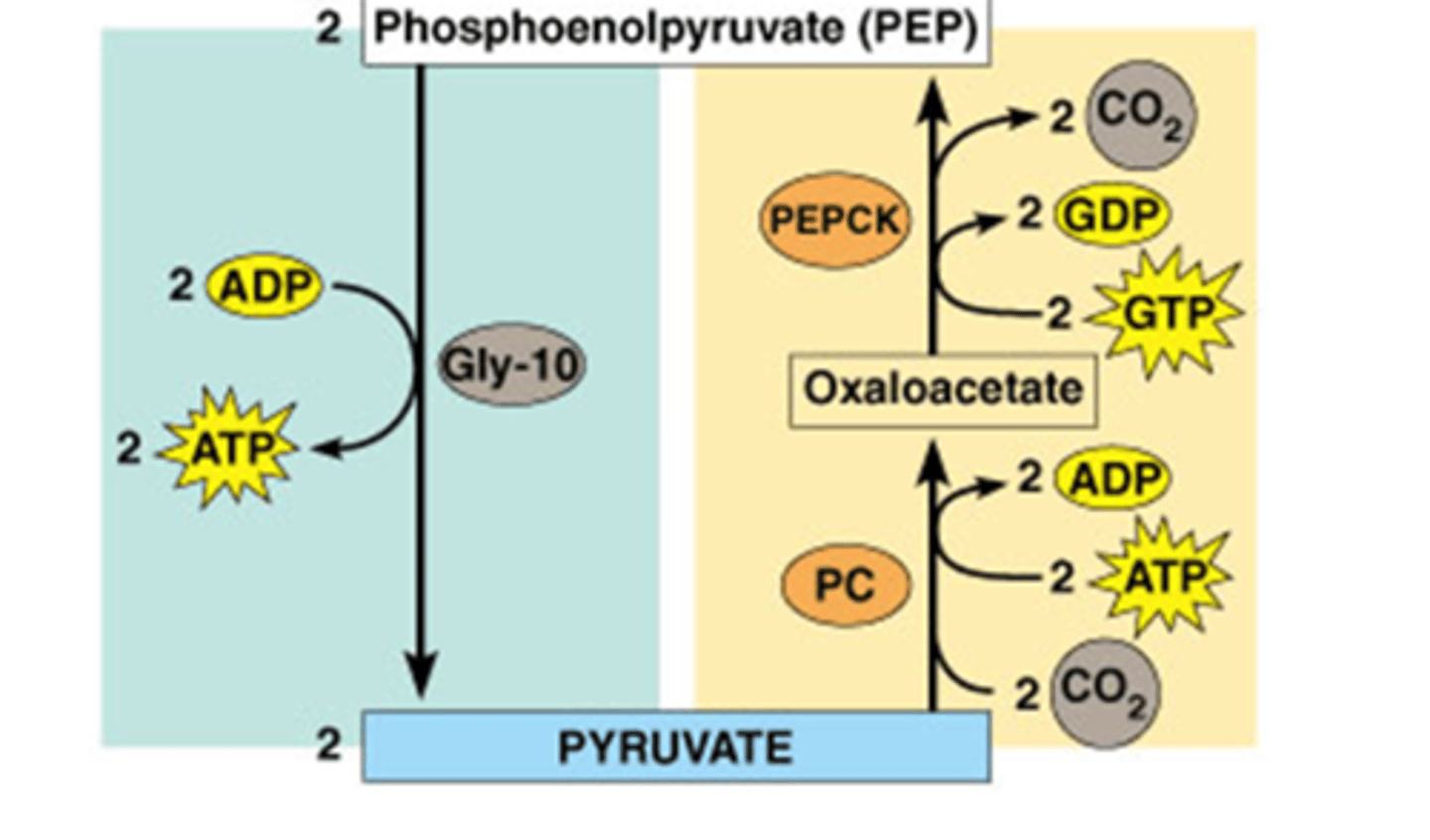
Hoe bypassen we stap 4, 5, 6, 7, 8 en 9 van de glycolyse?
Dit zijn perfect omkeerbare reacties, no worries dus
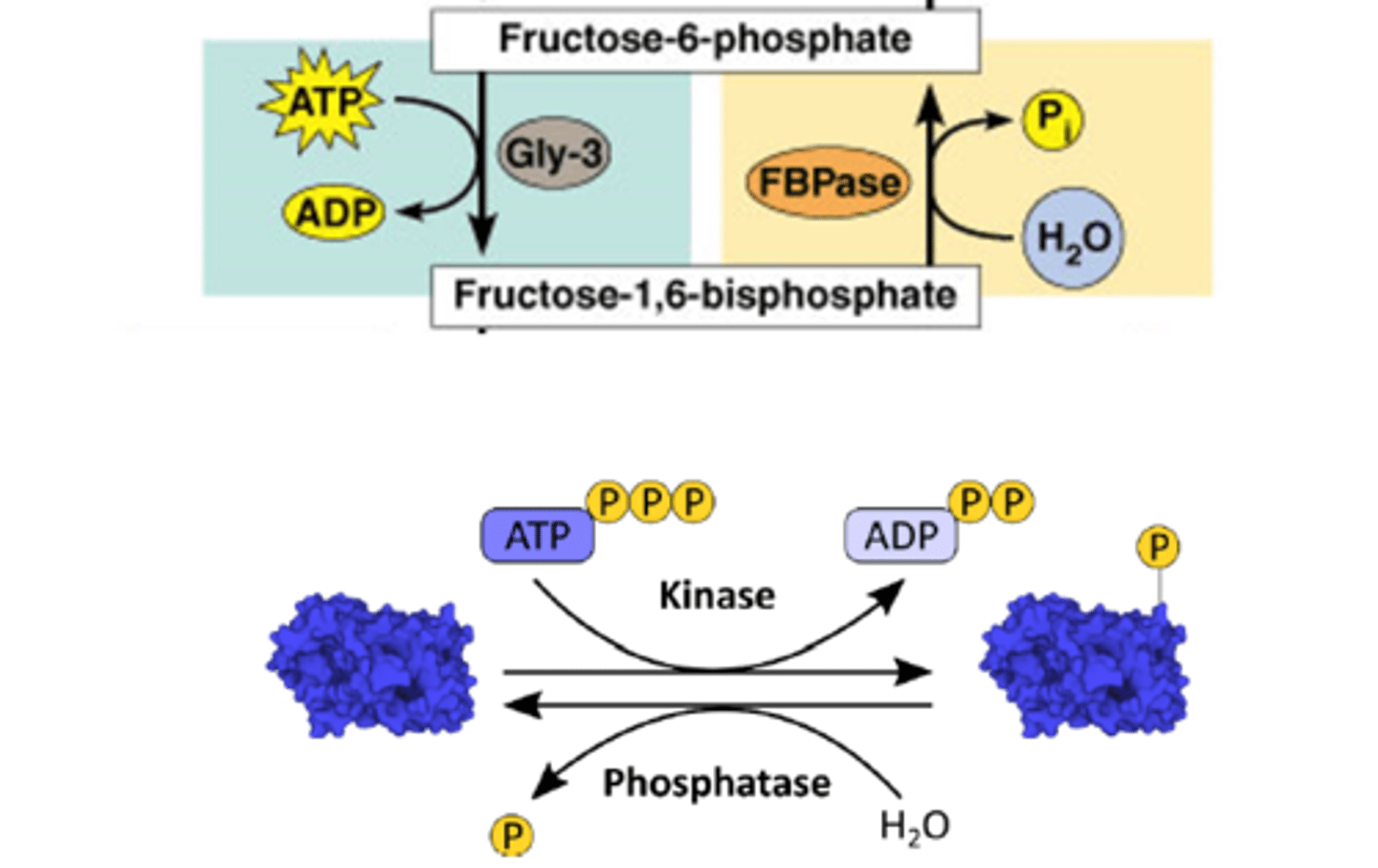
hoe bypassen we stap 3 van de glycolyse?
defosforylatie van fructose-1,6 - bisphosfaat naar fructose-6- fosfaat door een fosfatase
enzyme voor gluconeogenese: fructose 1,6-bisfosfatase is een hydrolase
enzyme voor de glycolyse: fosfofructokinase-1 is een transferase
zie onderste foto voor de link tussen kinasen en fosfatasen
hoe bypassen we stap 2 van de glycolyse?
die is gewoon omkeerbaar :))
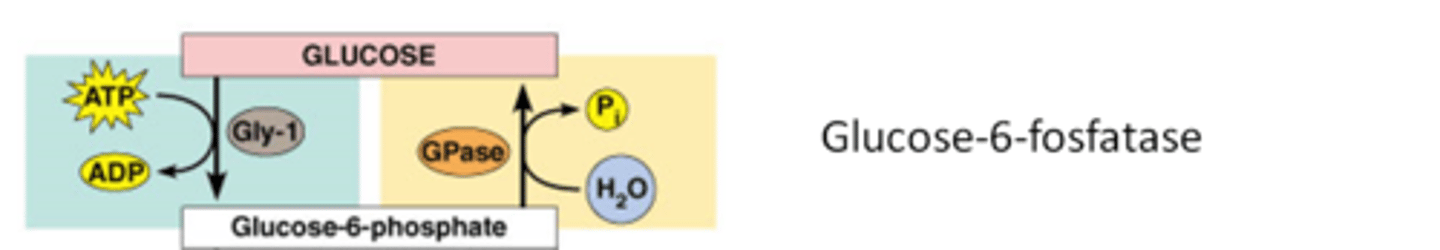
hoe bypassen we stap 1 van de glycolyse?
deze gebeurt eigenlijk alleen in de lever voor de bloedsuikerspiegel op pijl te houden, alle andere cellen gebruiken gewoon de glucose-1-fosfaat
glucose-6-fosfaat wordt gehydrolyseerd (door toevoeging van water) door glucose-6-fosfatase. Het enzym verwijdert een fosfaatgroep (Pi) van glucose-6-fosfaat, waardoor vrije glucose en een anorganische fosfaat (Pi) ontstaan.
Wat is de energiebalans van de glycolyse versus de gluconeogenese
omdat de gluconeogenese niet zomaar het tegenovergestelde is dan de glycolyse is er een andere stoichiometrie.
er moeten 4 fosfoanhydride bindingen EXTRA moeten geïnvesteerd worden (tov ‘omgekeerde glycolyse’) om de reactie exergonisch te maken in de richting van glucose.
∆G°’ gluconeogenese = +20 kcal/mol (=‘omgekeerde glycolyse’) – 4 x (7,3 kcal/mol) = -9,2 kcal/mol
9.8 Regeling van glycolyse en gluconeogenese
Waarom is de glycolyse en de gluconeogenese zo sterk geregeld?
Gelijktijdige activiteit van beide reactiewegen zou energetisch zeer belastend zijn voor de cel (hydrolyse van 4 fosfoanhydride bindingen per cyclus).
Om te vermijden dat beide reactiewegen samen actief zijn, worden de hoeveelheid en de activiteit van de enzymen van beide reactiewegen sterk gecontroleerd.
Hoe wordt de glycolyse en gluconeogenese geregeld?
Via allostere regeling
Via de hormonale regeling
Er is ook een ruimtelijke scheiding, aangezien de gluconeogenese vooral in de lever en beetje in de nieren voorkomt.
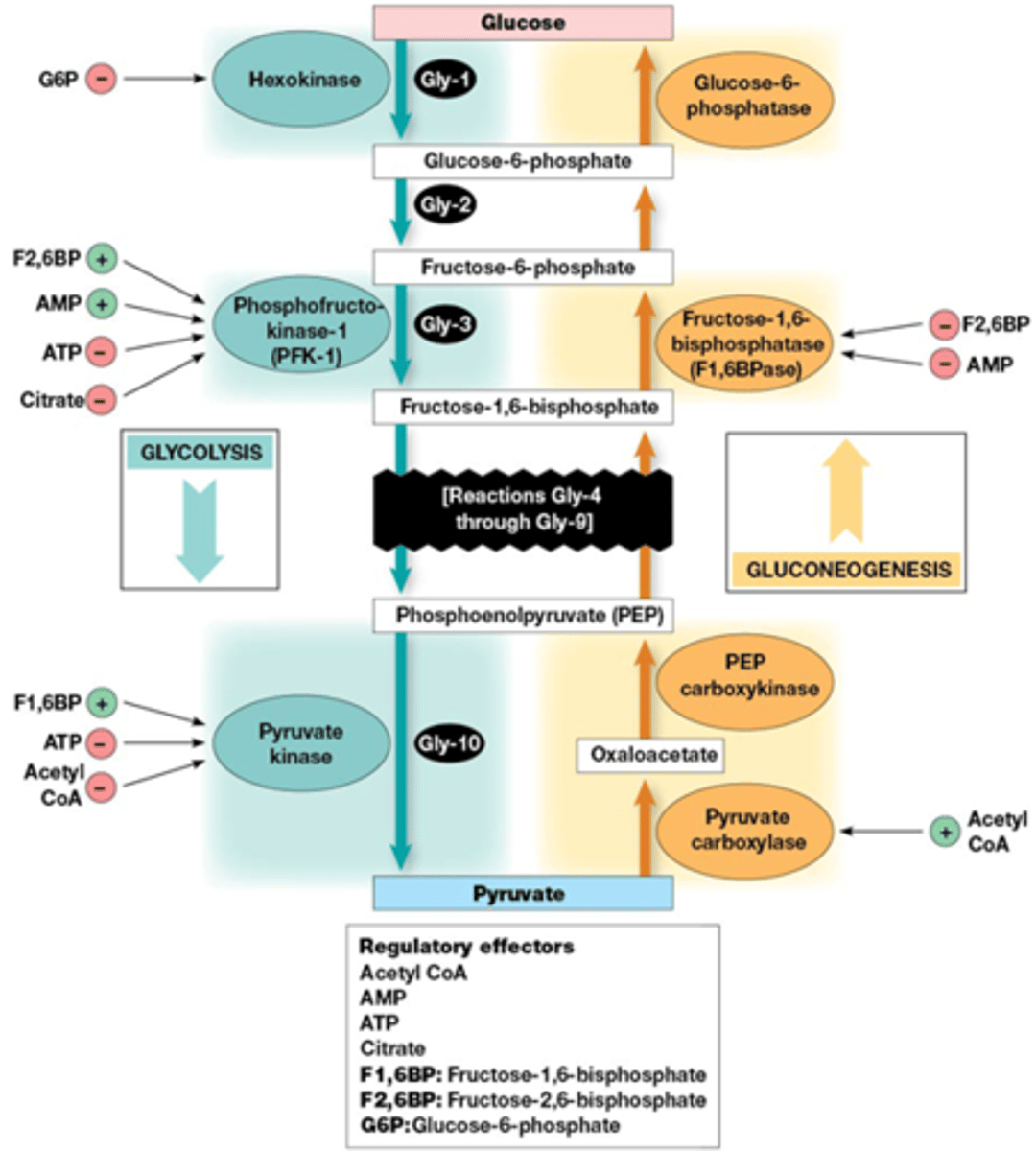
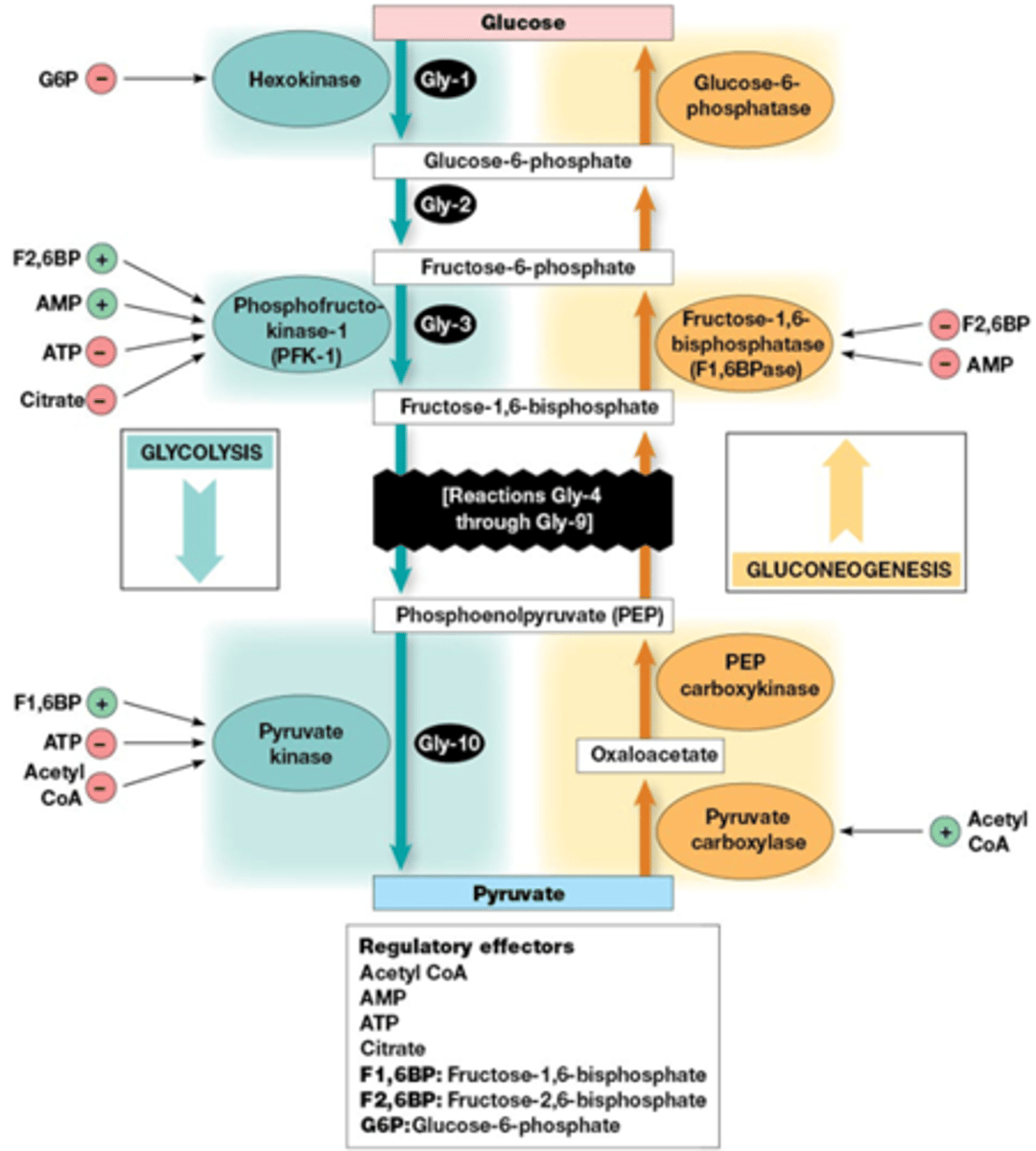
Hoe werkt de allostere regeling?
1) monitoring van voorraad energie (vb. spiercontractie)
->AMP stimuleert PFK-1, inhibeert FBPase-1
->ATP inhibeert PFK-1, inhibeert PK
->Citraat inhibeert PFK-1
->acetyl CoA inhibeert PK
2) monitoring van precursoren voor biosynthese
->Citraat inhibeert PFK-1
->Acetyl CoA stimuleert PC
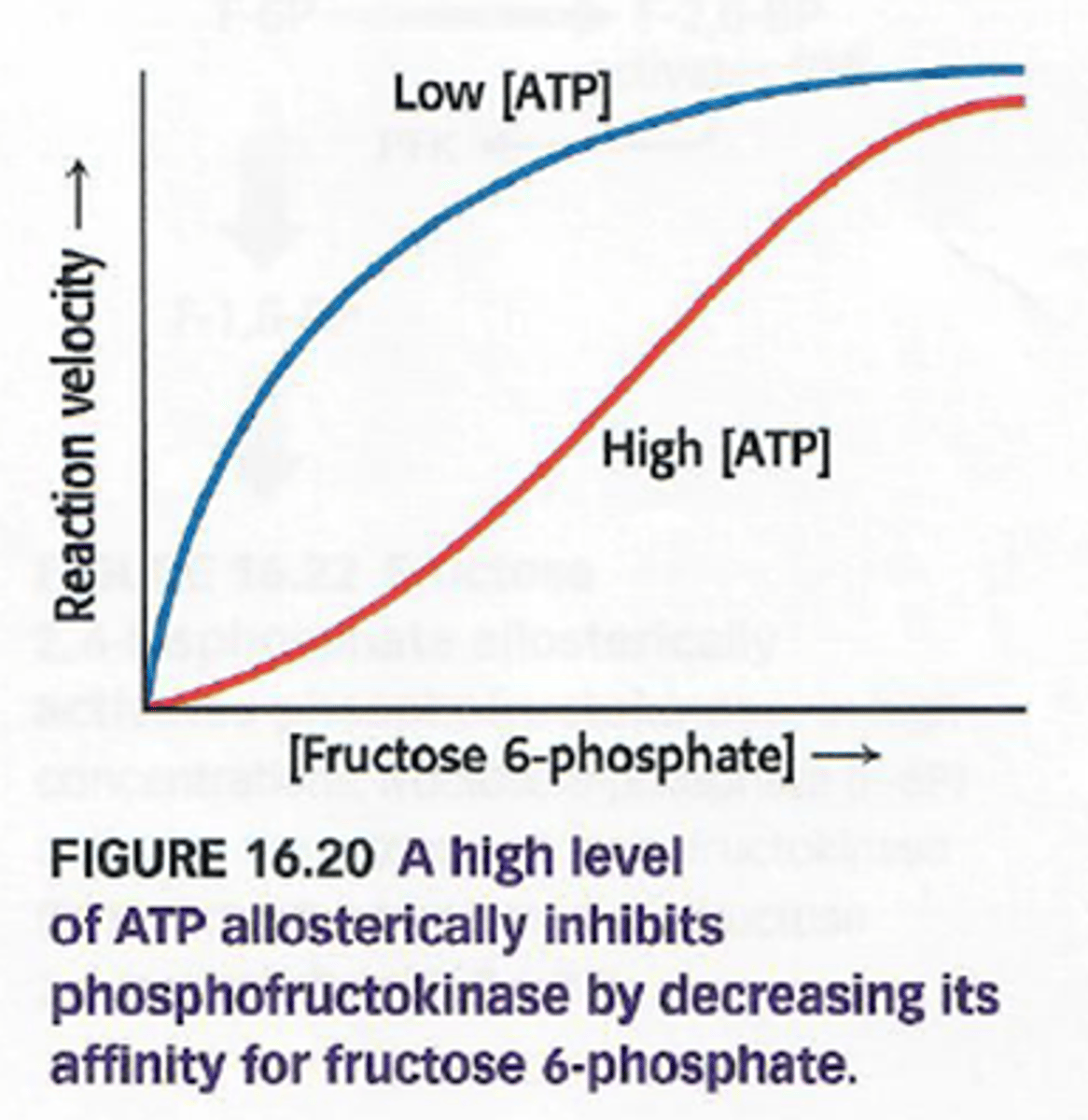
Hoe kan het dat ATP tegelijk substraat en allosterische inhibitor van PFK-1.
de Km van de actieve site voor ATP is veel kleiner dan de Km van de allostere site voor ATP
->bij lage concentratie gaat er vooral ATP op de actieve site zijn
Wat is het doel van de hormonale regeling?
op peil houden van [glucose] in het bloed= een van de belangrijkste functies van de lever
Hoe werkt de hormonale regeling?
we willen de [fructose-2,6-bisfosfaat*] regelen
-> het bifunctioneel enzyme PFK-2/FBPase-2 is hiervoor verantwoordelijk
PFK-2 is een kinase die F-6-P zal fosforyleren
FBPase-2 is een fosfatase dat een fosfaatgroep zal verwijderen
PKA (proteine kinase) wordt geactiveerd door cAMP en zal de omzetting doen van
PFK-2 -> FBPase-2
het enzyme wordt geregeld door omkeerbare fosforylatie.
*fructose-2,6-bisfosfaat wordt ook afgekort als F-2,6-BP, dit is een regulator van de glycolyse, geen substraat (dat is F1-6BP)
![<p>we willen de [fructose-2,6-bisfosfaat*] regelen</p><p>-> het bifunctioneel enzyme PFK-2/FBPase-2 is hiervoor verantwoordelijk</p><p>PFK-2 is een kinase die F-6-P zal fosforyleren</p><p>FBPase-2 is een fosfatase dat een fosfaatgroep zal verwijderen</p><p>PKA (proteine kinase) wordt geactiveerd door cAMP en zal de omzetting doen van </p><p>PFK-2 -> FBPase-2</p><p>het enzyme wordt geregeld door omkeerbare fosforylatie.</p><p>*fructose-2,6-bisfosfaat wordt ook afgekort als F-2,6-BP, dit is een regulator van de glycolyse, geen substraat (dat is F1-6BP)</p>](https://knowt-user-attachments.s3.amazonaws.com/b20b932f-e87d-4432-a226-3e83869bb715.png)
Wat gebeurt er als glucose laag is? Wat gebeurt er als glucose hoog is?
[glucose] laag => [glucagon] hoog => [cAMP] in lever hoog => fosforylatie van PFK-2/FBPase-2 door PKA => activering van FBPase-2, inhibitie van PFK-2 => [F-2,6-BP] daalt => gluconeogenese overheerst
[glucose] hoog => [insulin] hoog => [cAMP] in lever laag => defosforylatie van PFK-2/FBPase-2 => activering van PFK-2, inhibitie van FBPase-2 => [F-2,6-BP] stijgt => glycolyse overheerst
![<p>[glucose] laag => [glucagon] hoog => [cAMP] in lever hoog => fosforylatie van PFK-2/FBPase-2 door PKA => activering van FBPase-2, inhibitie van PFK-2 => [F-2,6-BP] daalt => gluconeogenese overheerst</p><p>[glucose] hoog => [insulin] hoog => [cAMP] in lever laag => defosforylatie van PFK-2/FBPase-2 => activering van PFK-2, inhibitie van FBPase-2 => [F-2,6-BP] stijgt => glycolyse overheerst</p>](https://knowt-user-attachments.s3.amazonaws.com/c2d54275-67c2-4e5d-a83b-f20b601a35ec.png)
Waarom is de hormonale regeling eigenlijk ook een allostere regeling?
De hormonen zorgen voor meer of minder F2,6BP
F2,6BP is deel van de allostere regeling
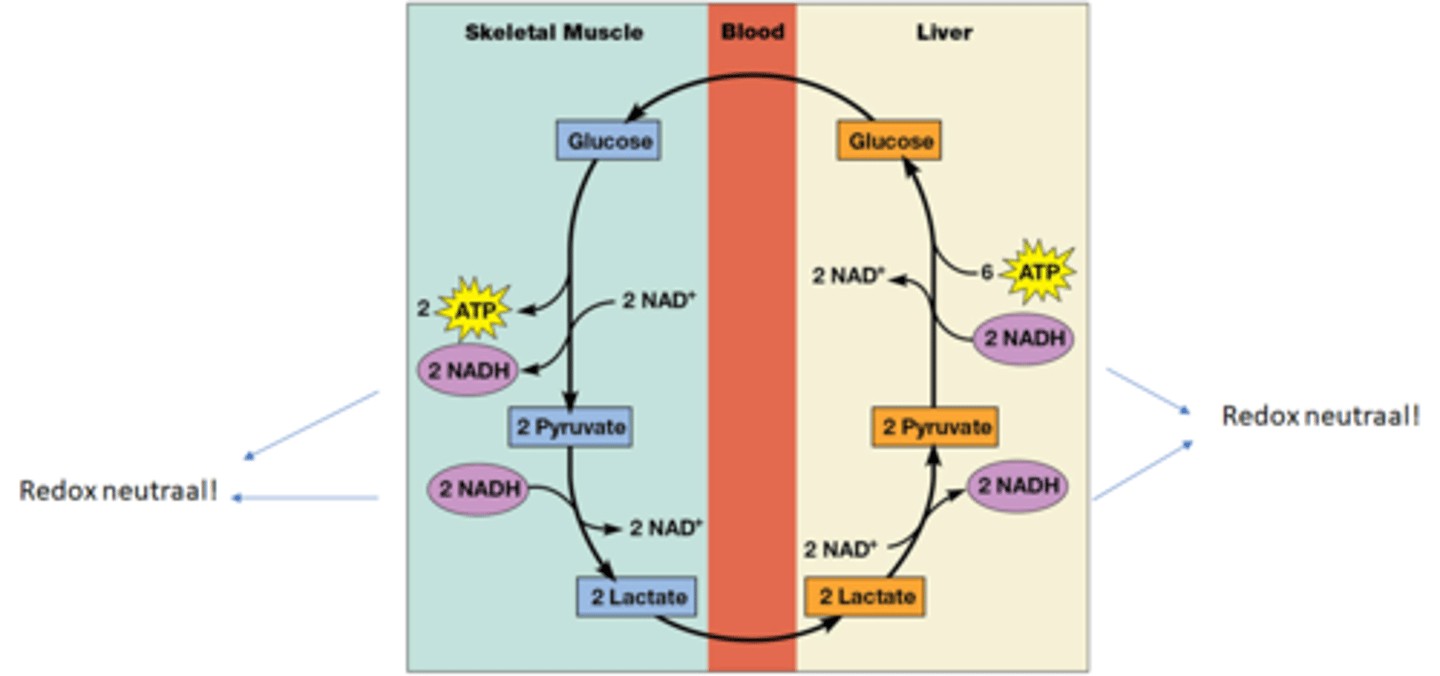
Hoe wordt lactaat terug omgezet in pyruvaat?
Via de cori cyclus: coördinatie tussen organen
-Lactaat wordt gecreerd in de spieren door glycolyse+lactaat fermentatie
-Lactaat gaat diffunderen naar het bloed
-het bloed vervoert het naar de lever
-In de lever wordt lactaat omgezet in de pyruvaat
-door de gluconeogenese gaat pyruvaat omgezet worden in glucose
Welke conclusies kunnen getrokken worden uit nieuwe onderzoeken over de glycolyse?
moonlighting: de enzymen uit de glycolyse hebben ook heel andere functie hebben
deze wijzigingen kunnen een gevolg zijn van een ander celtype, subcellulaire lokalisatie, conformatie, liganden, substraten, producten, cofactoren, interacties met DNA, RNA, andere eiwitten, membranen …
Wat zijn isotopen?
Isotopen zijn varianten van eenzelfde element met
•eenzelfde aantal protonen (p) (atoomnummer)
•een verschillend aantal neutronen (n) vb. 13C, 15N, 18O, 2H, 14C (massagetal=p+n)
•dezelfde chemische eigenschappen
radio isotoop (bv 14C) vs stabiel isotoop (bv 13C)
natuurlijke abundantie van isotopen
Toepassing: opvolgen van een atoom in een component doorheen een reeks chemische reacties
Detectie stabiele isotopen:
-nucleair magnetic resonance NMR
-massa spectrometrie MS
detectie radioactieve isotopen
-α, β, γ counter
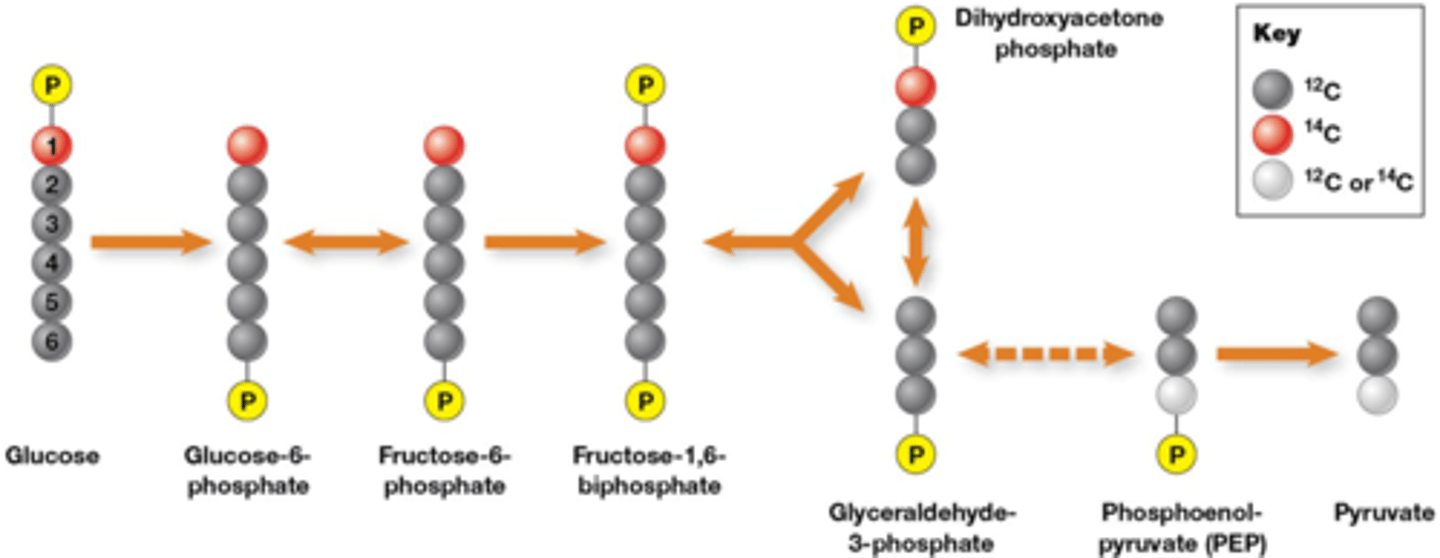
Wat is isotopic labeling
een radioactieve 14C wordt toegediend als substraat
->Koolstof 1 vervangen door radioactief 14C isotoop
-ze gaan door chromatografie celextracten scheiden
-ze gaan detecteren waar de radioactieve isotoop zit
-ze gaan nagaan welke moleculen daarin zitten via massaspectometrie
gevolg: de helft van de pyruvaat heeft een radioactieve isotoop omdat
Door het merken kan men dus nagaan hoe die koolstof 1 zich gedraagt in de glycolyse
Wat is massa spectrometrie
We willen nagaan in welk molecule het zwaardere isotoop zit via massa spectrometrie
-het bepaalt heel nauwkeurig de massa gedeeld door de lading van moleculen
->je krijgt een massaspectrum van een molecule en van fragmenten van het molecule
-je kan die vergelijken met de theoretische waarden waardoor we de positie van de zwaardere isotoop kunnen terugvinden
hierdoor kan je ook eiwitten identificeren, door die via proteasen op te splitsen tot peptiden
->alle peptiden meten via een massa spectrometrie
