8. Enzīmu aktivitātes regulācija (signālceļi), vitamīni - bioloģiskie katalizatori
1/78
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
79 Terms
Bioķīmiskās reakcijas ir sakārtotas metaboliskajos ceļos - PRINCIPS
- katrs produkts ir izejviela nākamajai enzimātiskajai reakcijai
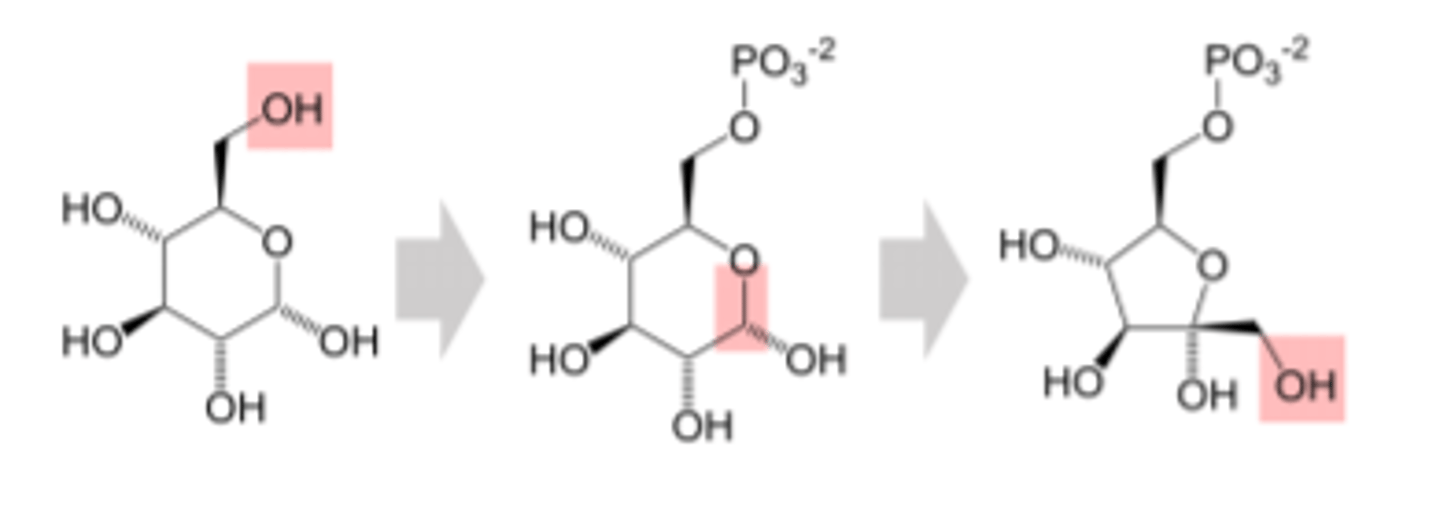
Metaboliskie ceļi
no metaboliskā ceļa substrāta iegūst produktu
visi starpā - metaboliskā ceļa starpsavienojumi

metaboliskie cikli
ja produktu var izmantot, lai atkal iegūtu sākotnējo substrātu
Krebsa cikls
Kādas ir metabolisko ceļu funkcijas?
•Enerģijas ieguve
•Enerģijas uzkrāšana
•Organisma strukturālo komponenšu veidošana
•Atkritumvielu izvadīšana
Katabolisms
= barības vielu un citu organismā esošo vielu noārdīšana, lai iegūtu materiālu un enerģiju anabolismam.
(iegūstam ATF)
Katabolismā organismā esošie biopolimēri vispirms tiek noārdīti līdz monomēriem, bet monomēri - līdz vēl sīkākām vienībām.
Anabolisms
visu organismam nepieciešamo vielu sintēze.
Sinonīms anabolismam
plastiskā vielmaiņa
asimilācija
Sinonīms katabolismam
enerģētiskā vielmaiņa
disimilācija
Kas ir metabolīti?
= ķīmiskās vielas, kas iesaistās metabolajās reakcijās (gan produkti, gan substrāti, gan starpsavienojumi)
Cilvēka šūnu metaboliskie ceļi
- aktīvi tikai noteikti ceļi, jo šūnas ir specializētas

Kā var intracelulāri ietekmēt metabolismu?
• Substrāta pieejamība
• Enzīma aktivitātes regulācija (kovalentā, allostēriskā, u.c.)
• «Atslēgas» enzīmu daudzuma regulācija
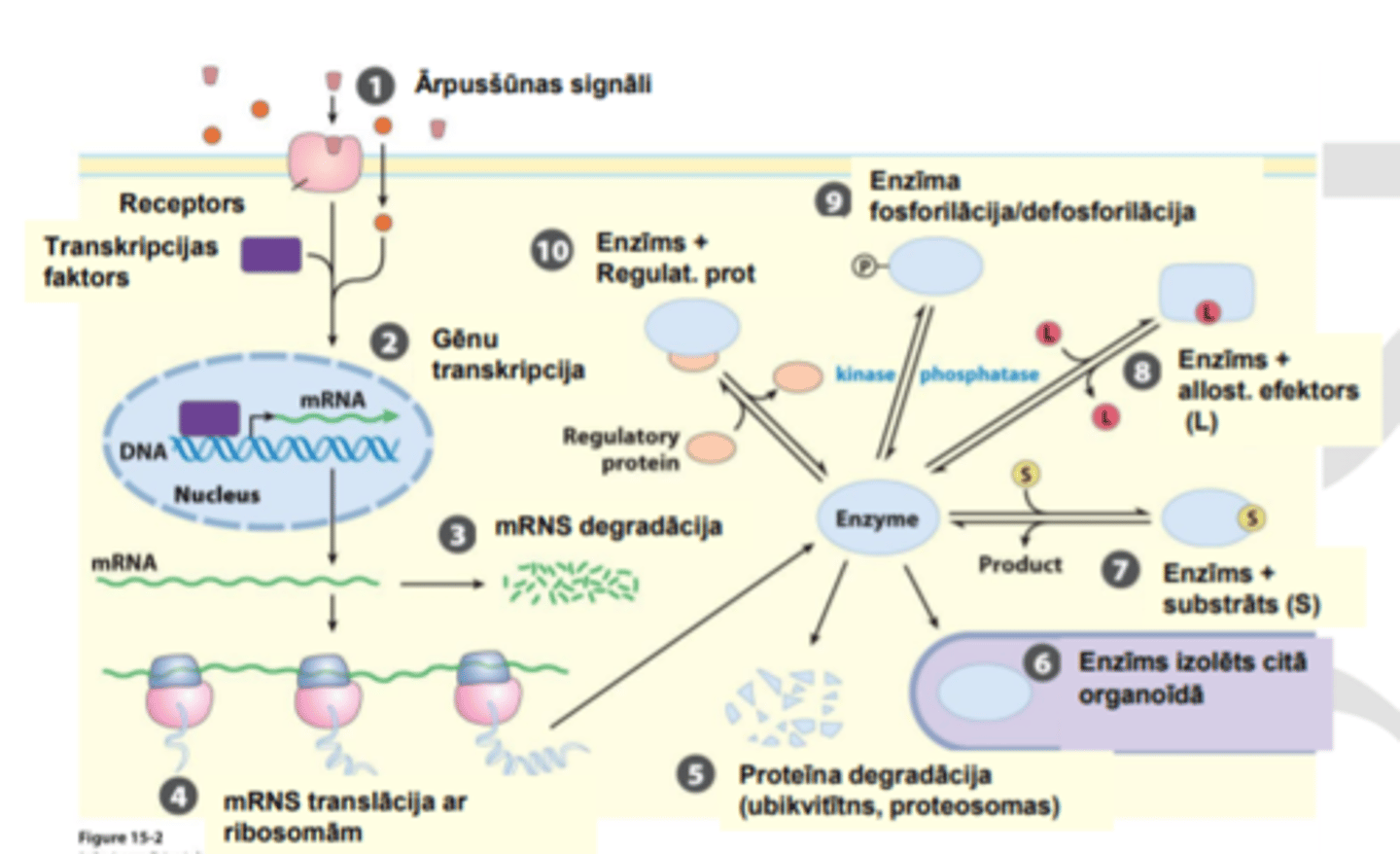
No kādiem faktoriem atkarīgs bioķīmisko reakciju ātrums?
•Substrāta un produkta daudzuma attiecība
•Katalizatora aktivitāte
- Enzīma koncentrācija
- Translācijas un degradācijas ātruma attiecība
- Paša enzīma aktivitāte
- Atkarīga no substrāta, efektoriem, enzīma modifikācijām
•Efektoru koncentrācija
- Allostēriskie efektorei
- Konkurējošas substances (gan substrāti, gan inhibitori)
- pH, joni
•Temperatūra
Reakcijas ātrums ir atkarīgs no substrāta koncentrācijas
•Ātruma izmaiņas ir ievērojamākas pie zemām koncentrācijām.
(Substrāts un enzīms «satiekas» biežāk )
•Ja substrāta koncentrācija ir augsta, koncentrācijas izmaiņas vājāk ietekmē ātrumu.
(Enzīms kļūst piesātināts ar substrātu)
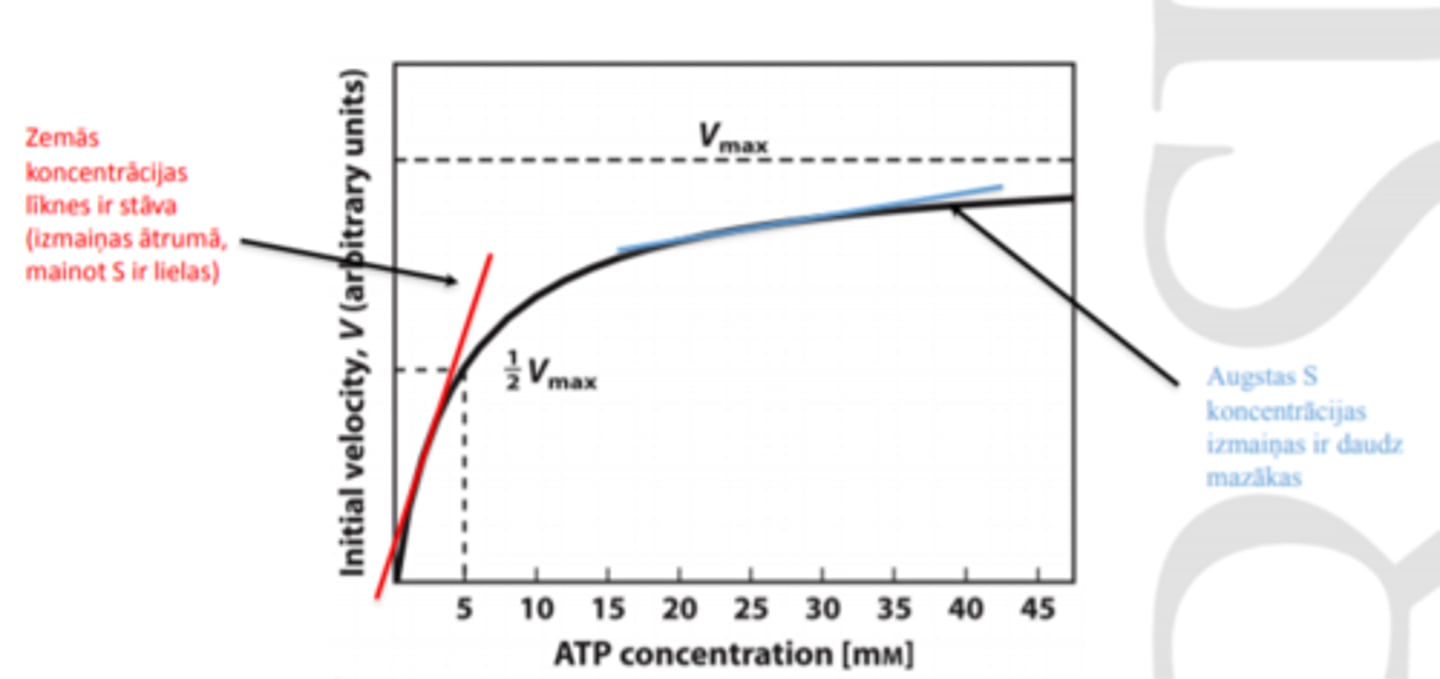
Km un metbolīta koncentrācijas ietekme uz reakcijas ātrumu
Daudzu enzīmu Km būs tuva vai lielāka nekā substrāta fizioloģiskā koncentrācija.
Īpaši enzīmiem, kas strādā ar ATF vai NAD(H)
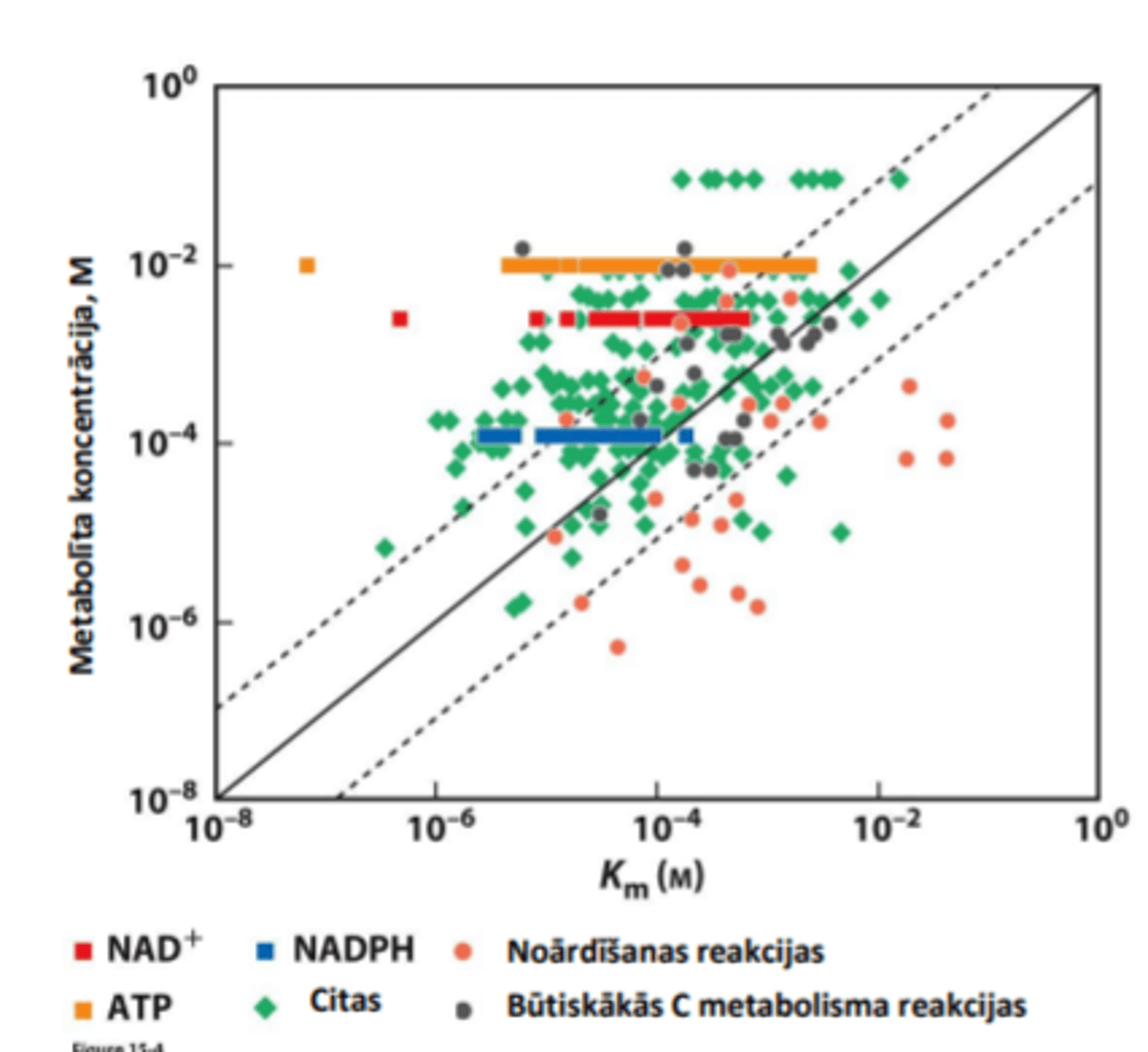
Kā kinētiskie parametri ietekmē enzīma īpašības?
Izozīmi (izoenzīmi) - ir atšķirīgi proteīni, kas katalizē to pašu reakciju

Kā bioķīmisko reakc. v ietekmē katalizatora aktivitāte (enzīma konc., translācijas un degradācijas ātruma attiecība)?
- proteīnu dzīves ilgums ir noteikts (atkarīgs no audiem - daži enzīmi vairākas dienas pastāv, acs lēcas proteīni - visu mūžu)
Kā tiek regulēts proteīnu dzīves ilgums? (tas ietekmē bioķīmisko reakciju ātrumu)
Proteīnus ražo ribosomas,
noārda proteosomas (atsevišķus proteīnus)
vai lizosomas (noārda lielākus organoīdus,..)
lai iezīmētu proteīnu noārdīšanai, proteīns tiek ubikvitinēts
Proteīnu ubikvitinēšana - nozīme, princips
lai iezīmētu proteīnu noārdīšanai, proteīns tiek ubikvitinēts
(ubikvitīns - neliels regulatorais proteīns, ir visos eikariotu audos)
- tā ir kovalentā modifikācija
- ubikvitīni tiek pievienoti noteiktā secībā (tas arī nosaka to, kas notiks ar proteīnu)
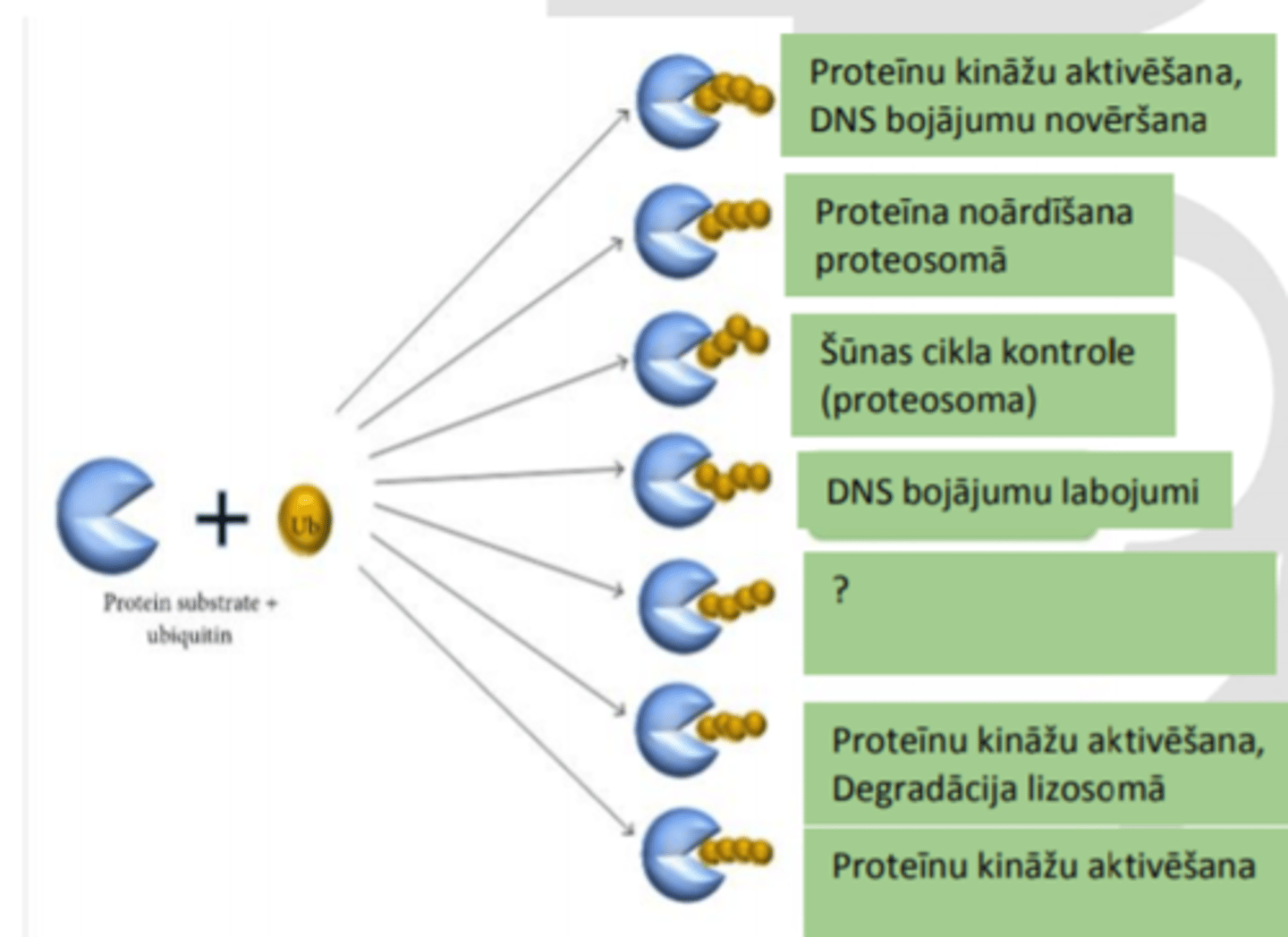
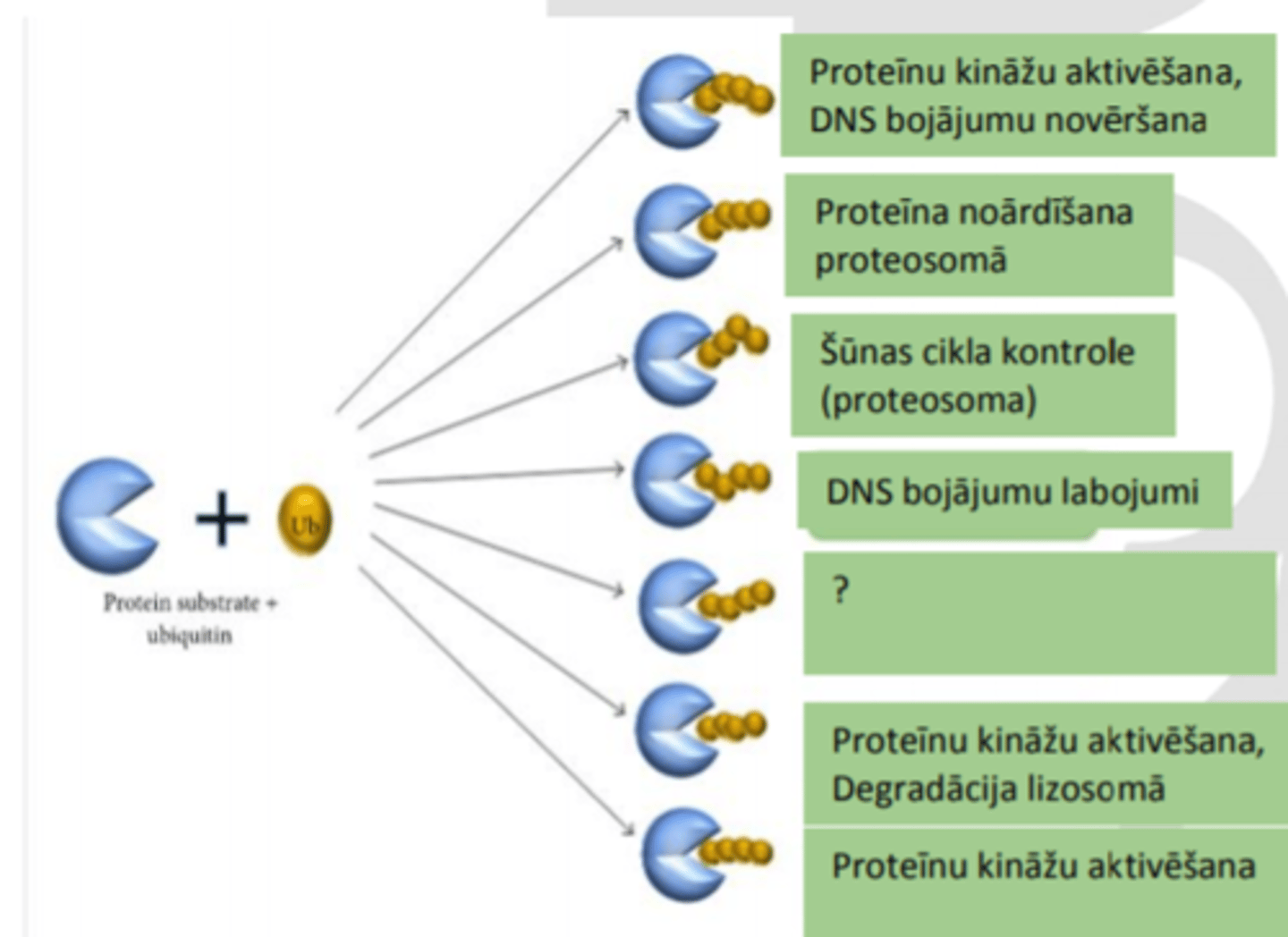
Kas var notikt ar ubikvitinētiem proteīniem?
Ubikvitinēti proteīni var tikt noārdīti, pārvietoti uz citām organellām, mainīt aktivitāti, iegūt vai zaudēt spēju saistīties ar citiem proteīniem.
Atgriezeniskā regulācija (arī ietekmē reakcijas ātrumu)
Bieži metabolisko ceļu galaprodukti tieši vai netieši inhibē tos izveidojušos metaboliskos ceļus.
-Piemēram: augsta ATF koncentrācija inhibē glikolīzi un novērš tālāku glikozes noārdīšanu.

ATF, AMF nozīme šūnā
= tie ir vieni no svarīgākajiem metabolisma regulatoriem šūnā
10% [ATF] samazinājums būtiski ietekmē ATF atkarīgo enzīmu aktivitāti.
10% [ATF] samazinājums krasi paaugstina [AMF]. AMF ir spēcīgāks allosteriskais regulators
![<p>= tie ir vieni no svarīgākajiem metabolisma regulatoriem šūnā</p><p>10% [ATF] samazinājums būtiski ietekmē ATF atkarīgo enzīmu aktivitāti.</p><p>10% [ATF] samazinājums krasi paaugstina [AMF]. AMF ir spēcīgāks allosteriskais regulators</p>](https://knowt-user-attachments.s3.amazonaws.com/f03a6bdd-dad2-4ad1-a0c1-60e817ce2e5d.png)
Kāda ir atgriezeniskās reakcijas būtība?
būtība - izvairīties no resursu «sagrābšanas»

Vai visi enzīmi metaboliskajos ceļos tiek regulēti?
NĒ
= regulēti tikai tie, kuri rada vislielāko ietekmi uz metabolisko ceļu
Kādas reakcijas metaboliskajos ceļos parasti tiek regulētas?
tās, kuras atrodas tālu no līdzsvara punkta
Metaboliskajos ceļos lielākā daļa reakciju atrodas tuvu līdzsvara stāvoklim (2. un 3. reakcija), bet ne pilnīgā līdzsvarā, kas nodrošina metabolītu plūsmu cauri ceļam
Atslēgas enzīmi atrodas tālu no līdzsvara (piem 1. enzīms) •Šādus enzīmus regulēs
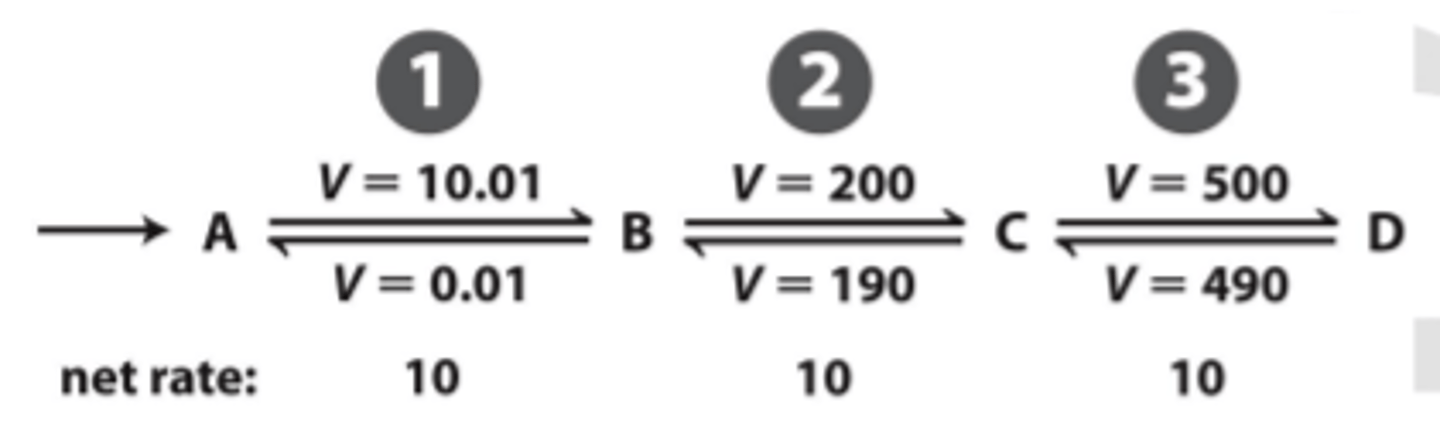
Kā var kontrolēt plūsmu ar reakcijas ātrumu?
pirmais enzīms, kurš nelielu skaitu substrāta var pārvērst, nosaka reakcijas ātrumu (tas ir ātrumu ierobežojošais solis)
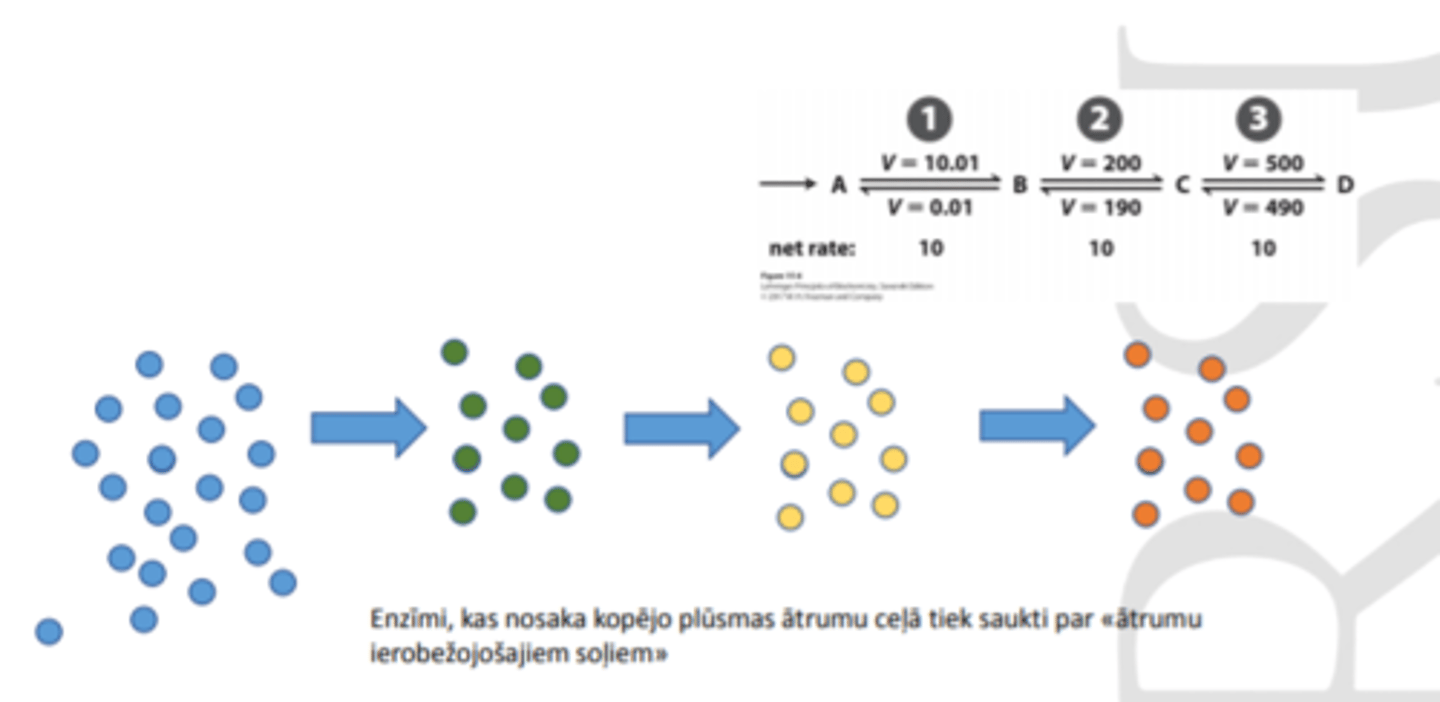
Kā var kontrolēt plūsmu ar reakcijas virzienu?
lai regulētu kopējās plūsmas virzienu, vajag regulēt enzīmus, kas atrodas tālu no līdzsvara punkta
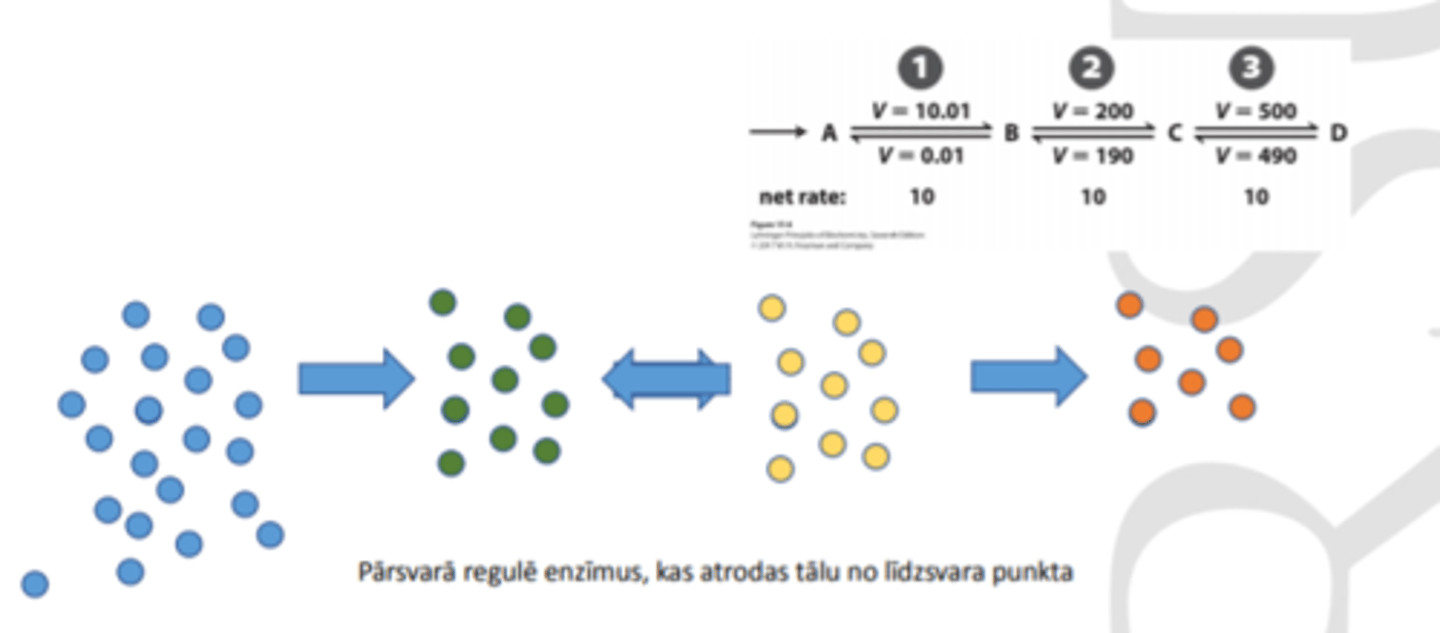
Zinot metabolītu koncentrācijas, var noteikt enzīmu, kurš ietekmēs reakcijas ātrumu visvairāk:
- iekrāsoti tie enzīmi, kas tiek regulēti
1. enzīms noteiks kopējo plūsmas ātrumu (jo glikozes koncentrācija ir lielāka nekā pārējo starproduktu koncentrācija - 1 . ir vislēnākais solis (limitējošais)

Metaboliskie ceļi savā starpā mijiedarbojas un dala metabolītus
Bieži tiek regulēti enzīmi metaboliskajos ceļos, kas dala metabolītus, bet tiek realizēti ar dažādiem enzīmiem.
ietekmēt labāk enzīmus, kuri netiek dalīti metaboliskajās reakcijās
Kas ir Saistošais solis (commited step)?
Ja vairāki ceļiem ir kopīgi pirmie soļi, tad ..pirmā enzimātiskā reakcija, kas «piesaista» metabolītu kādam noteiktam ceļam tiek saukta par saistošo soli.
= ķīmiskā reakcija, kas nodrošina metabolītu plūsmu tieši šajā metaboliskajā ceļā
Fosfofruktokināzes (tā ir saistošais solis glikolīzē) regulācija

Kas ir vitamīni?
=molekulas, kas nepieciešamas metabolisma norisei.
= organiska molekula (vai radniecisku molekulu kopa), kas ir kas organismam ir nepieciešama nelielos daudzumos, lai nodrošinātu tā funkcijas.
Kā vitamīni tiek sintezēti?
Vitamīnus organisms nesintizē vai sintezē nepietiekošos daudzumos, tādēļ tie papildus jāuzņem ar uzturu.
Kas ir vitamēri?
=organisko savienojumu kopums, kas uzrāda vitamīna aktivitāti.
Vitamīni ir molekulas, kas nepieciešamas metabolisma norisei.
- ir enzīmu kofaktori (arī minerālvielas)
Taukos šķīstošie vitamīni
K, E, D, A
Ūdenī šķīstošie vitamīni
B, C

Taukos šķīstošie vitamīni - īpašības
Var tikt uzkrāti audos
A un D vitamīniem hormonu daba.
K vitamīns vienīgais, kuram ir kofaktora daba.
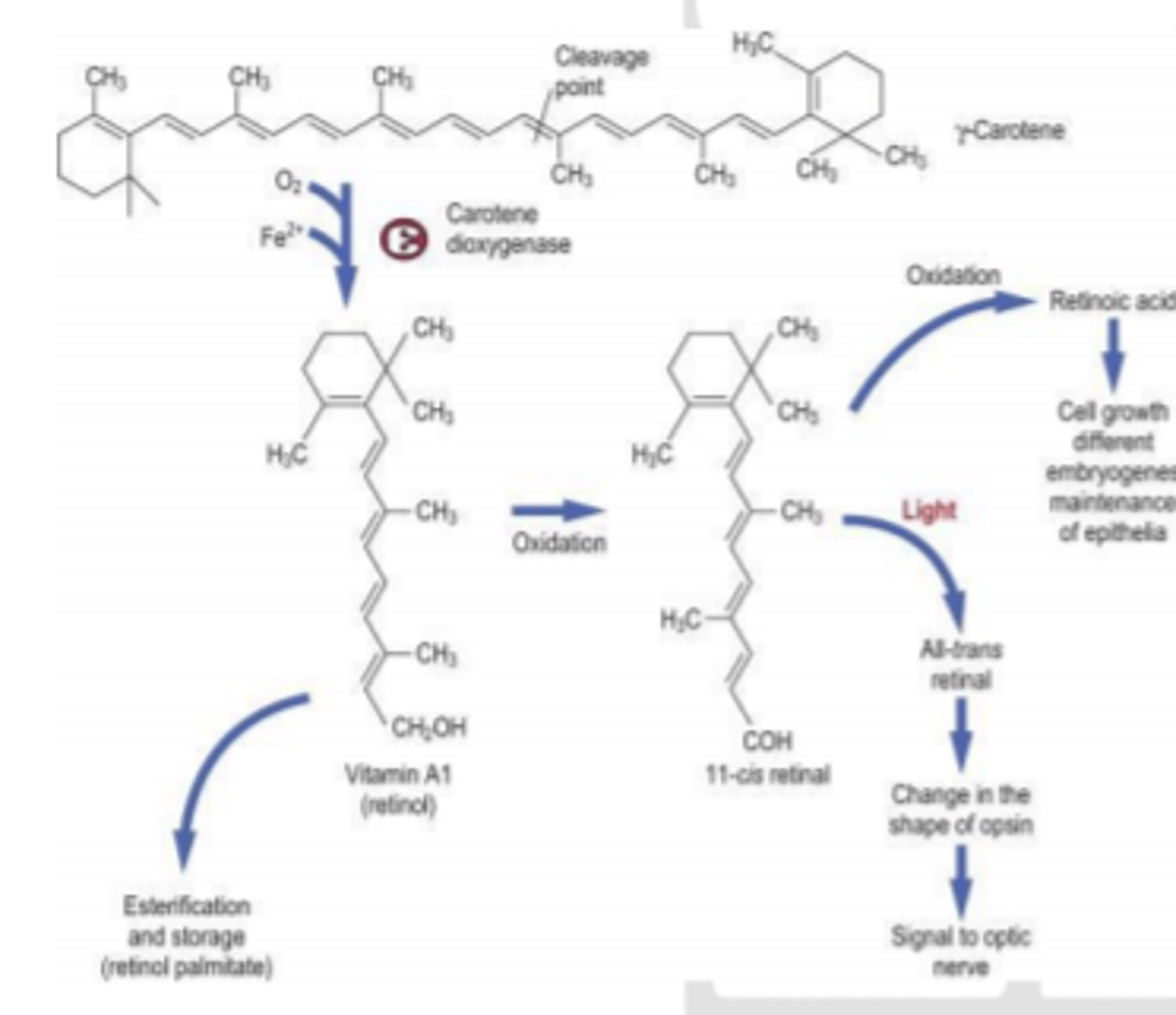
A vitamīns (nosaukums)
retinols, retināls un retīnskābe

A vitamīns - retinols, retināls un retīnskābe
Provitamīns - β-karotīns
Tiek uzkrāts aknās
Trūkums - redzes problēmas.
retīnskābe - hormonu daba (ietekmē šūnu augšanu, diferenciāciju)
retinols, retināls - redzes pigmenta veidošanās
Pārlieku lielos daudzumos
toksisks
D vitamīns - nosaukums
kalcitriols
D vitamīns - kalcitriols
- kā hormons darbojas (ietekmē gēnu transkripciju)
- ietekmē šūnu dalīšanos un apoptozi
- trūkums izeaisa rahītu bērniem

E vitamīns - nosaukums
tokoferoli
(vitamēri)
E vitamīns - tokoferoli
- antioksidants
- saistīts ar membrānām, lipoproteīniem, tauku nogulsnēm
- aizsargā lipīdus no reaktīvo skābekļa savienojumu (ROS) oksidēšanās
- iesaistīts imūnās funkcijās, šūnu signalizēšanā, gēnu ekspresijā
K vitamīns - nosaukums
fitomenadions, fitonadions, fillohinons
K vitamīns - fitomenadions, fitonadions, fillohinons
- vienīgais kofaktors no visiem lipofīlajiem vitamīniem
- asins recēšanai nepieciešams
- visvairāk augos
- Resnajā zarnā baktēriju ietekmē K1 vitamīns pārveidojas par K2 vitamīnu (aktīvo formu)
- nepieciešams, lai karboksilētu glutamātu
Vai organisms uzkrāj ūdenī šķīstošos vitamīnus?
- tikai B12 uzkrāj
- jebkurš vitamīnu pārpalikums izdalās ar urīnu
B- grupas vitamīni
- nepieciešami normālai pamatvielmaiņai
- ir kofaktori daudzām ogļhidrātu, lipīdu un proteīnu metabolisma reakcijām
B1 nosaukums
tiamīns
B1 tiamīns
- Būtisks ogļhidrātu metabolismā.
- Nepieciešama kā prostētiskā grupa enzīmos 2C vienību
pārvietošanai.
Būtiskākais piemērs piruvāta dehidrogenāze.
Arī α-ketoglutarāta dehidrogenāze, transketolāze
1) Kas spēj sintezēt B1 (tiamīnu)?
2) Kada ir tiamīna aktīvā forma?
1) bakt, sēnes, augi
2) tiamīna pirofosfāts
B2 - nosaukums
riboflavīns
B2 - riboflavīns
- Daļa no FADH2 - reducējošā kofaktora, ko izmanto
dehidrogenāzes.
Enzīmu piemēri: sukcināta dehidrogenāze, mitohondrija
glicerīna fosfāta dehidrogenāze
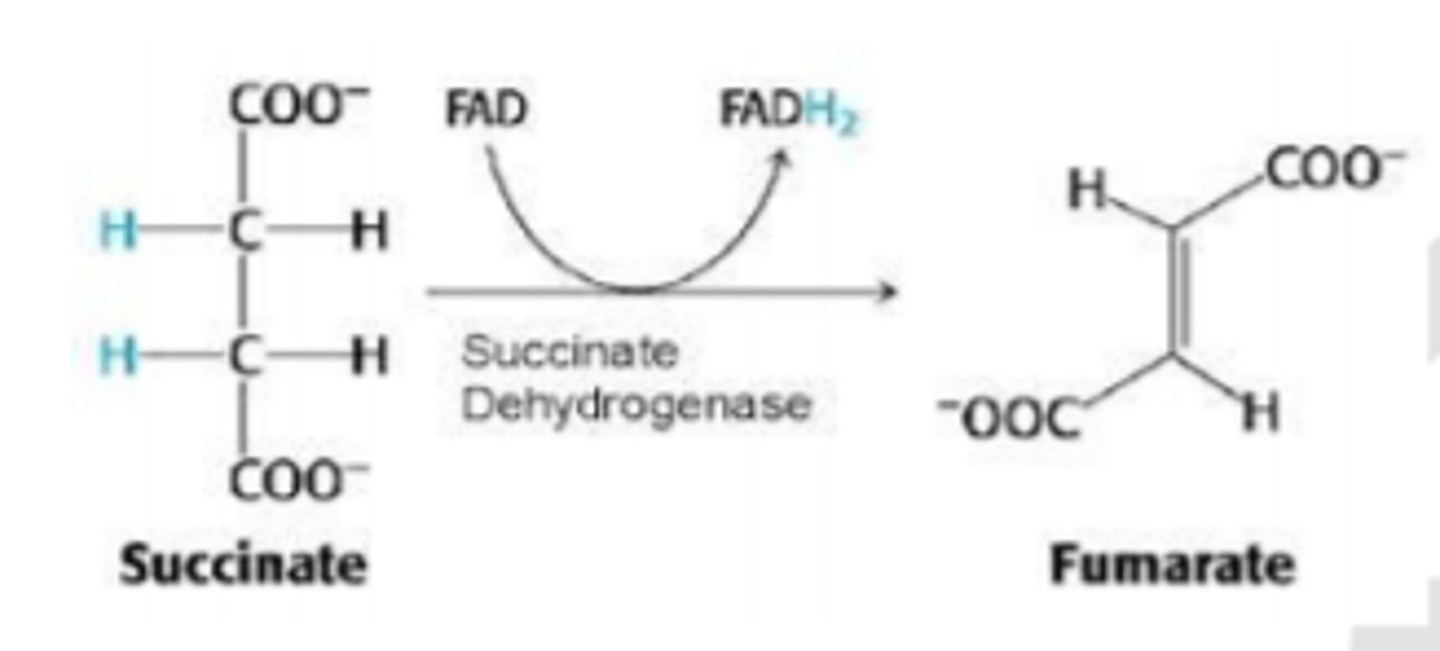
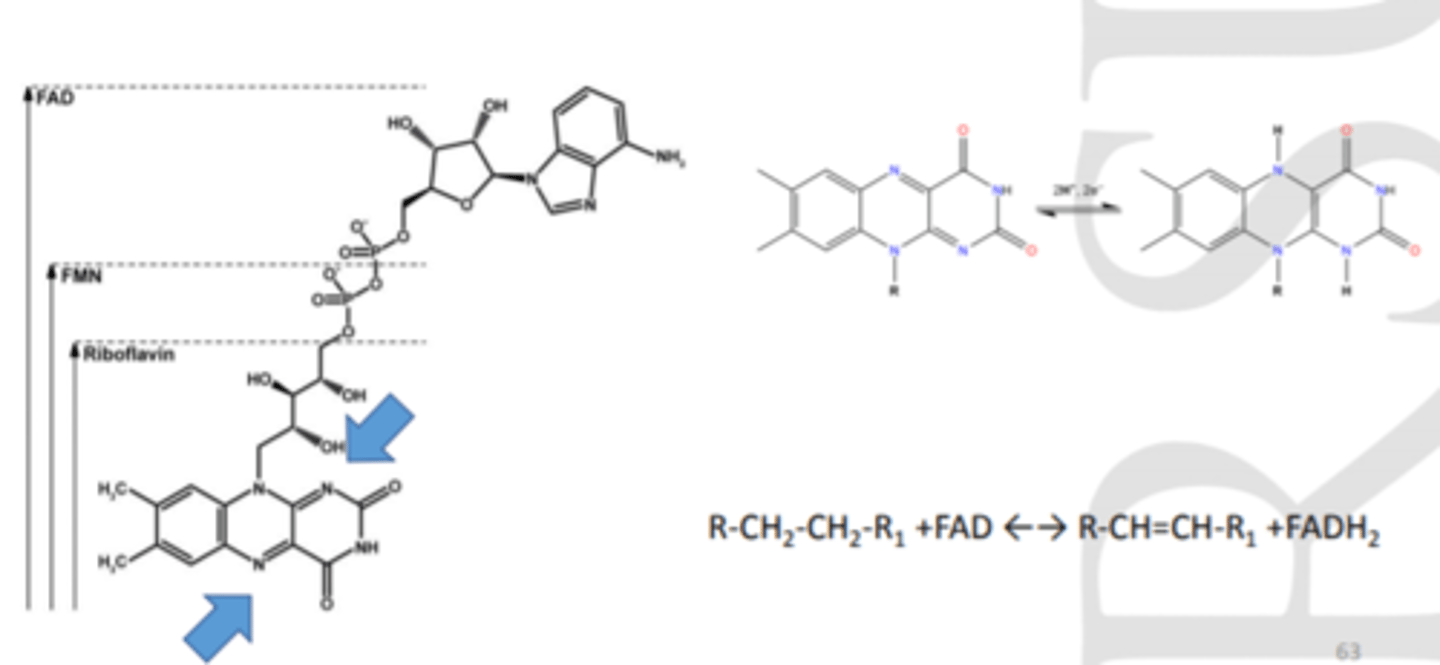
FAD- flavīna adenīna dinukleotīds
flavīna grupa uzņems e- un ūdeņražus
FAD ir spēcīgs oxidētājs. Novērojams reakcijās, kur veidojas C=C dubultsaite (dehidrogenēšanās reakcijas)
Kādos produktos ir sastopams B2 riboflavīns?
olas, lapu dārzeņi, piens, sēnes
Kas ir flavoproteīni?
- proteīni ar FAD vai FMN kā prostētisko grupu.
Galvenokārt iesaistīti enerģētiskajā metabolismā,
bet iesaisīti arī epidermas sintēzē
un eritrocītu antioksidantu sistēmās
B3 - nosaukums
niacīns (nikotīnskābe)
B3 - niacīns (ir daļa no kā..?)
Daļa no NADH + H+ un NADPH + H+ - reducējošajiem kofaktoriem, kurus izmanto dehidrogenāzes.
(veidojas karbonilgrupa, ja oxidētājs ir NAD)
Enzīmu piemēri - malāta dehidrogenāze, gliceraldehīda-3- fosfāta dehidrogenāze, 3-hidroksiacil-CoA dehidrogenāze
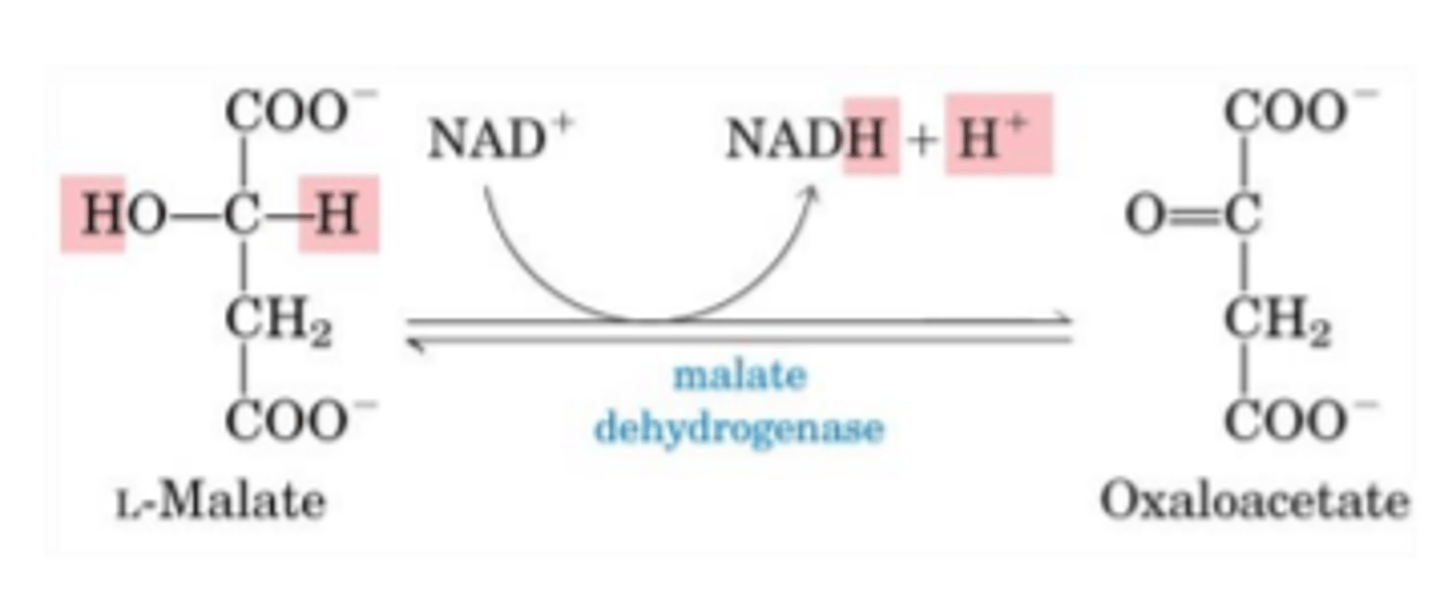
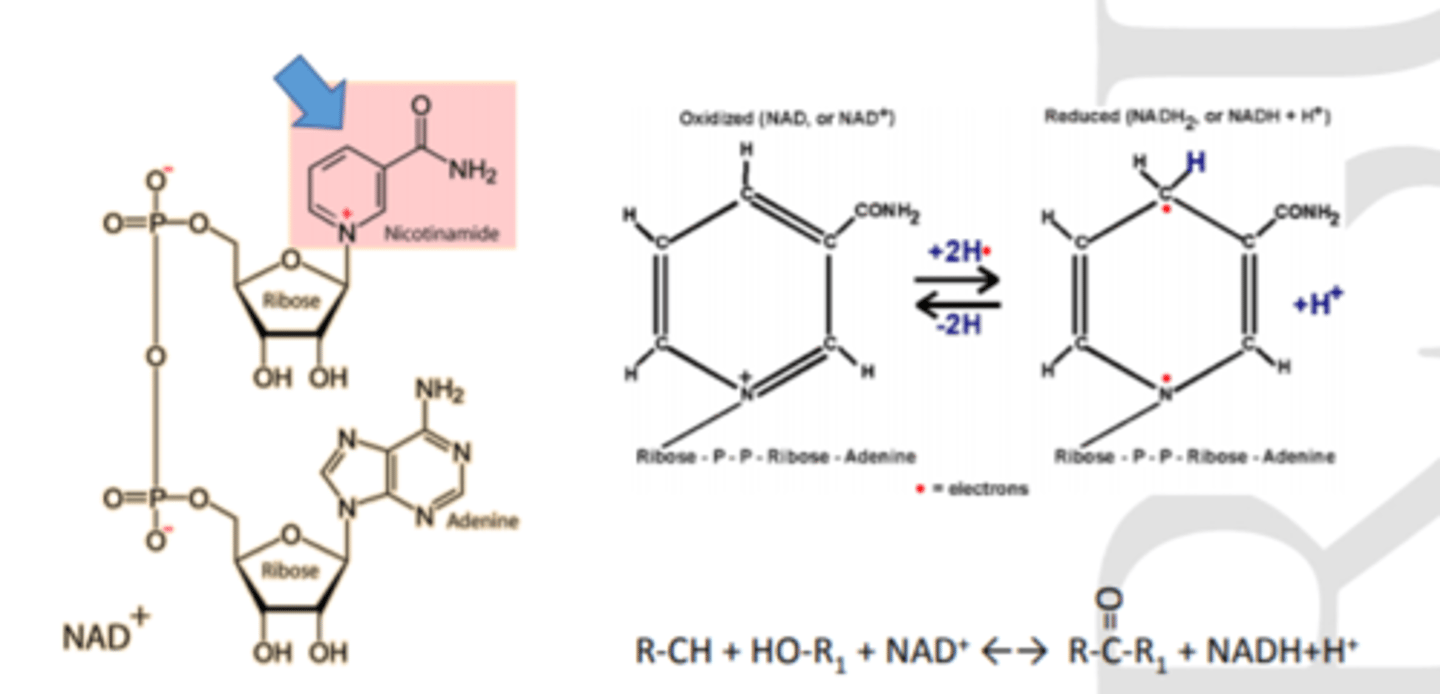
NAD - nikotīnamīda adenīna dinukleotīds
= adenīns + nukleotīds, kur N bāzes vietā ir nikotīnamīds
nikotīnamīda heterocikls ir ar pozitīvu lādiņu
NAD+ = oxidētā forma
NADH+ H+ = reducētā forma (piesaista 2 protonus, 2 elektronus)
B3 - niacīns
- kā kofaktors ox-red reakcijās
- tiek izmantots enerģijas patēriņa gadījumā
- to var sintezēt no triptofāna (cilvēku sintēze neefektīva, šādai pārveidei nepieciešami 3 citi vitamīni)
Slimība, kas rodas B3 niacīna trūkuma dēļ
Trūkums izraisa pelagru - ādas pārmaiņas, caureja, psihiski traucējumi
B5 - nosaukums
pantotēnskābe
B5 - pantotēnskābe
Daļa no koenzīma A.
Koenzīms A ir kofaktors, kas iesaistīts citronskābes ciklā un taukskābju metabolismā kā acetil vai acil grupu pārnesējs.
Enzīmu piemēri: acil-CoA sintetāze, α-ketoglutarāta dehidrogenāzes komplekss, tiolāze
Kas ir koenzīms A?
kofaktors, kas iesaistīts citronskābes ciklā un taukskābju metabolismā kā acetil vai acil grupu pārnesējs.
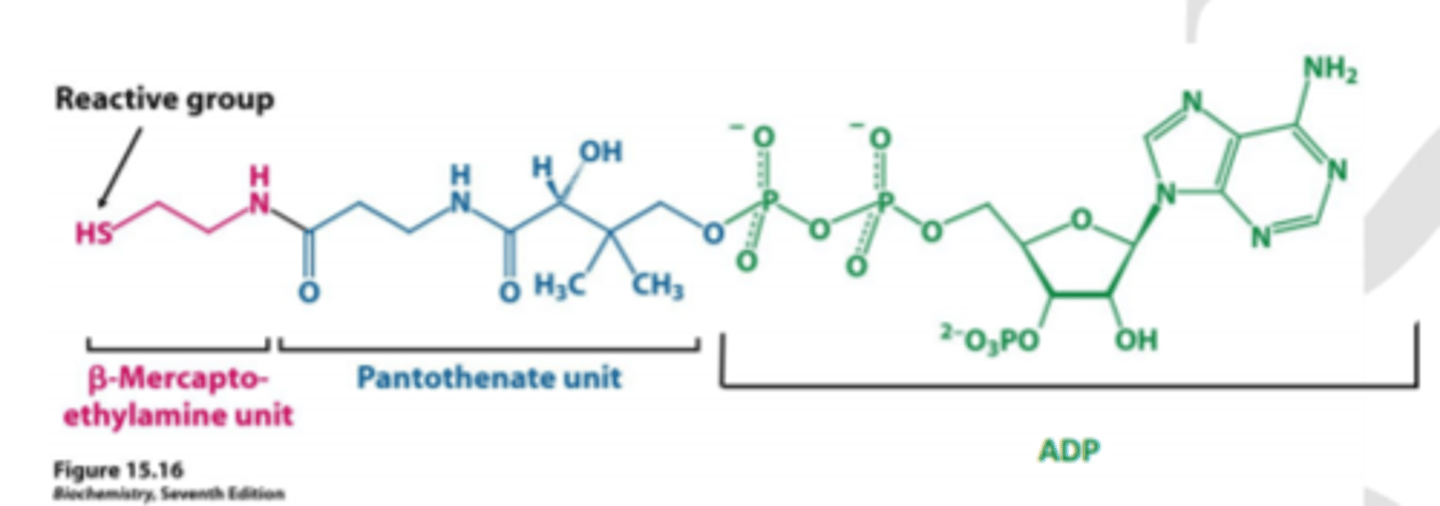
Koenzīma A uzbūve
- sastāv no 3 daļām
A - adenozīna nukleotīds
ir pantotēnskābe (ir visur)
...

B6 - nosaukums
piridoksīns
(ir vitamēru grupa)
B6 - piridoksīns
Piridoksālfosfāts ir enzīmu, kas iesaistīti dažādu funkcionālo grupu papildināšanā vai eliminācijā, kofaktors.
Visbiežāk novērotās izmaiņas ir dažādu aminoskābju transaminācija, deaminēšana, dekarboksilēšana.

B6 - piridoksīns - aktīvā forma, ko speēj darīt??
Vitamēru grupa - aktīvā forma piridoksāl-5-fosfāts (PLP)
PLP spēj kovalenti saistīties ar substrātu un veicināt reakcijas.
Kā izpaužas B6 piridoksīna trūkums?
- ādas bojājumi (saistīti ar B6 lomu B3 sintēzē), neiroloģiski simptomi (saistīti ar B6 lomu neirotransmiteru sintēzē unn sfingolipīdu sintēzē), anēmija (saistīta ar B6 lomu hēma sintēzē)
B7 - nosaukums
biotīns
B7 - biotīns
= prostētiskā grupa, kas nepieciešama karboksilēšanas reakcijās lipoģenēzē, glikoneoģenēzē un sazarotās alifātiskās ķēdes aminoskābju metabolismā.

Kā izpaužas B7 biotīna trūkums?
- diētas dēļ reti sastopams (problēmas saistītas ar tālāko biotīna apriti)
- Izteikta trūkuma simptomi - krampji, muskuļu vājums elpošanas traucējumi - hiperventilācija, balsenes stridors, apnoja, attīstības aizture, dzirdes zudums (sensoneirāls), redzes traucējumi (optiskā atrofija).
B9 nosaukums
folskābe
B12 nosaukums
kobalamīns
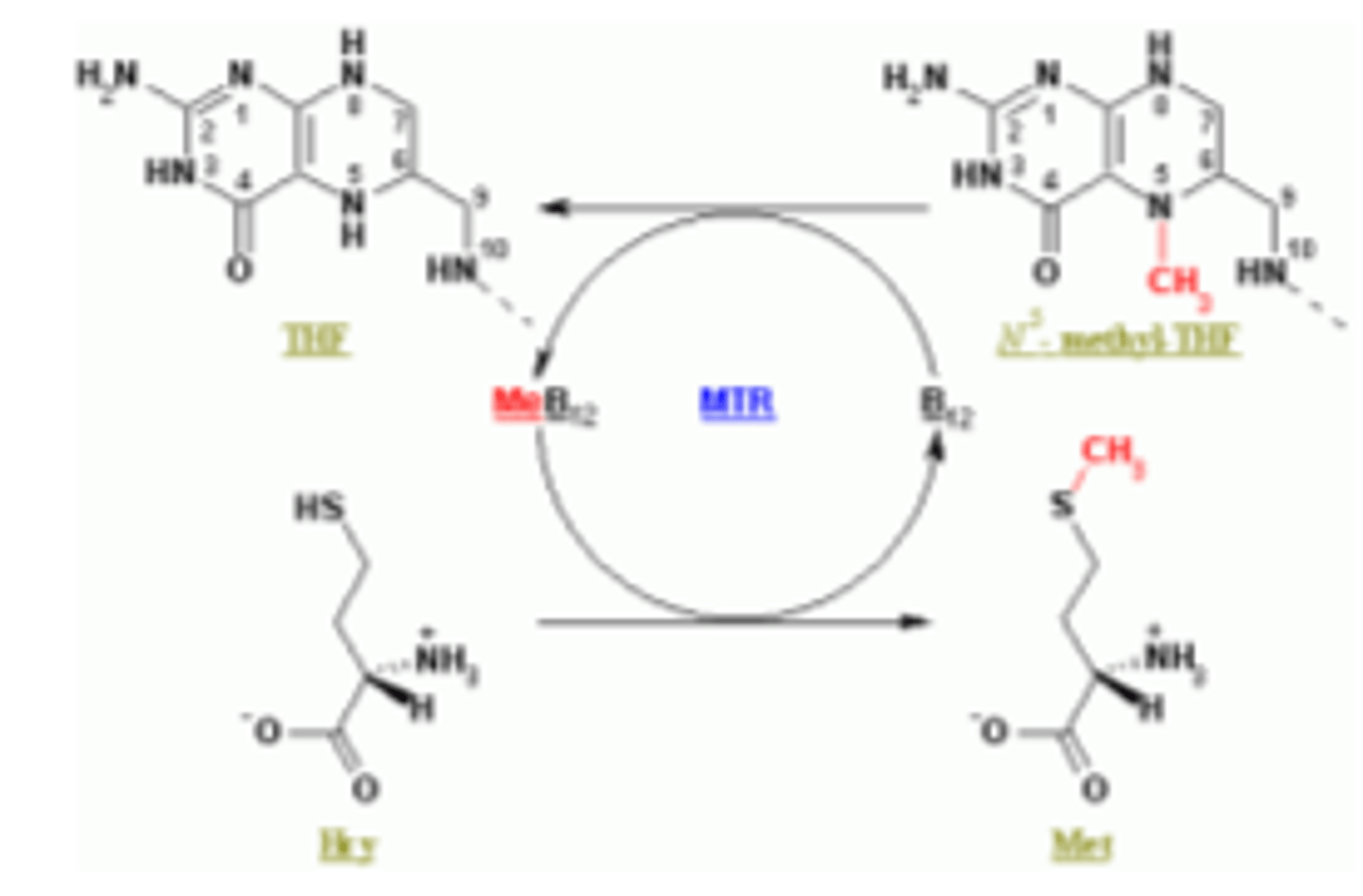
B9 - folskābe un B12 - kobalamīns
Folāts šūnā veido tetrahidrofolātu (THF), tas ir metil (C1) nesējs.
Kobalamīns ir otrs kofaktors, kas iesaistīts metilēšanā - metilgrupas CH3 pievienošana.
B9 - folskābe (lapu dārzeņos) - DEFICĪTS
- visbiežāk sastopams
- deficīta cēloņi ir nepietiekama uzņemšana, traucēta absorbcija, traucēta vielmaiņa un palielināts pieprasījums.

B12 - kobalamīns (kas sintezē, īpašības...)
- to sintezē tikai mikroorganismi
- Ēdot nemazgātus dārzeņus baktērijas kļūst par daļu no zarnu mikrofloras, tādēļ deficītam vairāk pakļauti jaundzimušie.
Trūkumu var izsaukt arī nespēja uzsūkt vitamīnu (glikoproteīna trūkums) atbrīvot to (zems skābes daudzums kuņgī)
B12 var uzkrāt aknās
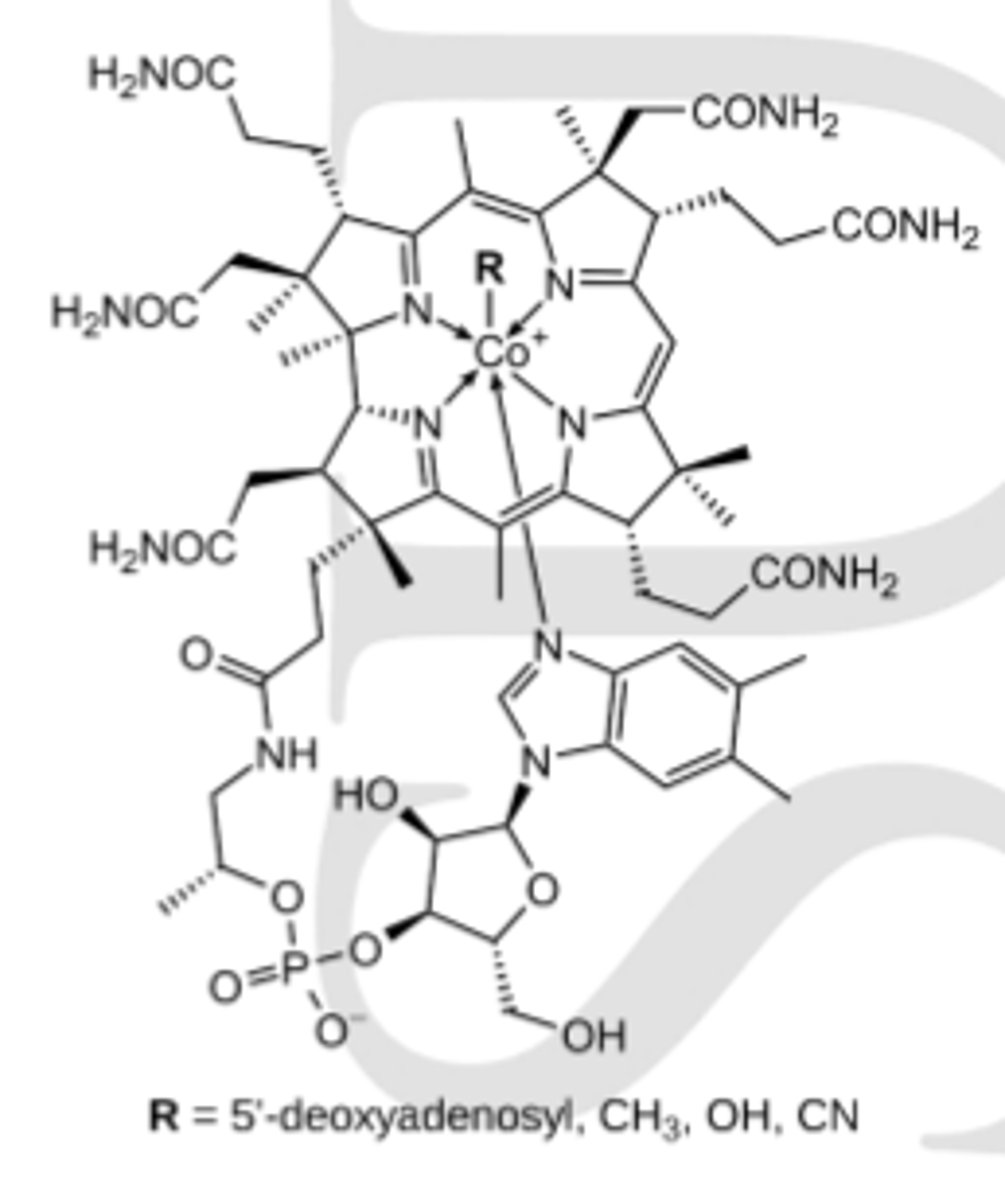
Kas ir C vitamīns - askorbīnskābe un E vitamīns?
antioksidanti
to galvenā funkcija - būt par molekulu, kura viegli oksidējas (atdod elektronus)
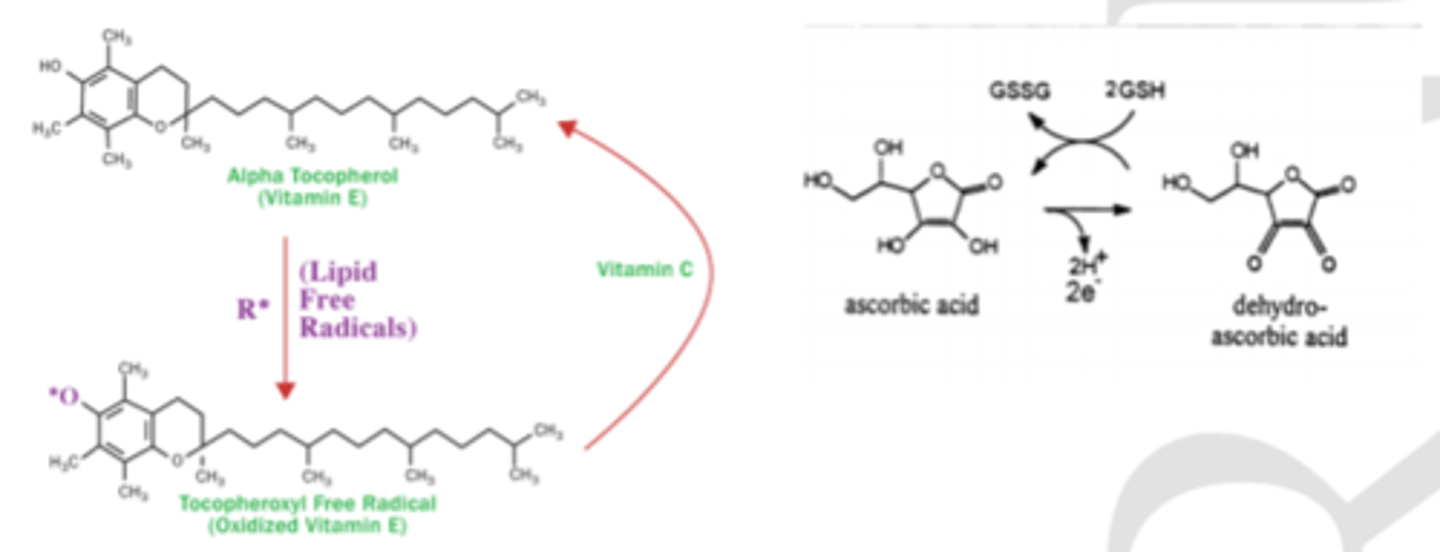
C vitamīns - askorbīnskābe
- augi, dzīvnieki sintezē to no glikozes
- enzimātiskajās reakcijās piedalās gan kā substrāts, gan kā kofaktors - kolagēna sintēzē, karnitīna sintēzē, dopamīna sintēzē, tirozīna metabolismā.

C vitamīna deficīta pazīmes
= cinga
- asiņojošas smaganas
- saistaudu vājums