TMT4130 - Eksamensforberedende pt. 2
1/116
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
117 Terms
Tegn energidiagrammet til et oktaedrisk kompleks
dz2 og dx2-xy
= høyere energi
dxy, dxz og dyz
= lavere energi
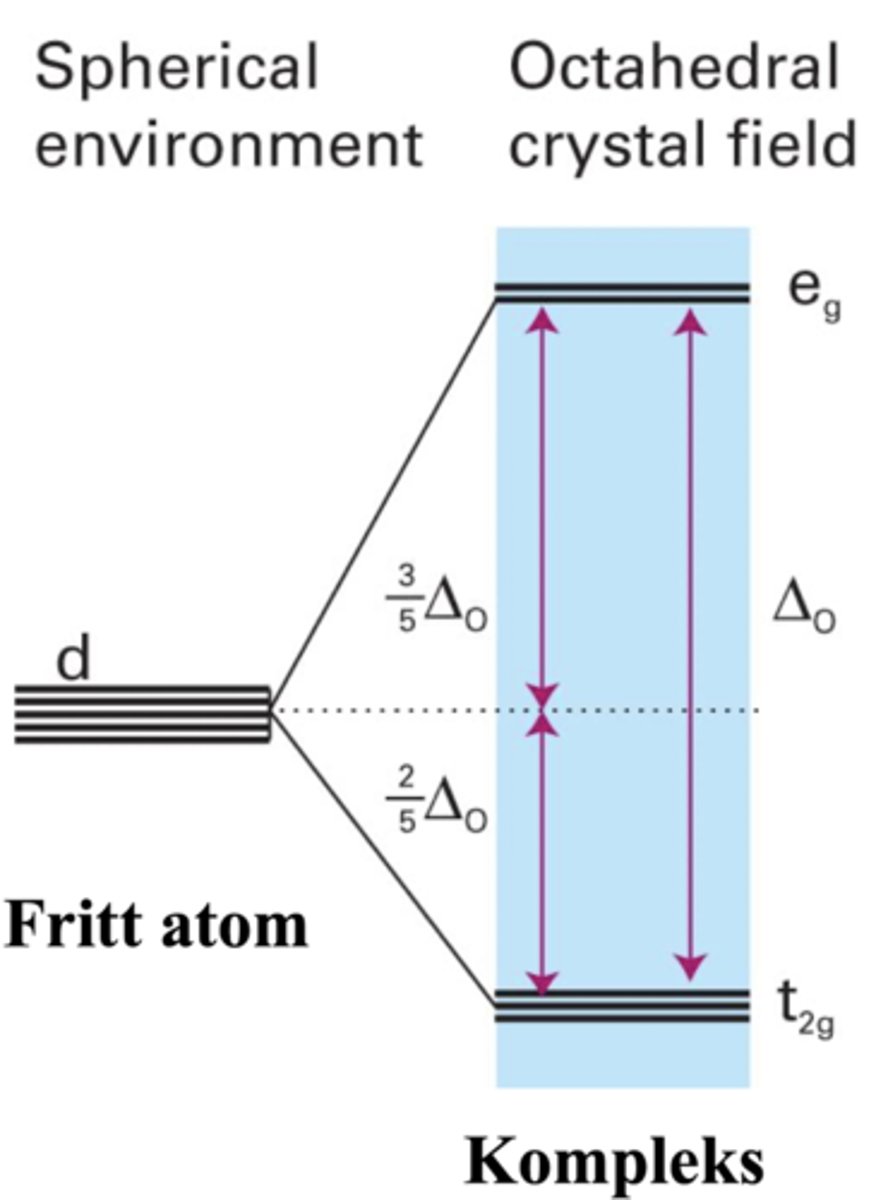
Tegn energidiagrammet til et tetraedrisk kompleks
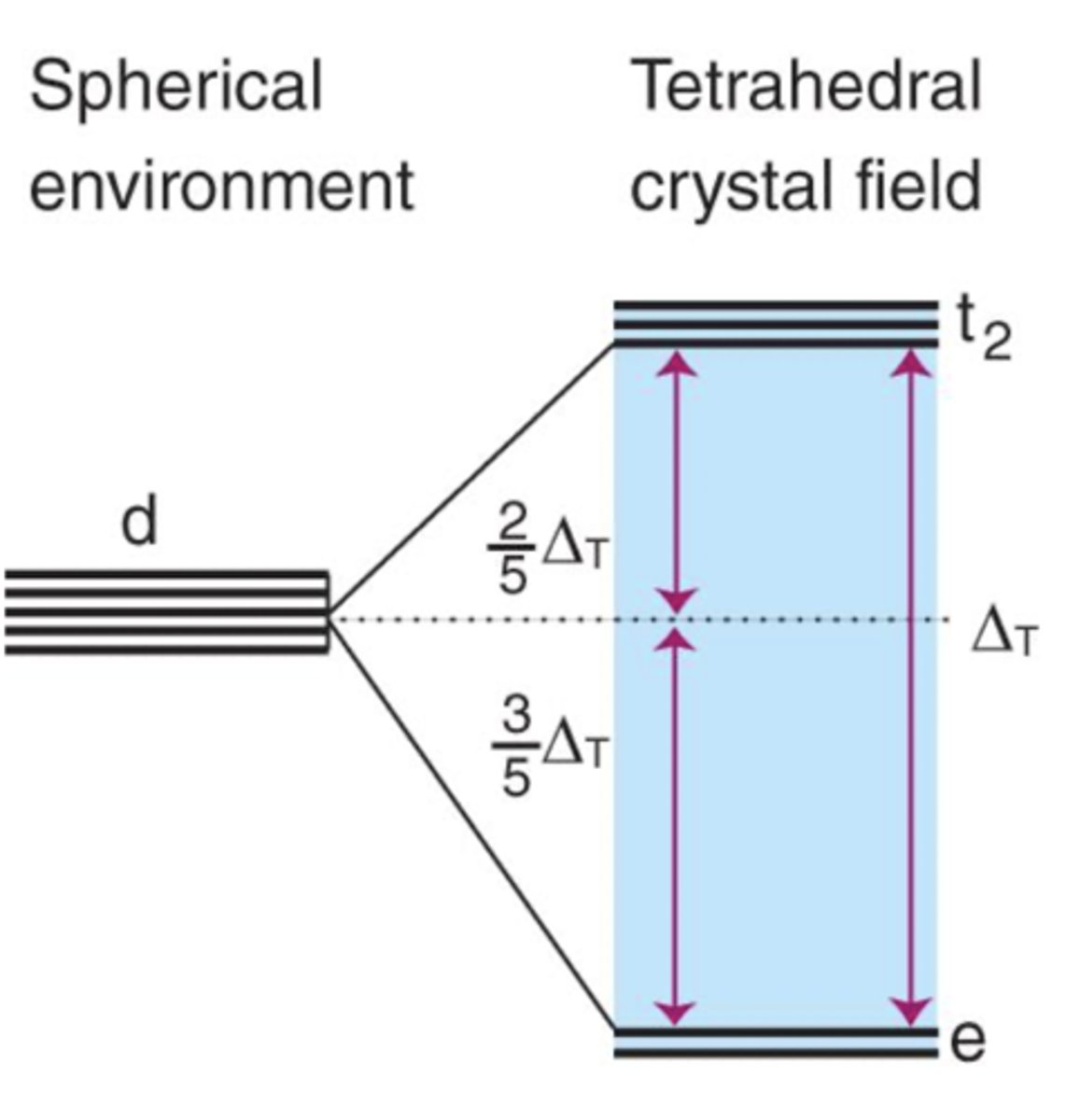
Hva forteller LFSE oss?
Hvor stabilt et kompleks er.
Desto høyere absoluttverdi, jo mer stabil.
Hva er LFSE for oktaedriske komplekser?
LFSE = -(0.4x - 0.6y)Δo + nP
Høyspinn => n = 0, så kan se bort fra nP delen
x = antall elektroner i t2g
y = antall elektroner i eg
n = hvor mange flere parede elektroner det er i komplekset i forhold til et sfærisk felt.
Hva er LFSE for tetraedriske komplekser?
Tetraedriske komplekser er nesten alltid høyspinn.
Antar alltid høyspinn i dette emnet.
LFSE = (-0.6x + 0.4y)ΔT
x = antall elektroner i e
y = antall elektroner i t2
Hvordan vet vi elektronkonfigurasjonen mtp energidiagram for komplekser?
Avhenger av stoffet og hva slags spinn det er.
Høyspinn = lav energi => elektronene fordeles jevnt mellom alle orbitalene
Lavspinn = høy energi => elektronen fordeles først i laveste energiorbtialene før de eksiterer opp til høyere.
Fordel elektronene i orbitalene for energidiagrammet.
F.eks. For et oktaedrisk kompleks har de tre laveste energi-orbitalene navn t2g og de to høyeste energiorbitalene navn eg.
Hvis komplekset har 4 elektroner og det er høyspinn så blir navnet:
t2g^4eg^0
Mens hvis det er lavspinn så blir navnet:
t2g^3eg^1
Hvis du får to ulike komplekser og skal bestemme hvilken som er mest stabil, hvordan kan du gå frem for å finne ut av dette?
Det er i hovedsak 4 uliker måter å vurdere dette på:
1. LFSE
Desto høyere absoluttverdi LFSE = jo mer stabil
(OBS! LFSE er alltid negativ, så man kan også se på det som at jo mer negativ LFSE-verdi, jo mer stabil)
2. Oksidasjonstall
Komplekser med høyere oksidasjonstall er mer stabile.
3. Ligandtype
(sterkt vs. svakt felt)
Sterkt felt = stor Δo -> favoriserer lavspinn som gir høyere stabilitet.
Svakt felt = lav Δo -> favoriserer høyspinn som gir lavere stabilitet.
4. Chelateffekten
Polydentate ligander er mer stabile enn monodentate.
Når et kelatkompleks dannes resulterer det i en økende mengde ligander i løsningen (en polydentat ligand erstatter flere monodentate) noe som fører til en mere positiv reaksjonsentalpi (og dermed mere negativ Gibbs fri energi)
Hva er kelateffekten, hva går det ut på og når oppstår det?
Hva kelateffekten er:
Økt stabilitet av metallkomplekser med flerleddede (kelator) ligander sammenlignet med tilsvarende monodentate ligander.
Metallkomplekser med flerleddede ligander (som binder seg med flere atomer) er mer stabile enn de med enkeltleddede ligander (som binder seg med ett atom).
Hvorfor kelateffekten oppstår:
Entropiøkning: Frigjør flere små molekyler når flerleddede ligander binder seg, øker systemets uorden.
Ringdannelse: Danner stabile ringstrukturer som er energimessig gunstige.
Kinetisk stabilitet: Flerleddede ligander danner mer robuste bindinger som er mindre sannsynlige å bryte.
Hva er sammenhengen mellom Δo og paringsenergien P?
Δo > P = sterkt felt, lavspinn
Δo < P = svakt felt, høyspinn
Tegn effekten av svake og sterke ligandfelt for et tetraedrisk kompleks
OBS! Pensumboken har en feil i vedlagt bildet. På høyre side skal det være tre orbital øverst og to orbitaler nederst.
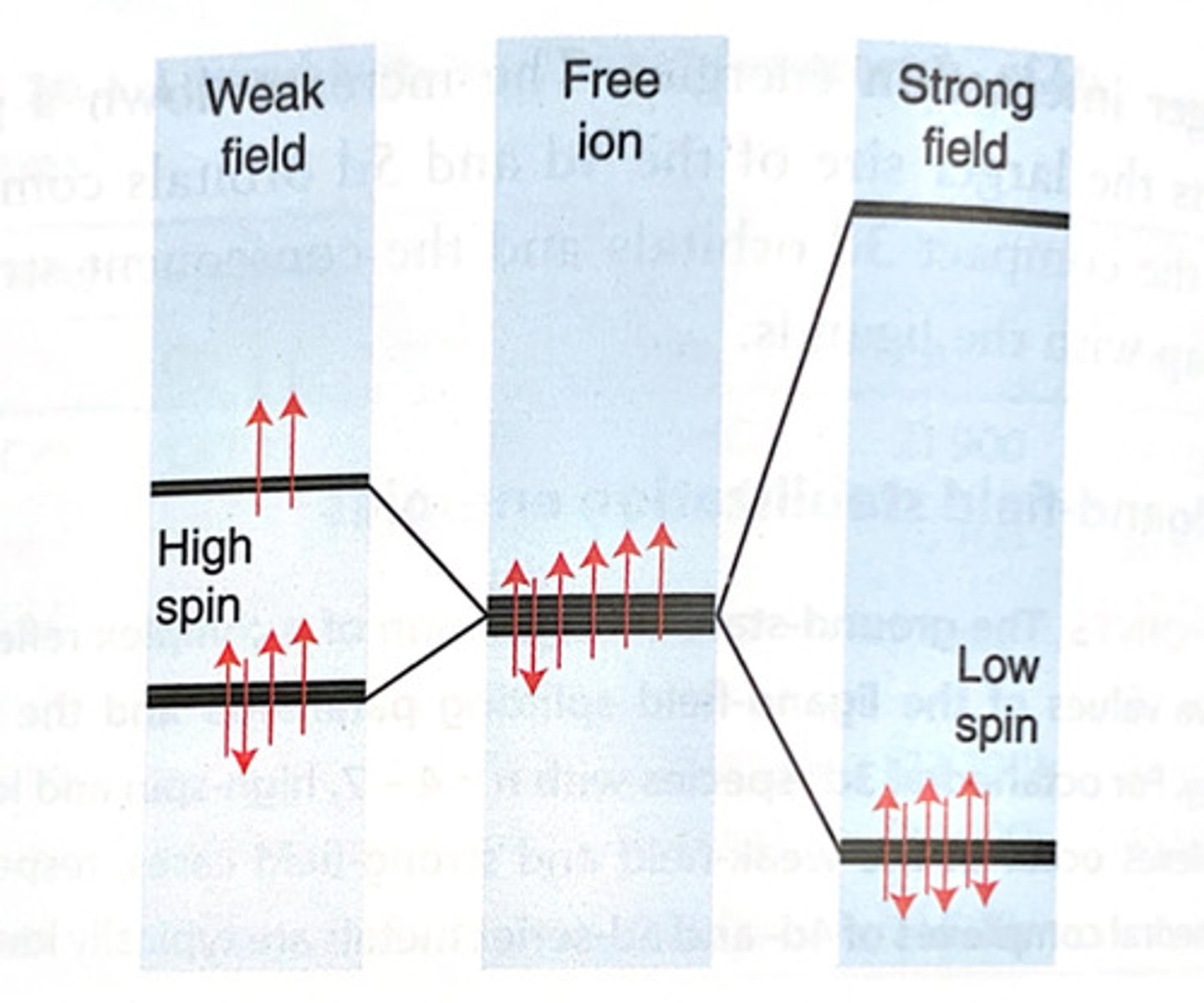
Tegn effekten av svake og sterke ligandfelt for et oktaedrisk kompleks
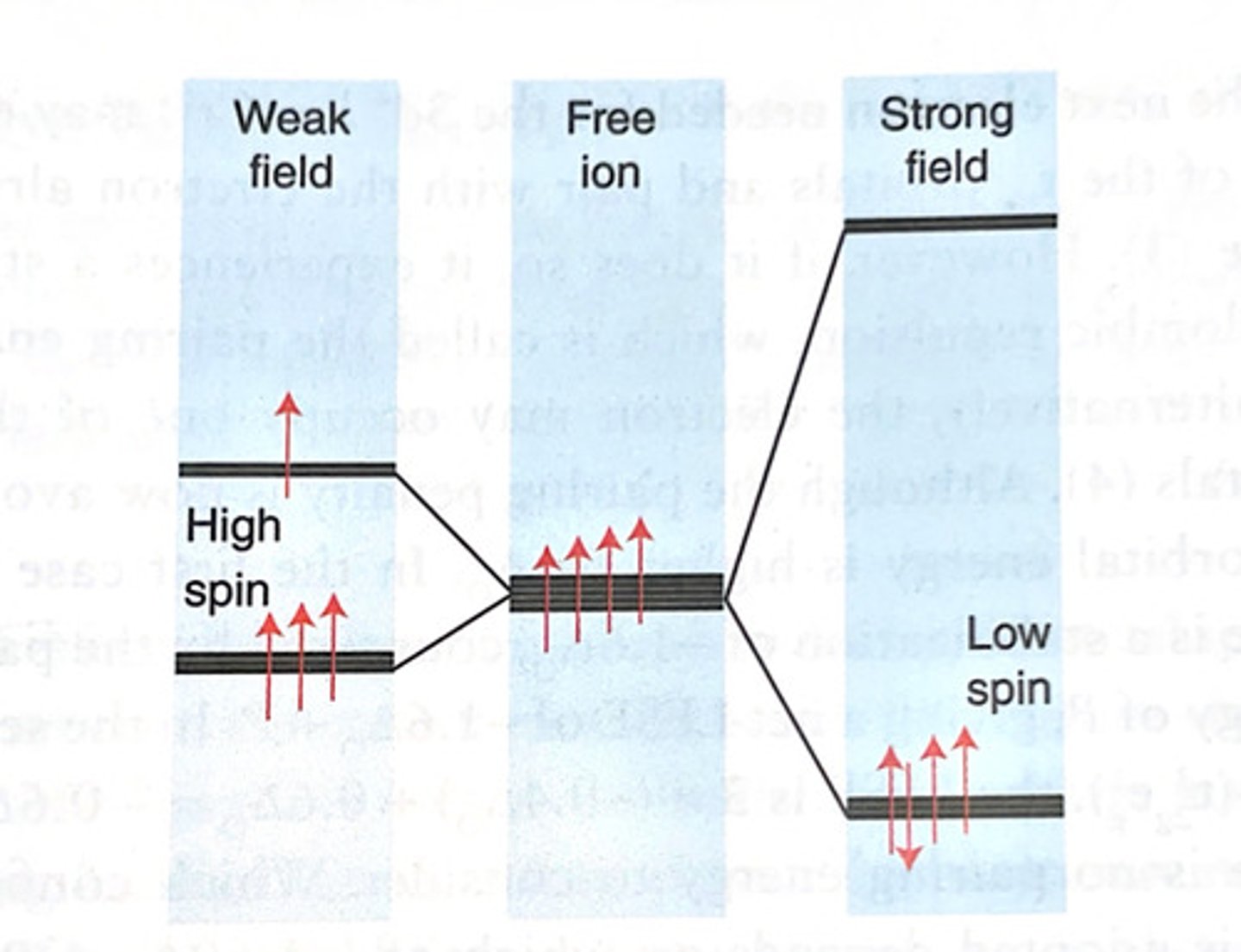
Hva er hovedprinsippet ved tegning av heteronukleære MO?
Desto mer elektronegativt stoffet er, jo lavere energi har det.
I tillegg er MO mer bindende jo mer elektronegativt det er,
og jo mer elektropositivt, jo mer antibindende.
Tegn MO-diagrammet for det heteronukleære molekylet AB.
Anta at A er mer elektronegativt.
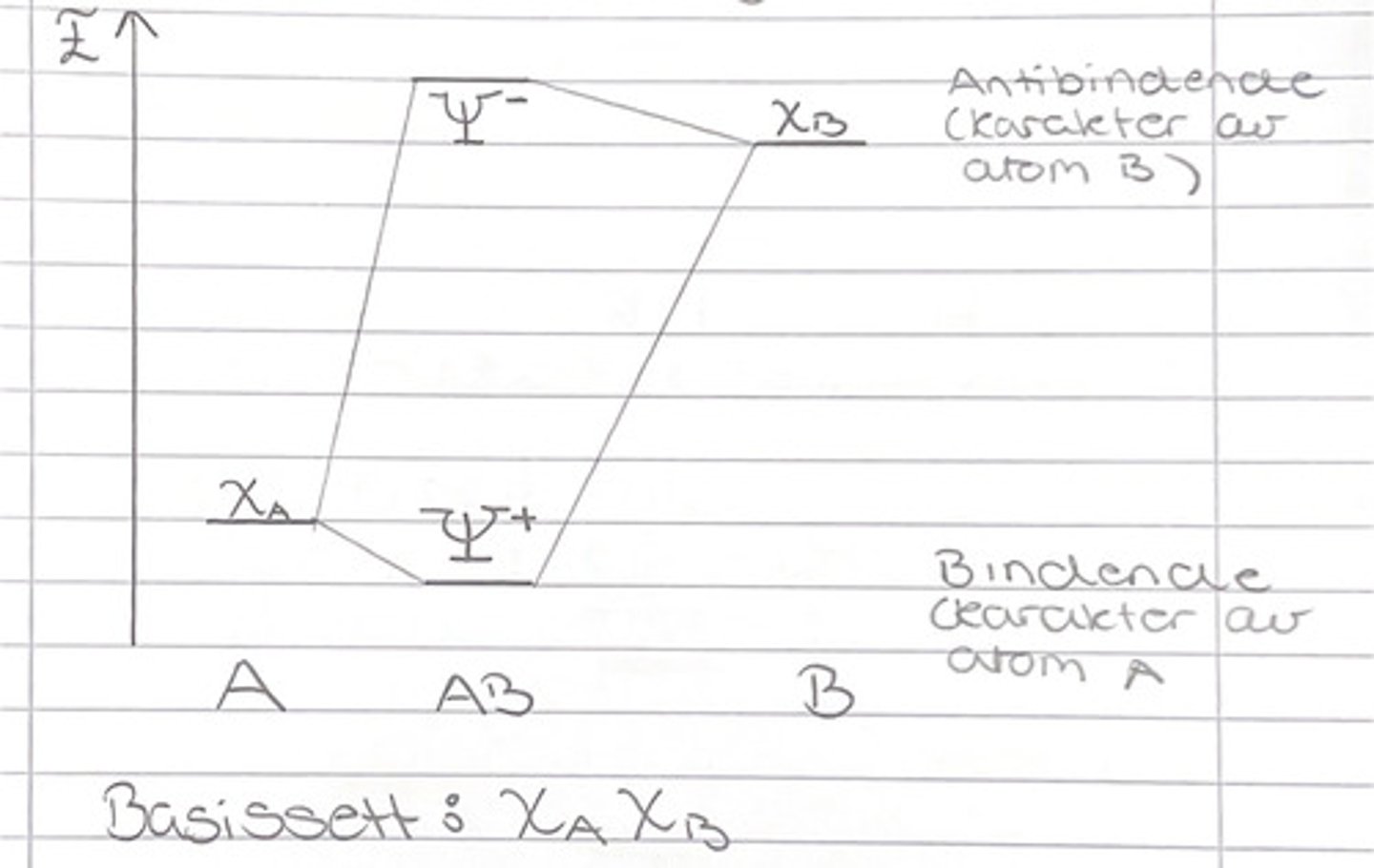
Tegn MO-diagrammet for HF, og skriv elektronkonfigurasjonen.
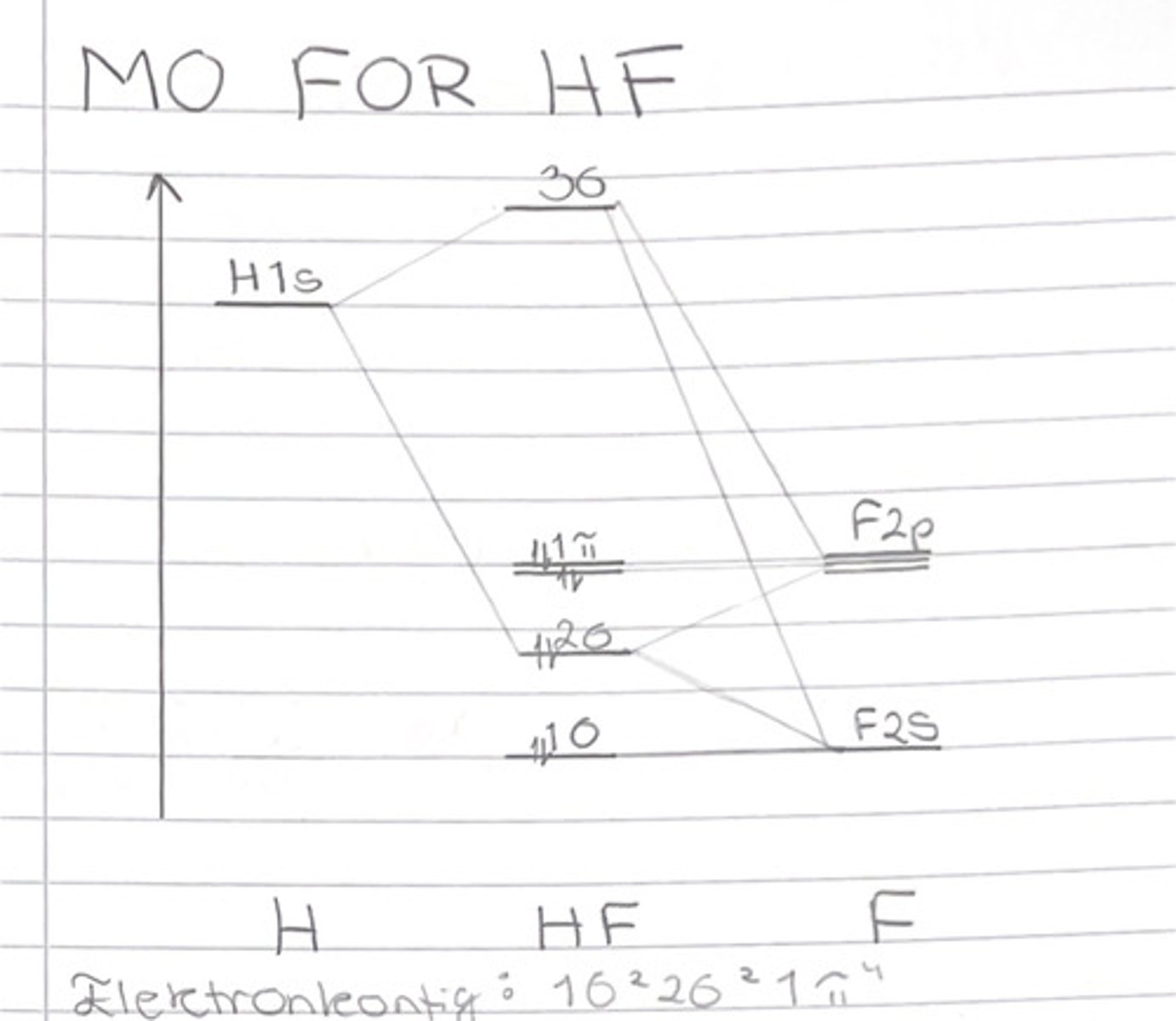
Tegn MO-diagrammet for CO, og skriv elektronkonfigurasjonen.
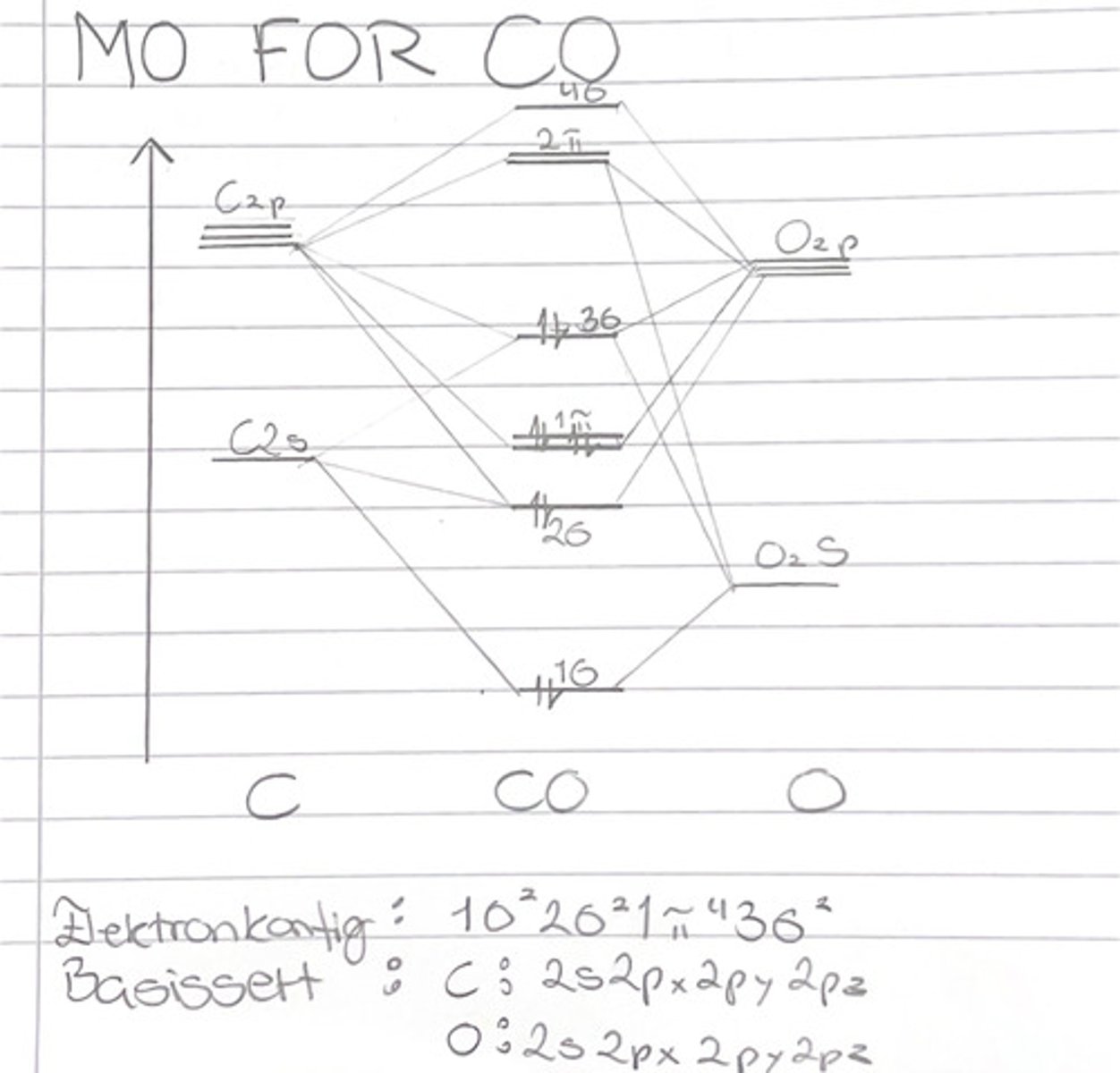
Definer hva som er bindende, antibindende og ikke-bindende
Bindende:
- Lavere energi enn AO den er laget av
- Stor elektrontetthet mellom atomkjernene
Antibindende:
- Høyere energi enn AO den er laget av
- Ingen elektrontetthet mellom atomkjernen
- Har nodalplan
Ikke-bindende:
- Samme energi som AO den er laget av
Til eksamen er vi nødt til å kunne navnet på noen ligander.
Kan du navngi følgende:
1. NH3
2. H2O
3. CO
4. H-
5. F-
6. NO3-
1. NH3 = Ammine
2. H2O = Aqua
3. CO = Carbonyl
4. H- = Hydrido
5. F- = Flourido
6. NO3- = Nitrato
Hvordan navngir man komplekser?
(Nomenklatur)
1. Antall ligander (mono, di, tris, tetra, penta)
2. Navnet på liganden
(Flere ligander -> alfabetisk orden
3. metallnavnet
4. Oksidasjonstallet til kationet angis i parantes
5. Anion: -at på slutten av metallnavn
Navngi:
1. [Fe(CN)_6]^3-
2. K_3[Co(CN)6]
1. Heksacyanidoferrat (III)
2. Kaliumheksacyanidokoboltat
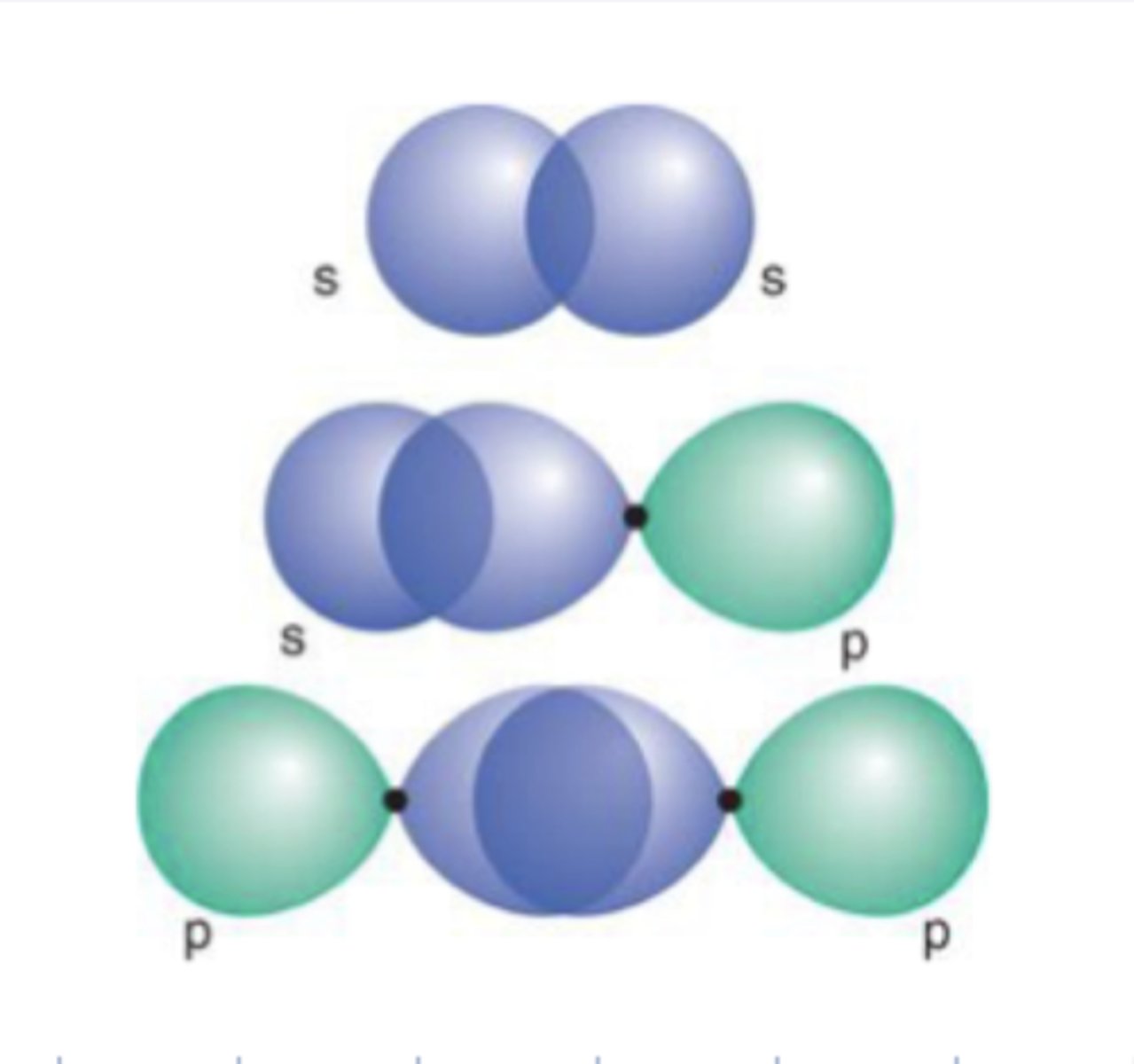
Fortell om sigma-binding
Overlapp mellom orbitaler som er symmetrisk om bindingsaksen.
s-s
s-p
p-p
Fortell om pi-binding
Overlapp mellom orbitalene som har nodalplan gjennom bindingsaksen.
p-p
p-d
d-d
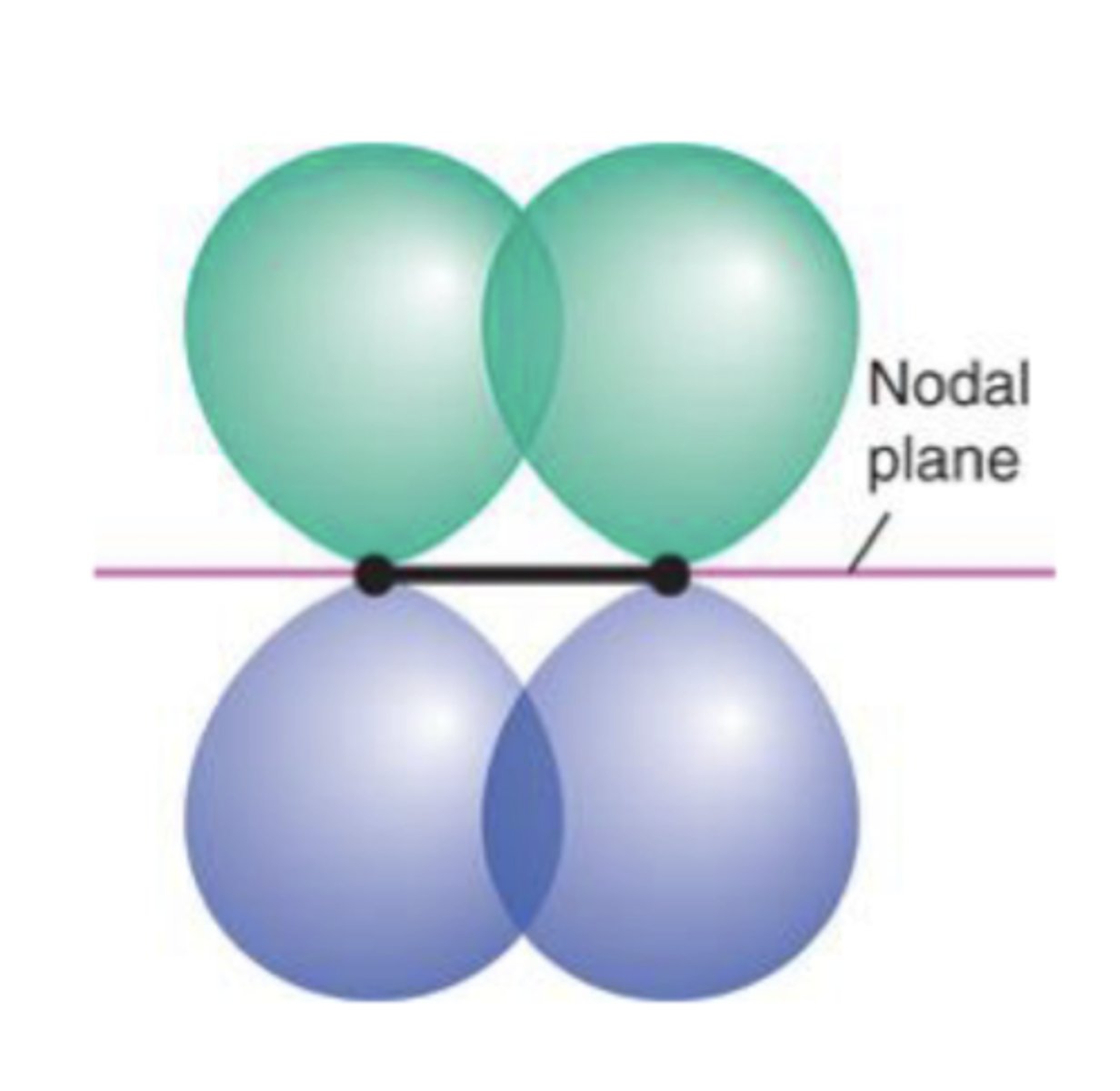
Hvordan kan man finne ut hvilken binding orbitalene har utfra formel?
Finn basissettet, og tegn
Hva er modentat og polydentate?
Ulike typer ligander - avhenger av hvor mange punkter de binder seg til sentralatomet
monodentat = ett bindingspunkt
polydentat = flere bindingspunkt
Hva er ambidentate ligander?
Ligander som kan binde seg til sentralatomet med forskjellige atomer.
De binder seg altså til et metallion gjennom to eller flere forskjellige atomer, men de binder seg ikke samtidig.
Eks.
nitritt , som kan binde seg via nitrogen ELLER via oksygen
Hva er koblingsisomere?
Isomerer som oppstår når en ambidentat ligand binder seg på forskjellige måter til et metallion, ved å bruke ulike atomer til å danne bindingen. Dette fører til ulike strukturelle former av komplekset med samme kjemiske sammensetning.
Hva er definisjonen på svake og sterke felt ligander?
Svake felt ligander:
- Ligander som forårsaker relativt liten splitting av metallionets d-orbitaler
- Fører til mindre energiforskjell mellom de høye og lave energitilstandene av d-orbitalene
Eks. Halogenider, vann og ammoniakk
Sterke felt ligander:
- Ligander som forårsaker en stor splitting av metallionets d-orbitaler
- Fører til større energiforskjell
Eks. Cyanid, karbonyl
Hva er den spektrokjemiske rekken?
Må hvertfall vite noen i endepunktene
Den spektrokjemiske rekken er ligander sortert etter økende Δo.
π-donor < svak π-donor < ingen π-effekt < π-akseptor
I– < Br– < Cl– < F– < H2O < NH3 < PR3 < CO
Utvidet spektrokjemisk rekke er avbildet.
Den svakeste liganden er altså I- og den sterkeste er CO.
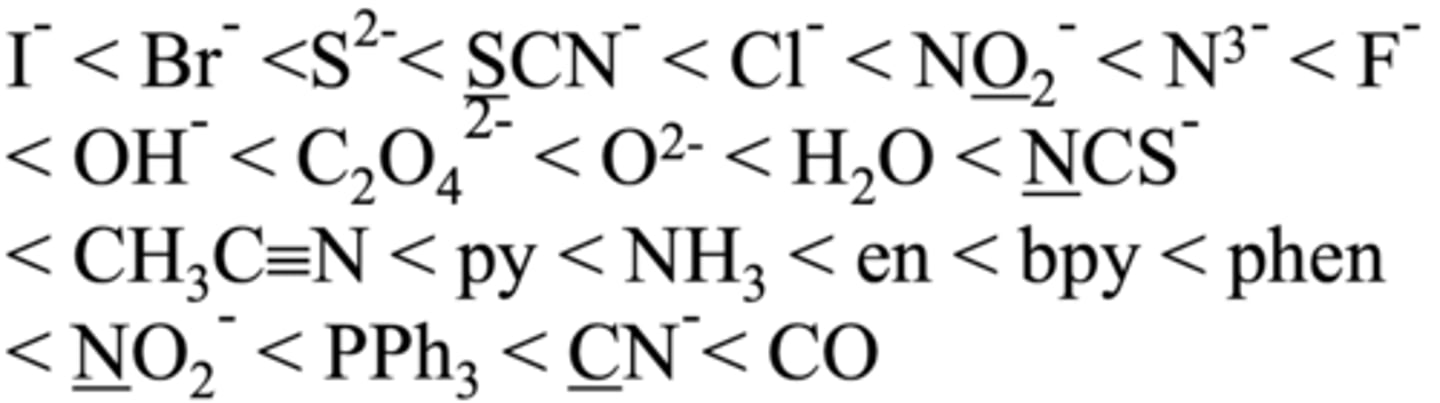
Nevn noen svake felt ligander og noen sterke felt ligander + deres kjennetegn
Svake felt ligander:
I^-, Br^-, Cl^-, F^-, OH^-, H2O
Kjennetegn: forårsaker liten splitting av d-orbitaler, gir ofte høy-spinn konfigurasjoner, paramagnetiske
Sterke felt ligander:
NH3, en, NO2^-, CN^-, CO
Kjennetegn: forårsaker stor splitting av d-orbitalene, gir ofte lav-spinn konfigurasjoner, diamagnetiske
Hva er definisjonen på gitterpunkt?
Et gitterpunkt (lattice) er et tredimensjonalt punkt i rommet som markerer en posisjon hvor en atom eller en gruppe av atomer gjentas periodisk i alle retninger i et krystallinsk materiale.
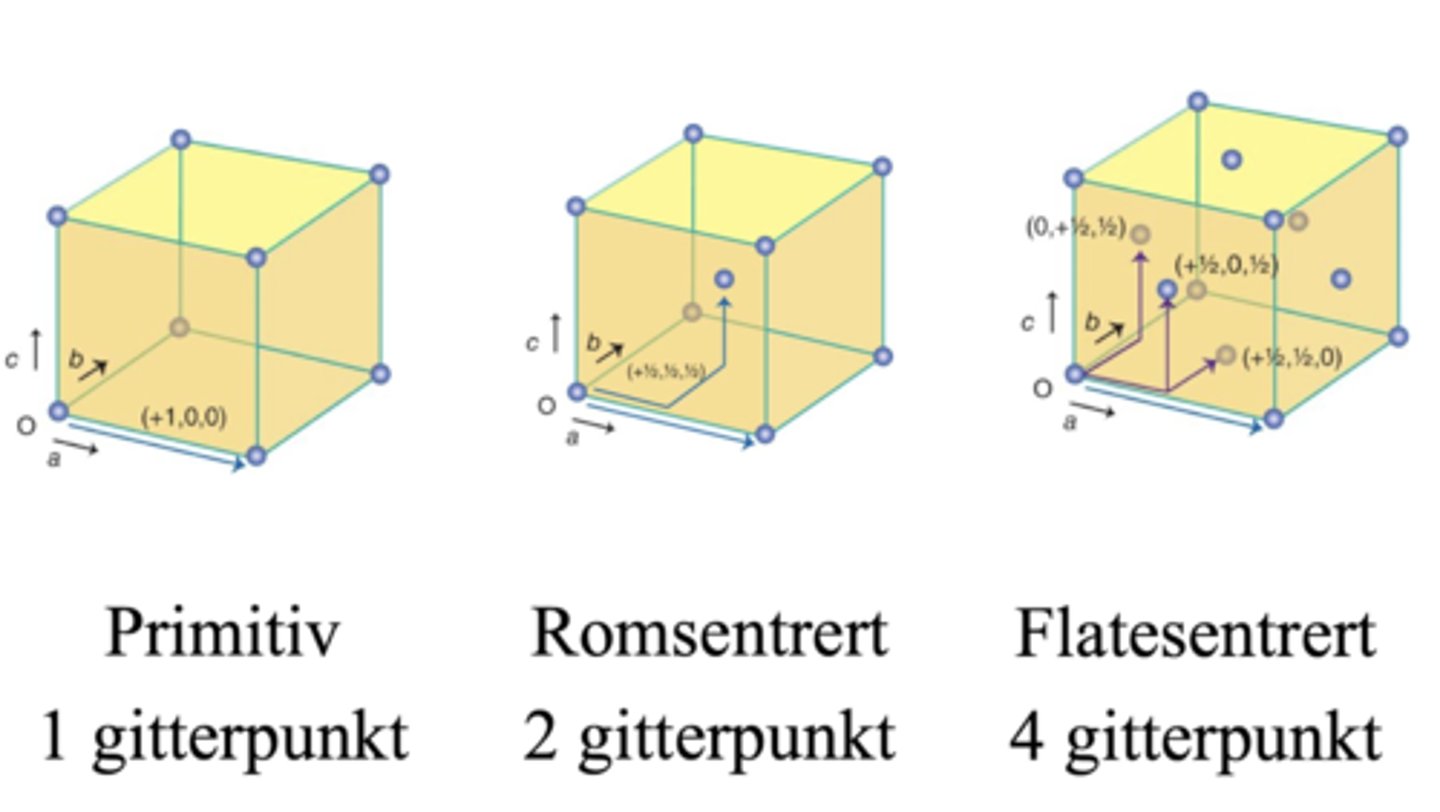
Hvor mange gitterpunkt har de ulike enhetscellene?
Primitiv: 1
Romsentrert: 2
Flatesentrert: 4
Hunds regel
Elektronkonfigurasjon med laveste energi for et atom er den som gir maksimalt antall uparede elektroner i et gitt sett av degenererte orbitaler.
Hva er Δo?
Liganfeltsplittingsparameteret.
Energiforskjellen mellom de høyere og lavere energinivåene i d-orbitalene i et oktaedrisk kompleks.
Hva er elektrisk ledningsevne?
Et mål på et materiales evne til å lede elektrisk strøm.
Dette avhenger med andre ord av hvor godt elektronene kan bevege seg gjennom materialet
Tegn båndstrukturen (elektrisk ledningsevne) for metall, semi-metall, isolator og halvleder
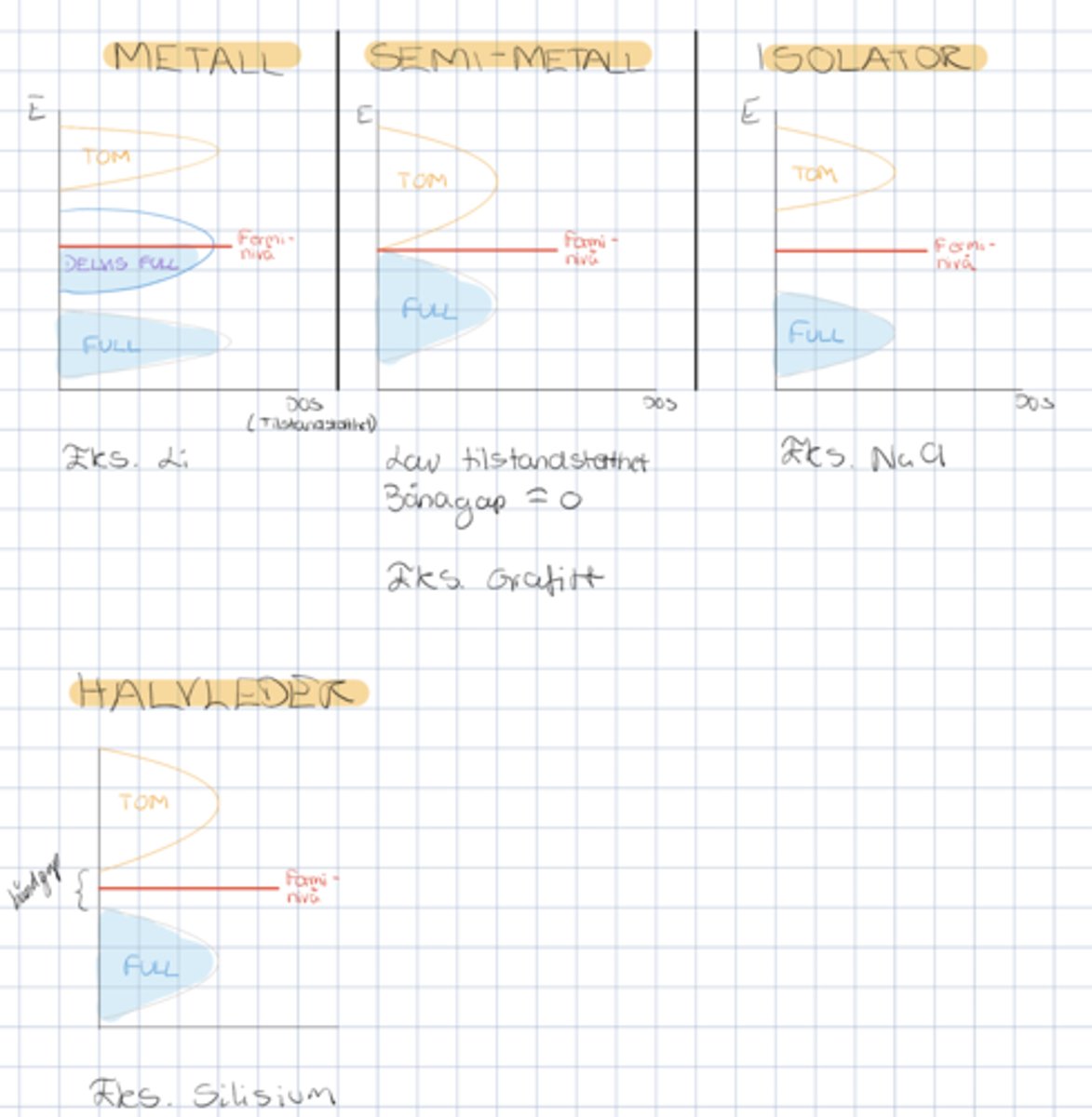
Hvordan identifserer man lewis syrer og baser?
Lewissyrer = elektronpar-akseptor
- Elektronmanglende eller tomt orbital som kan ta imot elektronpar
Typiske kjennetegn på Lewis-syrer inkluderer:
- De har ofte et ufullstendig oktett (for eksempel BCl₃, AlCl₃).
- De kan være metallioner som kan akseptere elektroner (for eksempel Fe³⁺, Zn²⁺).
- De kan ha flerbindinger som kan brytes for å akseptere elektronpar (for eksempel CO₂, SO₃).
Lewisbaser = elektornpar-donor
- Har ofte ensomme elektronpar som kan doneres
Typiske kjennetegn på Lewis-baser inkluderer:
- De har ofte et eller flere ledige elektronpar (for eksempel NH₃, H₂O).
- De kan være anioner som har ekstra elektroner (for eksempel OH⁻, Cl⁻).
- De kan ha flerbindinger som kan donere elektronpar (for eksempel CN⁻).
Hva er myke og harde lewissyrer?
Kom med eksempler
Myke = større anioner eller molekyler med lavere ladningstetthet og høyere polariserbarhet.
Eks. Cu+, Au+, Ag+, Cd2+
Harde = små, svært ladede kationer med høy elektrontetthet og lav polariserbarhet
Eks. Li+, H+, K+. Mg2+.
Hva er kjennetegn for hard syre-base interaksjon?
- Små kationer
- Små anioner
- Lite polarisasjon
- Hovedsaklig ionisk karakter
Hva er kjennetegn for myk syre-base interaksjon?
- Store kationer
- Store anioner
- Stor grad av polarisasjon
- Hovedsaklig kovalent karakter
Hva er forskjellen på sure, basiske og amfotære oksider? Gi noen eksempler på hver av de.
Surt:
Løst i vann vil binde til seg et vannmolekyl og så slippe løs ett proton.
Danner forbindelser med kovalent karakter.
Ikke-metall
Basisk:
Mottar et proton når de løses i vann.
Danner forbindelser med ionisk karakter.
Metall.
Amfotøre
Kan både ha sure og basiske trekk. Altså motta eller gi fra seg proton.

Hva er myke og harde lewisbaser?
Kom med eksempler
Myke lewisbaser =
Baser som har lavere elektrontetthet, større størrelse og høy polariserbarhet. De er ofte større anioner eller molekyler med mindre elektronegative atomer.
Eks. H-, CN-, I-, SCN-
Harde lewisbaser =
Baser som har høy elektrontetthet, liten størrelse og lav polariserbarhet. De er ofte anioner eller molekyler med høyt elektronegative atomer
Eks. F-, OH-, H2O, NH3
Hva er de ulike brønstedsyrene, og hva er deres definisjoner?
Akvasyre:
Surt proton sitter på vannmolekyl koordinert til sentralt metallkation
Hydroksysyre:
Surt proton sitter på en hydroksylgruppe uten nabo- oksogruppe
Oksosyre:
Surt proton sitter på en hydroksylgruppe med en oksogruppe på samme atom
Eksempler på Brønstedsyrer er:
HF og HNO3
Hva er en supersyre og superbase?
Supersyre:
Blanding av brønsted og lewissyre.
Sterkere enn 100% H2SO4
Superbase
Sterkere enn OH-
Hva er bineære forbindelser?
Komplekse forbindelser som består av to forskjellige metaller eller metallioner bundet sammen med en eller flere ligander.
Hva er karbider?
Bineære forbindelser mellom karbon og metaller eller metalloider
Karbider = C + metall/metalloid
Hva er formell ladning, hvordan regner man det ut og hva er betydningen av positiv og negativ formell ladning?
Formell ladning =
# valense e- atomet bidrar med - # elektroner rundt atomet
For resonansstrukturer vil den laveste verdien av formell ladning være den mest stabile strukturen.
For elektronegative atomer ønsker vi en negativ formell ladning

Hva går VSEPR-modellen ut på?
Å minimalisere frastøting mellom elektronpar
Hva er opphavet til atomradiustrendene?
Trenden til atomradius er at den øker nedover i periodesystemet, og synker mot høyre.
Denne trenden oppstår på grunn av den effektive kjerneladningen og lantanoiodekontraksjonene.
Kjerneladningen -> trekker elektronene nærmere kjernen
Lantanoidekontraksjonen -> fører til dårlig skjerming som gir økning i den effektive kjerneladningen og som gjør at 2. og 3. rekke overgangsmetaller har tilnærmet lik radius.
Hva er lantanoidekontraksjonen?
Hva er årsaken til lantanoidekontraksjonen?
Fenomen der atomradiusen til elementene i periodesystemet reduseres jevnt gjennom lantanoideserien (fra La til Lu) til tross for at protoner og elektroner legges til.
Årsak:
Dårlig skjerming: 4f-elektronene har dårlig skjermingseffekt.
Økt kjerneladning: Protoner legges til kjernen uten tilstrekkelig skjerming.
Økt Z_eff: Den effektive kjerneladningen (Z_eff) øker, trekker elektronskyen nærmere kjernen.
Hva er degenererte orbitaler?
Orbitaler med lik energi
Hva er kjennetegn for komplekser med lave koordinasjonstall (2-4)?
Koordinasjonstall 2:
Lages i laboratoriene.
Lineær geometri.
Eksempel: [Ag(NH3)2]^+
Koordinasjonstall 3:
Sjeldne blant metallkomplekser.
Trigonal plan eller trigonal pyramidal.
Eksempel: [HgI3]^−
Koordinasjonstall 4:
Tetraedrisk eller kvadratisk plan.
Eksempel: [Ni(CO)4] (tetraedrisk), [PtCl4]^2− (kvadratisk plan).
Hva er kjennetegn for komplekser med høye koordinasjonstall (6-12)?
Hva er også kjennetegnet for komplekser med koordinasjonstall 5?
Koordinasjonstall 5:
Trigonal bipyramide
Koordinasjonstall 6:
Oktaedrisk eller trigonal prisme. Eksempel: [Fe(CN)6]^4−
___________________________________________
resterende er muligens ikke pensum for TMT4130
Koordinasjonstall 7:
Pentagonal bipyramidal eller oktaedrisk med en ekstra ligand.
Eksempel: [ZrF7]^3−.
Koordinasjonstall 8: Kvadratisk antiprisme eller dodekaedrisk.
Eksempel: [Mo(CN)8]^4−.
Koordinasjonstall 9-12: Mer komplekse geometriske strukturer, ofte funnet i f-blokkelementer.
Fortell om nodalplan.
a. Hva er det?
b. Hva forteller oss antallet nodalplan?
c. Hvordan vet vi hvilket fortegn bølgefunksjonen har?
Nodalplan er et området hvor det er null sannsynlighet å finne elektroner. Altså der bølgefunksjonen går gjennom null.
Orbitalvinkelmomentkvantetallet l forteller oss antall nodalplan:
l = n - 1.
Bruk fortegnet til bølgefunksjonen:
Ved å vite hvordan bølgefunksjonen endres i de forskjellige regionene, kan vi bestemme fortegnet på hver side av nodalplanet.
Fortegnet bestemmes altså av bølgefunksjonen. Der bølgefunksjonen er 0 = nodalplan.
Hva er de 12 prinsippene for grønn kjemi?
1. Forebygging
2. Atom økonomi
3. Mindre giftige kjemikalier
4. Design sikrere kjemikalier
5. Sikrere løsemidler og hjelpemidler
6. Energieffektive prosesser
7. Bruk fornybare råvarer
8. Redusere antall prosesstrinn
9. Katalyse
10. Design for nedbryting
11. Overvåking
12. Tryggere prosesser
Hvilke prinsipper innen grønn kjemi er relevant for stoffkjemi?
1. Forebygging
2. Atom økonomi
3. Mindre giftige kjemikalier
4. Design sikrere kjemikalier
5. Sikrere løsemidler og hjelpemidler
6. Energieffektive prosesser
7. Bruk fornybare råvarer
8.. Katalyse
9. Design for nedbryting
Av de 12 prinsippene innen grønn kjemi, fokuserte foreleser spesielt på noen som er mer relevant for TMT4130.
Hva er disse prinsippene, og fortell hva de går ut på.
(Hint: fem punkter)
1. Forebygging
Bedre å unngå produksjon av avfallsprodukter enn å måtte ta hånd om avfall
-> Bruke færrest mulig grunnstoffer og forbedre kjemikalier.
- Kan regne ut E-faktor = masse avfall / masse produkt
(ønsker så lav e-faktor som mulig)
Eks. Fremstilling av TiO2
2. Atomøkonomi
Prosesser skal designes slik at mest mulig av materialer som brukes skal inngå i det endelige produktet
AØ = molekylmasse til ønsket produkt / molekylmasse til reaktanter * 100%
(ønsker høy)
3. Mindre giftige kjemikalier
Eks. Dannelse av polykarbonat
4. Energieffektive prosesser
Eks. Haber-prosessen
N2 + 3H2 -> 2NH3
3000 grader C uten katalysator
500 grader C med katalysator
5. Katalyse
Kjempe viktig!!
Eks. Haber-prosessen
N2 + 3H2 -> 2NH3
Hva er stereoismere?
Stereoisomeri er en form for isomeri hvor molekyler har samme molekylformel og samme rekkefølge av atomer (samme konnektivitet), men forskjellig tredimensjonal orientering av atomene i rommet
Hva er de ulike stereoismere?
1. Geometriske isomere
Cis/trans MB4C2
=> en rett opp og en rett ned
fac/mer MB3C3
=> 2x sidlengs T (bildet)
2. Optisk isomere MA2B2C2
=> Ser ut som speilbilde
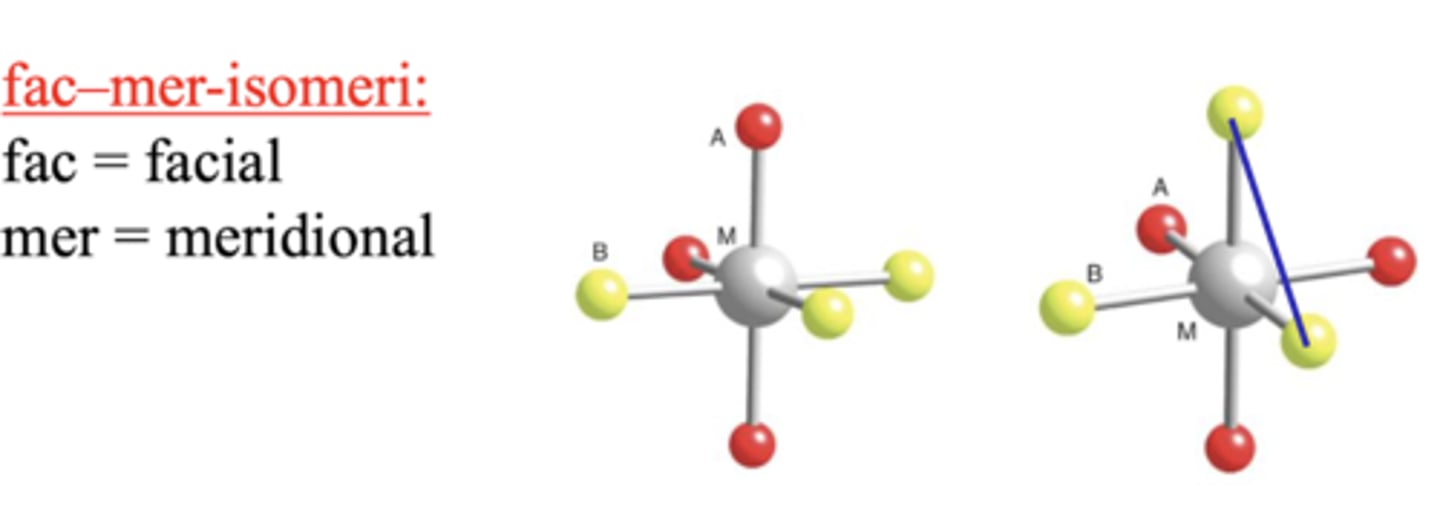
Hva er isomere og hva de to hovedgruppene?
Isomere =
molekyler som har samme molekylformel, men forskjellige strukturer eller arrangementer av atomer.
De to hovedgruppene:
1. Strukturelle isomerer
Molekyler som har samme molekylformel, men forskjellig kobling av atomer (forskjellig struktur)
2. Stereoismerer
Stereoisomerer er molekyler som har samme molekylformel og kobling av atomer, men forskjellig romlig arrangement av atomene
Hvilke ulike typer strukturelle isomerer har vi?
1. Koblingsisomere
Ulike strukturer og egenskaper
Eks. NO2, KN og KO
2. Ioniseringsisomere
Eks. Ligand eller motion bytter posisjon
(Motion = ladningsbalanserende)
3. Koordinasjonsisomere
Bytte av ligander mellom kation- og anionkomplekser.
4. Hydratisomere
Isomeri skyldes forskjellen i om løsemiddelmolekylene er bundet til sentralatomet eller er frie i krystallstrukturen
Hva er bindingsorden og hvordan regner man det ut?
Bindingsorden beskriver antall kjemiske bindinger mellom et par av atomer.
Gir en indikasjon på stabiliteten til en binding.
=> jo høyere bindingsorden => jo sterkere og mer stabil, og kortere bindingslengde
Hvis bindingsorden = 0 så er det ugyldig. Lager ingen binding.
Bindingsorden 1 = enkelbinding
Bindingsorden 2 = dobbelbinding
Bindingsorden 3 = trippelbinding

Hva er hypervalens?
Et atom som har mer enn åtte elektroner i sitt ytterste skall.
Aka unntak fra oktettregelen.
Forekommer hovedsaklig fra tredje periode og utover, hvor flere enn åtte elektroner kan delta i kjemiske bindinger på grunn av tilgjengeligheten av d-orbitaler eller ved delokalisering av elektroner i molekylære orbitaler.
Hva er gruppetrendene for lewis-syrer i periodesystemet?
Lewis-syrer aksepterer elektronpar.
Dermed vil lewissyrer bli sterkere fra venstre mot høyre pga økende elektronegativitet.
Desto høyere elektronegativitet, jo lettere trekker atomene til seg elektroner.
Hva er gruppetrendene for lewis-baser i periodesystemet?
Lewis-baser donerer elektronpar.
Desto høyere elektronegativ, jo mindre lett er det å gi fra seg elektroner.
Derimot når atomradiusen øker så er det lettere å gi fra seg elektroner.
De sterkeste lewis-basene er dermed nederst til venstre.
Hva er radikaler?
Molekyl/atom med ett uparet e-.
De er ekstremt reaktive
Hva er de ulike reaksjonene som forekommer med H2?
1. Homolytisk dissosiasjon
Skjer på metalloverflaten. Eks pt eller Ni
H2 -> 2H
2. Heterolytisk dissosiasjon
På metalloksidoverflate eller reaksjon med molekyl
H2 -> H+ + H-
3. Radikal kjedereaksjon
a. Initiering:
Dannelse av frie radikaler
b. Propagering:
De frie radikalene reagerer med andre molekyler, noe som fører til dannelsen av nye radikaler og produkter.
c. Terminering:
Kjedereaksjonen avsluttes når to radikaler møtes og danner et stabilt molekyl, slik at det ikke dannes nye radikaler.
Hva er silikater?
Nettverksforbindelser basert på SiO4-tetraeder
Annen info:
- Viktig for jordas geologi
- Forekommer i ildfaste materialer, porselen og glass
- Strukturen kan variere
Hva er prinsippet til krystallfeltteorien?
Ligandene har frie elektronpar, og man ser på disse som punktladninger.
Negativt: kan ikke forklare den spektrokjemiske rekke, eller hva som faktisk binder komplekset sammen -> ligandfeltteorien
Hva går ligandfeltteorien ut på?
Beskriver hvordan ligander påvirker energien og elektronfordelingen til d-orbitalene i overgangsmetallkomplekser.
Bruker MO-teorien på komplekser
Tegn MO-diagrammet for et oktaedrisk kompleks
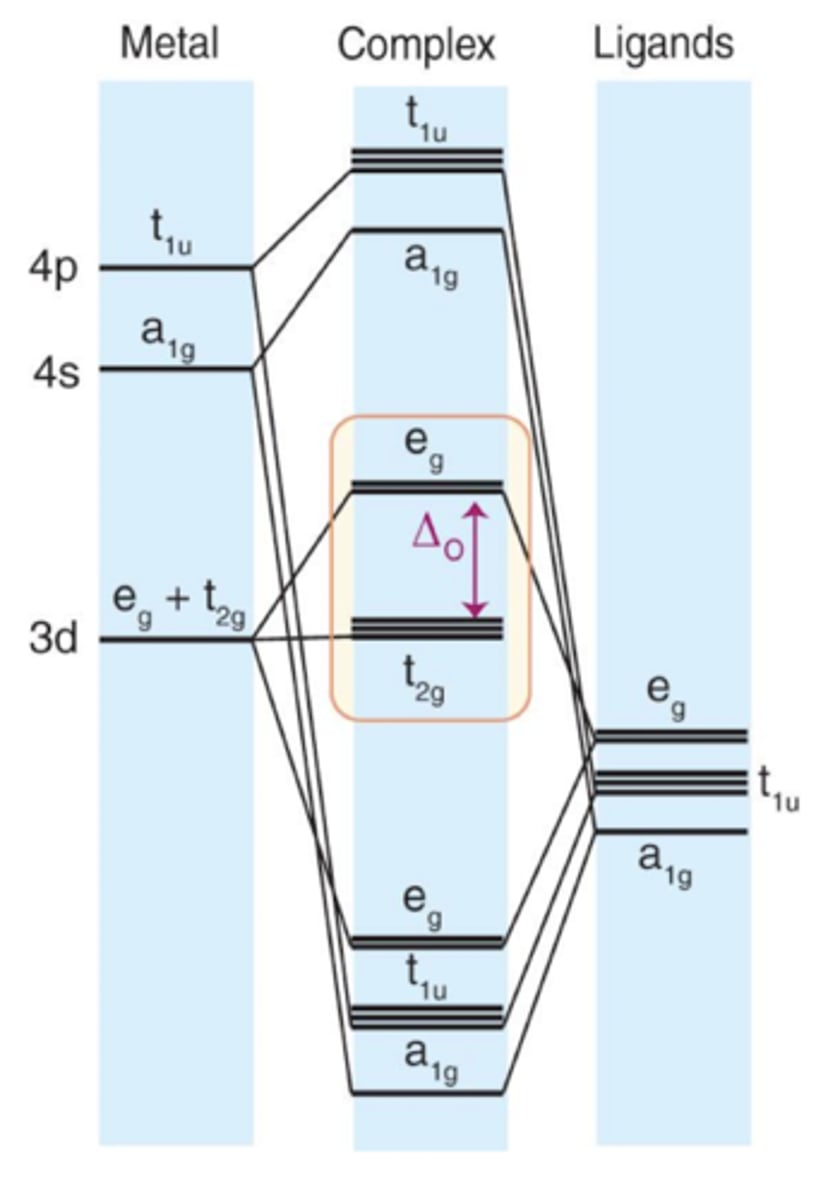
Hva skjer ved dannelse av syre/base-komplekser?
Vi får en senkning i total energi på grunn av at elektronparet fra basen går inn i den bindende molekylorbitalen i komplekset.
Hva er legering?
Blanding av metaller.
- Fast løsning
- Liten ΔX (altså liten forskjell i elektronegativitet)
- Elektropositive elementer
Deles i to grupper:
1. Substitusjonell legering
- Ulike atomer i samme gitter
- Lik radius (innen 15%)
- Like egenskaper
- Smibare/duktile (kan formes)
Eks. messing
2. Interstitiell legering
- Små atomer i hull (B,C,N)
- Ulik størrelse og egenskaper
- Sprø (kan knekkes)
Eks. støpejern
Hva er allotropi?
Et grunnstoff som kan danne flere forskjellige strukturer med forskjellige egenskaper.
Hva er sammenheng mellom atomradius og koordinasjonstall?
Atomradius avhenger av koordinasjonstall.
Størrelsen endrer seg med strukturen.
CN vs. relativ radius:
12 1
8 0.97
6 0.96
4 0.88
Hva går valensbåndteorien ut på?
Valensbåndteorien forklarer kjemiske bindinger ved å beskrive hvordan atomære orbitaler overlapper og danner kovalente bindinger gjennom deling av elektronpar, og hvordan hybridisering av orbitaler kan tilpasse seg for å danne sterkere bindinger.
Teorien fokuserer på følgende:
1. Overlapping av orbitaler:
Kjemiske bindinger dannes ved overlapping av atomorbitaler som inneholder uparrede elektroner fra hvert atom.
2. Kovalente bindinger: Når to atomorbitaler overlapper, deler de to elektroner og danner en kovalent binding.
3. Hybridisering: Atomorbitaler kan kombinere for å danne hybridorbitaler, som gir en optimal orientering for bindinger (f.eks. sp3, sp2, sp).
4. Geometri: VB-teorien forklarer molekylenes form og bindingers vinkel basert på hvordan atomorbitalene overlapper og hybridiserer.
Hva er interhalogener?
Kjemiske forbindelser som består av to forskjellige halogener.
Eks. CLf
XF, XF3, XF5 og XF7
- Vanligvis lewis-syrer
- Sterke oksidasjonsmidler
- Vanligvis struktur og reaktivitet som ligger mellom de rene halogene
- Kan være svært reaktiv
- Brukes ofte i kjemiske synteser
Hva er en utskiftingsreaksjon og en metatesereaksjon?
Utskiftningsreaksjon =
En av delene blir byttet ut
A-B + B´ = A-B´ + :B
Metatesereaksjon =
Bytte av "partnere"
A-B + A´-B´ = A-B´ + A´-B
Forklar Born-mayer-likningen.
Hva betyr de ulike symbolene, hva er konstantene og hvilke elementer er viktige?
NA = Avogadros konstant
|za*zb| = Absoluttverdien av ladning til ion a og b
e^2 = elementærladning
ε = permittiviteten i vakuum, 8.85 * 10^-12 Fm^-1
d = avstanden mellom ionene, r_ion a + r_ion b (gitteravstanden)
d* = 34.5 pm
Hvilke elementer er viktig?
|za*zb| og d er de viktigste verdiene for å kunne regne ut born-mayer likningen.
Hva er gitterentalpi?
ΔHL
Energien som kreves for å bryte opp et fast ionisk krystallgitter til gassfaseioner, eller energien som frigjøres når gassfaseioner danner et krystallgitter. Det måler styrken på de elektrostatiske kreftene mellom ionene.
NaCl (s) -> Na+ (g) + Cl-(g)
Kan regnes på ulike måter:
- Born-Mayer-likningen
- Born-Haber-syklusen
- Kapustinskii-likningen
- Coulombs lov
Forklar Kapustinskii-likningen
Brukes til å estimere gitterentalpi for ioneforbindelser.
K = 1.21 * 10^5 kJpm/mol
d = avstanden mellom ionene, r_ion a + r_ion b (gitteravstanden)
d* = 34.5 pm
Nion = antall ioner per formelenhet
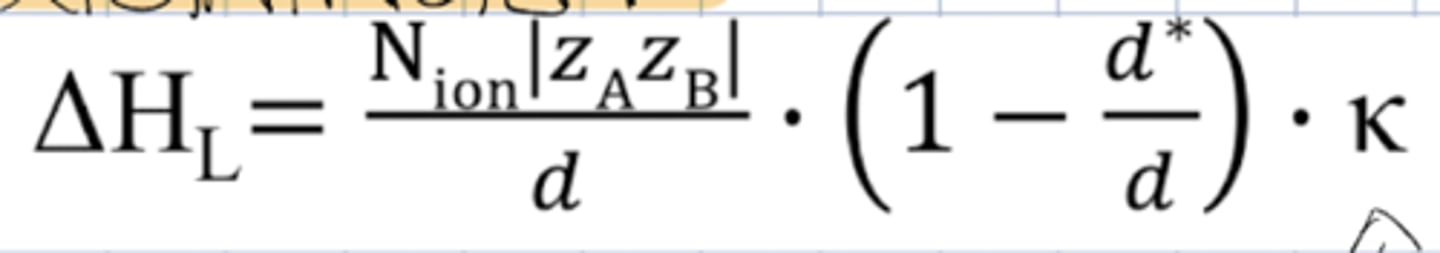
Forklar Coulombs lov
NA = Avogadros konstant
|za*zb| = Absoluttverdien av ladning til ion a og b
e^2 = elementærladning
ε = permittiviteten i vakuum, 8.85 * 10^-12 Fm^-1
d = avstanden mellom ionene, r_ion a + r_ion b (gitteravstanden)
A = Madelungkonstant
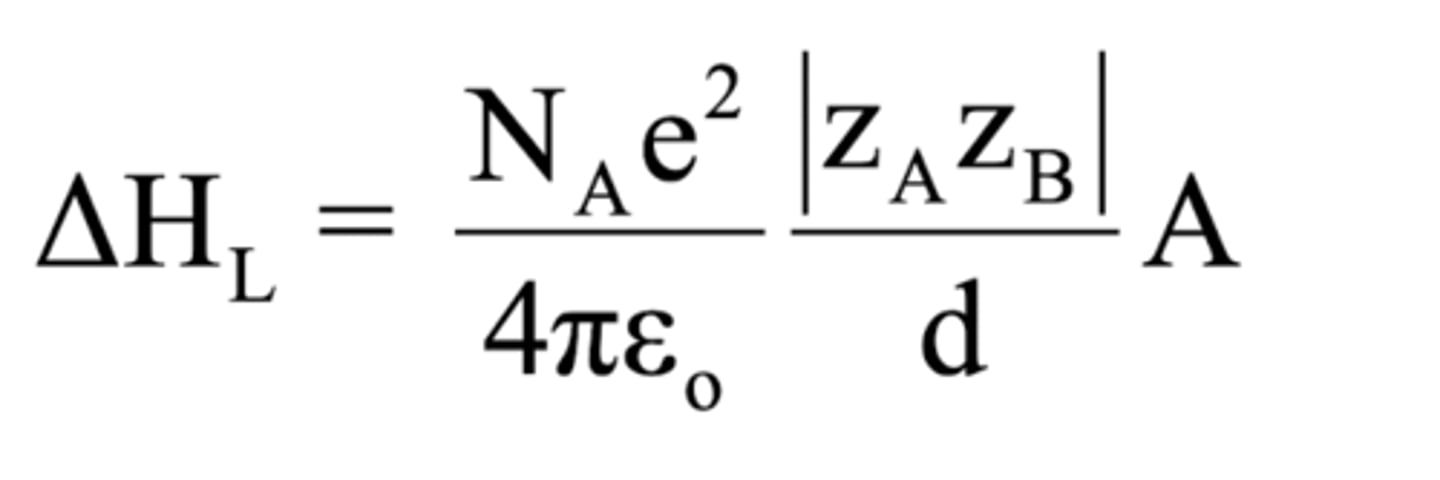
Hva er polymorfisme?
Et stoff som kan ha forskjellige krystallstrukturer.
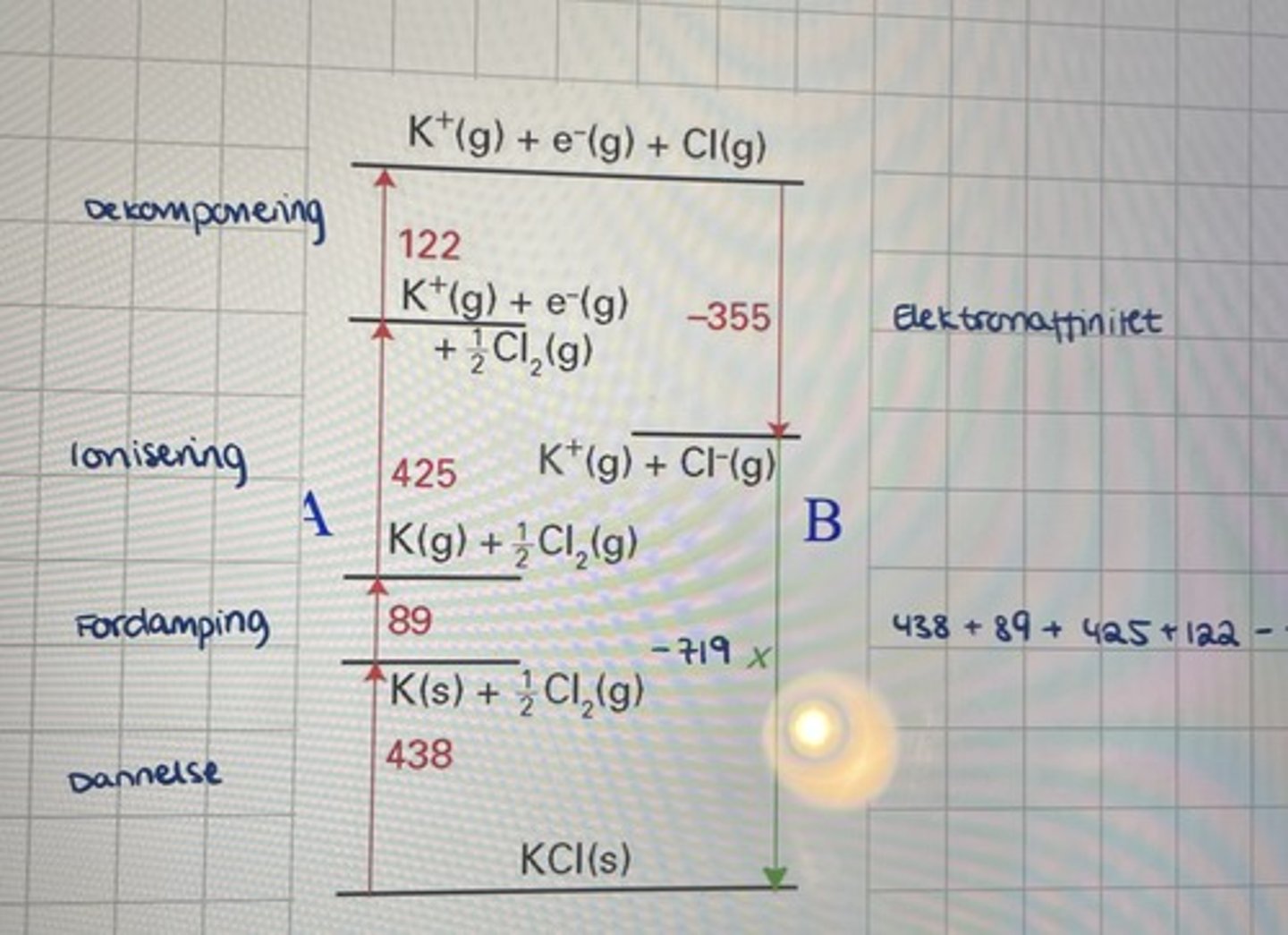
Forklar Born-Haber-Syklusen.
Born-Haber-Syklusen brukes til å regne ut gitterentalpi.
Syklusen:
1. Dannelse (ΔHf)
2. Fordampning (ΔHf)
3. Ionisering
4. Dissosiasjon
5. Elektronaffinitet
Dette er alle ulike entalpiverdier og regnes ut på følgende måte:
ΔHL = (1.) + (2.) + (3.) + (4.) - (5.)
Entalpiverdiene finnes i SI:
(1.), (2.), (4.) => Tabell 16
(3.) => Tabell 14
(5.) => Tabell 15
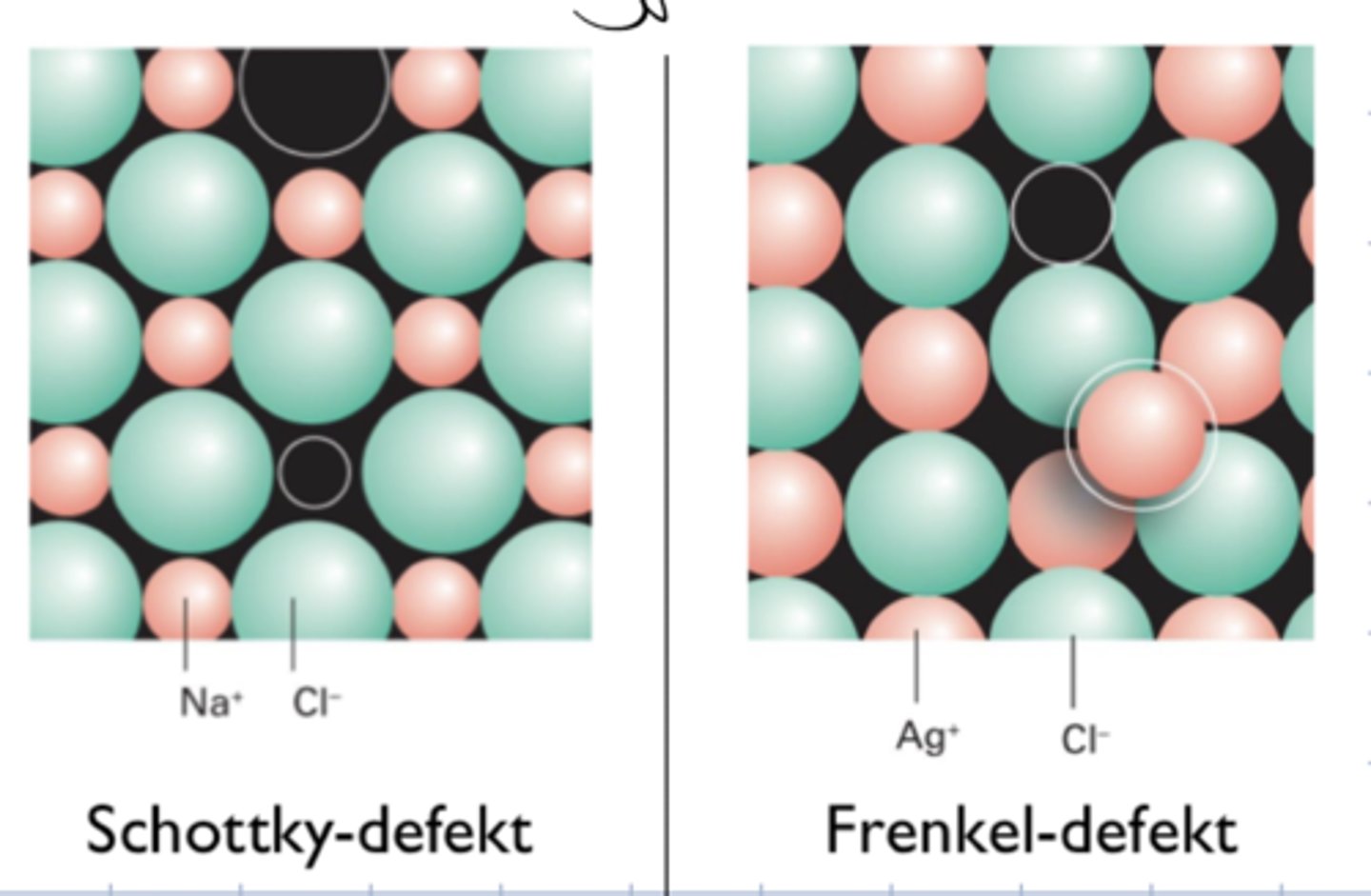
Hva er Schottky og Frenkel-defekt?
To ulike typer intrinsikke punktdefekter.
Schottky:
- Kation+anionvakans par
- Ioneforbindelser
Frenkel:
- Kation + interstielt kation par
- Mest vanlig ved forbindelse med kovalent innslag AgCl
- Lavt koordinasjonstall kation
(tetraedriske)
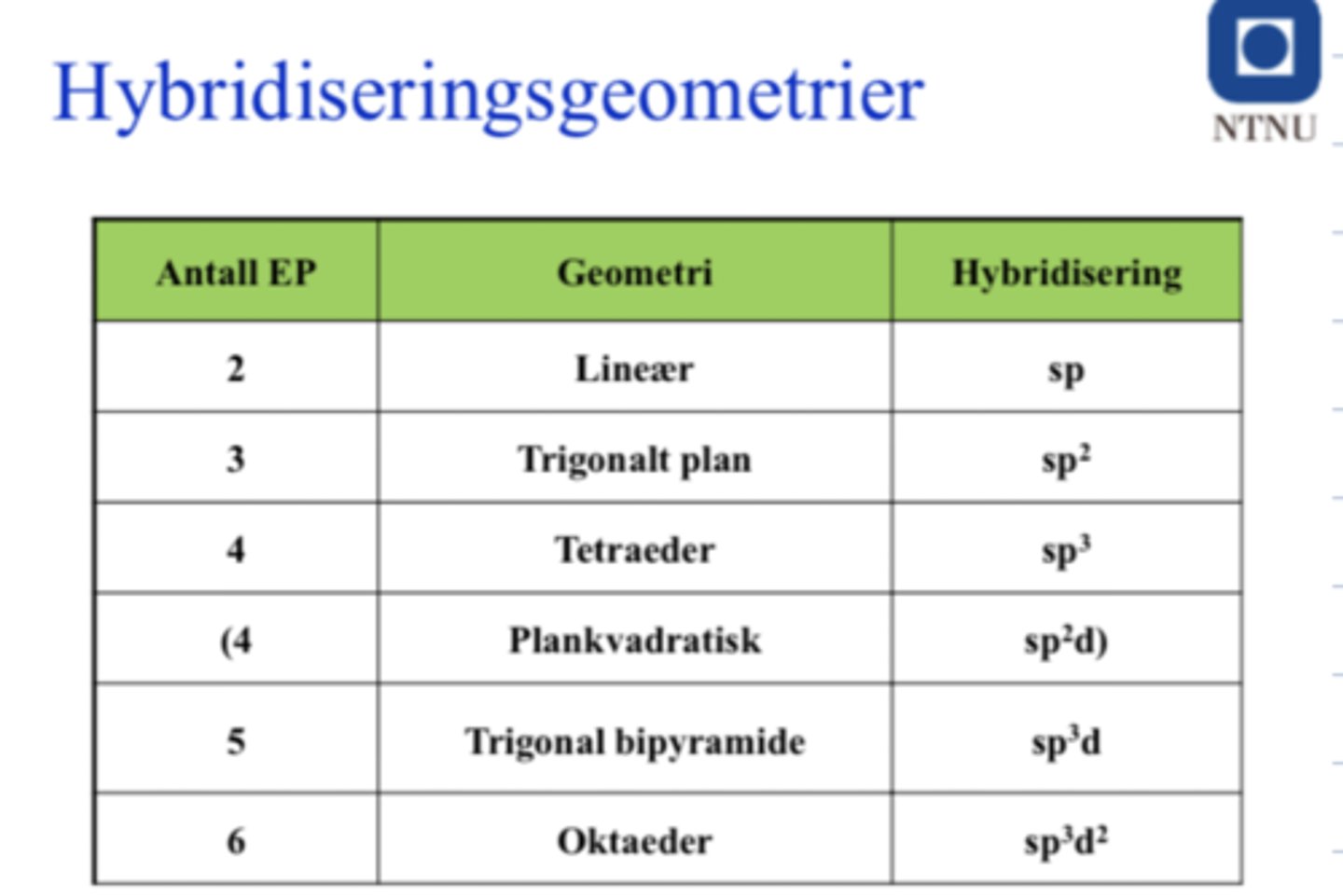
Hva er antallet elektronpar for de ulike hybridiseringsgeometriene?
Hva handler Paulings regler om og hva er disse reglene?
Generelt:
Syrestyrken til en oksosyre øker med økende antall O-atomer
Reglene:
1. For oksosyren O_pE(OH)_q så er
pKa = 8 - 5p
(p er antall oksogrupper)
2. pKa øker med ca. 5 for hvert proton som fjernes (hvis syren er flerprotisk)
OBS! Dette er regler, ikke lover. Betyr at det trender.
Syrestyrke:
HClO4 > HClO3 > HClO2 > HClO
Hva går Jahn-Teller-effekten ut på?
Spontan tetragonal deformasjon av komplekser. Gir lavere energi pga splitting av degenererte orbitaler.
Denne effekten beskriver den geometriske forvrengningen av ulineære molekyler i visse situasjoner.
Et kompleks får lavere energi ved at én akse blir lengre eller kortere enn de to andre
___________________________________________________________
Forklart på en annen måte:
Fenomen der molekyler endrer form for å oppnå lavere energi og økt stabilitet når de har degenererte orbitaler.
Hva er et sfærisk felt?
Et felt hvor det elektriske eller magnetiske feltet rundt et atom/ion er symmetrisk i alle retninger.
Styrken på feltet avtar jevnt med avstanden fra sentrum.
Atomorbitaler:
S-orbitalene i atomer er sfæriske, noe som betyr at sannsynligheten for å finne et elektron er lik i alle retninger rundt kjernen.
Krystallfeltteori:
I ligandfeltteori kan et sfærisk felt brukes som en referanse for å sammenligne effekten av forskjellige ligandfelt på d-orbitaler i overgangsmetallkomplekser.
Hvordan vet man hva slags magnetiske egenskaper et kompleks har?
Du tegner opp MO-diagrammet eller energidiagrammet for å se hvor mange enkle elektroner det er.
Hvis alle elektronene er i par => diamagnetisk, virker frastøtende
Hvis ett elektron er upared => paramagnetisk
Hvordan blir hydrogen produsert?
Industrielt blir det produsert fra naturgass
Hvordan oppstår fargen i mineraler og edelstener?
Tilstedeværelse av overgangsmetaller.
Dette er på grunn av at overgangsmetaller har ufullstendige d-orbitaler som kan absorbere bestemte bølgelengder av lys.
Når lys treffer mineralet, kan elektronene i overgangsmetallet eksiteres til høyere energinivåer.
Fargen vi ser er det komplementære lyset som ikke blir absorbert, men reflektert eller transmittert.
Hva betyr det at et materiale er fosforescerende?
Fosforescens er en undergruppe av luminescens som er et fenomen der lys stråler ut av et
materiale etter at det har absorbert energi.
Ved fotoluminescens kommer denne energien fra
fotoner som absorberes av materialet. Fotonene eksiterer elektroner til et høyere nivå og når
de relakserer sendes det ut lys.
Ved fosforescens må elektronet gå gjennom en forbudt
spinnovergang for å kunne relaksere, hvilket gjør at prosessen tar lengre tid enn for
fluorescens.
Hva er fluorescens?
Et fysisk fenomen hvor et stoff absorberer lys eller annen elektromagnetisk stråling ved en bestemt bølgelengde og deretter emitterer lys ved en lengre bølgelengde.
Dette resulterer i at stoffet lyser opp når det blir belyst.
Hva er problemet med Born-Mayer likningen?
Den tar ikke hensyn til innslag av kovalent karakter.
Hva er trendene for:
1. Atomradius
2. Polariserbarhet
3. Elektronegativitet
4. Elektronaffinitet
5. Ioniseringsenergi
Begrunn hvorfor.
1. Atomradius
Trend: Øker nedover. Synker mot høyre
Begrunnelse:
Høyre: Antall protoner i kjernen øker, som trekker elektronene nærmere
Nedover: Økning i elektronskall
2. Polariserbarhet
Trend: øker med økende ioneradius og minkende ladning.
Begrunnelse: Store anioner med lave ladninger har elektroner lenger fra kjernen, som er lettere å deformere (stor polarisérbarhet).
3. Elektronegativitet
Trend: Øker mot høyre og synker nedover.
Begrunnelse:
Høyre: økt kjerneladning gjør at atomer tiltrekker seg elektroner sterkere.
Nedover:
Økt antall elektronskall øker avstanden mellom kjernen og valenselektronene, noe som reduserer atomets evne til å tiltrekke seg ytterligere elektroner.
4. Elektronaffinitet
Trend: Øker mot høyre, minker nedover.
Begrunnelse: Atomer nær høyre side av en periode ønsker å oppnå oktettregelen, og derfor frigjør de mer energi når de får et ekstra elektron.
Økt avstand mellom kjernen og det ekstra elektronet gjør det mindre energetisk gunstig å legge til et elektron.
5. Ioniseringsenergi
Trend: Øker mot høyre, minker nedover.
Begrunnelse:
Høyre: økt kjerneladningen holder bedre på elektroner, så krever mer energi å fjerne ett elektron.
Nedover: Økt avstand fra kjernen og økt skjerming fjør det lettere å fjerne ion.
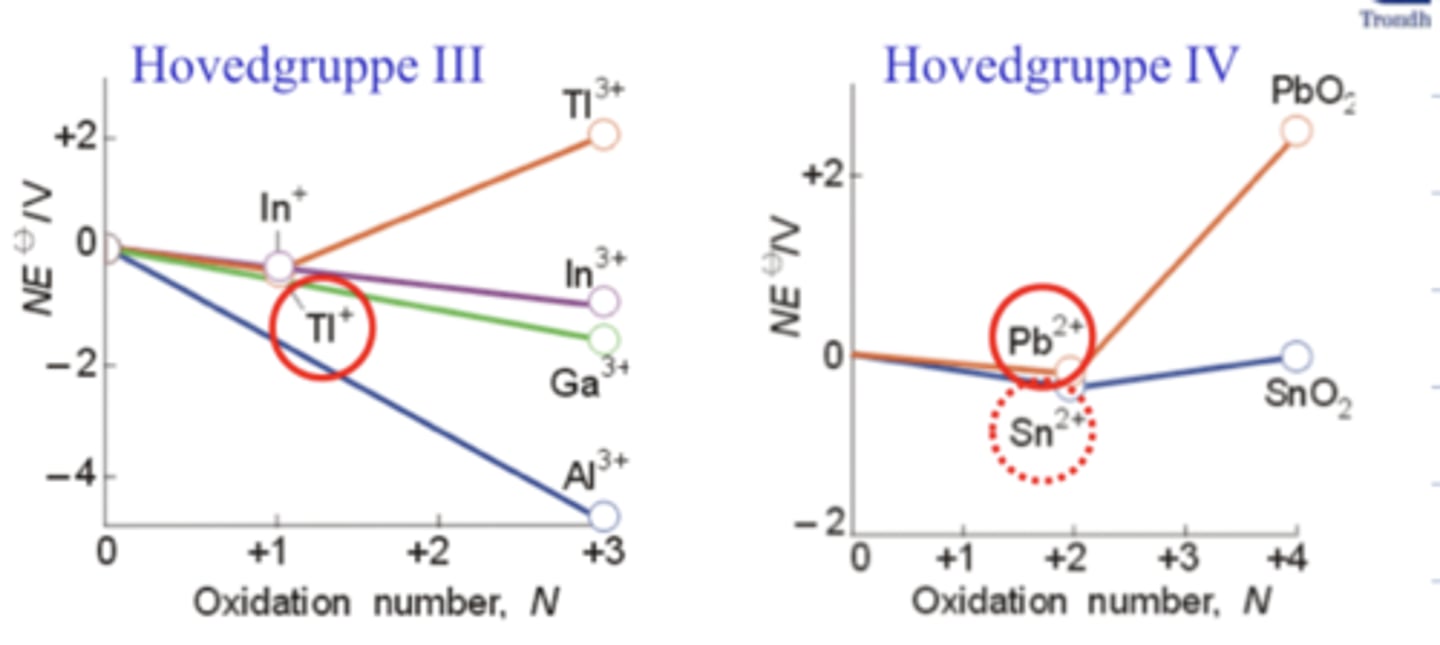
Hvordan leser man av et frost-diagram?
Den laveste verdien er det mest stabile oksidasjonstallet for et gitt element.
Hvordan finner man bindingslengden?
Finner summen av alle kovalente radiuser

Hva er relasjonen mellom elektronegativitet og bindingsenergi?
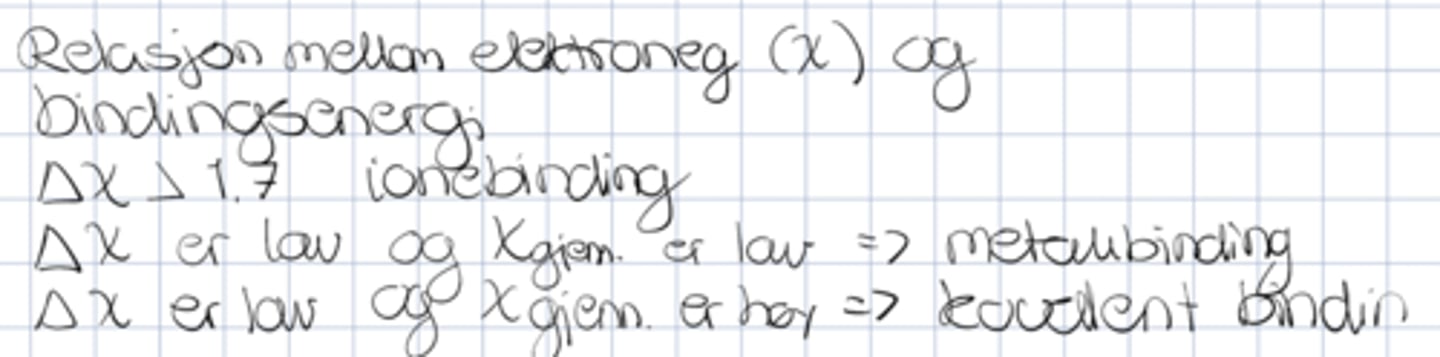
Hva kan forklares med krystallfeltteorien?
Optiske spektre, termodynamisk stabilitet og magnetiske egenskaper
Oktaedrisk kompleks:
Hva brukes for å symbolisere orbitaler med høyest og lavest energi?
Orbital med høyest E:
eg, dobbe degenerert
(dz^2 og dx^2-y^2)
Orbital med lavest E:
t2g, trippel degenerert
(dzx, dyz, dxy)
Tetraedrisk kompleks:
Hva brukes for å symbolisere orbitaler med høyest og lavest energi?
Orbital med høyest E:
t2, trippel degenerert
Orbital med lavest E:
e, dobbe degenerert