Quimica1-Tema 3
1/18
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No study sessions yet.
19 Terms
Forces de London (dispersió)
→ Dipol induït – dipol induït
→ Presentes en totes les molècules
→ Augmenten amb la massa molecular i la superfície
Forces dipol–dipol permanents
→ Entre molècules polars
Pont d’hidrogen
→ Quan H està enllaçat a N, O o F
→ Forces intermoleculars més fortes
Ordre de força intermolecular
→ London < dipol-dipol < pont d’hidrogen
Índex de coordinació (IC)
Nombre de veïns més pròxims
Factor d’empaquetament (fe)
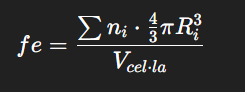
Densitat cristal·lina
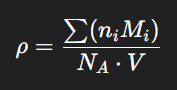
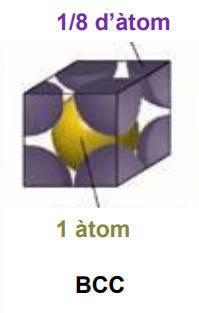
BCC
📘 Àtoms per cel·la
→ n = 2
📘 Índex de coordinació
→ IC = 8
📘 Relació a–R
a=4R/√3
📘 Factor d’empaquetament
→ fe = 68 %
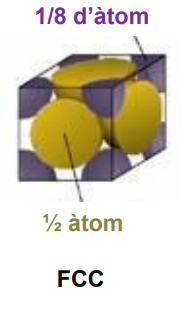
FCC
📘 Àtoms per cel·la
→ n = 4
📘 Índex de coordinació
→ IC = 12
📘 Relació a–R
a=R/√2
📘 Factor d’empaquetament
→ fe = 74 %
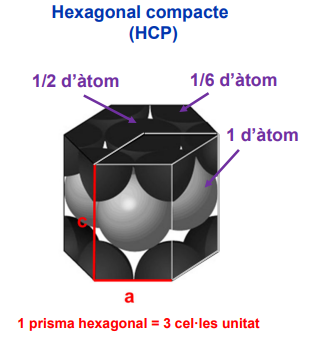
HCP
📘 Àtoms per cel·la
→ n = 2
📘 Índex de coordinació
→ IC = 12
📘 Factor d’empaquetament
→ fe = 74 %
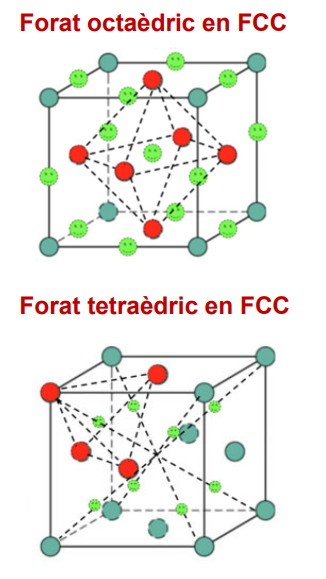
Forats HCP i FCC
📘 Nombre de forats octaèdrics
→ 1 per àtom
→ FCC: 4 forats/cel·la
📘 Nombre de forats tetraèdrics
→ 2 per àtom
→ FCC: 8 forats/cel·la
📘 Radi forat octaèdric
→ r_f = 0,414 R
📘 Radi forat tetraèdric
→ r_f = 0,224 R
📘 Relació radi forat octaèdric / radi metall rf. / R
→ a= 2ꞏR+ 2ꞏrf. octa
📘 Relació radi forat tetraèdric / radi metall rf. / R
→ a*√3/4= R+ rf. tetra
Forats BCC
📘 Tipus de forats
→ Pseudo-octaèdrics i pseudo-tetraèdrics
📘 Nombre de forats p-octaèdrics
→ 6 per cel·la // 3N //
📘 Nombre de forats p-tetraèdrics
→ 12 per cel·la // 6N
📘 Radi forat p-octaèdric
→ r_f = 0,155 R
📘 Radi forat p-tetraèdric
→ r_f = 0,291 R
NaCl

CsCl

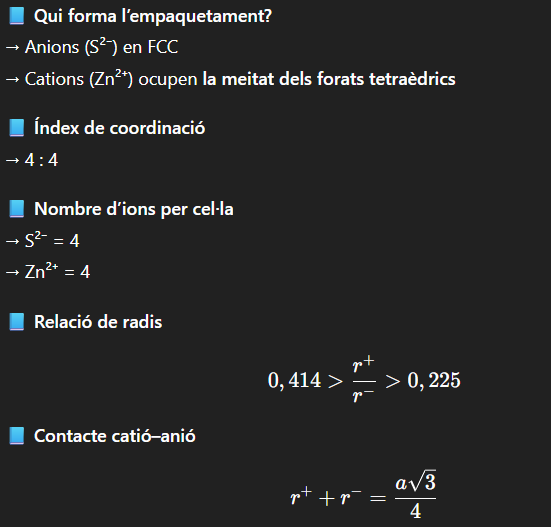
ZnS
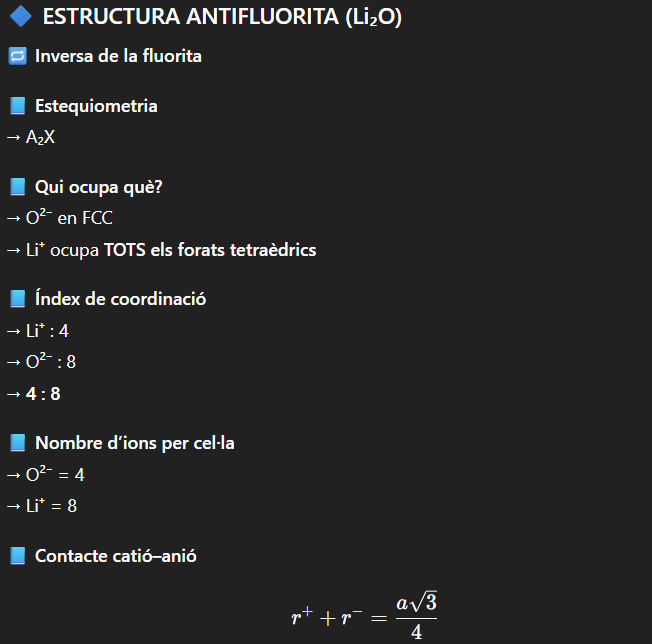
CaF2 Fluorita

Li2O Antifluorita