Uorganisk kjemi, TMT4130
1/241
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
242 Terms
Hva angir hovedkvantetallet?
Hovedkvantetallet angir energinivået til en orbital.
Hva angir orbitalvinkelmomentkvantetallet?
Orbitalvinkelmomentkvantetallet angir vinkelmomentent som et elektron i en orbital har. Orbitalvinkelmomentkvantetallet kan også fortelle oss hvilken form orbitalen har.
Hva angir det magnetiske kvantetallet?
Det magnetiske kvantetallet spesifiserer retningen på vinkelmomentet rundt en gitt akse (ofte z-aksen) gjennom atomkjernen. Lettere sagt: Angir orienteringen til orbitalen i rommet.
Magnetisk spinkvantetall
Angir om et elektron i en orbital har spin opp, eller spin ned.
Hvilke verdier kan hovedkvanteallet ta?
n≥1
Hvilke verdier kan orbitalvinkelmomentkvantetallet ta?
l=n-1
Hvilke verdier kan det magnetiske kvantetallet ta?
-l,...,0,...,l dvs for l=0, ml=0
for l=1, ml=-1,0,1
for l=2, ml=-2,-1,0,1,2
for l=3, ml=-3,-2,-1,0,1,2,3
Hvilke verdier kan det magnetiske spinkvantetallet ta?
±1/2
Hva slags type orbital er en orbital med orbitalkvantetallet l=0?
s-orbital
Hva slags type orbital er en orbital med orbitalkvantetallet l=1?
p-orbital
Hva slags type orbital er en orbital med orbitalkvantetallet l=2?
d-orbital
Hva slags type orbital er en orbital med orbitalkvantetallet l=3?
f-orbital
Hva skjer med verdien til energinivået til n=1 når atomnummeret (z) øker?
Energinivået for n=1 synker.
Hva skjer med energigapet mellom påfølgende energinivå (n=1, n=2 osv) når atomnummeret (z) øker?
Energigapet øker.
Hva er et nodalplan?
Et nodalplan er et punkt i rommet hvor det er ingen sannsynlighet for å finne et elektron.
ψn,l,ml=Rnl(r)*Yl,ml( θ,φ) er et generelt uttrykk for bølgefunksjonen for en partikkel. Hvilken del er beskriver den radielle delen, og hvilken beskriver den angulære delen?
Rnl(r) beskriver den radielle delen
Yl,ml( θ,φ) beskriver den angulære delen
Hva er den generelle regelen for antall radielle nodalplan for s,p,d,f?
Antall radielle nodalplan= n-l-1
Hva er den generelle regelen for antall angulære nodalplan for s,p,d,f?
Antall angulære nodalplan= l
Hvordan ser s-orbitalen(e) ut?
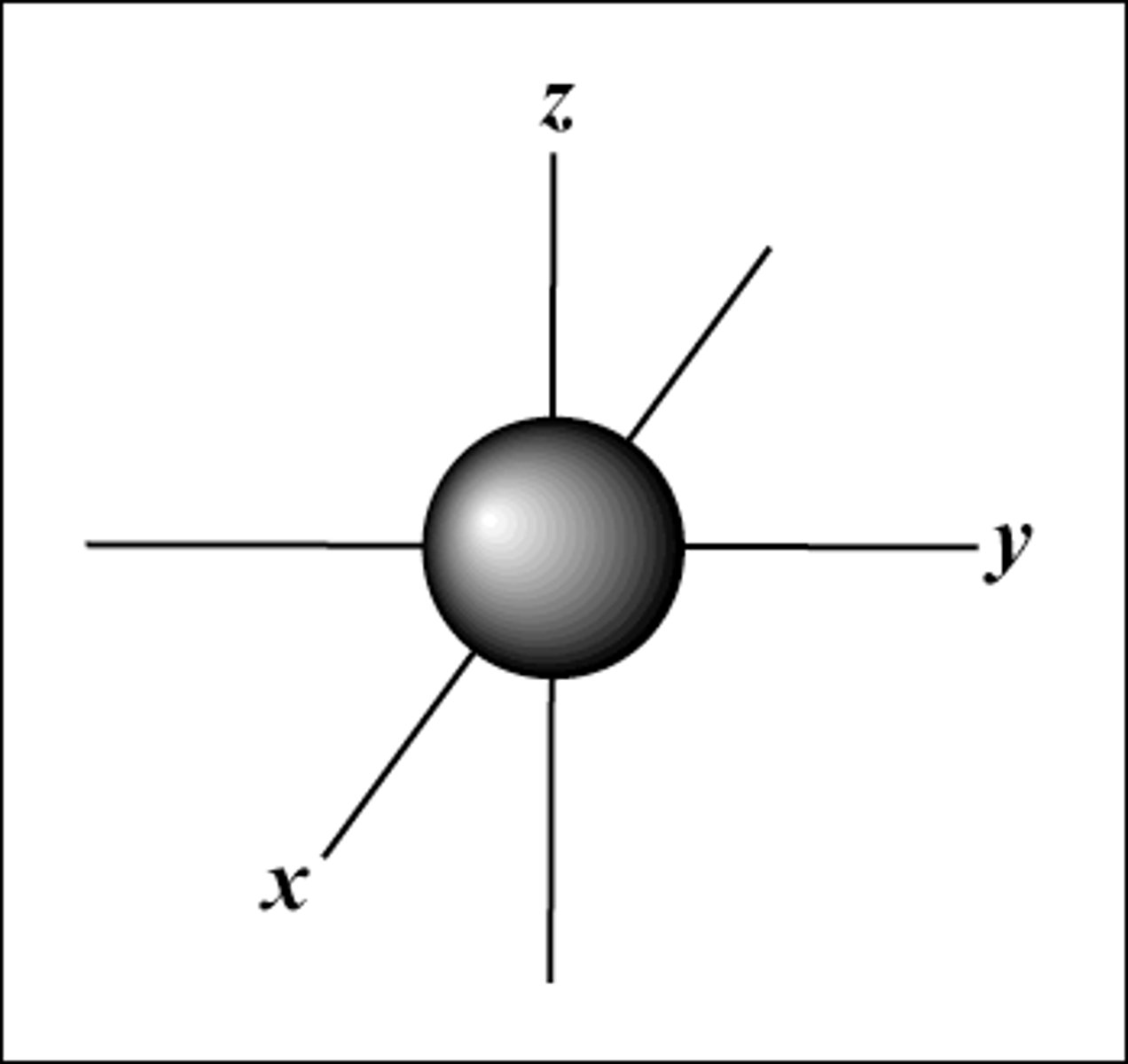
Hvordan ser p-orbitalen(e) ut?
Tre ballongformede orbitaler langs x-,y-,z-aksen. Hver orbital har et angulært nodalplan i 'origo'.
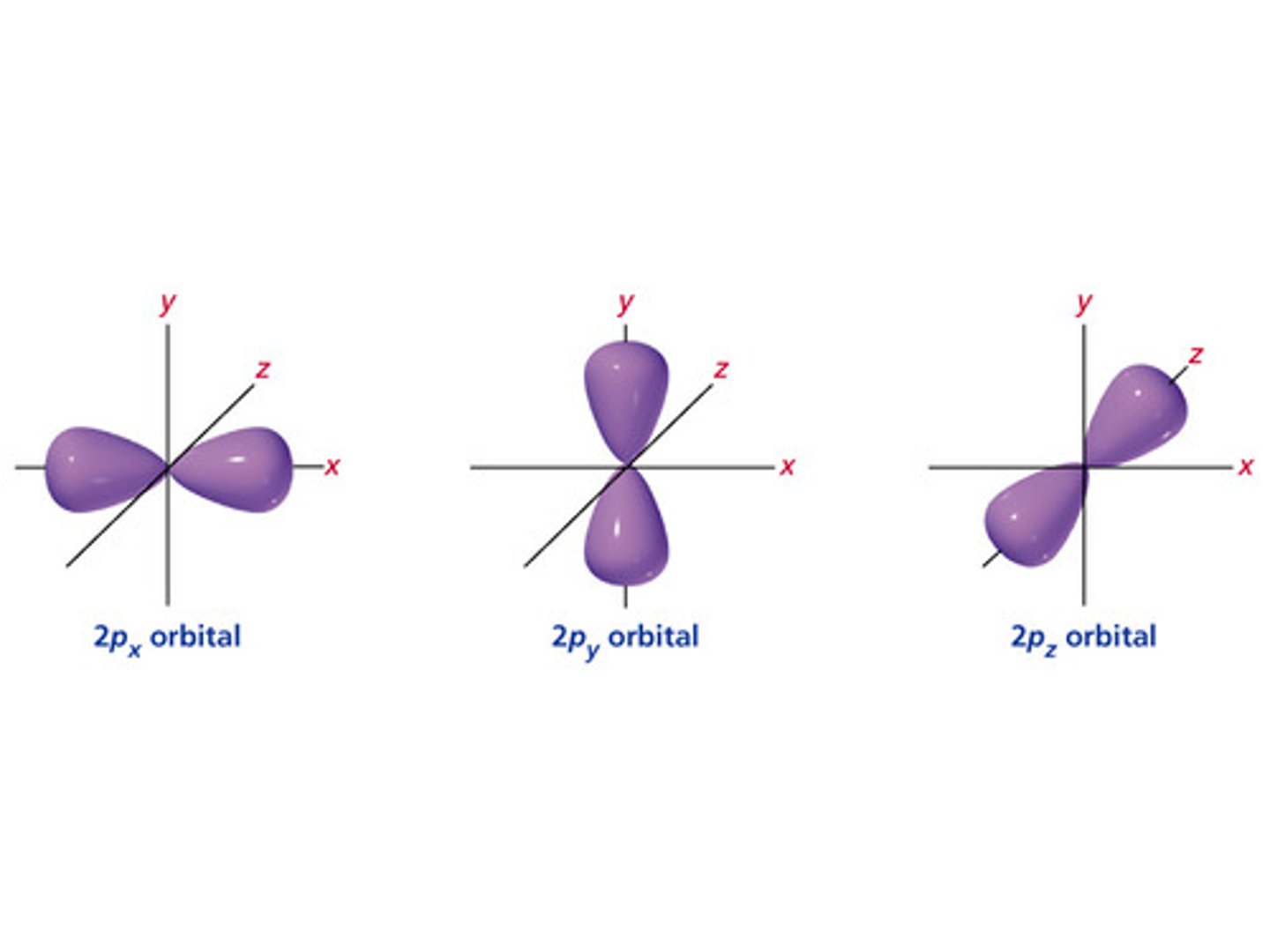
Hvordan ser d-orbitalen(e) ut?
Fire orbitaler som ser ut som firkløvere, en som ser ut som en p-orbital langs z-aksen med badering. Hver orbital har to angulærte nodalplan.
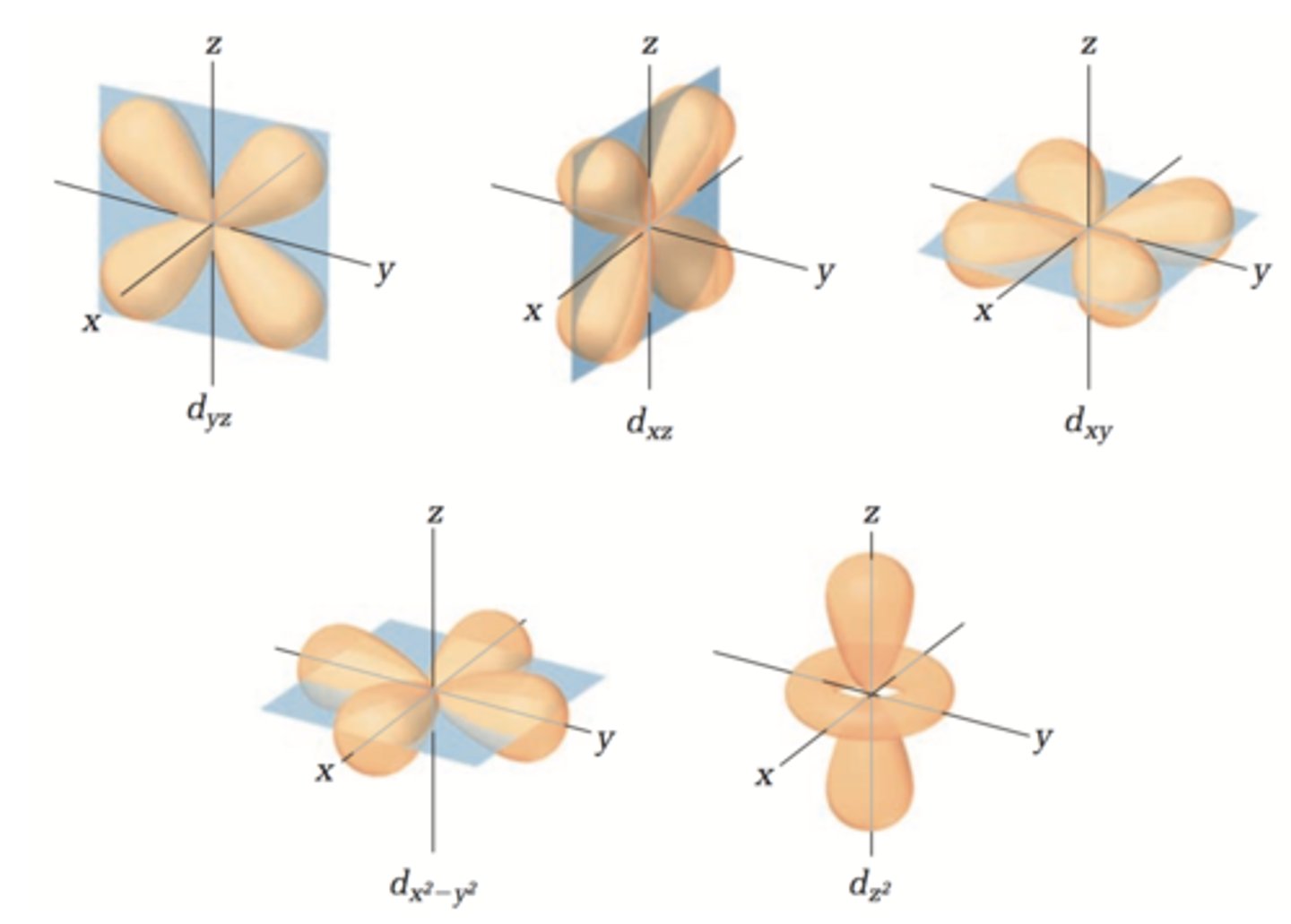
Hva sier Aufbau-prinsippet?
Blir også kalt oppbygnings-prinsippet.
1. Ett og ett proton blir lagt til kjernen når atomet blir 'bygd'
2. Elektroner blir først plassert i orbitaler med lavest energi
Har unntak, men et godt utgangspunkt.
Hva sier Pauli prinsippet?
To elektroner i en orbital kan ikke ha samme kvantetilstand.
Hva sier Hunds regel?
Elektronkonfigurasjonen med lavest energi for et atom er den som gir maksimalt antall uparede elektroner i et sett degenererte orbitaler.
Hva er er effektiv ladning?
Effektiv ladning(Zeff) er den kjerneladningen som et elektron 'ser'. Zeff=Kjerneladning(Z)-σ
Hva er skjerming?
Reduksjonen i virkelig kjerneladning til den effektive kjerneladning på grunn av andre elektroner.
Hva er Slater's regler for å regne ut effektiv kjerneladning (Zeff)?
Hvis ytterste orbital er s eller p:
-De andre elektronene i nsnp-gruppen bidrar til 0.35 til σ
-Hvert elektron i n-1 skall bidrar til 0.85 til σ
-Hvert elektron i lavere skall bidrar til 1.0 til σ
Hvis ytterste skall er d eller f orbital:
-De andre elektronene i nd eller nf gruppen bidrar med 0.35 til σ.
-Elektronene i lavere skall bidrar med 1.0 til σ.
Hvilke(n) orbital(er) regnes som valenselektroner i s-blokka?
ns- orbitalen
Hvilke(n) orbital(er) regnes som valenselektroner i p-blokka?
ns+np orbitalene
Hvilke(n) orbital(er) regnes som valenselektroner i d-blokka?
ns + (n-1)d orbitalene
Evnen orbitaler har til å skjerme i stigende rekkefølge:
f
Hvordan øker/minker Zeff i det periodiske system?
Zeff øker mot høyre i det periodiske system.
For Z≥21, ligger 3d lavere i energi enn 4s. Likevel fylles 4s opp først. Hvorfor?
4s fylles først for nesten alle atomer pga elketron-elektron interaksjoner i 3d.
Hvilke unntak finnes det fra regelen om at 4s orbitalen fylles først? Og hvorfor?
Cr: [Ar]4s^1 3d^5
Cu: [Ar]4s^1 3d^10
Dette skyldes at halvfulle og fulle underskall er mer stabile. Dette gjelder også for andre atomer i Cr og Cu sin gruppe.
Hvordan endres atomradiusen i det periodiske system?
Atomradiusen øker nedover en gruppe og avtar bortover en periode (gjelder mest i s og p blokken).
Forklar begrepet 'lantanidekontraksjon'.
Det faktum at 2 og 3 rekke i overgansmetaller har tilnærmet lik radius. Dette skyldes at 4f-elementer er i mellom. f-orbitaler skjermer dårlig og atomradiusen blir lite påvirket.
Definer ioneradius.
Ioneradius er definert som størrelsen på kationer eller anioner. For å bestemme verdien på ioneradius må det angis et referansepunkt og bestemte Pauling at O2- ionet skulle være 141 pm. Alle andre ioneradiuser er gitt relativt til dette. (med noen justeringer)
Hvordan endres ioneradiusen med økende/avtagende ladning?
Ioneradiusen øker med økende negativ ladning, og avtar med økende positiv ladning.
Hvordan påvirker koordninasjonstallet ioneradiusen?
Ioneradiusen øker når koordinasjontallet øker. Elektronskyen blir "dratt" utover når det er flere ioner rundt.
Definer ioniseringsenergi
Den energien som er nødvendig for å fjerne et elektron hver atom i et mol av atomer i gassfasen.
Hvordan øker/minker ioniseringsenergien i det periodiske system?
Ioniseringsenergien øker bortover en periode og reduseres nedover en gruppe. Finnes unntak mellom gruppe 2 og 3, og 5 og 6.
Hvorfor har B (gruppe 3) lavere ioniseringsenergi enn Be (gruppe 2)?
Dette skyldes B har kun ett elektron i p- orbitalen som den gjerne kan bli kvitt. Be har to elektroner i s- oribtalen, og det koseter mer å fjere et elektron fra en orbital som allerede er full.
Hvorfor har O (gruppe 6) lavere ioniseringsenergi enn N (gruppe 5)?
Dette skyldes at O få en halvfull p-orbital når ett elektron fjernes. N har allerede en halvfull p-orbital og blir mindre stabilt når ett elektron fjernes.
Definer elektronaffinitet
Energien det trengs for å legge til ett elektron til hvert atom i et mol atomer i gassfasen.
Definer elektronnegativitet
Et elements evne til å tiltrekke seg et delt elektronpar mot seg selv. Altså, evnen til å tiltrekke seg elektroner i et kovalent bånd.
Hvordan øker/avtar elektronaffinitet i det periodiske system?
Generelt, øker langs en periode, men er ikke så klare trender som for f.eks atomradius.
Hvordan øker /avtar elektronegativiteten i det periodiske system?
Øker langs en periode og avtar ned en gruppe.
Forklar begrepet polariserbarhet
Polariserbarhet er et atoms evne til å bli forskjøvet (pertubert) i et elektrisk felt.
Hvilke atomer/ioner er lett polariserbare?
Store tunge atomer og anioner, og kationer uten edelgasskonfigurasjon.
Hvilke atomer/ioner er lite polariserbare?
Små kationer med høy ladning og edelgasskonfigurasjon.
Nevn noen egenskaper til en ionebinding
-Elektrostatiske tiltrekninger mellom ladninger
-Sterk binding
-Stor forskjell i elektronengativitet mellom ionene, Δχ>1.7
-Den elektrostatike tiltrekningen er relativt langtrekkende og urettet (sprer seg radielt utover)
Nevn noen egenskaper til en kovalent bining
-Sterk binding
-Felles elektronpar som deles mellom atomer
-Relativt korttrekkende (sammenlignet med ionebinding) og rettet
Hva er en Lewisstuktur?
En Lewisstruktur er en måte å prediktere hvor mange bindingspar og frie elektronpar et molekyl har. Lewisstruktur tar utgangspunkt i at atomer følger oktettregelen.
Hva er resonans?
Hvis et molekyl har resonans betyr det at den kan ha flere Lewisstrukturer.
Hva er en resonanshybrid?
En resonanshybrid er 'gjennomsnittet' av alle Lewisstrukturene til et molekyl (e.g benzne har flere resonans strukturer). Energien til resonanshybriden er lavere enn for hver struktur.
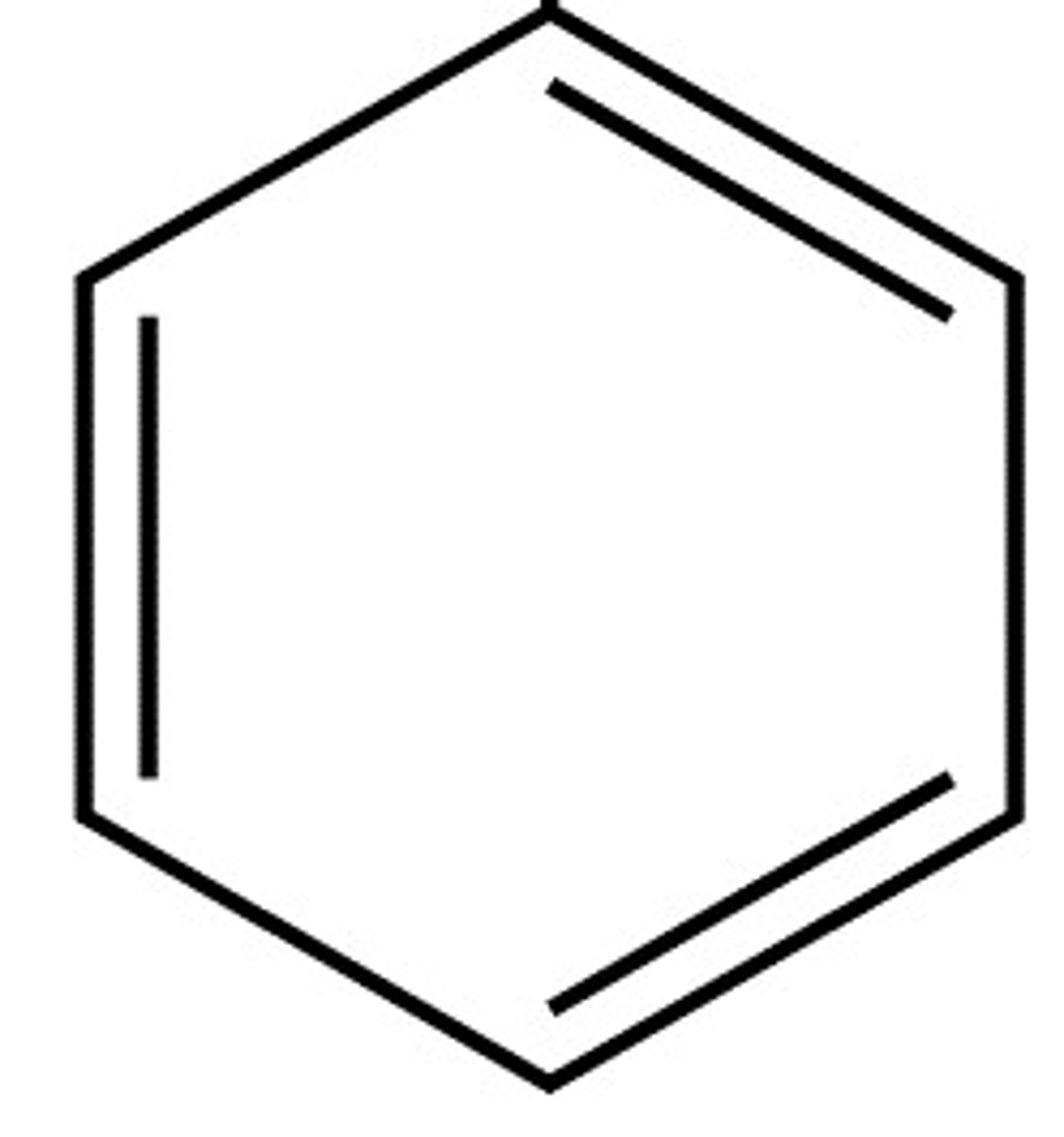
Hva er formell ladning?
Formell ladning er ladningen gitt til hvert atom i et molekyl med antakelsen at alle bånd er delt likt mellom atomene uten å ta hensyn til elektronegativitet.
Hva bruker man formell ladning til?
Hvis et molekyl har flere Lewisstukturer, beregner man den formelle ladningen og velger Lewisstrukturen med lavest formell ladning.
Hvordan beregner man formell ladning?
Man beregner formell ladning per atom. Deretter adderer man den formelle ladningen for alle atomene i molekylet. FC= antall frie elektronpar- (bindings elektronpar)/2
eller FC=valens elektroner - egne elektroner
Hva er valensbindingsteorien?
Valensbindingsteorien er basert på kvantemekanikk. Uttrykker Lewismodell ved hjelp av bølgefunksjoner. Bindinger dannes ved overlapp mellom orbitaler.
Hva kjennetegner en σ-binding?
-Sylindrisk symmetri rundt bindingsaksen
-Bindende elektroner ligger langs bindingsaksen
-Dannes av s-,p- eller d- orbitaler
Hva kjennetegner en π-binding?
-Bindende elektroner ligger parallellt med bindingsaksen
-Dannes av p- eller d-orbitaler
-Endrer fortegn ved rotasjon av bindingsakse
Hva er hypervalens, og hvorfor kan noen atomer ha hypervalens?
Hypervalens betyr at et atom har en utvided oktet dvs har flere enn 8 elektroner i ytterste skall. En forklaring er at noen elementer kan ha plass til flere elektroner fordi den har tomme 3d orbitaler som elektroner kan okkupere. Dette kan også forklares med MO-teori, da uten å ta i 3d-orbitalargumentet. Likevel betyr det ikke at 3d-orbitalene deltar i bindingen.
Hvilke elementer har muligheten til å ha hypervalens?
For å kunne ha hypervalens må atomet være stort nok for at det geometrisk sett skal være mulig + ha ledig 3d orbital (hvis man går for den forklaringen).
Hva er hybridisering?
Hybridisering er å sette sammen orbitaler fra samme atom. De lages ved lineærkombiansjoner av atomorbitalene (AO).
Hvorfor lager vi hybridiserte orbitaler?
Hybridiserte orbitaler er rettede dvs en konkret retning i rommet. Dette danner bedre overlapp av orbitaler.
Hvilke hybridiseringer må du huske til eksamen?
-sp3
-sp2
-sp
-dsp3
-d2sp3
Hva er sp3 hybridisering?
-Lages med en s orbital og 3 p orbitaler
-Danner 4 like hybridorbitaler
-Peker i forskjellige retninger, er et tetraeder
-eks CH4
Hva er sp2 hybridisering?
-Lages med en s orbital og 2 p orbitaler
-Danner 3 like hybridorbitaler
-Peker i forskjellige retinger, atomet har trigonal planar stuktur
-eks C2H4 og BF3
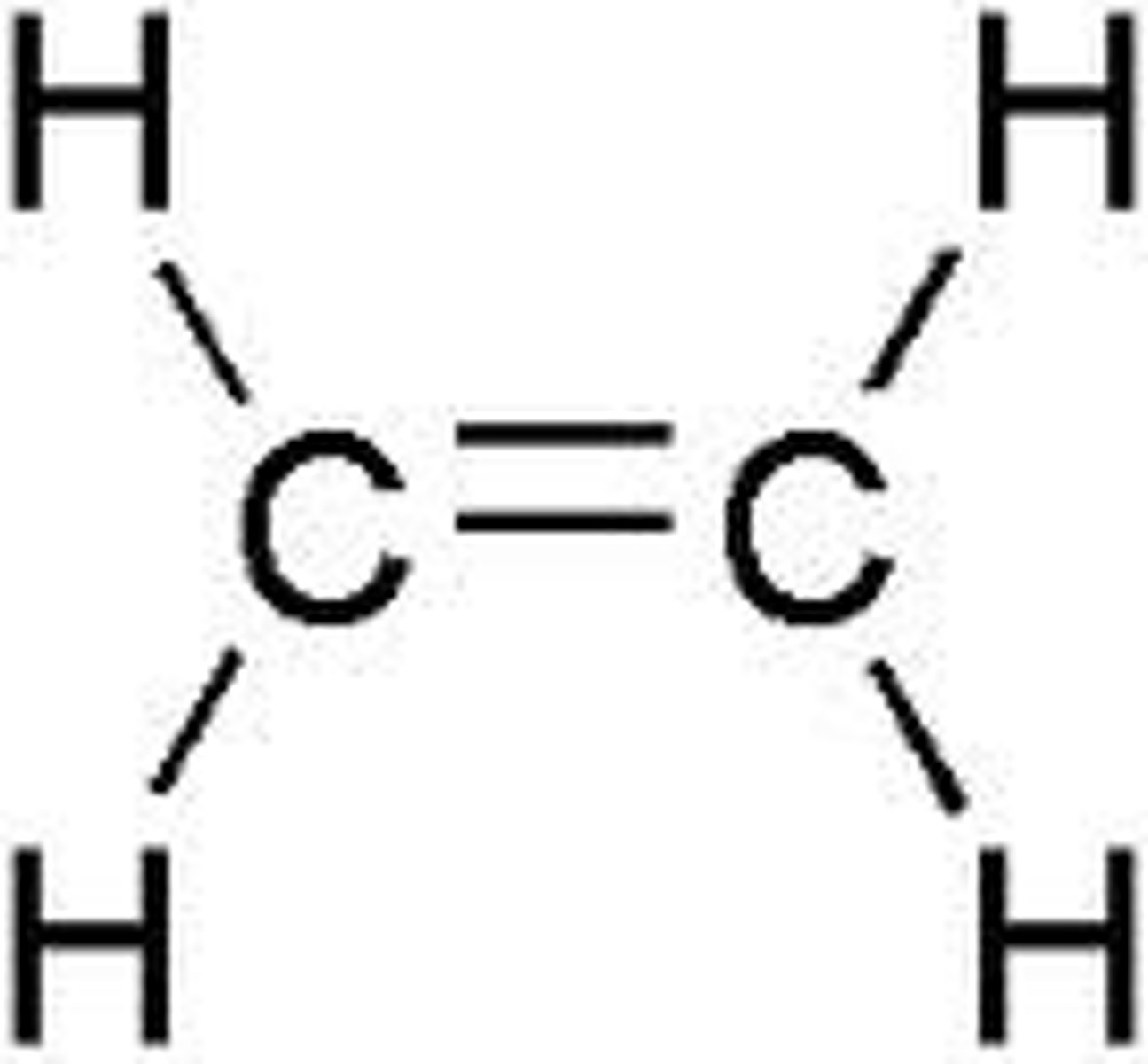
Hva er sp hybridisering?
-Lages med en s orbital og en p orbital
-Danner to like hybridorbitaler
-Peker i forskjellige retninger, er linært
-etyne og N2
Hva er dsp3 hybridisering?
-Lages av en d- og en s-orbital, og 3 p orbitaler
-5 hybridorbitaler som ikke er like, 3 ekvatorielle og 2 aksielle
-Ekvatorielle =sp2 (s+ px+ py), aksielle= (dz^2 og pz)
-Trigonal bipyramide struktur
Hva er d2sp3 hybridisering?
-Lages av to d-orbitaler, tre p-orbitalero g en s orbital
-6 hybridorbitaler som alle er like
-Orbitaler s, px,py,pz, dx^2-y^2,dz^2
-Oktraedrisk stuktur
Hva er molekylorbitalteorien?
Molekylorbitaler (MO) er tilsvarende løsnig for den kvantemekaniske behandlingen av molekyler. En approksimativ modell for MO er en linærkombinasjon av atomorbitalene til valenselektronene.
Hva er et basissett?
Et basissett er det settet av orbitaler som blir brukt for å danne molekylorbitaler(MO).
Hva er en anti-bindene MO?
En anti-bindende MO er en orbital som har høyere energi enn atomorbitalene (AO) den er laget av. Det er ingen elektrontetthet (nodalplan) mellom atomkjernene.
Hva er en bindende MO?
En bindende MO er en orbital som har lavere energi enn atomorbitalene(AO) den er laget av. Det er stor elektrontetthet mellom atomkjernene.
Hva er en ikke bindende MO?
En ikke bindende er en orbital som har samme energi som atomorbitalene den er laget av. Den er 'likegyldig' til binding.æ
Hva er det minste antall MO i et molekyl?
Det er minste antallet MO er lik antall AO for atomene i molekylet.
For hvilket element og nedover blir energiforskjellen mellom s og p orbitalene så liten at σ2g og π1u 'bytter plass' i et homonuklært molekyl?
Dette skjer for N2 og nedover. For O2 og oppover, er denne energiforskjellen så stor at π1u ligger over σ2g i energi.
Hva er viktig å tenke på for å konstruere et MO-diagram for et hetronukleært diatomisk molekyl?
-Energien til orbitalene er ulik for ulike atomer
-Økende elektronegativitet forskyver energi til valens AO ned relativt til AO for elektropositive element
Hva er bindingsorden, og hvordan beregnes den?
B=0.5(antall elektroner i bindene i MO- antall elektroner ianti-bindende MO)
Hvor degeneret er henholdsvis MO'ene a,e og t?
a=ikke degenerert
e=dobbelt degenerert
t=trippel degenerert
Hva kjennetegner krystallinske materialer?
-Regelmessig struktur/periodisitet
-Krystallgitter av ioner/atomer
Hva er enhetscellen til et krystalinsk materiale?
-Den minste representerbare enheten
Hva slags parametere har vi for krystallsystemer?
a,b,c,α,β og γ
Hva forteller de forskjellige parameterene oss?
a,b,c er lengder. Vinkel mellom a og b er γ, vinkelen mellom b og c er α, og vinkelen mellom c og α er β.
Hvor mange systemer gir disse paramterene?
De kan gi 7 ulike systemer
Hvilke antakelser gjelder for modellen for kystallsturkturer.
-Kulepakning (atomer/ioner som runde kuler)
-Basert på å 'fylle' rommet med kuler/byggestener
-Mindre fokus på bindinger i faste stoff (ione, kovalent, metallisk)
Hva slags antaklser gjelder for tetteste kulepakning?
-Antar at atomer som harde kuler med lik radius
-Pakker kuler så tett som mulig
Egenskaper til kubisk tetteste kulepakning?
-Rekkefølge på lagene ABCABC
-74% av volumet er fylt med kuler
-Heter cubic clodes- packed (CCP) eller face-centered cubic (FCC)
Egenskaper til heksagonal tetteste kulepakning?
-Rekkefølge på lagene ABABAB
-74% av volumet fylt med kuler
-Heter hexagonal close-packed(HCP)
Hva slags hull er det i tetteste kulepakning, og hvor mange er det per kulepakning?
Det finnes tetragonalt- og oktaedrisk hull. Det er to teragonale hull per tetteste kulepakning og ett oktaedrisk hull per tetteste kulepakning.
Hvor stort er et oktaedrisk hull?
r(oktaedrisk)=0.414*r(ion/atom)
Hvor stort er et tetraedrisk hull?
r(tetraedrisk)=0.225*r(ion/atom)
Hvor tett pakket er primitiv kubisk kulepakning?
54% av volumet er fyllt med kuler.
Hvor tett pakket er romsentrert kubisk kulepakning(BCC)?
68% av volumet er fyllt med kuler.
Hva betyr polymorfisme?
At et metall kan krystallisere i flere ulike strukturer.
Hva er en polymorf?
En polymorf er en fase med en gitt krystallstruktur.
Hva er en legering?
En legering er en blanding mellom metaller.
Hvilke egenskaper har legeringer?
-Er en fast løsning
-Har liten ∆χ (gjelder mest for substitusjonelle)
-Elektropositive elementer
To vanlige typer legeringer:
Substitusjonell og inerstitiell