Kemi
1/31
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
32 Terms
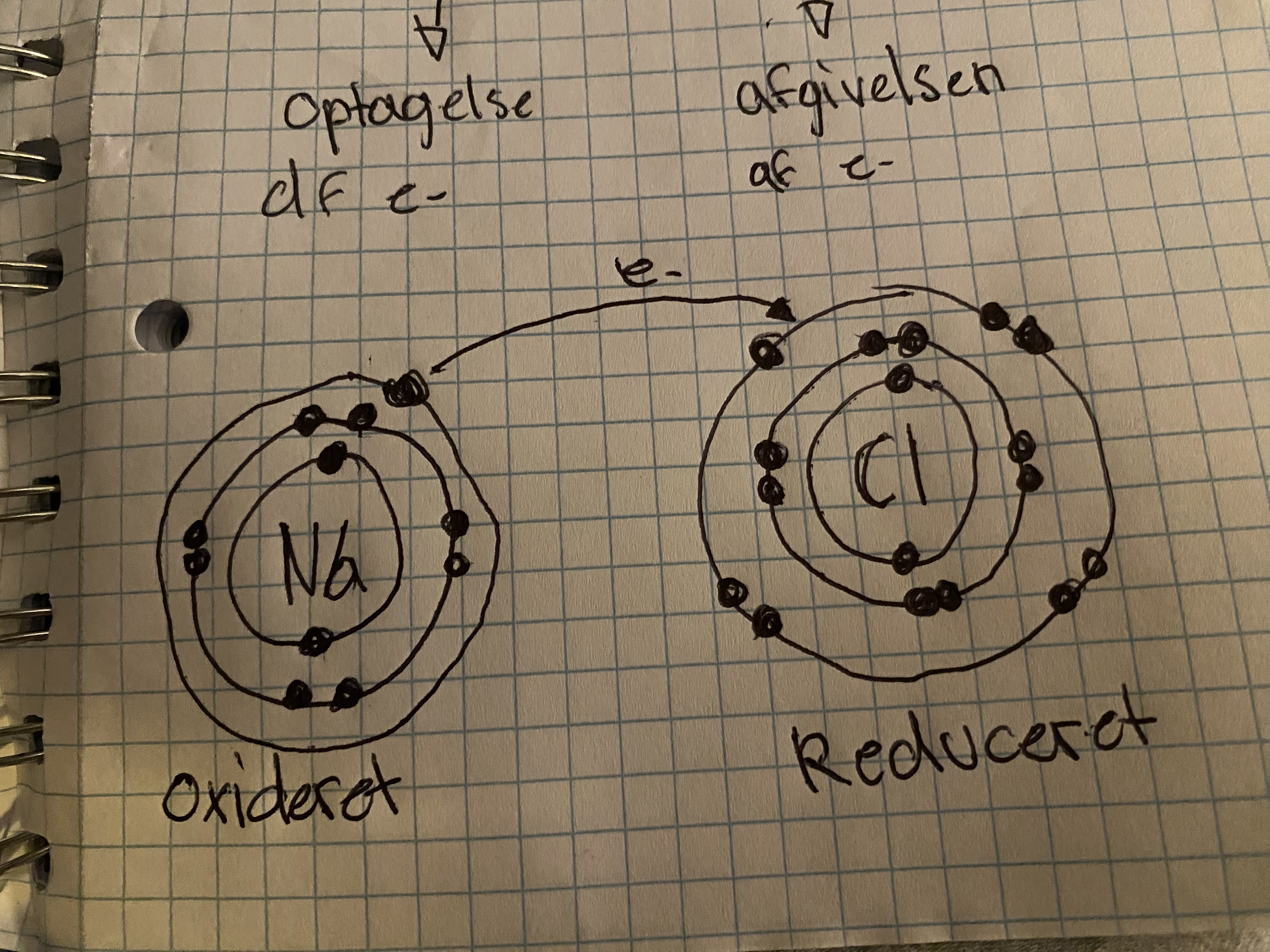
Hvad er en redoxreaktion?
Det er en reaktion hvor noget oxideres( afgiver e-) og reduceres (optager e-).
hvad er værdien for atom massen: u = 1,660540 * 10^-27 kg
Det er atommassen regnet om til kilogram
Hvad er en proton og neutron atom massen.
Neutroner har en lidt større atom masse, men er omkring 1u og det er en proton også
Hvad er istoper
Det er forskellige antal af neutroner i den samme atom
Hvordan finder man atom massen
Masse nummer = antallet af protoner + antallet af neutroner
Hvordan finder man antallet af neutroner
Antallet af neutroner = masse nummer - antallet af protoner
Hvordan afstemmer man kemiske reaktioner.
Det gør man ved at man skal have noget der passer med det der er på den ene side og den anden. Man må ikke ændre det lille tal der fortæller hvor meget der er af den.
Hvad for nogle stoffer bliver kovalente bindinger lavet af.
Ikke metaller og ikke metaller
Når det er ikke metal og metal der laver en binding, hvad er det så?
Så er er det en ionforbindelse der bliver lavet.
Metal og Metal, hvad for en binding bliver det til
En metalbinding
Hvordan ved man i en ionfobindelse, hvad for et stof der kommer til at tage elektroner.
Det gør man ved at kigge på antallet af e- i yderste skal
Hvad er de forskellige energi niveauers navne
Principal quantom
Hvordan for et atom energi til at komme til et højere energi niveau
Varme, kolination( ting går mod hinanden) lys

Hvorfor kan e- ikke være ved høje energi niveauer
e- bliver for ustabil ( husk e- skal være der hvor der er plads til den) e- vil prøve at hoppe tilbage ved at udsende energi.
Hvad har energi niveauerne med fotonernes energi
Når e- springer tilbage. Vil fotoner have energien på energi niveauet mellem de to skaller den hoppede fra ( foton præcis energi der svarer til forskellen af de to energi niveauerk)
Hvorfor er fotonens energi proportionel
Forones energi er afhængig af frekvens og bølgelængde, jo mere lys / energi større frekvens man kortere bølge længde.

Hvad gør folk for at finde ud af hvad for en gas der er u atmosfæren
Man varmer den op og ser hvad for nogle fotoner / bølger der kommer. Den har en farve pga. frekvensen
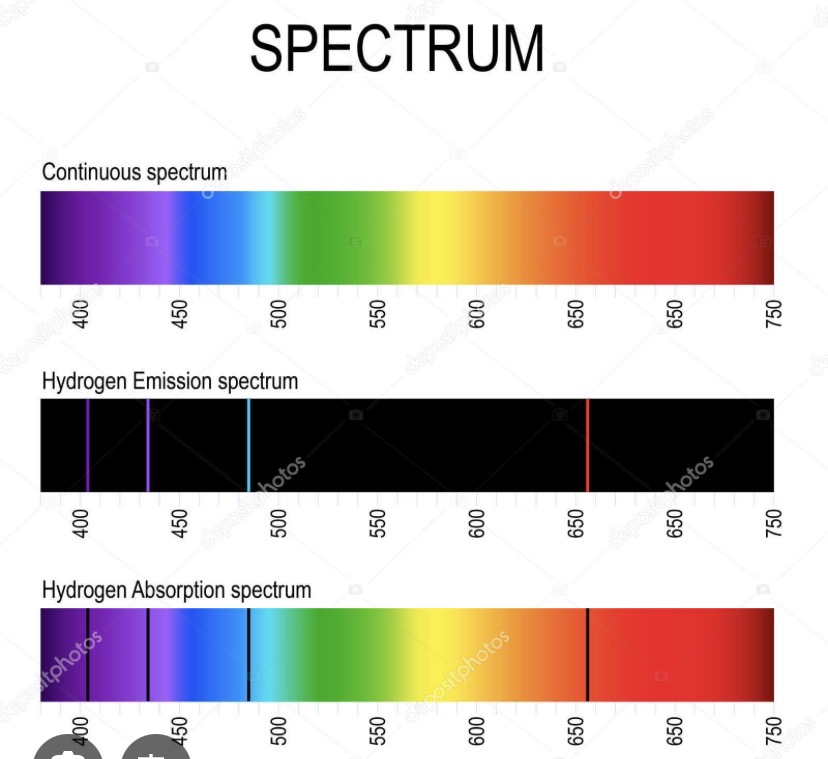
Atomis spektrum
Viser de farver der er unikt for hvert element(hver element vil have sit eget energi niveau)
Absorstion spektrum? Hvorfor bruger man den! Hvad med Emission linjer
Linjerne er sorte. Man bruger den ved køligt atmosfærisk luft. Solen er meget varm og giver hvidt lys. Det ydre lag er koldt, derfor vil atomerne absorbere fotoner fra solens kerne. De fotoner der bliver absorberet danner sorte linjer ved absorsition spektrum
Emission linjer
Glødende varme gasser udsender linjer af lys
Hvad er Khan Lewis diagram
Tegner valens e- op som prikker
Hvordan finder man valens e-
Grupper viser valens e-. Når man kommer til gruppe 13, så skal man minus 13 - 10 =3, så man får tre valens e-
Hvad er orbitaler?
Områder med størst sandsynlighed, for at finde e-. Hvis e- for meget energi, så kan de hoppe videre til næste skal, hvor den kan befinde sig mere k orbitaler der.
Hvad sker der når man giver e- lidt energi?
e- hopper til nyt energi niveau kaldes (exciteret tilstand)

Forklar hvad mander og hvordan kan man bruge det
Konfigurering:
Hvordan p, e og n er sat op og fordelt

Forklar

Hvorfor vil der være H: 1s^1 og disse
Det er så mange e- der kan blive udfyldt j hver skal
Hvad er de fire subshells
S, p, d og f, s er tættest på kernen

Forklar billedet
Det er subshells med deres specifikke orbitaler. Firkanterne er orbitaler mens pilen op og ned viser antallet af e-