H1: scheiden en reageren
1/24
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
25 Terms
chemische reacties
er treedt een energie-effect op.
energiediagram
geeft het energie-effect en de activeringsenergie van elk proces weer.
energie-effect
endotherm en exotherm
endotherm
er is energie nodig om de reactie gaande te houden.
exotherm
er komt bij de reactie energie vrij.
mengsel
heeft een smelttraject en een kooktraject. Verschillende varianten: oplossing, suspensie en emulsie.
emulsie
als dit ontmengt is het een twee-lagen systeem. Hierbij kan een emulgator helpen.
emulgator
voorkomt het ontmengen van de emulsie. Heeft een hydrofiele kop en een hydrofobe staart.
reactiesnelheid
hoeveelheid stof die per seconde en per liter reactiemiddel onstaat of verdwijnt.
verdelingsgraad van een stof
hoe fijner de stof verdeelt is, hoe sneller de reactie verloopt.
soort stof
de snelheid van een reactie ligt aan de soort stof waarmee gewerkt wordt.
temperatuur
Hoe hoger de temperatuur, hoe sneller de reactie verloopt.
concentratie van de reagerende stoffen
Hoe meer stof zich in een bepaald volume bevindt, hoe groter de kans is dat er deeltjes gaan botsen.
katalysator
dit kan nooit verbruikt worden en komt in de vorm van een enzym.
scheidingsmethoden
filtreren, bezinken (centrifugeren), indampen, destillatie, extraheren, adsorberen en chromatografie.
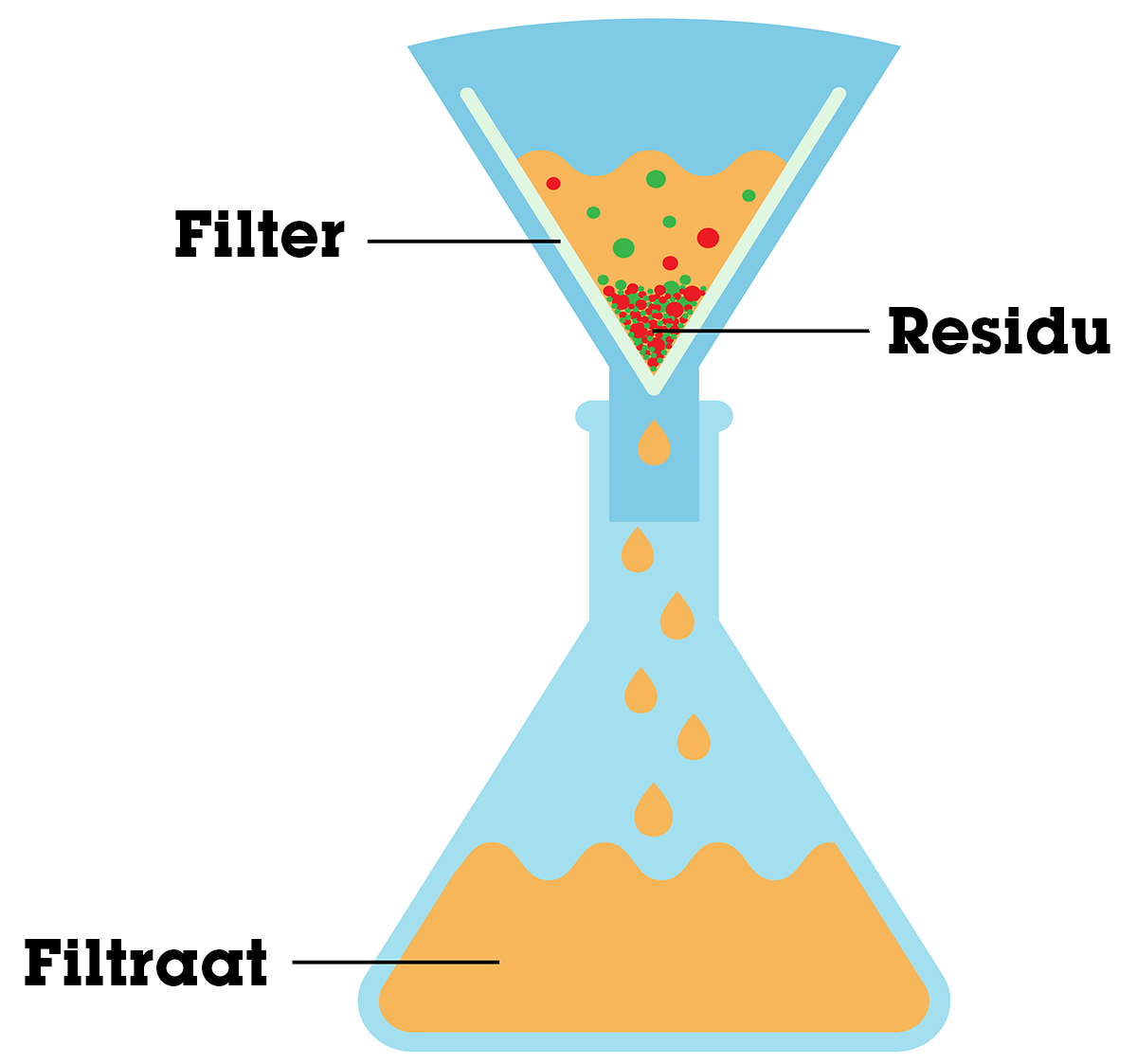
filtreren
verschil in deeltjesgrootte, hierbij heb je het filtraat en de residu.
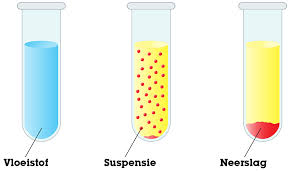
bezinken
verschil in dichtheid, na een bepaalde tijd zal er bijvoorbeeld een twee-lagen systeem ontstaan. Dit proces kan versneld worden door te centrifugeren.
indampen
verschil in kookpunt, een vloeistof met een lager kookpunt zal eerder in een gas veranderen.
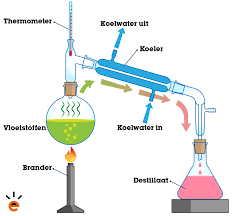
destillatie
verschil in kookpunt, het proces gaat zo: een mengsel wordt verhit, waardoor de gassen naar boven gaan, deze worden opgevangen en gekoeld en verandert dus weer in een vloeistof.
extraheren
verschil in oplosbaarheid, door een middel te gebruiken zal er 1 stof wel oplossen maar de ander niet.
adsorberen
verschil in adsorptievermogen, de opgeloste kleur-, geur- en smaakstoffen hechten zich aan het oppervlakte.
chromatografie
verschil in aanhechtingsvermogen en oplosbaarheid, hiervoor word een chromatogram gebruikt. Je kan hiermee uitzoeken uit hoeveel stoffen een mengsel bestaat.
zuivere stof
bestaat uit 1 soort bouwsteen. Heeft een smeltpunt en een kookpunt, ook is het een element.
element
is op microniveau 1 soort atoom.
verbinding
de bouwstenen bestaan uit 2 of meer soorten atomen.