Thermochemie
1/23
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
24 Terms
Wat is de inwendige energie
de totale energie dat aanwezig is in een stof
hoe kan inwendige energie aanwezig zijn in stoffen
atomair niveau | intramoleculair nvieau | intermoleculair niveau |
|
|
|
defenitie: toetstandsfunctie / grootheid
het verschil in inwendige energie tussen de reactieproducten en reagentia is meetbaar tijdens het proces niet. Alleen de begin en eind waardes.
wat beschrijft de systeem
Plaats waar de reactie plaatsvindt
wat beschrijft de omgeving
alles buiten systeem
de wet van behoud van energie
energie kan niet geschapen of vernietigd worden, wel van de ene vorm in de andere worden omgezet.
welke soorten systemen bestaan er
open | gesloten | geïsoleerd |
✅ Materie uitwisselen ✅ Energie uitwisselen | ✅ materie uitwisselen 🟥energie uitwisselen Energie is al op voorhand aanwezig door inwendige energie | 🟥materie uitwisselen 🟥energie uitwisselen |
wat is exotherm
Exotherm |
inwendige energie reagentia hoger dan producten |
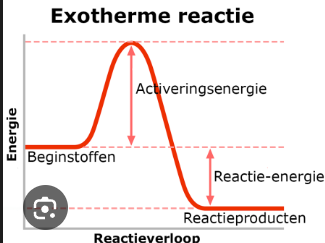 |
wat is endotherm
Endotherm |
Inwendige energie reagentia lager producten |
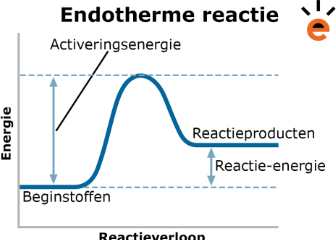 |
wat is enthalpie
een maat voor de totale energie van een systeem,
formule enthalpie vinden
H = w + q
Energie afgeven is
< 0
energie opnemen
> 0
wat voor grootheid is enthalpie
toetstandsgrootheid
wat zijn de facotren dat ke la gebruiken voor de absolute enthalpie inhoud
druk
temperatuur
agregatietoestand
welke vormen enthalpieveranderingen bestaan er
verbrandingsenthalpie
bindingenthalpie
neutralisatie enthalpie
vormingsenthalpie
sublimatieenthalpie
dissociatieenthalpie
wat is de wet van hess
Als een reactie kan worden geschreven als de som van 2 of meerdere deelreacties, dan is de reactie-enthalpie gelijk aan de som van de reactie-enthalpie van de deelreacties.
wat is entropie
streven naar een hoge wanorde
wat is het symbool van entropie
S
wat het het symbool van enthalpie
H
hoe bepaal je dat entropie positief of negatief is
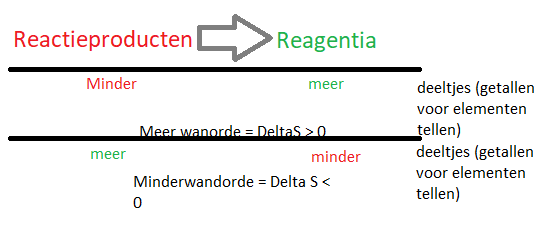
geef de gibbs kader pls :3
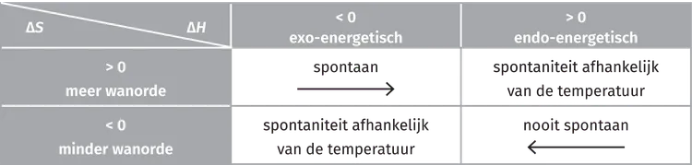
wat is de gipps formule
Enthalpieverandering gecorrigeerd voor de energie die het systeem gebruikt om wanorde te creëren.
DeltaG = DeltaH-T*deltaS
waar streven systemen naar
Systemen drijven naar minemale gis energie = vrije enerige