Thermo : Chapitre 5 - Grandeurs standard, molaire, de réaction Cartes | Quizlet
1/16
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No study sessions yet.
17 Terms
Pour une transformation élémentaire d'un système ouvert, formule de la grandeur X (T,P,ni)
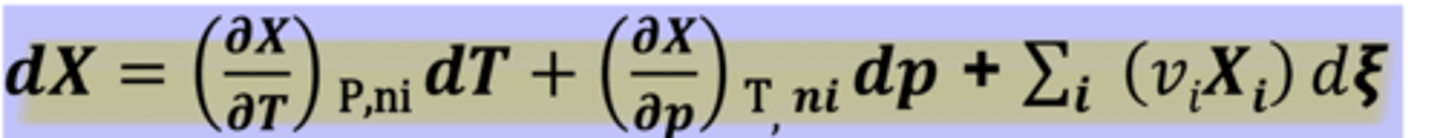
Opérateur de Lewis
- grandeur extensive molaire
- grandeur instantanée (pour tout état intermédiaire)
- Définie pour toute équation de transformation étudiée
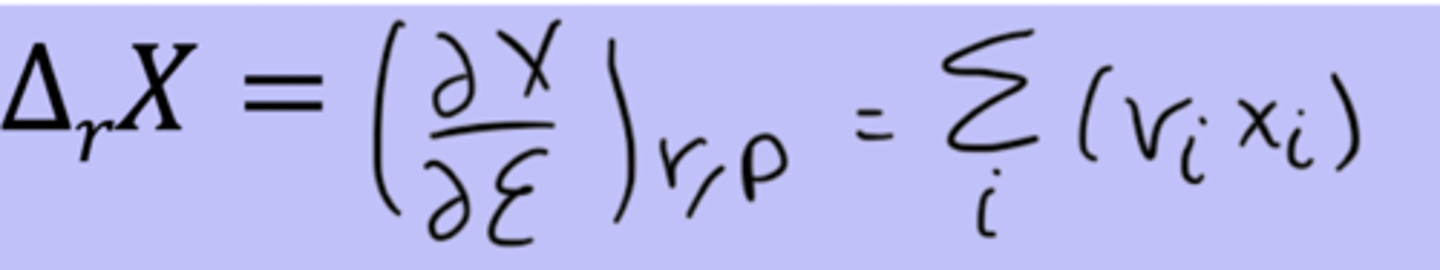
Définition état standard
Par convention, l'état standard d'un corps est l'état de ce corps quand il est pur sous une pression p° = 1bar et à une température T.
Il dépend aussi de l'état physique du corps
Définition état standard de référence
État standard de référence d'un élément est l'état standard de son état le plus stable thermodynamiquement parlant à la température considérérée
Formule d'une grandeur molaire standard X
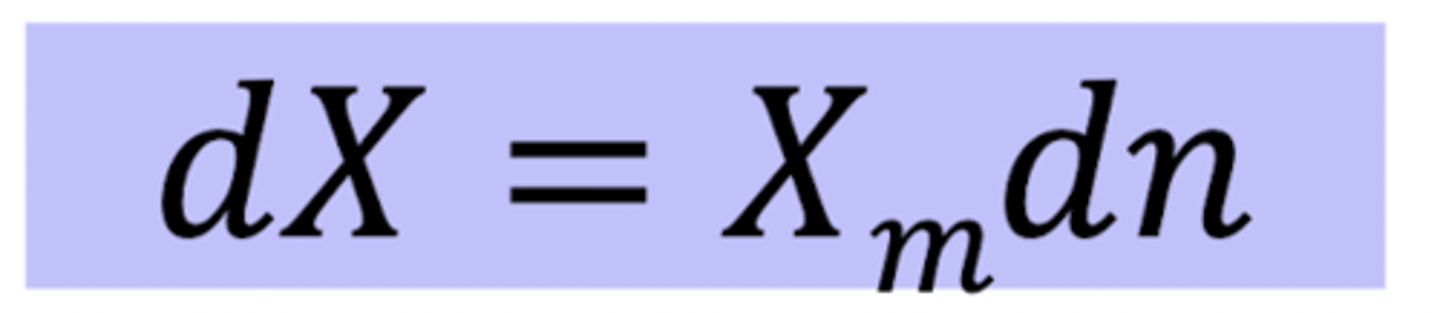
Grandeur de réaction
- grandeur extensive
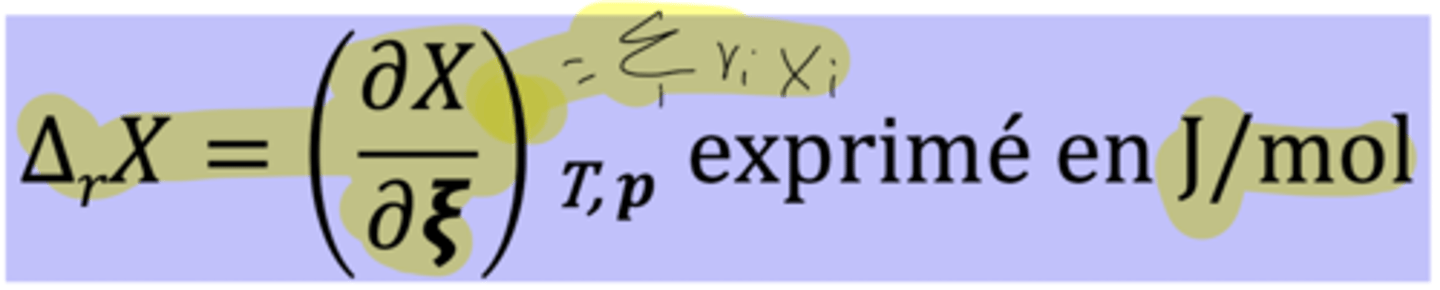
Loi de Hess
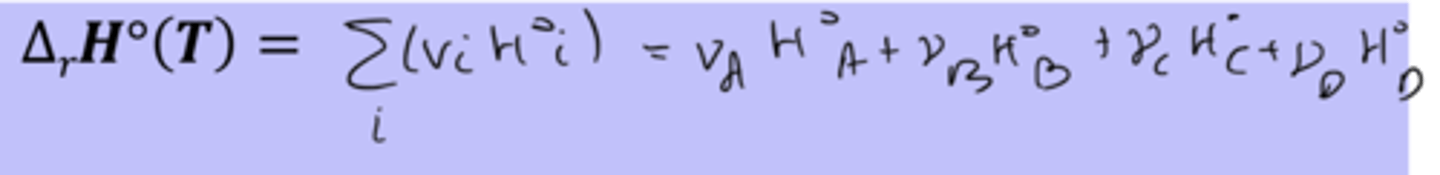
Loi de Kirchhoff
∆H2 - ∆H1 = ζ ∆CpdT
(Pas de changement d'état)
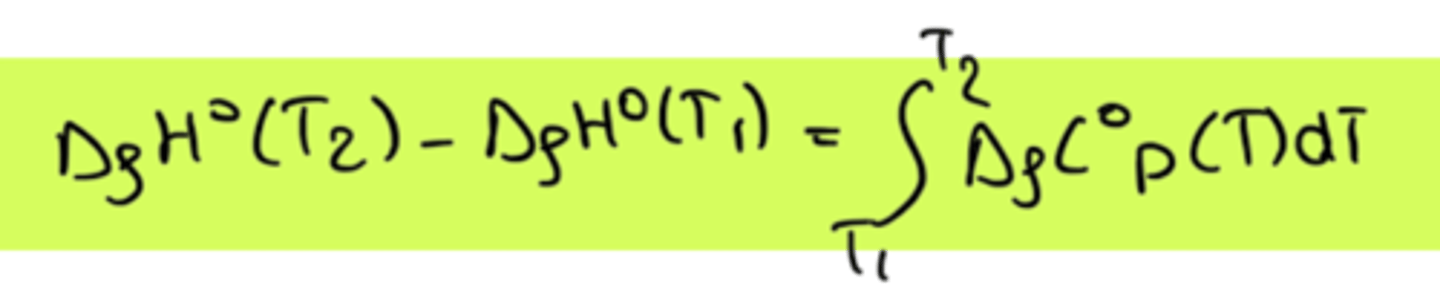
Loi de kirchhoff pour l'énergie interne
(Attention, ce n'est plus Cp mais Cv)
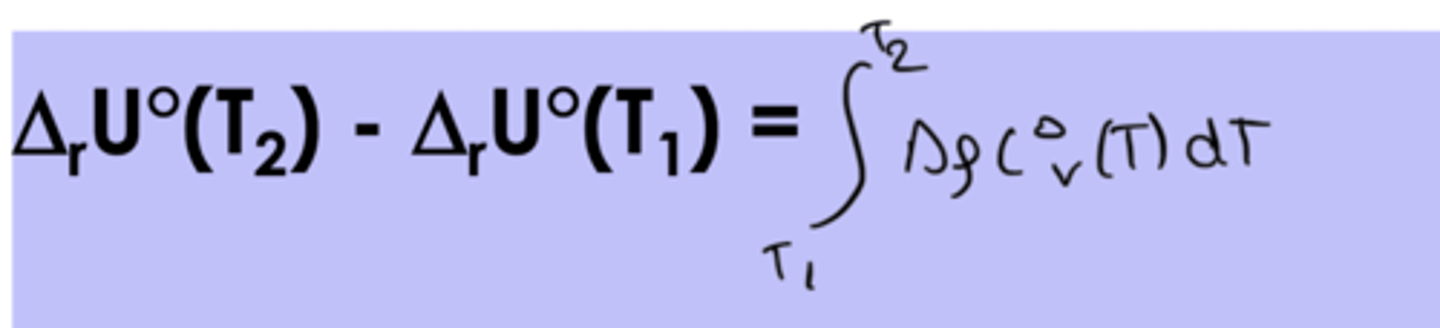
défintion formation standard d'un corps
Formation d'un corps composé à partir des éléments pris dans leur état standard. Le corps composé a un coef stochiométrique de +1
Def enthalpie standard de formation
Enthalpie échangée lors de la formation d'un corps composé à partir de ses éléments constituifs dans leur état standard de référence à la température considérée, le coefficient stoéchiométrique du corps est de +1
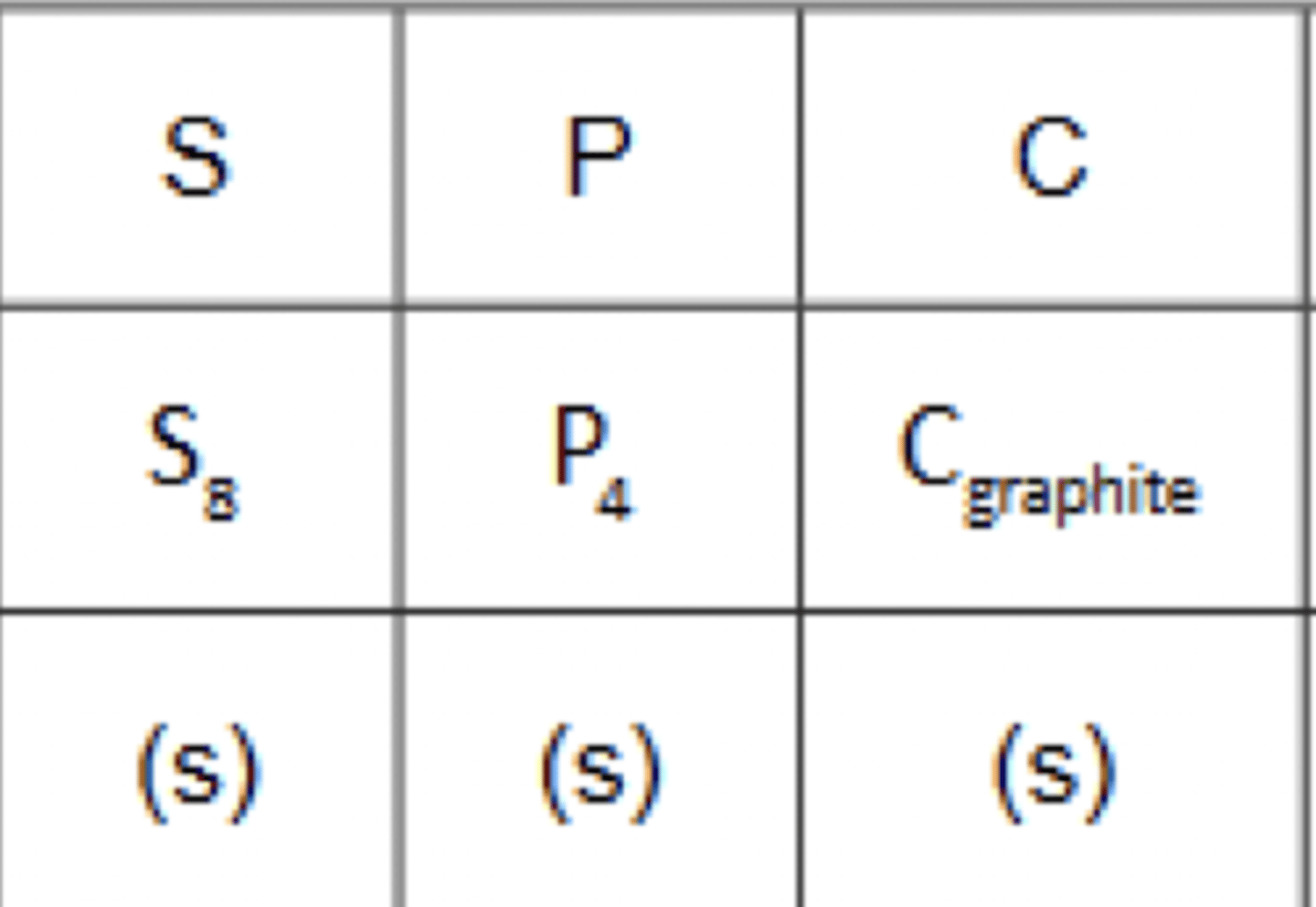
3 corps simple particulier
Sulfate, le phosphate et le carbone
Enthalpie standard de dissociation de liaison
- positive
= enthalpie associé à réaction de dissociation de liaison entre A et B, où ces derniers peuvent être des atomes ou groupes d'atomes en phase gaz.
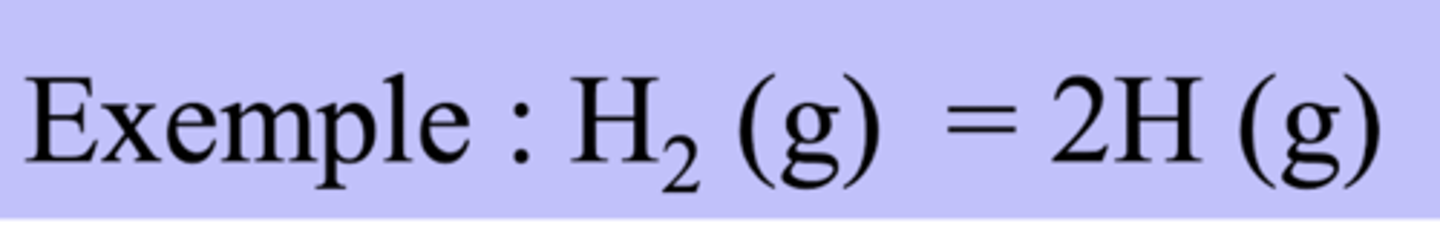
Enthalpie standard d'ionisation
- positive car il faut arracher un électron
= enthalpie associé la réaction d'ionisation d'un atome gazeux en ion positif gazeux
Enthalpie standard d'attachement électronique
- positive
= enthalpie associée à la réaction d'attachement d'un électron à un atome gazeux formant un ion gazeux négatif
- notion d'affinité électronique AE : opposé à l'enthalpie d'attachement électronique. AE est d'autant plus grande que l'anion gazeux est stable
Enthalpie standard de combustion
= enthalpie associée à l'oxydation complète d'une substance avec un coefficient stoechiométrique de -1
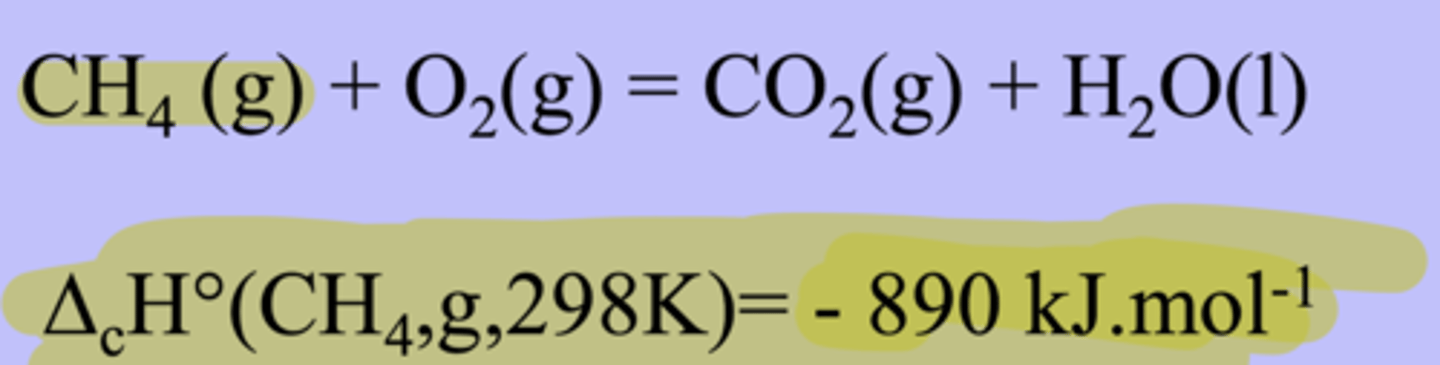
Enthalpie standard de changement d'état
= enthalpie associée au un changement d'état du corps pur A de la phase 1 à la phase 2 à la température de changement d'état sous pression standard P°