Bio Kap. 4 (Zelluläre Basis der Informationsverarbeitung in Nervenzellen)
1/79
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
80 Terms
Was ist die Voraussetzung für Informationsverarbeitung in biologischen Systemen?
Welche physikalische Grundlage nutzt das Nervensystem für Signale?
→ Das Vorhandensein von mindestens zwei stabilen Zuständen (Z1, Z2), zwischen denen ein Übergang (Signal) stattfinden kann.
→ Elektrische Phänomene: definierte Spannungszustände entlang der Zellmembran.
Was sind Ionen? Nenne Beispiele für Kationen und Anionen.
→ Geladene Teilchen:
Kationen: Na⁺, K⁺, Mg²⁺
Anionen: Cl⁻, Säurereste
Was ist eine elektrostatische Wechselwirkung?
→ Anziehung oder Abstoßung zwischen entgegengesetzt bzw. gleich geladenen Teilchen → Grundlage für Molekülbindung.
Wie beeinflusst Ladung die Struktur von Proteinen?
→ Unterschiedliche Ladungsverteilung → Anziehung/Abstoßung → bestimmt räumliche Struktur → Strukturveränderung = Funktionsänderung.
Was bewirken Strukturveränderungen von Proteinen im Nervensystem?
→ Ionenpumpen transportieren Teilchen
→ Enzyme ermöglichen Reaktionen durch Annäherung von Molekülen.
Wie entsteht das Membranpotenzial? Was bedeutet „elektrisch polarisiert“?
→ Durch ungleiche Verteilung geladener Ionen innen und außen → typisches Ruhepotenzial (nicht wirklich absolute Ruhe) in Nervenzellen: –70 mV, aber in tierischen Zellen irgendwo von -40 bis -90 mV.
→ Das Zellinnere ist negativer als das Zelläußere → konstante Spannung über die Membran.
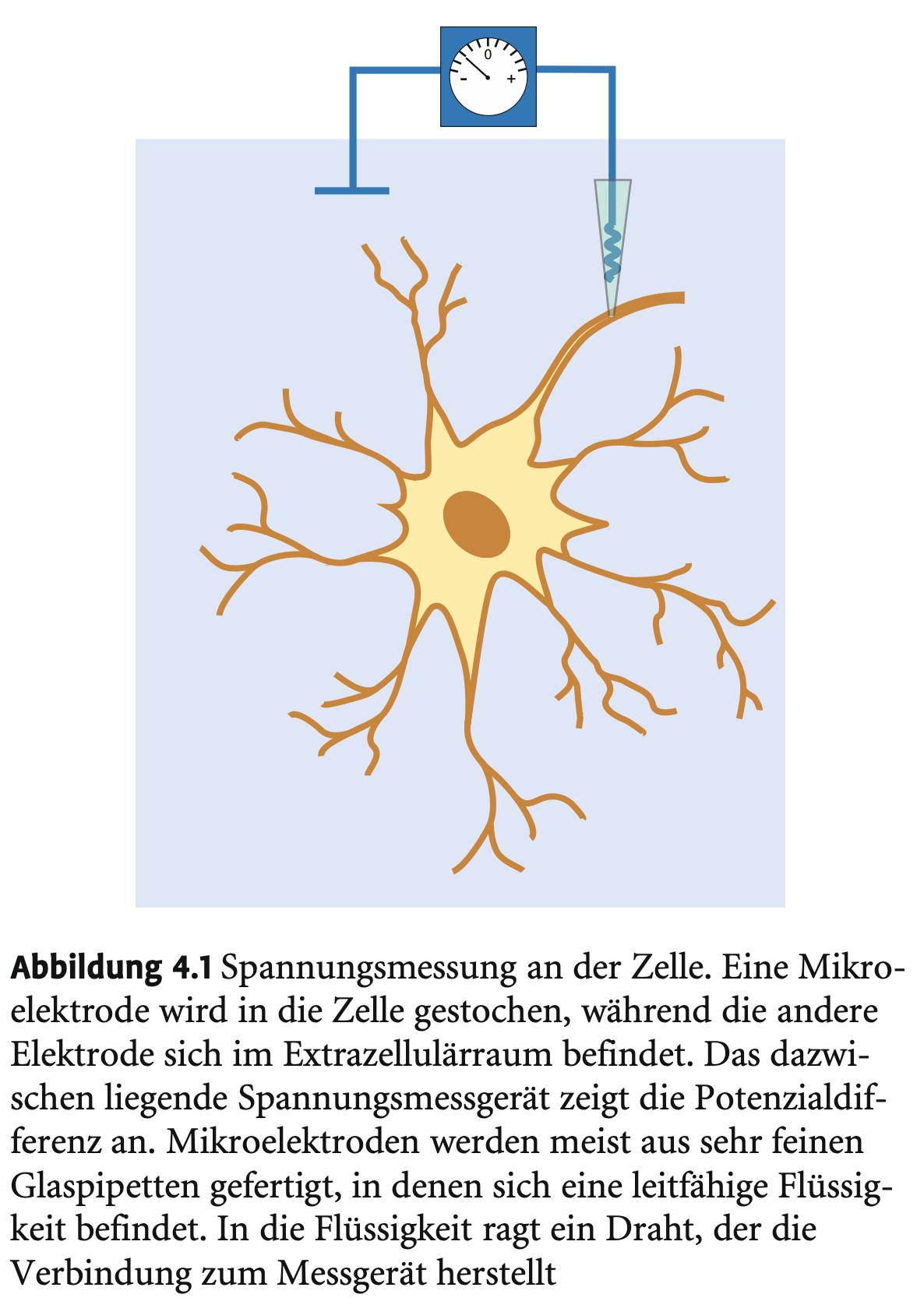
Wie misst man das Membranpotenzial?
→ Mit Mikroelektroden (feine, spitz zulaufende Glaspipetten, gefüllt mit leitfähiger Lösung): eine in der Zelle, eine außen, verbunden mit Spannungsmessgerät.
Warum kommt es nicht zu Ladungsausgleich zwischen innen und außen?
→ Membran ist selektiv permeabel, v.a. durch Ionenkanäle. Die Lipid-Doppelschicht verhindert unkontrollierte Diffusion.

Welche Moleküle können die Membran ungehindert passieren?
→ Kleine, ungeladene, fettlösliche Moleküle wie O₂, CO₂, Ethanol.

Was machen Ionenkanäle? Beschreibe die Ionen.
→ Selektive Passage bestimmter Ionen → sichern die Stabilität des Ruhepotenzials.

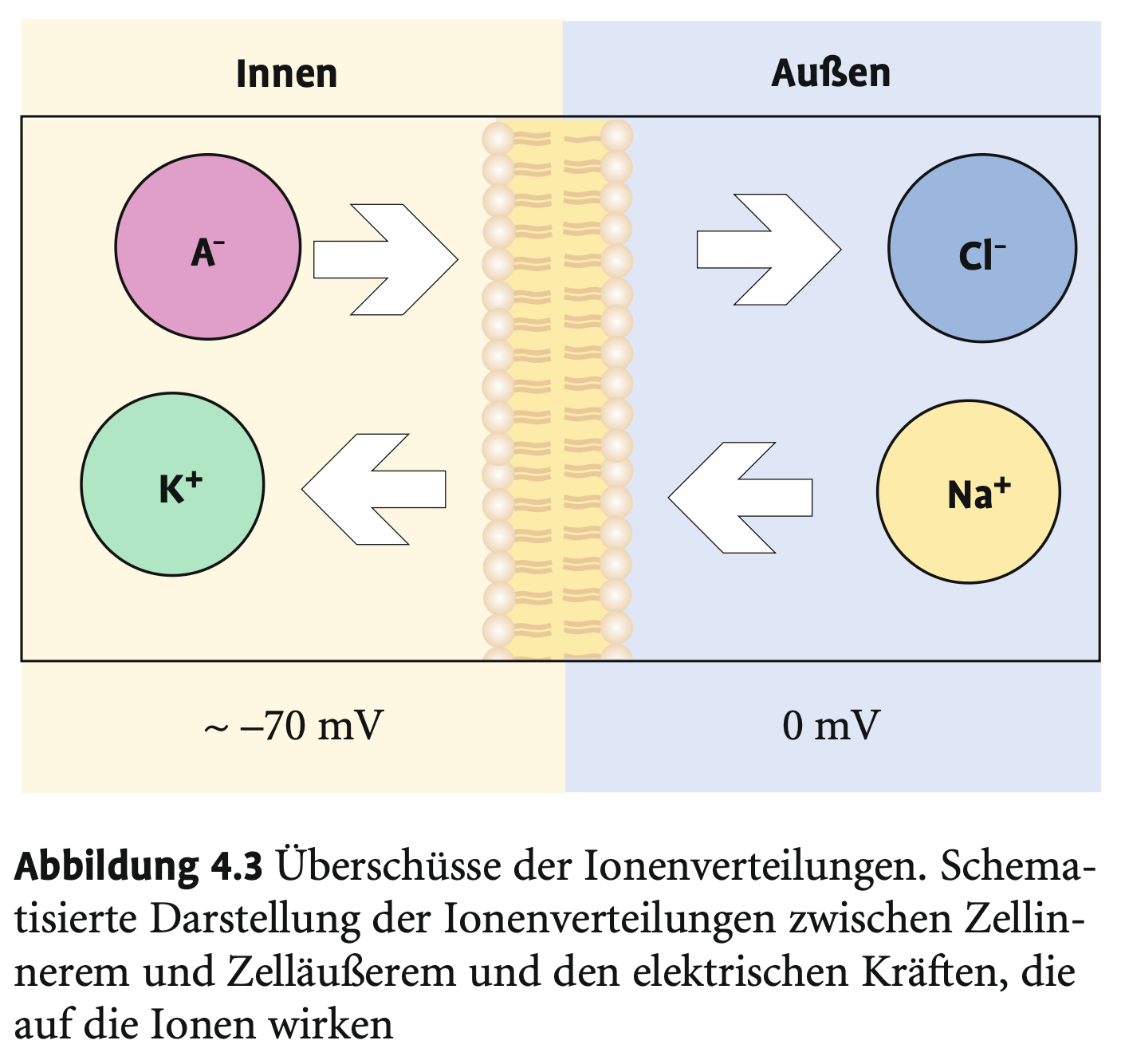
Wie beeinflussen elektrische Kräfte verschiedene Ionen?
→ K⁺ wird durch negatives Zellinnere angezogen → bleibt innen
→ Cl⁻ wird abgestoßen → bleibt außen
→ Na⁺ wird angezogen → will einströmen
→ Proteine können nicht raus → zu groß
Was ist die Brown-Molekularbewegung?
→ Zufällige Teilchenbewegung durch Kollisionen → treibt Diffusion an → keine Ruhe im biologischen „Ruhezustand“
→ Absolute “Ruhe” gelingt nur bei 0K, bzw. -273C.
In Gasen: Teilchen legen weite Wege zwischen Kollisionen zurück.
In Flüssigkeiten: Teilchen sind dichter gepackt, ständig in Bewegung durch Anziehungs-/Abstoßungskräfte.
In Festkörpern: Teilchen schwingen nur um ihre feste Position.
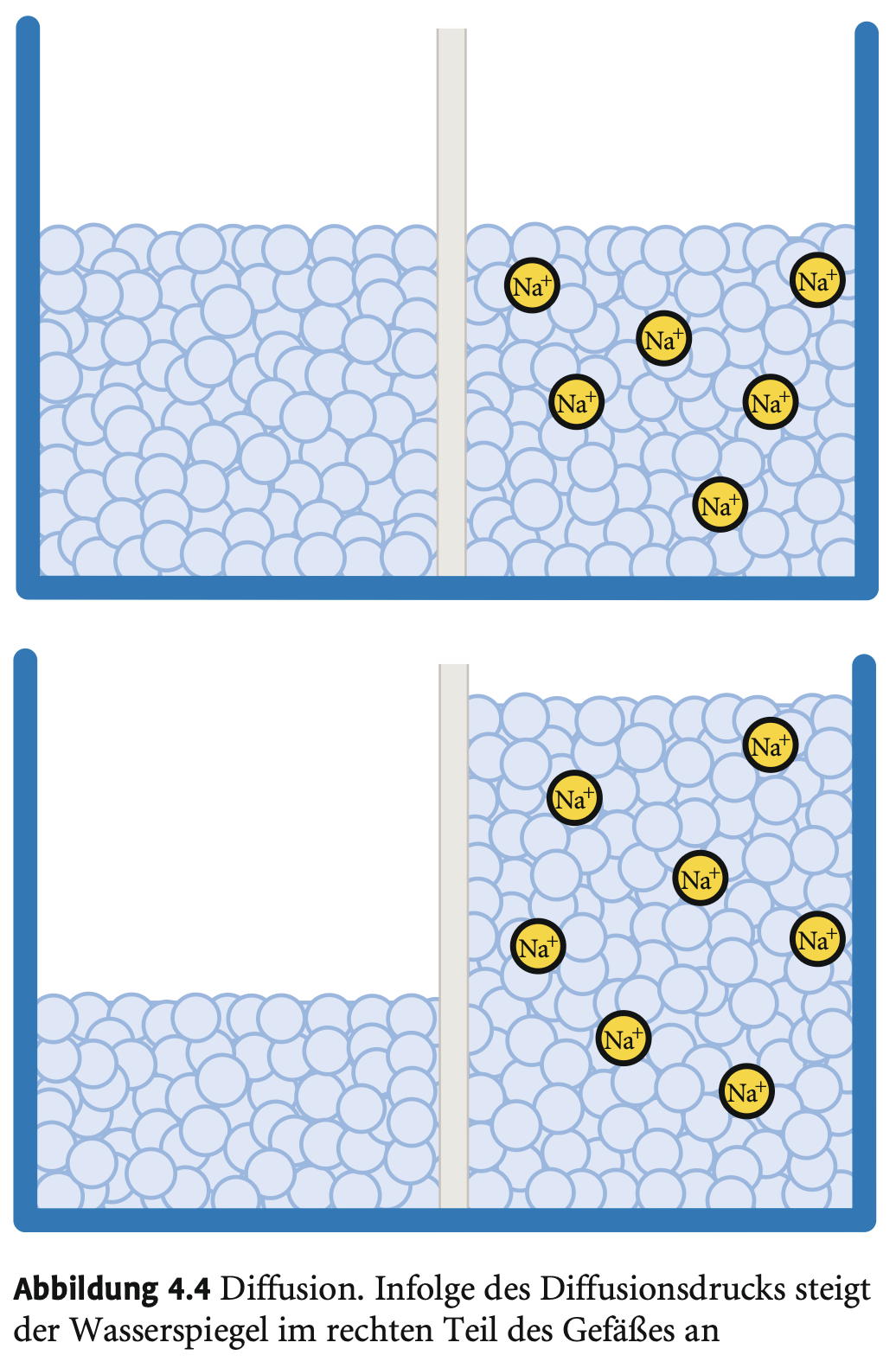
Was ist Diffusion?
→ Teilchenverteilung zur Konzentrationsangleichung durch Molekularbewegung → natürliche Durchmischung.
Was ist osmotischer Druck?
→ Wasser diffundiert durch semipermeable Membran zur Seite mit höherer Ionenkonzentration → Erzeugt hydrostatischen Druck.
Warum ist Osmose für Zellen gefährlich?
→ Hohe Ionenkonzentration innen → Wasser strömt ein → Zelle schwillt an und kann platzen.
Welche zwei Kräfte wirken auf Natriumionen?
→ 1. Elektrische Anziehung durch negatives Zellinnere
→ 2. Diffusionskraft (mehr Na⁺ außen als innen)
→ Beide wirken nach innen
Was verhindert das Eindringen von Na⁺ trotz beider Kräfte, die auf diese wirken?
→ Die geringe Permeabilität der Membran für Na⁺
→ Natrium-Kalium-Pumpe hält Ungleichgewicht aufrecht
Was ist das Gleichgewichtspotenzial (EG)?
→ Das elektrische Potenzial, bei dem keine Nettowanderung einer bestimmten Ionensorte mehr stattfindet.

Was beschreibt die Nernst-Gleichung?
→ Sie berechnet das EG aus:
Konzentrationen innen/außen (c₁/c₂)
Temperatur (T)
Wertigkeit des Ions (z)
Physikalische Konstanten (R, F)

Wie erkennt man elektrochemische Druckverhältnisse?
→ Ist das gemessene Membranpotenzial ≠ EG, besteht Wanderungstendenz für das Ion, bzw. eine elektrochemischer Druck.
→ Ist Membranpotenzial = EG → kein Nettofluss.
Beispiele für Gleichgewichtspotenziale:
K⁺: außen/innen = 1:40 → EG = –98 mV
Na⁺: außen/innen = 12:1 → EG = +67 mV

Welche Ionen sind meist im Gleichgewicht?
→ Kalium (K⁺) und Chlorid (Cl⁻) → ihr EG liegt nahe am Ruhepotenzial der Nervenzelle.
Was ist passiver Transport durch die Zellmembran?
→ Transport ohne Energieverbrauch, angetrieben durch Konzentrationsgradienten und elektrische Ladungsunterschiede.
Welche Moleküle passieren die Membran ohne Transportprotein?
→ Kleine, ungeladene Moleküle wie O₂, CO₂, Ethanol.
Welche Rolle spielen Carriermoleküle im Nervensystem?
→ Geringe Bedeutung; sie binden Ionen, verändern ihre Konformation und geben sie auf der anderen Seite frei.
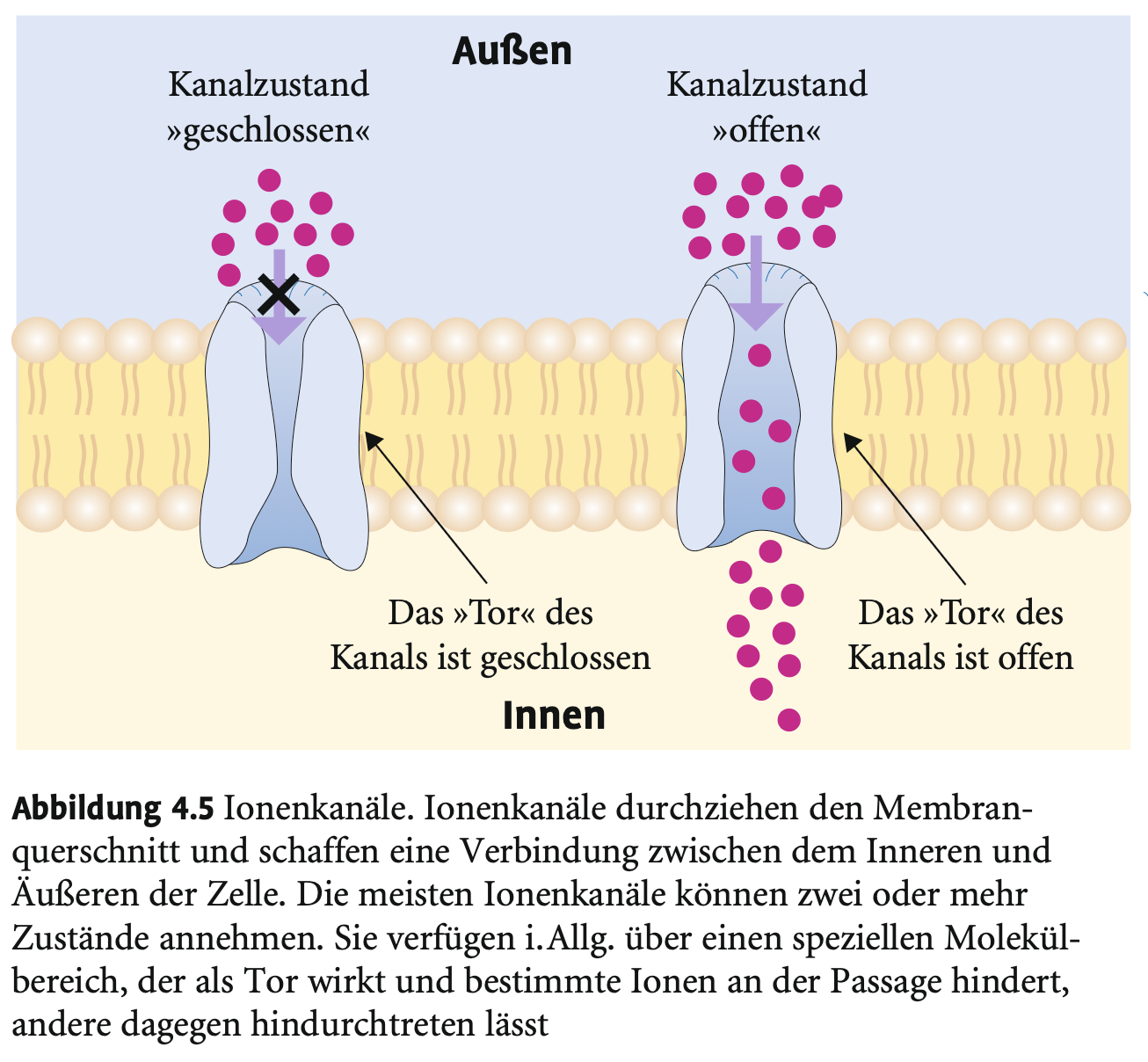
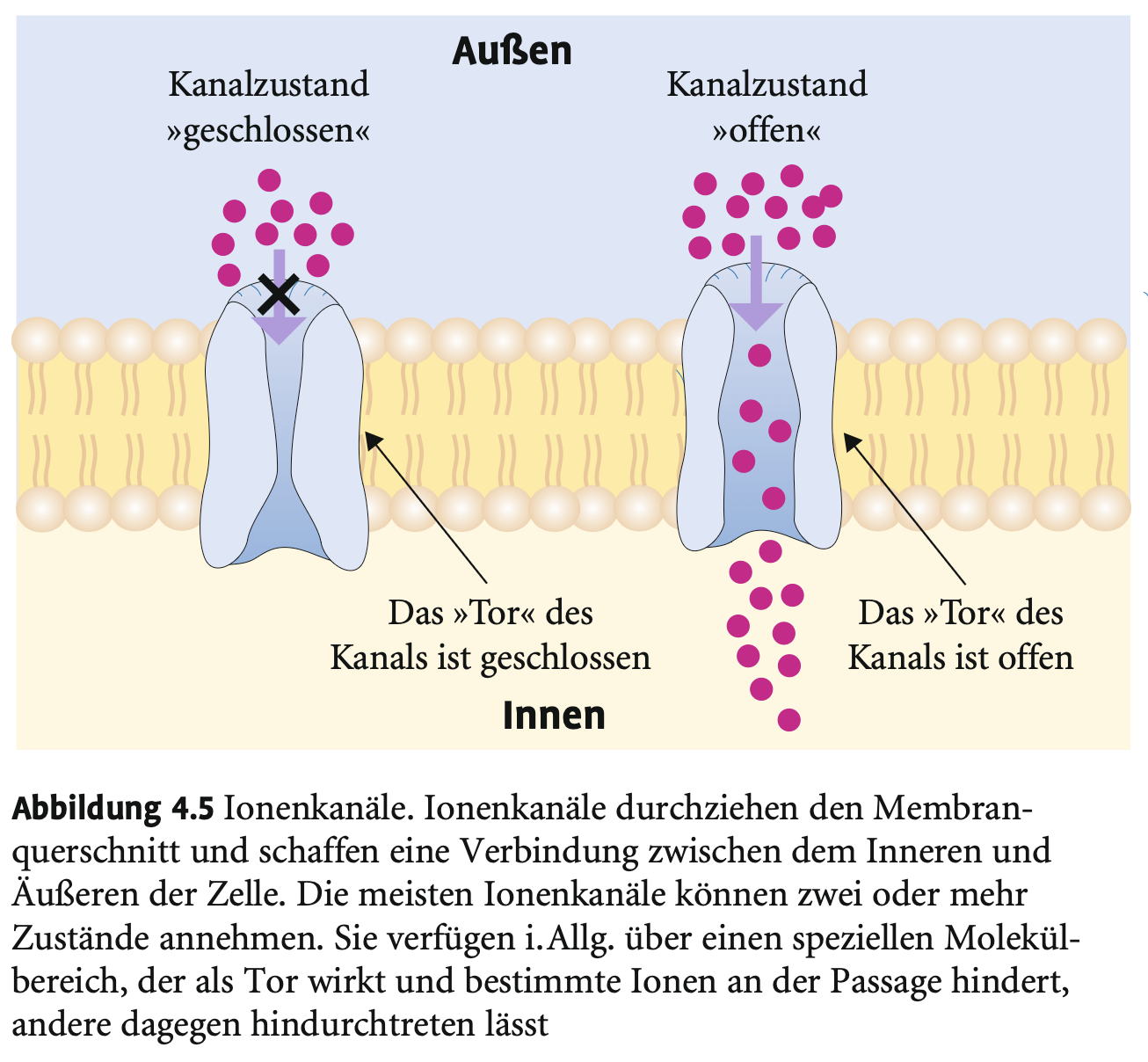
Was sind Ionenkanäle und wie sind sie aufgebaut?
→ Membranproteine aus 4–6 Untereinheiten, die eine Pore zwischen Zellinnerem und -äußerem bilden.
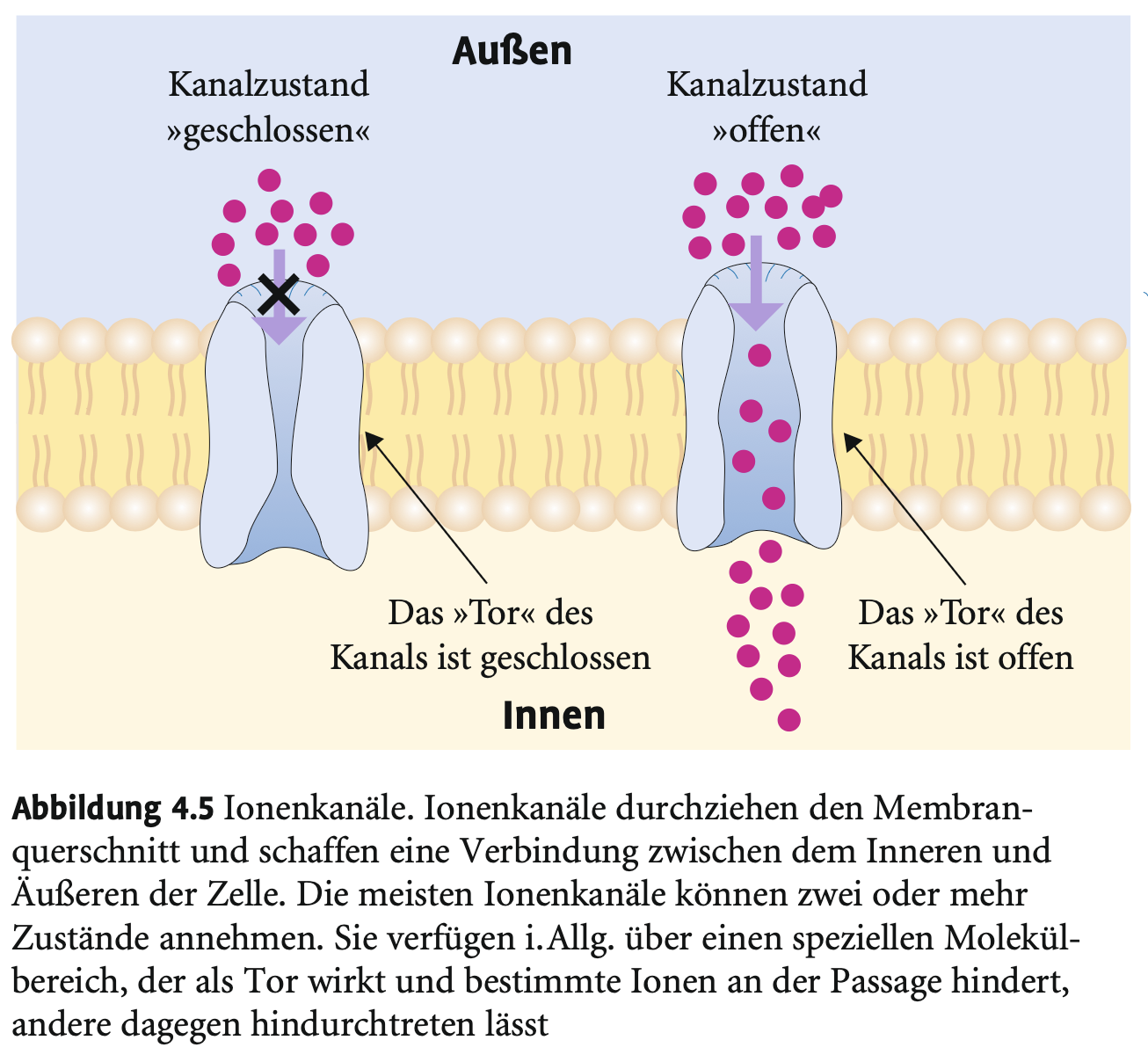
Was ist die Funktion von Ionenkanälen in Nervenzellen?
→ Schneller, selektiver Ionentransport (z. B. K⁺, Na⁺, Ca²⁺); zentral für neuronale Erregbarkeit.
Wie verändert sich die Zahl an Ionenkanälen?
→ Durch Proteinsynthese erhöhbar oder durch Abbau reduzierbar – wichtig für Lernen, Gedächtnis, Sucht.
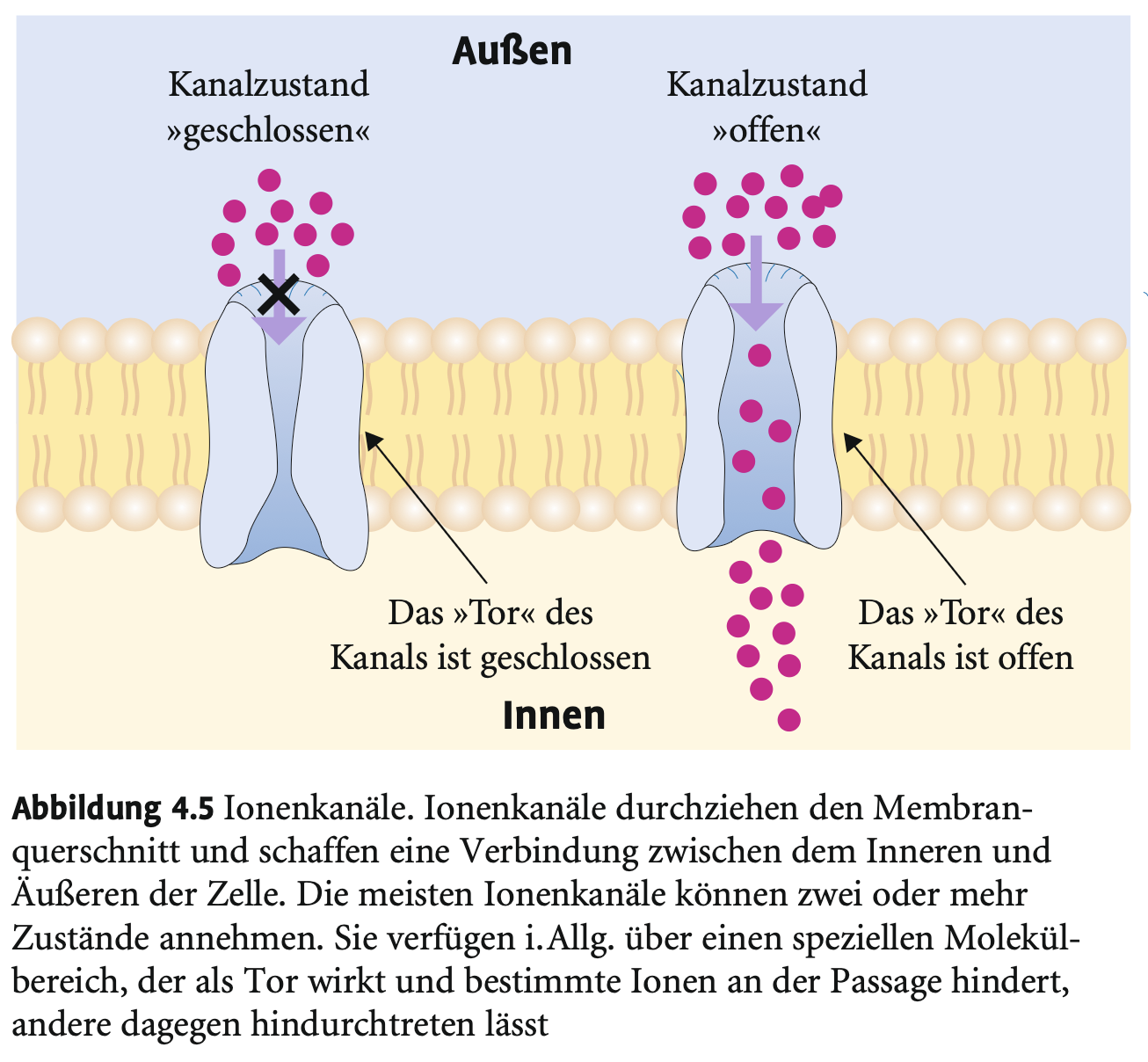
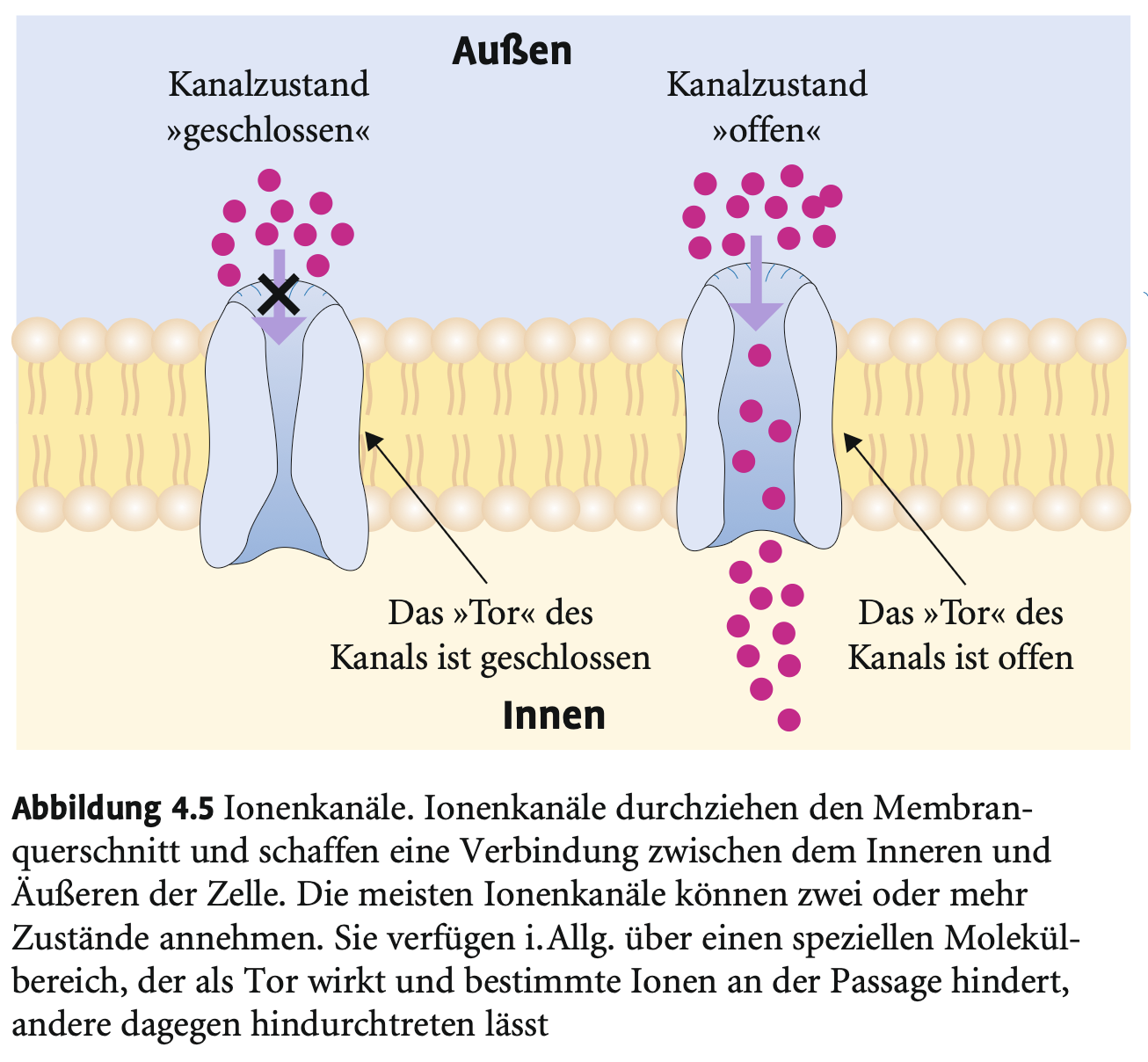
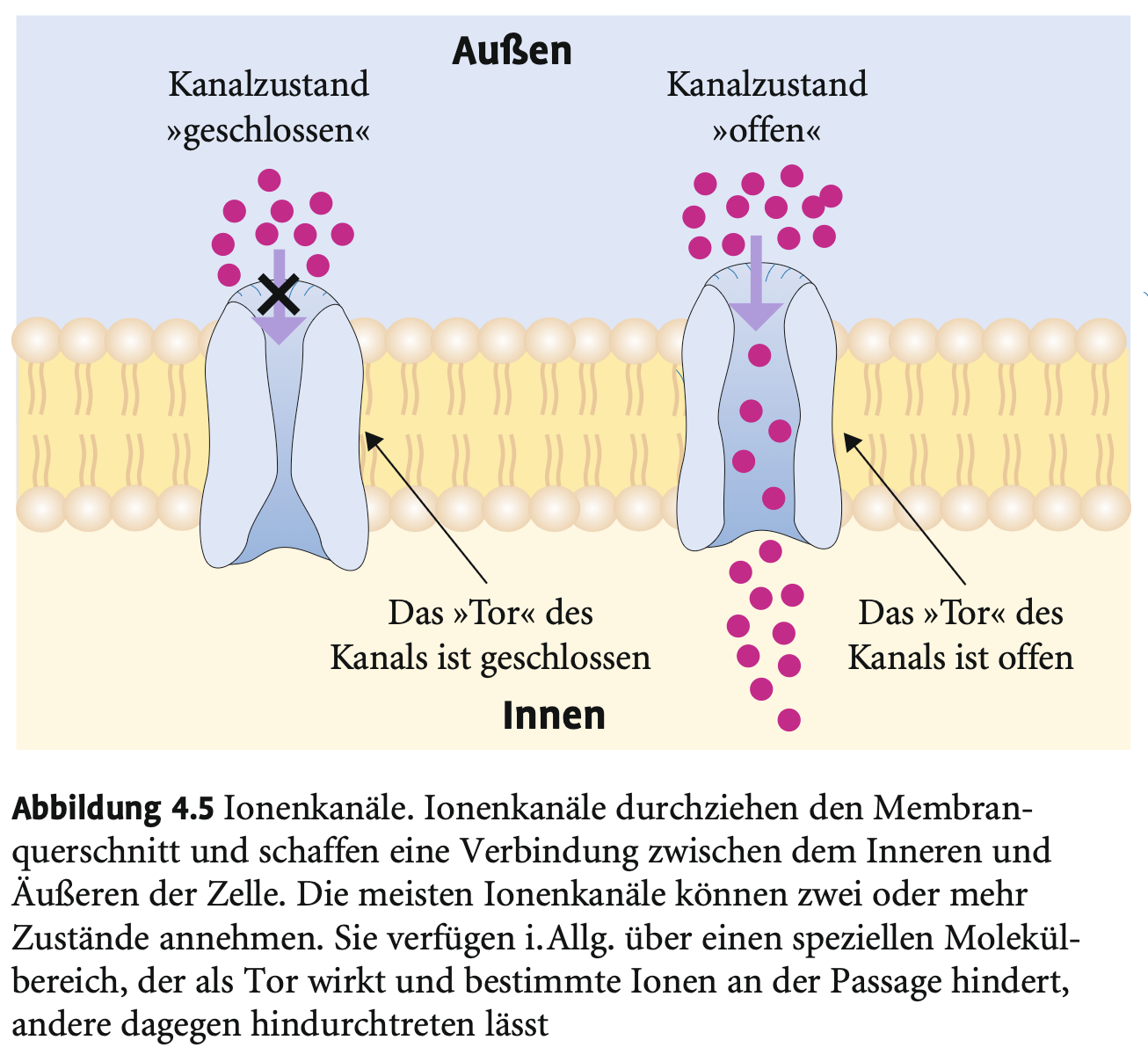
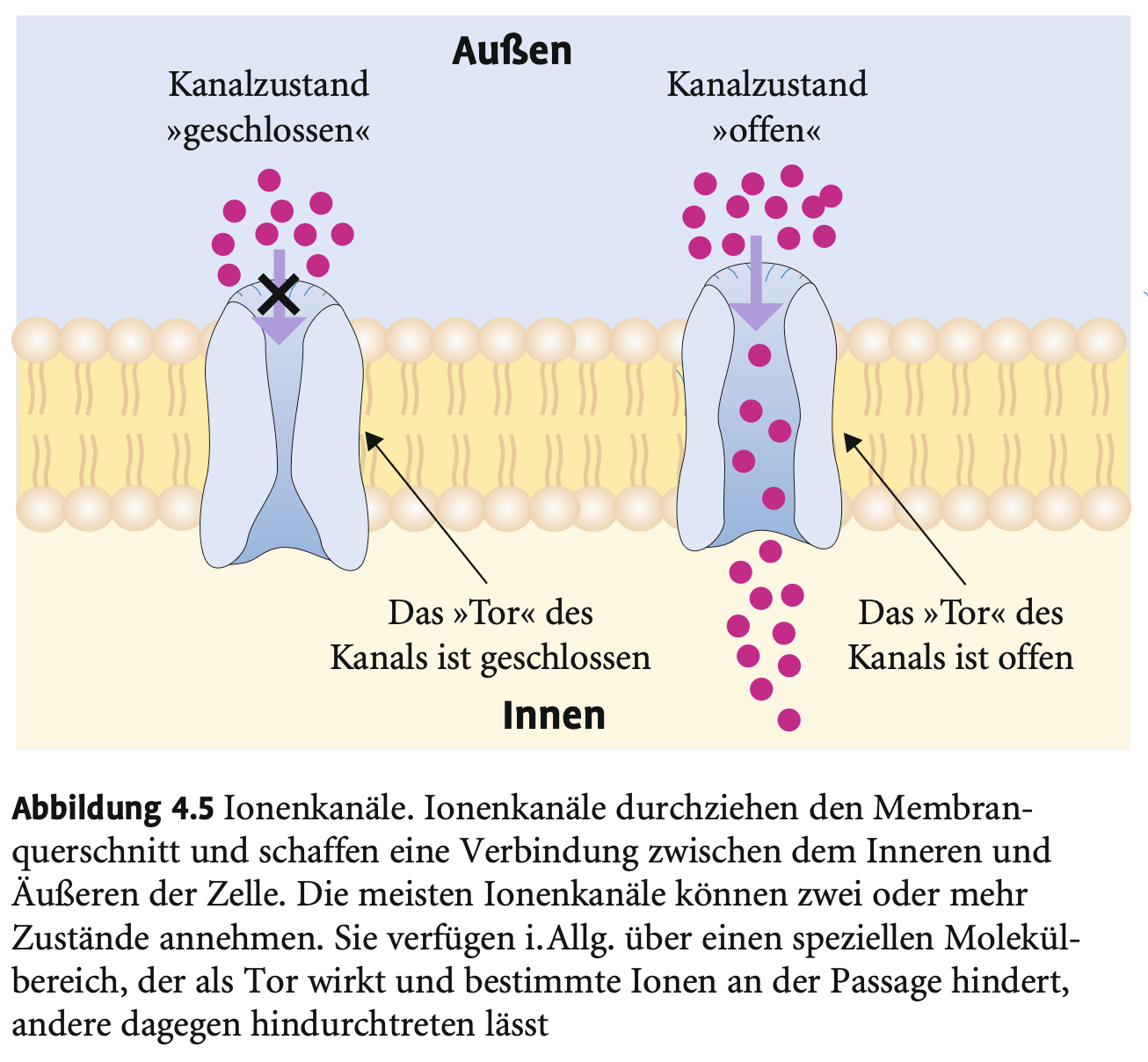
Welche Zustände können Ionenkanäle einnehmen?
→ Offen oder geschlossen; abhängig von Aktivierbarkeit, Spannung oder chemischen Reizen (z. B. Neurotransmitter).
Wie viele Ionenkanaltypen gibt es?
→ Über 100 verschiedene; in einer Membranregion einer Nervenzelle über 10 aktiv gleichzeitig.
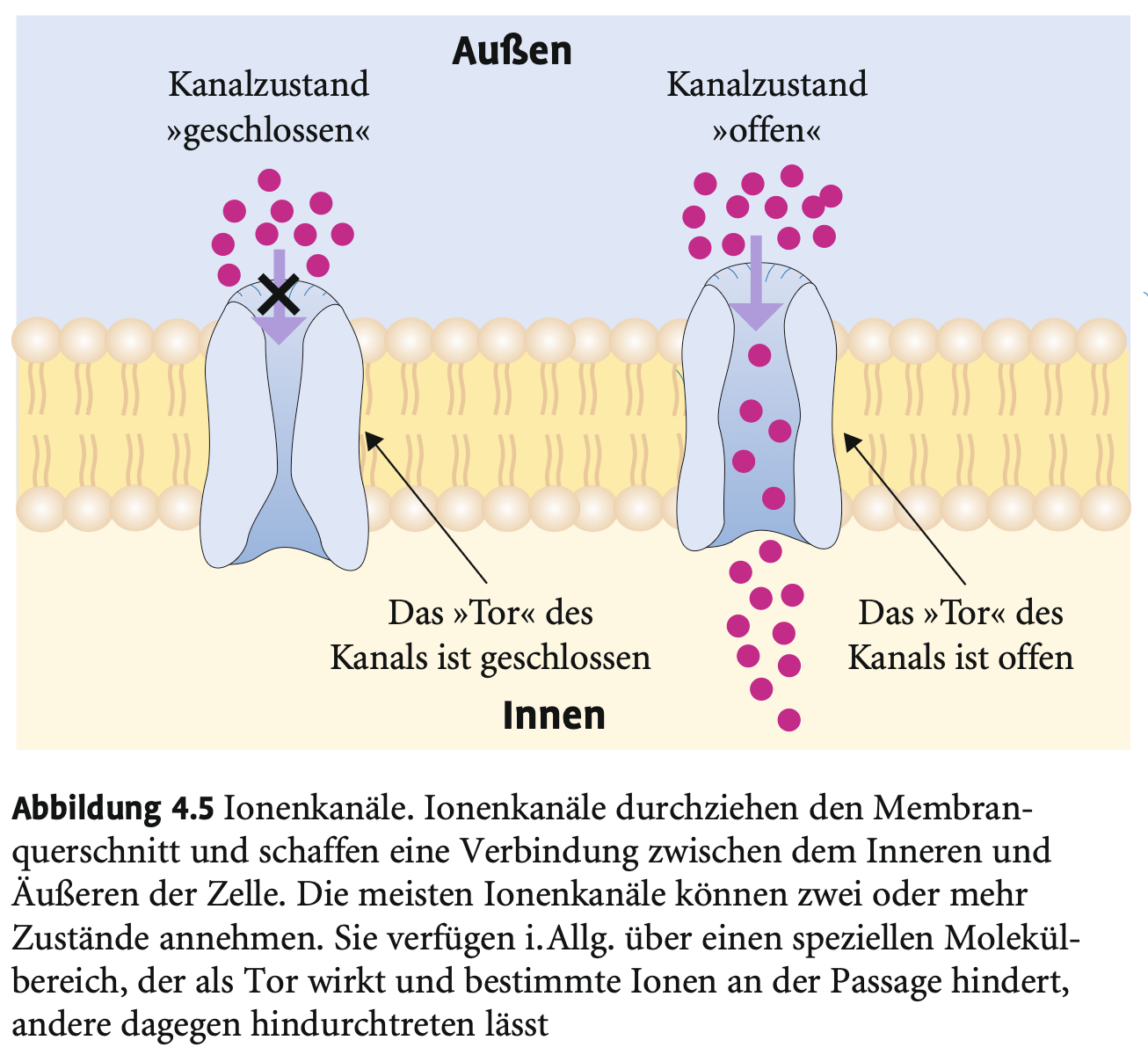
Wie schnell ist der Transport durch Ionenkanäle?
→ Bis zu 10 Millionen Ionen pro Sekunde – 1.000× schneller als Carrier.
Was bestimmt die Selektivität eines Ionenkanals?
→ Ionenladung, Kanalpolarität (z. B. Kaliumkanäle sind negativ polarisiert) und Aminosäurefilter im Kanalinneren.
Wie stark unterscheidet sich die Durchlässigkeit von Kanälen?
→ K⁺-Kanäle: 100× durchlässiger für K⁺ als für Na⁺.
→ Na⁺-Kanäle (während Aktionspotenzial): 10–20× durchlässiger für Na⁺ als für K⁺.
Welche externen Faktoren beeinflussen Ionenkanäle?
→
Molekülanlagerung (z. B. Neurotransmitter)
Spannungsänderungen (Depolarisation)
Physikalische Reize (z. B. Druck, Licht, Temperatur)
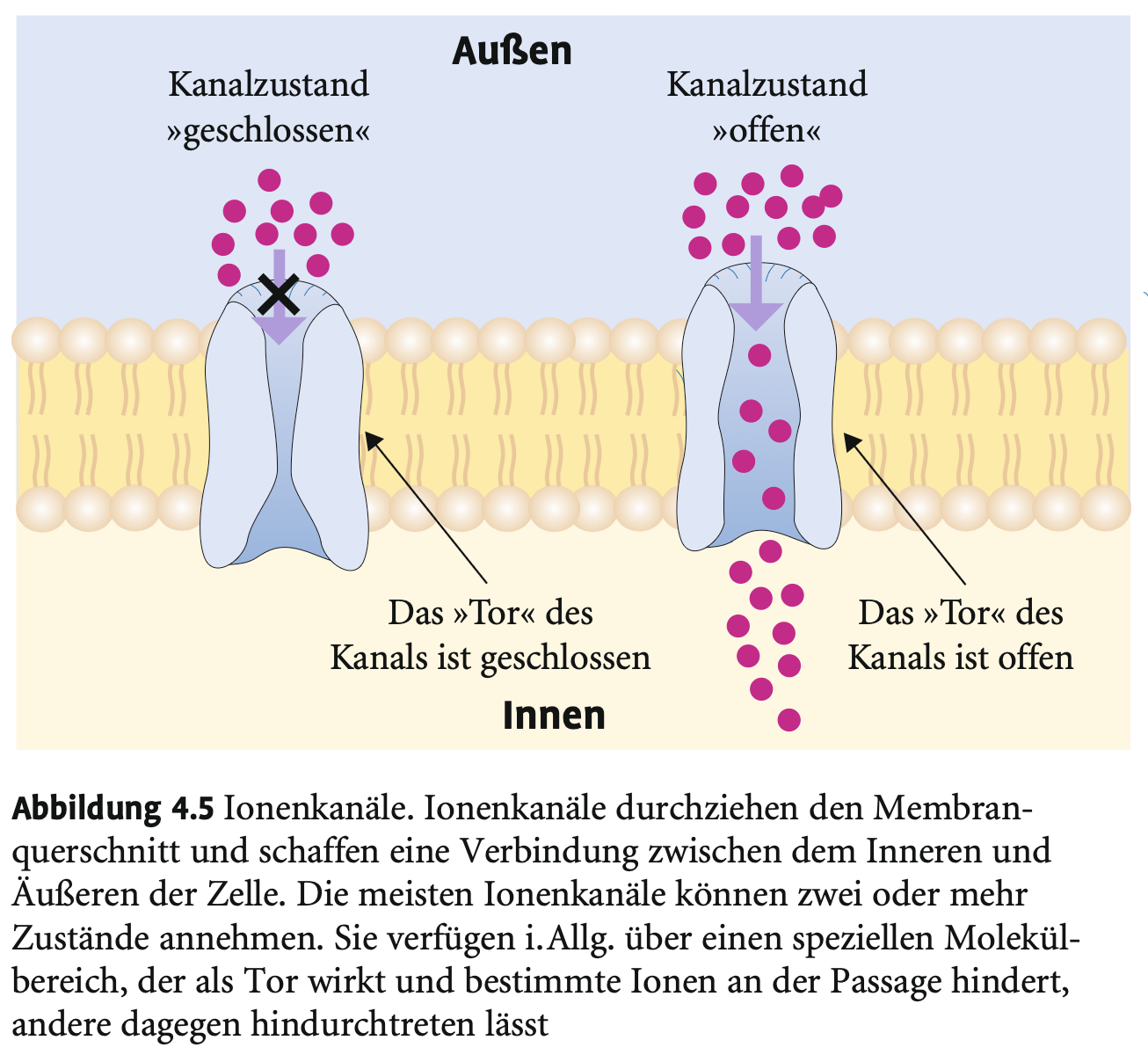
Wie wirken Lokalanästhetika auf Ionenkanäle?
→ Blockieren Na⁺-Kanäle, verhindern Ionenpassage, hemmen Reizweiterleitung → z. B. Schmerzempfindung.
Was ist ein elektrochemischer Gradient?
→ Das Nettoergebnis aus Konzentrations- und elektrischen Gradienten auf Ionen.
Was ist aktiver Transport?
→ Energieverbrauchender Transport gegen den elektrochemischen Gradienten, gerichtet und einseitig.
Warum würde ohne Regulation Na⁺ das Ruhepotenzial zerstören?
→ Na⁺ strömt passiv ein (da einige Kanäle immer offen sind) → Depolarisation → Membranpotenzial würde Richtung 0 mV gehen.
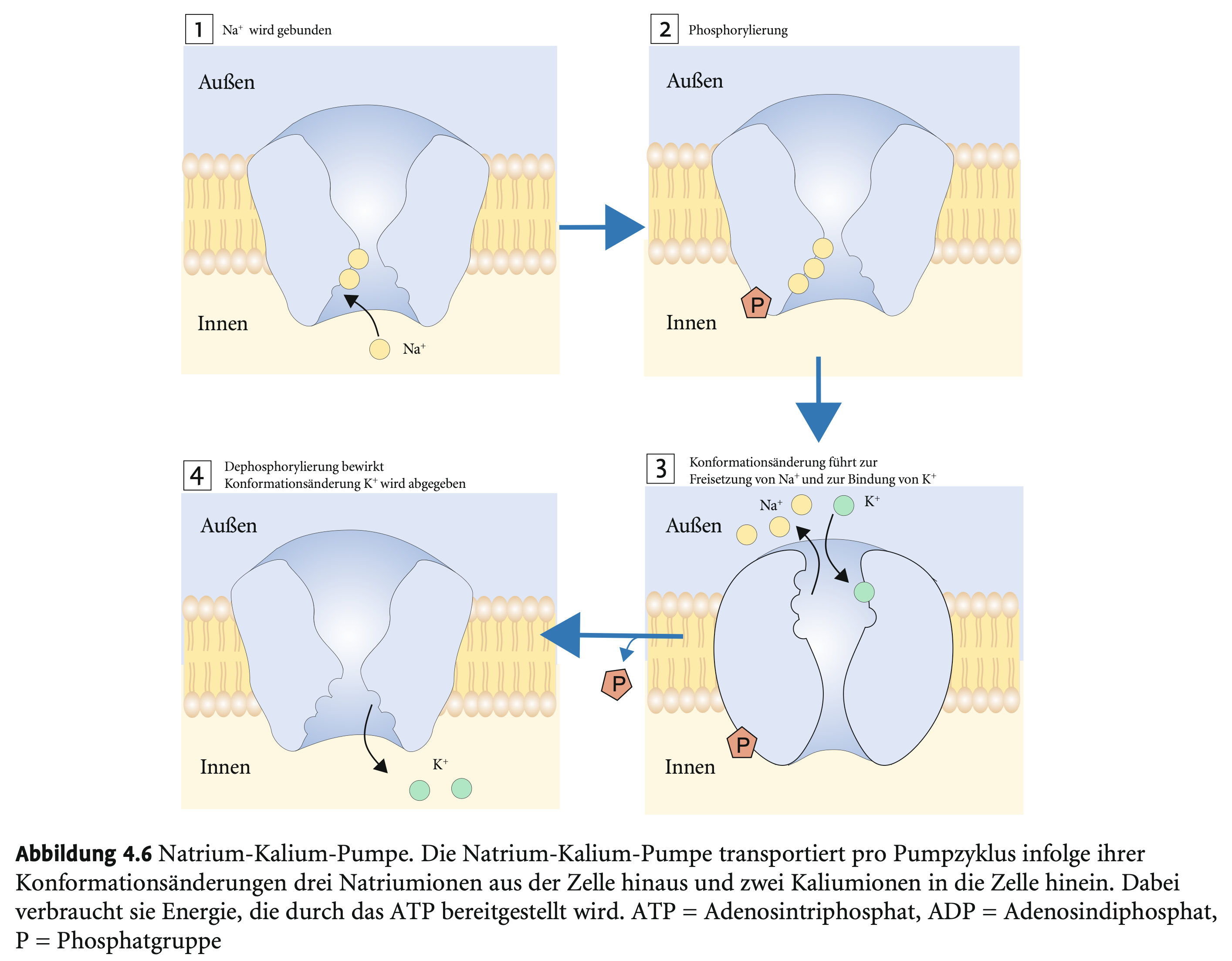
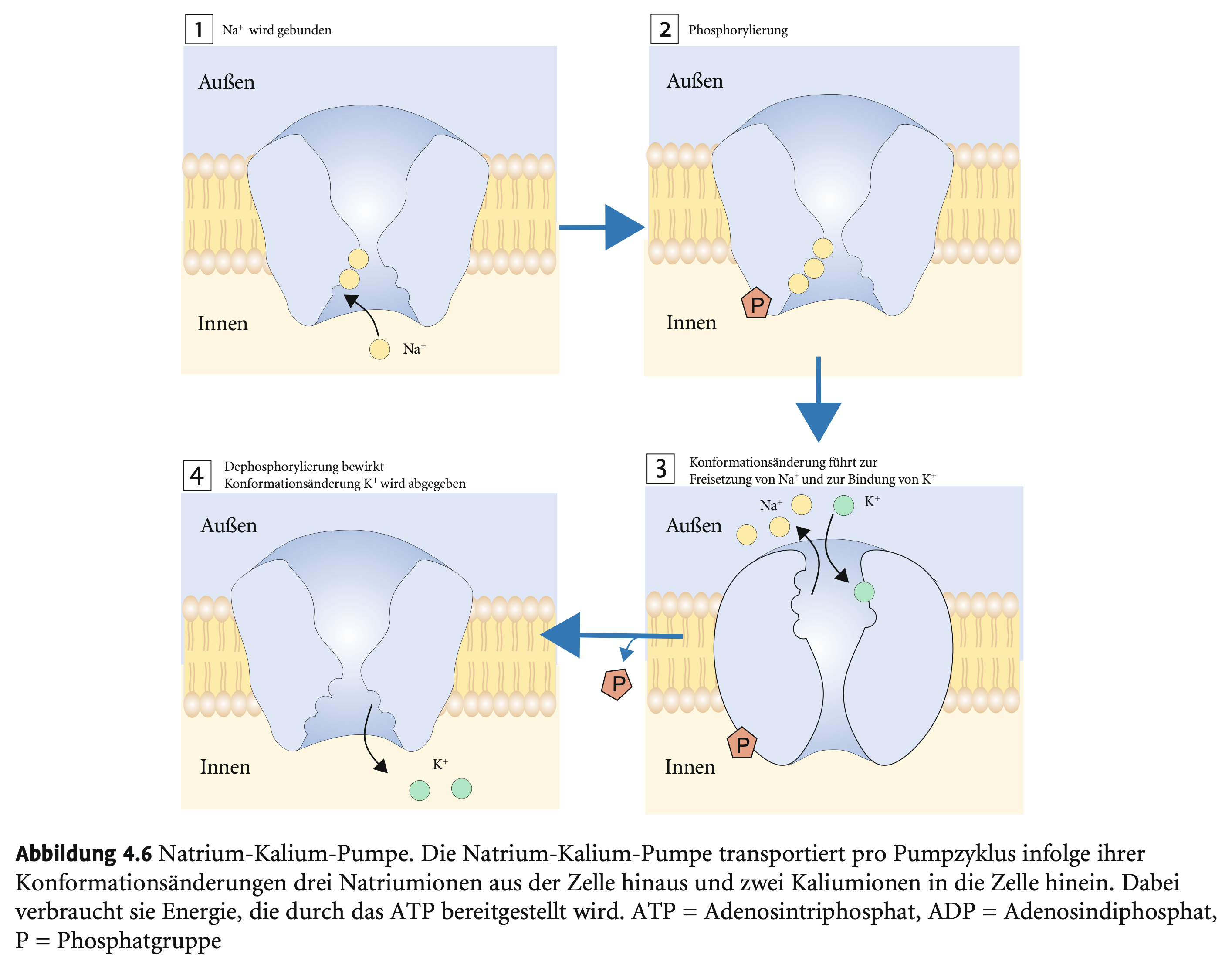
Was macht die Natrium-Kalium-Pumpe (Na⁺/K⁺-ATPase)?
→
Transportiert 3 Na⁺ aktiv aus der Zelle
2 K⁺ aktiv in die Zelle
Erhält so das Ruhepotenzial aufrecht
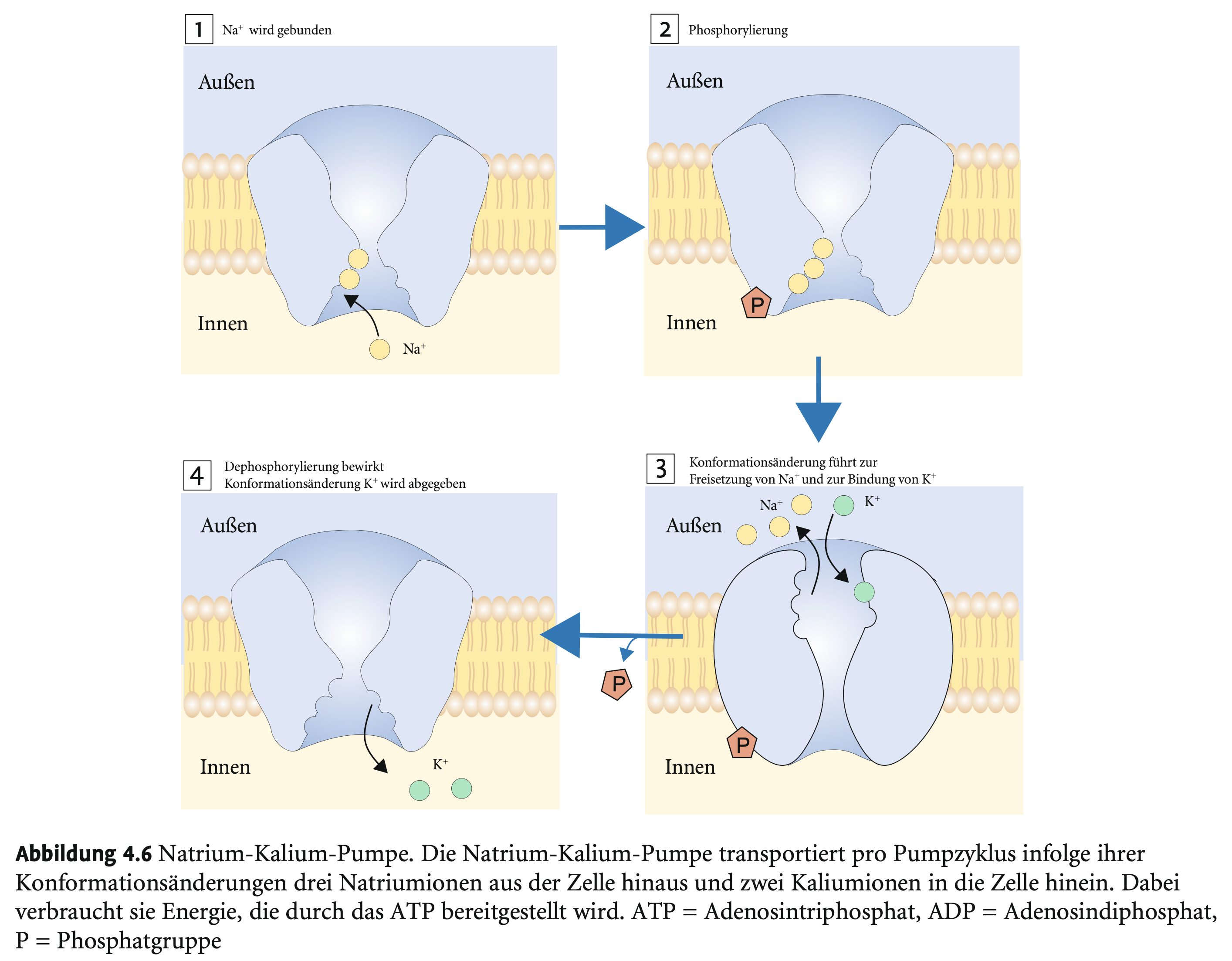
Was passiert mit dem K⁺, das von der Pumpe eingeschleust wird?
→ Es verlässt die Zelle wieder passiv über offene Kaliumkanäle → keine Akkumulation.
Wie wurde die Funktion der Na⁺/K⁺-Pumpe experimentell bewiesen?
→ Durch radioaktive Na⁺-Markierung: Einwärtsdiffusion ≠ Konzentrationsänderung → aktiver Ausgleich durch Pumpe.
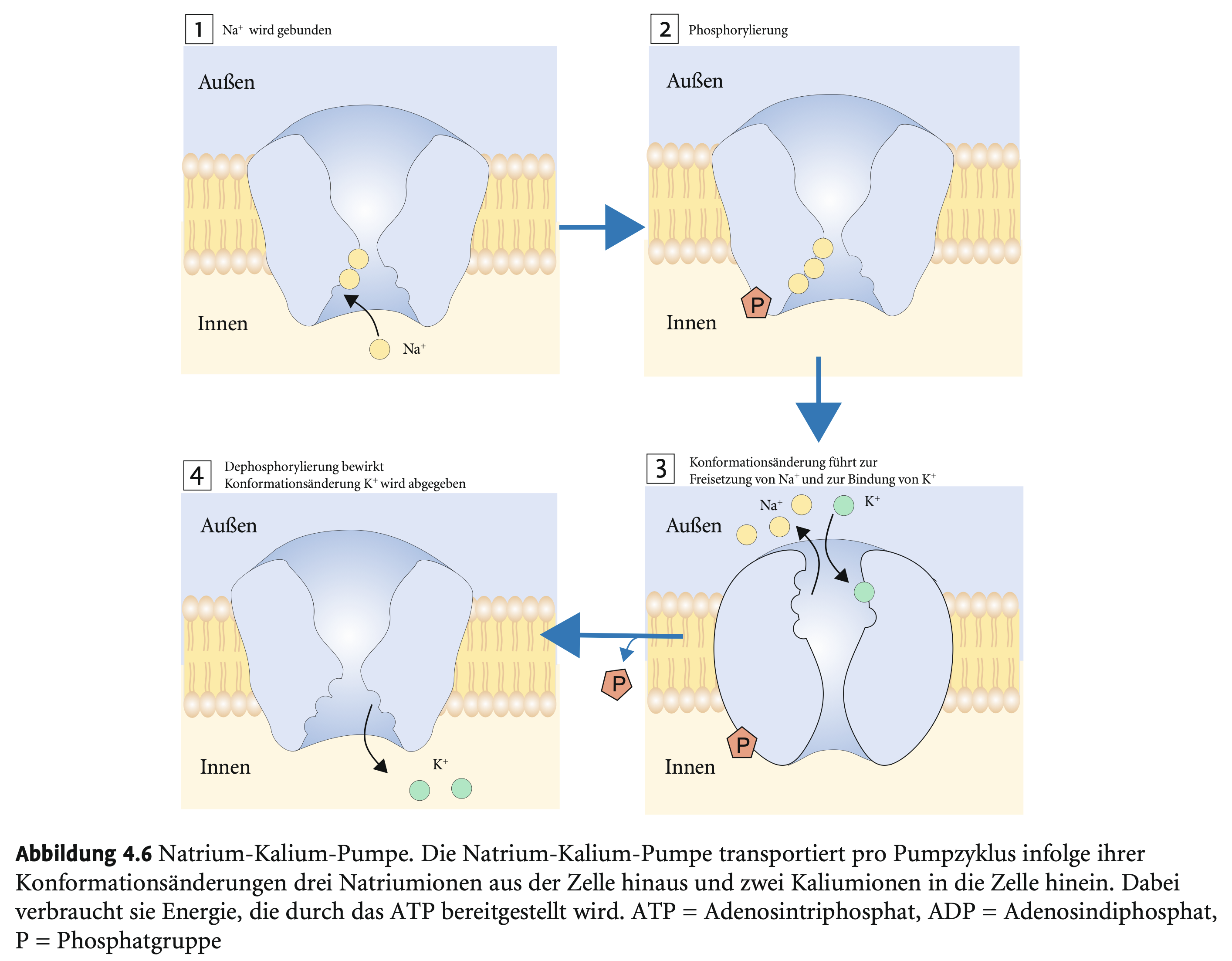
Welche Energieform nutzt die Na⁺/K⁺-Pumpe?
→ ATP → ADP + Phosphat → Energiefreisetzung → Konformationsänderung → Ionentransport.
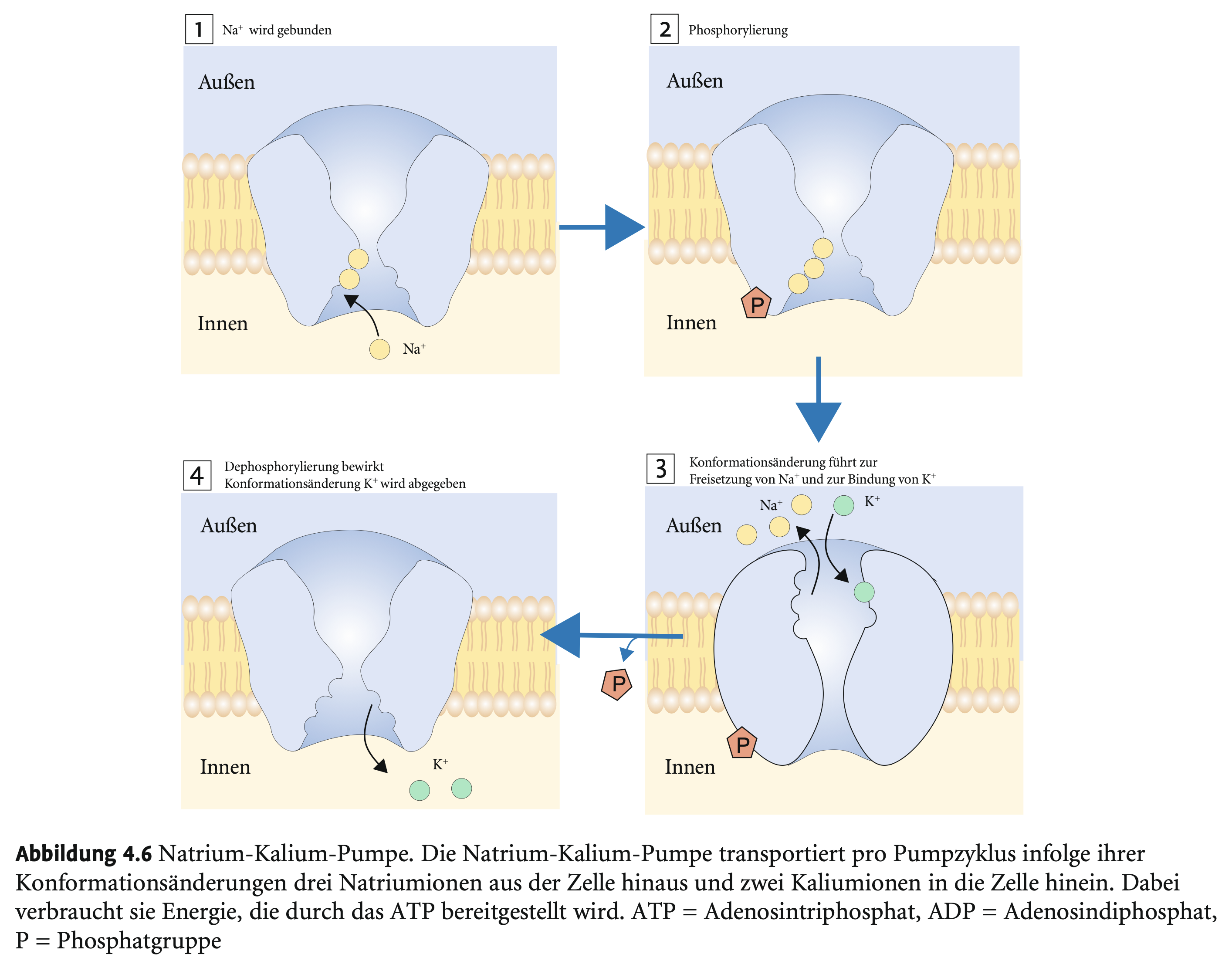
Warum ist die Na⁺/K⁺-ATPase ein Enzym?
→ Weil sie ATP spaltet (katalytisch) und dadurch den Ionentransport ermöglicht, ohne selbst verbraucht zu werden.
Was ist Ouabain und wie wirkt es?
→ Pflanzliches Pfeilgift (Glykosid), blockiert K⁺-Transport der Pumpe → Na⁺-Akkumulation → Cl⁻-Zuzug → Wasser strömt ein → Zelle schwillt → Funktionsverlust.
Welche zentrale Rolle spielt ATP im Organismus?
→
Na⁺/K⁺-Pumpe
Muskelkontraktion
Wärmeerzeugung
Biosynthese (z. B. Membranlipide)
Welche weiteren Pumpenproteine sind bekannt?
→
Kalziumpumpe (Ca²⁺ aus Zelle) – wichtig im ZNS
Pumpen für nicht-ionische Substanzen in anderen Geweben
Was sind spontan aktive Neuronen?
→ Neuronen, die ohne äußeren Reiz Aktionspotenziale generieren, weil ihr Ruhepotenzial instabil ist und sich spontan zur Schwelle hin depolarisiert.
(vgl. Schrittmacherneuornen, Bursting-Neuronen)
Welche Ionenkanäle ermöglichen spontane Aktivität?
→ Spannungsgesteuerte Na⁺- und K⁺-Kanäle mit verzögerter Aktivierungs- und Inaktivierungscharakteristik.
Was passiert nach dem selbst ausgelösten Aktionspotenzial bei spontan aktiven Neuronen?
→ Die Zelle kehrt wieder zum Ruhepotenzial zurück.
Was sind Schrittmacherneuronen?
→ Neuronen, die rhythmisch und kontinuierlich feuern und periodische Verhaltensweisen wie Atmung, Kauen oder Gehen steuern.
→ Sie sind mit anderen Neuronen gekoppelt und erzeugen gemeinsam einen konstanten, rhythmischen Output, der anpassbar bleibt.
Was sind Bursting-Neuronen? Welche Funktion haben Bursts in Neuronen?
→ Neuronen, die in Salven (Bursts) von Aktionspotenzialen feuern, unterbrochen von Ruhephasen.
→ Steuerung rhythmischer Abläufe, z. B. bei der hormonellen Sekretion nach festgelegtem zeitlichem Muster.
Warum sind Vestibularzellen auch in Ruhe aktiv?
→ Vestibuläre Haarzellen (in Bogengängen & Makulaorganen) sind spontan aktiv, d. h. sie feuern auch in absoluter Ruhe mit einer tonischen Grundfrequenz.
Bei Kopfstillstand feuern linkes und rechtes Vestibularorgan symmetrisch → das Gehirn interpretiert dies als „kein Bewegungssignal“.
Bei Kopfbewegung entsteht ein asymmetrisches Signal (eine Seite ↑, die andere ↓) → so wird Richtungs- & Beschleunigungsinformation codiert.
Ohne Grundaktivität wäre bidirektionale Wahrnehmung (z. B. links vs. rechts drehen) nicht möglich.
Wie erfolgt die Signalweiterleitung in Nervenzellen, und warum ist der Vergleich mit einem Draht nur begrenzt passend?
• Die Signalweiterleitung beruht auf einer lokalen Veränderung des Membranpotenzials, meist durch Na⁺-Einstrom.
• Die elektrischen Signale verlaufen entlang der Membran, nicht durch das Axoplasma.
• Vergleich mit einem Draht ist nur begrenzt sinnvoll, weil:
– Ionen, nicht Elektronen, transportiert werden (→ größer, träger)
– Das System ist nicht perfekt isoliert → Ladungsverlust möglich
– Mehrere Ionensorten wirken gleichzeitig → teils fördernd, teils störend
Was ist passive Leitung in Nervenzellen und wie funktioniert sie?
Eine lokale Depolarisation (z. B. durch Na⁺-Einstrom) verändert das Membranpotenzial. Diese Spannung breitet sich entlang der Membran sehr schnell, aber mit abnehmender Stärke aus – ohne echte Ionenwanderung, nur durch Verschiebung benachbarter Ladungsträger.
Ist typisch für Dendriten, reicht für kurze Distanzen in lokal vernetzten Neuronen und ist besonders wichtig in dicht gepackten Hirnarealen – daher im menschlichen Gehirn weit verbreitet.
(bzw. Elektrotonus/elektrotonische Leitung)
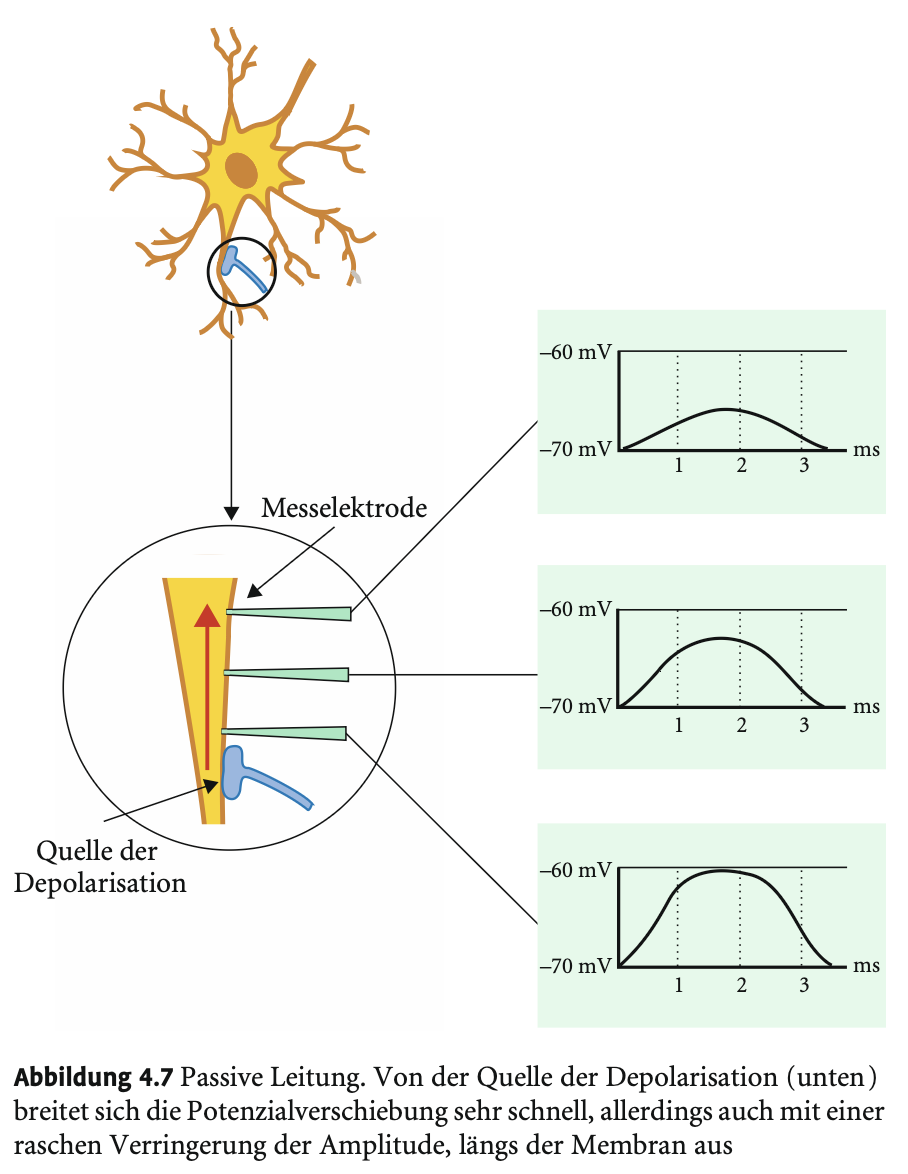
Warum reicht passive Leitung nicht für große Entfernungen?
Weil Leckströme (z. B. K⁺-Ausstrom) und die Aktivität der Na⁺/K⁺-Pumpe das Signal abschwächen. Nach 0.2–1 mm ist das Potenzial oft halbiert.
Wie beeinflusst der Faserquerschnitt die Leitungsgeschwindigkeit?
Unmyelinisiert: Geschwindigkeit ∝ √(Querschnitt).
Myelinisiert: Geschwindigkeit ∝ Durchmesser.
Dickere Fasern leiten schneller.
Warum reicht das passive Signal allein nicht aus, und was ist die Lösung?
Weil es sich nicht weit genug ausbreitet → Das Aktionspotenzial (AP) ermöglicht eine verlustfreie, selbstverstärkende Signalweiterleitung über lange Distanzen.
Wie wird ein Aktionspotenzial ausgelöst?
Wenn eine Reizschwelle überschritten wird, öffnen sich spannungsgesteuerte Na⁺-Kanäle → starker Na⁺-Einstrom → schnelle, sprunghafte Depolarisation.
Was besagt das Alles-oder-Nichts-Gesetz?
Ein Reiz unterhalb der Schwelle erzeugt kein AP.
Oberhalb: Immer gleich starke APs – unabhängig von Reizstärke (also nicht ein linearer Anstieg). Nur die Frequenz kann variieren.

Wo entsteht das Aktionspotenzial typischerweise zuerst und warum?
Am Axonhügel, da dort die Dichte spannungsgesteuerter Na⁺-Kanäle besonders hoch ist – höchste Erregbarkeit.
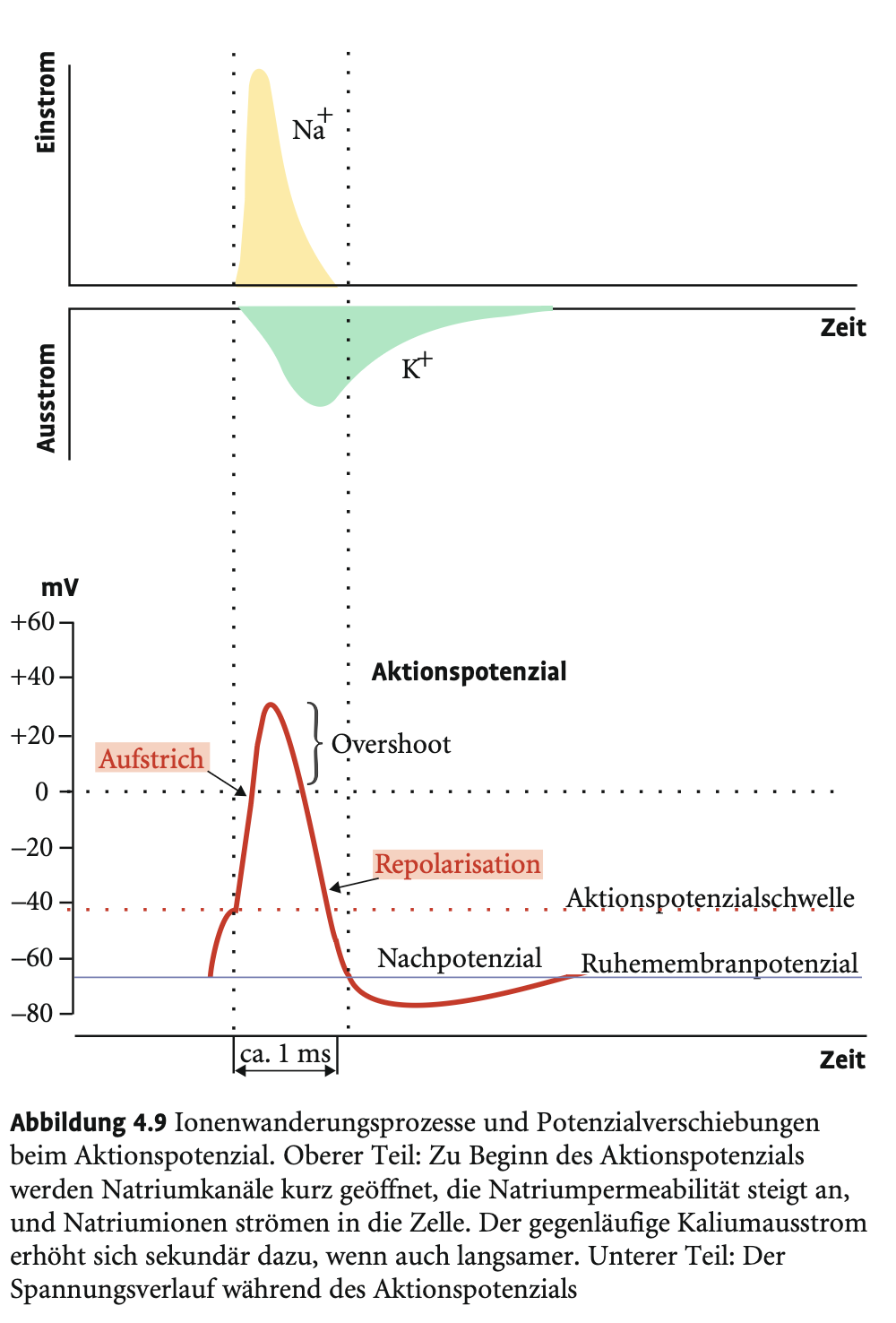
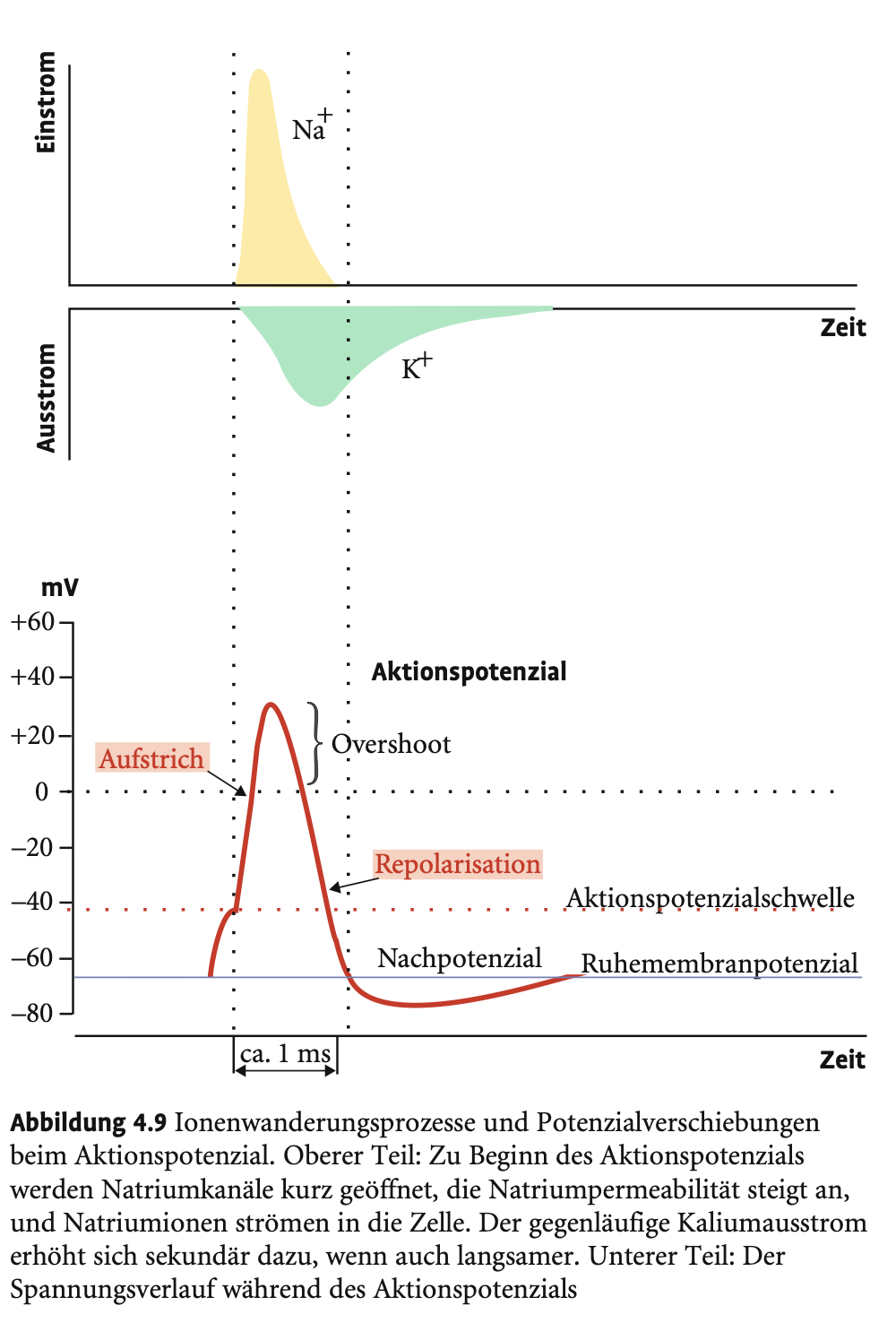
Welche Phasen durchläuft ein Aktionspotenzial?
Schwellenüberschreitung → Na⁺-Kanäle öffnen → Aufstrich & Overshoot
Na⁺-Kanäle inaktivieren → absolute Refraktärphase, bereits nach 1ms
Na⁺-Kanäle deinaktivieren nahe Ruhepotenzial
K⁺-Kanäle öffnen verzögert → Repolarisation & Hyperpolarisation
Na⁺/K⁺-Pumpe stellt Ausgangszustand wieder her
Was ist die absolute Refraktärphase?
Während Aufstrich und früher Repolarisation → Na⁺-Kanäle sind inaktiviert → kein neues AP möglich.
Was ist die relative Refraktärphase?
Während Hyperpolarisation → nur stärkerer Reiz löst neues AP aus → reduzierte Amplitude bei kurzem Abstand zum vorherigen AP.
Wie wird Reizintensität im Nervensystem codiert?
Nicht durch Amplitude, sondern durch Frequenz der Aktionspotenziale → stärkere Reize → kürzere Latenz → höhere Frequenz.
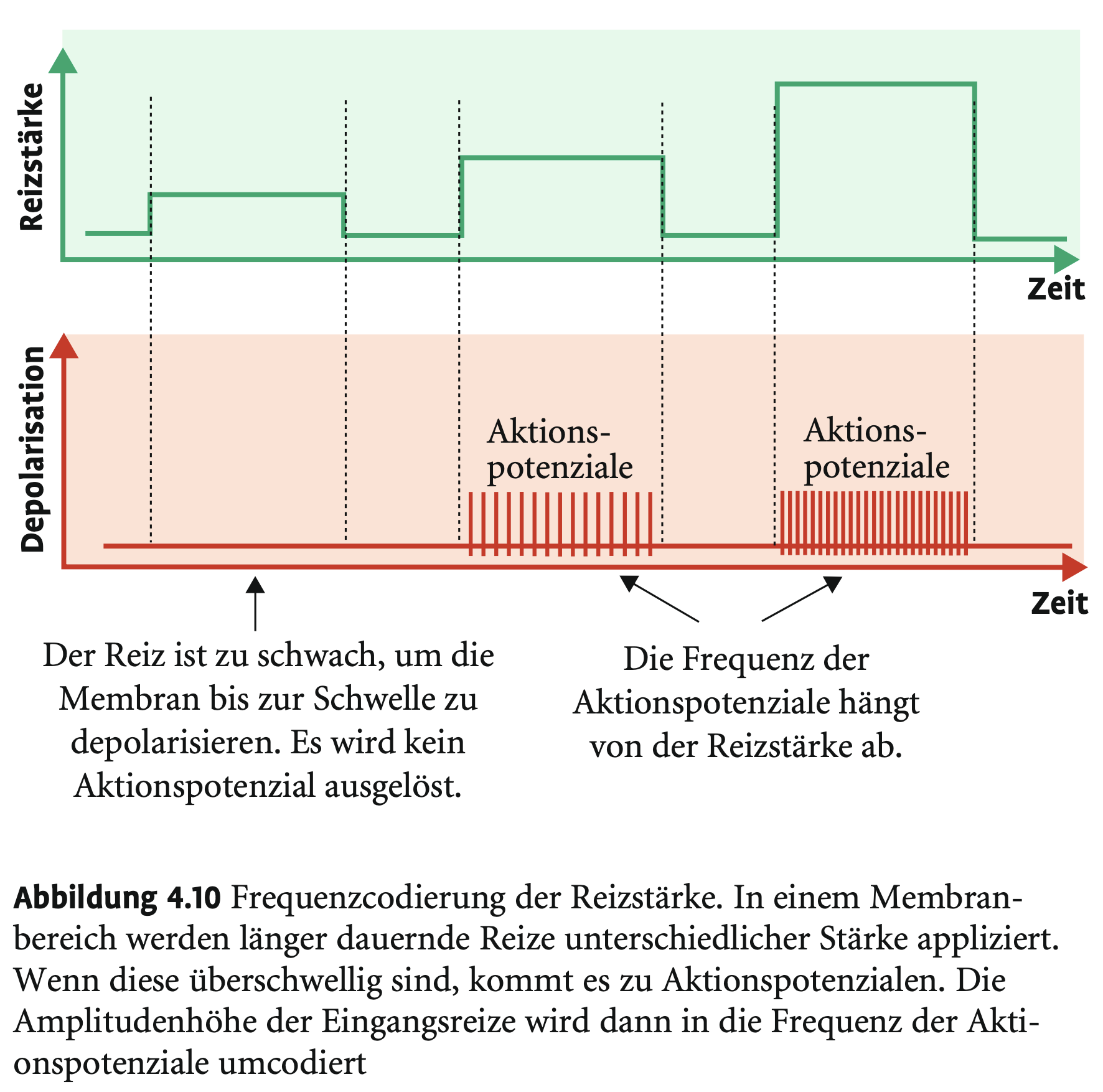
Welche Bedingungen müssen für AP-Salven erfüllt sein?
Der Reiz muss (1) länger dauern als ein AP und (2) stark genug sein, um auch während der relativen Refraktärphase zu depolarisieren.
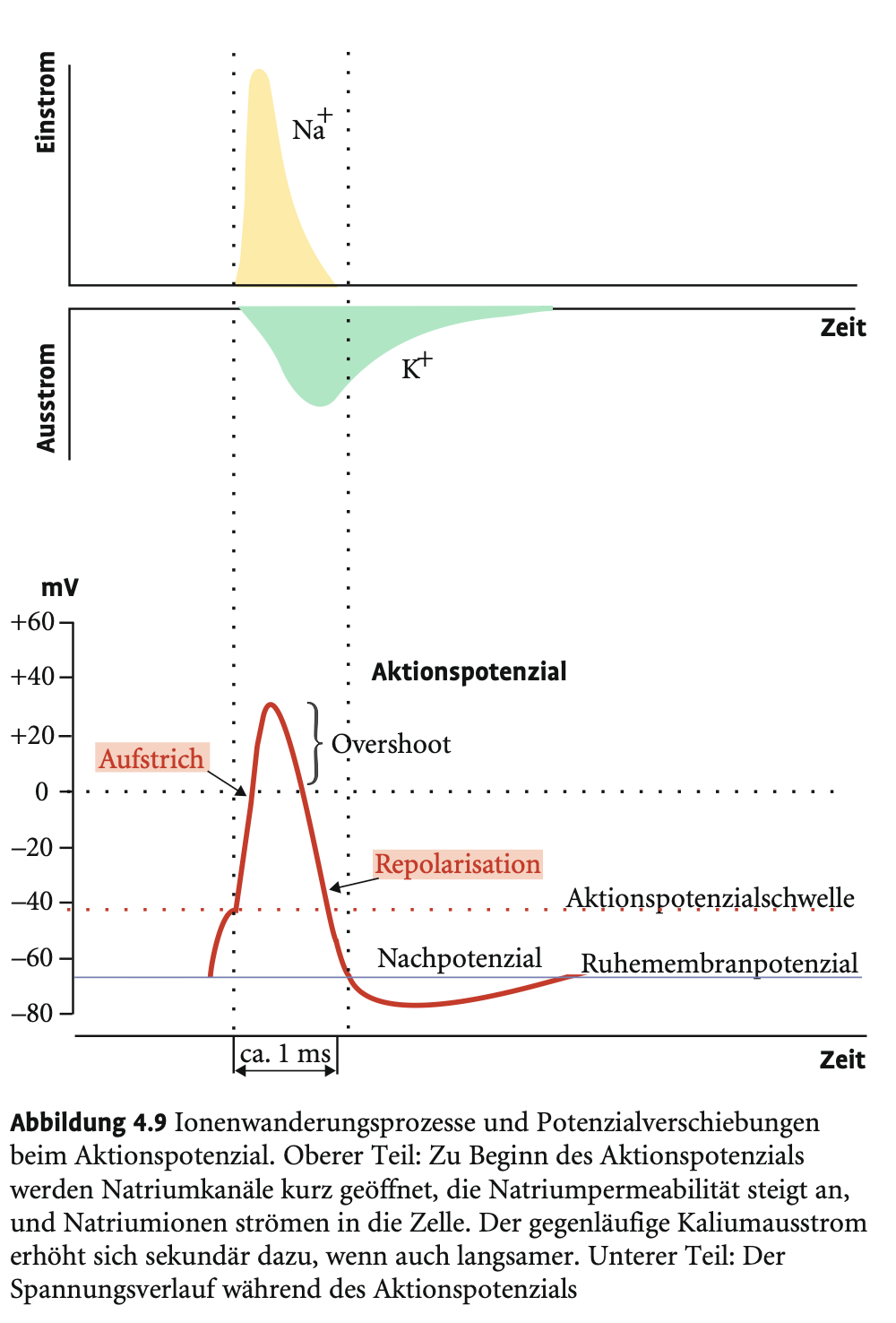
Wie funktionieren spannungsgesteuerte Na⁺-Kanäle?
Öffnen bei Erreichen der Schwelle, bleiben ~1 ms offen → dann inaktiv. Reaktivierung erst nahe Ruhepotenzial möglich.
Wie „öffnet“ sich ein spannungsgesteuerter Na⁺-Kanal technisch?
Spannung verändert Struktur großer Membranproteine (Domänen) durch elektrische Felder (~100.000 V/cm) → Konfigurationswechsel → Kanal öffnet/schließt.
Was ist die Leistung eines einzelnen spannungsgesteuerten Na⁺-Kanals?
Ca. 5.000–6.000 Na⁺-Ionen in 1 ms. Dichte: 35–500 Kanäle/μm², ≙ max. 1 % Membranfläche.
Welche Gifte beeinflussen spannungsgesteuerte Na⁺-Kanäle und wie?
Tetrodotoxin (Kugelfisch): blockiert Kanal → kein AP → Lähmung, Atemstillstand
Skorpion-/Seeanemonengifte: halten Kanal offen → verlängerte Depolarisation → längere Refraktärzeit → gestörte Signalweiterleitung
Welche weiteren spannungsgesteuerten Kanäle gibt es außer Na⁺?
• Ca²⁺-Kanäle → starker Ca²⁺-Einstrom, trägt zum Aufstrich bei
• Cl⁻-Kanäle in manchen Neuronen
• Subtypen unterscheiden sich im Schwellenwert & Vorkommen (Zelltyp, Region, Spezies)
Wie wirken Lokalanästhetika?
Blockieren die spannungsgesteurte Na⁺-Kanäle (und wenn in grosser Menge gegeben, dann auch K⁺) → keine APs → keine Schmerzleitung. Erstes Mittel: Kokain → ersetzt durch Prokain/Novokain.
Welche Zellen oder Systeme sind bei Überdosierung von Lokalanästhetika zusätzlich betroffen?
Erregbare Zellen wie Herzmuskelzellen → Gefahr von Herzrhythmusstörungen.
Welche Fasertypen werden durch Lokalanästhetika zuerst blockiert?
Dünne Fasern (Schmerz) eher als dicke (Motorik) → selektive Ausschaltung.
Wie breitet sich ein Aktionspotenzial entlang des Axons aus?
Wie eine Zündschnur → jeder erregte Bereich depolarisiert den nächsten. Rücklauf wird durch Refraktärzustand verhindert → anterograd.
Warum leiten dickere Axone schneller als dünne?
Mehr Ionen im Axoninneren sind vor Leckströmen geschützt → größere effektive Stromstärke → schnellere Depolarisation.
Was ist saltatorische Erregungsleitung?
APs springen von einem Ranvier-Schnürring zum nächsten → dazwischen passive Weiterleitung durch myelinisierten Abschnitt.
Welche Rolle spielen Ranvier-Schnürringe bei der saltatorischen Leitung?
Unmyelinisierte Bereiche mit hoher Na⁺-Kanaldichte (~10.000/μm²) → nur dort kann AP ausgelöst werden.
Warum ist saltatorische Erregungsleitung schneller und effizienter?
Weil myelinisierte Abschnitte isolieren → weniger Energieverlust & Ionenverschiebung → schnellere und energieeffiziente Weiterleitung.
Welche Funktionen erfüllt die Myelinscheide bei der Erregungsleitung?
– Sie wirkt als elektrischer Isolator, verhindert Leckströme, reduziert den Ionenfluss durch die Membran und enthält kaum spannungsgesteuerte Natriumkanäle → Aktionspotenziale können dort nicht ausgelöst werden.
– Die Signalweiterleitung erfolgt passiv (elektrotonisch): schnell, aber mit schnellem Amplitudenabfall.
Warum darf der Abstand zwischen zwei Ranvier-Schnürringen nicht zu groß sein?
Weil das Potenzial beim passiven Überbrücken sonst zu stark absinkt → am nächsten Schnürring kann kein Aktionspotenzial ausgelöst werden.
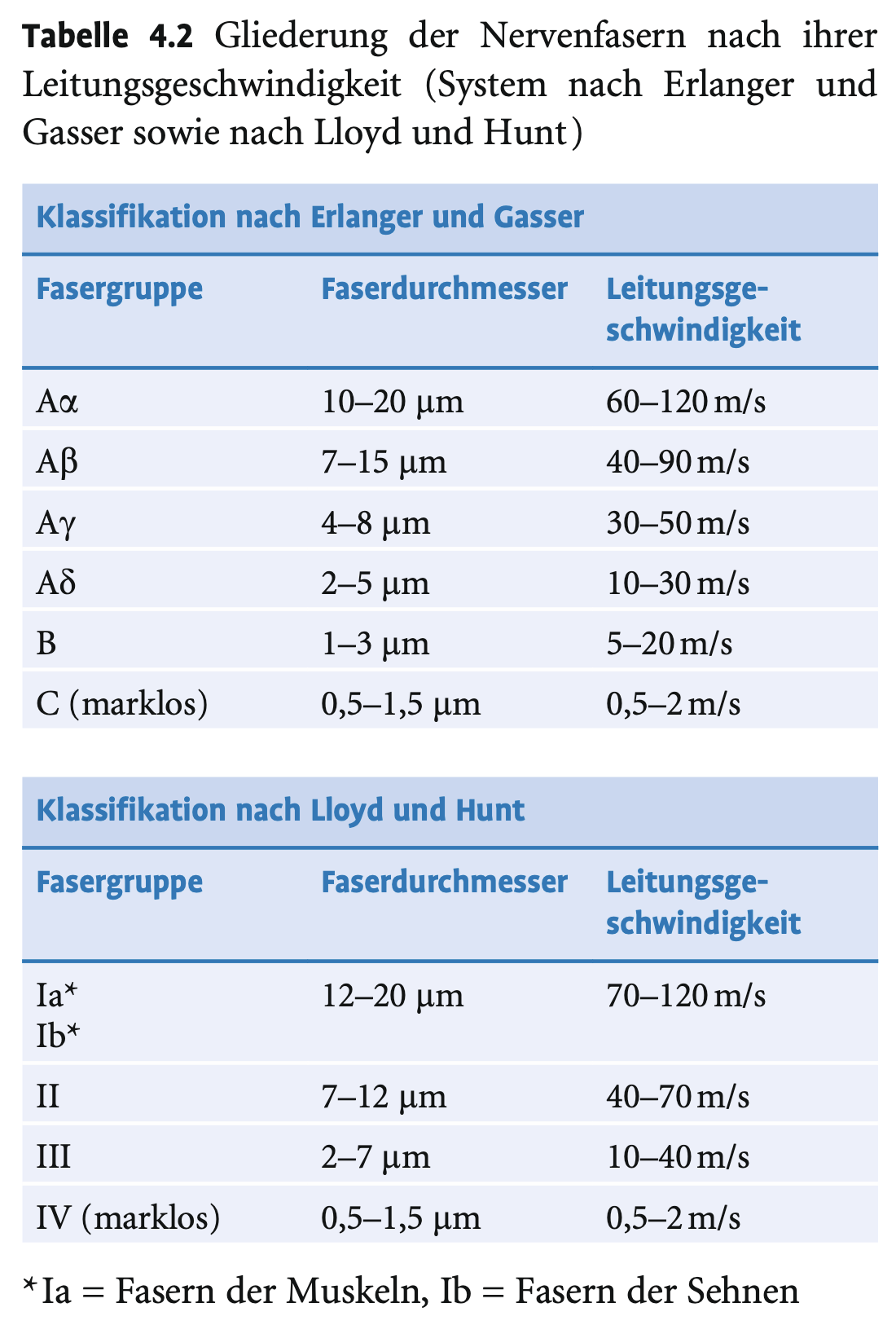
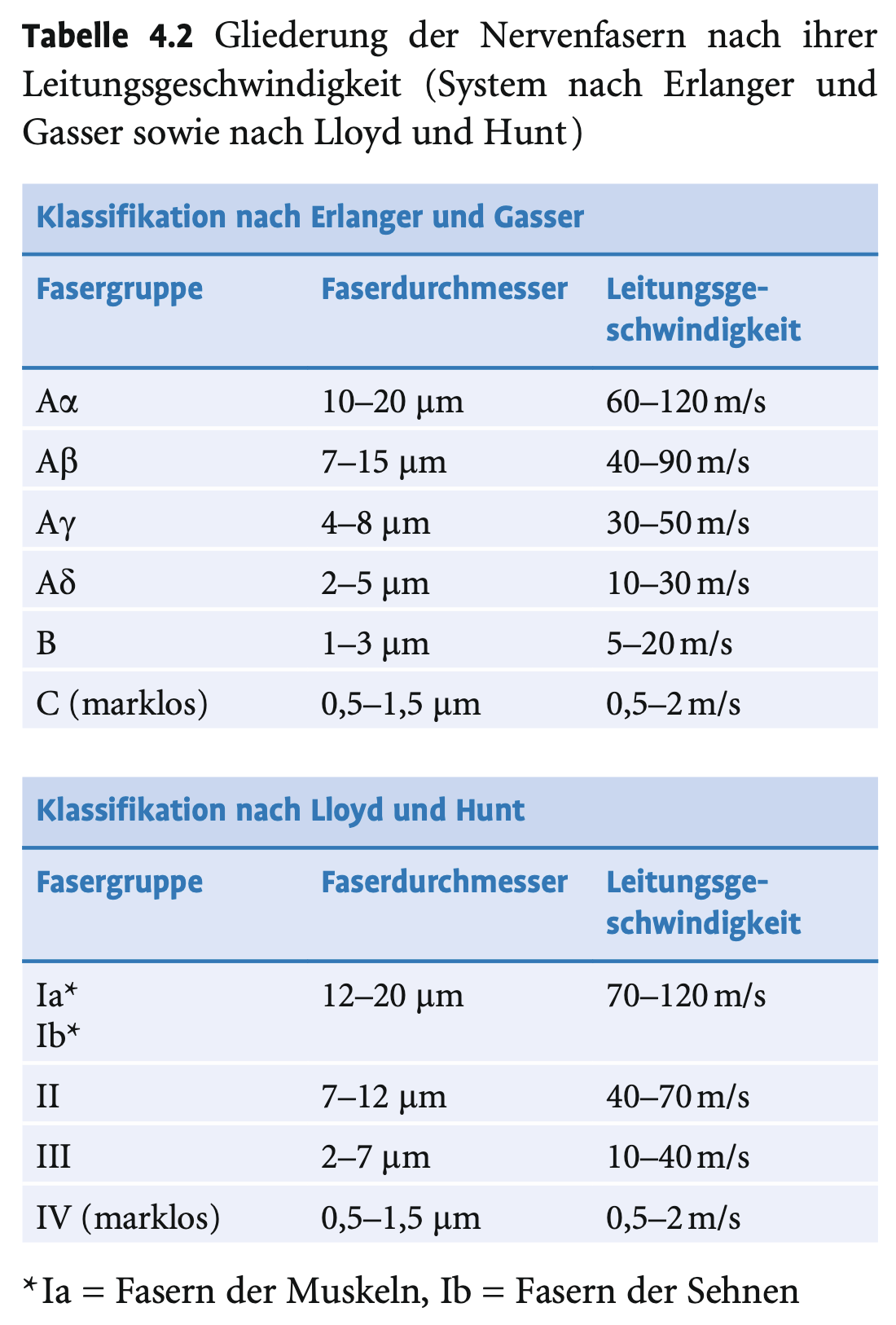
Wie hängt die Leitungsgeschwindigkeit von der Faserdicke ab?
– Die Erregungsgeschwindigkeit steigt mit dem Axondurchmesser – sowohl bei myelinisierten als auch bei unmyelinisierten Fasern.
– Der Durchmesser bezieht sich auf die gesamte Faser inklusive Myelinschicht.
– Zur Klassifikation der Fasern existieren zwei gebräuchliche Fasertyp-Systeme.