Kaarten: biochemie H10: Chemotroof Energie Metabolisme: Aerobe ademhaling | Quizlet
1/70
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
71 Terms
1) Welk proces gebeurt er in afwezigheid van zuurstof?
2) Welk proces gebeurt er in aanwezigheid van zuurstof?
1) fermentatie (regeneratie NAD+) glucose is donor en acceptor van elektronen
2) aerobe ademhaling (pyruvaat wordt verder geoxideerd tot CO2) gereduceerde Co-enzymen gaan hun elektronen overdragen op O2 (externe acceptor)
Hoe gaat O2 dienen als elektronen acceptor?
O2 gaat worden gereduceerd tot H2O tijdens de aerobe ademhaling
Wat zijn de drie grote stappen van de aerobe ademhaling
1) Oxidatie van brandstofmolecule en reductie van co-enzymen (NADH, FADH2) (glycolyse, pyr => acetyl coA, CAC)
2) oxidatie van co-enzymen en reductie van O2 tot H2O via elektronentransportketen
3) ATP synthese die mogelijk is door de protonengradient die is ontstaan in de elektronentransportketen
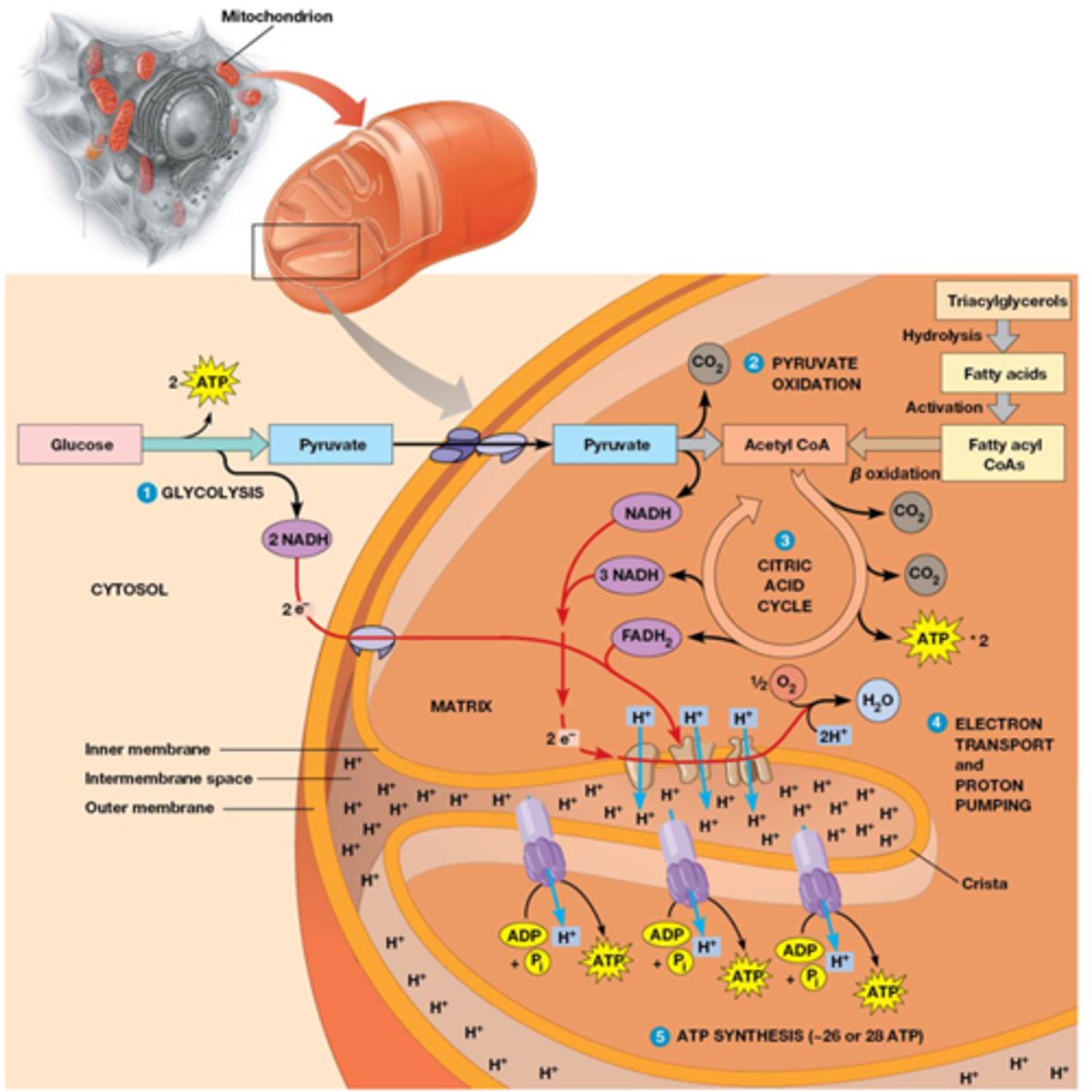
Aerobe ademhaling in vorm van een tekening
1) Glycolyse (aeroob of anaeroob)
2) Pyruvaat in aerobe omstandigheden: oxidatie tot acetyl CoA
3) CAC: vorming van 2 CO2 (oxidatie)
4) Transfer van elektronen van gereduceerde co-enzymen naar O2, gekoppeld aan pompen van protonen naar de intermembranaire ruimte (elektronen transport keten)
5) Energie van de protonen gradiënt wordt gebruikt voor ATP synthese: oxidatieve fosforylatie
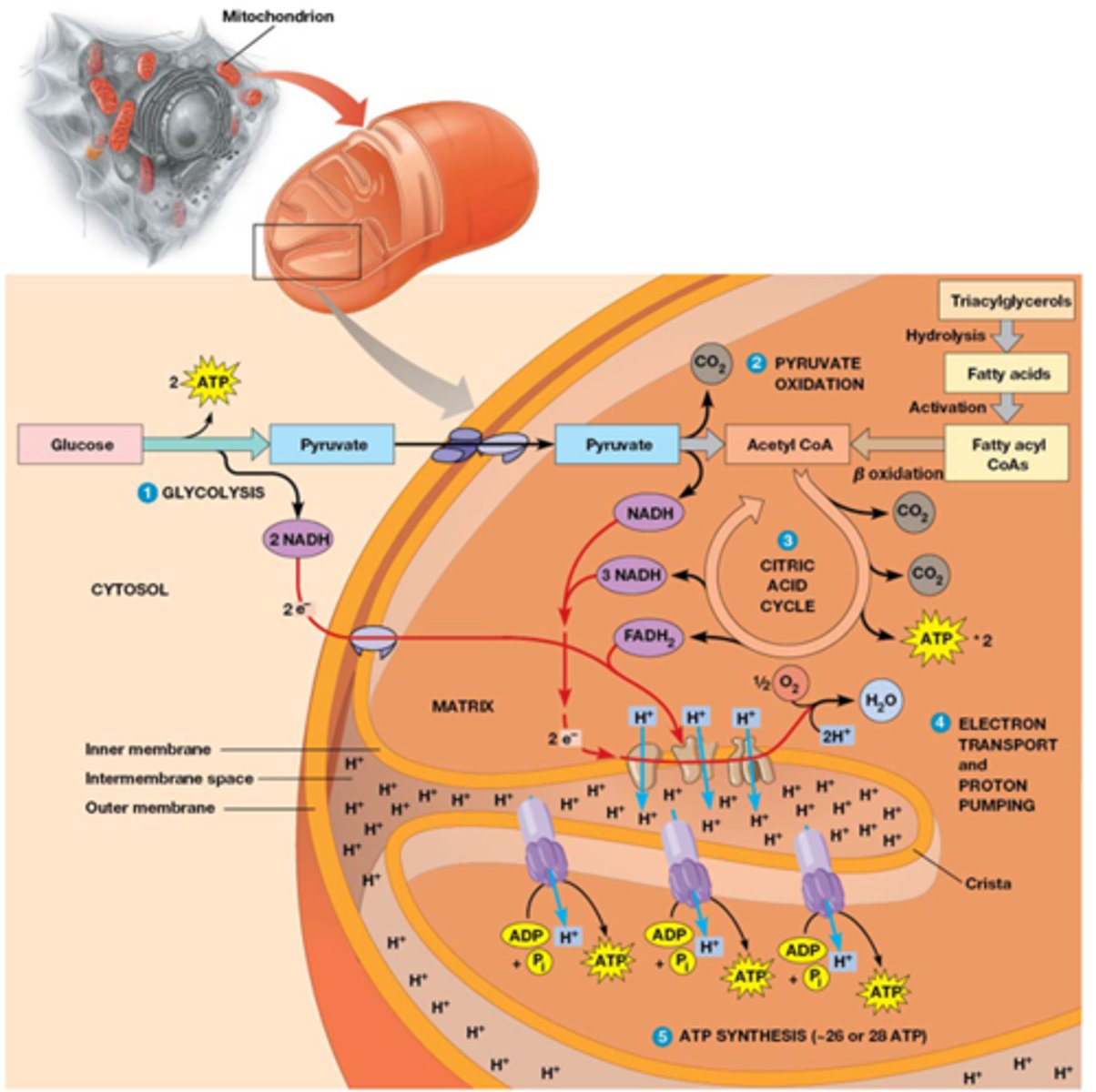
Waar gebeuren de verschillende stappen van de aerobe ademhaling?
1) glycolyse = cytosol
2) pyruvaat = via porines doorheen de buitenste mitochondriaal membraan, via pyruvaat symporter doorheen de binnenste membraan (pyruvaat => acetyl CoA in mitochondrien)
3) CAC = in mitochondrien
4) elektronentransportketen = innermembraan mitochondrien
5) ATP synthese: innermembraan mitochondrien -> matrix
(zie vooral tekeningen want op de slide is de info ook anders....)
Waarop steunt de hypothese dat mitochondriën van bacteriële oorsprong zijn?
- Circulair DNA
- Eigen eiwitsynthese
- dubbel membraan
- vergelijkbaar eiwitsysteem met prokaryote
->endosymbionten hypothese
de endosymbionten hypothese (van vorig jaar: Biologie 6.5: evolutie)
lang geleden geraakt een aerobe bacterie opgenomen in een prokaryote cel waardoor er mitochondrien ontstaan.
Daarna gaat de cyanobacterie dit ook doen waardoor er chloroplasten ontstaan.
->eukaryote cel
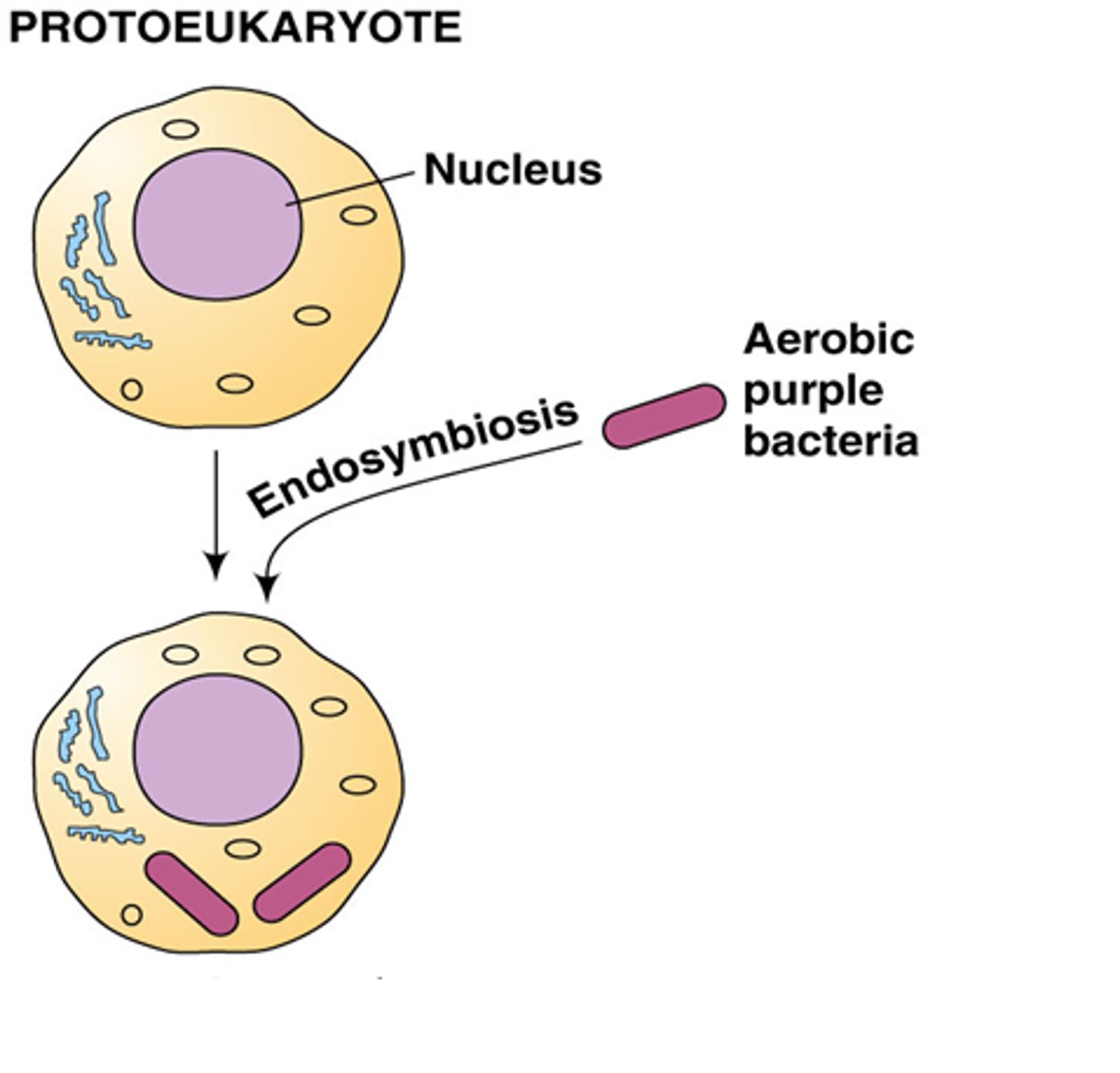
Mitochondrien structuur
- porines opgebouwd uit amfipatische beta platen
- intermembranaire ruimte zelfde samenstelling als cytosol
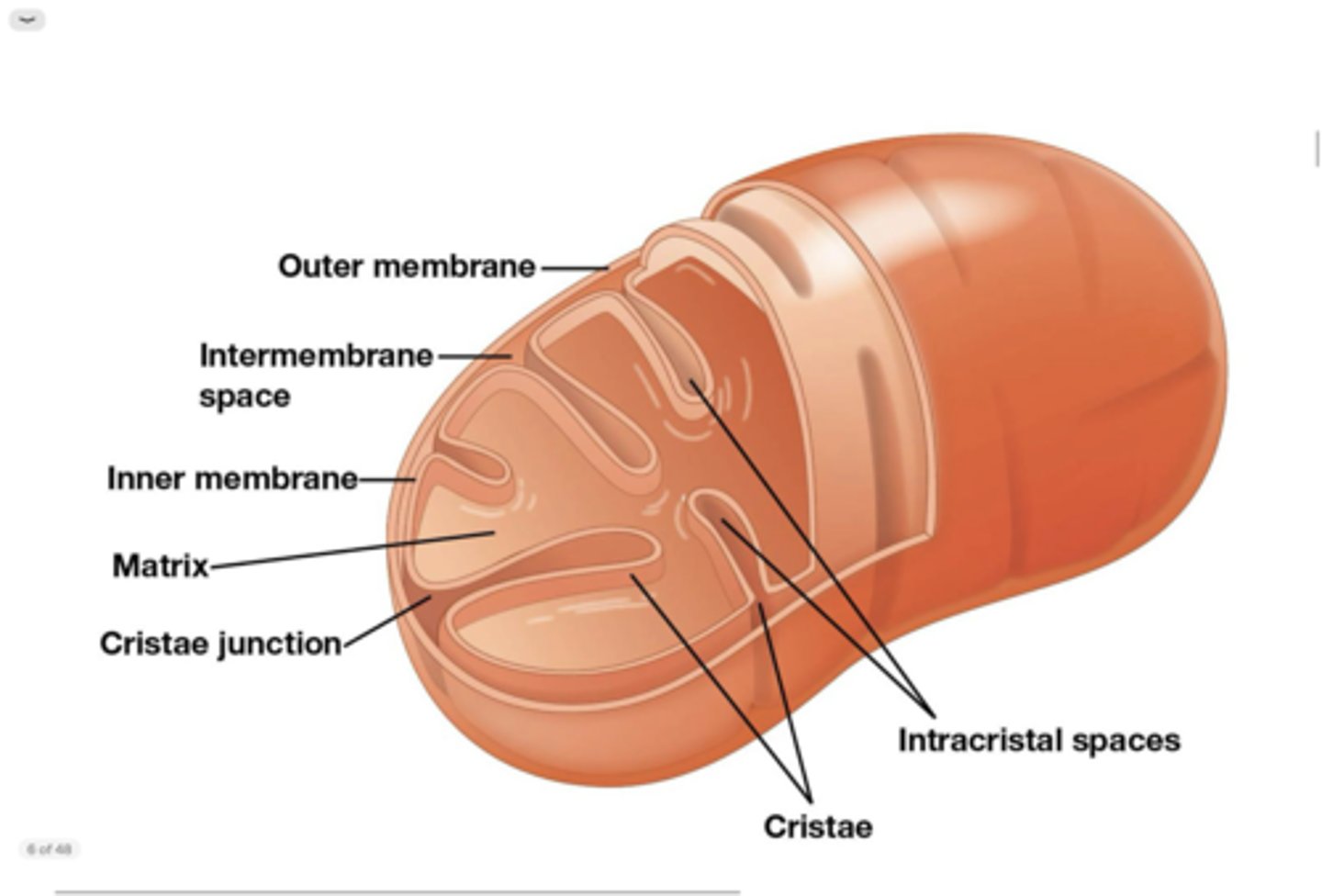
Functie cristae
- vergroten oppervlakte binnenste membraan
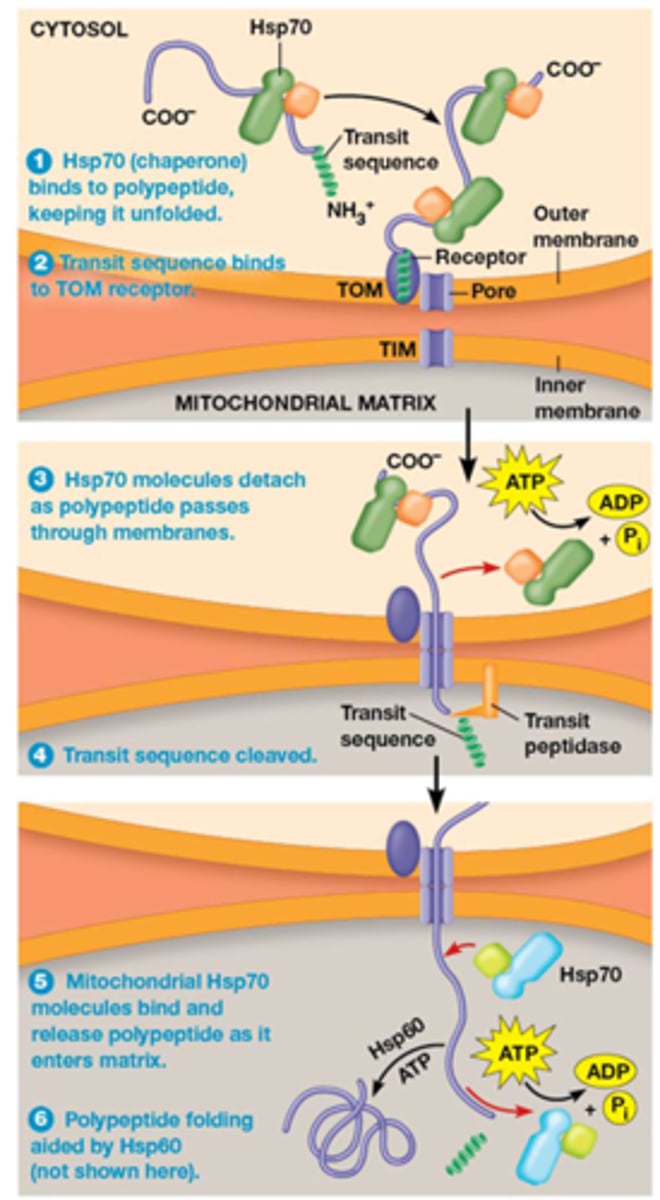
Hoe gebeurt het transport van cytosolaire eiwitten naar de mitchondrien?
Op sommige plaatsen zijn binnenste en buitenste membraan in contact: translocatie van eiwitten vanuit cytosol naar de matrix
- meer dan 95% van eiwitten in mitochondriën zijn gecodeerd door nucleaire genen
- gaan onopgevouwen (ahv Hsp70) door de eerste porie gaan
=> ze worden herkend door TOM receptor
=> dan gaat het onopgevouwen eiwit door de porie en wanneer hij uit de porie komt gaan er opnieuw Hsp70 binden aan het eiwit
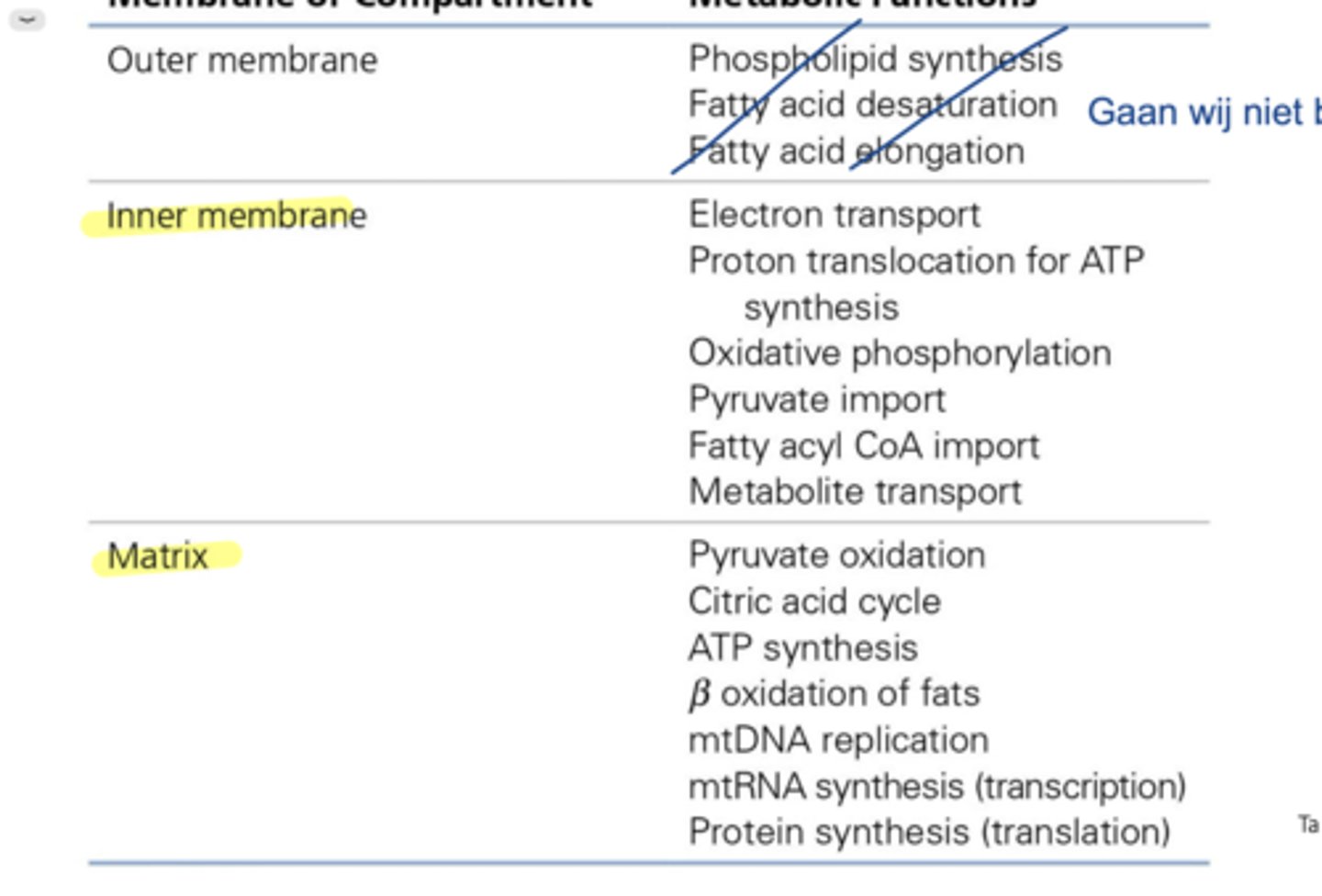
Overzicht lokalisatie processen in de mitochondriën
Wat is de kern van de citroenzuurcyclus
afbraak acetyl Coa en reductie NAD+ en FAD
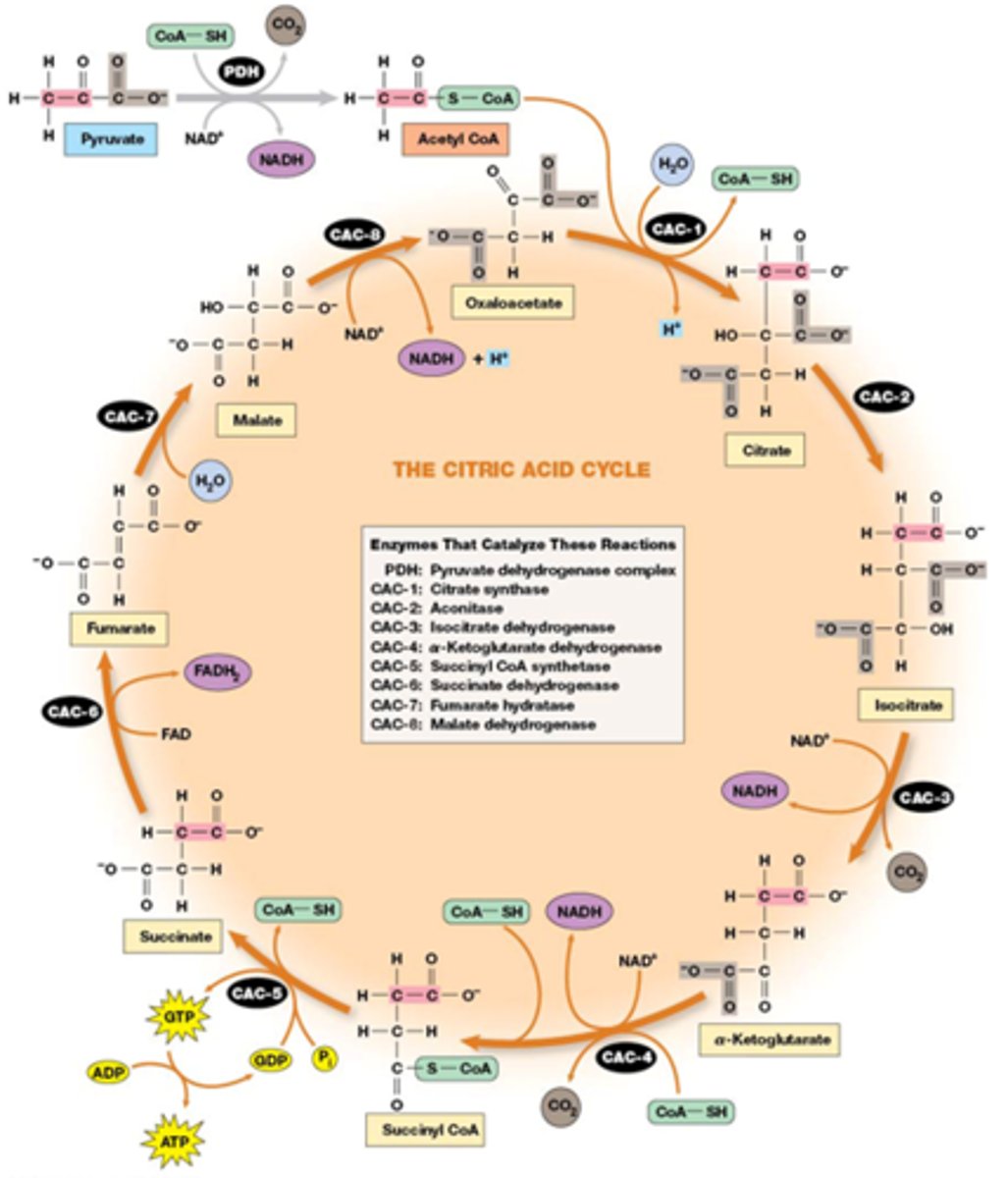
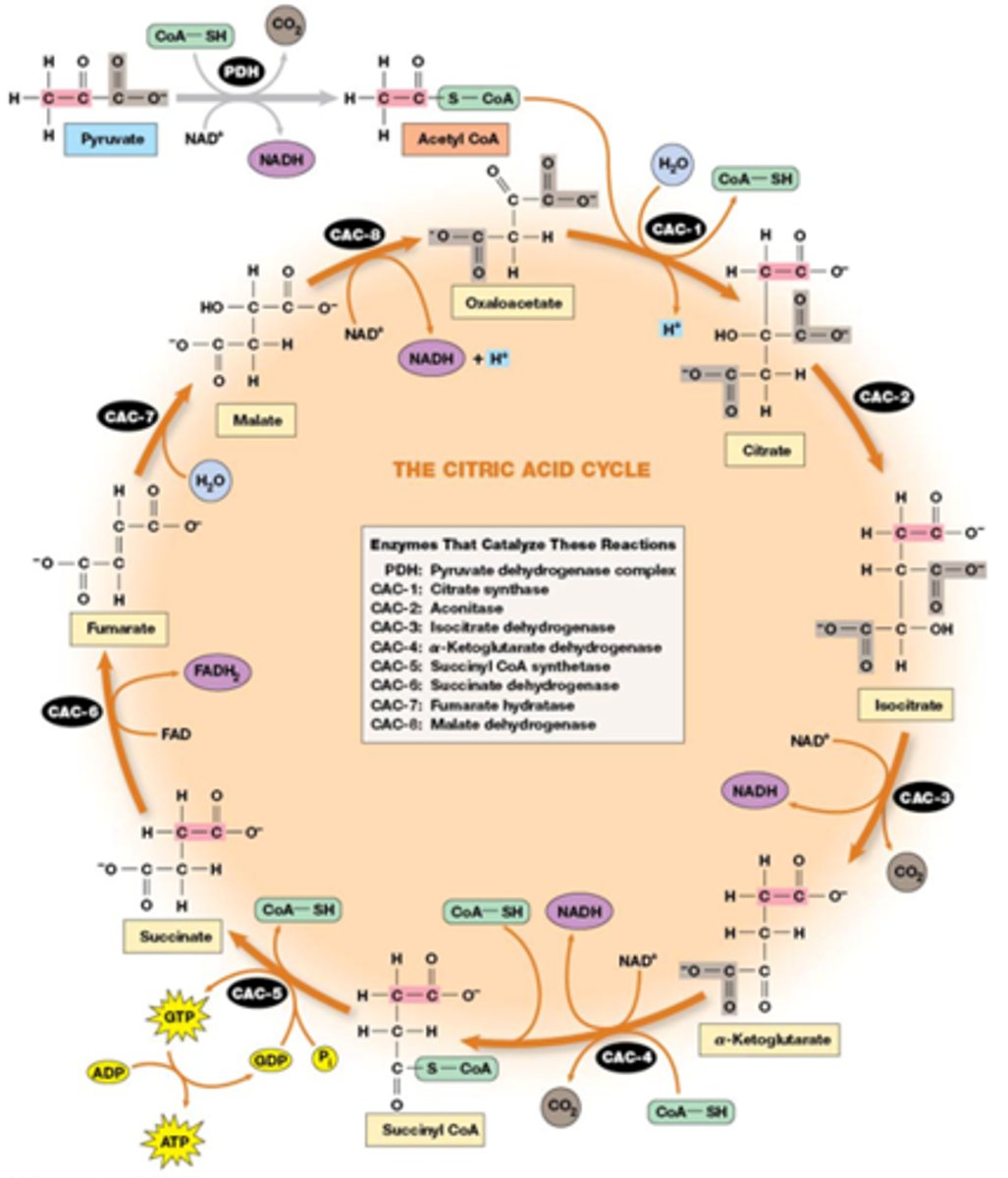
korte samenvatting van de citroenzuurcyclus, hierna wordt stap per stap het uitgelegd
1 Acetyl-CoA: Condensatie met oxaloacetaat door citraatsynthase, H+ komt vrij → Citraat
2 Citraat: Isomerisatie door aconitase, er gebeurt een hydratatie gevolgd door dehydratatie → Isocitraat
3 Isocitraat: Oxidatieve decarboxylatie door isocitraat dehydrogenase, NADH wordt gevormd, CO₂ komt vrij → α-Ketoglutaraat
4 α-Ketoglutaraat: Oxidatieve decarboxylatie door α-ketoglutaraat dehydrogenase, NADH wordt gevormd, CO₂ komt vrij → Succinyl-CoA
5 Succinyl-CoA: substrate level phoshporylation en klieving thio-esterbinding door succinyl-CoA synthetase, GTP wordt gevormd → Succinaat
6 Succinaat: oxidatie door succinaat dehydrogenase, FADH₂ wordt gevormd → Fumaraat
7 Fumaraat: Hydratatie door fumarase, water wordt toegevoegd → Malaat
8 Malaat: Oxidatie door malaat dehydrogenase, NADH + H+ wordt gevormd → Oxaloacetaat
De cyclus begint opnieuw door de toevoeging van een nieuwe acetylgroep aan oxaloacetaat.
Hoe wordt pryruvaat omgezet naar acetyl Coa + welk enzyme is hier verantwoordelijk voor?
- oxidatieve decarboxylering
- enzyme: pryruvaatdehydrogenase complex
- er wordt 1 NAD+ gereduceerd
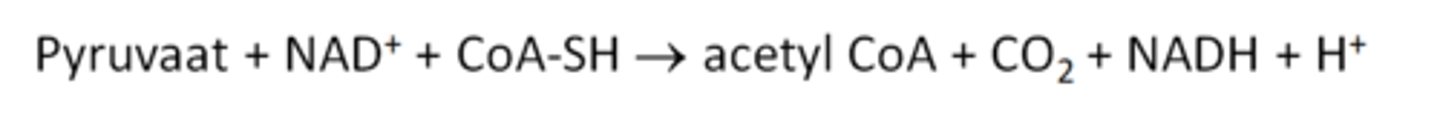
Wat is de actieve groep in acetyl CoA?
de thioesther binding tussen sulfihydril groep en de acetylgroep van pyruvaat
extra uitleg chatgpt: De thioësterbinding wordt de "actieve groep" genoemd omdat het een reactieve, energierijke binding is die de overdracht van functionele groepen mogelijk maakt en energie levert voor metabole processen.

Wat is de eerste stap van de CAC
Vorming van citraat uitgaande van oxaloacetaat (OA) en acetyl CoA (1)
Enzyme: citraat synthase (transferase)
Hydrolyse van het thio-ester levert de nodige energie voor de vorming van een nieuw molecule uitgaande van 2 precursoren.
Binding van OA aan enzyme => conformatieverandering => bindingsplaats voor acetyl CoA wordt gecreëerd
=> vorming van citryl CoA => conformatieverandering => hydrolyse van
Citryl CoA, CoA komt hierbij vrij en een H+ molecule

Wat is de 2e stap van de CAC
Isomerisatie van citraat tot iso-citraat (2)
Enzyme: aconitase
Doel: vorming van een geschikt substraat voor oxidatieve decarboxylatie
eerst een hydratatie, dan een dehydratatie en je krijgt isocitraat= een isomeer van citraat
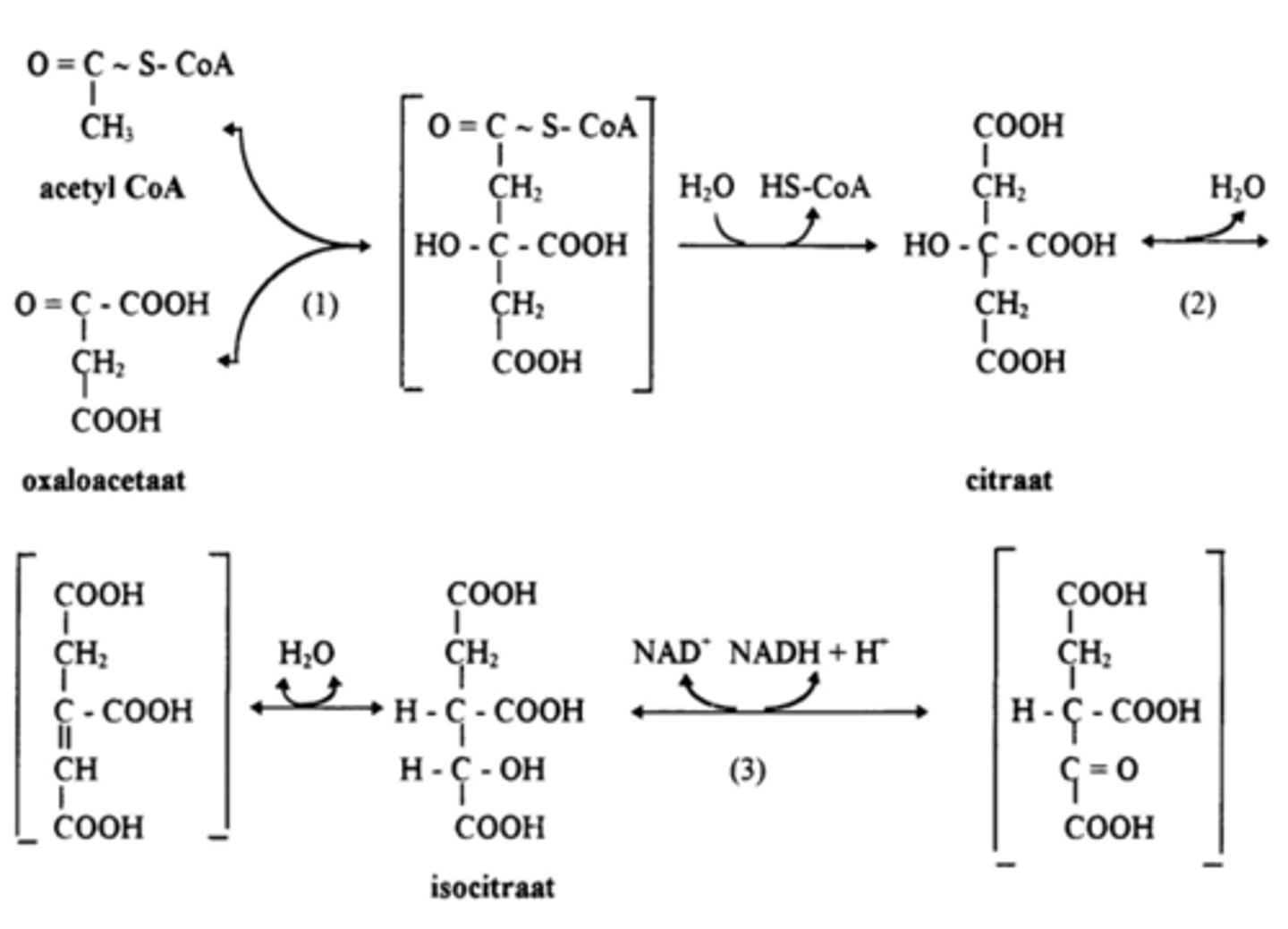
wat is de 3e stap van de CAC
oxidatieve decarboxylatie* van iso-citraat
enzyme: isocitraat dehydrogenase
->alpha-ketoglutaraat wordt gevormd
*Oxidatieve decarboxylatie is een reactie waarbij een CO₂ wordt verwijderd uit een substraat, terwijl het substraat tegelijkertijd geoxideerd wordt, deze elektronen worden overgedragen op een elektronendrager, meestal NAD⁺ of FAD, die daardoor gereduceerd worden tot NADH of FADH₂.
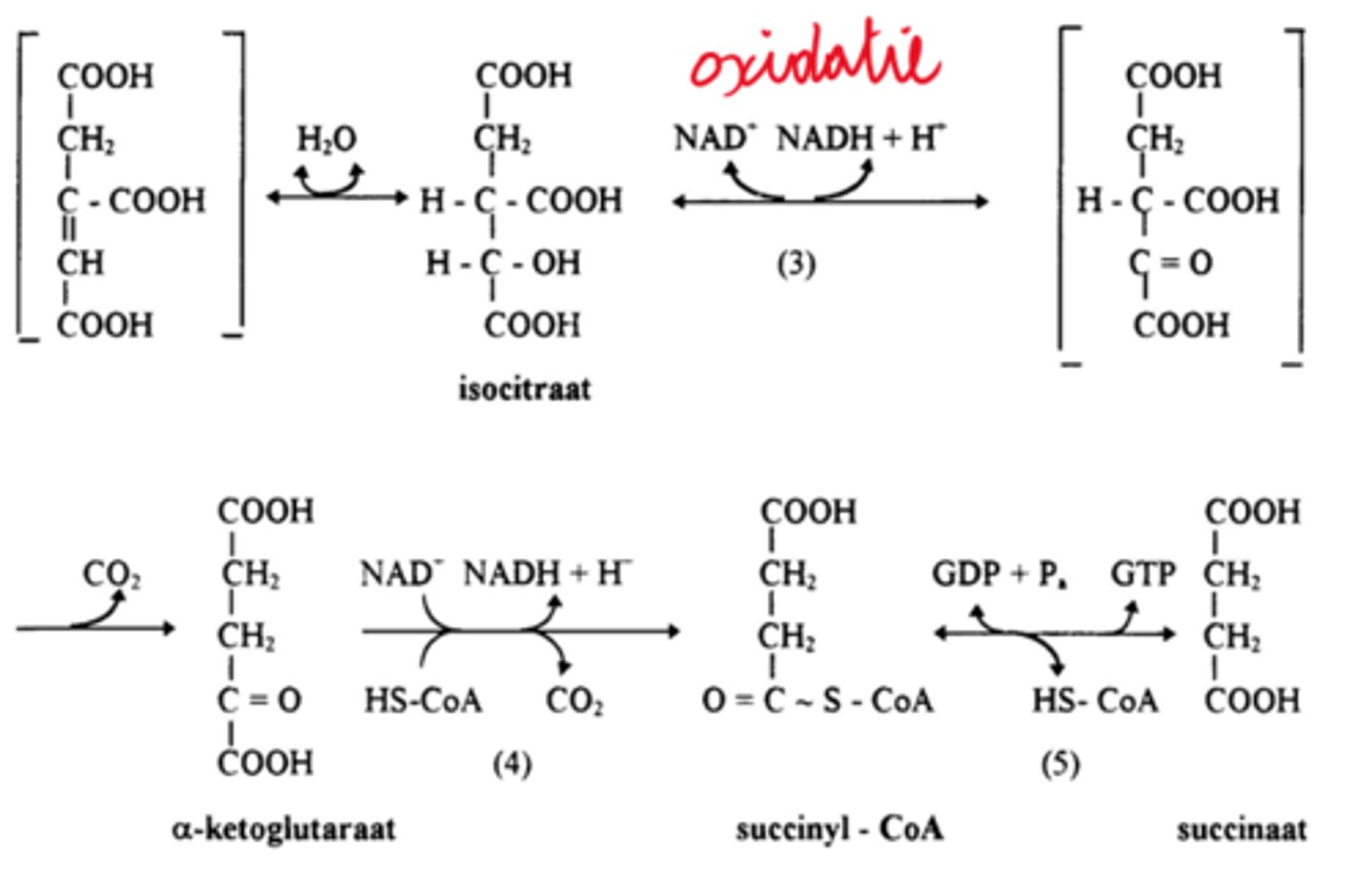
wat is de 4e stap van de CAC
Oxidatieve decarboxylatie van alpha-ketoglutaraat ter vorming van succinyl-Coa
Enzyme: alpha- ketoglutaraat dehydrogenase
extra info ter verduidelijking: De resterende vierkoolstofgroep bindt aan co-enzym A (CoA), waardoor succinyl-CoA ontstaat. Succinyl-CoA bevat een energierijke thioësterbinding (aangeduid met ~) , die in de volgende stap van de cyclus gebruikt kan worden om GTP (en vervolgens ATP) te genereren.
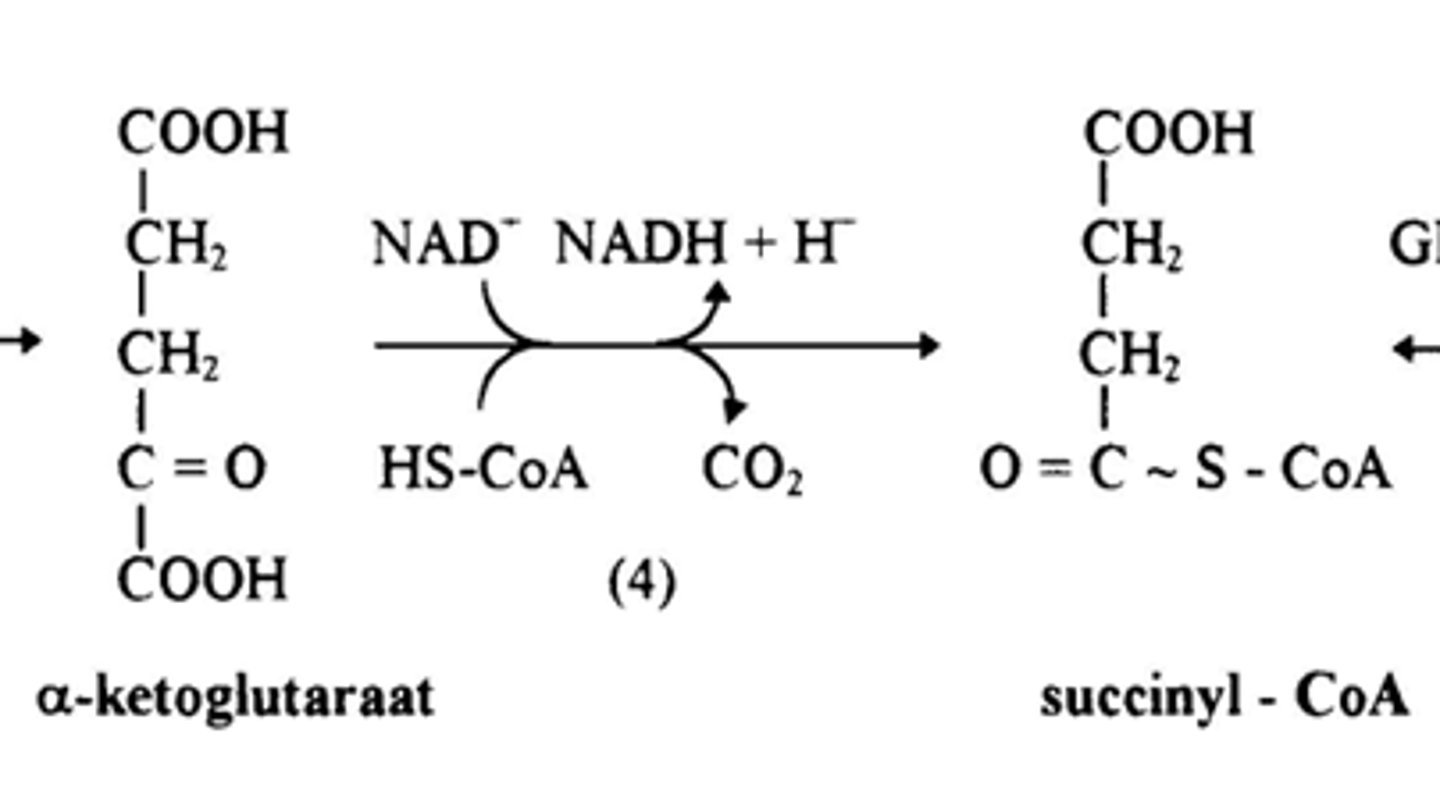
wat is de 5e stap van de CAC
Energie van klieving van de thio-ester binding (~) van succinyl- CoA wordt omgezet in fosfaat groep transfer potentieel (5)
Er gebeurt substrate level phosphorylation waarbij GTP ontstaat, deze wordt nadien omgezet in ATP
het molecule dat overblijft noemt men succinaat
Enzyme: succinyl CoA synthetase

Welke bindingen gaan verbroken worden bij de reductie van NAD+ en FAD (er gaan twee veel voorkomende situaties zijn)
1) bij NADH => koolstof met een waterstof en hydroxyl- groep
2) FADH2 => koolstof met twee waterstoffen
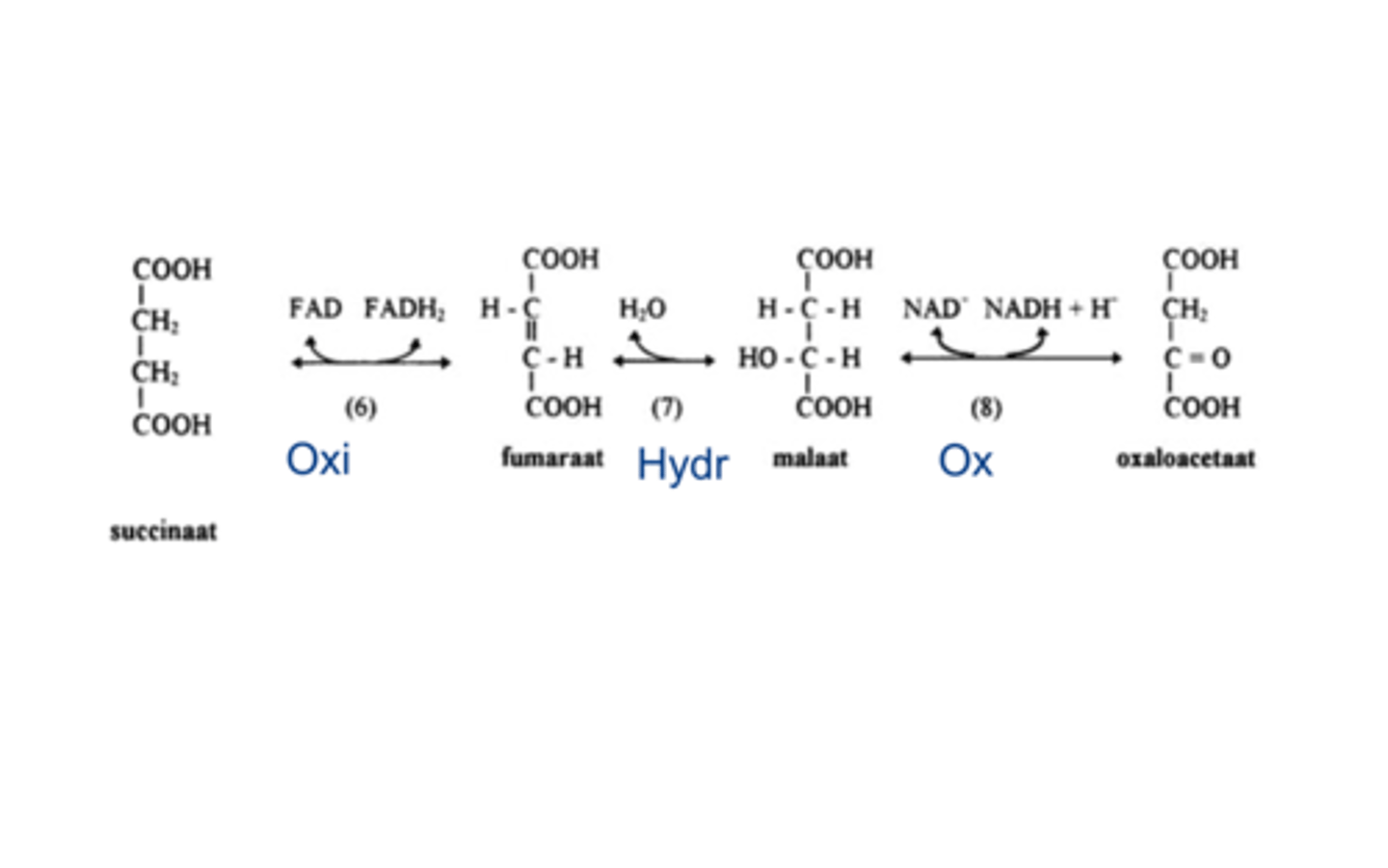
wat is de 6e stap van CAC
Regeneratie van oxaloacetaat in 3 opeenvolgende stappen:
oxidatie (6), hydratatie (7), oxidatie (8).
(6) enzyme: succinaat dehydrogenase (geïntegreerd in de binnenste mitochondriale membraan en onderdeel van de elektronen transport keten)
FAD is elektronen acceptor want ∆G is onvoldoende om NAD+ te reduceren.
FADH2 dissocieert niet van het enzyme (blijft op het enzyme aanwezig terwijl NADH’s vrij kunnen bewegen in de oplossing)
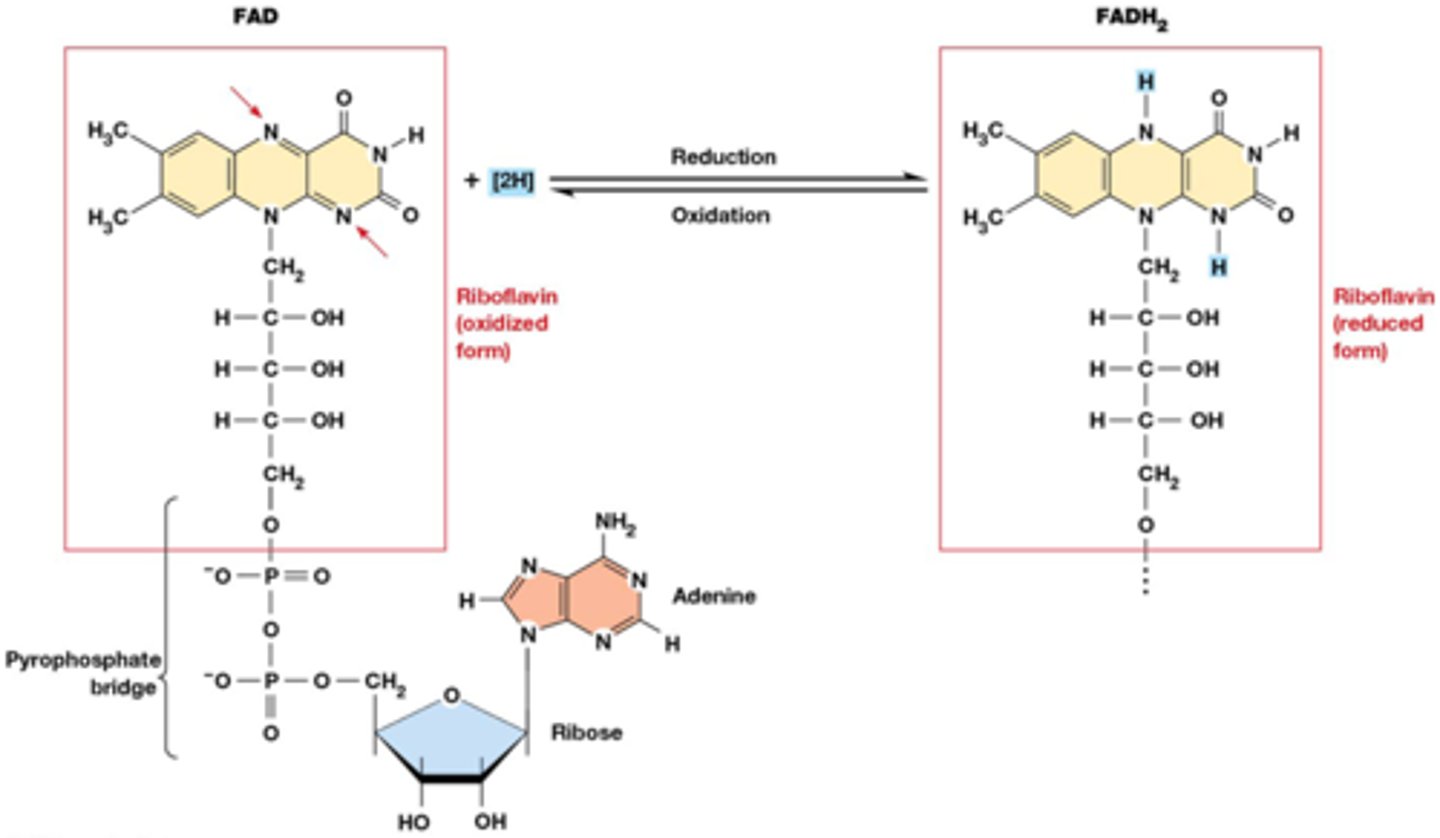
Geef de structuur en volledige naam van FAD
1) flavine adenine dinucleotide
2) zie foto
wat is de 7e stap van CAC
hydratatie van fumeraat ter vorming van malaat
enzyme: fumarase (katalyseert een stereospecifieke trans additie van H+ en OH-)
Regeneratie van oxaloacetaat in 3 opeenvolgende stappen:
oxidatie (6), hydratatie (7), oxidatie (8).
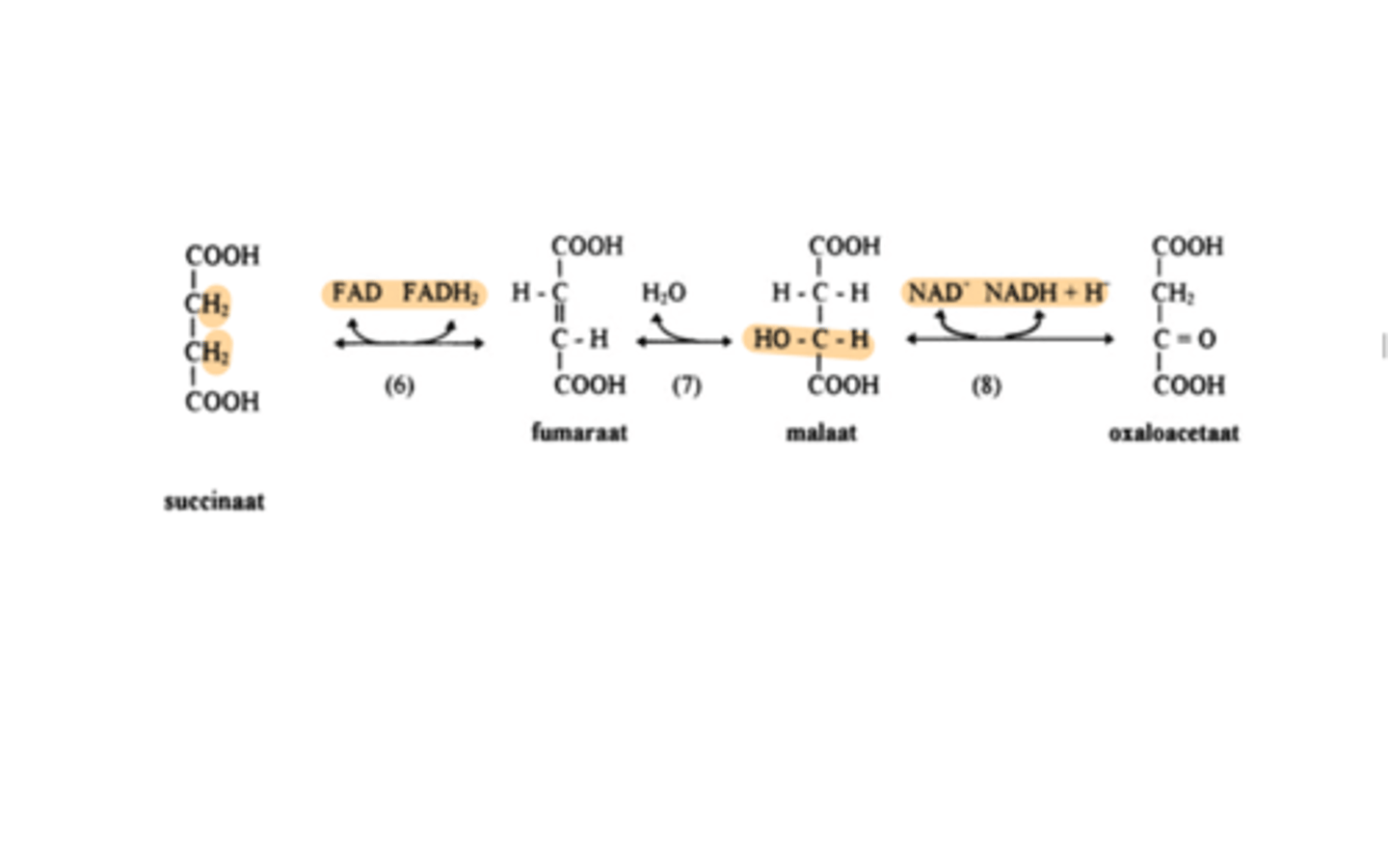
Wat is de 8e stap van CAC
oxidatie van malaat ter vorming van oxaloacetaat
enzyme (8): malaat dehydrogenase
NAD+ is elektronen acceptor.
H+ komt ook vrij
∆G°' = 7,1 kcal/mol
Reactie spontaan omwille van de consumptie van de producten die heel snel gebeurt (OA in CAC en NADH in elektronen transport keten)
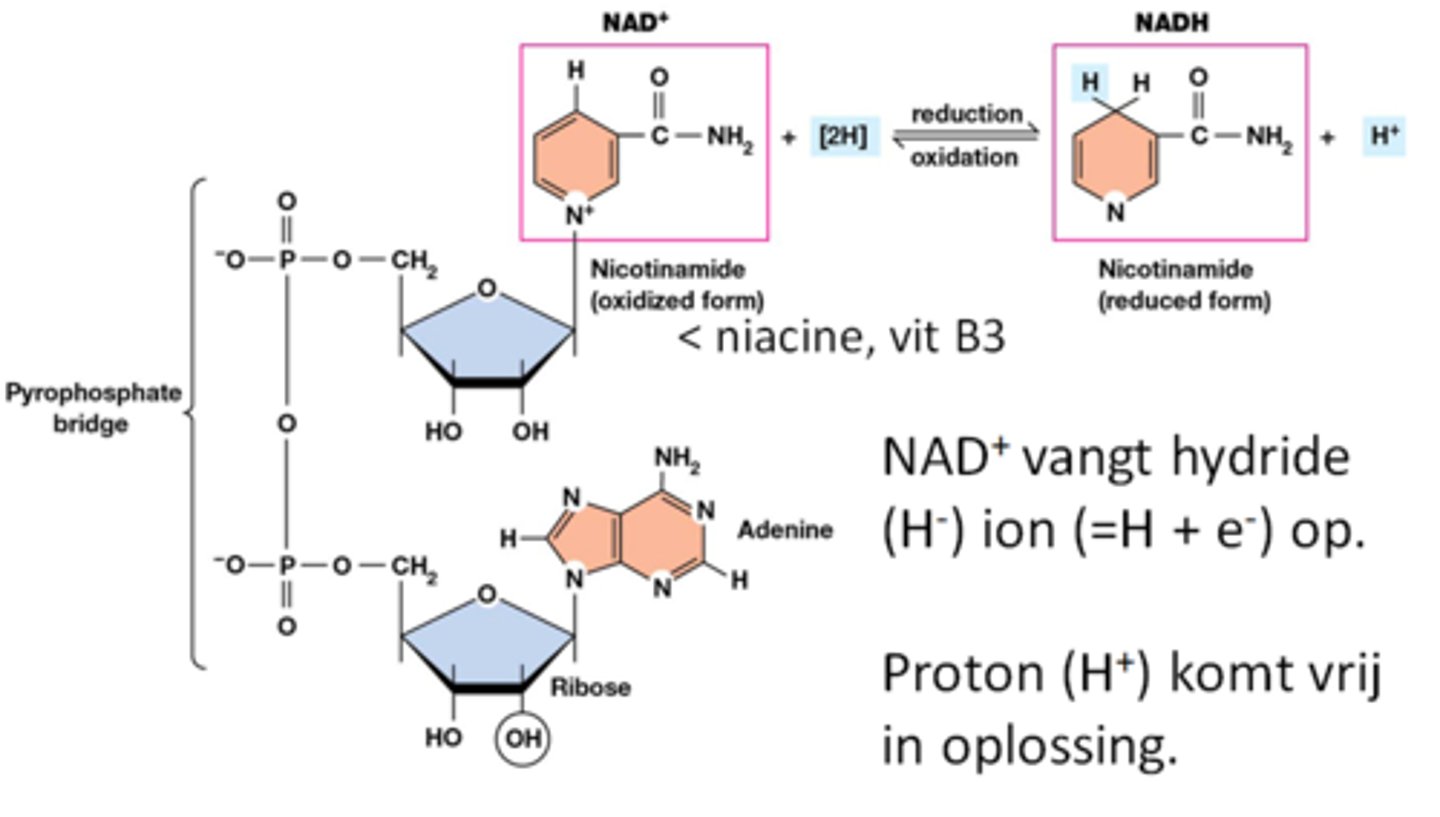
Geef de naam en structuur van NADH/NAD+
nicotineamide adenine dinucleotide
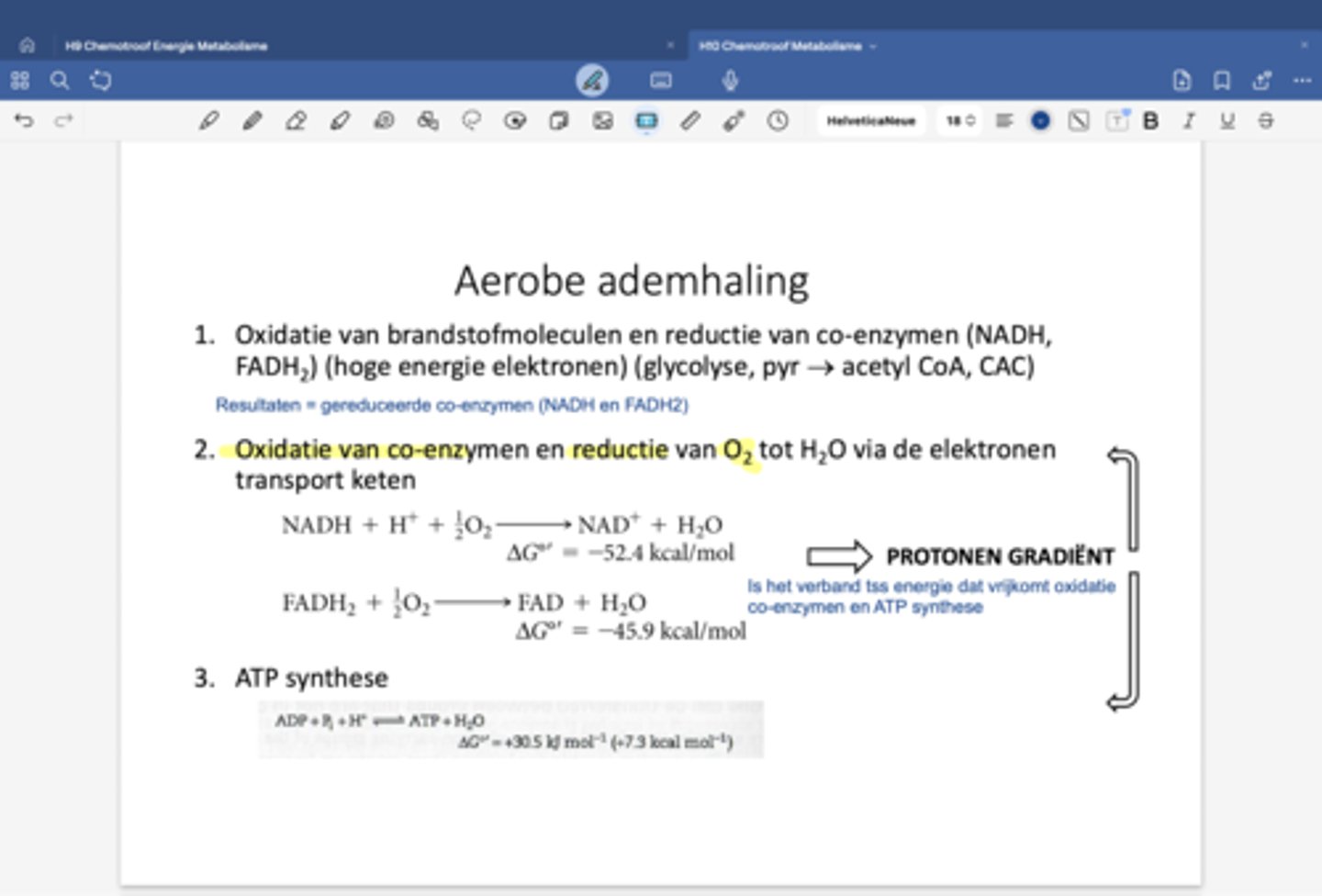
geeft de balans van de glycolyse, de decarboxylering van pyruvaat (2x) en de citroenzuurcyclus (2x) van de aerobe ademhaling
in totaal 4 oxidaties
2 oxidatieve decarboxylaties in de CAC, als je vertrekt van pyruvaat dan zijn het er 3
Energie van GTP en ATP is gelijk dus GTP wordt omgezet naar een ATP

Wat zijn de mechanismes om decarboxylatie van pyruvaat te regelen
3 allosterische inhibitors
- Acetyl CoA
- NADH
- ATP
3 activatoren
- CoA
- NAD+
- AMP (veel AMP duidt aan dat cellen veel energie nodig hebben)
omkeerbare covalente modificatie:
PDH kinase en PDH fosfatase

Waarom heeft decarboxylatie zoveel regelmechanismes?
Het is een onomkeerbare stap, wanneer acetyl CoA is aangemaakt kan men niet meer teruggaan naar suiker
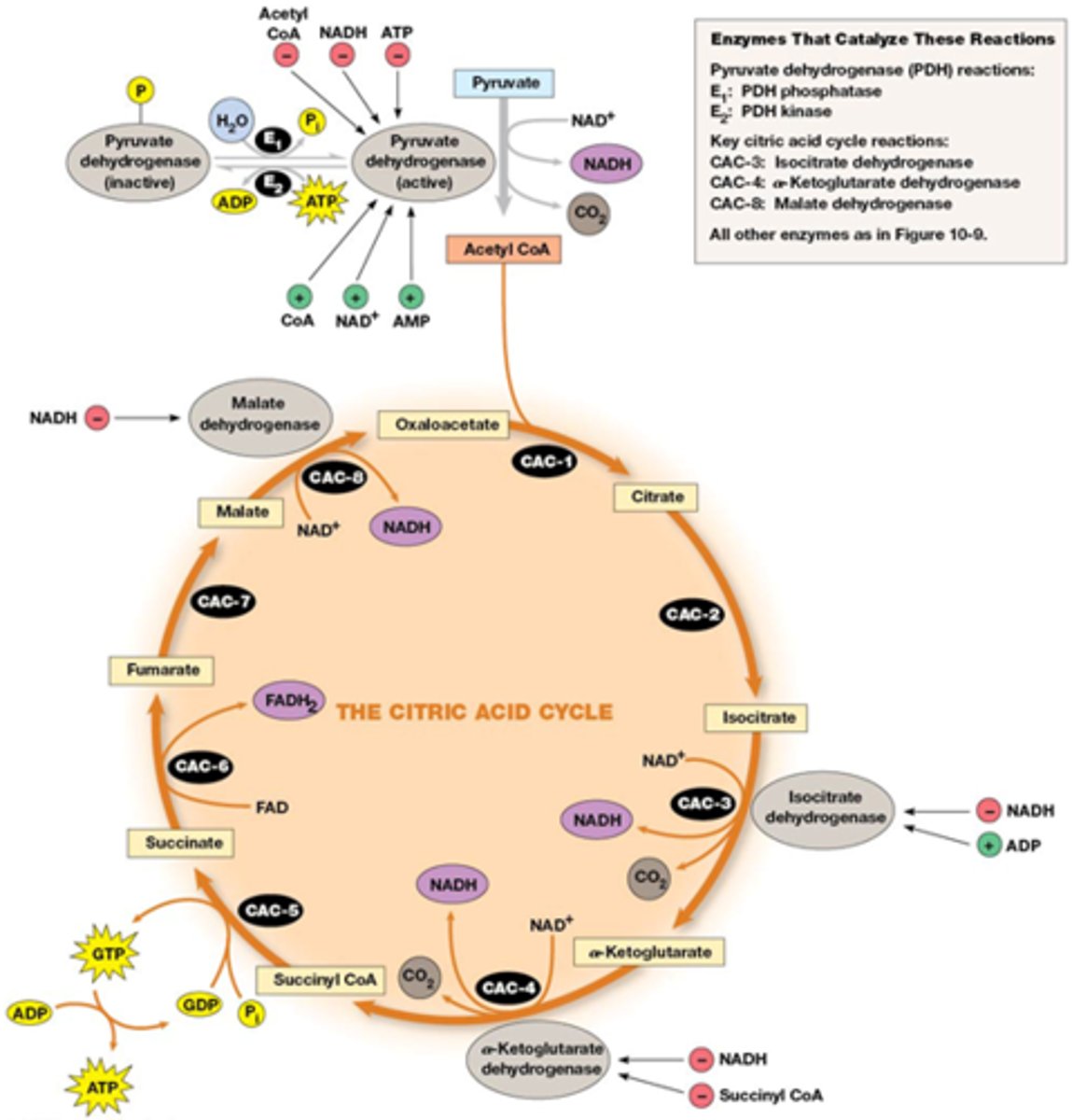
Hoe gebeurt de regeling van de CAC
- Allosterische stimulatie door ADP
- inhibitie door NADH
- inhibitie door succinyl CoA, ATP, NADH
cfr figuur
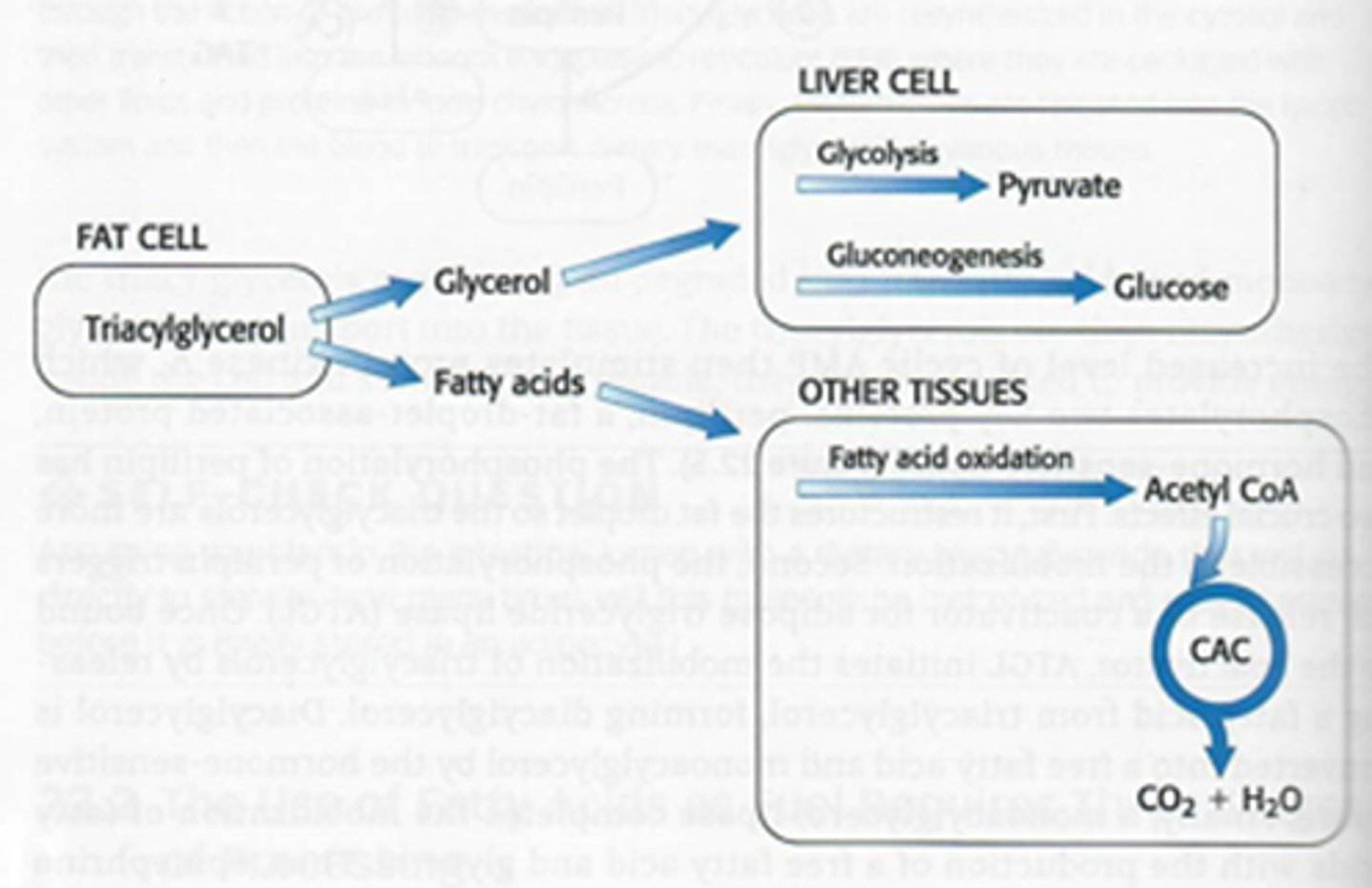
Waar gaan triglyceriden in worden omgezet bij glycolyse (1) en gluconeogenese (2)
1) pyruvaat
2) glucose
Hoe oxideren we vetzuren?
Door het te activeren, dit houdt in dat het gekoppeld wordt aan CoA
vorming van vetzuur acetyl CoA kost 1 ATP maar 2 fosfoanhybride bindingen worden verder gehydrolyseerd tot AMP

Hoe gebeurt de Beta oxidatie van vetzuren
1) oxidatie (er komt FADH2 vrij)
2) hydratie
3) oxidatie (er komt NADH + H+ vrij)
4) thiolyse (hydrolyse van acetyl coA)
->je gaat uw vetzuur afbreken tot acetyl coenzyme A's
->gebeurt in mitochondriale matrix
(ter info: stap 1,2,3 komt ook voor in de CAC om van succinaat naar oxaloacetaat te gaan)
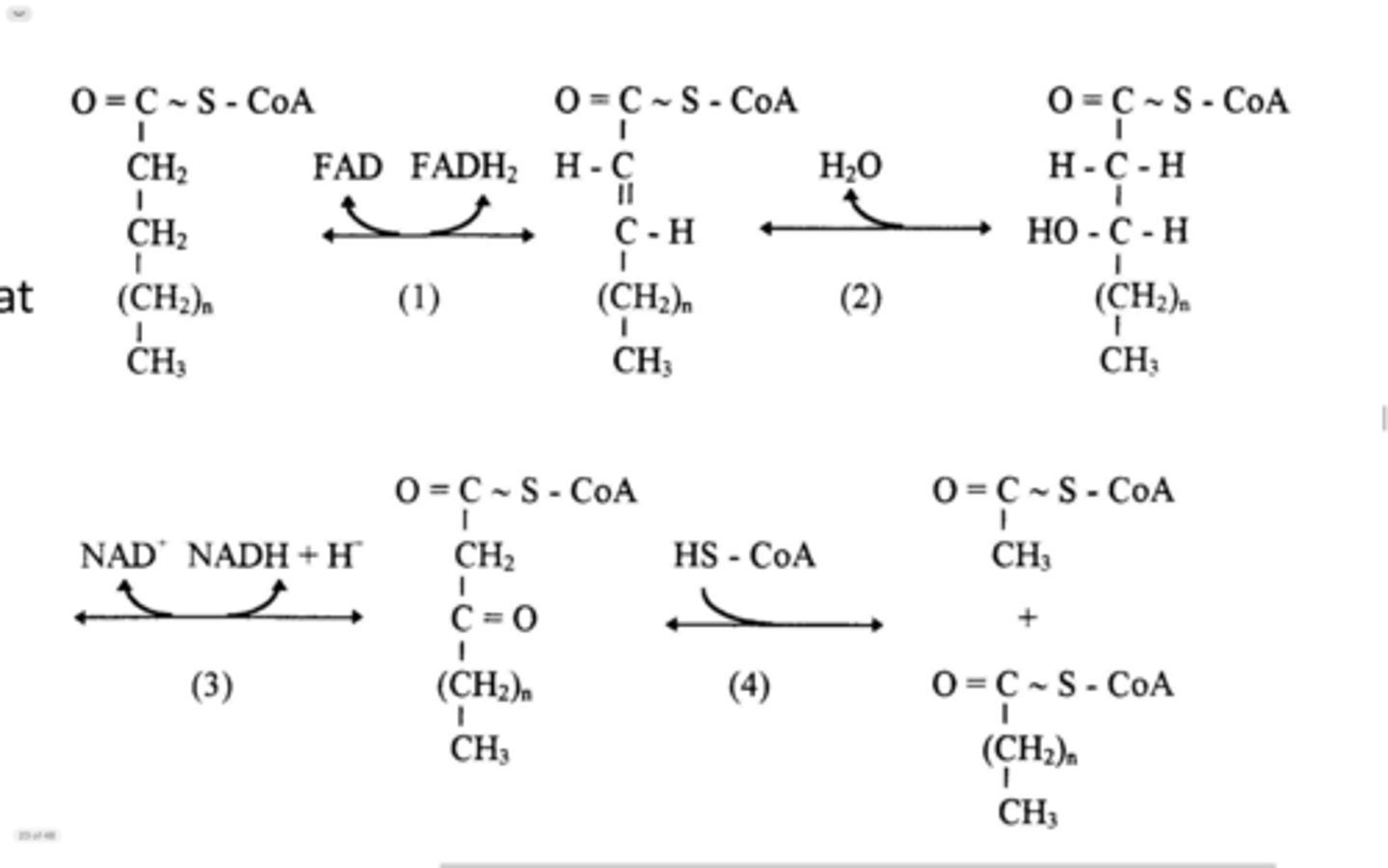
veel betere foto van de beta oxidatie
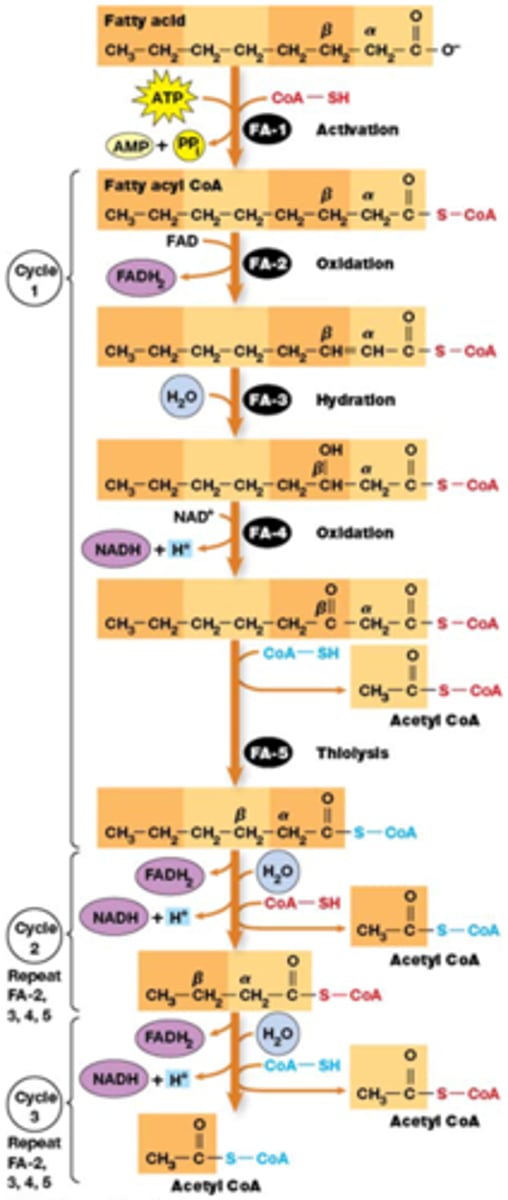
Wat is de algemene formule voor de totale ATP productie door eenverzadigd vetzuur met een even aantal (n) C atomen ?
Total ATP =
n/2 acetylCoA x 12 ATP/acetylCoA +
(n/2 - 1) FADH2 x 2 ATP/ FADH2 +
(n/2 - 1) NADH x 3 ATP/NADH
- 1
=8,5 n - 6
n/2 - 1= # cycli van beta oxidatie
TCA* cyclus => 1 ATP + 3 NADH + 1 FADH2 => 12 ATP
ß-oxidatie van vetzuren en de laatste stappen van de TCA cyclus zijn zeer gelijkend !!!
*nog een extra synoniem voor de citroenzuurcyclus/krebcyclus
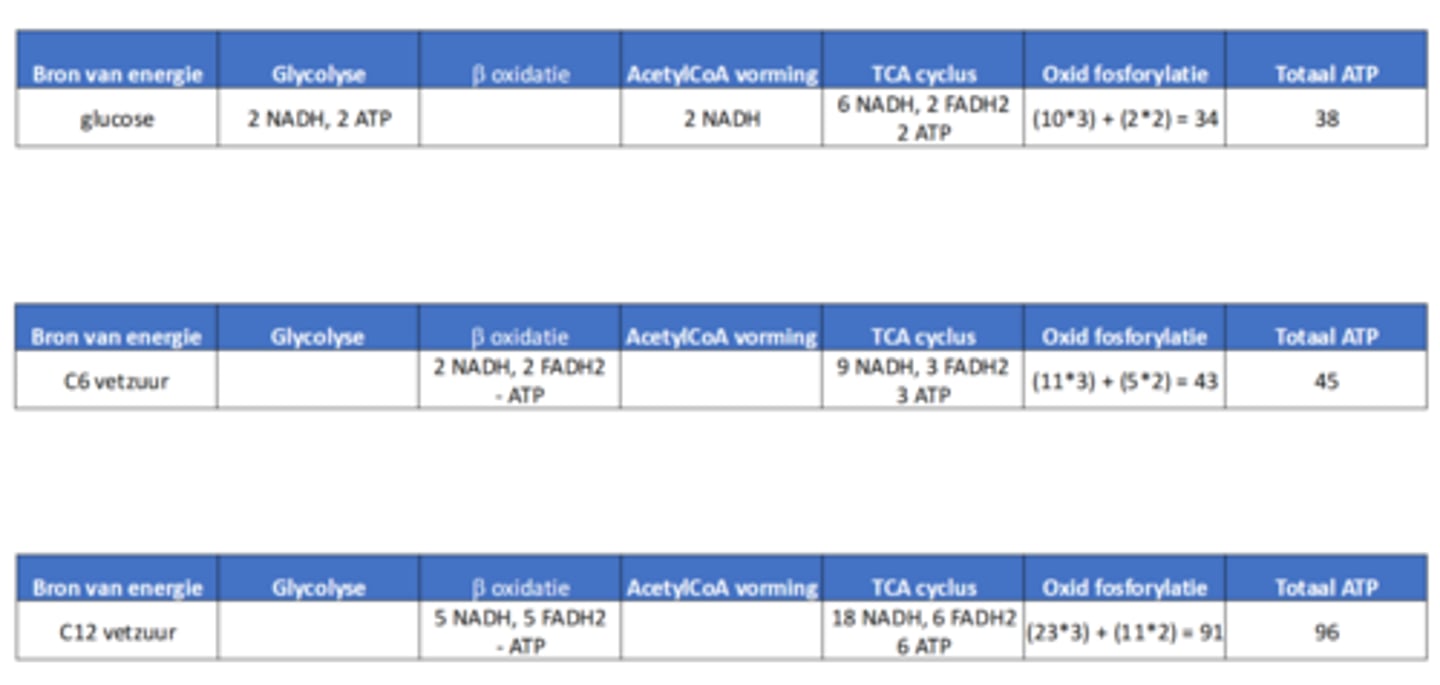
hoeveel mol ATP levert 1 mol vetzuur maximaal op? glucose staat er ook bij als herhaling
Wat is de vorming van ketonlichamen
In de lever, tijdens een vastenperiode, dieet laag in koolhydraten, langdurige inspanning, onbehandelde type 1 diabetes …
-> Oxaloacetaat (OA) wordt via de gluconeogenese omgezet in glucose.
-> OA is niet beschikbaar voor condensatie met acetyl CoA.
-> acetyl CoA wordt omgezet tot ‘ketonlichamen’ (acetoacetaat, hydroxybutyraat (reductie van acetoacetaat) en aceton (decarboxlatie van acetoacetaat)
-> Ketonlichamen komen vanuit de lever in het bloed:
--> Normale bron van energie in hartspier en niercortex
--> Noodbron van energie in hersenen (vasten en diabetes)(normale bron = glucose)
Overmatige vorming van ketonlichamen (zuren) kan verzuring van het bloed en weefselschade veroorzaken ->metabole acidose
Wat zijn de twee soorten aminozuren dat gebruikt worden als bron van energie + enkele voorbeelden
1) acetyl coA of acetoacetyl CoA (ketogene aminozuren)
2) pyruvaat alpha-ketogluteraat, succinyl CoA, fumaraat, oxaloacetaat (glucogene aminozuren)
Wat zijn de drie meest gekende ketonlichamen
1) aceton
2) acetonacetaat
3) beta-hydroxybutyraat
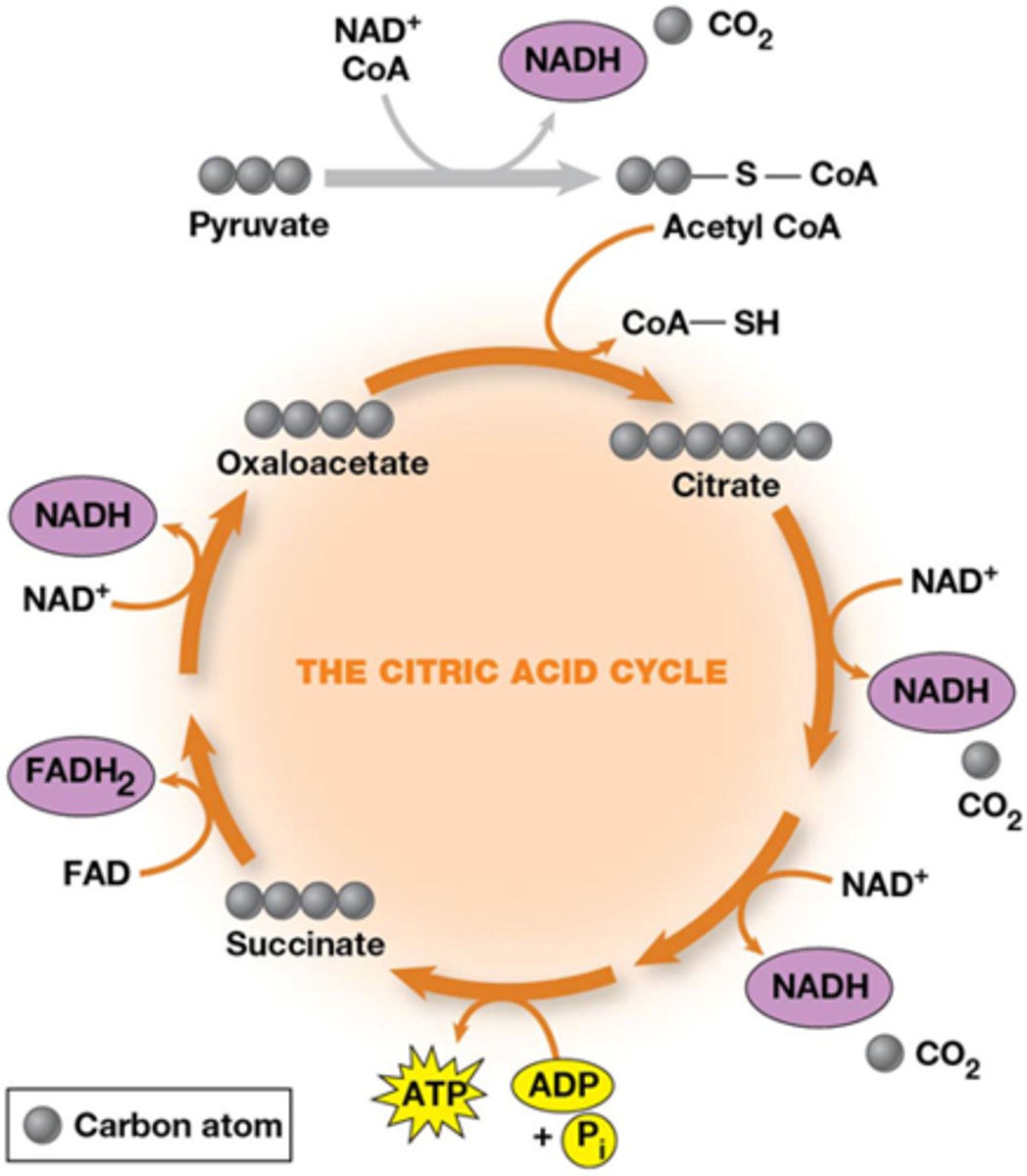
Leg de twee functies van de CAC uit
katabole functie: oogsten van hoge energetische elektronen vanuit brandstofmolecule (oxidatie)
anabole functie: bron van precursoren van aminozuren, nucleotide base, porfyrin vetzuren, ...
oxaloacetaat is een belangrijke precursor van glucose
OA wordt telkens geregenereerd niet de novo gevormd!->GEEN NETTO VORMING VAN OA
Amfibool= zowel katabool als anabool
Waarom gaan plantencellen netto AO aanmaken?
Nut: bij ontkiemen van olierijke zaden (vb. zonnebloem) moet olie omgezet worden naar koolhydraten totdat fotosynthese kan starten. Olie ('vet') bevat meer energie/g dan koolhydraten, het is meer massa-efficiënt om 'vet' te
stockeren dan om koolhydraten te stockeren.
Wat is het verschil tussen CAC en de glyoxylaat cyclus
Verschillen met CAC:
-in glyoxysomen (soort peroxisoom in planten)
-geen decarboxyleringen
-input van 2 moleculen acetyl CoA
per cyclus
-netto synthese van succinaat
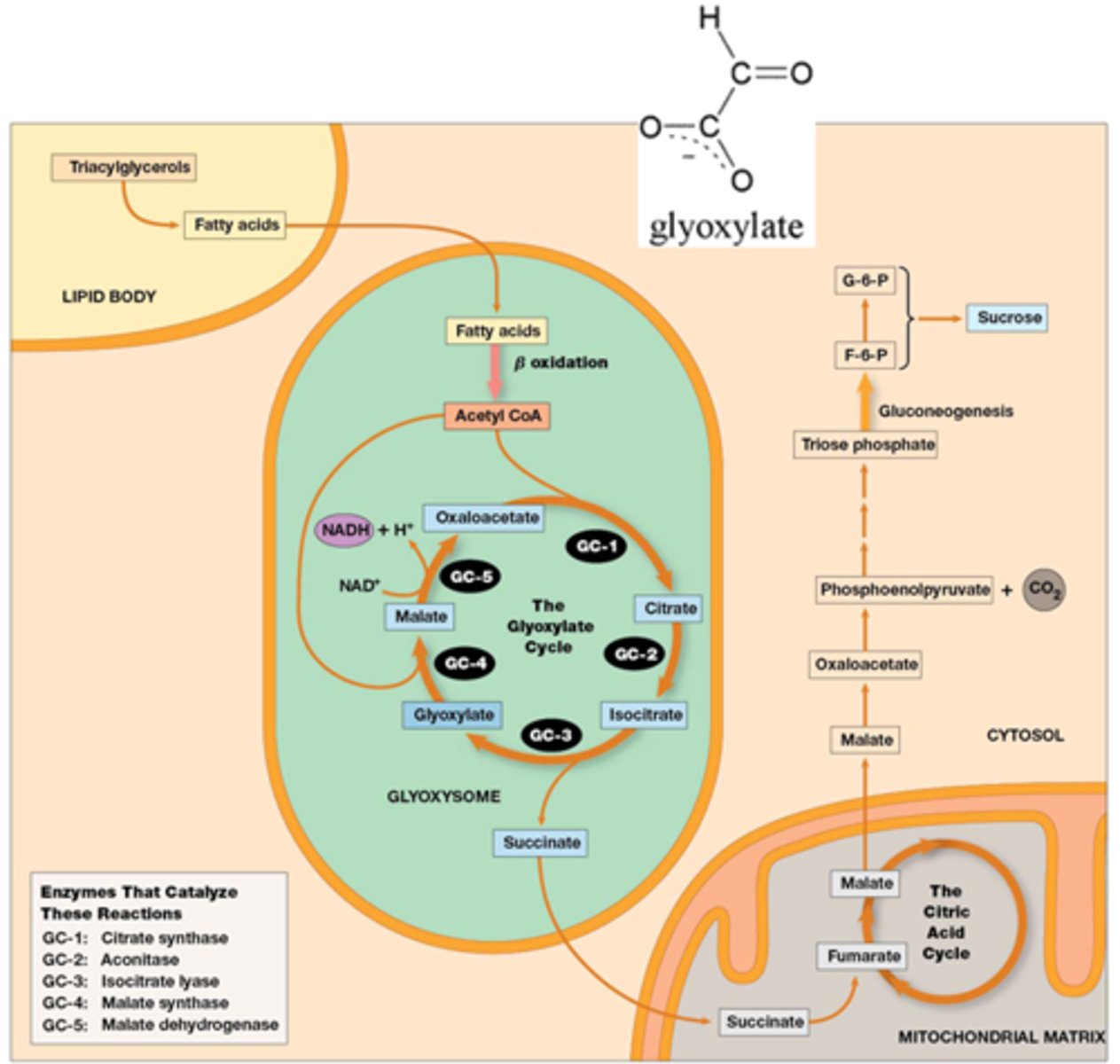
In wat gaat isocitraat worden gesplist tijdens de glyoxylaat cyclus?
1) succinaat C4
2) glyoxylaat
Welke stof gaat het meeste energie leveren: vet of koolhydraten?
vetten zijn meer gereduceerd dan koolhydraten (1g vet geeft ong 2x meer energie dan 1g koolydraten)
cfr werkzittingen
HC2 vanaf hier!
Wat zijn carriers?
Integrale membraaneiwitten met specifieke prostetische groepen (Co-enzyme Q is GEEN eiwit!) in binnenste mitochondriale membraan
elektronen transport keten: een geordende sequentie van (elektronen)carriers
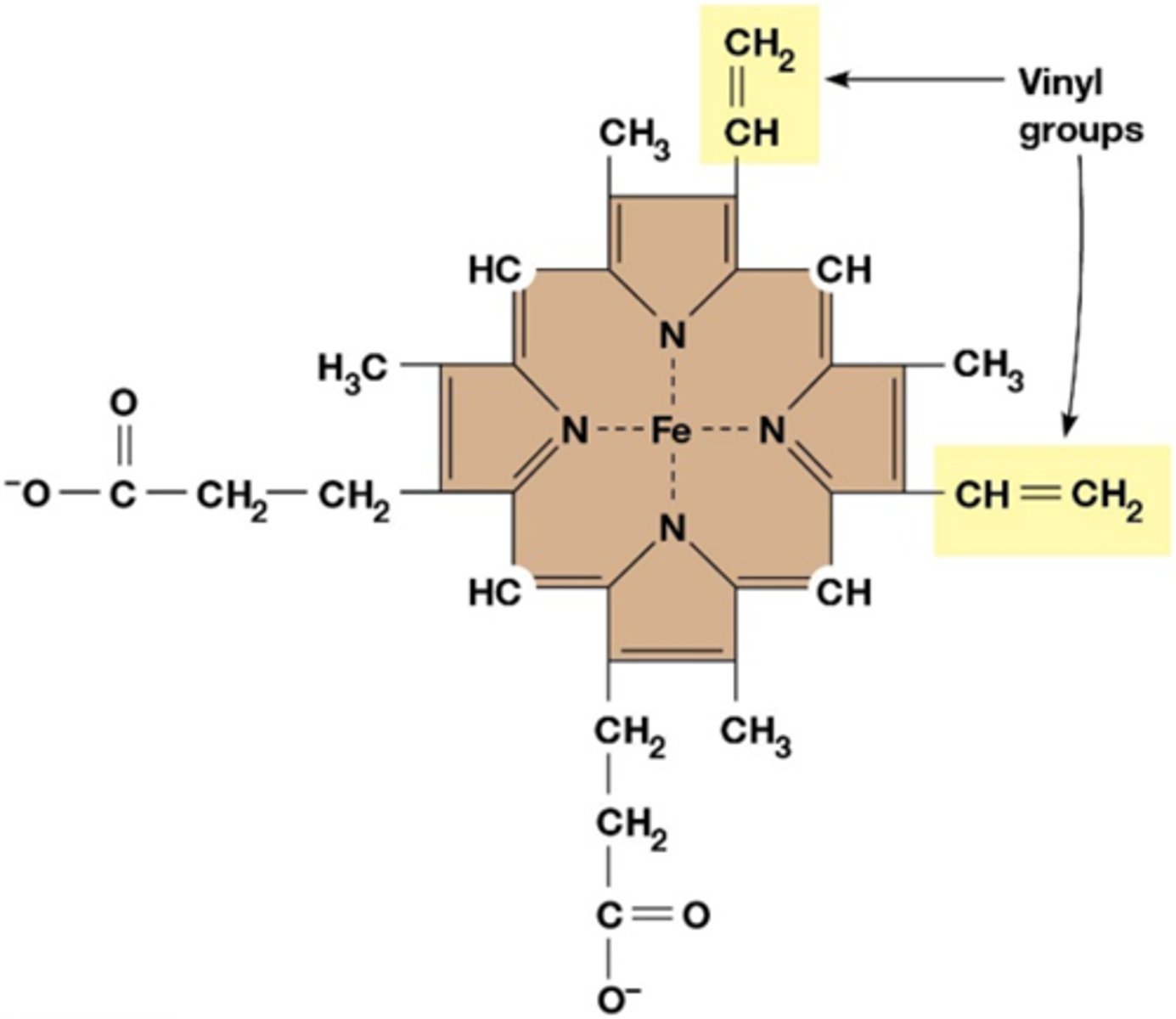
Wat is een heemgroep?
Een heemgroep is een porfyrinering met een centraal ijzeratoom (Fe), dat elektronen kan transporteren door te wisselen tussen Fe²⁺ en Fe³⁺.
Het kan covalent (via vinylgroepen) of niet-covalent aan het eiwit gebonden zijn, afhankelijk van het type eiwit.
Welke soorten carriers bestaan er?
ze verschillen in het feit dat ze enkel elektronen kunnen capteren of ook protonen
1.Flavoproteïnen (FAD of FMN): elektronen + protonen
2.Fe-S proteïnen (niet-heem ijzer: Fe3+ <-> Fe2+ ): elektronen opgevangen door ijzer
3.Cytochromen (heemgroep, ijzer: Fe3+ <-> Fe2+ ): elektronen
4.Cu bevattende cytochromen (heemgroep, bimetallisch Fe-Cu centrum; Fe3+ <-> Fe2+ , Cu2+ <-> Cu+): elektronen
5.Co-enzyme Q of ubiquinon (geen eiwit!): elektronen + protonen
verschil tussen 2 en 3: bij cytochromen zit ijzer in de heemgroep, bij Fe-S proteïnen niet
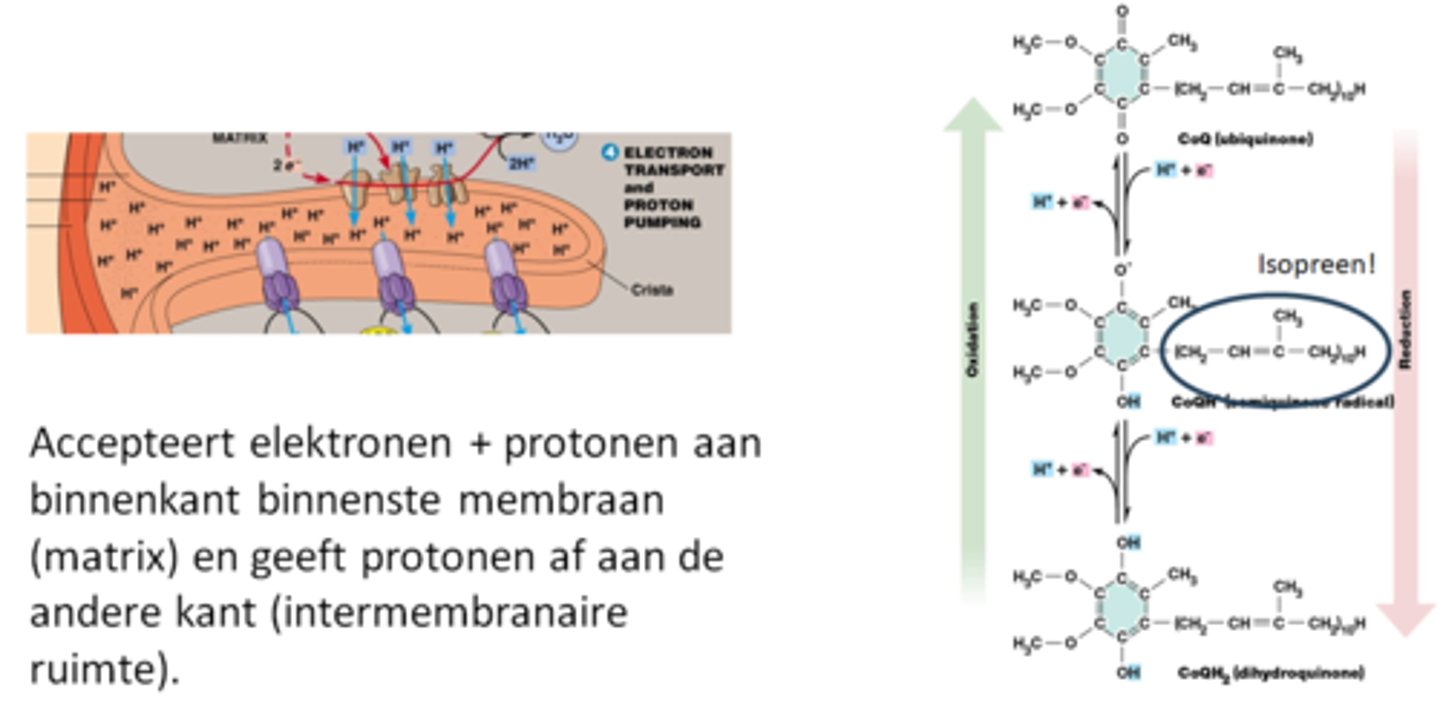
structuur van co-enzyme Q
herhaling hoofdstuk 3:
Terpenen of isoprenoïden worden gevormd uitgaande van isopreen (C5 molecule)
Vb. vitamine A, dolicholen (activering suikers), co-enzyme Q (elektronen carrier), …
Hoe zijn de eiwitten geordend in het binnenste mitochondriaal membraan? Via welke grootheid?
Ze zijn geordend op basis van hun affiniteit voor elektronen.
De standaard reductie potentiaal (E°') van een elektronen ‘carrier’ reflecteert de affiniteit voor elektronen.
-Hoge affiniteit voor elektronen gaan later in de elektronenketen voorkomen
-lagere affiniteit gaat vroeger in de elektronenketen voorkomen
zie tabel: alles is berekend op pH 0 maar dit veranderd wel iets aan de waarden maar niet aan de volgorde van de carriers

Wat kan je leren uit de tabel met standaard reductie potentialen?
je kan een deelreactie met een lagere affiniteit voor elektronen combineren met eentje met een hogere affiniteit voor elektronen
->spontaan elektronen overdragen
bv NADH gaat graag zijn elektronen afgeven aan O2

wat is de relatie tussen ∆G°' en ∆E°'?
als ∆E°' positief is, dan is ∆G°' negatief en krijg je een exergonisch proces
∆E°' en ∆G°' is een maat van de thermodynamische spontaneïteit voor een redoxreactie onder standaard condities.
foto: 1,136 komt uit het vorige kaartje (en die waarden kwamen uit de tabel)

foto van de elektronen transport keten
elektronen worden via heel veel exergonische processen uiteindelijk overgedragen naar O2 -> reduceert dan tot water
je ziet ook op deze afbeelding hoe de carriers geordend zijn in de ademhalingscomplexen van het binnenste mitochondriaal membraan
ademhalingscomplexen: de bruine ovalen, je hebt er dus 4
Je ziet op deze afbeelding ook dat succinaat dehydrogenase een buitenbeentje is
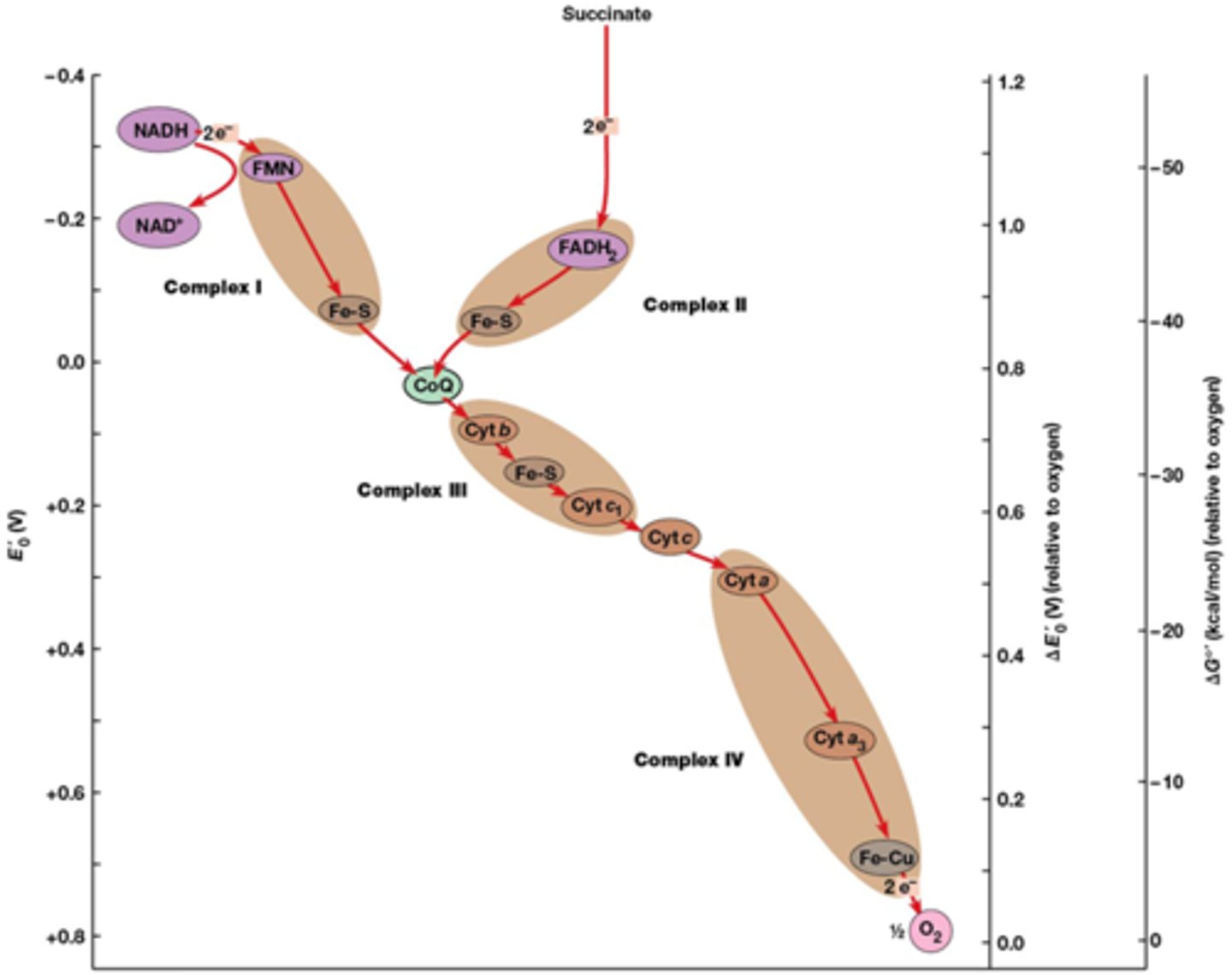
Wat is een ademhalingscomplex?
een eiwitcomplex in het binnenmembraan van mitochondriën dat betrokken is bij de elektronentransportketen.
Het zijn protonpompen die dus kunnen zorgen voor een protonengradient. Deze gradiënt drijft de productie van ATP aan via het enzym ATP-synthase.
Wat zijn de 4 ademhalingscomplexen?
2 elektronen volgen dit pad:
Complex I: NADH- coenzyme Q oxidoreductase
NADH levert 2 elektronen en 1 proton af.
De elektronen worden overgedragen aan co-enzym Q
Tijdens dit proces worden 4 protonen van de matrix naar de intermembranaire ruimte gepompt.
Complex II: Succinaat dehydrogenase
Bevat FADH₂ als prosthetische groep.
De 2 elektronen die vrijkomen omzeilen complex I, waardoor er minder protonen worden gepompt: in plaats van 10 protonen (bij NADH), worden er slechts 6 protonen (bij FADH2) in totaal verplaatst.
Complex III: Co-enzym Q-cytochroom C oxidoreductase
Verplaatst 4 protonen van de matrix naar de intermembranaire ruimte.
Complex IV: Cytochroom C oxidase
Cytochroom C draagt elektronen over aan zuurstof via cytochroom C oxidase.
Hierbij worden per cytochroom C 2 protonen naar de intermembranaire ruimte gepompt.
Zuurstof wordt gereduceerd tot water.
Om een volledige zuurstofmolecule (O₂) te reduceren, moet de reactie tweemaal plaatsvinden.
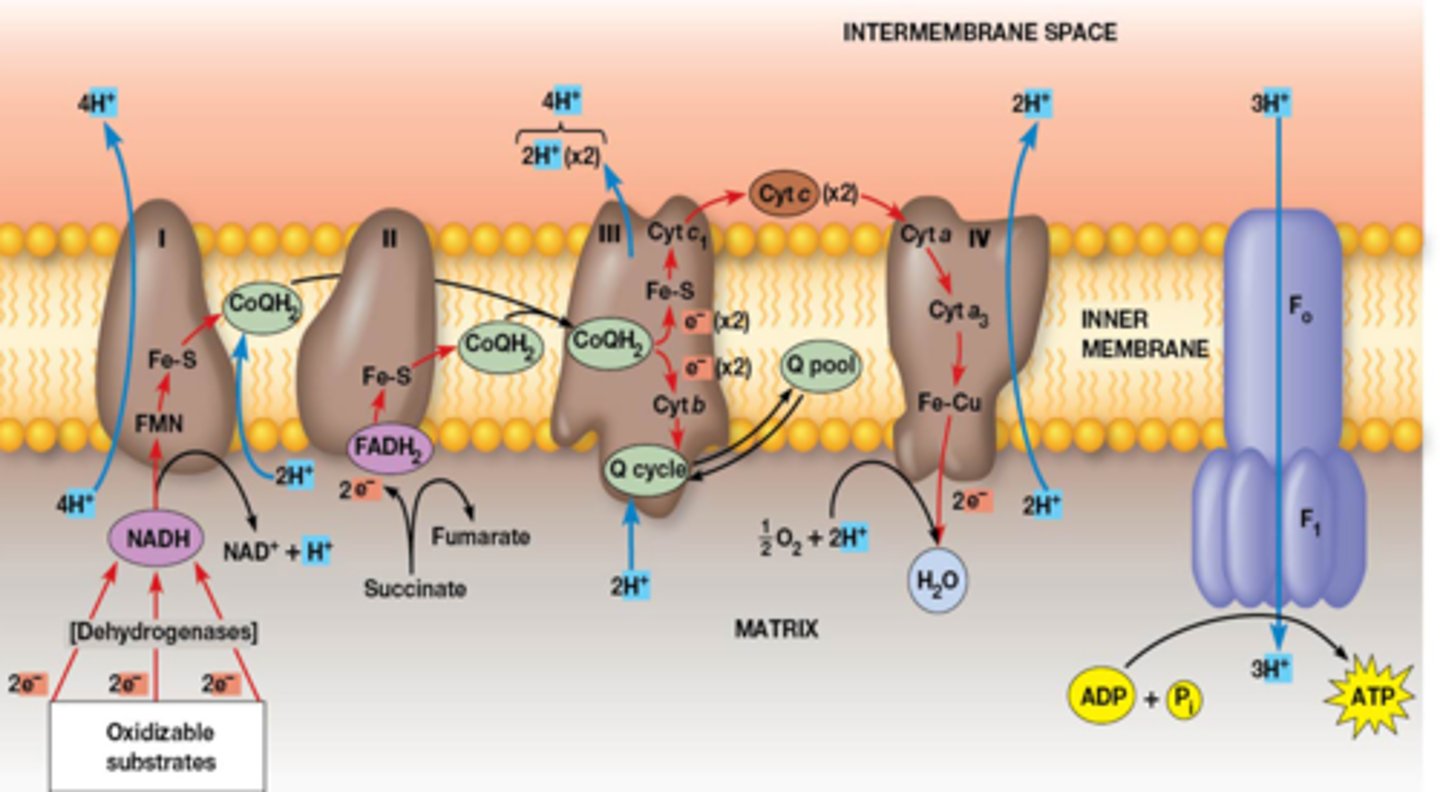
volledige foto van die slide, met extra reactievergelijkingen
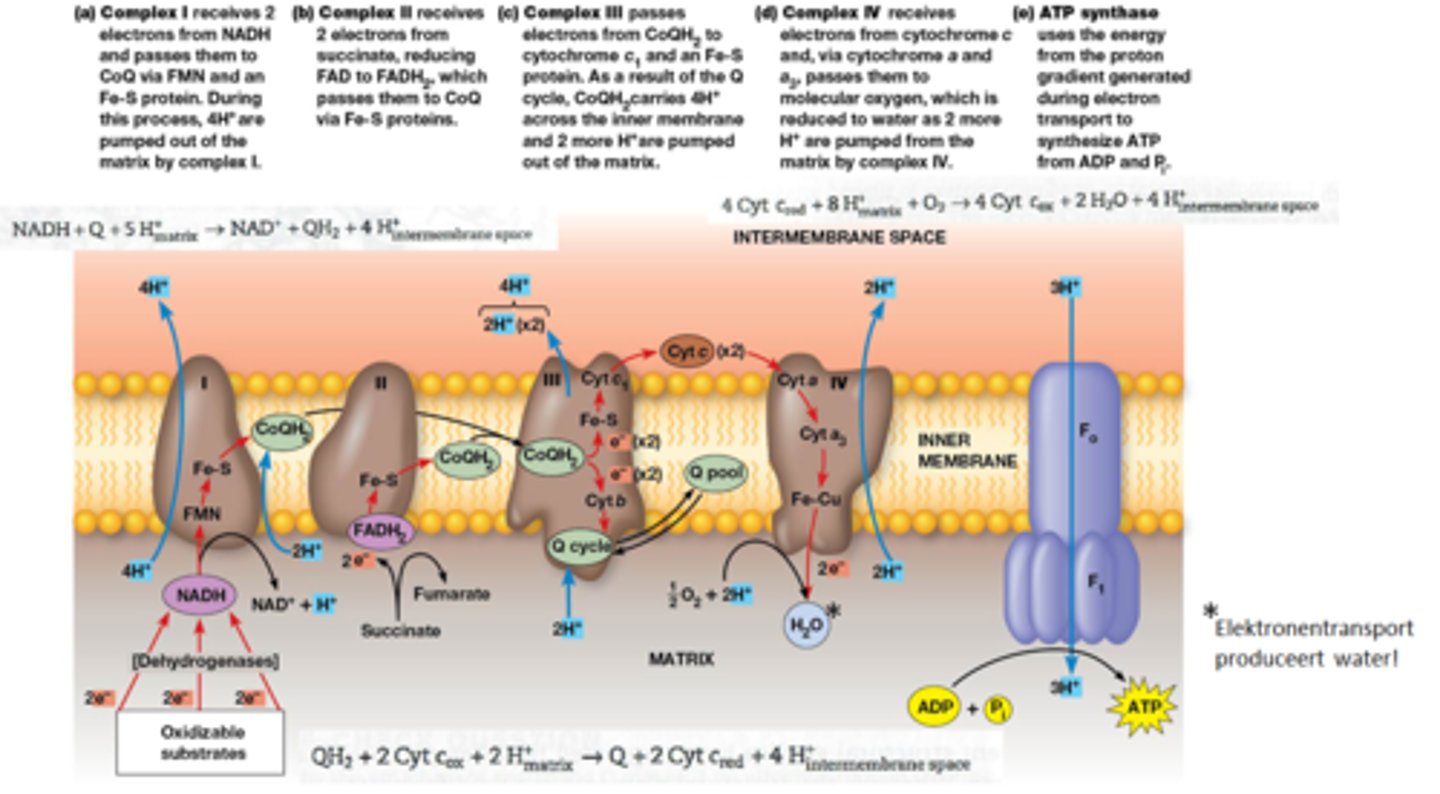
Wat doet cyanide en azide?
ze binden op het Fe-Cu centrum van cytochroom c oxidase en blokkeren elektronen overdracht naar O2
->zeer giftige stoffen
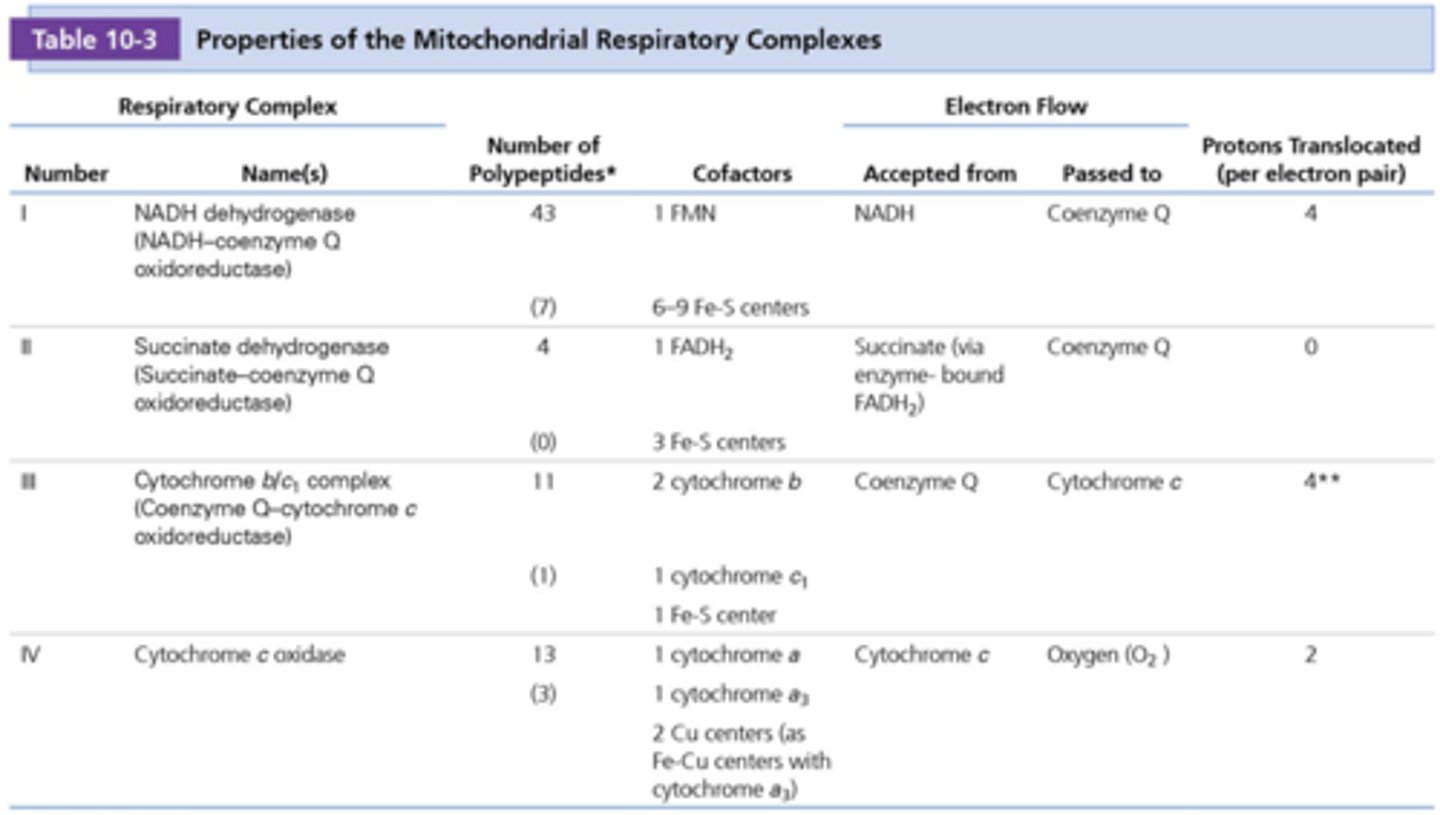
tabel van de 4 ademhalingscomplexen
-Je moet de namen kennen van de enzymen in het complex aanwezig
-cofactors
-welke centra er aanwezig zijn (niet alle letters van cytochromen)
-accepted from welke prostetische factor
-het aantal protonen dat getransloceerd worden tijdens dat elektronenproces
NADH- coenzyme Q oxidoreductase
succinaat dehydrogenase
coenzyme Q-cytochrome c oxidoreductase
cytochrome c oxidase
(zo heeft zij het gezegd in het HC)
ademhalingscomplex 1,3 en 4 maken deel uit van het supramoleculair complex
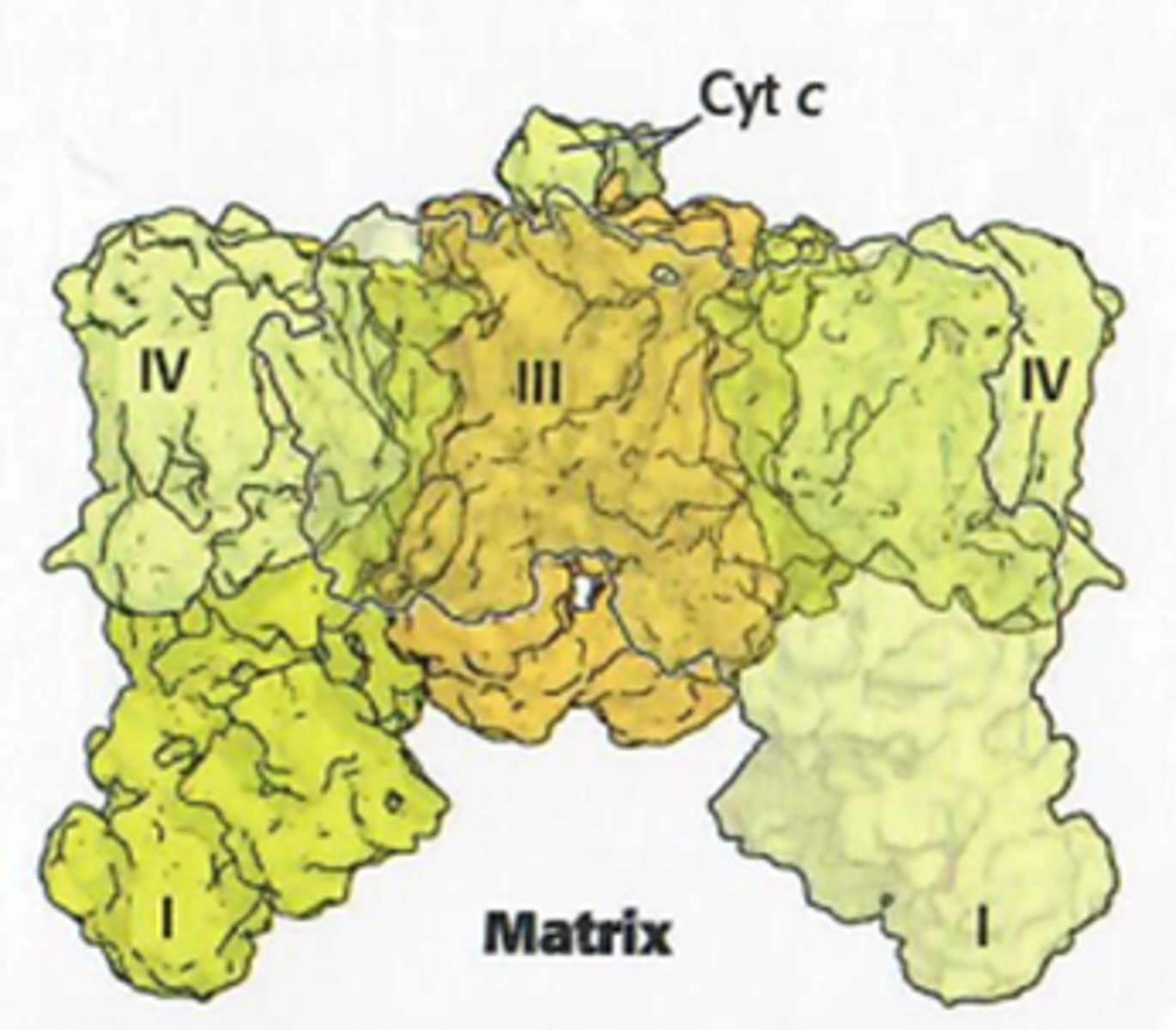
Wat zijn de mobiele componenten van de elektronentransportketen?
Co-enzyme Q en cytochrome c zijn de mobiele componenten van de elektronentransportketen, dwz dat ze kunnen bewegen tussen de ademhalingcomplexen en vervoeren dus elektronen tussen de ademhalingscomplexen
Hoe noem je een complex van ademhalingscomplexen?
een respirasoom: Het grootste deel van de ETS (elektronen transport keten) is georganiseerd in een massief complex
Het zorgt voor maximale efficiëntie, minimale diffusie
Zoals je ziet op de foto zit ademhalingscomplex II hier niet in, want het is een buitenbeentje met succinaat)
Hoeveel ATP komt er vrij bij de oxidatie van NADH en FADH2
3 ATP/NADH
2 ATP/FADH2
->dit zijn schattingen maar we gebruiken deze wel in oefeningen
Oxidatie van 1 NADH: transport van 10 protonen
Oxidatie van 1 FADH2: transport van 6 protonen
Wat is het chemiosmotisch model?
Een model dat Peter Mitchell heeft uitgevonden in 1961 dat de drijvende kracht voor ATP synthese de protonen gradiënt is over het membraan.
1. Flow van elektronen is geassocieerd met het pompen van protonen.
2. Elektronen ‘carriers’ zijn asymmetrisch georiënteerd in het membraan.
3. Membraanvesikels met complex I, III of IV vertonen protonen gradiënt in aanwezigheid van correct substraat.
4. Oxidatieve fosforylering vereist een membraan-omsloten compartiment.
5. In aanwezigheid van ontkoppelaar: normaal elektronen transport naar O2 , geen ATP synthese door mitochondriaal ATP synthase.
6.De elektrochemische gradiënt genereert voldoende energie om ATP synthese mogelijk te maken.
7. Een artificiële protonen gradiënt zonder elektronen transport kan ATP genereren (vesikels of mitochondriën blootgesteld aan pH gradiënt).
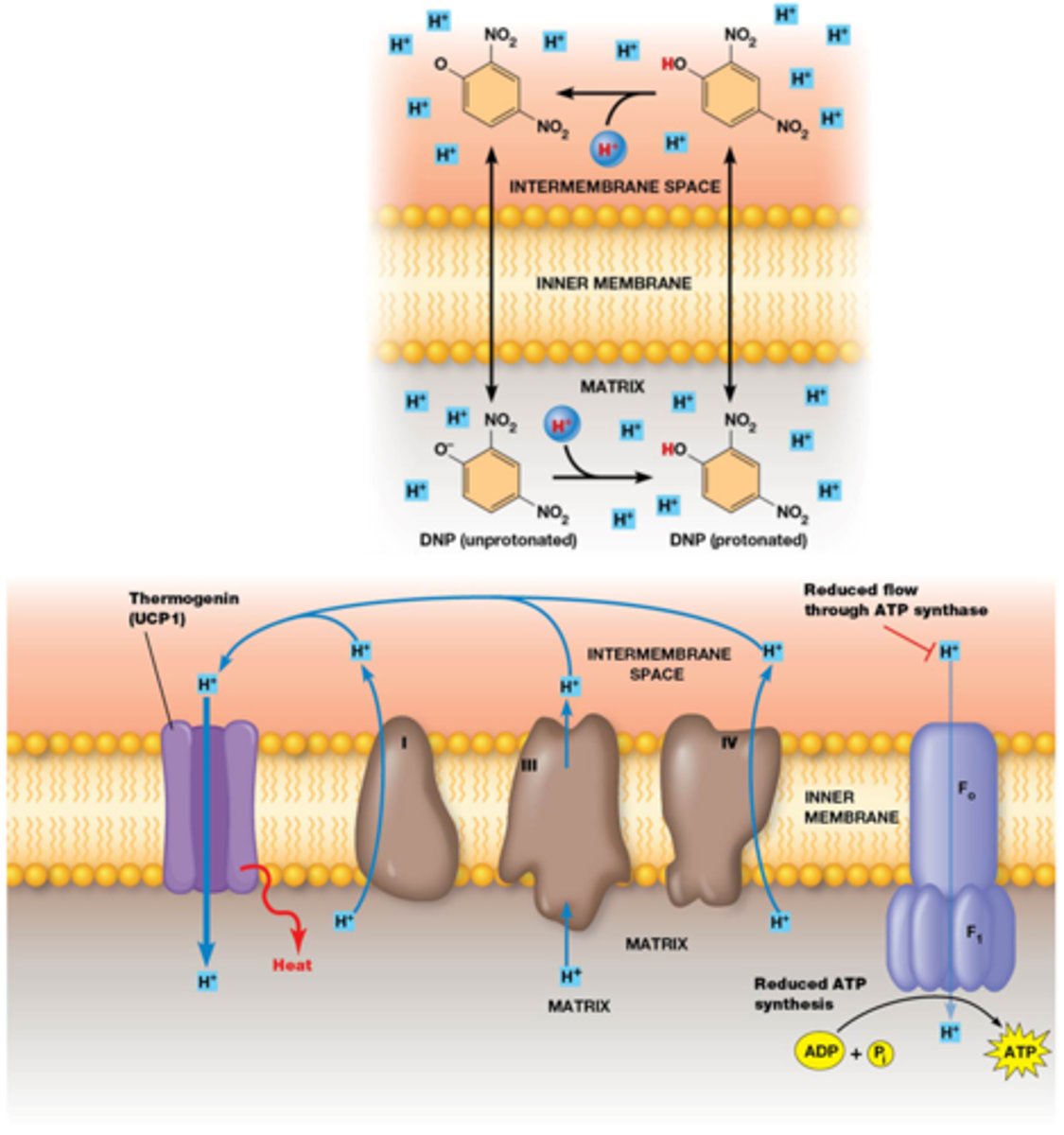
Wat is een ontkoppelaar
Een chemische stof/protonenkanalen die ATP synthase ontkoppelt
Gevolg: verhoogde consumptie en oxidatie van gereduceerde co-enzymen (hoge consumptie van brandstofmoleculen), warmteproductie.
Dinitrofenol (chemische ontkoppelaar)= een zwak zuur dat zowel geprotoneerd als niet geprotoneerd door het membraan kan->de protonengradient kan niet gecreëerd worden
->je valt af maar je krijgt koorts waardoor het gevaarlijk is
Thermogenine (biologische ontkoppelaar, bruin vetweefsel)= in jonge zoogdieren creeert het warmte
Uit wat bestaat ATP synthase
ATP synthase (classe 7 enzymen):
Fo : ‘proton translocator’ (in membraan)
vast gedeelte
-1 a subeenheid=het protonenkanaal: asp zijketen aanwezig in de c zijketen wordt geneutraliseerd wanneer er een proton door gaat
-2 b subeenheden: die het Fo gedeelte koppelen aan het F1 gedeelte
dynamisch gedeelte
-10 c subeenheden (8 - 14 c's verschillend per soort): binden via Asp aan Arg van a-subeenheid. Als de ionische binding van Asp dissocieert dan roteren de 10 c's en de bewegende delen van F1 (λ en ε) 1/10 van 360°
F1 : ATP synthese met energie van de protonen gradiënt (steekt uit in matrix)
vaste delen
-3 alpha (α) subeenheden, ondersteunen de β-subeenheden
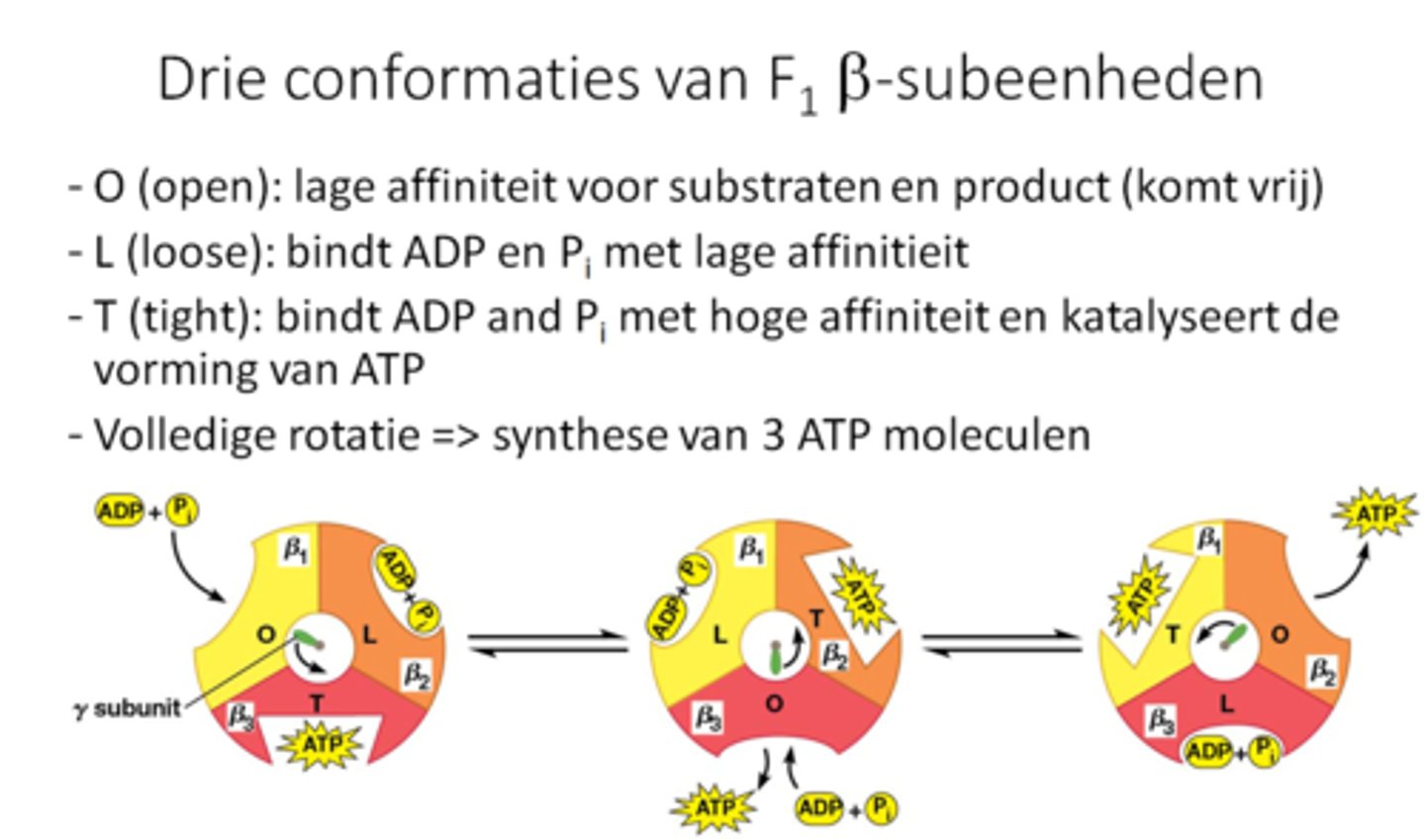
-3 beta (β) subeenheden: 3 confirmaties: open (producten komen vrij), loose (substraten met lage affiniteit worden gebonden) en tight (substraten met hoge affiniteit worden gebonden)
-1 delta (δ) subeenheid
bewegende delen
-1 gamma (λ) subeenheid als deze draait gebeurt er een conformatieverandering van de beta subeenheid
-1 epsilon (ε) subeenheid, verankert λ aan 10c ring
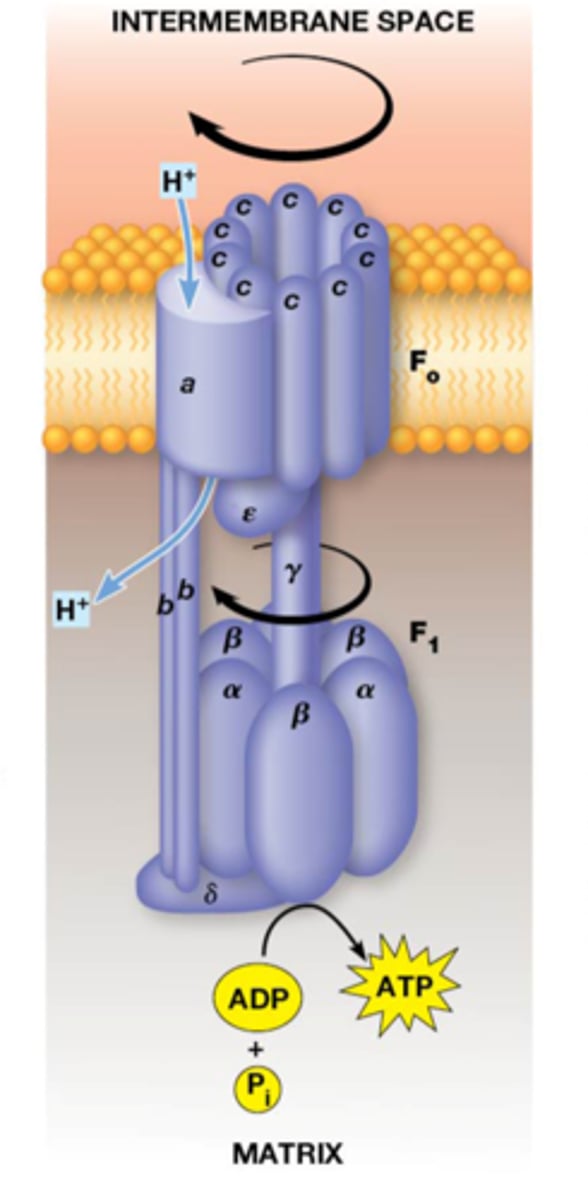
foto dat het bewegende deel van F1 duidelijk maakt
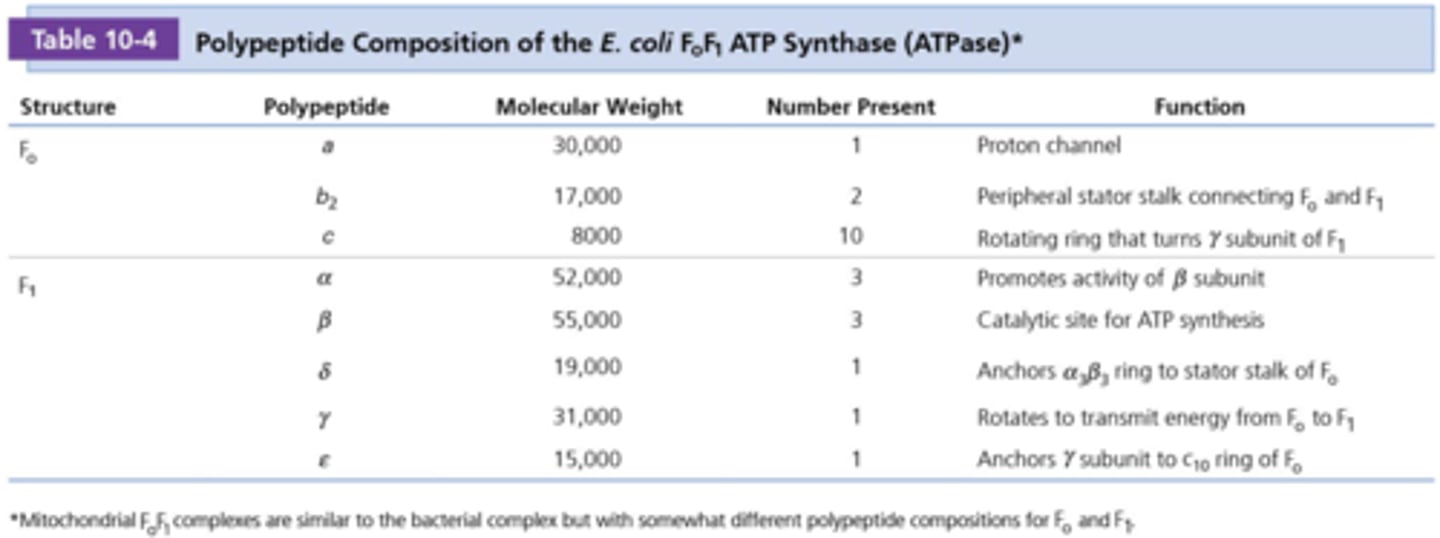
Tabel waar je alles van moet kennen behalve het gewicht
Hoe veel protonen zijn vereist om 1 ATP molecule te vormen?
Bij een volledige rotatie van ATP synthase komt 3 ATP vrij!Afhankelijk van het aantal c-subeenheden (8-14) zijn er dus 3 à 4 protonen nodig om 1 ATP molecule te vormen
per proton dat er door de alpha subeenheid gaat schuift de subeenheid 1/10 360° op als er 10 c-subeenheiden zijn
Hoezo verloopt ATP synthese, wat is de ∆G?
ATP synthese verloopt onder condities waarbij ∆G°'~ 0 en er is geen directe input van energie
Het verloopt omwille van het mechanisch werk (het ronddraaien van c-ring en λ subeenheid) dat eigenlijk de energie levert zodat ATP synthese kan verlopen
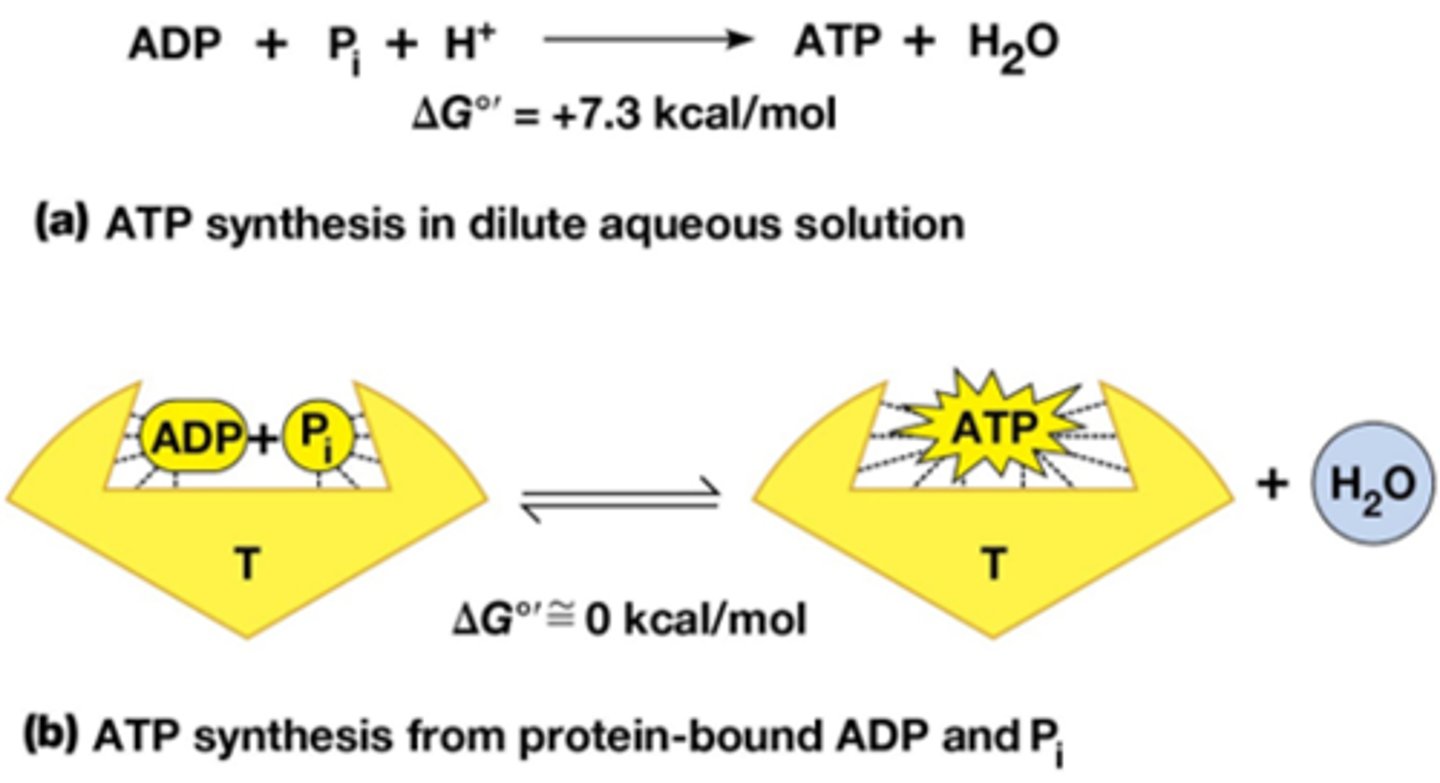
Waarom is het reële rendement van ATP productie lager dan het theoretische rendement?
1) De binnenste mitochondriale membraan heeft geen transporteiwit voor NADH gevormd in het cytosol tijdens de glycolyse
cytosol => transport van elektronen van NADH doorheen de binnenste mitochondriale membraan dmv ‘shuttle’ systemen:
-malaat-aspartaat shuttle (zie volgend kaartje)
-glycerol-fosfaat shuttle (zie volgend volgend kaartje)
2) De protonen gradiënt wordt niet enkel gebruikt voor ATP synthese, maar wordt ook gebruikt voor transport van metabolieten en ionen doorheen de binnenste* mitochondriale membraan via symporters en antiporters. Hierbij gaan er protonen naar binnen of negatief geladen deeltjes (zoals ATP) naar buiten (zie foto)
3) Soms zijn binnenste mitochondriale membranen ‘lek’ voor protonen.
*buitenste mitochondraal membraan heeft porines dus niet nodig daar

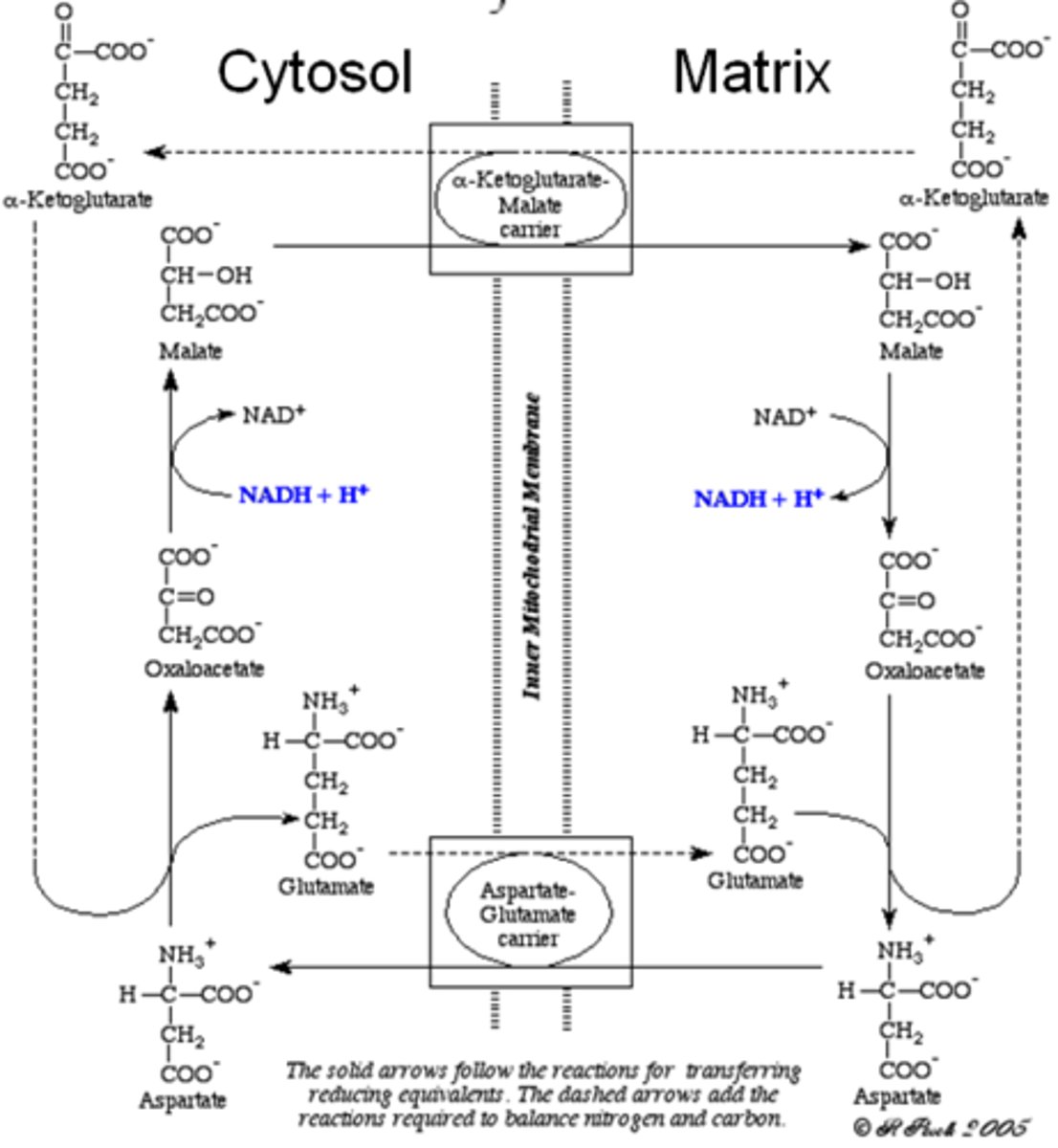
Wat is de malaat aspartaat shuttle?
In lever, nieren, hart: malaat-aspartaat shuttle
-NADH moet naar de andere kant van het membraan gaan
-elektronen van NADH wordt gebruikt om oxaloacetaat te reduceren tot malaat
-oxaloacetaat moet omgezet worden tot aspartaat zodat het terug kan in het cytosol
-alpha ketoglutaraat blijft over en moet teruggebracht worden naar het cytosol
->geen verlies van energie want NADH buiten=NADH binnen
uitleg is juist maar niet helemaal volledig dus kijk ook naar de foto...
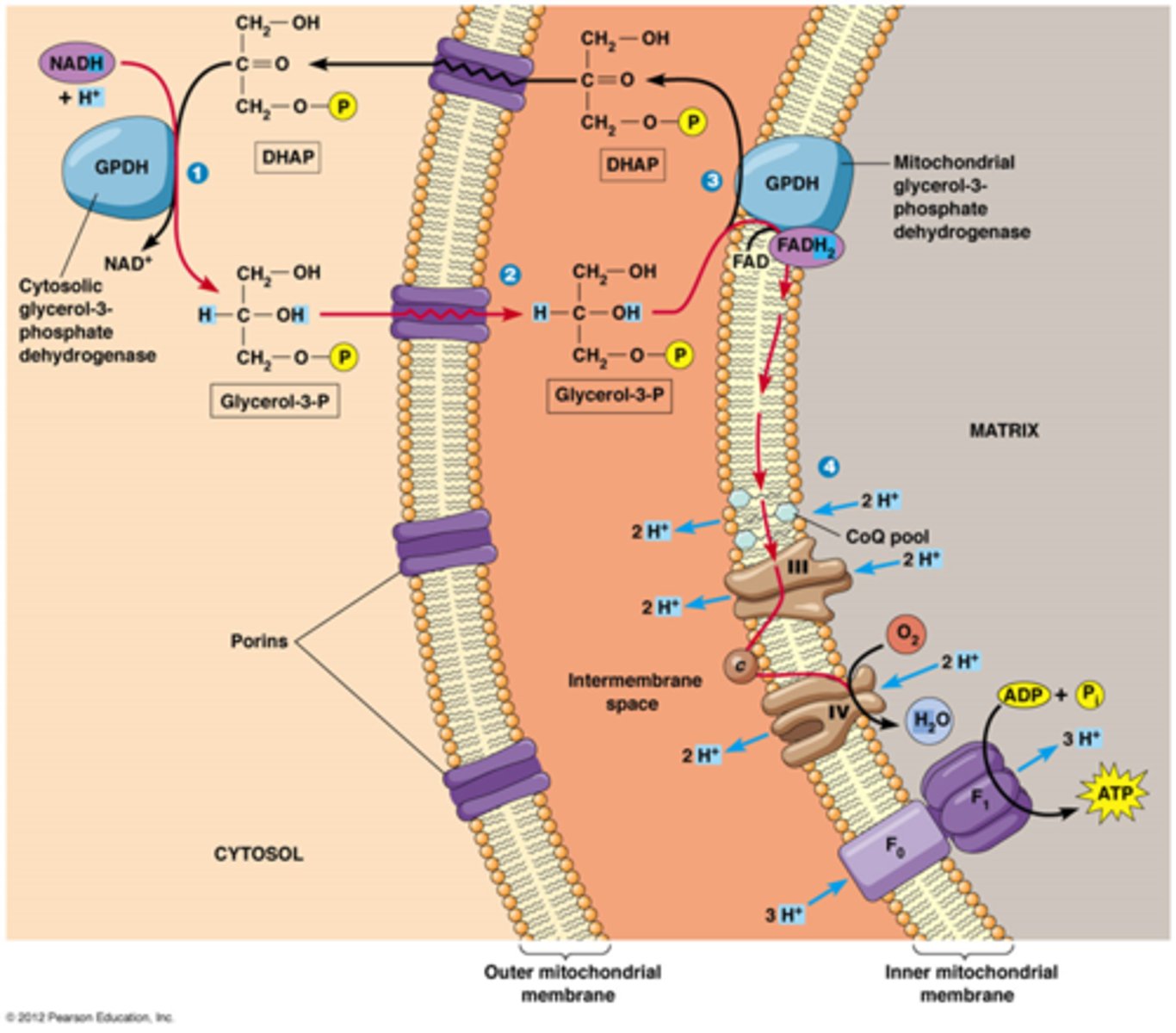
Wat is de glycerol-fosfaat shuttle
-NADH wordt gebruikt om dihidroxyacetonfosfaat (DHAP) te reduceren tot glycerol-3-fosfaat
-glycerol 3 fosfaat passeert door buitenste mitochondriaal membraan
-glycerol 3 fosfaat geeft zijn elektronen af aan FAD+ ter vorming van FADH2
-FADH2 gaat op ademhalingscomplex II zijn elektronen afgeven
->verlies van energie want NADH buiten= FADH2 binnen
slechts 6 protonen bij FADH2 terwijl er 10 protonen naar buiten worden gepompt bij NADH
Som van de aerobe ademhaling:
4 tijdens de glycolyse en CAC, 34 bij ETS en ATP synthese
reele waarde: 32 ATP, 30ATP als je de glycerol fosfaatshuttle gebruikt
∆G°' voor glucose -> CO2 + H2O is -686 kcal/mol
ATP hydrolyse onder cellulaire condities = -10 to -14 kcal/mol
=>totaal: 360–380 kcal (300-320 kcal)
=>efficiëntie van 52–55% (44-47%) (andere energie gaat naar lichaamswarmte)
Dit is heel efficient!