METABOLISME
1/37
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
38 Terms
Biomolècules orgàniques
Lípids, proteïnes, àcids nucleics i glúcids
Funció dels glícids
Energètica (principal), proporciona energia i actua com a reserva energètica (midó dels vegetals, glicogen dels mamífers)
Estructural: paret cel·lular dels fongs (quitina) i de les cèl·lules vegetals (cel·lulosa)
Funció dels lípids
Estructural → forma la membrana plasmàtica
Energètica → Reserva energètica en els mamífers
Reguladora → algunes vitamines i hormones són lipídiques
Funció dels àcids nucleics
Portadora d’informació genètica en forma d’ADN o ARN
Energètica → ATP (moneda energètica)
Funció dels pròtids
Estructural → citoesquelet (esquelet intern de la cèl·lula) , (tmb cabells)
Reguladora → enzims, vitamines, hormones (insulina…)
Energètica
Definició enzims
Molècules que faciliten o presenten moltes de les reaccions químiques necessàries per a un bon funcionament del nostre metabolisme. Estan formats per proteïnes.
Estructura primària de les proteïnes
L’estructura primària d’una proteïna consisteix en la unió de molts aminoàcids mitjançant enllaços peptídics. (enllaços entre l’extrem COOH i l’estructura NH2 de l’altra)

Descriu el procés de la formació d’un enllaç peptídic
Extrem COOH d’A1 i l’extrem NH2 d’A2 reaccionen → el grup OH s’ajunta amb un H del NH2
S’uneixen els aminoàcids i s’allibera aigua (condensació)
**A1/A2: aminoàcid 1/2

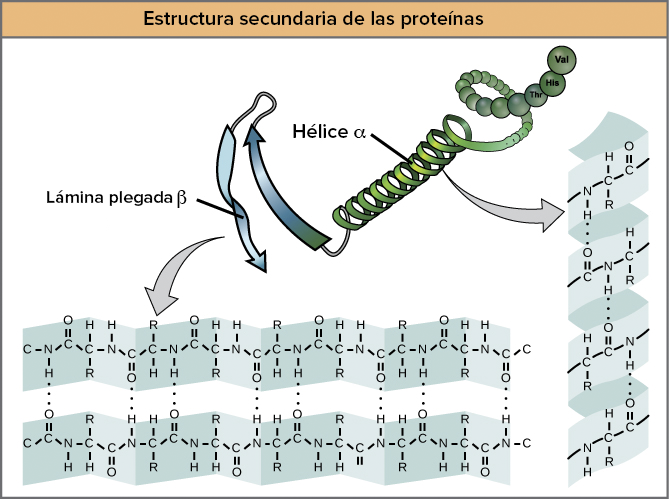
Estructura secundària de les proteïnes
Els diferents aminoàcids de la cadena interaccionen entre si formant ponts d’hidrogen. Fa que la cadena comenci un plegament en una forma determinada.
→ Estructures de plegament
Làmina plegada beta
Hèlix alfa
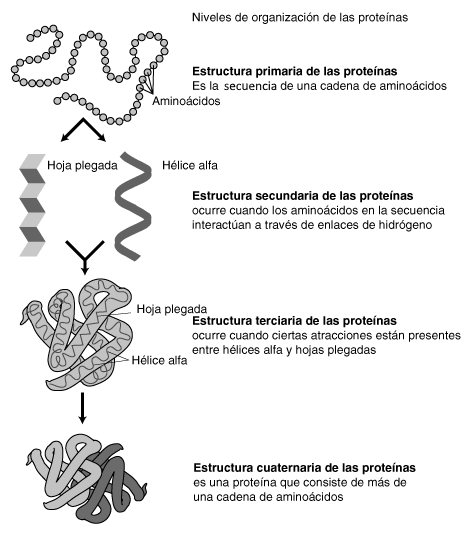
Estructura terciaria
Es forma per la interacció de les estructures alfa i beta de l’estructura secundària. Això li dona la forma definitiva. (la forma definitiva depèn de l’ADN i la funció de la proteïna depèn de la seva forma)
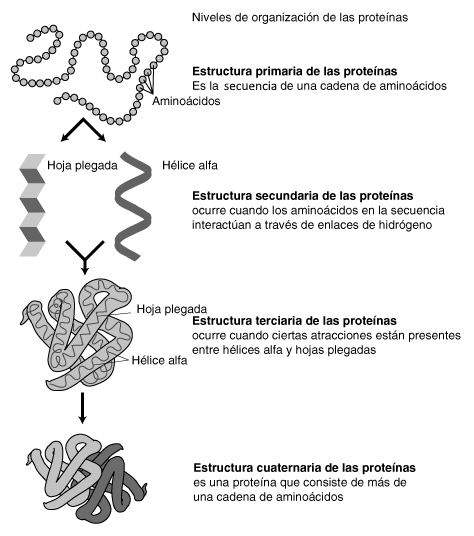
Estructura quaternaria
Es dona en les ocasions en què s’uneixen diferents proteïnes (ex: hemoglobina)
Què són els enzims i l’activitat enzimàtica? Que determina la seva especificitat?
Molècules (normalment proteiques) que faciliten o permeten diferents reaccions químiques. Cada enzim és específic de catalitzar una reacció química.
L’activitat enzimàtica es mesura com la velocitat de les reaccions catalitzades d’un enzim: el nombre de molècules de substrat transformades en producte per unitat de temps.
(mesura la velocitat de la capacitat d’un enzim de transformar un substrat en un producte)
La forma de l’enzim determina l’especificitat.
De quins factors depèn l’activitat enzimàtica?
— Zona activa/centre actiu: Unió del substrat amb un lloc de l’enzim constituït per certs aminoàcids on només pot unir-se a un substrat determinat. (Regió d’unió entre un substrat i un enzim)
— Concentració de l’enzim: com més gran sigui el nombre de molècules de l’enzim → més gran la capacitat de transformar el substrat en producte
— Concentració del substrat: Més concentració del substrat → augment de velocitat (més probable que substrat i enzim es trobin).
S’assoleix la velocitat màxima (tots els enzims estan ocupats, per tant, saturats pel substrat)
— Temperatura i pH: En temperatura/pH òptims s’assoleix la velocitat màxima.
— Modificacions covalents de l’enzim: ex: fosforilació →modifica l’estructura de lloc actiu o l’estructura tridimensional de l’enzim i la seva afinitat pel substrat.
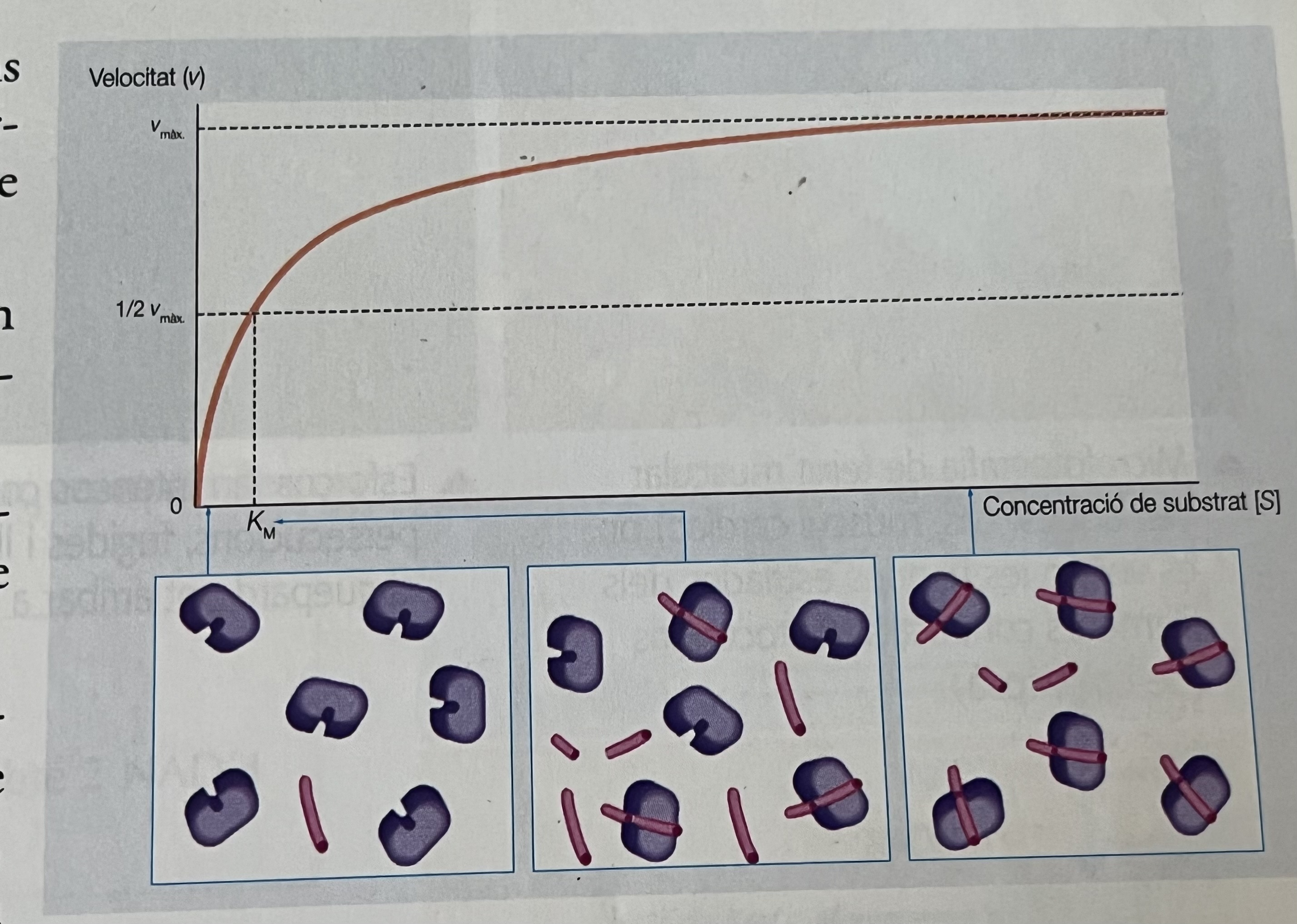
Què és la KM?
És la meitat de la velocitat màxima. Defineix l’afinitat entre el substrat i l’enzim. Expressa la concentració de substrat quan s’arriba a la meitat de la velocitat màxima.
🡡 KM = 🡣 afinitat entre el substrat i l’enzim
Anabolisme
Síntesi de molècules. (De molècules simples a molècules complexes)
Catabolisme
Digestió de molècules. (De molècules complexes a molècules simples)
Equació de la respiració cèl·lular
C6H12O6 + O2— (produeix ATP) —> 6CO2 + 6H2O
Equació de la fotosíntesi
6CO2 + 6H2O — (utilitza llum) —> 6C6H12O6 + 6O2
Fosfocreatina
Molècula que presenta un enllaç ric en energia al qual permet el pas d’ADP a ATP (forma més ràpida d’aconseguir ATP)
Sempre present en la musculatura (però és limitada, si no → glucosa)
Es trenca i l’energia s’utilitza (ATP → ADP)
Procés de glicogen a ATP
Procés anaeròbic
Glicogen — (glicogenòlisi, hidròlisi del glicogen) —> glucosa 6-P
6C Glucosa 6-P — (Glucòlisi, es redueix 2NAD+ a 2NADH) -> Piruvat 3C
2 ATP → 2 ATP (2 és valor net, originalment 4, però hem invertit 2 ATP d’entrada)
3- 2Pirvuat — (Fermentació làctica, Oxidació del 2NADH a 2NAD+) —> 2lactat
S’acumula lactat i ATP
Conseqüències de l’acumulació de lactat
Disminució del pH → enzims funcionen pitjor (disminució de l’activitat enzimàtica) i es deixa de fer la glucòlisi (la glucòlisi està catalitzada per enzims)
Teixit muscular perd la capacitat de contracció
Acumulació de lactat genera un deute d’oxigen (cos requereix molt oxigen per oxidar el piruvat i que el lactat es vagi convertint en piruvat)
Fermentació i organismes que la realitzen
Procés catabòlic on hi ha una oxidació incompleta de compostos orgànics.
Normalment anaeròbic (existeix la fermentació aeròbica)
Es produeixen 2 ATP per cada glucosa (rendiment energètic baix)
— Microorganismes o teixits: llevats, bacteris, algunes cèl·lules vegetals i cèl·lules animals (eritròcits)
Tipus de fermentació
Segons la substància que s’obté com a producte final
Làctica: lactosa → àcid làctic + ATP
Alcohòlica: glucosa → etanol i CO₂ + +ATp
Pútrida: (descompon) restes orgàniques → matèria orgànica
Fermentació làctica procés
Lactosa — (lactasa) —> Glucosa + galactosa — (isomerasa) —> 2 Glucoses → 4 àcids pirúvics —(lactat deshidrogenasa) —> 4 àcids làctics + 4 ATP (de la glucòlisi)
Procés dels triacilglicèrids del teixit adipós fins al cicle de krebs
Triacilglicèrids — (lipòlisi) —> àcids grassos — (beta oxidació) — acetil-COA —> cicle de krebs
Definició de beta oxidació i fórmula
S’obtén molècules d’acetil-CoA a partir d’una molècula d’àcid gras
Nombre d’Acetil CoA = nombre de C de l’àcid gras/2
Procés de la beta oxidació
Activació de l’àcid gras per la unió d’un enzim CoA.
Entrada al mitocondri.
Oxidació del tercer carboni.
La molècula es trenca i es forma un àcid gras de 2 carbonis menys i un acetil CoA.
Aquest procés es repeteix fins que l’àcid gras s’ha acabat i s’ha convertit en acetil CoA.
Cada acetil CoA entra al cicle de Krebs.
Cicle de Krebs
Es dona al mitocondri.
La molècula que inicia el cicle de Krebs és l’Acetil CoA (2C)
L’Acetil CoA s’uneix a una molècula de 4 carbonis, l’oxolacetat, que prové del cicle de Krebs i formen el citrat (6C)
El citrat pateix 2 descarboxilacions (se li treuen 2 carbonis) i això produeix 2CO₂.
(Durant el procés de descarboxilacions es produeixen: 3NADH, 1FADH2, 1 GTP)
El 3NADH i 1FADH2 s’utilitzen a la cadena respiratòria.
Localització i estructura de la cadena respiratòria/de transport d’electrons. Que forma cada complex proteic?
Localització: membrana interna mitocondrial
4 complexos proteics de membrana:
(Complex 1,2,3 són bombes de protons que gràcies al poder reductor del NADH i el FADH2 bombardegen H+ a l’espai intermembranós.)
— Complex 1: NADH → NAD+
— Complex 2: FADH2 → FAD (S'utilitzen al cicle de krebs)
— Complex 3: H+ + 1/2O2 →H₂O
— Complex 4 → ATP sintasa: fa passar protons des de l’espai intermembranós a la matriu mitocondrial. Com ho fa a favor de gradient (passa protons d’on hi ha més a on n’hi ha menys) es genera energia potencial que li permet per produir ATP (fosforilació oxidativa).
ADP + P → ATP
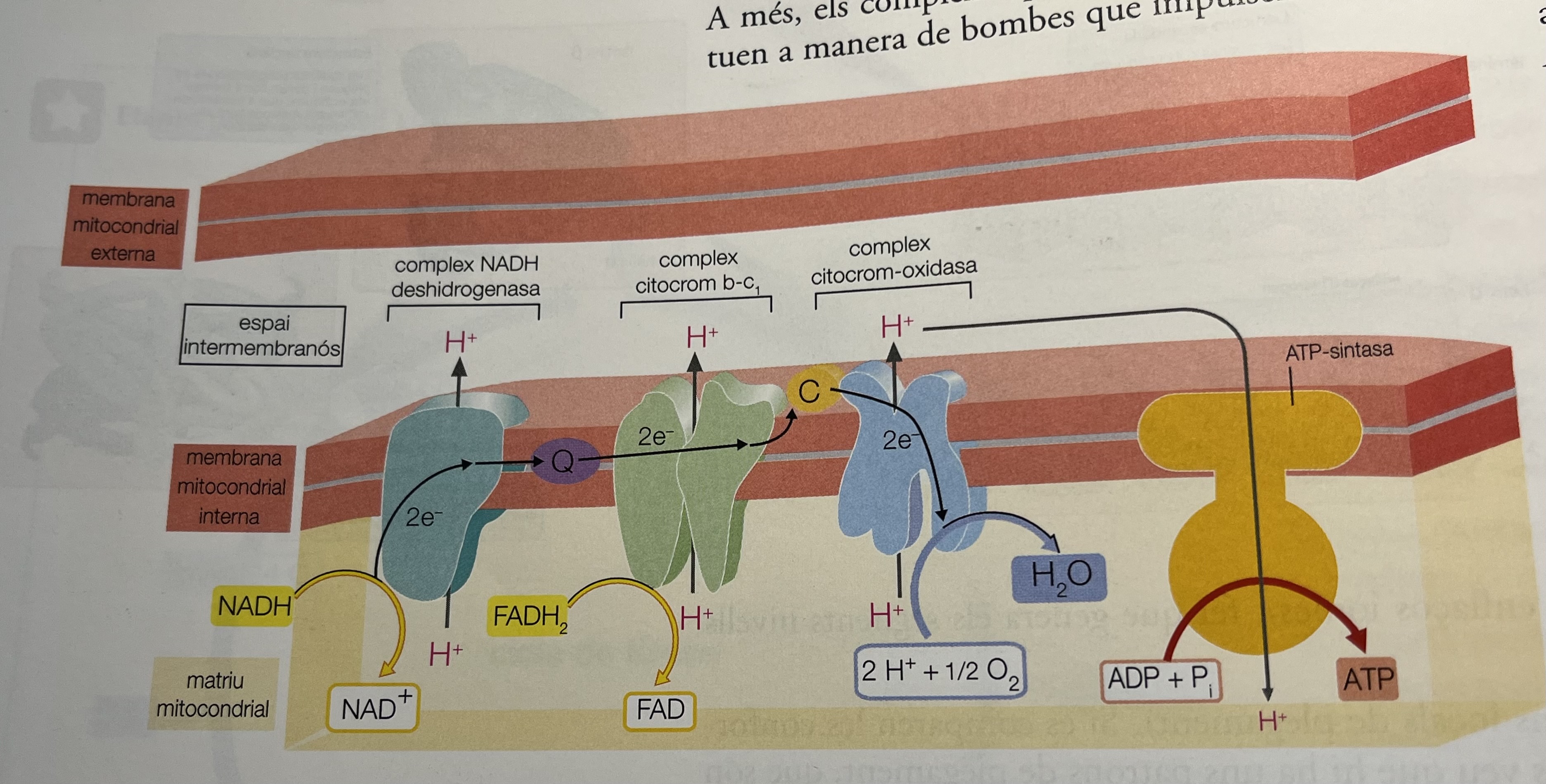
Fosforilació oxidativa
Fabricació d’ATP per part de l’ATP sintasa
Vies metabòliques s’han de donar per acumular glucosa que sobra en forma de greix
Glucosa a piruvat (glucòlisi)
Piruvat a acetil-CoA
Acetil-CoA a àcids grassos (lipogénesi)
Àcids grassos a triacilglicèrid (esterificació)
Balanç energètic de la glucosa en un exercici aeròbic
36 a 38 ATP (depenen del tipus de cèl•lula)
Fotosíntesi
Procés anabòlic (construcció de materia orgánica) mitjançant el qual organismes fotoautòtrofs produeixen glucosa i oxigen a partir de CO2, llum i H2O
Té lloc als cloroplasts
Consumeix ATP
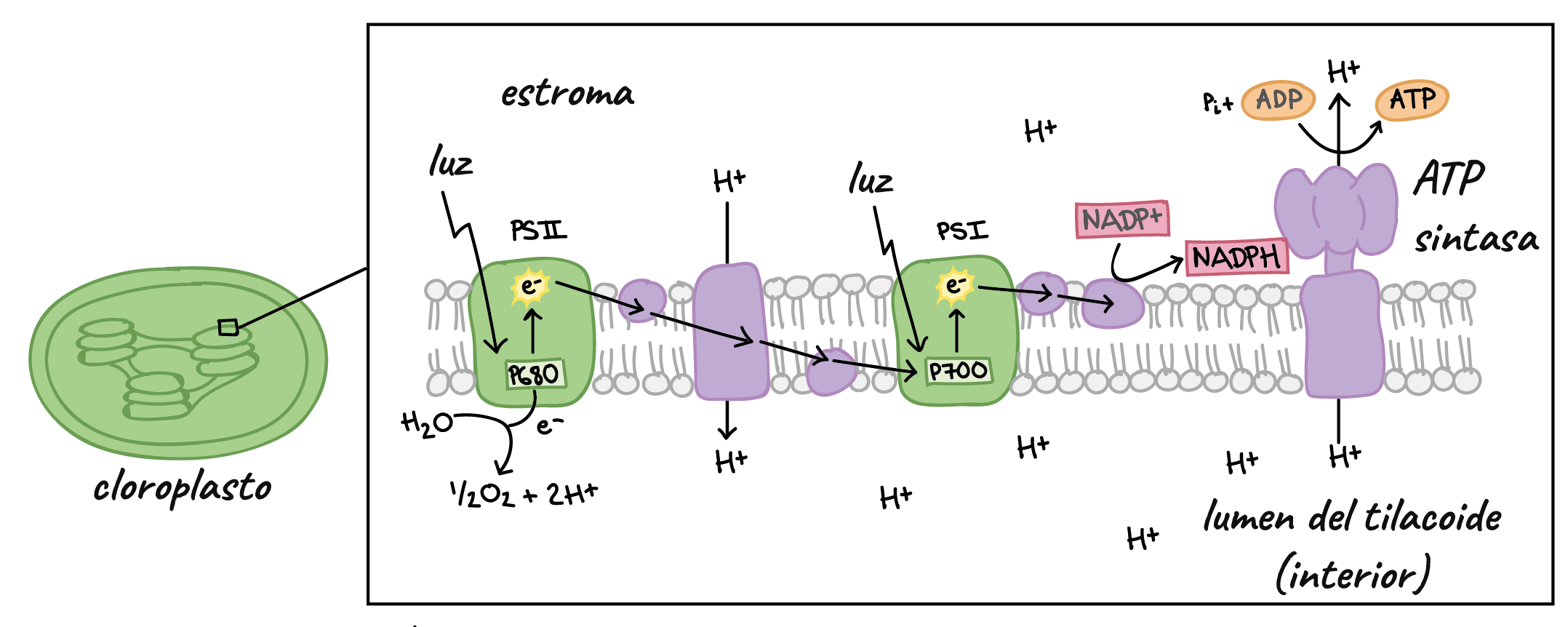
Procés de la fase lluminosa/dependent de la llum/fotoquímica, on té lloc i en quin complex proteic es dona cada pas
(Té lloc al cloroplast dins la membrana tilacoidal)
Captació de llum
Fotòlisi de l’H2O, les molècules d’aigua tenen un paper com a donadors d’electrons, es descomponen en oxigen, protons i electrons. S’allibera O2 al medi. — (Fotosistema II)
Generació de poder reductor amb el NADPH (producció NADPH) — (NADP+ reductasa)
Es bombardegen ions H+ des de l’espai tilacoidal a l’estroma (a favor de gradient) i es produeix d’ATP gràcies a l’acumulació de protons dins de l’espai tilacoidal. — (ATP sintasa)
Amb l’ATP i el NADPH que produeix durant la fase lluminosa s’inicia la següent fase.
Fase no lluminosa/Cicle de Calvin
Localització: estroma (espai interior del cloroplast)
Fixació del carboni on un àtom de carboni, en forma de matèria inorgànica (perquè forma part del CO₂), passa a formar part d’una molècula orgànica (glucosa normalment).
Se sintetitza 1 glucosa a partir de 6CO2 (prové de l’atmosfera) per cada glucosa i es consumeix 9ATPs i 6 NADPH (provenen de la fase lluminosa)
Enzim encarregat: Rubisco
Els organismes quimioheteròtrofs depenen d’aquest procés
Cicle tancat
Procés bioquímic fermentació alcohólica
Glucosa → 2Etanol + 2CO2 + 2ATP
Importància biològica de la fotosíntesi
Controlar el nivell de CO₂ a l’atmosfera
Produir O2
Fixació del C per produir matèria orgànica (dona aliment a tots als organismes quimioheteròtrofs)
Explica la importància del paper del CO₂ en la fotosíntesi
El CO₂ captat en l’atmosfera s’utilitza en la fase no lluminosa en el cicle de Calvin perquè és fixat i el carboni passa a formar part de matèria inorgànica a formar part d’una molècula orgànica.