SBP 2052 - Cours 2
1/115
Earn XP
Description and Tags
Les études non cliniques
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
116 Terms
Qu’est-ce qu’une loi?
Énoncés de références ultimes décrivant les grands principes
Mandat des institutions
Votée par les élus
Loi est juridiquement contraignante
Vrai ou faux? Les règlements sont sujets à interprétation
Vrai, juridiquement contraignants mais sujets à interprétation
Qui suis-je? Je suis la standardisation des processus via les “bonnes pratiques”
Les règlements
Quels sont les 3 types de bonnes pratiques?
Bonnes pratiques de Laboratoire
Bonnes pratiques Manufacture
Bonnes pratiques Clinique
Qu’est-ce que les règlements?
Modes d’application de la loi, rédigées par des fonctionnaires
Qu’est-ce que sont les lignes directrices?
Énoncés d’orientation reflétant la pensée de l’agence règlementaire
Recommandations de stratégie pour planification et conduite des études
FDA
1990 - harmonisation FDA, EMA et ICH
Pourquoi les bonnes pratiques de laboratoire ont été mises en place?
À cause de :
Originaux de rapports d’autopsie non disponibles
Fiches d’observation en laboratoire non datées, non signées
Différences inexpliquées entre les données brutes de laboratoire et le rapport final
Animaux morts rapportés vivants et normaux (apparence, appétit, etc)
Soumis à la FDA : rapport d’histopathologie sans prélèvement de tissus
Politique interne de falsification de données
Quelles sont les conclusions de la FDA considérant l’instauration des bonnes pratiques de laboratoire, aka pourquoi la FDA a décidé cela?
Il y a eu de la négligence dans la gestion des laboratoires, des soins aux animaux et des données
Absence de surveillance adéquate par les compagnies commanditaires des études reliées par des labos
Absence de vérification systématique des données scientifiques dans les rapports d’études non cliniques sont exactes et exhaustives avant la présentation à la FDA
Besoin d’un cadre règlementaire pour l’assurance de qualité des données et de la documentation scientifique
Quel type (design) d’études est effectué avec les BPL (GLP)?
Design d’études est prospectif
Vrai ou faux? Toutes déviations du protocole originales doivent être documentées
Vrai
Vrai ou faux? La signature d’une seule personne du cahier de laboratoire est suffisante
Faux, la signature de 2 personnes est nécessaire
Qu’est-ce qui doit être inclus dans la collecte des données? (3)
Calibration appareils
Stockage des produits (où, à quelle température, etc)
Signature quotidienne du cahier de lab par 2 personnes
Quelles sont les 2 choses importantes que l’on veut lorsqu’on dit que les archives doivent être complètes et sécuritaires
Tracabilité - historique du développement dans ses moindres détails
Imputabilité - Qui a fait quoi, quand et comment ? (Ø anonymat)
Le(s)quel(s) est/sont vrai(s)? La conformité aux standards BPL est :
Obligatoire pour des études non cliniques qui visent à supporter l'a soumission de dossier pour approbation par une agence règlementaire
Utile pour les dossiers légaux (défense de brevets, poursuite légales contre la compagnie)
1 et 2 sont vrais
Diapo à étudier solo

Qui suis-je? Je suis la police interne
a) le personnel
b) directeur de l’étude
c) unité de l’assurance qualité
c) unité de l’assurance qualité
Vrai ou faux? L’équipe d’assurance qualité fait partie du personnel impliqué dans la conduite de l’étude
Faux, l’unité d’assurance qualité doit être entièrement indépendante de la conduite de l’étude
Vrai ou faux? Le directeur de l’étude est responsable de surveiller si l’étude est conforme aux règlements
Faux, c’est le travail de l’équipe d’assurance qualité
Vrai ou faux? Pour la FDA, si ce n’est pas documenté, ce n’est pas grave
Faux, pour la FDA si ce n’est documenté, ça n’existe pas! Ça ne s’est jamais produit ou bien c’est une rumeur !
Il faut documenter absolument tout, toutes les infos (raw data), protocols, specimens, etc…
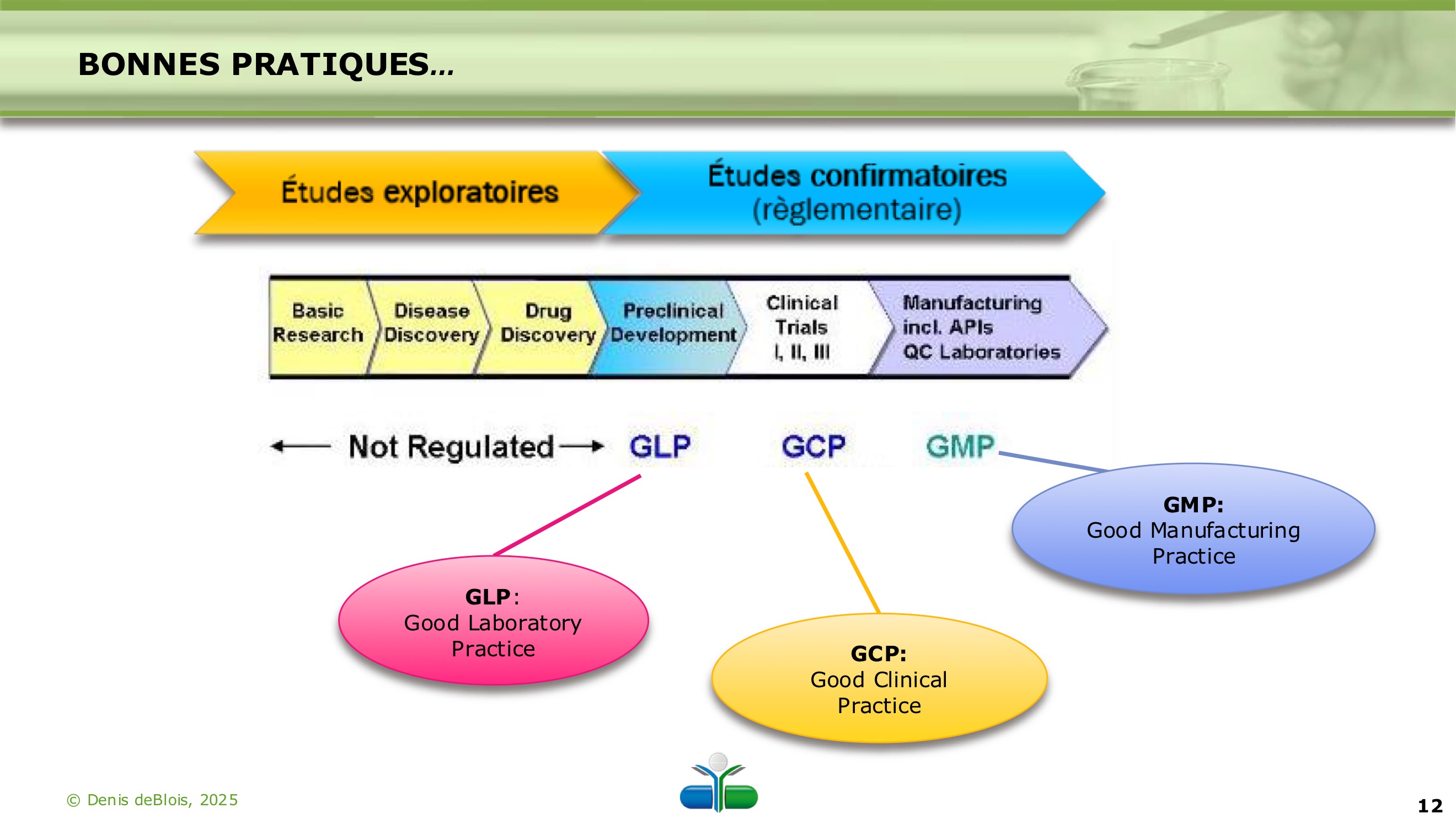
Vrai ou faux? Les GLP, GCP et GMP font partie des études exploratoires et des études confirmatoires (règlementaires)
Faux, seulement des études confirmatoires. Les études exploratoires “not regulated”
Quels sont les 2 animaux qui reproduisent la TOX observée chez l’humain?
Rat
Chien
Comprendre le schéma
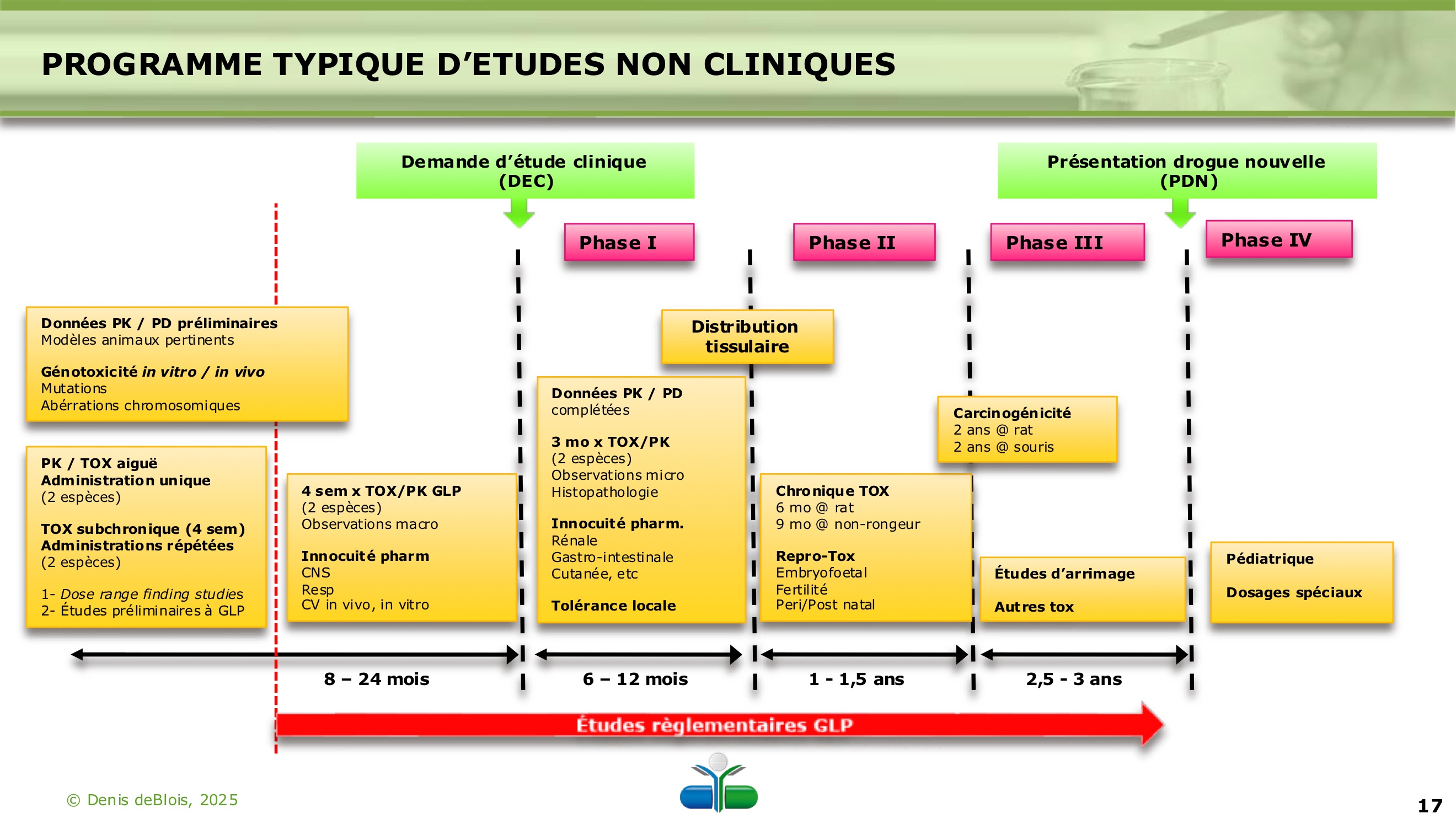
Vrai ou faux? Le début de la phase I peut avoir lieu avant la demande d’étude clinique (DEC)
Faux, elle débute après la DEC
Dans quelle phase étudie-t-on la tox chronique et tox de reproduction?
Phase 2
Vrai ou faux? On observe la carcinogénicité chez les non-rongeurs
Faux, seulement chez les rats et souris.
Pourquoi? La vie des non-rongeurs (ex : chien) est plus longue, donc le temps d’observation du développement du cancer peut s’avérer long, tandis que le span life de la souris est de 2 ans, donc plus rapide pour observer si un cancer se développe.
Durant quelles phases observe-t-on la distribution tissulaire?
Phase 1 et 2
Vrai ou faux? La génotoxicité est évaluée in vivo et in vitro durant la phase 1
Vrai, updated de Vincent, il a dit que la génotox est évaluée mostly avant la phase 1 mais aussi un peu en phase 1 également
Vrai ou faux? Les données PK et PD doivent être complétées au moment de débuter les études cliniques phase 1
Vrai
À quel moment est évaluée la carcinogénicité?
Phase 1
Phase 2
Phase 3
Phase 1-2
Phase 2-3
Phase 2-3
À quel moment est-ce qu’on dépose la demande PDN (présentation drogue nouvelle)?
Début Phase 1
Fin Phase 2
Fin Phase 3
Fin Phase 4
Fin Phase 3
Parmi toutes les phases des études cliniques, laquelle est la plus courte (8-24 mois)?
Phase 1
Parmi toutes les phases des études cliniques, laquelle est la plus longue (2-3 ans)?
Phase 3
Quand est-ce que débute les GLP?
Avant la phase 1
Phase 1
Phase 2
Fin phase 4
Avant la phase 1
Durant quelle phase observe-t-on la tolérance locale?
Phase 1
Phase 2
Phase 3
Phase 4
Avant phase 1
Phase 1
Durant quelle phase évalue-t-on les populations spéciales (pédiatrie) et détermination des doses spéciales?
Phase 1
Phase 2
Phase 3
Phase 4
Phase 2-3
Phase 3-4
Phase 4
À quel moment la DEC (demande essai clinique) est faite?
À la fin du développement/études pré-clinique
Quel autre nom est fourni pour les études pré-cliniques?
Toxicologie exploratoire (non-GLP)
Toxicologie régulatoire (GLP)
Toxicologie exploratoire (non-GLP)
Vrai ou faux? L’innocuité pharmacologique et la génotoxicité in vitro et in vivo sont requises pour la DEC (demande essai clinique)
Vrai, 2 espèces doivent recevoir le traitement sur une période de 28 jours. La récupération est également essentielle à démontrer.
Vrai ou faux? On étudie la toxicité chronique sur une période de 3-12 mois chez 2 espèces pour pouvoir faire une demande de PDN (présentatrice drogue nouvelle)
Vrai, pendant une période de 3-12 mois, on étudie :
La récupération au niveau d’une espèce
La fertilité et reproduction suite au RX
Développement foetal
Les effets pré-natal et post-natal
Carcinogénicité chez les 2 espèces
Vrai ou faux? Concernant le design des études cliniques, il est conseillé de commencer avec la fin en tête
Vrai
Quels sont les aspects à considérer lorsqu’on établit un design des études non cliniques? (5)
Indication
Population cible
Schéma posologique
Dose maximale
Plans des phases 1,2,3
Vrai ou faux? Si un élément manque du plan de développement des études non cliniques, les études seront inadéquates et devront être répétées
Vrai
Qu’est-ce que la monographie de produit?
Document scientifique factuel sur un médicament qui, sans avoir recours à des documents promotionnels, décrit :
Propriétés, allégations, indications et mode d’emploi du médicament
Effets indésirables, interactions médicamenteuses
Symptômes, traitement en cas de surdose, posologie et mode administration
Pharmacologie et toxicologie
Vrai ou faux? Les effets pharmacologiques primaires et secondaires peuvent contribuer aux effets indésirables du médicament
Vrai
Vrai ou faux? Seule la pharmacocinétique (PK) aide à choisir le modèle animal pertinent
Faux, la PD contribue à ce choix aussi
Vrai ou faux? Il n’est pas nécessaire d’avoir des données PK de plusieurs espèces animales, 1 seul suffit, pour initier le programme d’étude de toxicologie
Faux, plusieurs modèles animaux sont requis
Vrai ou faux? La PD contribue aux choix de l’éventail de dose
Faux, c’est la PK. Elle permet d’exclure les doses plus élevées et réduire les coûts
Vrai ou faux? On DOIT avoir une méthode d’analyse validée AVANT le début du programme
Vrai
Qui suis-je? Je permet de mieux comprendre la TOX et/ou l’absence de TOX
PK
PD
PK
Quel est le niveau d’impuretés accepté défini par ICH Q3?
Max 10%
Diapo à étudier solo

Vrai ou faux? Concernant la formulation:
Le véhicule et la formulation doivent être biologiquement compatible
Vrai
Vrai ou faux? Concernant la formulation, il est important d’éviter autant que possible l’utilisation de nouveaux excipients ou autres composantes qui ne sont pas caractérisées du POV TOX
Vrai
Durant l’étude, qu’est-ce qui doit être monitoré? (2)
Concentration formulation (au début et à la fin)
Homogénéité formulation (au début)
Vrai ou faux? Les résultats obtenus à la fin de l’étude sont préférables
Faux, les résultats obtenus en temps réel sont préférables car ils permettent de résoudre les problèmes + rapidement
Vrai ou faux? Il est important de mesurer la stabilité d’un produit congelé pour évaluer s’il a le même taux de dégradation qu’un produit non-congelé
Vrai
Quelles sont les questions à se poser en toxicocinétique?
Quelle est la dose requise pour atteindre un niveau X dans les compartiments pertinents?
Est-ce que l’effet maximal ou l’exposition sont affectés par la durée ou la fréquence d’administration du médicament?
Quels sont les effets à long terme?
Quelle est la relation dose VS tox
Bon choix de l’animal
Vrai ou faux? La biodisponibilité du médicament est relativement toujours la même chez l’animal que chez l’humain
Faux, la biodisponibilité est parfois réduite chez l’animal p/r à l’humain
Vrai ou faux? Il n’y a aucune limite à l’augmentation de la dose
Faux, la solubilité limite
Vrai ou faux? Avec un temps de ½ vie court, le médicament nécessite des administrations moins fréquentes qu’avec un temps de ½ vie plus longue
Faux, c’est le contraire
Sur quoi se base le choix du modèle animal?
Pk et PD
La plupart des programmes requièrent …
un rongeur
un non-rongeur
les deux
les deux
Quel est le rongeur le plus souvent utilisé?
Souris
Rat
Les deux
Rat
Vrai ou faux? Le porc fait partie des rongeurs utilisés dans les programmes d’étude
Vrai
Qui suis-je? Je suis un rongeur qui est utilisé pour les études chroniques du potentiel cancérigène
Souris
Rat
Souris
Vrai ou faux? Le lapin est un modèle non-rongeur utilisé pour mesurer la tox embryo-foetale et tox spéciale
Vrai
Vrai ou faux? Le chien est un modèle de non-rongeur utilisé pour la tox : (2)
Embryo-foetale
Cardiaque (long QT)
Clinique
Non-clinique
Cardiaque (long QT) 4. Non-clinique
Qui suis-je? Je suis le modèle animal non-rongeur utilisé pour mesurer des éléments qui se rapportent aux systèmes cardiovasculaires et tégumentaire grâce aux ressemblances à l’humain (systèmes wise)
Le porc
Quel est le modèle animal non-rongeur utilisé si une barrière d’espèce existe?
Primate non-humain
Le pouvoir prédictif des études animales pour la tox humaine est : (2)
Au mieux 70%
Au mieux 30%
Proportionnel à la durée de l’étude
Non proportionnel à l’étude
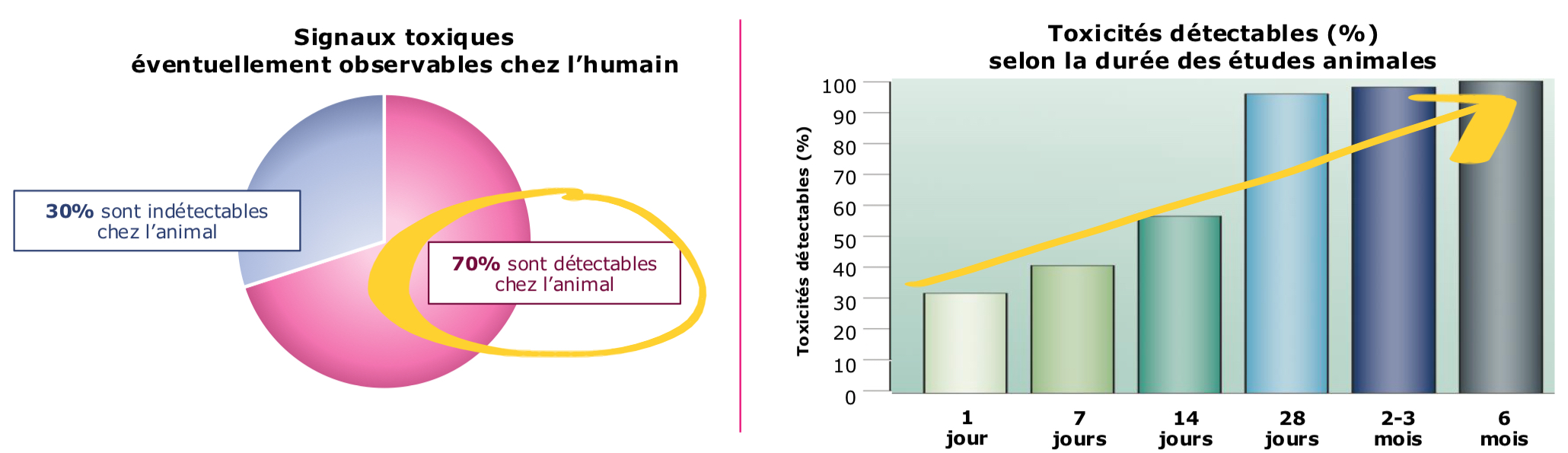
1 et 3
Vrai ou faux? La prédictivité des tox humaines détectées chez l’animal est constante
Faux, la prédictivité varie
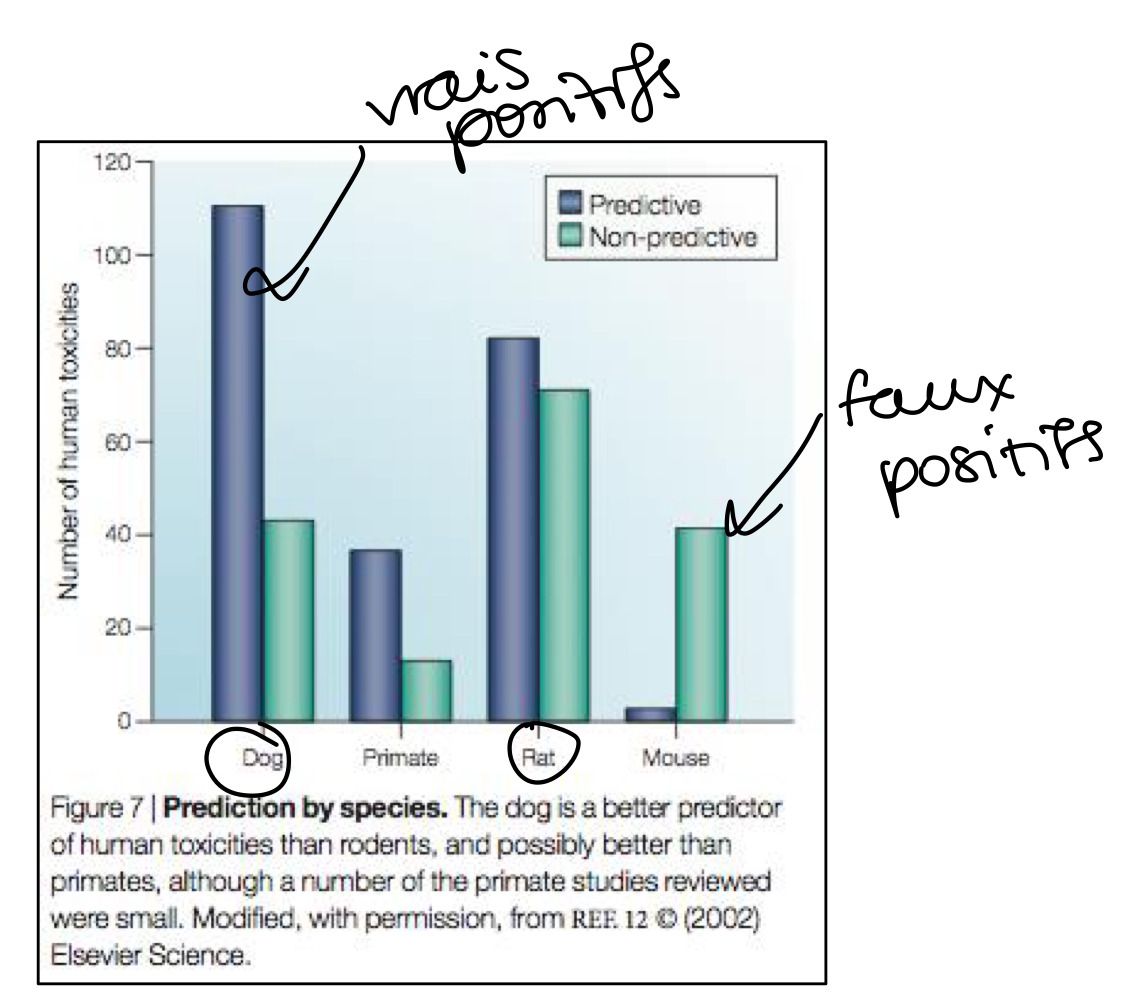
Quelles sont les espèces les plus sensibles?
Chien
Rat
Primate
Souris
Chien
Rat
Placez en ordre d’importance les espèces suivantes (le + important au - important) :
Rat
Primate
Souris
Chien
4-1-2-3
Vrai ou faux? Les souris sont l’espèce qui donne le + de faux positifs
Vrai
Quel système a le plus de concordance entre la toxicité humaine et animale?
Cardiovasculaire
Hépatique
Endocrine
Hématopoïétique
Hématopoïétique
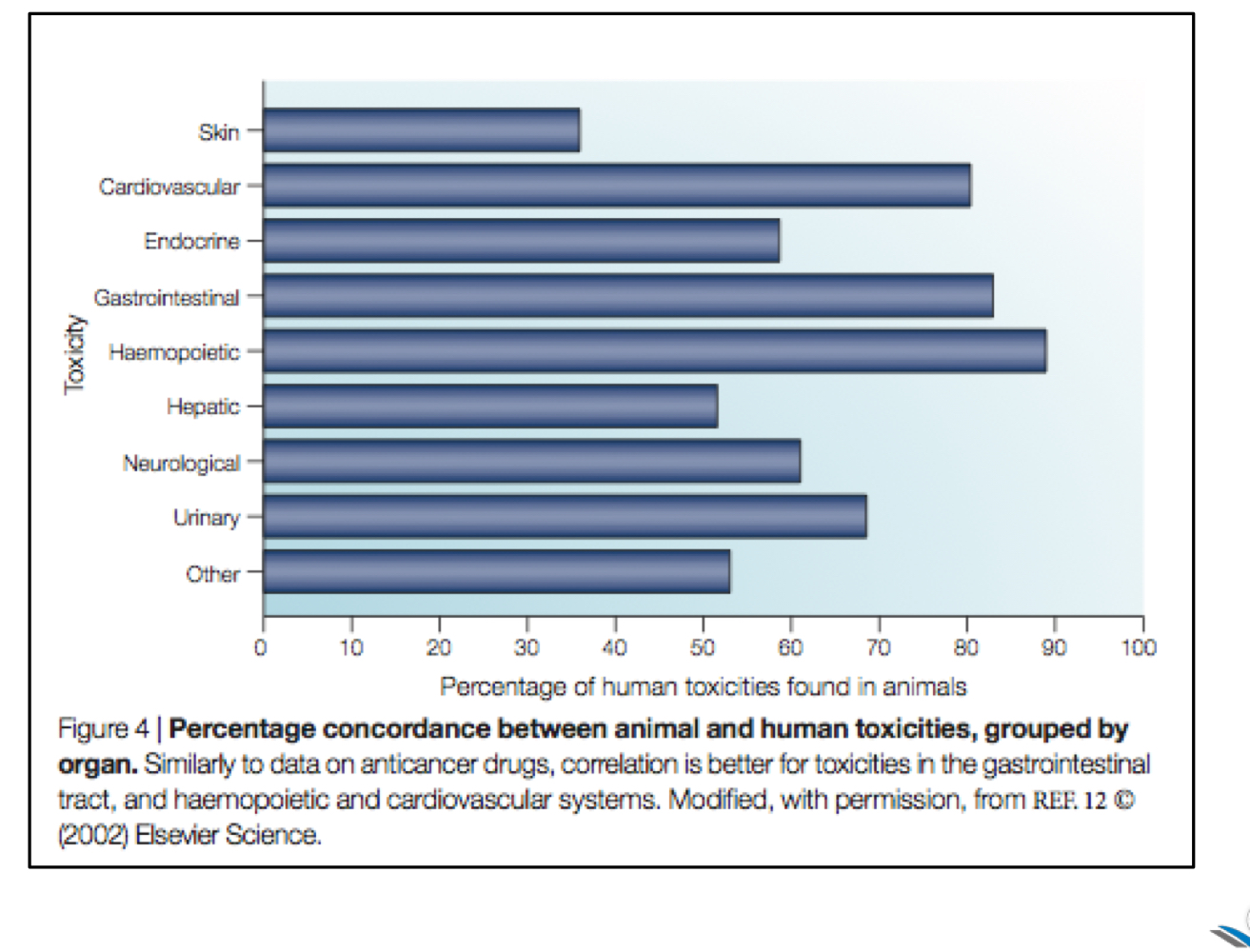
≈ 90%
Vrai ou faux? Dans le choix de l’animal, on recherche un profil PD et PK comparable à ce qui est attendu chez l’humain
Vrai
PD : Pas de barrière à l’espèce
Cible primaire présente et est sensible à la molécule optimisée pour une action chez l’humain
PK : Études de tox parallèles peuvent être requises pour évaluer des métabolites majeurs présents chez l’humain mais pas chez l’animal choisi
Quels sont les 3 “R” dans les critères de sélection des modèles animaux
Le plus possible on cherche à :
Réduire
Raffiner
Remplacer
L’usage des animaux
Vrai ou faux? Une fois l’animal utilisé, il ne peut être réutilisé
Faux, il peut être réutilisé
Vrai ou faux? Des animaux des 2 sexes doivent être évalués dans les études de tox
Vrai, sauf si le composé à tester est destiné à un seul sexe
Concernant le nombre d’animaux… Apprendre diapo

Comment sont appelées les cohortes séparées?
Cohortes satellites
Vrai ou faux? Les rongeurs requièrent des groupes d’étude plus petits
Faux, les non-rongeurs ont besoin de groupes plus petits. Les rongeurs sont habituellement des grosses cohortes
Études non GLP : Administration aiguë
Apprendre la diapo

Études non GLP : Administration de doses répétées
Diapo à apprendre

Dose range finding studies
La relation PK/PD est très importante pour le design des études TOX : On vise à déterminer 3 doses critiques, lesquelles?
MABEL
NOEL
NOAEL
Intermédiaire
MTD
NOAEL
Intermédiaire
MTD
Qui suis-je? Dose sans effet toxique. Calcul de la 1ère dose chez l’humain (petite molécule)
Dose maximale sans effet indésirable
MABEL
NOEL
NOAEL
Intermédiaire
MTD
NOAEL (no observed adverse effect level)
Qui suis-je? Je suis la dose la plus élevée qui ne donne rien chez l’animal in vivo (aucun effet pharmacologique ou toxicologique)
MABEL
NOEL
NOAEL
Intermédiaire
MTD
NOEL (No observed effect level)
Qui suis-je? Aucun effet biologique quel qu’il soit (in vitro ou in vivo). Calcul de la 1ère dose chez l’humain (médicaments biologiques)
MABEL
NOEL
NOAEL
Intermédiaire
MTD
MABEL (minimum anticipated biological effect level)
Quels sont les critères de cut off du MTD (maximum tolerated dose)? (2)
Perte de poids <10%
Perte de poids >10%
Aucun signe de morbidité pouvant réduire l’espérance de vie de l’animal
Aucun signe de morbidité pouvant réduire l’espérance de vie de l’humain
1 - Perte poids <10%
3 - Aucun signe de morbidité (non-réversible) pouvant réduire l’espérance de vie de l’animal
Lesquels parmi les suivants sont dans la catégorie des effets indésirables in vivo?
MABEL
NOEL
NOAEL
Intermédiaire
MTD
NOAEL
Intermédiaire
MTD
Lequel parmi les suivants sont dans la catégorie des effets thérapeutiques in vivo?
MABEL
NOEL
NOAEL
Intermédiaire
MTD
NOEL
Lequel parmi les suivants est dans la catégorie des effets biologiques appréhendés sur la base d’études in vitro?
MABEL
NOEL
NOAEL
Intermédiaire
MTD
MABEL
Vrai ou faux? Les humains métabolisent plus rapidement que les rats?
Faux, les rats métabolisent plus rapidement que les humains
Vrai ou faux? La limite acceptable de MTD est ≤ 50X la dose thérapeutique
Vrai
Concernant l’algorithme pour la dose maximale, quels sont les 4 situations desquels il faut “meet” au moins une pour dire que la dose testée est acceptable?
MTD
Exposure saturation (enzyme inhibée à 100%)
MFD (maximum feasible dose)
Mean exposure margin (50x clinical)
Quelles sont les données recueillies avant, pendant et après le test de la dose?

Qu’est-ce qu’on évalue avant la phase 1 dans les études non cliniques GLP (pour le dossier règlementaire) (3)
Génotoxicité in vitro
Toxicité à doses répétées avec évaluation toxicocinétique pendant 14-28 jours
Innocuité pharmacologique sur les systèmes vitaux (coeur, poumons, cerveau)
Qu’est-ce qu’on évalue avant la phase 2 dans les études non cliniques GLP (pour le dossier règlementaire) (7)
Génotoxicité in vivo
Données PK PD complétées
Toxicité à doses répétées prolongée avec histopathologie
Tolérance locale (TGI)
Innocuité pharmacologique (TGI)
Toxicocinétique : distribution et accumulation tissulaire (bilan flux de masse)
Carcinogénicité : doses répétées proches de la MTD
Qu’est-ce qu’on évalue avant la phase 3 dans les études non cliniques GLP (pour le dossier règlementaire) (1)
Études de toxicité sur la reproduction et le développement
Qu’est-ce qu’on évalue avant l’approbation dans les études non cliniques GLP (pour le dossier règlementaire) (4)
Toxicité à doses répétées prolongées avec histopathologie
Carcinogénicité : doses répétées proches de la MTD x 2 ans
Irritation locale par voie d’administration prévue et accidentelle (veineuse, artérielle…)
Études d’arrimage (bridging studies) au besoin si changement dans la formulation ou voie d’administration