CM1: Bio-énergétique thermodynamique
1/4
Earn XP
Description and Tags
Généralités Définitions systèmes transformation variables d’état fonctions d’état convention Principes de thermodynamique Energie libre de Gibbs (G) Définition Energie d’activation Calcul/Relation Utilisation (couplage)
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
5 Terms
Generalité
Par quelles réactions l’énergie externe devient exploitable par la cellule?
Anabolisme? Catabolisme?
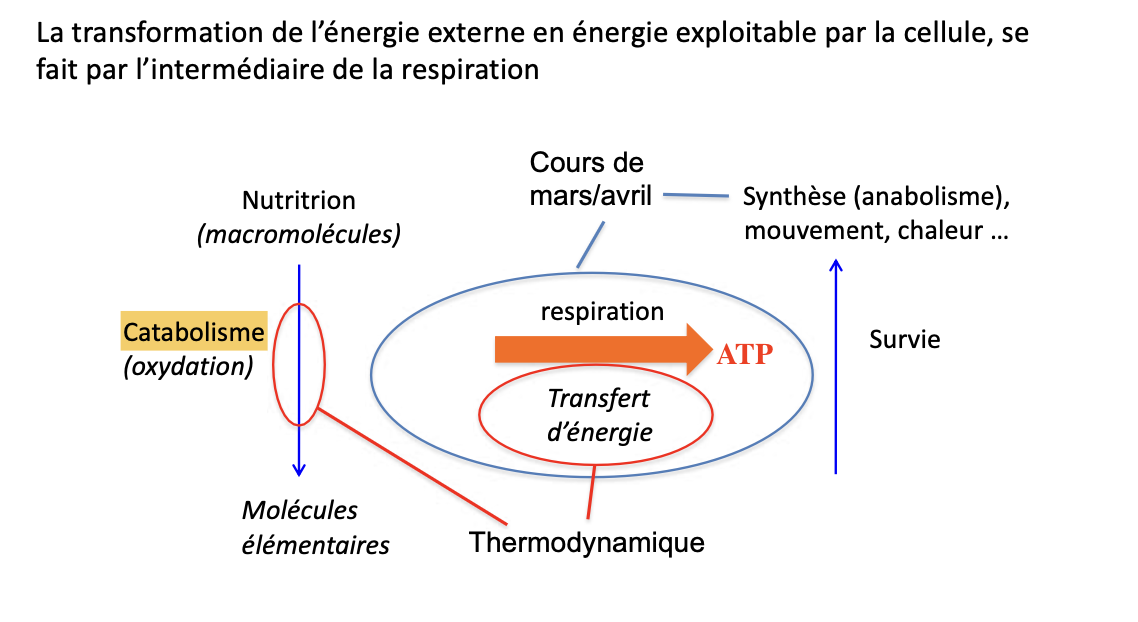
Definitions
Qu’est ce que la thermodynamique et sur quels concepts repose t elle?
Qu’est ce qu’un système? Quels sont les différents types de système?



Systeme fermé:
vers quel etat evolue un systeme fermé, quelle constante est associé à cet état ? un etat d’équilibre

Quelle est la différence entre K et Q?

Système ouvert:
vers quel etat evolue un systeme fermé, quelle phenome est associé à cet état en biologie? etat stationnaire, homéostasie
Definition : transformation
Quelles sont les deux grandes classes de transformations?
En biologie quelle conditions permettent ces réactions?
Donner des exemples de ces transformations?

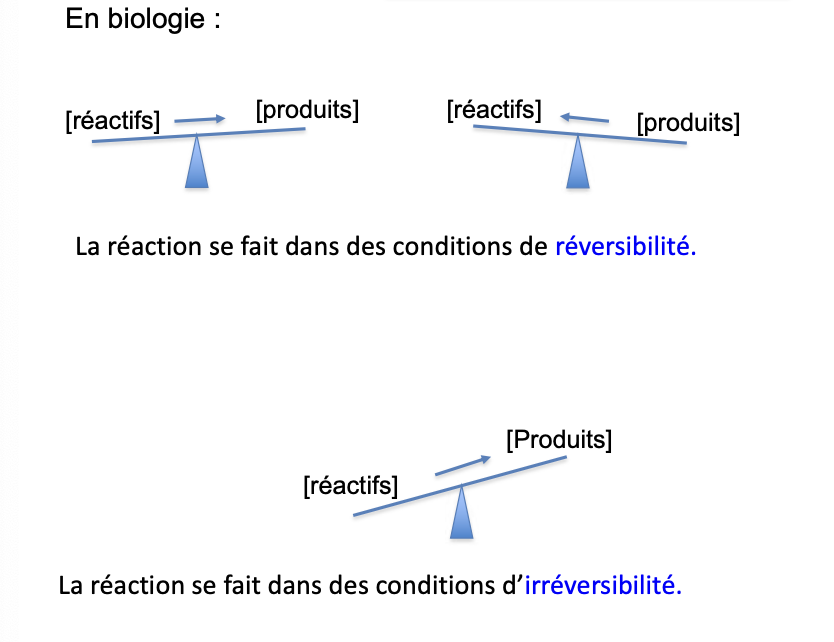
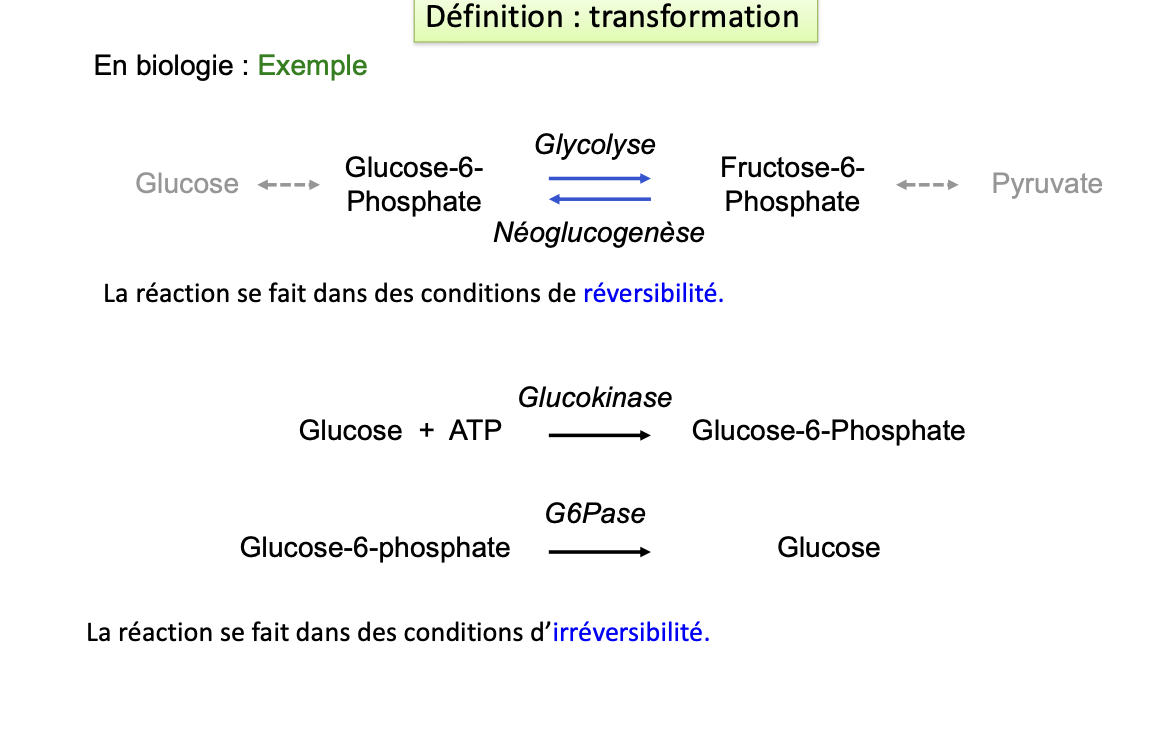

Définitions: variable, fonctions
Qu’est ce qu’une variable extensive? Intensive?
Qu’est ce qu’une fonction d’état? Quelles sont les fonctions d’état principales en thermodynamique? Quelles variables thermodynamique ne sont pas des fonctions d’état?
Donnez les définitions d’une reaction chimique, isotherme, isobare, isochore, isenthalpique, isentropique, adiabatique?
Par convention quel signe attribue t on à de l’énergie qui rentre dans le systeme et ce qui sort du syteme?







Quels sont les deuxx premiers principes de thermodynamique?
En considerant delta rH dans quel cas la reaction est elle endothermique? exothermique?
En considerant delta rG quand parle t. on de reaction exergonique? endeergonique?



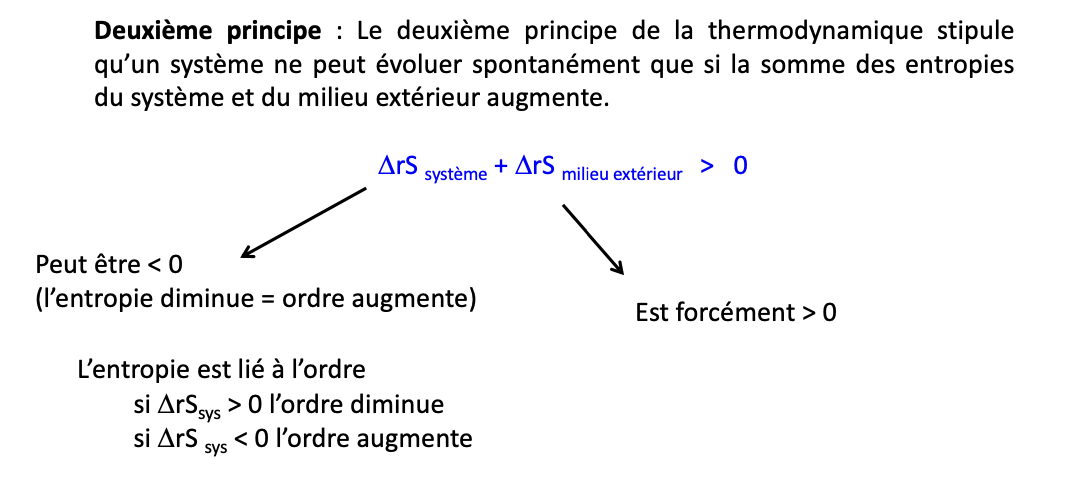
formule de l’énergie entropique:


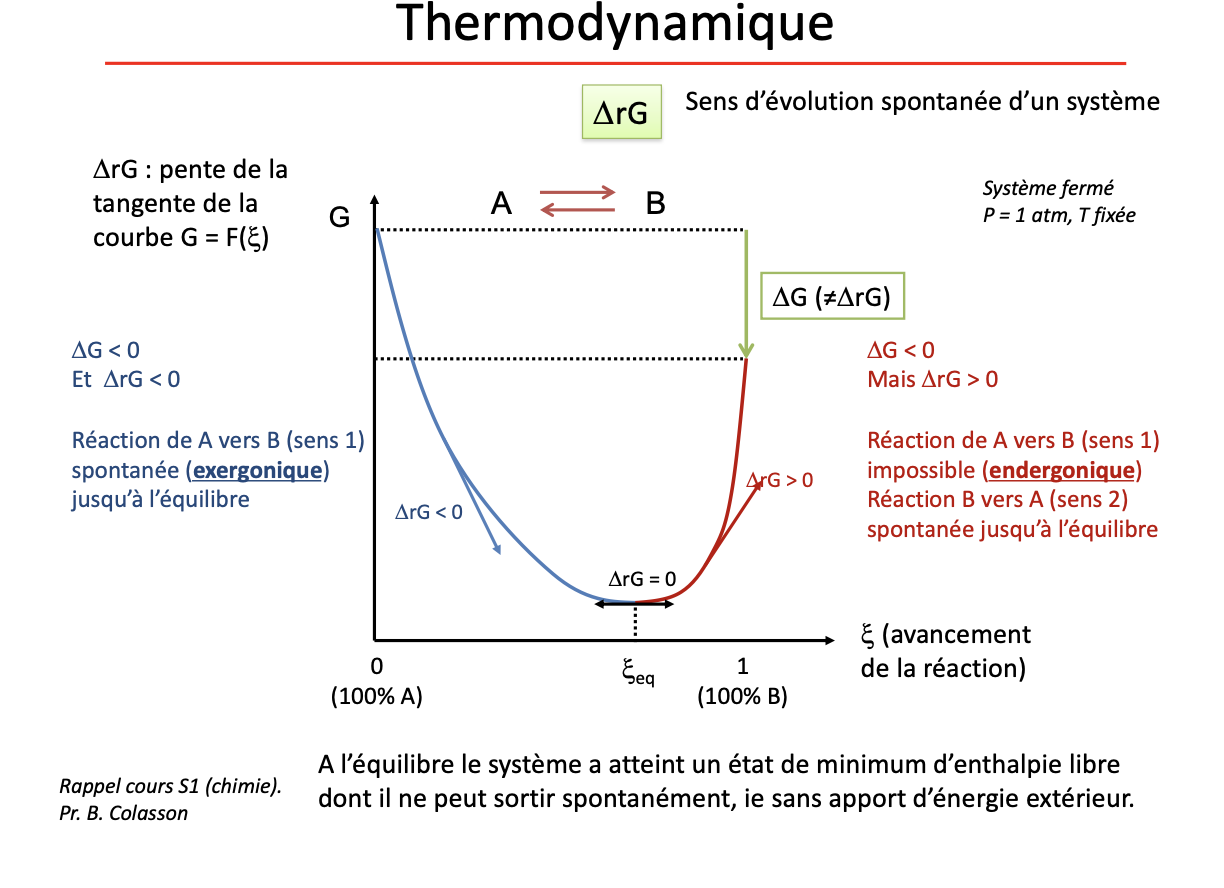
l’energie d’activation est diminue par un catalyseur