Frågor & Svar kap 2
1/49
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
50 Terms
Vilka två huvuddelar har det autonoma nervsystemet?
Sympatiska och parasympatiska nervsystemet.
Var har sympatiska nervsystemets preganglionära neuroner sitt ursprung?
Sympatiska nervsystemet (ditt "fight-or-flight"-system) har sina preganglionära neuroner (de första nervcellerna i signalvägen) i thoracolumbala ryggmärgen, alltså från ryggkotorna T1 till L3.
Förenklat exempel:
Tänk dig att du blir skrämd av ett högt ljud. Ditt sympatiska nervsystem aktiveras direkt:
Preganglionära neuroner i T1–L3 skickar en signal till en ganglion (en klustercell nära ryggmärgen).
Därifrån tar postganglionära neuroner över och för signalen till målorganet (t.ex. hjärtat, lungorna).
Resultatet blir att ditt hjärta slår snabbare, dina pupiller vidgas, och du är redo att springa eller kämpa!
Varför just T1–L3?
Thoracal (T1–T12): Kontrollerar organ i bröstet/buken (t.ex. hjärta, lungor).
Lumbal (L1–L3): Kontrollerar nedre delen av kroppen (t.ex. blodkärl i benen).
Exempel på funktioner:
T1–T4: Ökar hjärtfrekvensen vid stress.
T5–L3: Styr blodflöde till muskler (t.ex. när du springer).
Nyckelpoäng:
"Thoracolumbal" = Bröst- och ländryggens ryggkotor (T1–L3).
Preganglionära nervtrådar är korta (jämfört med parasympatiska som är långa).
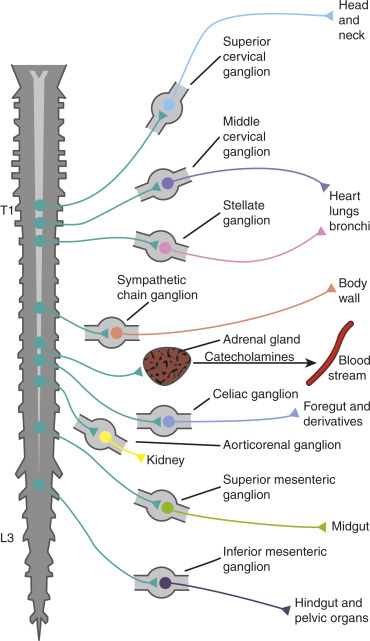
Vilka kallas parasympatiska nervsystemets preganglionära neuroner?
Parasympatiska nervsystemet (ditt "vilande och smältningssystem") har sina preganglionära neuroner (de första nervcellerna) i craniosacrala området, alltså:
Cranialnerverna III, VII, IX, X (i hjärnan)
Sakrala segmenten S2–S4 (i korsbenet, nedre delen av ryggmärgen).
Förenklat exempel:
Tänk dig att du ätit en stor måltid och vilar:
Cranialnerverna (t.ex. vagusnerven, X) skickar långa preganglionära trådar till ganglion nära eller i organen (t.ex. magen, hjärtat).
Postganglionära neuroner (korta) frisätter signalsubstanser som saktar ner hjärtat och stimulerar matsmältningen.
Sakrala delarna (S2–S4) styr t.ex. urinblåsan och tarmar:
När du är avslappnad och behöver kissa, aktiveras parasympatiska signaler härifrån.
Varför "craniosacral"?
Craniala delar (III, VII, IX, X):
III (Oculomotorius): Styr pupillernas förminskning (t.ex. i mörker).
VII (Facialis): Stimulerar tår- och salivkörtlar (t.ex. när du luktar mat).
IX (Glossopharyngeus): Salivproduktion i munhålan.
X (Vagus): 90% av parasympatisk aktivitet! Sänker hjärtfrekvens, stimulerar tarmar.
Sakrala delar (S2–S4):
Styr urinblåsa, könsorgan, och nedre tarmen (t.ex. avslappning vid urinering).
Nyckelpoäng:
Craniosacral = Hjärnan + nedre ryggmärgen.
Preganglionära nervtrådar är långa (jämfört med sympatiska som är korta).
Målorgan: Hjärta, mag-tarmkanal, urinblåsa, könsorgan.
Exempel på funktioner:
Vagusnerven (X) saktar hjärtat när du sover.
S2–S4 hjälper dig att kissa utan stress.
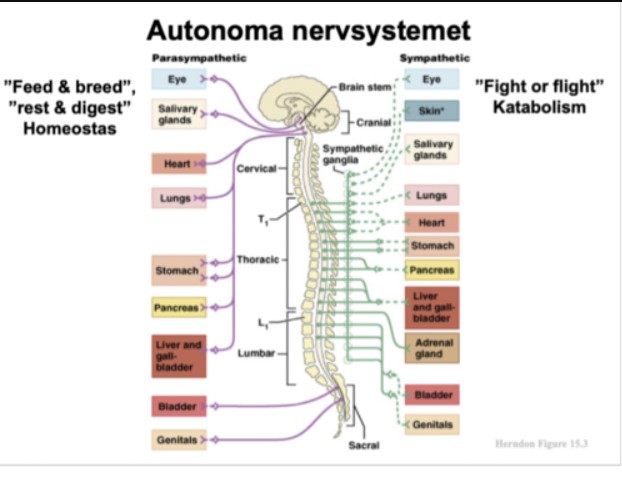
Vad är skillnaden mellan pre- och postganglionära axoner i sympatiska systemet?
Preganglionära axoner är korta, postganglionära är långa.
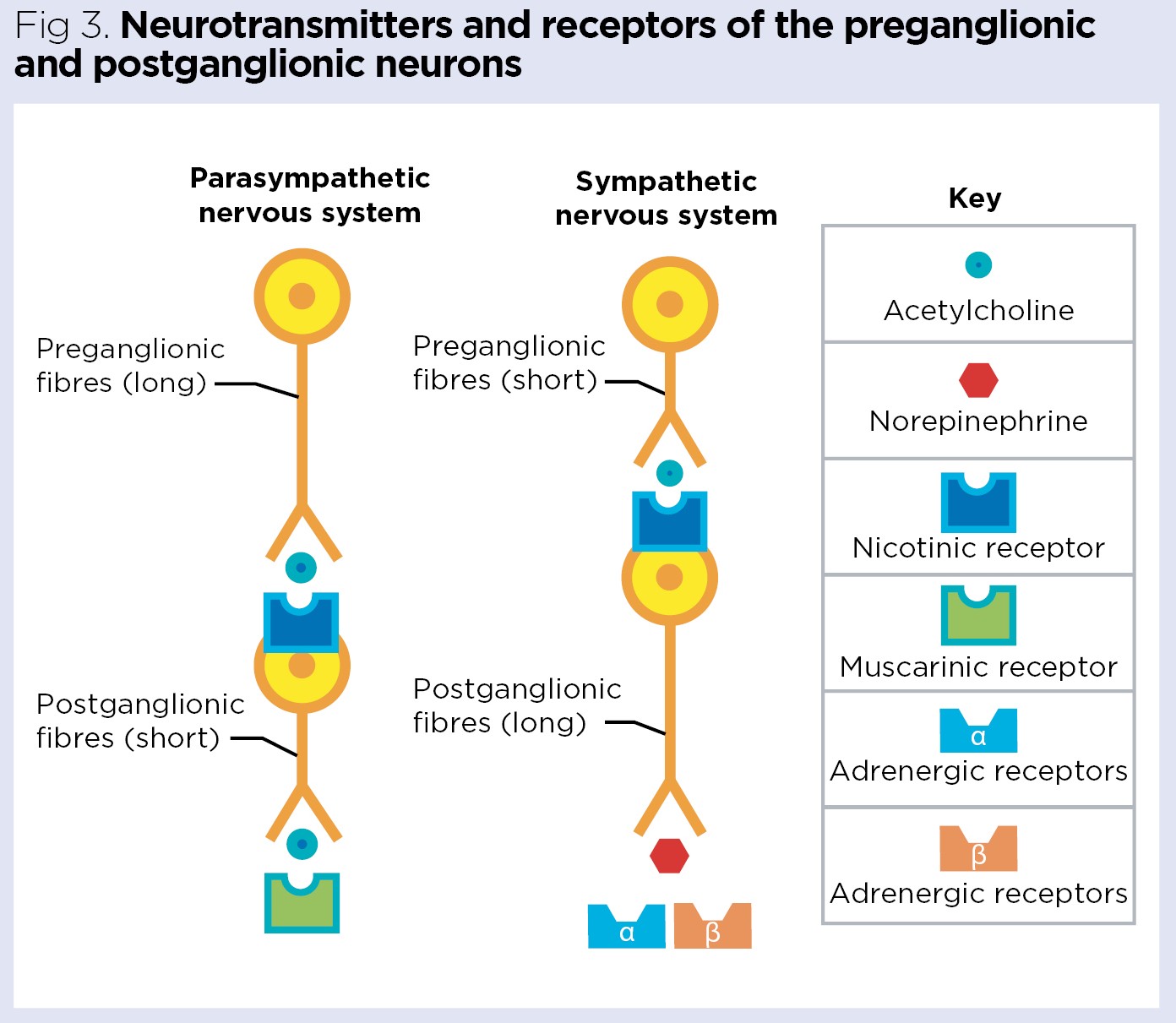
Vilken neurotransmittor använder alla preganglionära neuroner och varför?
Acetylkolin (ACh).
Varför just acetylkolin (ACh)?
Evolutionär konservering:
ACh är en av de äldsta och mest grundläggande neurotransmittorerna i nervsystemet. Det används även i det somatiska nervsystemet (t.ex. för muskelkontraktion), vilket gör det till ett "universellt" verktyg för snabb signalering.Snabb signalering via nikotinreceptorer:
Preganglionära neuroner frisätter ACh som binder till nikotinreceptorer (ligandstyrda jonkanaler) på postganglionära neuroner. Dessa receptorer öppnas direkt, vilket skapar en omedelbar depolarisering – perfekt för att aktivera "fight-or-flight" eller "rest-and-digest" snabbt.Enkelhet och effektivitet:
Genom att använda samma neurotransmittor i båda delarna av det autonoma nervsystemet minskar komplexiteten. Skillnaderna mellan sympatiska och parasympatiska effekter kommer istället från:Postganglionära neuroners neurotransmittor (t.ex. noradrenalin i sympatiskt, ACh i parasympatiskt).
Målorganens receptorer (t.ex. muskarinreceptorer för parasympatiskt ACh).
Exempel för tydlighet:
Sympatisk aktivitet:
Preganglionär neuron (ACh) → Nikotinreceptor i ganglion → Postganglionär neuron (noradrenalin) → Målorgan (t.ex. hjärta).Parasympatisk aktivitet:
Preganglionär neuron (ACh) → Nikotinreceptor i ganglion → Postganglionär neuron (ACh) → Målorgan (t.ex. mag-tarmkanalen).
Vad händer om ACh blockeras?
Om ACh-signaleringen störs (t.ex. av nikotinblockerare som hexamethonium), påverkas både sympatiska och parasympatiska funktioner:
Ingen signalering i ganglier → Ingen "fight-or-flight" eller "rest-and-digest".
Resultat: Lägre blodtryck, sänkt hjärtfrekvens, förlamad tarmaktivitet.
Nyckelpoäng:
ACh är en universell startknapp för det autonoma nervsystemet.
Nikotinreceptorer säkerställer snabb respons utan mellanled (ingen second messenger).
Skillnaden mellan sympatiskt/parasympatiskt ligger i postganglionära neuroner, inte preganglionära.
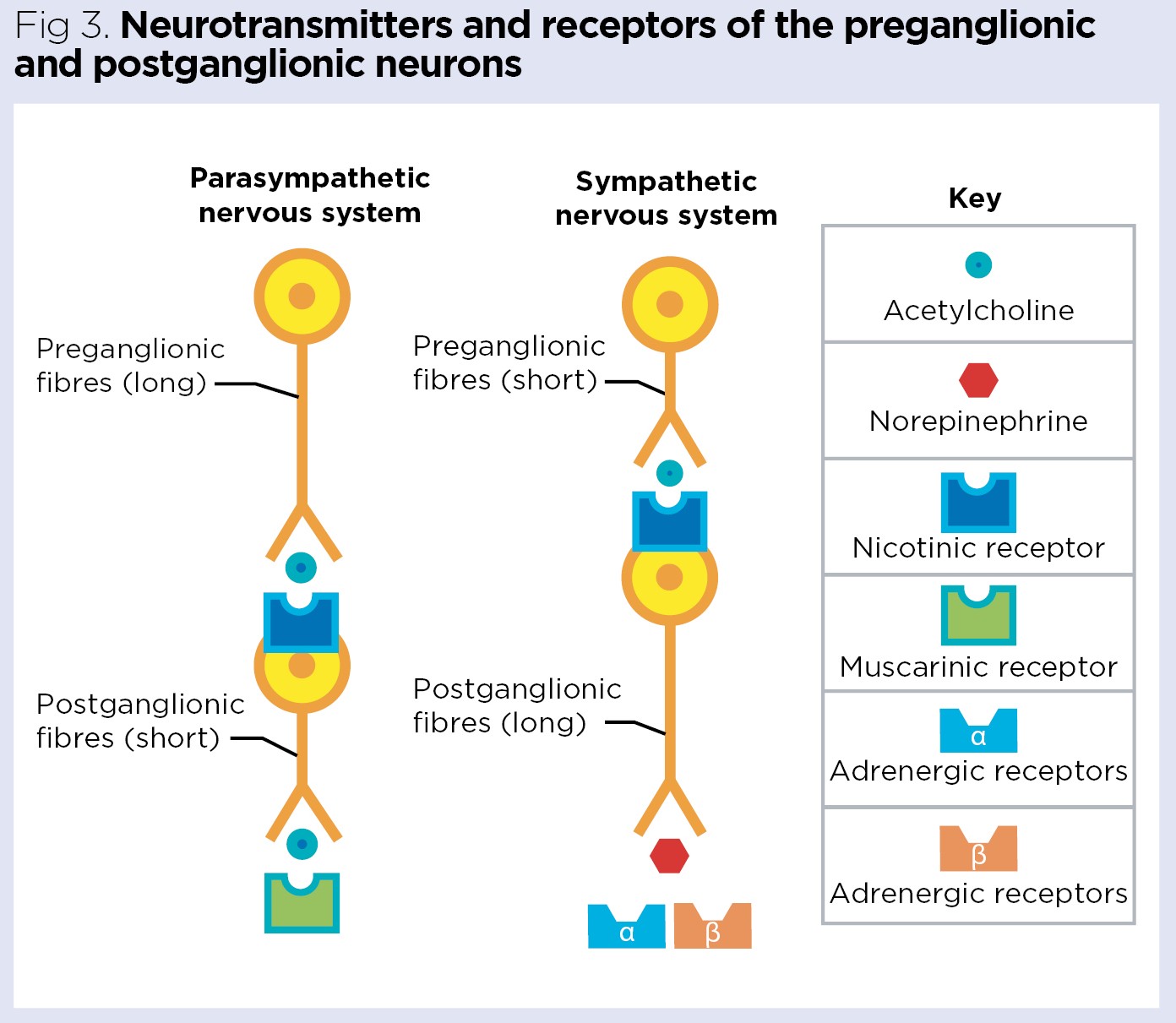
Vilken typ av receptor finns på postganglionära sympatiska neuroner?
Nicotinreceptorer (N₂).
Vilken neurotransmittor frisätts av sympatiska postganglionära neuroner?
Sympatiska postganglionära nervceller använder mest noradrenalin som signalsubstans. Men det finns ett kul undantag:
Huvudregel:
Noradrenalin används för att:
Gör hjärtat snabbare 💓 (t.ex. när du är stressad).
Dra ihop blodkärl 🩸 (höjer blodtrycket).
Öka energin i kroppen 🔋 (som att bryta ner socker i levern).
Undantag:
Svettkörtlarna använder acetylkolin (ACh) istället!
Varför? För att svettning behöver en annan typ av signal 🌀 (ACh ger mer exakt kontroll).
Exempel: När du är nervös eller har feber → ACh gör att du svettas 💦.
Varför spelar detta roll?
Om du tar läkemedel som blockar noradrenalin (t.ex. betablockerare mot högt blodtryck) → påverkar inte svettningen, eftersom den använder ACh!
Sammansfattning:
Sympatiska nervceller: Noradrenalin = huvudregel.
Undantag: ACh i svettkörtlarna (för att kunna svettas när du är stressad).
Vilken effekt har sympatisk aktivering på hjärtat?
Sympatisk aktivering påverkar hjärtat på två huvudsakliga sätt:
Ökar hjärtfrekvensen (positiv kronotrop effekt):
Noradrenalin (sympatisk signalsubstans) binder till β₁-receptorer i sinusknutan (hjärtats "pacemaker").
Detta ökar hur snabbt hjärtcellerna depolariserar → fler hjärtslag per minut.
Ökar kontraktionskraften (positiv inotrop effekt):
Samma β₁-receptorer i hjärtmuskelceller aktiveras.
Leder till starkare sammandragningar → mer blod pumpas ut vid varje slag.
Varför sker detta?
Det är en del av kroppens "fight-or-flight"-respons. När du är stressad, rädd, eller tränar behöver hjärtat leverera mer syre och energi till musklerna.
Exempel:
Om du springer från en björn → sympatiska nervsystemet kickar igång → hjärtat slår snabbare och hårdare för att du ska kunna fly.
Vad händer om β₁-receptorer blockeras?
T.ex. med betablockerare (som metoprolol):
Hjärtfrekvensen sänks.
Kontraktionskraften minskar (används vid högt blodtryck/hjärtsvikt).
Enkelt sagt: Sympatisk aktivering gör hjärtat till en effektivare pump! 😊
Vad är 'fight or flight'-responsen?
Sympatisk aktivering vid stress: ökad puls, blodtryck och energi.
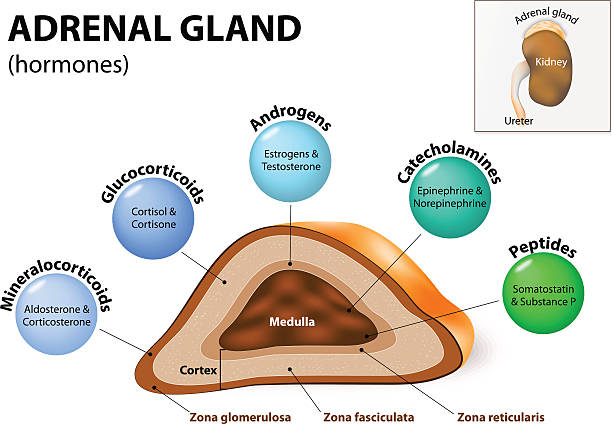
Vilken del av binjurarna producerar adrenalin?
Adrenalin produceras i binjuremärgen (den inre delen av binjuren), medan den yttre delen (binjurebarken) producerar hormoner som kortisol. Binjuremärgen släpper ut 80% adrenalin och 20% noradrenalin direkt i blodet vid stress.
Förtydligande:
Binjurens uppdelning:
Binjuremärg (innersta del):
Består av nervliknande celler.
Frisätter adrenalin/noradrenalin vid sympatisk aktivering (t.ex. stress, rädsla).
Binjurebark (yttre del):
Producerar kortisol, aldosteron och könshormoner.
Varför just binjuremärgen?
Binjuremärgen är egentligen en förlängning av det sympatiska nervsystemet. När det sympatiska systemet aktiveras, skickar det signaler till binjuremärgen som en "nödlösning" för att öka hormonutsläpp i hela kroppen snabbt.
Exempel på funktion:
När du får en chock (t.ex. en bil tutar högt):
Sympatiska nervsignaler når binjuremärgen.
Adrenalin/noradrenalin pumpas ut i blodet.
Effekter:
💓 Hjärtat slår snabbare.
💪 Blod flödar till musklerna.
🧠 Pupiller vidgas (för bättre fokus).
Vad händer utan binjuremärg?
Utan adrenalin/noradrenalin från binjuremärgen skulle kroppen inte kunna mobiliseras lika snabbt vid akut stress – du skulle bli mindre redo att "kämpa eller fly".
Enkelt sagt: Binjuremärgen är din kropps nödknapp för stress! 😊
Vilken neurotransmittor använder parasympatiska postganglionära neuroner?
Acetylkolin (ACh).
Vilken receptor aktiveras i effektororgan av parasympatiska neuroner?
Muskarinreceptorer (M).
Vad händer med matsmältningen vid parasympatisk aktivering?
Ökar motilitet och sekretion i mag-tarmkanalen.
Vilken nerv är viktigast för parasympatisk kontroll av hjärtat och lungor?
Nervus vagus (kranialnerv X).
Vilken effekt har parasympatisk aktivering på pupillen?
Pupillkontraktion (mios) via muskarinreceptorer.
Vilka receptorer binder adrenalin/noradrenalin?
Adrenerga receptorer (α₁, α₂, β₁, β₂).
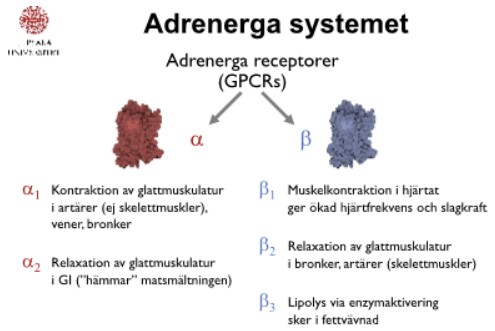
Vad gör α₁-receptorer i blodkärl?
Vasokonstriktion (blodtryckshöjning).
Vilken receptor ansvarar för bronkdilatation?
β₂-receptorer.
Vad är skillnaden mellan nikotin- och muskarinreceptorer?
Nikotinreceptorer är jonkanaler; muskarinreceptorer är G-protein-kopplade.
Vilken receptor blockerar atropin?
Muskarinreceptorer.
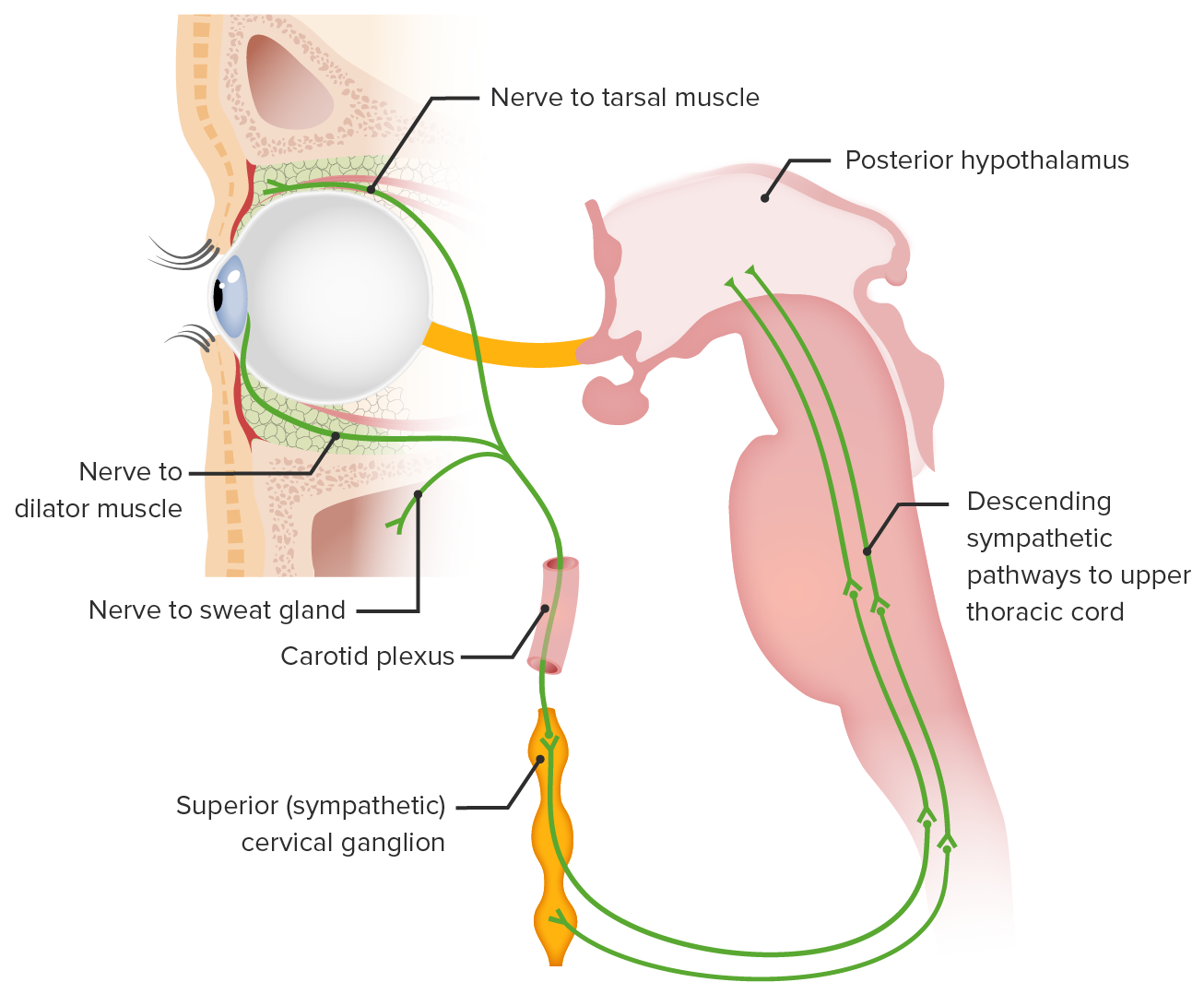
Vad orsakar Horner syndrom?
Horner syndrom uppstår på grund av en skada eller ett avbrott i de sympatiska nervbanorna som styr ansiktet. Detta leder till den klassiska triaden:
Ptos (hängande ögonlock)
Mios (liten pupill)
Anhidros (minskad eller ingen svettning på den drabbade sidan)
Var kan skadan vara lokaliserad?
Den sympatiska nervbanan till ansiktet består av tre neuroner. Skador kan uppstå längs hela dess väg:
Första neuronet (hjärnan → ryggmärg T1–T3)
Orsaker: Stroke, tumör i hypotalamus/hjärnstammen, ryggmärgsskada
Andra neuronet (ryggmärg → halsganglion)
Orsaker: Pancoast-tumör (i lungtoppen), trauma, skada vid halskirurgi
Tredje neuronet (halsganglion → ansikte)
Orsaker: Carotisdissektion (blödning i halsartären), migrän, infektion
Vanliga orsaker i kliniken
Pancoast-tumör (lungcancer som trycker på nervbanan)
Carotisdissektion (t.ex. efter whiplash eller spontant)
Skada vid halskirurgi (t.ex. vid sköldkörteloperation)
Stroke eller multipel skleros (MS) (skador i hjärnstammen)
Medfött (kan uppstå hos nyfödda efter förlossningstrauma)
Varför uppstår dessa symtom?
Ptos: Sympatiska nerver aktiverar Musculus tarsalis, som hjälper till att hålla ögonlocket uppe. Vid skada uteblir signalen → ögonlocket hänger.
Mios: Sympatiska nerver styr pupillens vidgning genom Musculus dilator pupillae. Vid skada förloras denna funktion → pupillen förblir liten.
Anhidros: Sympatiska nerver kontrollerar svettkörtlarna. Vid skada minskar svettproduktionen → torr hud på den drabbade sidan.
Diagnostik
Läkare kan använda kokainögondroppar för att bekräfta Horner syndrom:
Friska ögon: Pupillen vidgas.
Horner syndrom: Pupillen vidgas inte, eftersom den sympatiska funktionen saknas.
Sammanfattning
Horner syndrom beror på en skada i den sympatiska nervbanan och kännetecknas av hängande ögonlock, liten pupill och torr hud på den drabbade sidan. Vanliga orsaker inkluderar tumörer, trauma och kärlsjukdomar. 😊
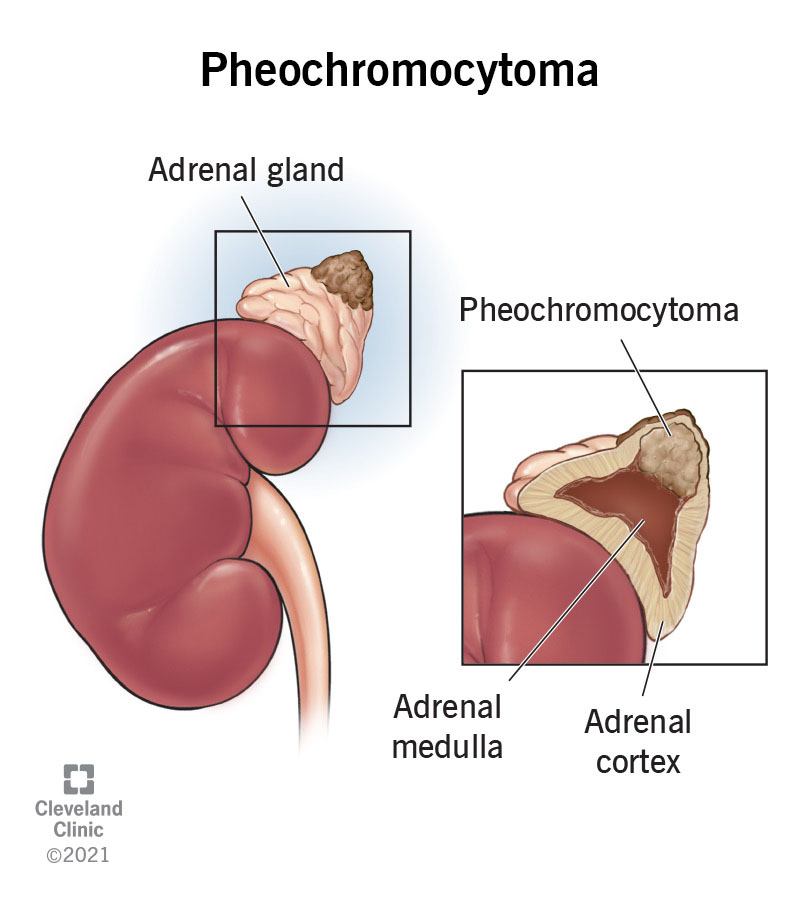
Vad är ett feokromocytom?
Feokromocytom är en tumör i binjuremärgen (den inre delen av binjuren) som producerar för mycket katekolaminer – främst adrenalin och noradrenalin. Detta leder till attacker av extremt högt blodtryck, hjärtklappning och andra symtom, som kan vara livshotande om de inte behandlas.
Enkelt förklarat:
Var? I binjuremärgen, där adrenalin och noradrenalin normalt produceras.
Vad gör den? Tumören släpper ut stora mängder stresshormoner i blodet, vilket triggar kroppens "fight-or-flight"-respons – oavsett om det finns en verklig fara eller inte.
Vanliga symtom:
✅ Extremt högt blodtryck (över 200/120 mmHg) i attacker
✅ Hjärtklappning 💓 (känns som att hjärtat ”rusar”)
✅ Kraftig svettning 💦 (ofta kallsvett)
✅ Huvudvärk 🤕 (orsakad av det höga blodtrycket)
✅ Skakningar/ångest 😰 (kroppen upplever en "falsk stressreaktion")
✅ Blekhet eller rodnad i ansiktet
Orsaker:
🔹 Sporadisk (ingen känd ärftlig orsak – vanligast)
🔹 Ärftlig (kan förekomma vid sjukdomar som MEN 2, Von Hippel-Lindau)
Tumören är oftast godartad (90%), men i vissa fall elakartad (10%).
Diagnostik:
🩸 Blod- och urintest: Mäter nivåer av metanefriner (nedbrytningsprodukter av adrenalin/noradrenalin).
💻 CT/MR: Hittar tumörens placering.
🧬 Genetisk testning: Vid misstanke om ärftlighet.
Behandling:
🔹 Kirurgi: Tar bort tumören (botande om den är lokaliserad).
🔹 Läkemedel före operation: Blockerar effekten av adrenalin/noradrenalin (t.ex. alfablockerare som fenoxybenzamin).
🔹 Livsstilsanpassning: Undvik stress, koffein och fysisk överansträngning som kan trigga attacker.
Varför är feokromocytom farligt?
⚠ Hypertensiv kris: Extremt högt blodtryck kan leda till stroke, hjärtsvikt eller njurskada.
⚠ Hjärtarytmier: Överskott av noradrenalin kan orsaka livshotande hjärtrytmrubbningar.
Regeln om "10:or" (lätt att komma ihåg!):
🔟 10% är elakartade
🔟 10% är bilaterala (finns i båda binjurarna)
🔟 10% upptäcks utanför binjurarna (t.ex. i buken)
🔟 10% är ärftliga
Sammanfattning:
Feokromocytom = en "adrenalinpumpande" tumör som orsakar plötsliga attacker av skräckliknande symtom. Diagnosen är livsviktig att ställa – behandling kan rädda liv! 😊
Varför ger feokromocytom högt blodtryck?
Ökad noradrenalin frisättning → vasokonstriktion och ökad hjärtverkan.
Vad är Shy-Drager syndrom?
Shy-Drager syndrom är ett äldre namn för en neurodegenerativ sjukdom som numera kallas multisystematrofi (MSA) med dominant autonom dysfunktion (MSA-A). Det innebär en progressiv nedbrytning av neuroner i det autonoma nervsystemet (som styr ofrivilliga funktioner) och motoriska systemet, vilket leder till svåra symptom. Här är en enkel förklaring:
Huvudsymptom:
Svår dysautonomi (autonom nervsystemsbrott):
Orthostatisk hypotension: Kraftigt fall i blodtryck vid upprätt ställning → yrsel/svimning.
Urinproblem: Svårt att tömma blåsan eller inkontinens.
Sexuell dysfunktion: Impotens hos män.
Svettningsstörningar: Överdriven eller ingen svettning.
Magsmärtor/constipation.
Motoriska symptom (liknar Parkinsons sjukdom):
Stelhet, långsamhet, skakningar (Parkinsonism).
Balansproblem och falltendens.
Andra neurologiska symptom:
Sväljsvårigheter, hes röst.
Dubbelseende eller synproblem.
Orsak:
Okänd, men orsakas av felvikning av alfa-synuklein (ett protein som klumpar ihop sig i hjärncellerna).
Skador i basala ganglier, cerebellum och autonoma nervsystemet.
Skillnad mot Parkinsons sjukdom:
Shy-Drager/MSA har tidig autonom dysfunktion (Parkinsons utvecklar detta sent).
Motoriska symptom svarar dåligt på levodopa (Parkinson-medicin).
Diagnostik:
Blodtrycksmätning vid ställningsändring (orthostatiskt test).
MRI-hjärna: Visar förändringar i cerebellum/basala ganglier.
Urinkateterisering (vid blåsproblem).
Behandling:
Ingen bot, men symptomlindring:
Fludrocortison eller midodrin för att höja blodtrycket.
Kompressionsstrumpor mot yrsel.
Kateter för urinproblem.
Fysioterapi mot stelhet.
Prognos:
Progressivt försämrande.
Medianöverlevnad: 6–10 år efter insjuknande.
Sammanfattning:
Shy-Drager/MSA är en obotlig nervsjukdom som förstör kroppens automatiska funktioner (blodtryck, urin, svettning) och ger motoriska symptom. Den är sällsynt och svårbehandlad. 😢
Varför ger atropin torr mun och pupilldilatation?
Blockering av muskarinreceptorer i salivkörtlar och pupillmuskler.
Vilket enzym omvandlar noradrenalin till adrenalin?
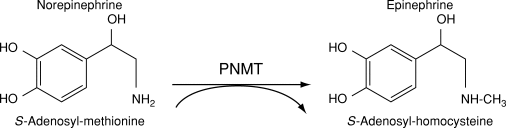
Enzymet som omvandlar noradrenalin till adrenalin heter phenylethanolamin-N-metyltransferas (PNMT). Här är en enkel förklaring till varför:
Vad gör PNMT?
PNMT lägger till en metylgrupp (CH₃) från S-adenosylmetionin (SAM) till noradrenalin, vilket skapar adrenalin. Detta är det sista steget i syntesen av adrenalin i kroppen.
Var finns PNMT?
PNMT finns främst i binjuremärgen (adrenalmedulla). Det är därför binjuremärgen är huvudkällan till adrenalin, medan sympatiska nervändar mest släpper ut noradrenalin.
Varför är detta viktigt?
Adrenalin är kroppens "nödhormon" vid stress (fight-or-flight).
Utan PNMT skulle vi inte kunna producera adrenalin, vilket försvagar förmågan att hantera akut stress.
Reglering av PNMT:
Kortisol (från binjurebarken) stimulerar PNMT-aktivitet. Detta förklarar varför binjuremärgen och -barken ligger nära varandra – de samarbetar för stressresponsen!
Exempel på processen:
Steg 1: Tyrosin → DOPA (via tyrosinhydroxylas).
Steg 2: DOPA → Dopamin (via DOPA-dekarboxylas).
Steg 3: Dopamin → Noradrenalin (via dopamin-beta-hydroxylas).
Steg 4: Noradrenalin → Adrenalin (via PNMT).
Skillnad mot andra enzymer:
PNMT är specifikt för adrenalin, medan t.ex. tyrosinhydroxylas behövs i alla katekolaminers syntes.
Sammanfattning:
PNMT är det avgörande enzymet som gör noradrenalin till det mer potenta adrenalin – en kritisk del av vår överlevnadsmekanism! 😊
Vilken second messenger aktiverar β₁-receptorer?
β₁-receptorer aktiverar cAMP (cykliskt adenosinmonofosfat) som en second messenger genom att stimulera enzymet adenylcyklas. Här är en steg-för-steg-förklaring:
Vad händer när β₁-receptorer aktiveras?
Ligandbindning: Noradrenalin eller adrenalin binder till β₁-receptorn (t.ex. i hjärtat).
Gs-proteinet aktiveras: Receptorn aktiverar ett Gs-protein (stimulerande G-protein).
Adenylcyklas aktiveras: Gs-proteinet aktiverar enzymet adenylcyklas i cellmembranet.
cAMP bildas: Adenylcyklas omvandlar ATP till cAMP, som fungerar som second messenger.
Effekter via PKA: cAMP aktiverar proteinkinas A (PKA), som fosforylerar målproteiner, vilket leder till:
Ökad hjärtfrekvens (positiv kronotropi).
Stärkta hjärtsammandragningar (positiv inotropi).
Varför just cAMP?
cAMP är en snabb och effektiv signalöverförare för β₁-receptorns effekter, särskilt i hjärtat.
Systemet är evolutionärt konserverat – används av många hormoner och neurotransmittorer (t.ex. glucagon, TSH).
Skillnad mot andra receptorer:
α₁-receptorer: Använder IP3/DAG som second messenger.
β₂-receptorer: Använder också cAMP, men har andra effekter (t.ex. bronkdilatation).
Klinisk relevans:
Betablockerare (t.ex. metoprolol) blockerar β₁-receptorer → minskar cAMP → sänkt hjärtfrekvens/blodtryck.
Toxiner: Vissa bakterietoxiner (t.ex. kolera) kan manipulera cAMP-nivåer.
Sammanfattning:
β₁-receptorer → Gs-protein → adenylcyklas → cAMP → PKA → ökad hjärtprestation. 😊
Vad gör IP₃ i α₁-receptorers signalväg?
IP₃ (inositol-1,4,5-trisfosfat) i α₁-receptorers signalväg fungerar som en "nyckel" som öppnar kalciumförråd i cellen. Här är en enkel förklaring av hur det fungerar:
Steg-för-steg:
Aktivering av α₁-receptor:
När noradrenalin/adrenalin binder till en α₁-receptor (t.ex. i blodkärlens glatta muskelceller) aktiveras ett Gq-protein.Frisättning av IP₃:
Gq-proteinet aktiverar enzymet fosfolipas C (PLC), som bryter ner PIP₂ (ett fett i cellmembranet) till IP₃ och DAG.IP₃ släpper ut kalcium (Ca²⁺):
IP₃ reser till endoplasmatiska retiklet (ER, cellens kalciumlager) och binder till IP₃-receptorer. Dessa öppnar sig och släpper ut Ca²⁺ i cytoplasman.Effekter av Ca²⁺:
Glatta muskler drar ihop sig (t.ex. blodkärl vid vasokonstriktion → högre blodtryck).
Enzym aktiveras (t.ex. proteinkinas C med hjälp av DAG).
Varför är detta viktigt?
IP₃/Ca²⁺-systemet är en snabb och kraftfull signalväg för att få celler att reagera direkt, som vid stress när blodtrycket måste öka.
Exempel i kroppen:
När du blir arg eller rädd:
α₁-receptorer i blodkärl aktiveras → IP₃ frisätts.
Ca²⁺ frigörs → blodkärl dras samman.
Resultat: Blodtrycket stiger, mer blod pumpas till musklerna! 💪
Skillnad mot β-receptorer:
β-receptorer använder cAMP som second messenger (för energimobilisering).
α₁-receptorer använder IP₃/Ca²⁺ (för snabba strukturella ändringar).
Sammanfattning:
IP₃ i α₁-signalvägen = kalciumutlösare som gör att celler kan reagera omedelbart, t.ex. genom muskelkontraktion eller hormonutsöndring. 😊
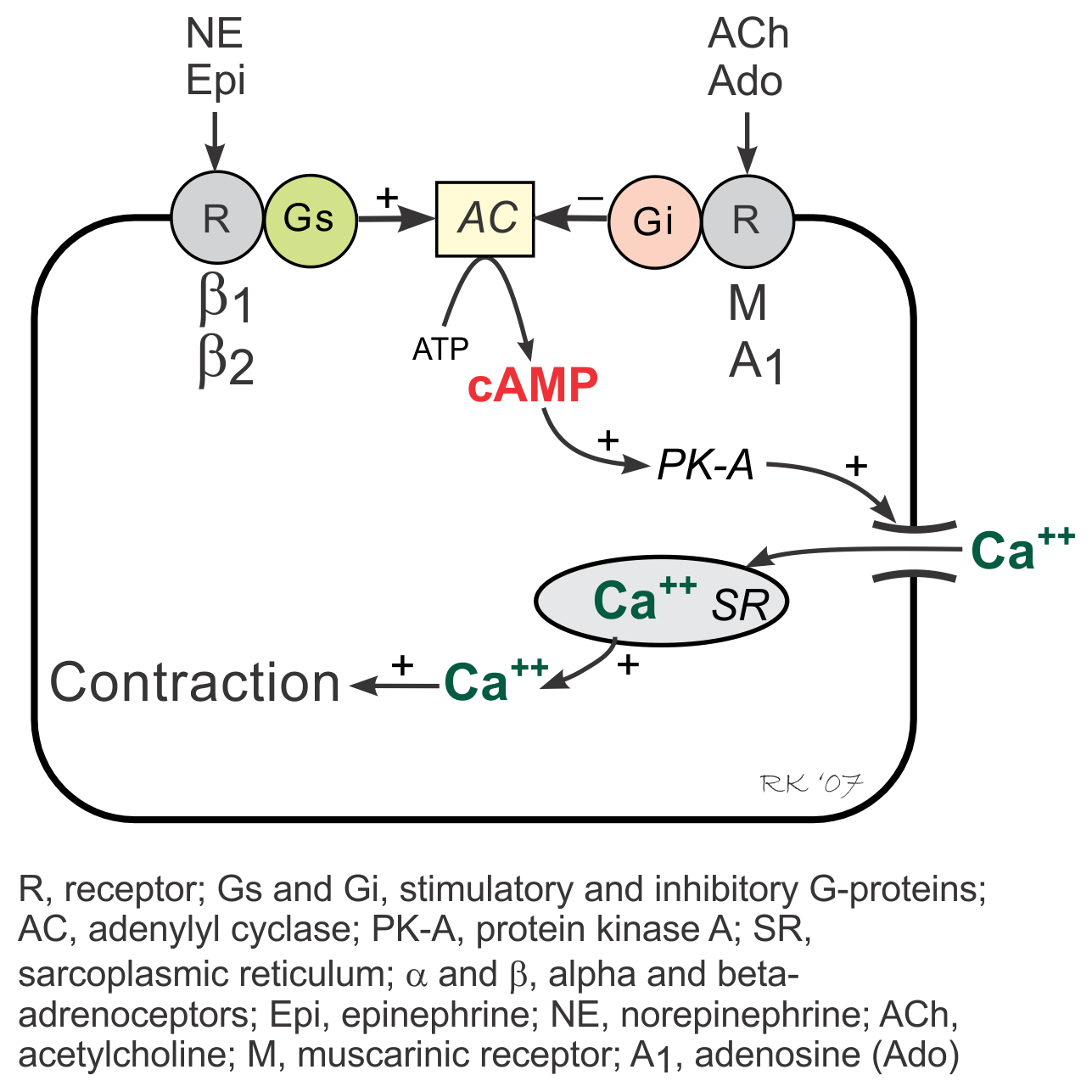
Vilken G-protein kopplas till β-receptorer?
β-receptorer (som β₁ och β₂) är kopplade till Gₛ-protein (stimulerande G-protein). När adrenalin eller noradrenalin binder till β-receptorn aktiveras Gₛ, vilket i sin tur stimulerar enzymet adenylcyklas. Detta leder till ökad produktion av cAMP (cykliskt adenosinmonofosfat) – en viktig second messenger som utlöser effekter som:
💓 Ökad hjärtfrekvens och kontraktionskraft (β₁ i hjärtat).
🌬 Bronkdilatation (β₂ i lungor).
🔋 Nedbrytning av fett och glykogen (β₃ i fettvävnad).
Skillnad mot andra G-protein:
α₁-receptorer: Kopplas till Gq (aktiverar IP₃/Ca²⁺).
α₂-receptorer: Kopplas till Gᵢ (hämmar adenylcyklas → minskar cAMP).
Klinisk relevans:
Betablockerare (t.ex. metoprolol) blockerar β-receptorer → minskar cAMP → sänkt hjärtfrekvens/blodtryck.
Astmamedicin (t.ex. salbutamol) aktiverar β₂-receptorer → bronkdilatation via Gₛ/cAMP.
Hur påverkar sympatikus svettkörtlar?
Sympatiska nervsystemet reglerar svettkörtlarna via en speciell kolinerg signalväg (t.ex. vid stress eller värme), trots att sympatiska nervbanor normalt använder noradrenalin. Här är en tydlig förklaring:
Steg-för-steg-process:
Preganglionär neuron:
Från ryggmärgen (thoracolumbala regionen T1–L3) skickas signaler med acetylkolin (ACh) till sympatiska ganglier.
ACh binder till nikotinreceptorer på postganglionära neuroner.
Postganglionärt neuron:
Till skillnad från andra sympatiska nervbanor använder dessa neuroner ACh (inte noradrenalin) som neurotransmittor.
ACh frisätts från nervändarna och binder till muskarinreceptorer (M3) på svettkörtlarna.
Effekt på svettkörtlarna:
Muskarinreceptorer aktiverar en intracellulär signalväg (via Gq-protein) som leder till ökad svettproduktion.
Svettet bidrar till termoreglation (svalning) eller emotionell stressrespons.
Varför används ACh här?
Evolutionär anpassning: Svettreglering är en äldre funktion som troligtvis utvecklades innan den typiska "fight-or-flight"-responsen med noradrenalin.
Exakt kontroll: Muskarinreceptorer ger en långsammare men mer precist reglerad svettning jämfört med adrenerga receptorer.
Termisk vs. emotionell svettning:
Värmereglerad svettning (kroppen överhettas) styrs också av sympatiska ACh-signaler.
Stressinducerad svettning (t.ex. nervositet) aktiveras av samma mekanism.
Klinisk relevans:
Antikolinerga läkemedel (t.ex. atropin) blockerar muskarinreceptorer → minskad svettning (kan leda till överhettning).
Hyperhidros (överdriven svettning) behandlas ibland med botox, som blockerar ACh-frisättning lokalt.
Skillnad mot övriga sympatiska effekter:
Organ | Sympatisk signalväg | Neurotransmittor |
|---|---|---|
Hjärta/blodkärl | Noradrenalin → β₁/α₁-receptorer | Noradrenalin |
Svettkörtlar | ACh → muskarinreceptorer | Acetylkolin (ACh) |
Sammanfattning:
Sympatiska nervsystemet använder ACh och muskarinreceptorer för att styra svettkörtlarna – ett unikt undantag från den vanliga noradrenalinbaserade signaleringen. Detta möjliggör både termisk och stressrelaterad svettning! 😊
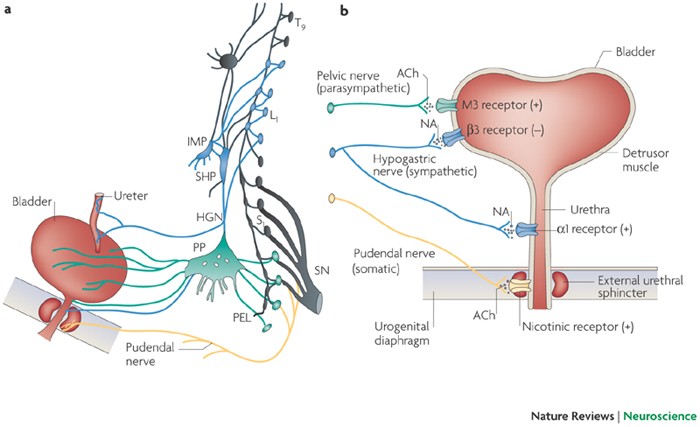
Sympatisk effekt på urinblåsan?
Sympatiska nervsystemet (ditt "fight-or-flight"-system) har en hämmarroll vid urinering för att förhindra att du kissar under stress. Effekterna delas upp i två delar:
1.Avslappnar detrusormuskeln (muskeln i urinblåseväggen)
Receptor: Traditionellt tillskrivs detta β₂-adrenerga receptorer, men nyare forskning visar att β₃-receptorer är dominerande i människors urinblåsa.
Effekt: När sympatikus aktiveras, släpper noradrenalin ut och binder till β-receptorer → detrusorn slappnar av → urinblåsan fylls utan att trycka ut urin.
Klinisk koppling: Läkemedel som β₃-agonister (t.ex. mirabegron) används mot överaktiv urinblåsa för att lugna detrusorn.
2.Kontraherar den inre urinrörssfinktern
Receptor: α₁-adrenerga receptorer i den glatta muskulaturen i sfinktern.
Effekt: Noradrenalin binder till α₁-receptorer → sfinktern drar ihop sig → förhindrar urinläckage.
Klinisk koppling: α₁-blockerare (t.ex. tamsulosin) används vid prostataförstoring för att slappna av sfinktern och underlätta urinering.
Varför är detta viktigt?
Sympatikus säkerställer att du håller urinen när du är stressad, rädd eller fysiskt aktiv. Det är en överlevnadsmekanism – att kissas skulle vara ofördelaktigt om du behöver fly eller kämpa!
Skillnad mot parasympatikus:
Parasympatikus (via acetylkolin och M₃-receptorer):
Kontraherar detrusorn → urinblåsan töms.
Slappnar av sfinktern → urin kan passera.
Sammanfattning i bild:
Sympatisk aktivering:
[Urinblåsan] → β₃ → 😌 (avslappnad detrusor)
[Sfinkter] → α₁ → 🔒 (kontraherad)
Resultat: Ingen kissning under stress! 🚫💦 Parasympatisk effekt på urinblåsan?
Det parasympatiska nervsystemet (ditt "vila och smältningssystem") aktiverar urinering genom att:
1.Kontrahera detrusormuskeln(muskeln i urinblåseväggen):
Signalväg: Parasympatiska nervceller frisätter acetylkolin (ACh) som binder till muskarinreceptorer (M₃) på detrusorn.
Effekt: Muskeln drar ihop sig → ökat tryck i urinblåsan → urin pressas ut.
2.Avslappna den inre urinrörssfinktern(glatt muskulatur):
Signalväg: ACh från parasympatiska nervändar kan minska sympatisk aktivitet (som normalt håller sfinktern stängd via α₁-receptorer). Samtidigt kan kväveoxid (NO) frisättas, vilket direkt slappnar av sfinktern.
Effekt: Sfinktern öppnas → urin kan passera.
Varför sker detta?
När du är avslappnad och behöver tömma urinblåsan tar parasympatikus över:
"Pumpa ut"-fas: Detrusorn trycker urinen ut.
"Öppna dörren"-fas: Sfinktern släpper igenom urinen.
Skillnad mot sympatisk effekt:
Funktion | Sympatisk | Parasympatisk |
|---|---|---|
Detrusormuskel | Avslappnad (via β₃-receptorer) | Kontraherad (via M₃-receptorer) |
Sfinkter | Kontraherad (via α₁-receptorer) | Avslappnad (via NO/minskad sympatisk ton) |
Klinisk koppling:
Överaktiv urinblåsa: Behandlas med antimuskarinika (t.ex. oxybutynin) som blockerar M₃-receptorer → minskar detrusorkontraktioner.
Urinretention: Vid försvagad parasympatisk funktion (t.ex. diabetesneuropati) kan urinblåsan inte tömmas ordentligt.
Sammanfattning:
Parasympatikus = "Kissa nu!"-systemet 🚽💦
ACh aktiverar M₃ → detrusorn trycker ut urinen.
Sfinktern öppnas för att släppa igenom den.
Sympatisk effekt på matsmältning?
Minskar motilitet och sekretion (α₂ och β₂).
Vilken receptor ökar hjärtats kontraktilitet?
β₁-receptorer.
Vilken receptor sänker hjärtfrekvensen?
Muskarinreceptorer (M₂ i SA-noden).
Vad gör propranolol?
β-blockerare → minskar hjärtfrekvens och kontraktilitet.
Vilken effekt har en α₁-blockerare?
Vasodilatation → sänkt blodtryck.
Varför används atropin vid bradykardi?
Blockering av parasympatisk effekt (ökar hjärtfrekvens).
Vad är effekten av hexamethonium?
Hexamethonium är en ganglieblockerare som hindrar signalöverföringen i både det sympatiska och parasympatiska nervsystemet genom att blockera nikotinreceptorer i autonoma ganglier. Här är en detaljerad förklaring av dess effekter:
Mekanism:
Blockering av nikotinreceptorer:
Hexamethonium binder till nikotinreceptorer på postganglionära neuroner i autonoma ganglier.
Detta förhindrar acetylkolin (ACh) från preganglionära neuron att aktivera postganglionära neuron → signalen bryts i både sympatiska och parasympatiska banor.
Konsekvenser av ganglieblockad:Sympatiska effekter (minskas):
Vasodilatation: Utan sympatisk tonus slappnar blodkärlen av → blodtrycket sjunker kraftigt (hypotension).
Sänkt hjärtfrekvens: Sympatisk stimulering av hjärtat (via β₁-receptorer) blockeras → hjärtat kan inte öka pumpkraften.
Minskat svettning: Sympatiska nervbanor till svettkörtlarna (som är kolinerga) blockeras → torr hud.
Parasympatiska effekter (minskas):
Sämre matsmältning: Parasympatisk stimulering av mag-tarmkanalen blockeras → nedsatt tarmrörelse och salivproduktion.
Urinretention: Svårigheter att tömma urinblåsan (avslappnad detrusormuskel).
Pupillvidgning: Parasympatisk pupillförtunning (mios) blockeras → pupiller blir vidare.
Kliniska effekter (huvudsakligen):
Kraftig hypotension: Sympatisk blockad leder till förlust av perifer vasokonstriktion (huvudeffekt).
Orthostatisk kollaps: Blodtrycket faller brutalt vid upprätt ställning → risk för svimning.
Torra slemhinnor: Minskat parasympatiskt saliv- och tårflöde.
Användning och historik:
Hexamethonium var ett av de första läkemedlen mot högt blodtryck på 1950-talet, men används inte längre på grund av:
Biverkningar: Allvarlig hypotension, urinretention, förstoppning, synstörningar.
Bättre alternativ: Moderna läkemedel är mer specifika (t.ex. α- eller β-blockerare).
Skillnad mot andra blockerare:
Läkemedel | Målreceptor | Effekt |
|---|---|---|
Hexamethonium | Ganglionära nikotinreceptorer | Blockar alla autonoma funktioner |
Atropin | Muskarinreceptorer | Blockar endast parasympatiska effekter |
Propranolol | β-adrenerga receptorer | Blockar sympatiska hjärt- och lungfunktioner |
Sammanfattning:
Hexamethonium är en "brute force"-blockerare som stör hela det autonoma nervsystemet. Effekterna domineras av hypotension p.g.a. förlust av sympatisk vasokonstriktion, men den påverkar också matsmältning, urinering och svettning. 😊
Exempel: Om du tar hexamethonium och sedan springer → blodtrycket sjunker istället för att öka, eftersom kroppen inte kan mobiliseras via sympatikus.
Vad händer vid överdos av nikotin?
En överdos av nikotin leder till hyperstimulering av nikotinreceptorer i kroppen, vilket orsakar en kaotisk effekt på flera system. Här är en tydlig förklaring av vad som händer:
Mekanism:
Nikotin imiterar acetylkolin (ACh) och binder till nikotinreceptorer, som finns i:
Autonoma ganglier (sympatiska och parasympatiska).
Neuromuskulära korsningar (mellan nerver och skelettmuskler).
Hjärnan (centrala nikotinreceptorer).
Vid överdos blir dessa receptorer överaktiverade, vilket leder till en först stimulerande, sedan hämmande effekt (receptorerna blir "utmattade" och slutar svara).
Symtom och progression:
Tidiga symtom (stimulerande fas):
Gastrointestinala: Illamående, kräkningar, diarré, salivflöde.
Hjärt-kärl: Hjärtklappning, högt blodtryck, svettning.
Neurologiska: Huvudvärk, yrsel, skakningar, muskelryckningar (fasciculationer).
Svåra symtom (hämmande fas):
Muskelkramper och svaghet: Överstimulering av neuromuskulära korsningar → musklerna kan inte slappna av → smärtsamma kramper, följt av paralys (muskeldomning).
Andningsproblem: Andningsmuskler förlamas → andningssvikt.
CNS-depression: Förvirring, kramper, medvetslöshet (koma) och potentiell död.
Varför leder detta till koma?
Hjärnan: Överstimulering av centrala nikotinreceptorer kan utlösa kramper, följt av energibrist och nedstängning av nervsystemet.
Syrebrist: Andningsförlamning minskar syretillförseln till hjärnan, vilket snabbar på medvetslöshet.
Riskgrupper och källor:
E-cigaretter: Koncentrerad nikotinvätska (e-juice) är farlig, särskilt för barn.
Vuxna: 30–60 mg ren nikotin kan vara dödligt (motsvarar ~5–10 cigaretter om det sväljs).
Behandling:
Akut: Aktivt kol (vid förtäring), andningshjälp (ventilator), krampmedel.
Långsiktigt: Övervakning av hjärtfunktion och neurologisk status.
Sammanfattning:
En nikotinöverdos lamslår kroppens signalsystem genom att först överstimulera och sedan utmatta nikotinreceptorer. Det leder till muskelskador, andningsuppehåll och medvetslöshet – en potentiellt livshotande situation. 😟
Vad är 'slow waves' i mag-tarmkanalen?
Rytmiska elektriska signaler som styr muskelkontraktioner.
Vilka celler genererar 'slow waves'?
Interstitiella Cajal-celler (ICC).
Vad är MMC (migrerande motoriska komplex)?
Migrerande Motoriska Komplex (MMC) är ett cykliskt mönster av muskelkontraktioner i mag-tarmkanalen som uppträder mellan måltider (under fasta). Dess huvudsyfte är att "städa bort" rester av mat, sekret och bakterier från tunntarmen, vilket förhindrar bakterieöverväxt och förbereder tarmen för nästa måltid.
Fyra faser av MMC:
Fas I (Vila): Inga kontraktioner i 60-70% av cykeln.
Fas II (Oregelbundna kontraktioner): Sporadiska rörelser som förbereder för Fas III.
Fas III (Intensiva "städböljor"): Kraftiga, rytmiska kontraktioner som tränger fram innehåll i 5-10 minuter (drivs av hormonet motilin).
Fas IV (Övergång): Återgång till vila.
Viktiga funktioner:
Rengör tunntarmen genom att skjuta ut överskottsmaterial.
Förhindrar bakterieöverväxt genom att minska stillastående innehåll.
Regleras av enteriska nervsystemet och hormonet motilin.
Klinisk relevans:
Vid störda MMC (t.ex. diabetesneuropati eller IBS) kan bakterieöverväxt (SIBO) eller förstoppning uppstå.
Läkemedel som erytromycin (motilinagonist) kan stimulera MMC vid vissa tillstånd.
MMC är alltså kroppens interna "städrulle" som håller mag-tarmkanalen ren och funktionell mellan måltiderna! 😊
Vad triggar gastrokolisk reflex?
Gastrokolisk reflex är en automatisk reaktion i mag-tarmkanalen som triggas när magsäcken utvidgas (t.ex. vid måltider). Den leder till ökad rörelseaktivitet (motilitet) i tjocktarmen, vilket skapar en "våg" som driver tarminnehållet framåt. Här är en enkel förklaring av processen:
Steg-för-steg:
Utlösande faktor: När du äter och magsäcken fylls, aktiveras mekanoreceptorer i magväggen (de känner av utvidgningen).
Signalering:
Nervsignaler skickas via enteriska nervsystemet (tarmens eget nervsystem) och vagusnerven till tjocktarmen.
Hormoner som gastrin och cholecystokinin (CCK) frisätts och förstärker effekten.
Effekt:
Tjocktarmens muskler drar ihop sig kraftigare och oftare → snabbare transport av avfallsämnen mot ändtarmen.
Detta kan leda till avföringsträngning (särskilt morgonmåltiden, därav "morgontoalettbehovet").
Varför existerar reflexen?
Evolutionär fördel: Skapar plats i tarmen för nytt matinnehåll genom att snabbt rensa ut rester.
Förebygger obstipation: Stimulerar regelbunden tarmfunktion.
Exempel i vardagen:
Efter en stor måltid känner du plötsligt behov av att gå på toa.
Kaffe eller varm dryck på morgonen kan förstärka reflexen (därför många får "tarmrusning" efter kaffe).
Klinisk relevans:
Irritabel tarm (IBS): Hos vissa är reflexen överaktiv → diarré eller smärta efter måltider.
Postoperativ ileus: Efter bukkirurgi kan reflexen vara nedsatt → tarmförlamning.
Sammanfattning:
Gastrokolisk reflex = "Matsäckens utvidgning kickar igång tarmstädningen" 🍽🚽. En smart mekanism för att hålla mag-tarmkanalen effektiv! 😊
Vilket hormon neutraliserar magsyra i tunntarmen?
Sekretin (stimulerar bikarbonatutsöndring).
Vad är enteriska nervsystemet?
Mag-tarmkanalens eget nervsystem ('andra hjärnan').
Vad är rollen för vagusnerven?
Parasympatisk kontroll av hjärta, lungor, mag-tarmkanal.
Vilka receptorer finns på svettkörtlar?
Muskarinreceptorer (sympatisk kolinerg aktivering).
Vad är den parasympatiska effekten på ögat?
Pupillkontraktion (mios) och närseende (ciliärmuskelkontraktion).
Vilken receptor aktiveras av nikotin?
Nikotin aktiverar nikotinreceptorer, som är en typ av acetylkolinreceptorer (ligandstyrda jonkanaler). Dessa delas in i två huvudtyper baserat på deras placering och funktion:
1. N₁ (muskeltyp) – i neuromuskulära korsningar:
Plats: Skelettmuskler (t.ex. i armar, ben).
Funktion: Styr muskelkontraktion genom att öppna jonkanaler för natrium (Na⁺) och kalium (K⁺).
Exempel: Nikotinöverdos kan leda till muskelkramper eller förlamning (p.g.a. överstimulering).
2. N₂ (neuronalt/autonoma ganglietyp) – i ganglier och hjärnan:
Plats:
Sympatiska/parasympatiska ganglier (styr "fight-or-flight" och "rest-and-digest").
Centrala nervsystemet (hjärnan, där nikotin ger beroendeeffekter).
Funktion: Överför signaler i det autonoma nervsystemet och påverkar humör/kognition.
Exempel: Nikotin i cigaretter stimulerar N₂-receptorer i hjärnan → frisättning av dopamin (belöningssystem).
Skillnader mellan N₁ och N₂:
Egenskap | N₁ (Muskeltyp) | N₂ (Neuronalt/Ganglietyp) |
|---|---|---|
Plats | Skelettmuskler | Autonoma ganglier, hjärnan |
Subenheter | α1, β1, δ, ε/γ | α3, α4, β2, β4 |
Effekt | Snabb muskelkontraktion | Autonoma reflexer, beroende |
Klinisk relevans:
Nikotinberoende: N₂-receptorer i hjärnan är nyckeln till nikotinets belönande effekt.
Läkemedel:
Succinylkolin (N₁-blockerare) används vid intubation för muskelavslappning.
Vareniklin (partiell N₂-agonist) hjälper mot rökavvänjning.
Sammanfattning:
Nikotin "lurar" kroppen genom att imitera acetylkolin och aktiverar N₁-receptorer i muskler (kramper) och N₂-receptorer i ganglier/hjärnan (stressrespons, beroende). 😊