3.12 - DE CARBOXYLGROEP EN DERIVATEN
1/25
Earn XP
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
26 Terms
carboxylgroep
COOH
carbonylgroep (C=O) + hydroxylgroep (–OH)
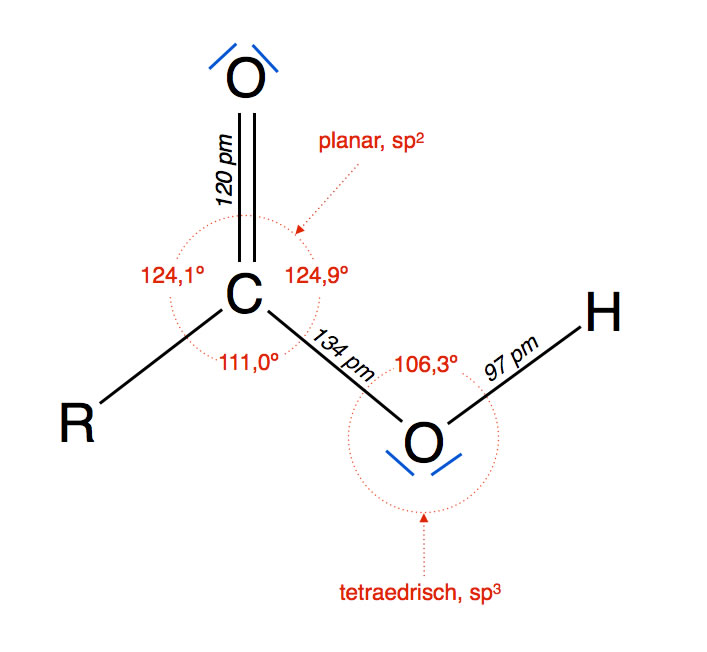
carboxyl vs carbonyl
carbonyl
additie
carboxyl
substitutie; want LG
sterische hinder + elektronische binding
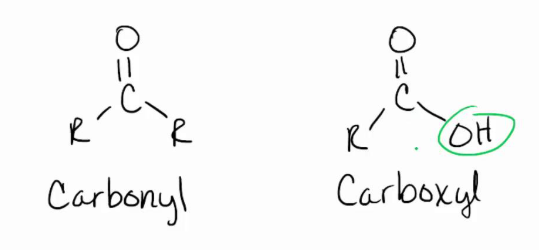
sterische hinder
hydroxylgroep zorgt voor sterische hinder
→ carboxylgroep minder toegankelijk dan carbonylgroep
elektronische binding
hydroxylgroep versterkt de elektronenverdeling rond de carbonylgroep
→ carbonylgroep minder elektrofiel
→ carboxylgroep minder reactief
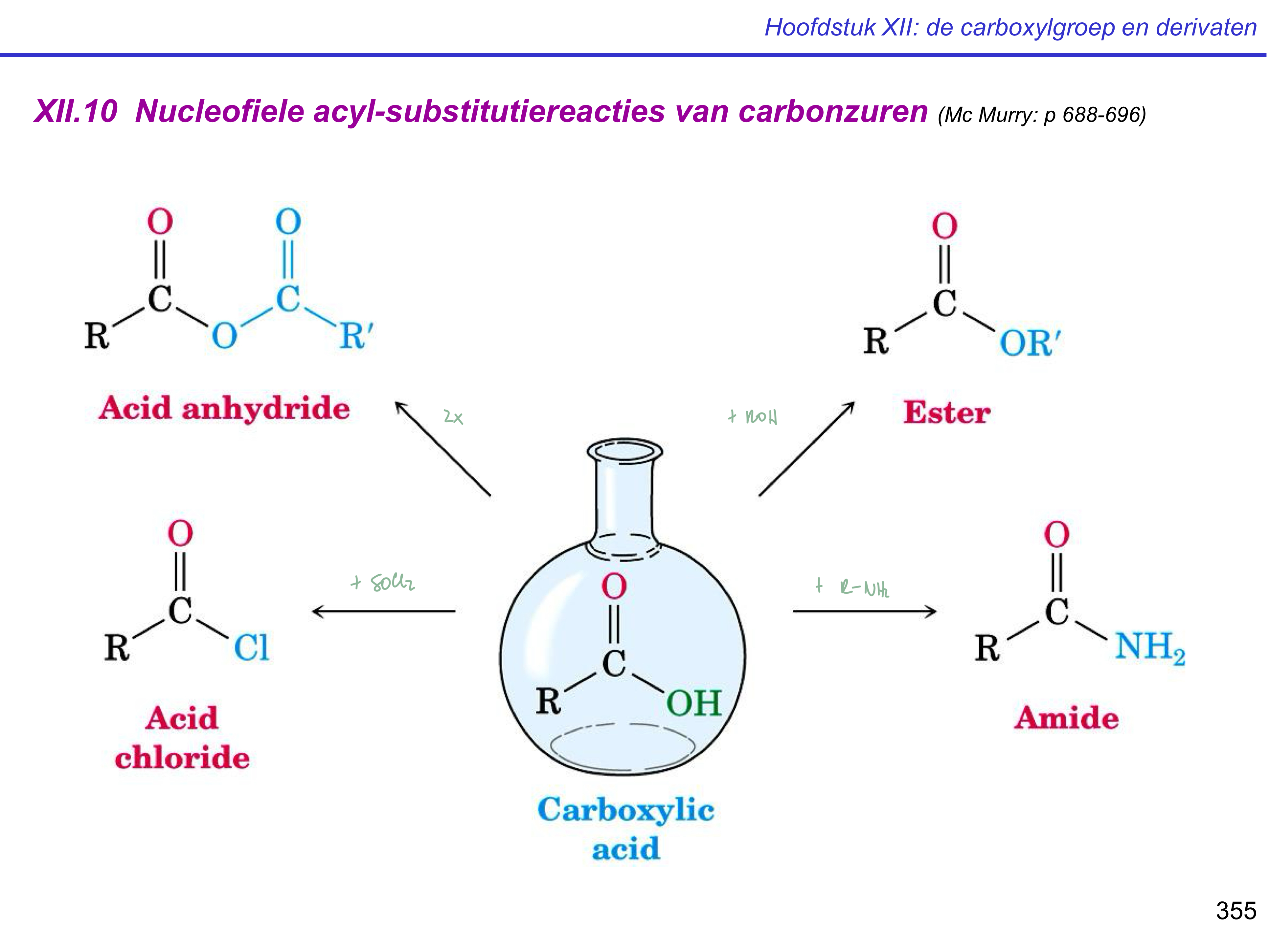
derivaten carbonzuur
(carbon)zuuranhydriden
esters
zuurhalogenide
amiden
carboxylaatzouten
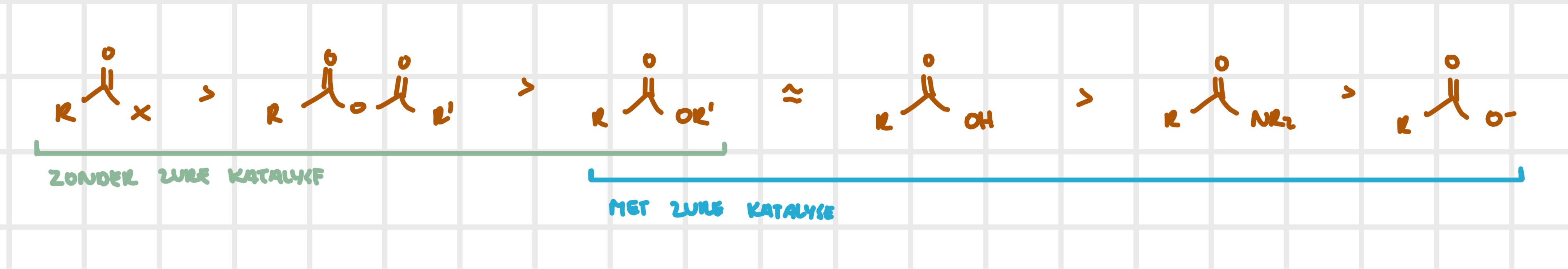
reactiviteit
zuurhalogenide
zuuranhydride
ester ~ carbonzuur
amide
carboxylaat
hoe beter de leaving group, maw de zwakste base, hoe reactiever
zuurchloride — vorming
1 methode;
carbonzuur + SOCl2
OH = slechte LG; ipv directe aanval op carbonyl gaat OH aanvallen op S
Cl = LG; valt aan op carbonyl
OH wordt gedeprotoneerd
elektronen verspringen; SO2 en Cl- zijn LG’s
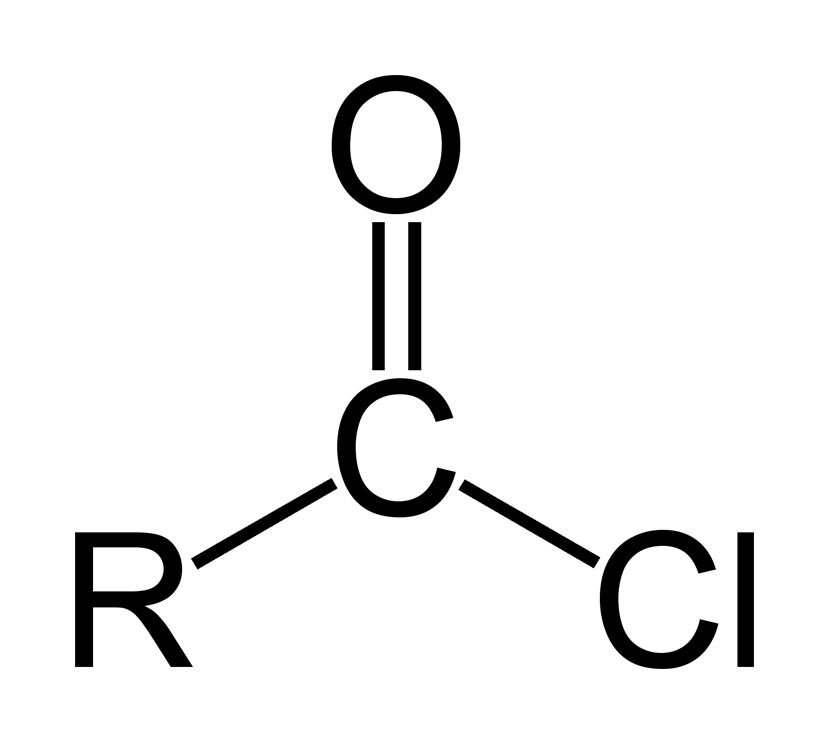
zuurchloride — mogelijke reacties
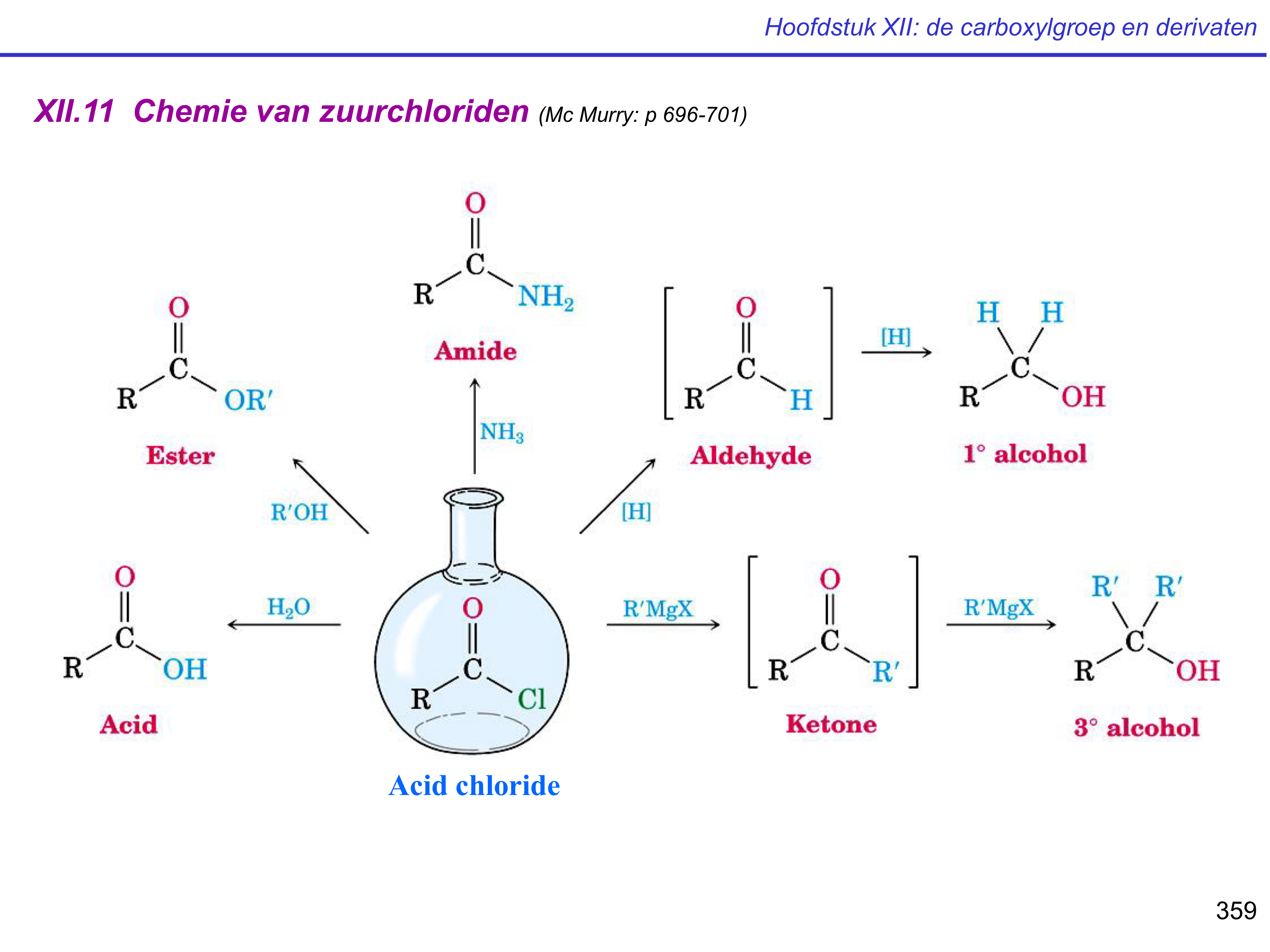
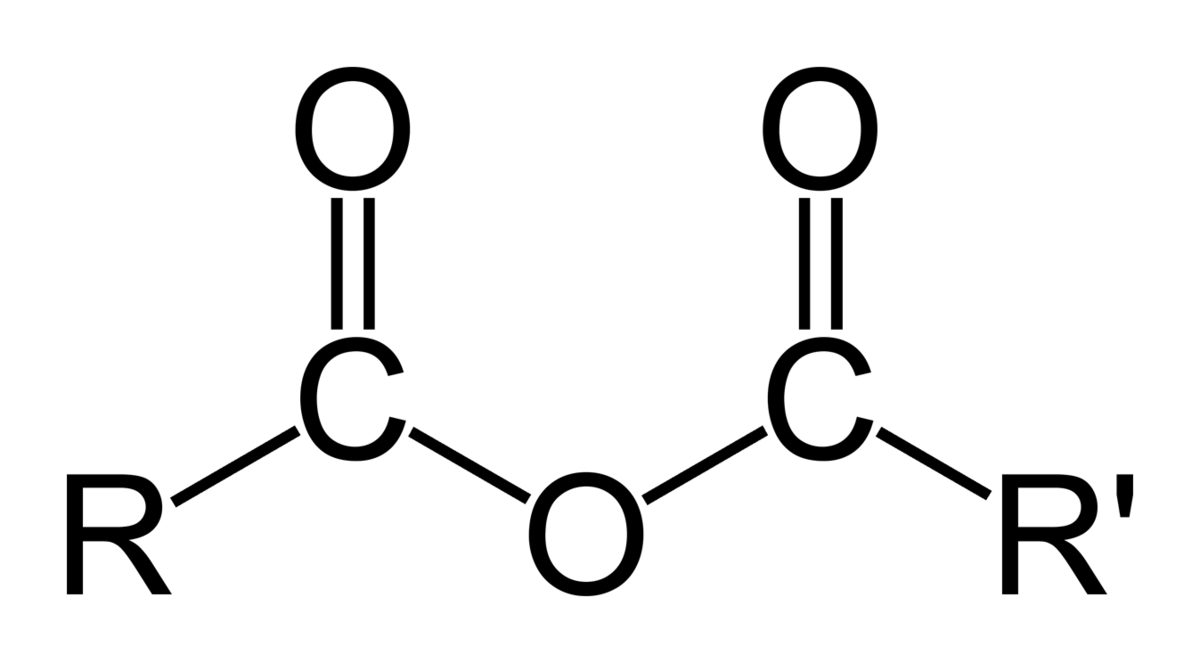
(carbon)zuuranhydride — vorming
2 methoden;
2× carbonzuur + afsplitsen van water
zuurchloride + carboxylaat
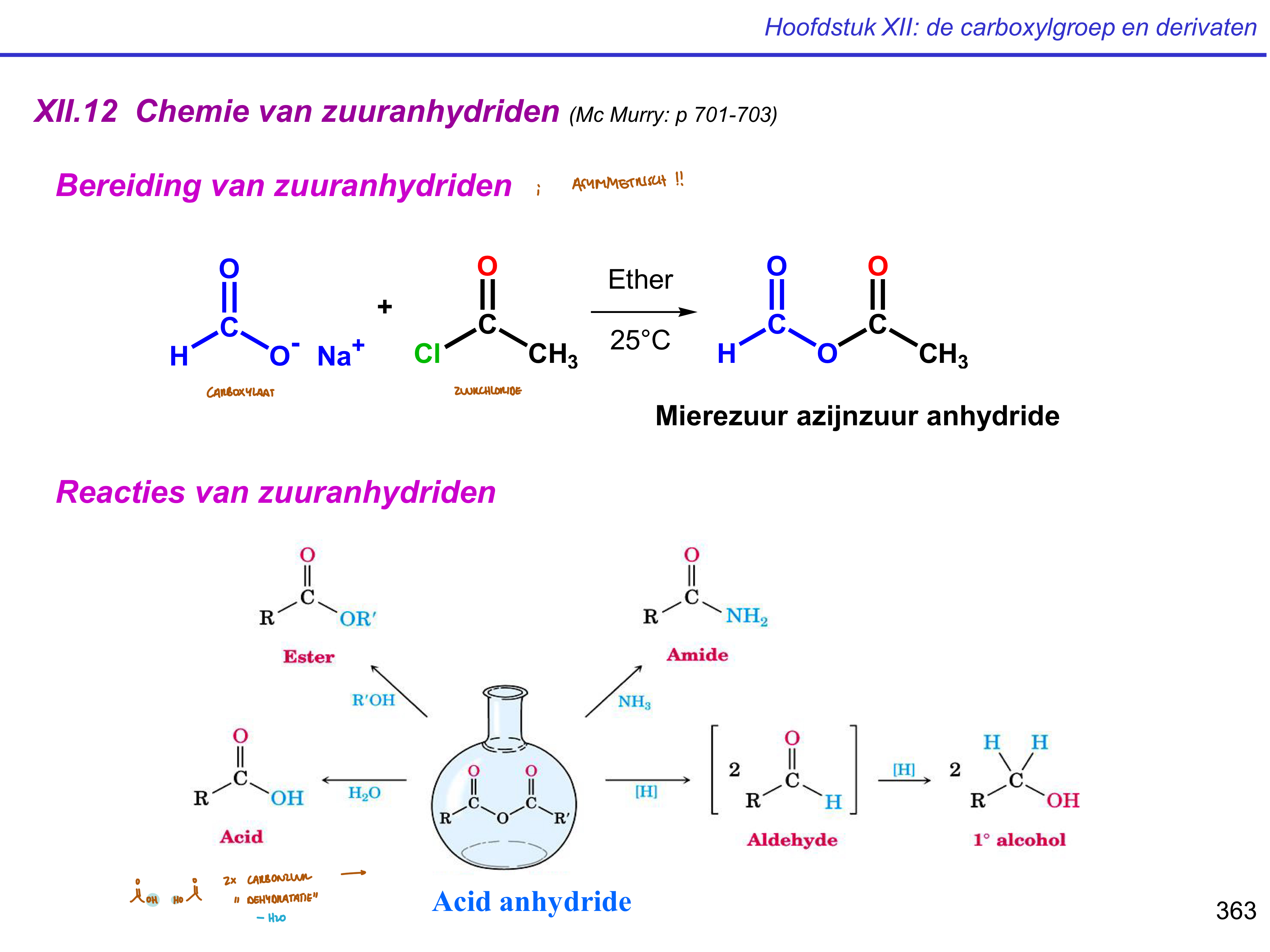
zuuranhydride — mogelijke reacties
ester — vorming
3 methoden;
Fischer esterificatie; carbonzuur + alcohol
zuur gekatalyseerd; simpele alc
zuurchloride + alcohol
meest algemene methode
carbonzuur + NaOH + R-X
opm; enkel 1° halogeenalkanen
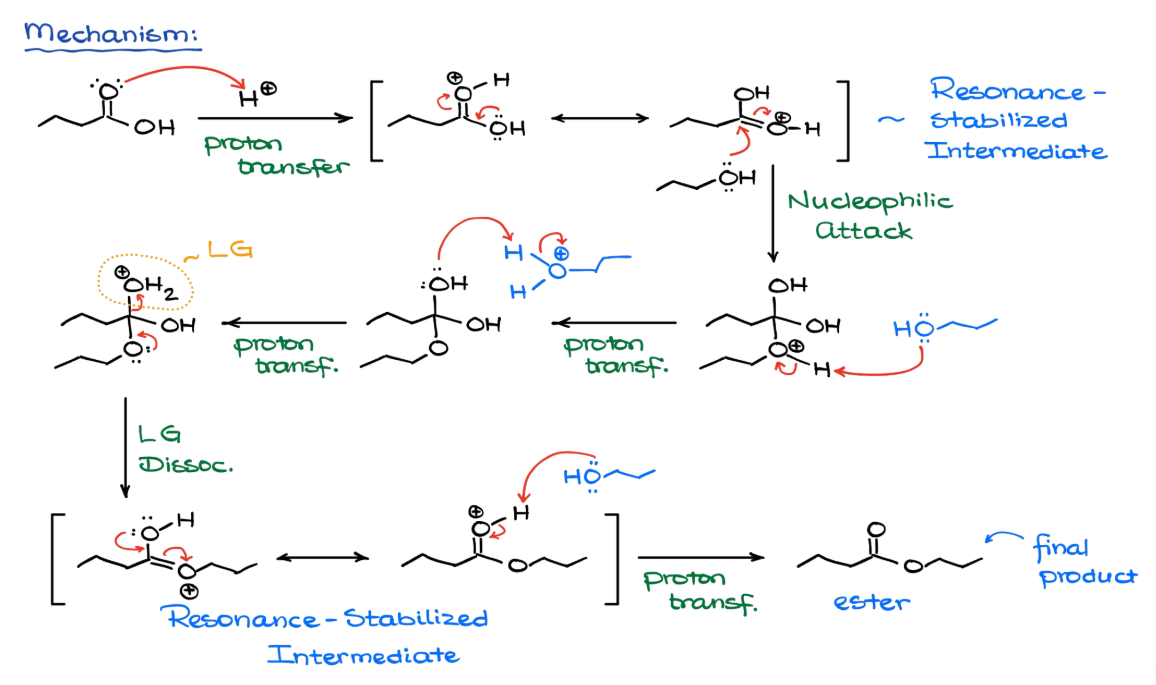
Fischer esterificatie — mechanisme
ester — mogelijke reacties
basische hydrolyse = verzeping → carbonzuur → carboxylaat
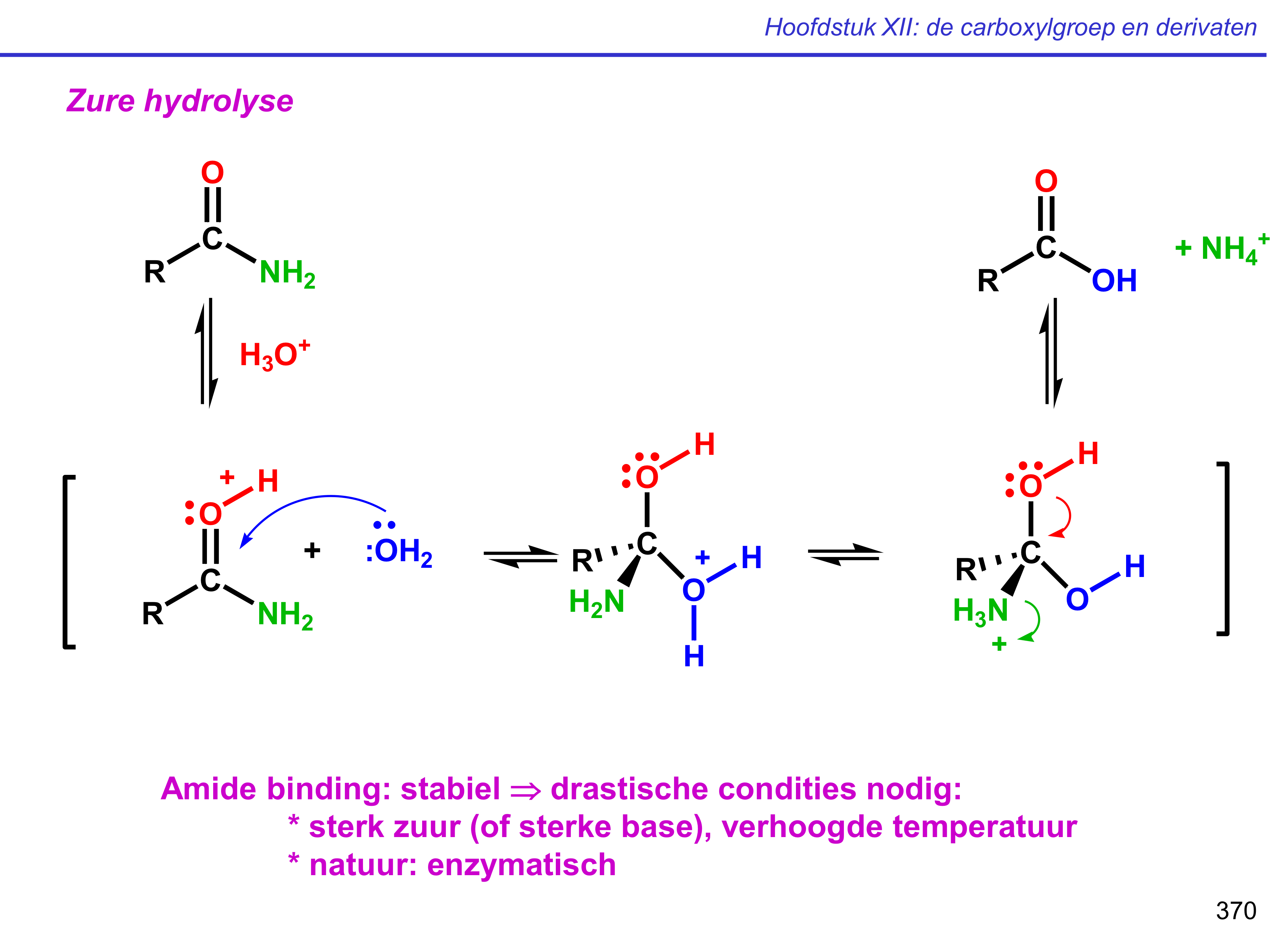
zure hydrolyse → carbonzuur
aminolyse → amine
2× Grignard → keton → 3° alc
carbonzuur — vorming
Grignard + CO2
RX + Mg → Grignard
let op voor nevenreacties!!
nitril → amide → carbonzuur (zie verder)
RX + NaCN → R-CN + NaX
SN2 moet mogelijk zijn!!
oxidatie alkylbenzenen
oxidatieve splitsing alkeen
oxidatie 1° alc / aldehyde
carbonzuur vorming via Grignard — opm
R-MgBr = Grignardreagens is;
sterk nucleofiel
sterke base
kan dus aanleiding geven tot;
nucleofiele aanval;
zowel inter- als intramoleculair
zuur/base;
indien H aanwezig is
geen “droog” solvent gebruikt; zoals THF, ether …
carbonzuur — mogelijke reacties
let ook op voor mogelijke zuur/base reacties
carbonzuur + SB → carboxylaat
amide — vorming
1 methode = amidatie
zuurchloride + amine → amide
NH3 → 1°
R-NH2 → 2°
R2-NH → 3°
opm; carbonzuur + amine = ZUUR-BASE REACTIE!!!!
amide — mogelijke reacties
+SB → amide met N- (zuur/base reactie)
+SZ → carbonzuur + NH3 → carboxylaat + NH4+
amide → carbonzuur
zuur gekatalyseerde hydrolyse
protonering op O ipv N;
meer EN
activatie carbonyl
NH2 geprotoneerd tot NH3+ = enige mogelijke LG om tot carbonzuur te komen (anders vorm je weer amide)
amide → carbonzuur — mechanisme
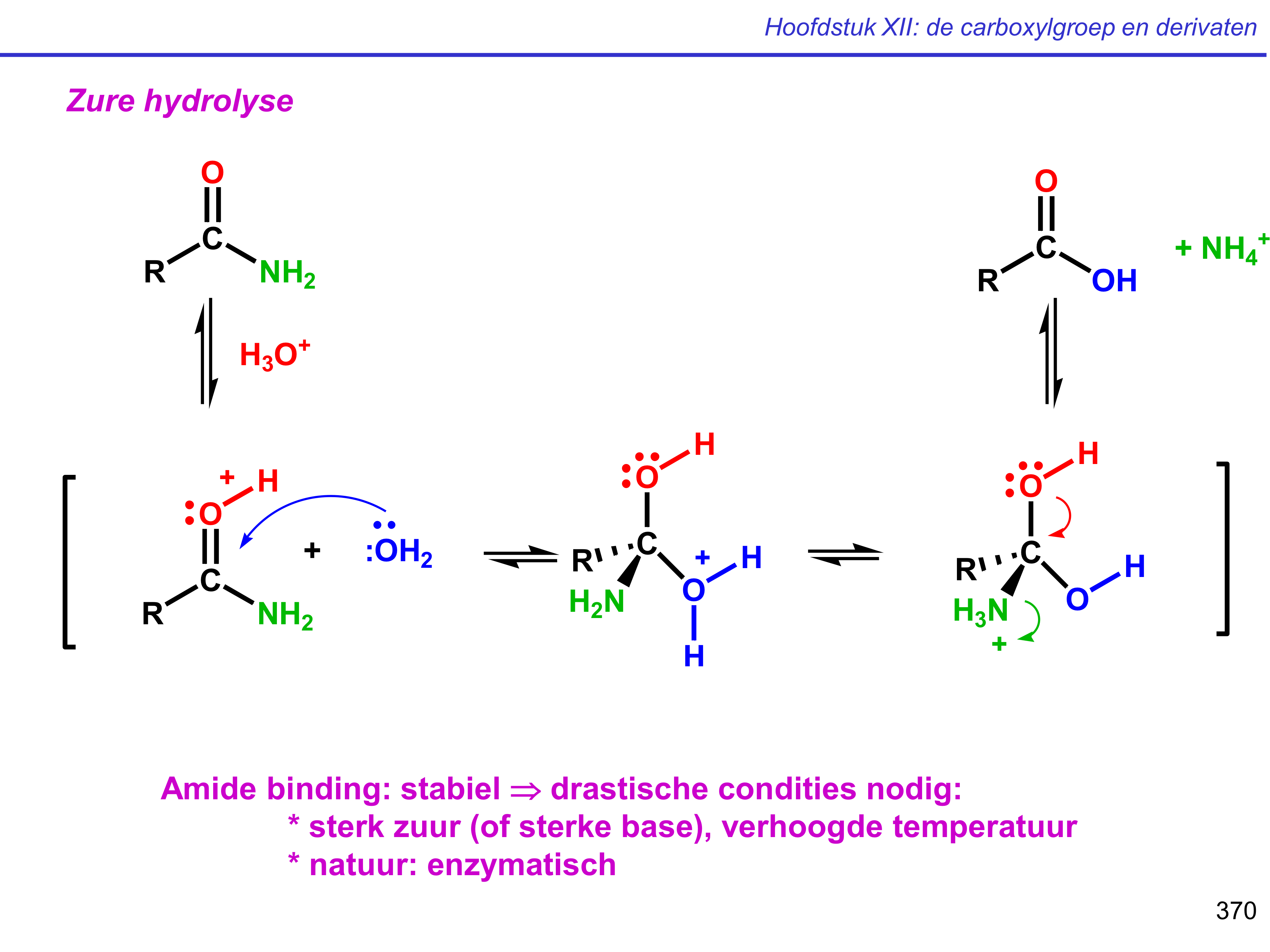
carbonzuur → amide
gaat niet, want
carbonzuur + amine = ZUUR-BASE REACTIE!!!!
carbonzuur + SOCl2 → zuurchloride
zuurchloride + amine → amide
carboxylaatzout — vorming
1 methode = neutralisatie
carbonzuur + base
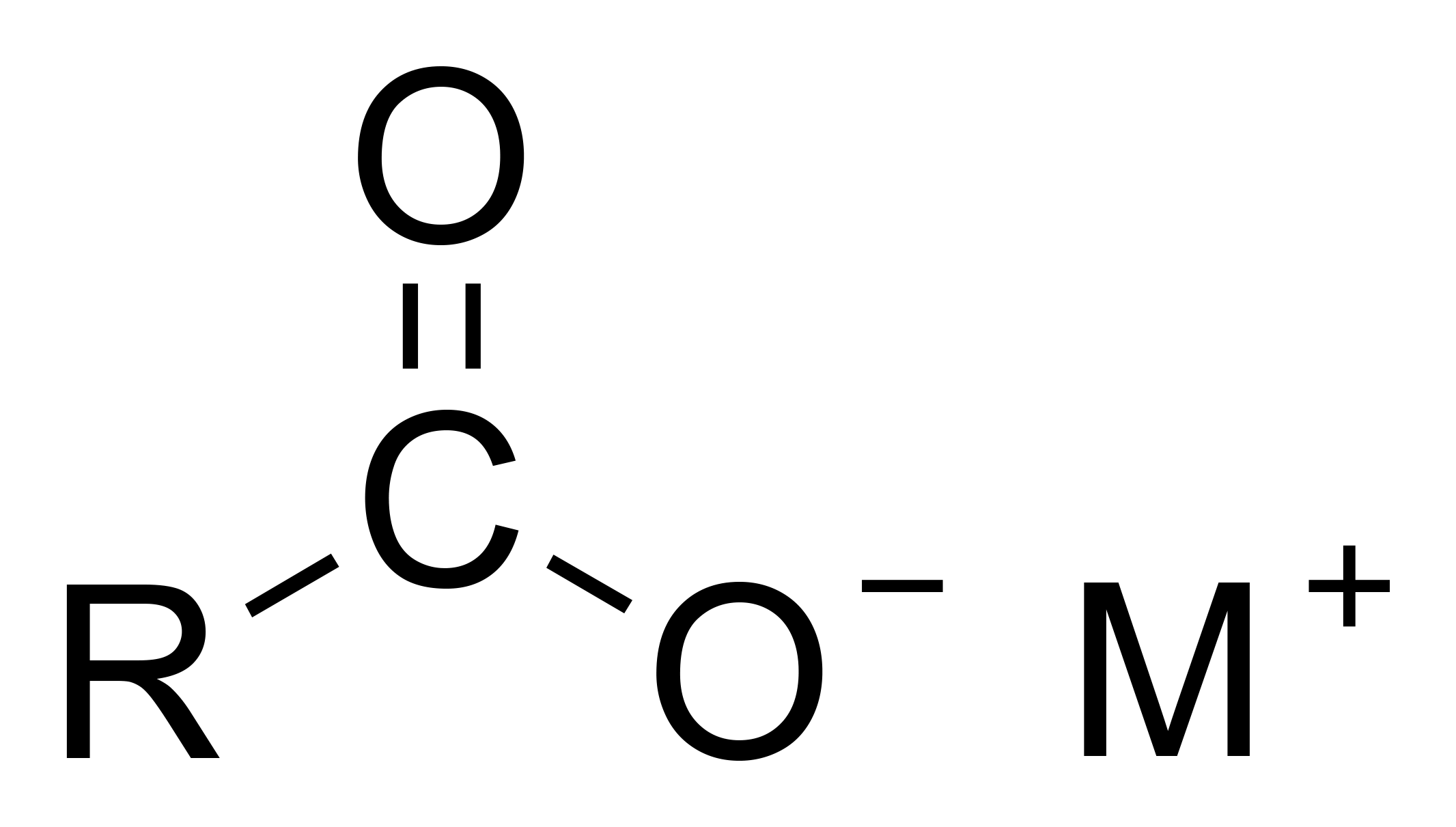
nitril — vorming
1 methode;
R-X + NaCN → R-CN + NaX
SN2
nitril — mogelijke reacties
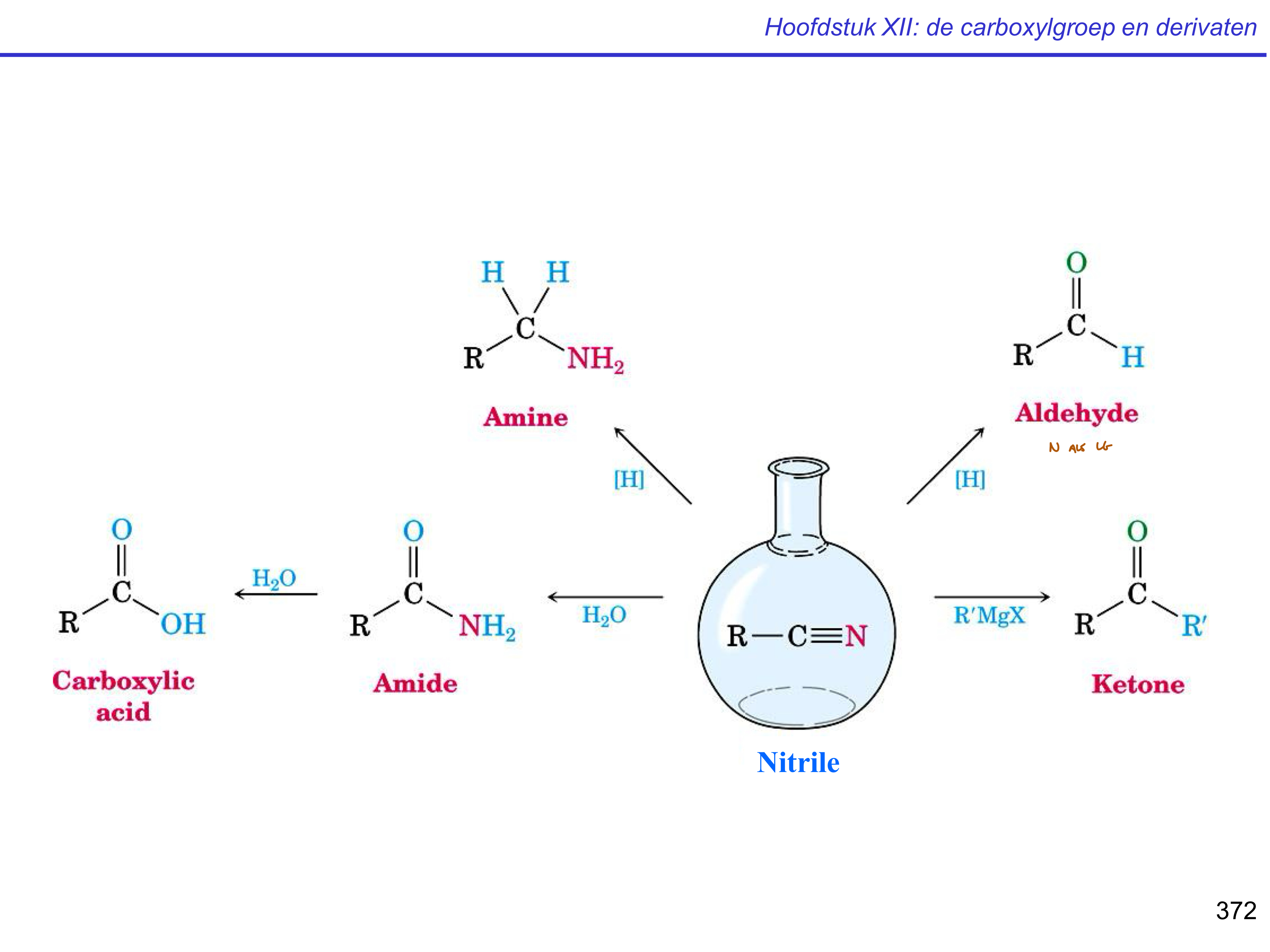
nitril → amide → carbonzuur — deel 1
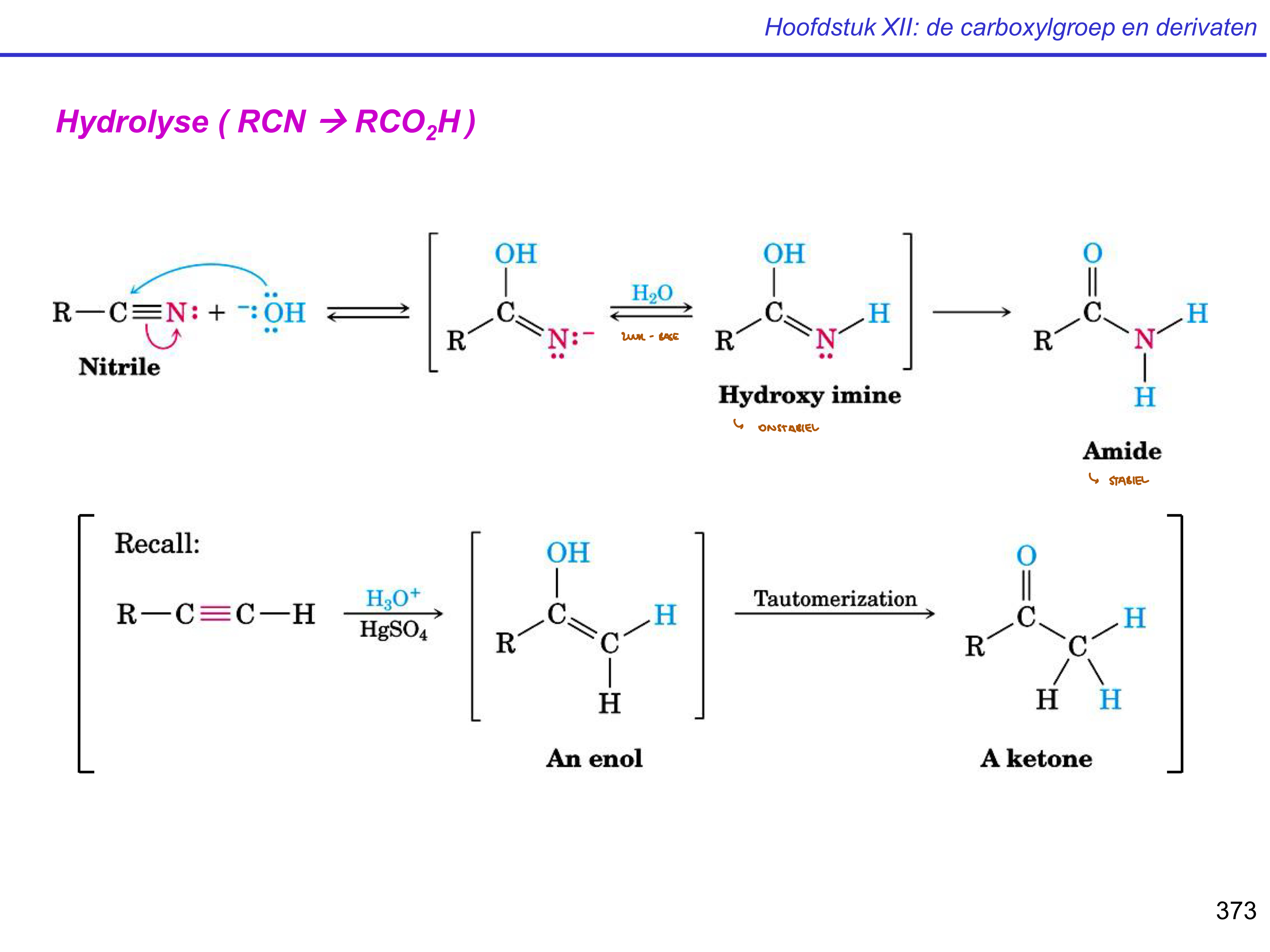
nitril → amide → carbonzuur — deel 2