Kjemi VG 2 Kapittel 2.1 - 2.2
1/19
Earn XP
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
20 Terms
Redoksreaksjon
En Reaksjon der det skjer en Hel eller delvis elektron overføring
2(AgNO3) (aq) + Cu (s) —> 2NO3- (aq) + 2Ag (s) + Cu²+
Eksempel på en Redoksreaksjon
Forbrennings reaksjon
Når et stoff reagerer med oksygen og det blir frigjort energi.
Fellingsreaksjoner
Denne reaksjonen skjer når vi blander to lett løselige stoffer i vann og får et tungt løselig stoff. Det positive ionet fra et av saltene reagerer med det negative ionet fra det andre saltet.
Ag+(aq) + NO3- (aq) + Na+ (aq) + Cl- (aq) —> AgCl (s) + NO3- (aq)+ Na+ (aq)
Fellingsreaksjon
2(AgNO3) (aq) + Cu (s) —>
2NO3- (aq) + 2Ag (s) + Cu²+ (med tilskuer ion)
Ag+(aq) + NO3- (aq) + Na+ (aq) + Cl- (aq) —>
AgCl (s) + NO3- (aq)+ Na+ (aq)
Kompleksreaksjon
En Reaksjon hvor et positivt metallion (sentralionet) er omgitt av negative ikke-metallioner eller molekyler (ligander). Reaksjonen kan ha både negativ og positiv ladning. Den totale ladningen avhenger av sentralatomets ladning og ligandenes ladning og antall.
Ladningsbevaring
I en balansert reaksjons likning er den samlede ioneladningen det samme på begge sider av reaksjons pila.
[CoCl4]²- + 6(H2O) —> 4Cl- + [Co(H2O)6]²+
Eksempel på Kompleks reaksjon
HCl + H2O —> Cl- + H3O+
Syre - base Reaksjon (syre)
NaOH + H3O+ —> Na+ + 2(H2O)
Syre - base reaksjon (base)
Syre - base reaksjoner
Reaksjoner der H+ -ioner overført mellom de stoffene som reagerer.
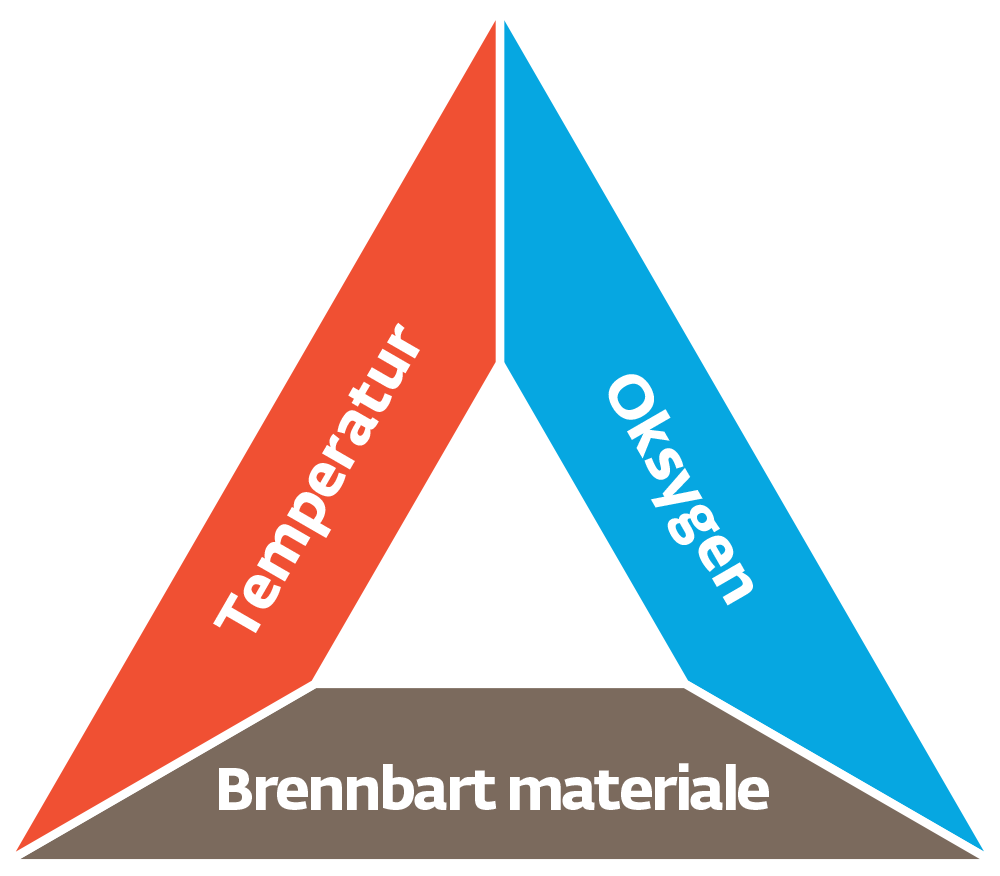
Hva er dette?
Branntrekanten
Kjemiske Reaksjoner (Resultater)
Temperaturendfringer, gassutvikling, Farge endringer og utfelling av fast stoffer.
Kjemiske Reaksjon (Definisjon)
I en kjemisk reaksjon skjer det en forandring der det blir dannet et nytt stoff. Dette stoffet har som regel en ny egenskap enn stoffene vi startet med.
Reaktanter blir til produkter.
S
Fast stoff (Solid)
g
gass (Gas)
l
Væske (Liquid)
aq
vannløsning (aqua)