C.A Prima parte
1/19
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
20 Terms
Definizione di chimica analitica
La chimica analitica è la disciplina che utilizza strumenti, strategie e metodi volte all'identificazione all’ottenimento di informazioni sulla composizione e struttura di sostanze chimiche e materiali, si occupa di determinare qualitativamente e quantitativamente i componenti di un determinato campione.
Quali sono i tipi di analisi che si possono effettuare su un campione?
Analisi qualitativa: permette di rivelare l’identità chimica delle specie presenti in un campione
Analisi quantitativa: consente di stabilire in termini numerici la quantità relativa di una o più specie presenti in un campione
Come si possono suddividere i metodi analitici?
I metodi analitici si dividono in 2 macrogruppi, metodi classici e strumentali, i quali a loro volta possiedono delle suddivisioni.
Metodi classici:
Metodi gravimetrici: determinano la massa dell’analita o di un composto derivante da esso, sono basati su misure di peso. Tra i vantaggi troviamo l’accuratezza e la presenza di poche interferenze; dall’altra parte però richiedono esperienza e tempi lunghi.
Metodi volumetrici: sono metodi basati su misure di volume, come ad esempio le titolazioni, reazioni acido-base, stechiometria. Tra i vantaggi abbiamo la rapidità, la semplicità, e i bassi costi; mentre come svantaggi il LOD fino ai mg/L.
Quali domande bisogna porsi per scegliere in modo saggio un metodo analitico?
Quali sono le proprietà fisiche e chimiche degli analiti?
Quali sono le proprietà chimiche e fisiche della matrice?
Che accuratezza e precisione sono richieste?
Qual è l’intervallo di concentrazione previsto dell’analita?
Quali componenti presenti nel campione possono causare interferenze?
Quanti campioni devono essere analizzati?
Altre caratteristiche da tenere in considerazione nella scelta del metodo:
Velocità di esecuzione
Facilità e praticità
Abilità richiesta dall’operatore
Costo e disponibilità della strumentazione
Costo del campione
Quali sono le fasi di un’analisi chimica?
Scelta del metodo
Campionamento
Trattamento del campione
Isolamento dell’analita
Definizione dei replicati
Preparazione delle soluzioni
Eliminazione degli interferenti
Calibrazione e misura
Calcolo die risultati
Valutazione dei dati e stima della loro attendibilità
Presentazione dei dati
Il Campionamento
L’obiettivo del campionamento è quello di ottenere dei campioni rappresentativi, ossia la loro composizione deve essere la stessa del materiale da cui è stato eseguito il prelievo. Inoltre, è importante che siano omogenei, ossia che la loro composizione sia la stessa in ogni sua parte. Infine il campione deve rimanere integro, evitando perdite di materiale (sostanze volatili, contaminazioni)
Trattamento
Trasporto e conservazione (il campione deve essere nelle stesse condizioni del momento del prelievo) + operazioni analitiche generali
Operazioni analitiche generali
Calcinazione, ulteriore riscaldamento del residuo dopo l’essicamento, con decomposizione di alcuni componenti
Centrifugazione, separazione di un solido da liquido mediante impiego di centrifuga
Concentrazione, eliminazione di parte del solvente mediante evaporazione, è il passaggio inverso della diluizione (riscaldamento diretto, rotavapor, bagnomaria)
Decantazione, si lascia depositare un solido sul fondo del recipiente e successivamente si versa o si pipetta il liquido senza trascinare le particelle del precipitato
Diluizione, operazione mediante al quale viene diminuita la concentrazione della soluzione
Dissoluzione, porta in soluzione il materiale da analizzare
Essicamento, evaporazione spinta fino all’eliminazione totale del solvente (rotavapor, capsula su fiamma diretta, stufa)
Filtrazione, impiego di una parete porosa (filtro) che lascia passare il liquido e trattiene le particelle solide.
Precipitazione, formazione di una fase solida all’interno della soluzione
Preparare una soluzione
“Il simile scioglie il simile”
Pesare. Bilancia tecnica (2000g/0,01g) o analitica (200g/0,001g)
Solubilizzazione completa del solido
Portare a volume (lettura menisco)
Usare pipette
Filtrazione
Parametri strumentazione (+ grafico)
Portata/capacità= quantità massima che lo strumento può apprezzare
Sensibilità= capacità dello strumento di discriminare tra piccole variazioni. Rapporto tra risposta strumentale e quantità dell’analita.
Risoluzione= capacità di discriminare tra due valori, la risposta
Accuratezza= capacità di dare un risultato vicino a quello vero
Precisione=capacità di riprodurre lo stesso dato in seguito a misure ripetute nelle stesse condizioni
Estrazione
Isolamento di una sostanza dalla matrice
Parametri da considerare per avere una resa alta (7): tempo, tipo di solvente, quantità di solido e solvente, temperatura, agitazione, numero di estrazioni, pressione.
Legge di distribuzione di Nerst
k= coefficiente di ripartizione
Ca= concentrazione all’equilibrio della sostanza in fase “a“
Cb= concentrazione all’equilibrio della sostanza in fase “b“
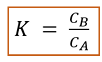
Quali sono le 4 tipologie di estrazione che abbiamo visto?
Estrazioni multiple, Liquido/Liquido, Solido/Liquido e in continuo, In fase solida (SPE)
Estrazioni multiple
E una pratica molto ordinaria quella di estratte più volte con piccole aliquote di solvente. Solo quando la K è molto grande allora la quota che rimane nella fase acquosa è molto piccola e basta un’estrazione.
Estrazione Liquido/Liquido
I solventi più usati per estrarre sostanze organiche d auna soluzione acquosa sono generalmente:
+ densi dell’H2O: etere dietilico, acetato di etile, benzene
- densi dell’H2O: cloroformio, diclorometano
Estrazione Solido/Liquido o in continuo
L’obiettivo è separare gli analiti in una sostanza liquida, e di separarli da una matrice in base alle loro proprietà fisiche e chimiche. La sostanza estratta si chiama eluto.
(+ spiegazione disegni)
Importante ricordare che nel sistema di estrazione liq/liq, man mano che il solvente contenente le sostanze estratte rifluisce nel pallore, è soggetto a continuo riscaldamento. Le sostanze NON devono essere termolabili.
Campioni reali ed effetto matrice
L’analisi di un campione reale è complicata dalla presenza di una matrice che può contenere specie chimiche con proprietà simili a quelle dell’analita. Distinguiamo quindi tecniche analitiche:
Specifiche, impiegano proprietà chimiche/fisiche caratteristiche per solo analita in esame (saggi colorimetrici)
Selettive, impiegano reazioni o proprietà caratteristiche di un gruppo ristretto di composti (saggi per i carboidrati)
Estrazione in fase solida (SPE)
Metodologia utilizzata per purificare, in seguito ad estrazione. L’obiettivo è quello di separare una sostanza dal solvente in cui si trova sfruttando la sua affinità con la fase solida, una fase stazionaria impaccata e compressa. In seguito, viene utilizzato un secondo solvente, ancora più affine all’analita, in modo che questo si stacchi dalla fase stazionaria e scenda dalla cartuccia.
(+ DISEGNO CARTUCCIA) cartuccia, serbatoio, filtro, fase solida, filtro
Conditioning, attivazione della fase solida attraverso solvente
Loading, caricamento del campione
Washing, altro solvente per lavare il volume morto dalla fase stazionaria
Eluition, si và ad agire sull’analita per staccare le molecole e farle uscire separatamente da tutto il resto
Accuratezza e precisione
3 disegni:
elevata accuratezza, poca precisione: i risultati sono si vicini al valore reale, ma sono dispersi
elevata precisione, poca accuratezza: i risultati sono tutti simili ma non sono vicini al valore reale
elevata accuratezza e precisione: i risultati sono vicini tra loro e al valore reale
Errori
Casuali= errori che possono avvenire con la stessa probabilità sia in eccesso che in difetto. Non si possono evitare (es: correnti d’aria). Pe rimediare bisogna effettuare tante misure. è stato provato statisticamente che, all’aumentare del numero di prove, questi errori si annullano l’un l’altro.
Sistematici= errori che avvengono sempre nella stessa direzione. Sono dovuti quasi sempre da errori di taratura dello strumento. Questo tipo di errori può essere corretto effettuando dei controlli sugli strumenti.
S. Costanti, il valore dell’errore è costante e non dipende dalla quantità misurata. SI ottiene una retta parallela ai valori reali
S. Proporzionali, il valore dell’errore aumenta o diminuisce in base alla quantità misurata. Errori piccoli su pesi piccoli, errori grandi su pesi grandi. Otteniamo uno spostamento della pendenza della curva di calibrazione
Grossolani
Difetto strumento utilizzato, imperfetta realizzazione del fenomeno, interazione strumento-sperimentatore (di “parallasse“), interazione strumento-fenomeno, errate condizioni di lavoro, errore off-set (“di zero”)