H3 de chemische binding
1/70
Earn XP
Description and Tags
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
71 Terms
welke elmenten kunnen op zichzelf bestaan
de edelgassen
wat bepaald het chemisch gedrag van een atoom
de valentie-elektronen
edelgassen
heel stabiel
reagreen niet met andere elementen → chemisch inert
8 elektronen op buitenste schil
edelhasconfiguratie / octetstructuur
waar streven atomen naar
de stabiele edelgasconfiguratie te bereiken
op welke manieren kunnen atomen binden
vormen van ionbindigen
covalente bindingen
metaalroosters
wanneer komt de bindijng tussen atomen spontaan tot stand
wanneer dit leidt tot een hogere stabiliteit of een kleinere energie-inhoud dan in ongebonden toestand
ion
als elektronen worden toegevoegd aan of weggenomen van het atoom wordt een geladen deeltje gevormd
ionbinding
komt tot stand wanneer er een overdracht optreedt van één of meer valentie-elektronen van het ene atoom naar het andere
is het resultaat van de elektrostatische aantrekkingen tussen de tegengestelde geladen ionen
wat kunnen ionen niet doen in een rooster
vrij bewegen
kation
een atoom dta een of meerdere elektronen afgeeft, verkrijgt een positieve lading
halfedelgasconfiguratie
kationen die geen edelgasconfiguratie vertonen, maar in de laatste schil toch vollledig opgevilde subniveaus pf orbitalen bevatten
metalen
anion
een atoom dat een of meerdere elektronen opneemt, verkrijgt een negatieve lading
niet-metalen
polyatomische ionen
bevatten meerdere atomen die onderling covalent gebonden zijn
vb ammoniumion NH4+, carbonaation CO3²-
ionverbinding
is een bindijng tussen positieve en negatieve ionen die door elektrostatische aantrekkingskrachten of coulombkrachten wordt samengehouden.
ontstaan ionverbindijng (is de stof)
ionrooster
een regelmatig patroon waarbij elk positief ion omgeven wordt door negatieve ionen en omgekeerd
het aantal kationen en anionen in het ionrooster is niet gekend, maar is afhankelijk van ?
de grootte van het kristal (rooster)
de verhouding van beide ionen (die ligt welvast → ionverbonding is neutraal)
formule / roostereenheid
geeft de samenstellijng weer van de kleinste eenheid waaruit het ionrooster is opgebouwd
= verhoudingsformule
subscripten
kleinste gehele getallen die de verhouding van de ionen weergeven
roosterenergie Er
is de energie die vrijkomt bij de vroming van 1 mol kristallijne ionverbindngen uit de samenstellende positieve en negatieve ionen in de gasfase
wordt uitgredrukt in kj / mol
wanneer komt er meer energie vrij bij de vroming van een rooster
hoe sterker de ionen elkaar aanytrekken
wordt groter wanneer de ionladingen groter zijn en de ionstralen kleiner
wanneer is een ionverbinding stabieler
naarmate er meer energie vrijkomt bij zojn vorming uit atomen dus naarmate (Er-Ea-Ei) groter is
de kans dat een ionbinding gevormd wordt is groter naarmate
de ionsitaie-energie van het metaal kleiner is, de absolute waarde van de elektronenaffiniteit van het niet-metaal groter is en de roosterenergie groter is
waarom zijn ionverbindingen meestal vast en bestaan zij niet uit afzonderlijke ionenparen
omdat de vormin van een ionverbinding een bedruidend groter energievoordeel oplevert
kenmerken van ionverbindingen
door sterke elektrostatische krachten (coulombkrachten)
hoog smeltpunt (hoe groter de roosterenergie, hoe hoger het smeltpunt)
kleine vluchtigheid
grote hardheid
zijn bros : door er een kracht op uit te oefenen kunnen gelijke ionen tegen elkaat komen t eliggen, de afstoting die hiermee gepaard gaat, leidt dan tot een breuk van het kristal
goed oplossibaar in polaire oplosmiddelen (vb water) → ze dissocieren in ionen
bij oplossen of smelten komen de ionen uit het rooster vrij, waardor geleiding van de elektrische stroom mogelijk wordt
covalente binding
in gemeenschap brengen van elektronen
twee gelijke atomen of atomen met gering verschil in elektronegativiteit zich verenigen
meestal moleculair
binding tussen twee niet-metalen → steeds covalent
gewone covalente binding
een ongepaard elektron van een atoom in gemeenschap gesteld met een ongepaard elektron van een ander atoom
datief covalente binding
wordt een niet bindend elektronpaar van het ene atoom (donor) in gemeenschap gesteld met een ander atoom dat een tekort heeft aan elektronen (acceptor)
gedelocaliseerde bindingen / mesomerie of resonantie
voor sommige molecuen en polyatomische ionen kan meer dan een lewisformule worden getekened die voldoen aan de octetregel
de elektronen worden daarbij telkens op een andere manier voorgesteld
geen van beide formules de ware situatie correct beschrijft
de werkelijke structuur ligt ertussen
het zijn gedelocaliseerde elektronen die verspreid zijn
welke krachten zijn er bij een diwaterstof molecule
afstoting tussen de 2 elektronen van beide atomen
afstoting tussen de 2 kernen
aantrekking tussen de kern van het ene atoom en het elektron van het ander atoom
bindingsenergie
is de energie die nodig is om de moleculen t everbreken tot de samenstellende atomen
de bindingsenergie is afhankelijk van
de afstand van de deelnemende atomen
het aantal bindingen (enkel, dubbel.)
valentiebindingstheorie
ontstaan de covalente bindijngen tussen twee atomen door het overlappen an hun atoomorbitalen; een orbitaal van het ene atoom neemt een deel in van het orbitaal van het ander atoom = molecuulorbitaal
in de overlappingsruimte kan een gemeenschappelijk elektronenpaar ontstaan, dat door beiede kernen wordt aangetrokken en ze dus samenhoudt
promotie van een elektron
als er een 2s-elektron overgebracht wordt naar een onbezet 2p-orbitaal
waarom vindt hybridisatie plaats
omdat de deelnemende atomen zoveel mogelijk ongepaarde elektronen nodig hebben
wanneer een elektron naar een orbitaal met hetzelfde hoofdkwantumgetal gepromoveerd wordt …
is de energie dir vrijkomt groter dan de energie nodig voor de promotie
hybridisatie
het combineren van de oorspronkelijke atoomorbitalen tot vorming van speciale orbitalen voor binding
sp³ orbitalen karakteristieken
1s en 3p orbitalen
heeft ¼ s karakter
¾ p-karakter
overwegend de vorm van een p orbitaal
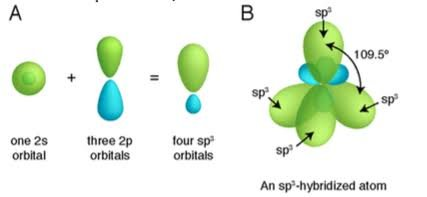
sp³ hybridisatie (principe)
wanneer een set van equivalente tetraëdische atoomorbitalen vereist zijn door een atoom, dan veronderstelt dit model dat het atoom een set van sp³ orbiatlen aannemeent, het atoom wordt sp³ gehybridiseerd
VB CH4
principe van sp² hybridisatie
wanneer een atoom omringd is door drie effectieve oaren, is een set sp² hybride orbitalen vereist
kenmerken van hybride-orbitalen binnen één atoom
alle hybride-orbitalen zijn gelijk van vorm
alle hybride-orbitalen hebben ene gelijke energie
de hybridisatie grijpt slechts plaats op het ogenblik van de binding
hybride-orbiatlen liggen zo ver mogelijk van elkaar
op welke manieren kunnen sigma-molecule orbitalen ontstaan
overlapping van 2s-orbitalen
hybride-hybride overlapping
s-hybride overlapping
welke (pi of sigma) bindijngen zijn het sterkst
sigma langer en sterker
pi binding is veel reactiever
elektrpnegativiteit EN
van een atoom is een maat voor de neiging van het atoom om de bindende elektronen naar zich toe te trekken
(onbenoemd getal)
apolaire bindingen
bindingen tussen 2 identieke atomen, de bindende elektronen behoren voor 50% tit ieder atoom
polaire binding
een binding waarin de elektronen asymmetrisch verdeeld zijn over de bindende atomen
dipoolmoment p
is een vector met een richting en een grootte
p = delta . r
met lading delta : fractie van 1.6× 10^-19 C en r de bindingsafstand
zorgt voor permanene vervorming van de elektronenwolk
dipoolmoleculen
als bindende elektronenparen zich naar de meest elektronegatieve bindspartner verplaatsen kan dit aanleiding geven tot moleculen die een positieve en een negatieve (elektrische) pool bezitten
wanneer zijn enkelvoudige stoffen polair / apolair
geen verschuivng van de bindende elektronenparen plaatsgrijpt, nooit dipoolmomenten optreden, steeds apolair
wanneer zijn samengestelde (di-atomische moleculen) stoffen polair / apolair
als er een verschil in EN is tussen de bindingspartners, steeds polair zijn
afhankelijk van het verschil in elektronegatieve waarde tussen beide bindingspartners kunnen we hte karakter van een binding afleiden :
delta ENW = 0 : zuivere covalente binding
o < delta ENW < 1.7 = covalente binding met ionkarakter
delta ENW > 1.7 = ionbinding
dispersiekrachten
zwakke intermoleculaire krachten die voorkomen bij alle moleculen, ook tusse, apolaire moleculen
zelfs moleculen zonder dipoolmoment kunnen krachten op elkaar uitoefenen
polarizeerbare elektronenwolken
geinduceerde dipool
de vorming van een ogenblikkelijk dipool (door beweging van elektronen op een bepaalde moment) in een gegeven atoom kan ene gelijkaardige dipool induceren in een naburig atoom
wanneer worden de dispersiekrachten groter
naarmate de moleculen meer elektronen bevaten (dus groter met toenemende atoommassa) en hte oppervlakte tussen de moleculen griter wordt (rechte ketens hebben grotere dispersiekrachten dan vertakte ketens)
dipoolkrachten
de tegengestelde polen van dipoolmoelculen trekken elkaar aan
waterstofbruggen
elektrostatische interacties die optreden tussen moleculen waarin waterstofatomen gebonden zijn aan kleine atomen met een grote elektronegativiteit
N,F,O
zijn sterk tov andere dipool-dipool krachten
ion-dipoolkrachten
zeer sterke intermoleculaire krachten tussen ionen en polaire moleculen
verantwoordelijk voor hydratatie van ionen in water en de oplosbaarheid van ionverbindingen
bindingsterkte is afh van de lading van het ion, dipoolmoment en afstand tussen ion en dipoolmolecule
grotere ionen, hebben keienre intercaties
aggregatietoestand van covalente verbindingen
laag smelt en kookpunt
cohesiekrachten zijn linder sterk dan de roosterkrachten die ionverbindingen samenhouden
hangt samen met molecule massa, zwaardere moleculen komen moeilijker los, de dispersiekrachten worden ook sterker
diamant (en grafiet)
macromoleculen
diamant : een groot moleucle waarbij alle C atomen aan elkaar gebonden zijn in tetraedische structuren → 1 van de sterkste stoffen
grafiet : atomen laagsgewijs sterk aan elkaar gebonden, de bindingen tussen de lagen zijn minder sterk
geleidingsvermogen covalente bindingen
geleiden niet in vaste / gesmolten toestand de elektrische stroom
oplosbaarheid covalente bindingen
apolaire stoffen : niet oplosbaar in water, wel in apolaire oplosmiddelen
3 mechanismen voor de oplosbaarheid van verbindingen in water
een ionverbinding kan dissocieren in ionen : door inetracties van het polair water molecule en de ionen van het ionrooster
polaire covalente verbindingen oplosbaar in water (zoals ionverbindingen)
stoffen zoals suiker en ethankol lossen goed op in water omdat er tussen de water moleculen en de opgeloste stoffen H-bruggen gevormd worden → gebrek aan ionen, kunnen de elektrische stroom niet geleiden → niet elektrolyten
sterke elektrolyten
sommige polaire covalente bindingen worden in water geïoniseerd
niet-elektrolieten
stoffen die door gebrek aan ionen, de elektrische stroom niet geleiden
complexe ion
ion waarop een of meerdre moleuclen of ionen gebonden zijn
vb gehydrateerde ionen
liganden
de gebonden moleculen of ionen die aan de complexe ion hangt
negatieve ionen en moleculen die vrije elektronenparen hebben
welke orbitalen spelen een belangrijke rol bij het vormen van complecen
de d orbitalen
oxidatietrap / oxidatiegetal
is de lading die het atoom in dat deeltje bezit, zelfs al is die lading slechts een minieme partiële lading
= de reele of fictieve lading die aan een atoom wordt toegekend op bass van de electronegativiteit
gedelokaliseerde elektronen
elektronen die rondzweven
waarom geleiden metalen (vaste stof) toch de elektrische stroom?
ze hebben allemaal 1.2.3 valentielektronen, voor stabiliteit willen ze die afstaan, maar andere metaalatomen willen die niet opnemen,
er ontstaan dus positieve metaalionen en er ontstaat een elektronezone, bestaande uit vrije elektronene → houden de metaalionen samen
eigenschappen van metalen
hebben een sterke glans → door de beweeglijke gedelokaliseerde elektronen die het licht weerkaatsen
goede geleidbaarheid
hoog smeltpunt en kookpunt en dichtheid door sterke bindingskrachten
bros (plooibaar, pletbaar, rekbaar) = pos ionen die dicht bij elkaar zitten kunnen de lagen gemakkelijk splijten
legeringen
metalen in vloeibare toestand mengen