organische chemie hoofdstuk 4
1/88
Earn XP
Description and Tags
alkanen, naamgeving en reactiviteit
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
89 Terms
Wat is de algemene formule van acyclische verzadigde koolwaterstoffen?
CₙH₂ₙ₊₂
Wat betekent het dat een koolstofverbinding "verzadigd" is?
Elke C-atoom vormt vier enkelvoudige bindingen, dus er zijn geen dubbele of drievoudige bindingen aanwezig.
Wat voor soort bindingen komen er voor in verzadigde koolwaterstoffen?
Alleen enkelvoudige C–C en C–H bindingen.
Wat is het verschil tussen een vertakt en niet-vertakt alkaan?
Niet-vertakt: alle C-atomen vormen een rechte keten
Vertakt: de C-keten bevat zijketens of vertakkingen
Wat betekent het voorvoegsel “n-” in n-alkanen?
Waarom is het gebruik van “n-” belangrijk?
“N-” staat voor “normaal”, en duidt op een niet-vertakte rechte koolstofketen.
Om onderscheid te maken tussen rechte ketens en vertakte isomeren met dezelfde brutoformule.
Wat is de uitgang van alle alkaannamen?
De uitgang is altijd -aan.
Wat is de systematische naam van CH₄?
Wat is de systematische naam van C₂H₆?
Wat is de systematische naam van C₃H₈?
Wat is de systematische naam van C₄H₁₀?
methaan
ethaan
propaan
butaan
Vanaf welk aantal C-atomen worden Griekse telwoorden gebruikt?
Wat zijn de Griekse telwoorden voor 5 t.e.m. 10?
Vanaf vijf koolstofatomen → C₅ en hoger
5 = penta, 6 = hexa, 7 = hepta, 8 = octa, 9 = nona, 10 = deca
Geef de namen van n-alkanen van C₅ tot C₁₀.
C₅H₁₂ → n-pentaan
C₆H₁₄ → n-hexaan
C₇H₁₆ → n-heptaan
C₈H₁₈ → n-octaan
C₉H₂₀ → n-nonaan
C₁₀H₂₂ → n-decaan
Waarom is systematische naamgeving belangrijk?
Omdat elk isomeer een unieke naam moet krijgen, gebaseerd op de ketenstructuur en vertakkingen → essentieel voor correcte communicatie in chemie.
Waarom worden telwoorden gecombineerd met de uitgang –aan?
Het telwoord duidt het aantal C-atomen aan, en “–aan” bevestigt dat het om een verzadigd alkaan gaat.
Wat is een zijgroep of zijtak in een vertakt alkaan?
Een groep koolstofatomen die van de hoofdketen af splitst en één extra binding vormt met een C-atoom uit de hoofdketen.
Hoe wordt het aantal C-atomen in een zijgroep benoemd?
Via een stamnaam afgeleid van het overeenkomstig alkaan, maar de uitgang –aan wordt vervangen door –yl.
Wat betekent de uitgang “-yl” in een molecuulnaam?
Het duidt op een alkylgroep: een zijgroep die voortkomt uit een alkaan en nog één vrije binding heeft om zich te hechten aan een hoofdketen.
Wat is de algemene naam van een vertakt alkaan?
→ naam van de zijgroep (alkylgroep) + naam van het alkaan
Wat is de brutoformule van methyl?
Wat is de brutoformule van ethyl?
Wat is de brutoformule van propyl?
Wat is de brutoformule van butyl?
Wat is de brutoformule van pentyl?
Wat is de brutoformule van decyl?
CH₃–
→ afgeleid van CH₄ (methaan)C₂H₅–
→ afgeleid van C₂H₆ (ethaan)C₃H₇–
→ afgeleid van C₃H₈ (propaan)C₄H₉–
→ afgeleid van C₄H₁₀ (butaan)C₅H₁₁–
→ afgeleid van C₅H₁₂ (pentaan)C₁₀H₂₁–
→ afgeleid van C₁₀H₂₂ (decaan)
Waarom komt de alkylgroep niet alleen voor?
Omdat een alkylgroep altijd nog één binding te kort komt: het moet zich hechten aan een hoofdketen om stabiel te zijn.
Hoe duid je in een structuurformule een zijgroep aan?
Met een pijl (→) om aan te geven waar de binding met de hoofdketen ligt.
Waarom mag je een pijl voor een zijgroep niet verwarren met een dative binding?
Omdat de pijl hier geen elektronenoverdracht betekent, maar gewoon de locatie van de binding tussen zijgroep en hoofdketen aanduidt.
Wat is de systematische naam van de structuur:
→CH–CH₃ (en CH₃ op bovenste C)?
Dit is een methylgroep (CH₃) aan een CH-atoom, met nog een CH₃ eraan → dit is de structuur van isopropyl, maar hier moet je eigenlijk nog het volledige hoofdketen kennen voor een correcte naamgeving.
(Op basis van alleen deze structuur is geen volledige naam af te leiden, tenzij de hoofdketen ook gekend is.)
Waarom is er extra informatie nodig bij vertakte ketens?
Zonder extra info zouden verschillende moleculen dezelfde naam kunnen krijgen. Positieaanduiding maakt de structuur eenduidig en uniek.
Wat is een positietelwoord?
Vanaf hoeveel C-atomen in een keten wordt positienummering gebruikt?
Waar moet het positietelwoord altijd worden geplaatst?
Wat is het gevolg als je géén positietelwoorden gebruikt?
Kan één molecule meerdere positietelwoorden hebben?
Een cijfer vóór een zijgroep dat aanduidt op welk C-atoom van de hoofdketen de zijgroep zich bevindt.
Vanaf 5 C-atomen in de stam wordt standaard een positietelwoord gebruikt.
Voor de groep waar het betrekking op heeft, dus voor de zijgroep of alkylgroep.
De naam is onvolledig of fout. Je kunt dan niet ondubbelzinnig afleiden waar de zijgroepen zitten, wat leidt tot verkeerde structuurinterpretatie.
Ja, bij meerdere zijgroepen of meervoudige vertakkingen geef je voor elke zijgroep een afzonderlijk positietelwoord.
Wat is de algemene structuur van een systematische naam van een vertakt alkaan?
x-R₁-y-R₂-ALKAAN
waarbij:
x en y = positietelwoorden
R₁, R₂ = alkylgroepen
ALKAAN = stamnaam van de langste keten
Alkylgroepen alfabetisch gerangschikt
Waarom wordt alfabetische volgorde gebruikt bij zijgroepen?
Om een internationaal gestandaardiseerde en eenduidige naamgeving te garanderen. Onafhankelijk van structuurtekening.
Wat leer je uit de structuurvoorbeelden in deze oefening?
Dat kleine verschillen in plaatsing van zijgroepen leiden tot totaal andere moleculen, dus ook andere namen.
Wat is de rol van de hoofdketen bij naamgeving?
De hoofdketen bepaalt:
De stamnaam (bv. hexaan)
De nummering van C-atomen (voor positienummers)
De plaats van vertakkingen
Wat is het voordeel van dit systematisch naamgevingsprincipe?
Het zorgt voor een unieke, universeel herkenbare naam voor elk mogelijk vertakt alkaan, ongeacht hoe complex.
Wat bepaalt de stam van een organisch molecuul?
De langste ononderbroken keten van C-atomen in het molecuul.
Wat wordt bedoeld met een “vloeiende lijn”?
Een keten zonder onderbrekingen of splitsingen; de stam mag niet afbuigen of zijtakken bevatten.
Hoe noem je atoomgroepen die H vervangen in de stam?
Substituenten
Welke stam kies je als er meerdere ketens met evenveel C-atomen zijn?
en wat bepaald het
De keten met de meeste vertakkingen krijgt voorrang.
Het nummer van het C-atoom waar de zijgroep aan vast zit → aangeduid met een positietelwoord.
Hoe bepaal je van waar je de keten nummert?
Zo dat de eerste zijgroep het kleinst mogelijke nummer krijgt (→ lowest set of locants).
Wat is de correcte systematische naam voor:
→ 3 methylgroepen op posities 2, 7 en 8 van een decaan?
2,7,8-trimethyldecaan
Worden Griekse telwoorden meegeteld in alfabetische volgorde?
Nee. Di-, tri-, tetra-... worden genegeerd bij alfabetisch rangschikken.
Wat is fout aan de naam: 3,4,9-trimethyldecaan?
De correcte naam volgens IUPAC is:
3,4,9-trimethyldecaan, tenzij een andere nummering een lagere set locants oplevert.
Wat is de correcte naam:
3-ethyl-4-methylhexaan of 4-ethyl-3-methylhexaan?
3-ethyl-4-methylhexaan
→ laagste nummer voor ethyl, die alfabetisch vóór methyl komt
Wat is het principe van de lowest set of locants?
Bij keuze tussen verschillende nummeringen kies je die waarbij de set plaatsnummers zo laag mogelijk is.
Hoe benoem je meerdere identieke zijgroepen?
Met een Griekse prefix:
2x = di-
3x = tri-
4x = tetra-
...
En elke krijgt een eigen positietelwoord, bv. 2,2-dimethylbutaan.
Wat betekent het voorvoegsel “iso-” bij isoalkanen?
Het duidt op de aanwezigheid van een methylgroep op het 2e C-atoom van de hoofdketen.
Geef een voorbeeld van een isoalkaan.
Isopentaan = CH₃–CH(CH₃)–CH₂–CH₃
Waarom is draairichting bij vertakkingen belangrijk?
Een vertakking plaatst zich altijd aan het verlengde van de keten, niet aan de zijkant van het laatste C-atoom.
Hoe duid je een vertakte zijgroep aan?
Met haakjes en volledige naam, voorafgegaan door een positie:
bv. 3-(1,1-dimethylethyl)heptaan
Wat betekent n-(3,3-dimethylbutaan-2-yl)?
Een vertakte zijgroep met 6 C-atomen, vertakt op C3 en gehecht op C2 → een complexe alkylgroep benoemd als een alkaan met -yl en positietelwoorden.
Wat is de triviale naam van propaaan-2-yl?
Wat is de triviale naam van 2-methylpropaaan-1-yl?
Wat is de triviale naam van butaan-2-yl?
Wat is de triviale naam van 2-methylpropaan-2-yl?
Isopropyl
Isobutyl
sec-butyl
tert-butyl
Welke informatie blijft essentieel bij vertakte zijgroepen?
Exacte structuur
Positie van aansluiting op hoofdketen
Eventuele vertakkingen binnen de zijgroep
Telwoorden en haakjes bij systematische naam
Wanneer spreken we van een cyclische koolwaterstof?
Hoe wordt een cyclische verzadigde koolwaterstof genoemd?
Wat is de brutoformule van een cycloalkaan?
Wanneer de stam van een organisch molecuul een ringstructuur vormt i.p.v. een lineaire keten.
Cycloalkaan – de naam begint met “cyclo” gevolgd door de naam van het alkaan (vb. cyclohexaan).
CₙH₂ₙ
→ Omdat er één binding extra is (gesloten ring), zijn er twee H-atomen minder dan bij alkanen (CₙH₂ₙ₊₂).
Wat gebeurt er als een ringstructuur dubbele bindingen bevat?
Dan spreekt men van een onverzadigde of zelfs aromatische verbinding (vb. benzeen).
Hoe benoem je een vertakte cycloalkaan?
Zoek de langste ring → stam
Begin met “cyclo”
Voeg de uitgang -aan toe
Geef de plaats van vertakkingen aan met positietelwoorden
Rangschik de substituenten alfabetisch
Wat is de correcte systematische naam van deze molecule?
CH3
|
CH3 — C6H10 — CH3
1,1-dimethylcycloheptaan
Wat is de naam van een molecule met 6 C-atomen in een ring zonder vertakkingen?
Cyclohexaan
Hoe bepaal je het beginpunt van nummering bij cycloalkanen?
Zo dat de substituenten de laagst mogelijke nummers krijgen.
Wat betekent “onverzadigd” in de context van organische chemie?
Dat één of meer C-atomen slechts twee of drie bindingspartners hebben → er ontstaan dubbele of drievoudige bindingen.
Welke groepen vallen onder de onverzadigde koolwaterstoffen?
Alkenen (dubbele bindingen) en alkynen (drievoudige bindingen).
Waarom zijn alkanen algemeen weinig reactief?
Omdat ze enkel bestaan uit σ-bindingen (sigma-bindingen), die sterk en stabiel zijn. Er zijn geen zwakke of reactieve bindingsplaatsen.
Wat bedoelt men met een "interne factor" bij reactiviteit?
De interne factor verwijst naar de chemische opbouw en bindingsstructuur van het molecule zelf (dus niet omgevingsfactoren).
Wat is de standaardbindingsenthalpie (ΔHᵇ⁰) en waarvoor dient die?
ΔHᵇ⁰ geeft de hoeveelheid energie (in kJ/mol) die nodig is om een binding homolytisch te verbreken. Het helpt bij het inschatten van reactieve plaatsen in een molecule.
Waarom zijn C-H- en C-C-bindingen minder reactief?
Omdat hun ΔHᵇ⁰ hoog is:
C-H: 413 kJ/mol
C-C: 347 kJ/mol
→ Er is veel energie nodig om deze bindingen te verbreken.
Welke binding is zwakker en dus makkelijker te verbreken: een C=C of een C-C?
De π-binding in C=C is zwakker. De ΔHᵇ⁰ van een π-binding is 267 kJ/mol, dus lager dan een gewone C-C-binding (347 kJ/mol).
Welke uitzondering op de lage reactiviteit van alkanen wordt genoemd?
Krakingsprocessen: hierbij worden grotere alkanen homolytisch gebroken tot kleinere fragmenten, bij hoge temperatuur.
Waarom is de verbranding van alkanen zo moeilijk op gang te brengen?
Omdat het breken van de sterke C-H- en C-C-bindingen veel energie vereist → dus hoge activeringsenergie.
Welke binding is sterker: H–O of H–H?
H–O is sterker:
ΔHᵇ⁰(H–O) = 463 kJ/mol
ΔHᵇ⁰(H–H) = 436 kJ/mol
Welke bindingen worden gebroken bij volledige verbranding van alkanen?
Alle bindingen:
C–H
C–C
→ Alles wordt omgezet tot H₂O (met H–O-bindingen) en CO₂ (met C=O-bindingen)
Waarom zijn alkenen en alkynen reactiever dan alkanen?
Omdat ze π-bindingen bevatten die zwakker zijn dan σ-bindingen → makkelijker te verbreken en dus reactiever.
Welke binding wordt het eerst verbroken in het molecule:
CH₂=CH–CH₂–CH₂–CH₃
De π-binding van de dubbele binding (C=C), omdat die het laagste ΔHᵇ⁰ heeft (267 kJ/mol).
Wat zijn radicalen en hoe ontstaan ze in het menselijk lichaam?
Waarom zijn radicalen gevaarlijk voor het lichaam?
Radicalen zijn deeltjes met een ongepaard elektron, wat ze zeer reactief maakt. Ze ontstaan bij stofwisselingsprocessen of externe invloeden zoals sigarettenrook, vervuiling, UV-licht, stress, en uitlaatgassen.
Radicalen kunnen andere moleculen beschadigen, zoals DNA, eiwitten en lipiden. Dit leidt tot veroudering en ziekten zoals kanker, cataract, hartkwalen en ontstekingen doordat radicalen reageren met belangrijke celstructuren.
Wat is de rol van antioxidanten in het lichaam?
Antioxidanten neutraliseren radicalen door hen een elektron te geven zonder zelf instabiel te worden. Ze beschermen cellen tegen oxidatieve stress. Voorbeelden zijn vitamine C, E, zink, selenium, enzymen en lycopeen.
Wat is lycopeen en welke rol speelt het in radicalenvangst?
Lycopeen is een natuurlijk carotenoïde pigment met antioxiderende werking, vooral aanwezig in tomaten, watermeloen en paprikasoorten. Het vangt radicalen af en is effectiever dan vitamine E in het beschermen tegen oxidatieve schade.
Waarom hebben rijpe tomaten een hogere antioxidantwaarde?
Tijdens het rijpingsproces neemt het lycopeengehalte toe. Daarom bevatten rijpe tomaten meer antioxidanten dan onrijpe.
Wat gebeurt er bij de homolytische splitsing van een binding in een radicaalreactie?
Bij homolytische splitsing wordt een binding zó verbroken dat elk van de twee gevormde deeltjes één elektron meeneemt. Dit leidt tot vorming van twee radicalen.
Wat wordt aangeduid met de pijltjes in radicalaire mechanismes?
Een halve pijl duidt op de beweging van één enkel elektron. Bij het vormen van een radicaal ontstaan per verbroken binding dus twee halve pijlen.
Wat is het verschil tussen een substraat en een reagens in een radicaalmechanisme?
Het substraat is het grotere molecuul dat wordt aangevallen (vaak een alkaan), het reagens is het kleinere, meestal reactieve deeltje zoals een halogeenradicaal.
Wat is het verschil tussen de vorming van radicalen in een substraat vs. een reagens?
Bij substraten: homolytische splitsing naar elk atoom een pijl (1 pijlpunt)
Bij reagentia: splitsing tussen twee elektronenparen, 2 pijlen (twee pijltjes)
Geef een voorbeeld van een organische reactie waarbij radicalen een rol spelen.
De halogenering van alkanen zoals n-butaan met chloorgas (Cl₂) via een radicaalmechanisme. Hierbij ontstaat een chlorobutaan en een HCl-molecule.
Waarom worden alkanen als weinig reactief beschouwd?
Omdat alkanen enkel sterke σ-bindingen bevatten tussen C-C en C-H, zonder reactieve centra zoals elektronenparen of geladen atomen.
Ze bezitten geen functionele groepen die gemakkelijk reageren.
Wat is de sterische getal (SG) rond elk C-atoom in een alkaan, en wat betekent dit voor de structuur?
SG = 4 → Tetraëdrische oriëntatie met bindingshoek van 109,5°.
Gevolg: ruimtelijke structuur is symmetrisch → weinig sterische hinder.
Wat is de relatie tussen paraffine en alkanen?
Paraffine = Latijn voor ‘weinig reagerend’.
Alkanen worden ‘paraffinen’ genoemd door hun lage reactiviteit.
Ze reageren enkel met apolaire stoffen zoals O₂.
Wat is de ecologische impact van alkanen (uit bv. aardolie)?
Slechte afbreekbaarheid → olievervuiling, vissterfte, verstopte veren van vogels.
Wat is het doel van het kraken van alkanen?
Lange ketens → kortere alkanen, alkenen en H₂ (voor bruikbare toepassingen).
Industrieel zeer belangrijk (benzine, plastics, etc.).
Wat is het verschil tussen thermisch en katalytisch kraken?
Thermisch: bij hoge T° (700–900 °C), via radicalair mechanisme.
Katalytisch: bij lagere T° met katalysator (economisch efficiënter).
Wat is pyrolyse en in welke processen komt het voor?
Pyrolyse = thermische ontleding zonder zuurstof.
Komt voor bij cokesproductie, houtskool, houtvergassing, pyrolyse-ovens.
Praktisch voorbeeld: oven met pyrolysefunctie → 500 °C → vetten verdampen.
Waarom ontstaan bij pyrolyse ook alkenen?
Door radicalaire mechanismen → σ-bindingen breken → alkanen → alkenen + H•.
Wat is een homolytische substitutie en wat is het verschil met ionaire reacties?
Homolytisch: elk atoom houdt 1 elektron bij splitsing → radicalen.
Ionair: elektronenparen verschuiven asymmetrisch → ionen.
Wat is de rol van UV-licht bij de homolytische substitutie van alkanen?
Initiatie: UV-licht breekt Cl–Cl → vorming van Cl•-radicalen.
Geef het volledige mechanisme van Sₕ-reactie van n-butaan met Cl₂.
a. Initiatie: Cl₂ → 2 Cl• onder invloed van UV.
b. Propagatie: Cl• + C₄H₁₀ → HCl + C₄H₉•
→ C₄H₉• + Cl₂ → C₄H₉Cl + Cl•c. Terminatie: 2 Cl• → Cl₂ / C₄H₉• + Cl• → C₄H₉Cl / 2 C₄H₉• → C₈H₁₈
Waarom wordt Cl₂ gebruikt en geen HCl?
HCl is polair → vormt Cl⁻ ionen i.p.v. radicalen → geen Sₕ-reactie.
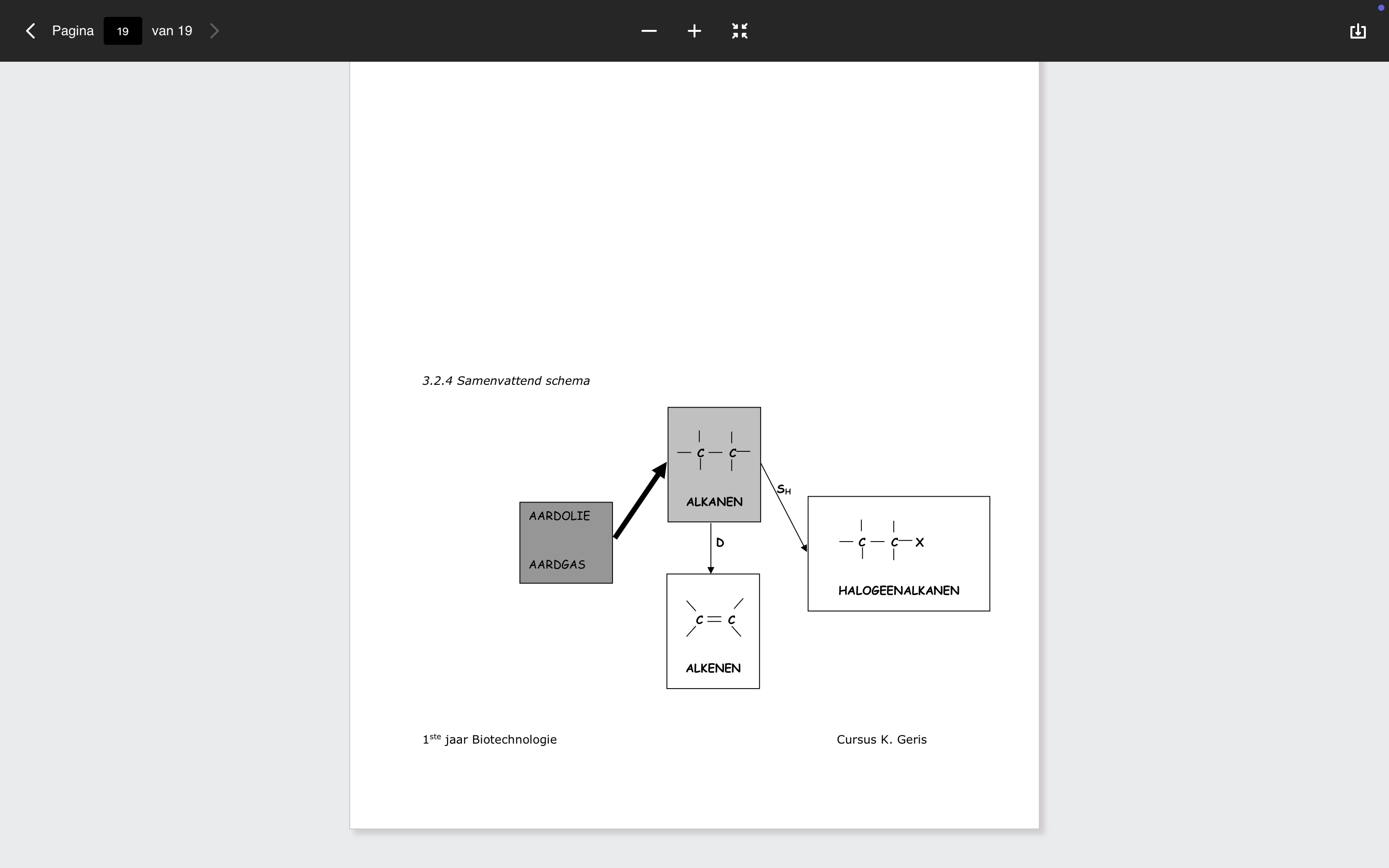
Wat zijn de drie belangrijkste transformaties van alkanen volgens het schema?
a. Verbranding (D): met O₂ → CO₂ + H₂O
b. Kraken (D): naar kortere alkanen + alkenen + H₂
c. Homolytische substitutie (Sₕ): naar halogeenalkanen
Wat is het verschil tussen D en Sₕ in het schema?
D = degradatiereactie (bindingen breken)
Sₕ = substitutie van H door halogeen (zonder verandering van C-skelet)
Waarom leidt Sₕ tot halogeenalkanen terwijl kraken tot alkenen leidt?
Sₕ = vervanging H door X via radicalen (met UV)
Kraken = splitsing C-C → nieuwe C=C via radicalen en T°