Les 3
1/13
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced |
|---|
No study sessions yet.
14 Terms
Hoe werkt activating O en P directing substituents
alkyl groep (alkeen) stabiliseert sigma complex via inductie, doneren elektron dichtheid via sigma binding. Substituenten met vrij elektronen paar stabiliseren complex via resonantie
snelheid van deactivating meta directing substituents
electrofiele substitutie van nitrobenzeen is 100.000x langer dan voor benzeen
Wordt para en orth isomeers gevormd wanneer gewerkt wordt met deactivating meta-directing substituents?
er wordt vooral meta isomeer gevormd, klein beetje ortho en para
waarom vormt orhto substitutie op nitrobenzeen niet?
door onstabiele versie met positieve lading dicht bij elkaar, hetzelfde geld voor para substitutie
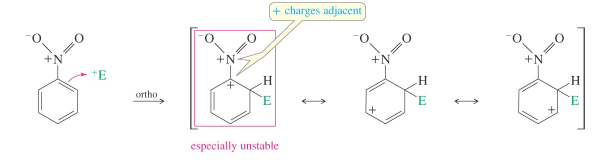
structuur van meta directing deactivator
het atom verbonden aan de aromatische ring is gedeeltelijk positief geladen. Elektrondichtheid is withdrawn inductively langs de sigma binding, hierdoor is de ring minder elektron rijk dan de benzeenring
Waarom zijn halogenen deactiverend (zuigend) naar elektrofiel substitutie maar wel ortho/para directing?
door de hoge elektronegativiteit van de halogenen, hierdoor zuigen ze de weggetroken elektronen dichtheid langs de sigma bond en het vrije elektronen paar stabiliseert sigma complex via resonantie. Since halogens are very electronegative, they withdraw electron density from the ring inductively along the sigma bond. • But halogens have lone pairs of electron that can stabilize the sigma complex by resonance.
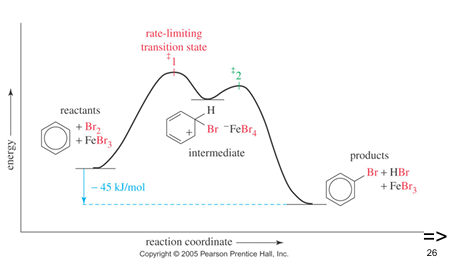
energie diagram van brominatie
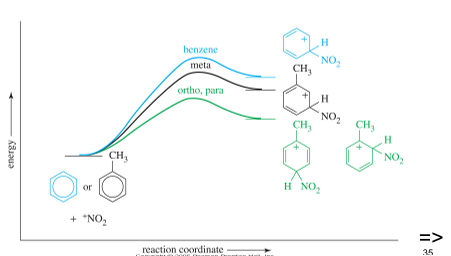
Energie diagram van nitrificatie, laat zien dat ortho-para meest stabiel is
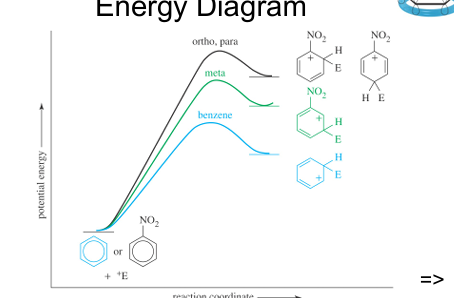
energie diagram van ortho/meta/para substitutue van nitrobenzeen, ortho en para onstabielst. benzeen is stabielst
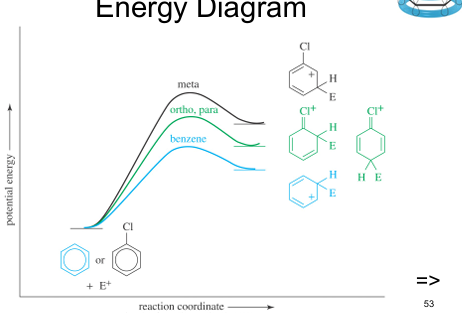
energie diagram van ortho.meta.para substitutie op benzeen met chloor. benzeen is meest stabiel, ortho para minst