H2 reacties || 2B - Organische chemie: reactiviteit - H2 Alkanen - reacties
1/6
Earn XP
Description and Tags
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
7 Terms
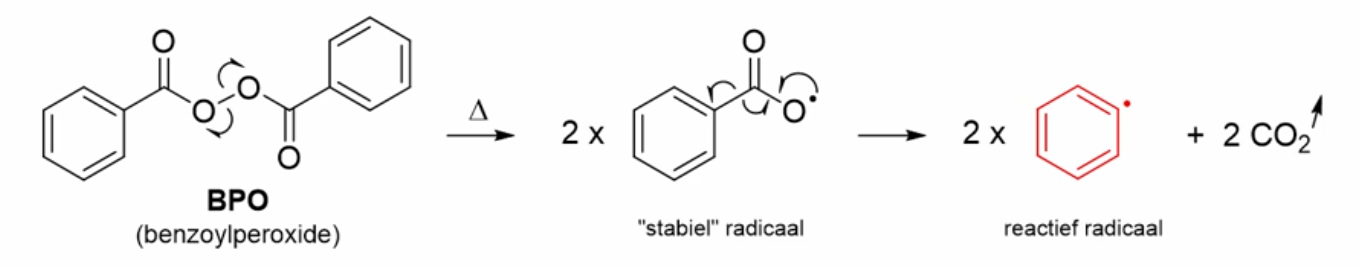
radicaalinitiator BPO
p11
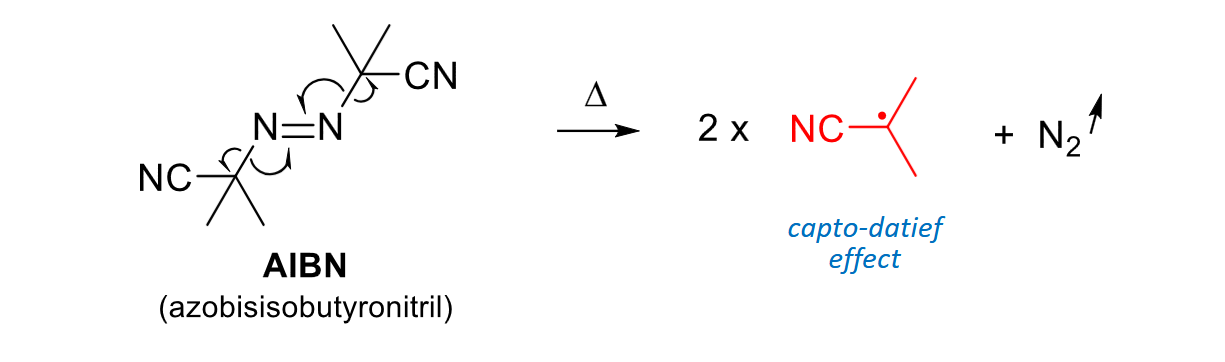
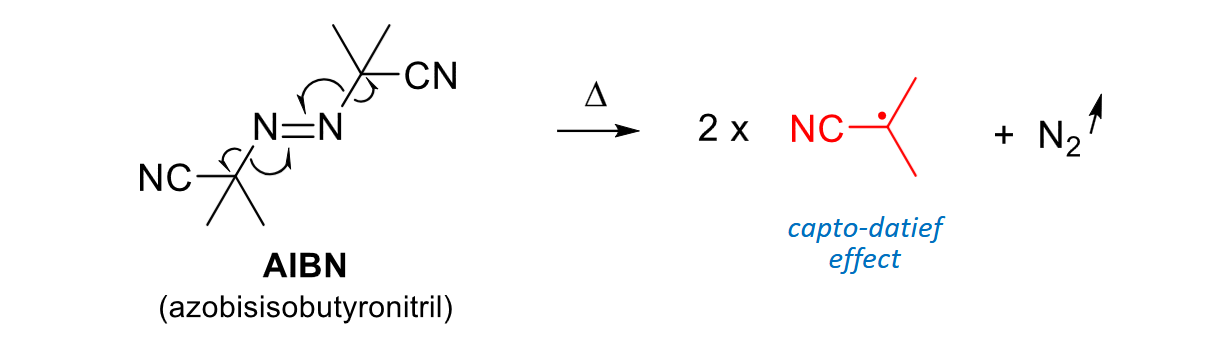
radicaalinitiator AIBN
p11
radicaalinitiator di-t-BU-peroxide
p11
fotochemische halogenering
alkaan → halogeenalkaan
RCH2R → RCHClR
p11.5
Initiatie
Br2 of Cl2
via UV-lamp → UV-licht doet zwaktste binding breken, nl Cl-Cl
Propagatie
Cl. is heel reactief
H’s zitten aan buitenkant alkaan → kost weinig energie om binding te breken + zijn makkelijk bereidkbaar
door toevalligheden van botsingen
blijft heel de tijd doorgaan → tot radicalen elkaar beginnen tegenkomen en ze op geraken (en lamp uit waardoor geen nieuwe radicalen) → terminatie stap
Terminatie
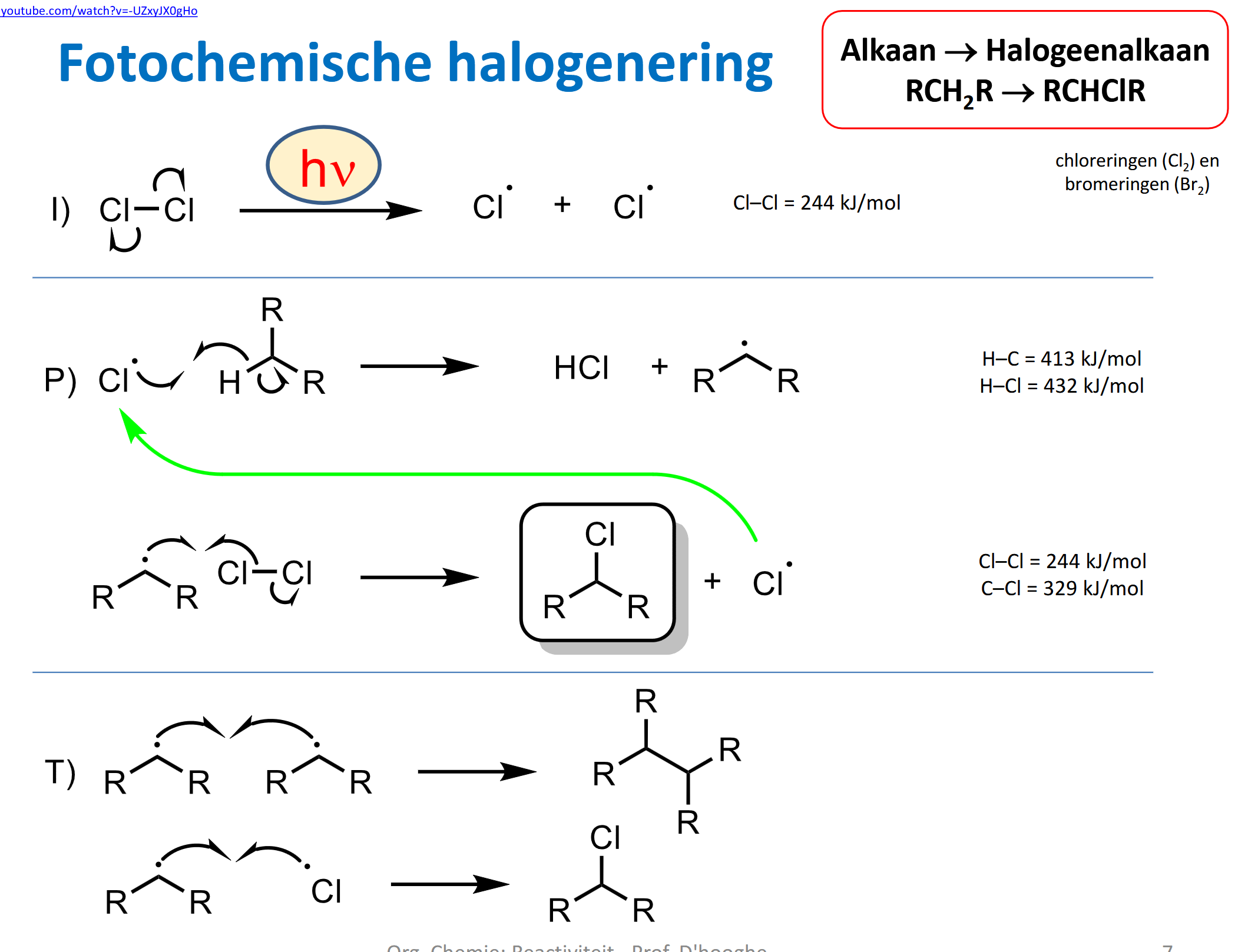
Kraking
p12
thermische kraking
alkanen breken op willekeurige plaatsen
vorming reactieve, primaire radicalen
korte alkeen ketens worden uitgestoten
niet kunnen uittekenen, enkel dit weten
Oxidatie: radicalaire reactie met O2
p 12.5
O2 is stabiel diradicaal
vorming hydroperoxide
belangrijk proces bij oa oxidatie van vetten in levensmiddelen
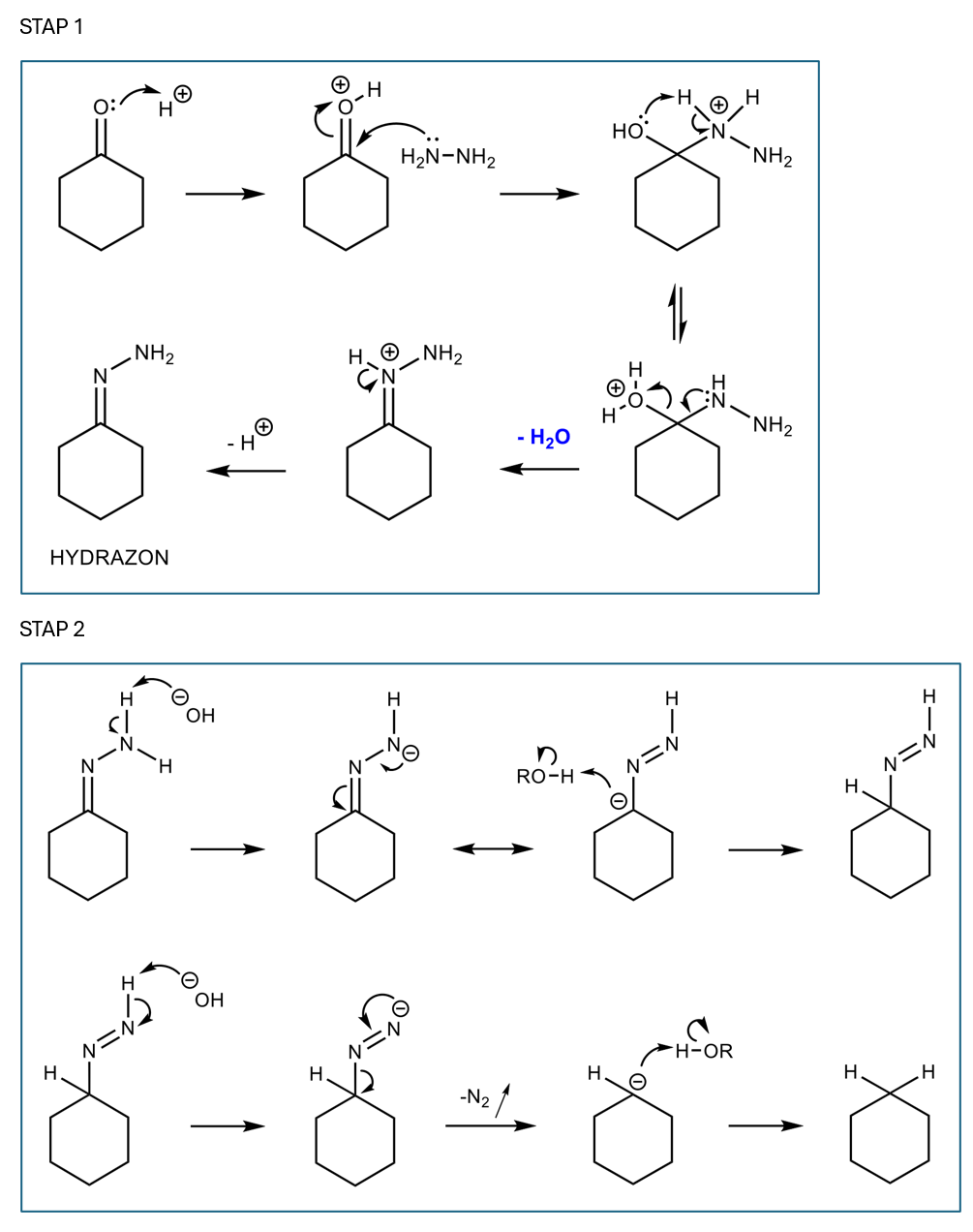
Wolff-Kishner-reductie
Reductie aldehyden en ketonen: C=O vervangen door CH2
p13.5
Stap 1: nucleofiele additie, vorming hydrazon
protoneren carbonyl, zo kan nucelofiel deeltje beter aanvallen
// gaat open
H2O+ is goede LG (wordt als neutraal water uitgestoten)
door wat zuur toe te voegen wordt H+ uitgestoten
vorming hydrazon
Stap 2: in nieuw medium, basisch milieu
base toevoegen
mesomere pijl! ((-) verandert van plaats)
N is meer elektronegatief dan C → 2de structuur is stabieler; 3de structuur is minder stabiel en reactiever
N2 uitstoten: kleine molecule uitduwen is entropisch interessant
laatste pijl is sws aflopen door groot pKa verschil