24.3: Regulatie van de celcyclus
1/30
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
31 Terms
slide regulatie celcyclus

Van welke fase van de celcyclus is de G0 fase eigenlijk een verlengde
G1
Wat gebeurt er eigenlijk in de G1 fase
coördinatie van de celgroei en celdeling (veel eiwit- en RNA synthese nodig)
bv eiwitkinase TOR regelt eiwitsynthese en overgang naar S-fase
De cel zal voldoende in volume moeten toegenomen zijn, dan pas zal het naar de S-fase kunnen overgaan.
Na het delen zijn de dochtercellen kleiner en moeten ze dus toenemen in volume (groeien).
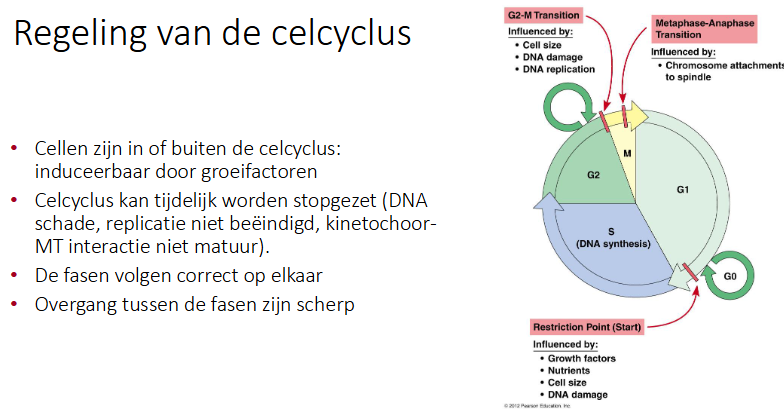
Welke transitiepunten vinden we terug in de celcyclus
Overgaan van de ene naar de andere fase:
G1/S (restrictiepunt)
als je voorbij het restrictiepunt gaat, weet je dat de cel zal delen. Als een cel in de G0 zit, moet het dat punt kunnen overwinnen om te kunnen delen.
Groeifactoren zullen initiëren dat de cel klaar is om in de celcyclus te treden.
Voldoende voedingsstoffen zijn nodig.
Voldoende volume is nodig.
Cel zal niet beslissen over te gaan als er veel DNA schade is, deze moet eerst hersteld worden.
G2/M
Kan pas wanneer de replicatie volledig verlopen is, DNA schade moet volledig hersteld zijn
Metafase-anafase transitie
MT moeten correct verbonden zijn met de kinetochoren (voorxwarde voor deze stap).
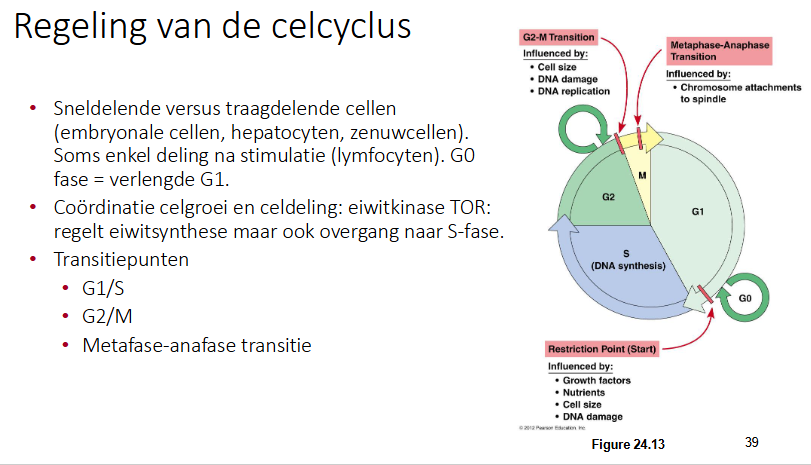
Wanneer kan de celcyclus tijdelijk worden stopgezet
DNA shade
replicatie niet afgerond
kinetochoor-MT interactie niet matuur
Wat is een heterokaryon
Een fusiecel met meerder kernen
Bespreek de regeling van de celcyclus door overdraagbare componenten
Microscopie
Genetica
Biochemie
Microscopie: celfusie-experimenten → we kunnen van 2 cellen één cel maken door een bepaalde chemische component toe te voegen. Dit is een ARTIFICIEEL experiment.
Heterokaryon S-fase + G1 fase → S-fase inductie
Heterokaryon M-fase + G1 fase → M-fase inductie
→ Er moet iets overgedragen worden van de ene naar de andere cel waardoor dit gebeurt. Er moet een overdraagbare component zijn.
Genetica: identificatie van cell-division-cycle (CDC) genen in gist
Temperatuur afhankelijke mutanten, ondermeer cycline afhankelijke kinase (vc Cdc2 induceert mitose, Cdc2 = Cdk1)
als de gist op een normale temperatuur groeit → geen fenotype, het eiwit is niet functioneel, zelfs met de mutatie
Temperatuur verhogen → eiwit is niet functioneel, fenotype is blokkage celcyclus en gisten zullen niet meer delen
Biochemie: injectie cytoplasma van een rijpe oöcyt in oöcyt geblokkeerd in meiose induceert vervollediging van meiose (Mitosis promoting factor = MPF = Cdc2 + mitotisch cycline)
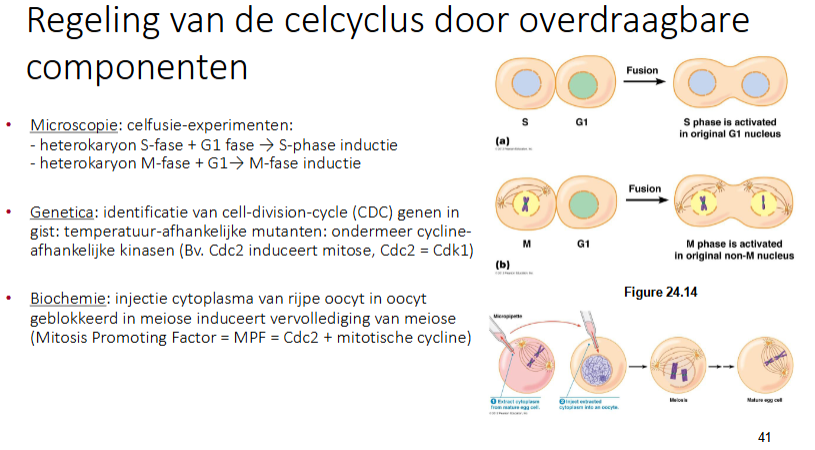
wat is mitosis promoting factor (MPF)
Cdc2 + mitotisch cycline
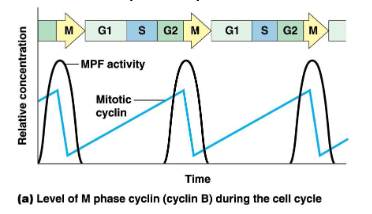
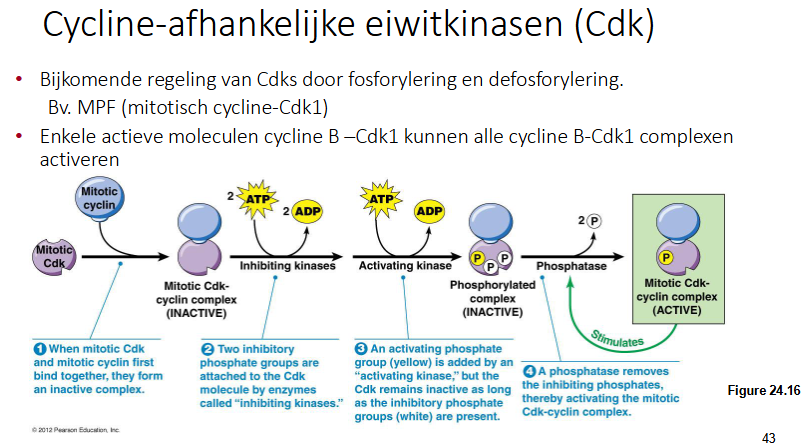
Wat kun je uit deze grafiek halen
Cdk’s zijn overdraagbare componenten die in staat zijn mitose te induceren (bv Cdc2 = Cdk1).
We zien dat het proteïne-kinase enkel op de G2/M overgang actief is, dan gaat het weer naar beneden.
Het kinase zelf (cdc2 = cdk1) heeft zekf geen cyclische expressie, het cdk is namelijk altijd aanxezig.
Het is de cycline die van concentratie verandert.
Cyclinen zijn activatoren van bepaalde cdk’s dus daarom piekt de activiteit van het MPF op een bepaald moment.
Wat zijn cyclinen
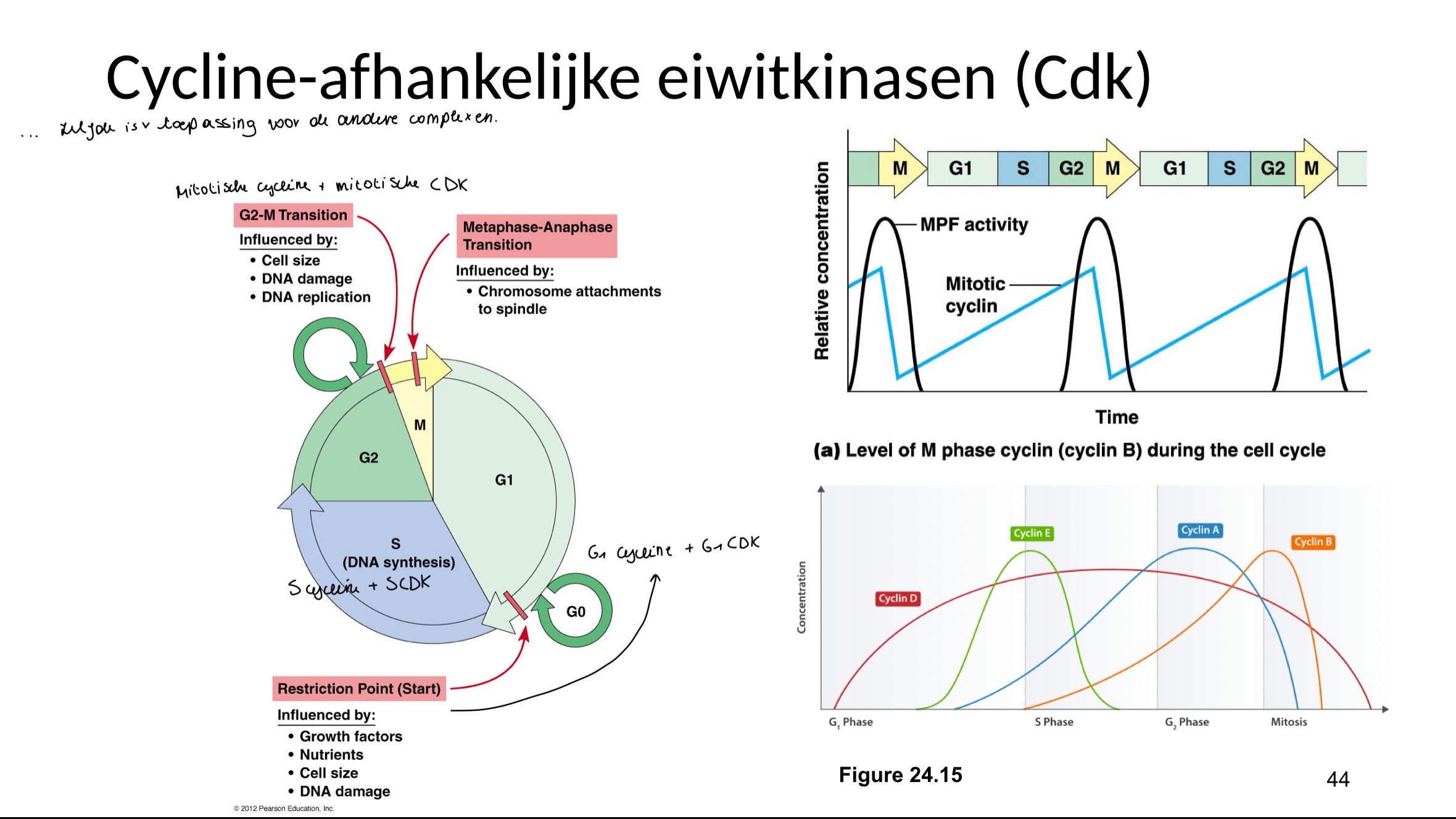
Voor G1, S, G2, G2-M: activatoren voor specifieke Cdk’s bv cycline B in MPF
‘+’ = geassocieerd met:
G1 cycline + G1-CDK (restrictiepunt)
S-cycline + S-CDK (S-fase)
Mitotisch (G2/M) cycline + mitotisch CDK (samen MPF)
Cyclines komen verschillend tot expressie in de celcyclus: G1 cycline heeft een grotere expressie in G1 fase, mitotisch cycline in de G2/M fase.
een CDK kan maar met 1 cycline associëren
nee, een CDK kan met meerdere cyclines associëren
Wat is cycline B
cycline in MPF
vb’en van ander kinases die ook belangrijk zijn
Polo-kinase
Aurora B
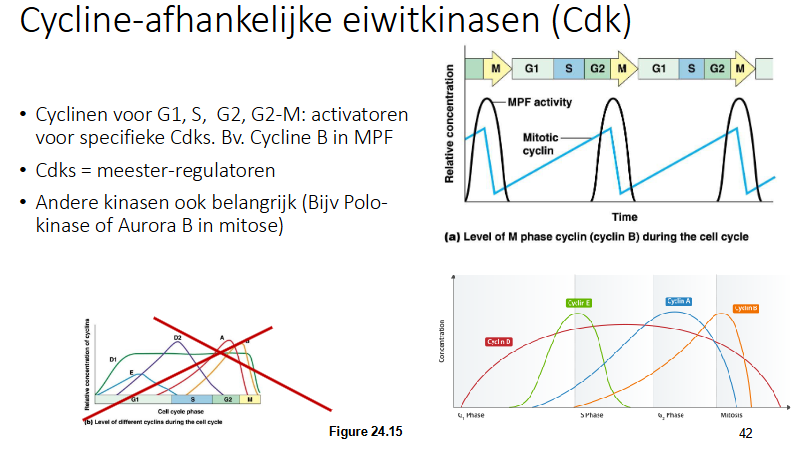
Hoe gebeurt de bijkomende regeling van CDKs door fosforylering en defosforylering
Uitgelegd voor mitotisch cycline en CDK
Mitotisch cycline bindt op mitotisch CDK en dit complex is nog steeds inactief.
CDK wordt gefoforyleerd door een inhiberend kinase. Het fosoforyleert CDK op 2 plaatsen.
3e fosforylering van mitotisch CDK door een activerend kinase (noodzakelijk om complex te activeren).
Wanneer de activerende fosfaatgroep gebonden is samen met de 2 inhiberende, is het complex nog steeds inactief.
Om het te activeren, zal een fosfatase de 2 inhiberende fosfaten verwijderen, dan pas hebben we een actief CDK. Dit verklaart ook de plotse stijging van de grafiek van daarnet.
Vanaf er enkele actieve mitotische CDK-cycline complexen zijn, zal het het fosfatase fosforyleren. Dit stimuleert het fosfatase waardoor het actiever is, hierdoor worden alle moleculen finaal gedefosforyleerd.
Positieve feedback loop
slide Cdk
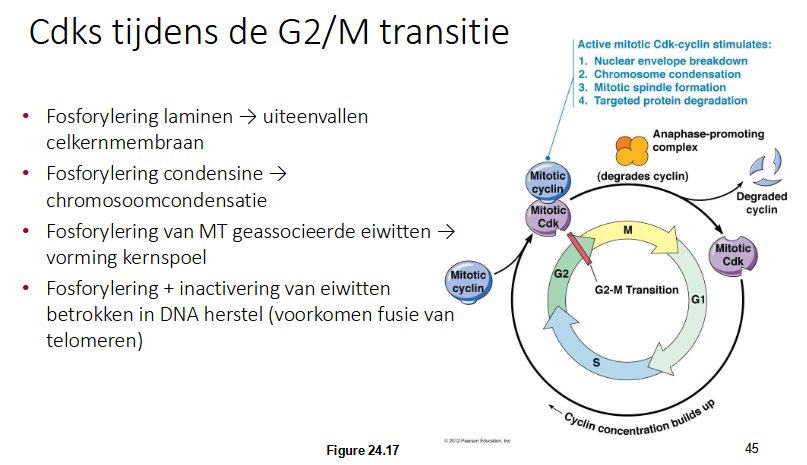
Wat weet je over Cdks tijdens de G2/M fase
Actief mitotisch Cdk-cycline stimuleert:
Fosoforylering van laminen → uiteenvallen celkernmembraan
Fosforylering van condensine → chromosoomcondensatie
Fosforylering van MT geassocieerde eiwitten → vorming kernspoel
Fosforylering + inactivering van eiwitten betrokken in DNA herstel (voorkomen fusie van telomeren)
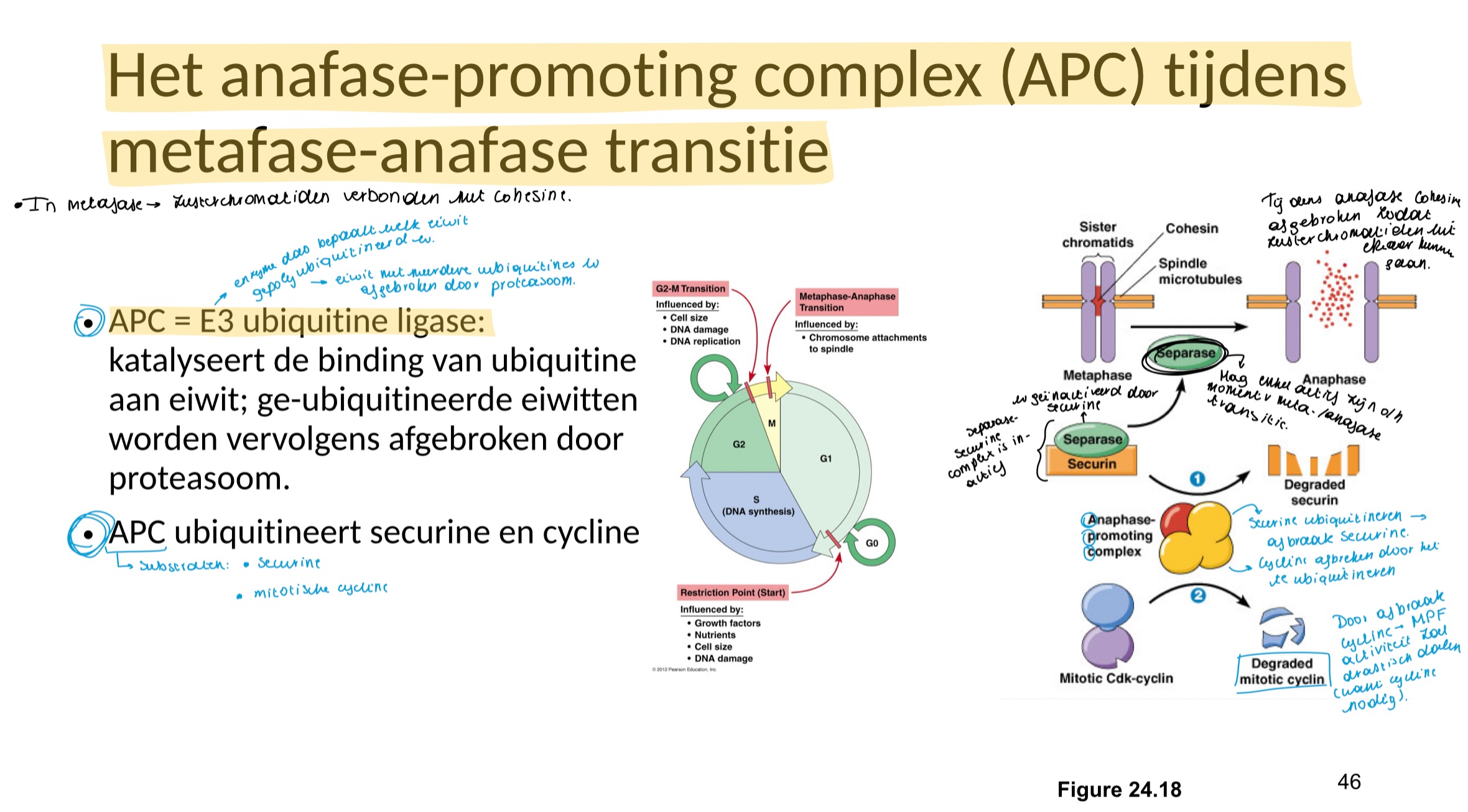
Wat is het anafase-promoting complex (APC) tijdens metafase-anafase transitie
APC = E3 ubiquitine ligase (enzyme dat bepaalt welke eiwitten geubiquitineerd moeten worden, een eiwit met meerder ubiquitinasen wordt afgebroken door een proteasoom
APC katalyseert de binding van ubiquitine aan een eiwit.
wat ubiquitineerd APC
securine en mitotisch cycline
slide proteasoom

WAt gebeurt er ivm cdk’s en cyclines in de overgang van G1 naar S fase
Door G1 cycline zal G1 CDK actief worden.
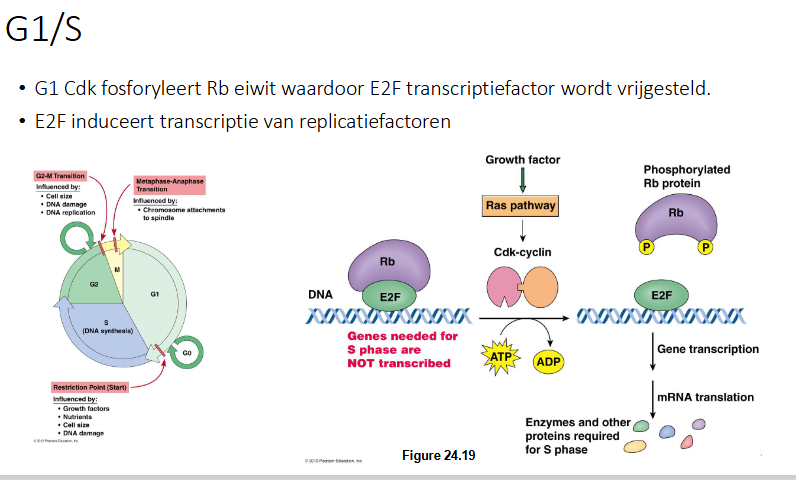
G1 CDK fosforyleert Rb eiwit (retinoblastoma) waardoor E2F regulerende transcriptiefactor wordt vrijgesteld.
E2F induceert transcriptie van replicatiefactoren.
Als E2F en retinoblastoma gebonden zijn, is het niet actief en is er geen transcriptie van de genen.
Een goeifactor activert de Ras pathway → CDK cycline complex.
CDK-cycline complex fosforleert retinoblastoma, waardoor het zal dissociëren van de E2F factor.
E2F komt vrij en zal transcriptie induceren.
Meerder eiwitcoderende genen worden afgeschreven die nodig zijn voor S-fase.
Wat zijn controlepunten ‘checkpoints’ en waar vinden we ze terug
Checkpoints (controlepunten): controle voor overgang naar volgende fase, zoniet aneuploidie, chromosoomfragmentatie, accumulatie van beschadigd DNA…
G1/S transitiepunt
G2/M transitiepunt
Metafase-anafase transisitiepunt
S-fase
DNA-schade controlepunt

In welke fase wordt het pre-replicatiecomplex gevormd, wat gebeurt er in de S-fase
G1
in de S-fase zullen ORC en de helicase laders dissociëren, MCMblijft want moet DNA strengen uiteen halen tijdens replicatie
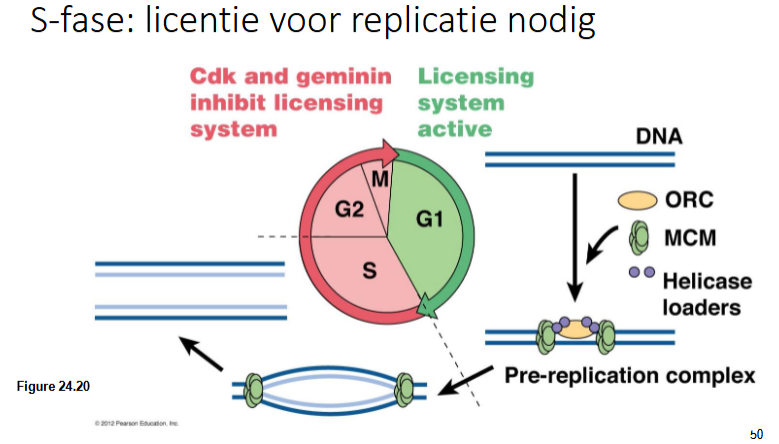
Hoe gebeurt de licentie voor replicatie in de S-fase
DNA kan maar 1 maal gerepliceerd worden in de S-fase
S-fase CDK fosforyleert MCM, ORC en helicase laders: activatie van replicatie
fosfo-ORC en fosfo-helicase laders dissociëren van het DNA, voorkomt hervergunning (door gefosforyleerd te zijn kunnen ze niet meer binden op het DNA)
fosfo MCM haalt de 2 DNA strengen uiteen tijdens de replicatie
als de replicons samenkomen, komt fosfo MCM los van het DNA
geminine bindt fosfo-MCM zpdat het niet terug op het DNA kan binden, geminine is aanwezig tot einde van mitose want in G1 moet het pre-initiatie complex weer gevormd kunnen worden
substraten APC complex
securine
cycline
geminine
Hoe gebeurt het DNA-replicaite controlepunt
Verzekert dat mitose niet kan beginnen zolang er nog replicatievorken zijn of er DNA schade is.
Herkenning replicatievorken door eiwitkinase ATR
kan ook geactiveerd worden door DNA schade
als er nog replicatievorken aanwezig zijn → replicatie is niet volledig
zolang replicatievorken aanwezig zijn is ATR actief
ATR fosforyleert fosfatase, maar inactiveert het
ATR inactiveert fosfatase nodig voor activatie van MPF (cel zorgt dat we geen G2/M transitie hebben)

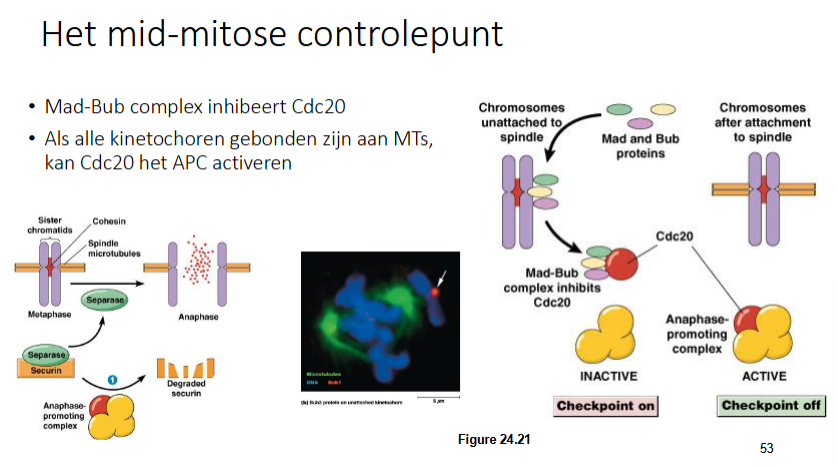
Hoe werkt het mid-mitose controlepunt
Mad en Bub eiwitten zullen tijdelijk associëren met kinetochoren die geen MT gebonden hebben.
Mad-Bub complex bindt aan een Cdc20, waardoor cdc20 niet actief is (cdc 20 is nodig voor activatie APC)
Het Mad-Bub met Cdc20 gebonden zal enkel gevormd worden als er chromosmen zijn met een kinetochoor die geen MT geassocieerd hebben. Het APC is dan inactief.
Als alle chromosomen gebonden zijn met de spoelfiguur, zal Mad-Bub niet meer cdc20 inhiberen, waardoor cdc20 APC kan activeren.
APC zal dan securine, mitotisch cycline en geminine ubiquitineren.
Hoe gebeurt het DNA schade controlepunt
Resulteert in inhibitie van G1, S of G2/M Cdks
Door DNA schade wordne eiwitkinasen ATR en ATM gefosforyleerd (geactiveerd)
Die activeren andere kinasen door fosforylering (checkpoint kinasen)
checkpointkinasen zullen p53 fosforyleren
Wanneer p53 niet gefosforyleerd is heeft het Mdm2 gebonden; wat een E3 ubiquitine ligase is en er dus voor zorg dat p53 afgebroken wordt door proteasoom
Als p53 gefosforyleerd wordt, wordt het gestabiliseerd door de fosforylering en zal Mdm2 dissociëren
p53 bindt op DNA regulerende transcriptiefactoren
2 opties
p53 induceert de expressie van p21 (Cdk inhibitor is)
Cdk cycline wordt geïnhibeerd waardoor het retinoblastoma niet kan fosforyleren en zo krijg je een cell cycle arrest
p53 zorgt voor exressie van Puma
Puma inhibeert Bcl2
Bcl zou normaal de apaptose inhiberen, maar omdat Puma Bcl2 inhibeert kan dat niet en gaat de cel in apoptose.
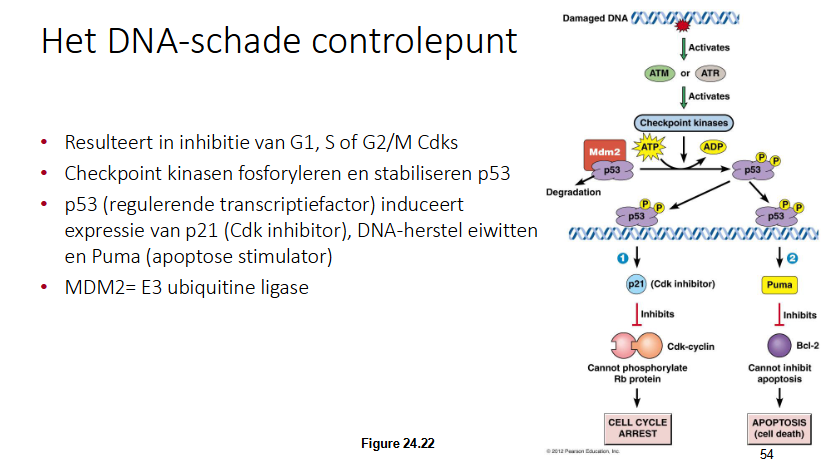
samenvatting controlepunten

welke oplossingen zijn er voor volgende uitdagingen
Juiste volgorde van de fasen
Voorgaande fase moet beëindigd zijn
Respons aan interne en externe stimuli (DNA schade; kinetochoor-microtubule interacties; omgevingsfactoren…)
Specifieke kinases (CDKs) die overgangen regelen.
Controlepunten: G1/S, S, G2/M, mid-mitose, DNA schade
Apoptose
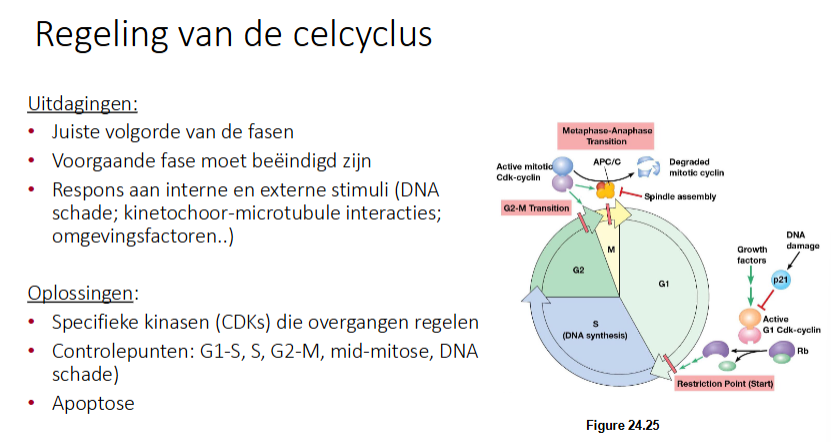
slide regeling celcyclus
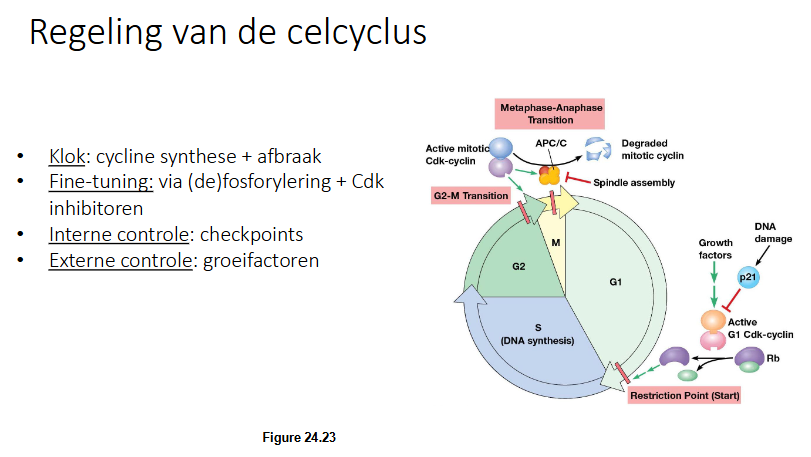
Cycline D vormt samen met Cdk een G1 Cdk-Cycline complex.
Cycline D komt dikwijls tot overexpressie in kankercellen. Waarom zou
overexpressie van cycline D tot kanker leiden?
Ontregeling van het G1/S: Het Cdk van het G1 cdk-cyclin D complex fosforyleert het Rb eiwit bij de G1/S
transitie. Door de aanwezigheid van meer cycline D zal meer Rb gefosforyleert worden zodat een cel
gemakkelijker voorbij de ‘restrictiepunt’ gaan en zal, zelf in de afwezigheid van een normaal groeifactor
signaal, overgaan in de S-fase.
(2) Ontregeling van het DNA-schade controlepunt: DNA schade zal minder vlug leiden tot stoppen van de
DNA replicatie bij verhoogde expressie van cycline D. Waarom? Bij DNA damage komt p21 (= cdk
inhibitor) tot expressie en inactiveert het G1 cdk-cyline complex. Maar nu zijn er véél meer cdk-cycline
complexen, zodat het moeilijker zal zijn voor p21 om alle cdk-cycline complexen te inactiveren.
(1) en (2) zal leiden tot verhoogde proliferatie en andere problemen geassocieerd met kanker.