Chapitre 6 : Equilibre acide-base
1/44
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
45 Terms
Quel rôle joue le CO2 dans l’équilibre acide-base ?
Le CO2 est un acide produit quotidiennement à hauteur de 20 moles par jour.
Il participe directement à l’acidité du sang via sa conversion en acide carbonique.
Comment le CO2 est-il éliminé ?
Les reins éliminent au maximum 100 à 150 mmol de CO2 en 24h
C’est le poumon qui joue le rôle principal dans l’élimination du CO2
Que se passe-t-il si on hypoventile ?
Il y a une rétention de CO2 → sa concentration augmente dans le sang
Cela conduit à une acidose respiratoire
Peut-on modifier notre pH volontairement ?
Oui : en respirant plus lentement (ex 7x/ min au lieu de 15x/min), on double la concentration en CO2 dans le sang
Le pH chute plus rapidement, menant à une acidose
Le réflexe naturel est de revenir à une ventilation normale pour éliminer le CO2

Quel est le rôle des systèmes tampons ?
Ils servent à stabiliser le pH du sang et éviter des variations trop importantes.
Quels sont les principaux systèmes tampons ? (1)
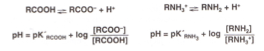
1. Les protéines plasmatiques :
Comportent des groupements amine (−NH₂) et carboxyle (−COOH).
Ces groupes peuvent agir comme acide ou base, ce qui permet d’appliquer l’équation d’Henderson-Hasselbalch.
Quels sont les principaux systèmes tampons ? (2)
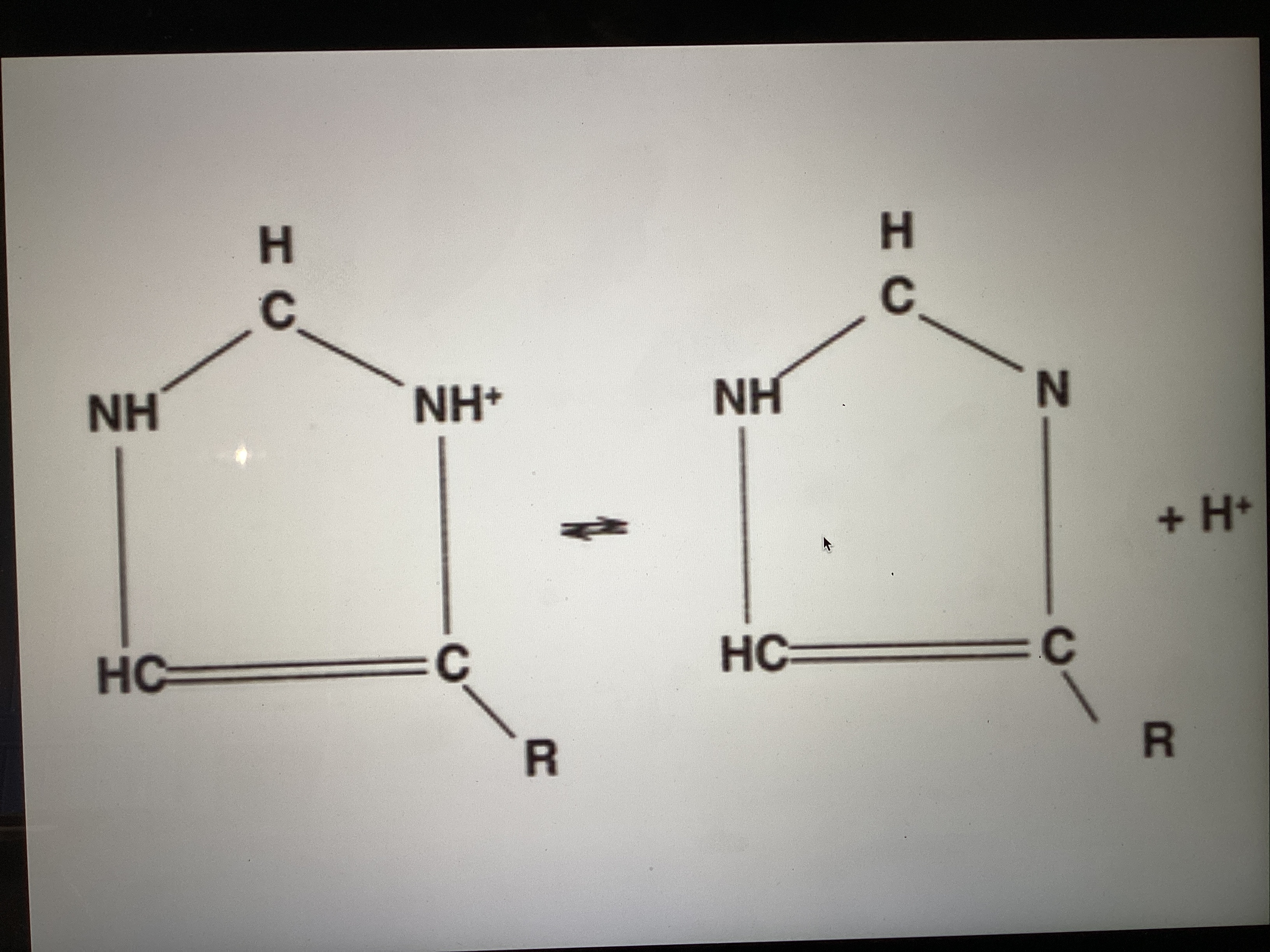
2. Le groupe imidazole de l’histidine dans l’hémoglobine :
Le groupe imidazole peut donner ou capter un H⁺.
Il y a 38 résidus d’histidine par molécule d’hémoglobine, ce qui donne une très grande capacité tampon.
Quels sont les principaux systèmes tampons ? (3)
3. Le système acide carbonique – bicarbonate (H₂CO₃ / HCO₃⁻) :
H₂CO₃ (acide carbonique) se dissocie en H⁺ + HCO₃⁻.
Ce système est le plus important dans le sang.
L’équation d’Henderson-Hasselbalch peut être utilisée ici aussi.

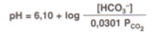
De quoi dépend la concentration en H₂CO₃ ?
De la concentration en CO₂, car le CO₂ + H₂O → H₂CO₃.
On peut donc exprimer cette concentration en fonction de la PCO₂ grâce au coefficient de solubilité du CO₂.
Pourquoi ce système est-il si efficace ?
Parce qu’il est à double régulation :
Le rein gère la concentration en HCO₃⁻
Le poumon gère la PCO₂
Il représente donc le tampon principal du sang.
Quelle est la valeur normale du pH sanguin ?
7,4
Qu’est-ce qu’un bon tampon ?
Un tampon est optimal quand son pKa est proche du pH cible.
Ici, le pKa du système bicarbonate est de 6,1, donc moins que 7,4, ce qui en fait un tampon imparfait chimiquement.
Pourquoi est-il malgré tout très efficace dans la nature ?
Car c’est le seul système de tampon régulé activement
Poumon → PCO2
Rein → HCO3-
C’es donc le tampon physiologique idéal, malgré un pKa sous-optimal
Quelles sont les valeurs typiques ?
[HCO₃⁻] = 24 mmol/L
PCO₂ = 40 mmHg
Cela permet d’avoir un pH de 7,4.
Quels sont les principaux systèmes tampons ? (4)
Le tampon phosphate est intéressant au niveau intracellulaire, car abondant à cet endroit.
Mais dans le plasma, sa concentration est faible, donc rôle marginal dans le sang.
Réaction d’équilibre :
HPO₄²⁻ + H⁺ ⇄ H₂PO₄⁻
Quelle est la relation normale entre le pH et le bicarbonate plasmatique ?
pH normal = 7,4
[HCO₃⁻] plasmatique normale = 24 mmol/L
Cette relation correspond à une PCO₂ artérielle de 40 mmHg.
Elle est représentée sur un schéma de référence où chaque PCO₂ a une courbe spécifique et parallèle.
![<ul><li><p class=""><strong>pH normal = 7,4</strong></p></li><li><p class=""><strong>[HCO₃⁻] plasmatique normale = 24 mmol/L</strong></p></li><li><p class="">Cette relation correspond à une <strong>PCO₂ artérielle de 40 mmHg</strong>.</p></li><li><p class="">Elle est représentée sur un schéma de référence où chaque PCO₂ a une <strong>courbe spécifique et parallèle</strong>.</p></li></ul><p></p>](https://knowt-user-attachments.s3.amazonaws.com/d7771afa-dcfb-49b6-8c83-ad6f7073a826.png)
Que se passe-t-il dans un choc cardiogénique ?
Les tissus produisent des acides lactiques (lactates).
Cela peut provoquer une acidose métabolite aigüe
Quels sont les effets sur le bicarbonate et le pH dans un choc cardiotonique?
Le bicarbonate va être consommé pour tamponner les protons (H+)
Il chute par exemple de 24 → 14 mmol/L
Le pH chute rapidement jusque 7,2, voire moins
Comment l’organisme réagit-il ?
Le pH acide stimule la respiration
La personne hyperventile, ce qui fait baisser la PCO2 (ex 40 → 21 mmHg)
Le pH remonte jusqu’à 7,34 grâce à la compensation respiratoire
Attention : les lactates sont toujours présents et le bicarbonate est toujours bas mais le pH est corrigé
Pourquoi le pH est-il si vital à maintenir ?
Le pH conditionne l’activité des enzymes : chaque enzyme a un pH optimal de fonctionnement
Une variation de pH perturbe la structure des protéines, leur activité et les réactions biochimiques
L’organisme tolère très mal les écarts de pH → Il dispose de multiples systèmes de régulation
🔼 Alcalose métabolique (ex. vomissements répétés)
Que se passe-t-il lors de vomissements fréquents ?
Le patient perd du H+ (contenu acide de l’estomac)
cela provoque une alcalose métabolique car [HCO₃⁻] augmente et le pH aussi
🔼 Alcalose métabolique (ex. vomissements répétés)
Comment l’organisme compense-t-il ?
Il y a une hypoventilation réflexe → PCO₂ augmente.
Cela ramène le pH vers la normale.
🔼 Alcalose métabolique (ex. vomissements répétés)
Pourquoi cette compensation est-elle moins efficace ?
L’hypoventilation entraîne une baisse de l’O₂ → hypoxie.
L’hypoxie relance la respiration via d’autres boucles de régulation.
👉 La compensation par hypoventilation est donc limitée.
📊 Le diagramme de Davenport
Que représente-t-il ?
Il montre la relation entre [HCO₃⁻] plasmatique et le pH.
Chaque ligne correspond à une PCO₂ spécifique :
Ligne normale : PCO₂ = 40 mmHg
Hypoventilation → on passe aux lignes 60 → 80 mmHg
Hyperventilation → on passe aux lignes 30 → 20 mmHg
![<ul><li><p class="">Il montre la <strong>relation entre [HCO₃⁻] plasmatique et le pH</strong>.</p></li><li><p class="">Chaque <strong>ligne correspond à une PCO₂ spécifique</strong> :</p><ul><li><p class="">Ligne normale : <strong>PCO₂ = 40 mmHg</strong></p></li><li><p class=""><strong>Hypoventilation</strong> → on passe aux lignes <strong>60 → 80 mmHg</strong></p></li><li><p class=""><strong>Hyperventilation</strong> → on passe aux lignes <strong>30 → 20 mmHg</strong></p></li></ul></li></ul><p></p>](https://knowt-user-attachments.s3.amazonaws.com/6cf1ec64-501d-4adc-bfda-d3d4c86a9a14.png)
📊 Le diagramme de Davenport
Que permet-il de visualiser ?
L’effet de la ventilation sur le pH, à bicarbonate constant.
Il synthétise les compensations respiratoires dans les troubles acido-basiques.
Quelles sont les deux types d’acide ou d’alcalose ?
Respiratoire donc liées à la ventilation trop ou pas assez et donc liées au CO2
Métabolique donc il y a soit une acide ou une base qui s’accumule
🟥 Acidose respiratoire (tuyau)
Quelle est la cause d’une acidose respiratoire ?
Hypoventilation (ex. crise d’asthme sévère, bronchite chronique).
→ Les bronches ne permettent pas d’amener suffisamment d’air au niveau des alvéoles
🟥 Acidose respiratoire
Que se passe-t-il au niveau du CO₂ et du pH en cas d’acidose respiratoire ?
Le CO₂ augmente → pH diminue → acidification du sang.
🟥 Acidose respiratoire
Quelle est la compensation d’une acidose respiratoire ?
Compenstion métabolique par le rein → production de HCO3- augmente
🟥 Acidose respiratoire
Mécanisme de la compensation rénale dans l’acidose respiratoire ?
Plus de CO₂ → pousse la production de HCO₃⁻ par le rein → pH remonte vers 7,4.
🟥 Acidose respiratoire
Comment savoir si une acidose respiratoire est aiguë ou chronique ?
Si HCO₃⁻ est normal = aiguë ;
HCO₃⁻ élevé (> 24 mmol/L) = chronique (compensation rénale active).
🟦 Alcalose respiratoire
Quelle est la cause d’une alcalose respiratoire ?
Hyperventilation (anxiété, haute altitude, volontaire).
Si on est à 5000m, on respire beaucoup plus vite que si l’on est au niveau de la mer.
🟦 Alcalose respiratoire
Que se passe-t-il au niveau du CO₂ et du pH en cas d’alcalose respiratoire ?
CO₂ diminue → pH augmente.
🟦 Alcalose respiratoire
Quelle est la compensation d’une alcalose respiratoire ?
Compensation métabolique → rein diminuent la réabsorption de HCO3-
🟦 Alcalose respiratoire
Pourquoi la compensation n’est-elle pas complète ?
Le rein compense lentement et pas totalement.
🟥 Acidose métabolique
Quelle est la cause d’une acidose métabolique ?
accumulation d’acide qui va consommer le HCO3-. Son taux va donc diminuer.
🟥 Acidose métabolique
Exemples de causes d’acidose métabolique ?
Diarrhée importante (perte de base)
Acidose lactique = dysfonctionnement globale de l’organisme
→ Le débit cardiaque ne suffit pas et donc les tissus passent par le métabolisme anaérobie. Il y a une production de lactates par réduction du pyruvate. Cela permet à la glycolyse de continuer à fonctionner puisque le NADH doit continuer à être oxydés pour pouvoir être réutilisé
Acidocétose diabétique
→ Il y a des corps cétoniques qui peuvent être produits lors d’une crise diabétique
Intoxication à l’aspirine
→ Tentative de suicide marchent mieux avec de la benzodiazépines
→ Donne une acidose dû à l’acide salicylique
🟥 Acidose métabolique
Que se passe-t-il au niveau du bicarbonate et du pH ?
HCO₃⁻ est consommé → baisse → pH diminue.
🟥 Acidose métabolique
Quelle est la compensation d’une acidose métabolique ?
Compensation respiratoire → hyperventilation → CO₂ ↓ → pH ↑.
🟦 Alcalose métabolique
Quelles sont les causes d’une alcalose métabolique ?
Perte d’acide gastrique (vomissements)
Apport exogène de HCO₃⁻
🟦 Alcalose métabolique
Q : Que se passe-t-il au niveau du bicarbonate et du pH ?
HCO₃⁻ ↑ → pH ↑.
🟦 Alcalose métabolique
Q : Quelle est la compensation d’une alcalose métabolique ?
Compensation respiratoire → hypoventilation → CO₂ ↑ → pH ↓.
🟦 Alcalose métabolique
Pourquoi cette compensation est-elle limitée ?
Hypoventilation → hypoxie → respiration relancée → compensation stoppée.
Quelles sont les 4 grandes situations à retenir ?
Acidose respiratoire → compensation métabolique
Acidose métabolique → compensation respiratoire
Alcalose respiratoire → compensation métabolique
Alcalose métabolique → compensation respiratoire
Quel système compense plus rapidement : respiration ou rein ?
Respiration : compensation en quelques minutes
Rein : compensation en quelques jours