Säure-Basen GG
1/38
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
39 Terms
Grundlage Broensted
Teilchen, die Protonen abgeben gelten als Säuren (Protonendonatoren) und Teilchen, die Protonen aufnehmen, als Basen (Protonenakzeptoren)
Säure-Base Reaktion → Protolyse (Protonenübergang)
Es sind 2 korrespondierende S-B- Paare an der Reaktion beteiligt
Wasser Besonderheit
H2O und andere Teilchen können sowohl als Säure als auch als Base wirken
→ Ampholyt (amphotere Teilchen)
Bei Reaktion mit starken Säure Protonenaufnahme
Bei Reaktion mit starken Base Protonabgabe
H2O + HA → H3O+ + A-
H2O + B → OH- + BH-
Ionenprodukt Wasser
Die Konzentration der entstehenden Oxonium- und Hydroxid-Ionen ist sehr klein (ampholyt-Reaktion)
c(H3O+) = c(OH-) = 10-7 mol/L
Daraus mithilfe MWG Berechnung Ionenprodukts:
Kw=c(H3O+) * c(OH-) = 10-14 mol2/ L2
Gilt nicht nur für reines H2O, sondern auch für verdünnte Lösungen
→ c(H3O+) und c(OH-) hängen voneinander ab
Aus Ionenprodukt folgende Definition:
pH+pOH = 14
c(H3O+) = 10-pH
Ph-Wert
Der pH-Wert einer Lösung ist definiert als der negative dekadische Logarithmus des Bertrags der in mol/L angegeben Konzentration der H3O+-Ionen:
pH= -lg(c(H3O+))
Analog gilt für den pOH-Wert: pOH=-lg(c(OH-))
Bsp: c(H3O+)= 3,5×10-5 mol/l
pH → -lg(3,5×10-5mol/l) = 4,46
Zusammenhang c(H3O+) mit ph Wert
Saure Lösung:
0<pH<7 ; c(H3O+)>10-7mol/L
Neutrale Lösung:
pH= 7
c(H3O+) = 10-7 mol/L
Alkalische Lösung:
7<pH<14
c(H3O+) < 10-7 mol/L Daraus
→ Je saurer Lösung, desto höher H3O+ Konzentration
Säure und Basenkonstanten
sind Stoffkonstanten → Vergleich Bestreben von Teilchen, in wässrigen Lösungen Protonen abzugeben/aufzunehmen
Produkt aus GG-Konstante und c(H2O)
Starke Säuren/Basen:
vollständige Protolyse
Schwache Säuren/Basen:
unvollständige Protolyse
Auch: pKs/pKb zum Vergleich von Säuren/Basen untereinander
!! Ks * Kb = 10-14 oder pKs+pKb=14
Je kleiner pKs/pKb, desto stärker ist Säure/Base
Je stärker eine Säure, desto schwächer korrespondierende Base
Was ist mir Säure/Base Konstanten möglich ?
Ermittlung pH-Werte von Lösungen
Ermittlung Konzentration Säure/Base mit pH-Wert
Bei starker Säure/Basen:
Konzentration der H3O+/OH- Ionen entspricht Anfangskonzentration c0 der Säure/Base
Bei schwachen Säuren/Basen:
Säure steht im GG mit ihrer korrespondierenden Base:
HA + H2O → A- + H3O+
Ks: c(H3O+) * c(A-)/c(HA)
C(H3O+) = c(A-)
Ks= c(H3O+)2/c(HA)
Schwache Säuren disoziieren nur wenig → c(HA) ungefähr c0(HA)
Was kann mit den Formeln der schwachen Säure machen, wenn pH bekannt?
Konzentrationen der Säure/Base berechnen
c0(HA) = c2(H3O+)/Ks
c0(B) = c2(OH-)/Kb
Titration / ÄP bei starker oder schwachen Säure/Base
quantitaves Analyseverfahren; unbekannte c kann durch Zugabe Maßlösung bekannter c bestimmt werden
Reaktion muss messbaren Endprodukt haben
Säure/Base Titrationen : Indikatoren/pH-Elektroden
ÄP erreicht wenn Stoffmenge Säure/Base = Stoffmenge Säure/Base in Analyselösung
→ starke Säure/Base: ÄP bei pH 7 (Neutralisationstitration)
→ schwache Säure + starke Base: pH-Wert am ÄP größer als 7 (Anionen aus schwachen Säure basisch reagieren
→ schwache Base+ starke Säure: pH-Wert am ÄP kleiner als 7

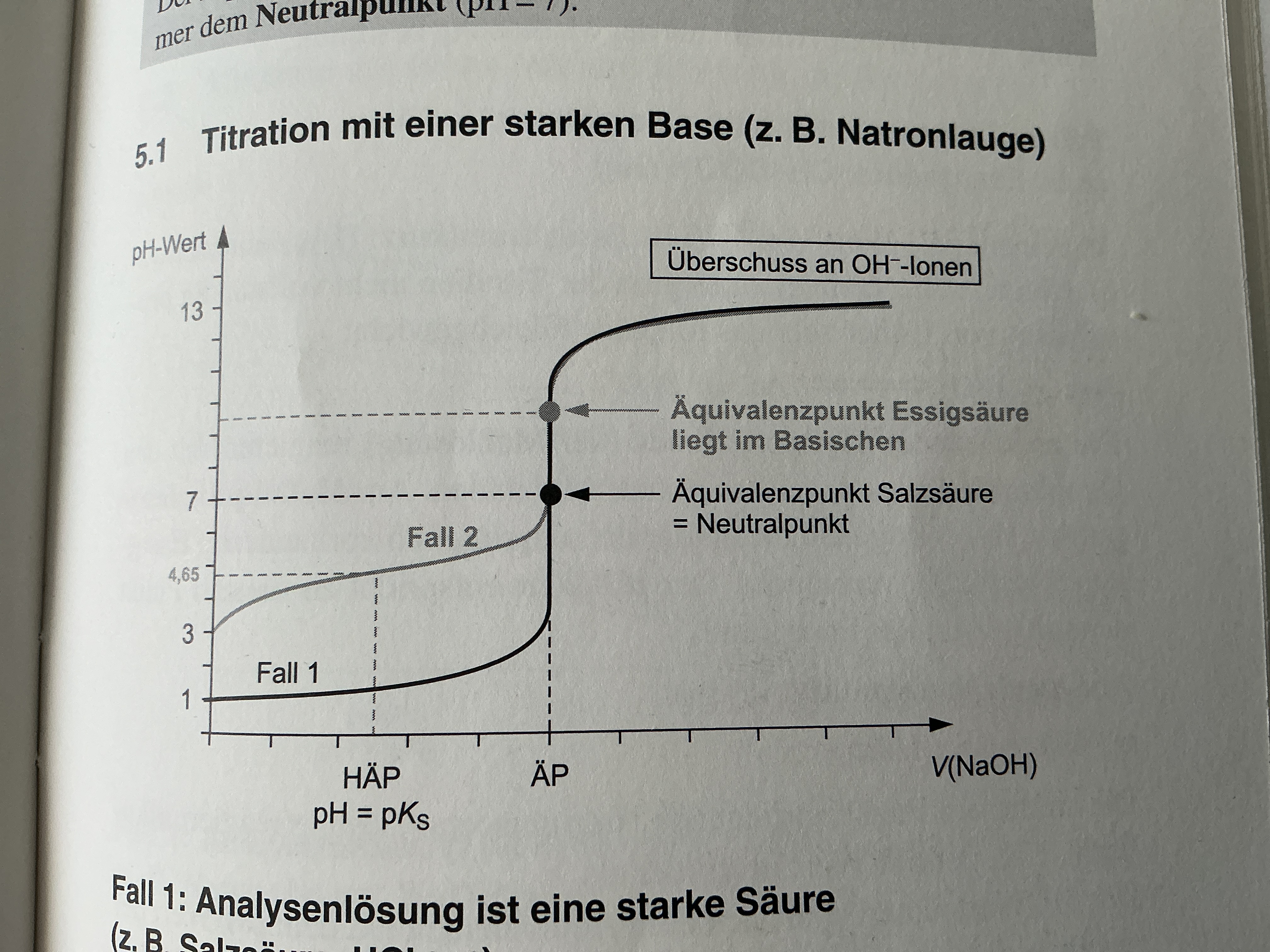
Titrationskurve mit starker Base
Starke Säure wird mit starker Base titriert
Anfangs pH-Wert → pH= -lg(c(Säure))
c(H3O+) = c0(Säure)
ÄP → Genauso viel Base hinzugegeben, wie Säure vorhanden ist, liegt bei pH=7 (Neutralisationspunkt) n0(H3O+) = nz(OH-)
pH-Wert über den ÄP wird mit folgender Gleichung für überschüssige OH- Ionen bestimmt:
c(OH-) = cü(Base) * Vü / V+ Vü
pOH= -lg(OH-) → pH= 14-pOH
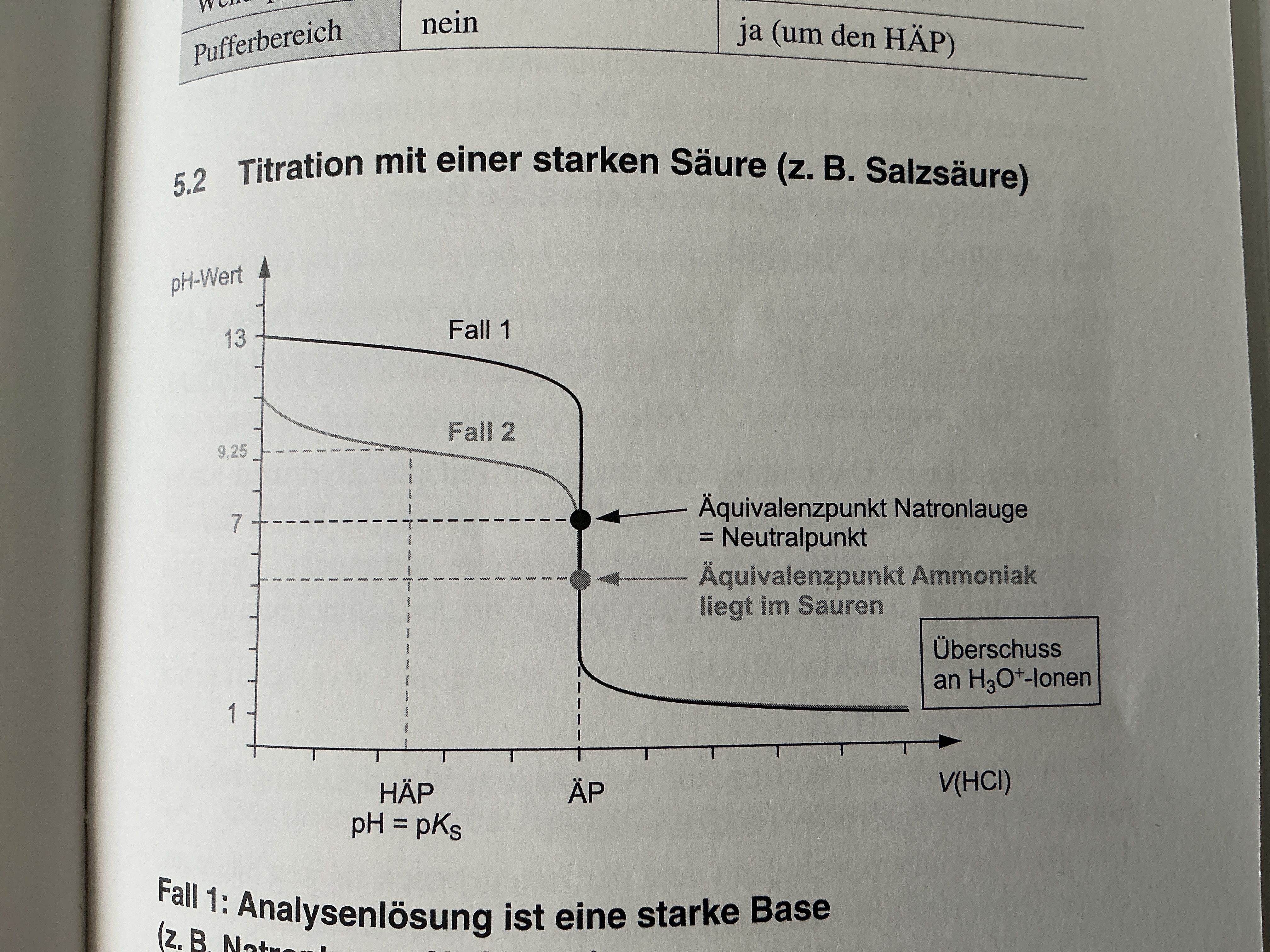
Titrationskurve mit starker Säure
Starke Base wird mit Starker Säure titriert
Alles analog zu Titration mit starker Base → Kurve gespiegelt
pH-Wert Bzw. pOH-Wert
ÄP stoffmenge gleich
Überschuss Oxonium Ionen über ÄP
c(H3O+) = cü(Säure) + Vü / V + Vü
pH wert aus c ausrechnen
Wie muss sich der Kw Wert verhalten, wenn eine Konzentration steigt
Wenn eine Konzentration steigt, muss die andere dementsprechend sinken, damit Kw im Gleichgewicht bleibt ( 10-14)
Wenn c(H3O+) = 10-3 , dann muss c(OH-) = 10-11 → 10-14
Zusammenhang pH und pOH Wert
pH + pOH = pKw = 14
Herleitung von Ks
Man betrachtet die Reaktion
HA + H2O ←→ A- + H3O+
Ks = c(A-) c( H3O+) / c(HA) * c(H2O)
Wasser weg, da konstante
Ks * c(H2O) = c(A-) * c(H3O+) / c(HA)
Je höher Ks, desto stärker ist die Säure
Herleitung von KB
Reaktion betrachtet:
H2O + B ←→ OH- + HB+
Ks= c(OH-)*c(HB+) / c(H2O) * c(B)
H2O weg, da konstante
Ks c(H2O) = c(OH-)*c(HB+) / c(B)
Zusammenhang Ks/KB mit Konzentrationen
Je größer c(H3O+) / c(OH-), desto größer Ks/KB
Wenn der Ks wert steigt, wie verhält sich dann der pKs wert ?
pKs-Wert sinkt
→ steigender Ks wert entspricht höhere Konzentration der H3O+-Ionen, daher sinkt der pH Wert und der pKs-Wert
Was passiert, wenn der pOH wert kleiner wird?
Konzentration der OH- -Ionen steigt
Welchen pKs wert haben ungefähr sehr starke Säuren ?
pKs < -1,34 → vollständige Protolyse
Keine GG-Reaktion, GG auf Produkt Seite
Schwache Säuren pKs Ks wert
pKs > 4 bzw Ks < 10-4
(Ungefähre Angabe)
Wenn der KB wert steigt, wie verhält sich pH und pOH wert ?
pH steigt
pOH sinkt
pKB sinkt , nichts anderes als pOH wert (muss man mit 14 abziehen für pH )
Ab welchen pKb wert spricht man ungefähr von einer schwachen Base
wem pKB > 3,67
Nachweis von Ammonium Ionen (NH4+)
→ schwache Säure
NH4+ + OH- ←→ NH3 (g) + H2O (l)
Gasförmige Ammoniak kann durch blaufärbung vom feuchten UI-Papier nachweisen
Reaktion mit H2O
NH3 (g) + H2O (l) ←→ NH4+ + OH-
Ammoniak bildet mit H2O alkalische Lösung, Identifikation auch mit Geruch von Ammoniak
Nachweis von NH4+ durch Kreuzprobe
NH4Cl wird mit NaOH im Mörser zerkleinert → feuchtes UI Papier am Uhrglas über den Behälter gestülpt → pH Wert steigt an da Papier blau färbt
Im Mörser: NH4+ + Cl- + Na+ + OH- ←→ NH3 + Na+ +Cl- + H2O
Uhrglas: NH3 + H2O ←→ NH4+ + OH-

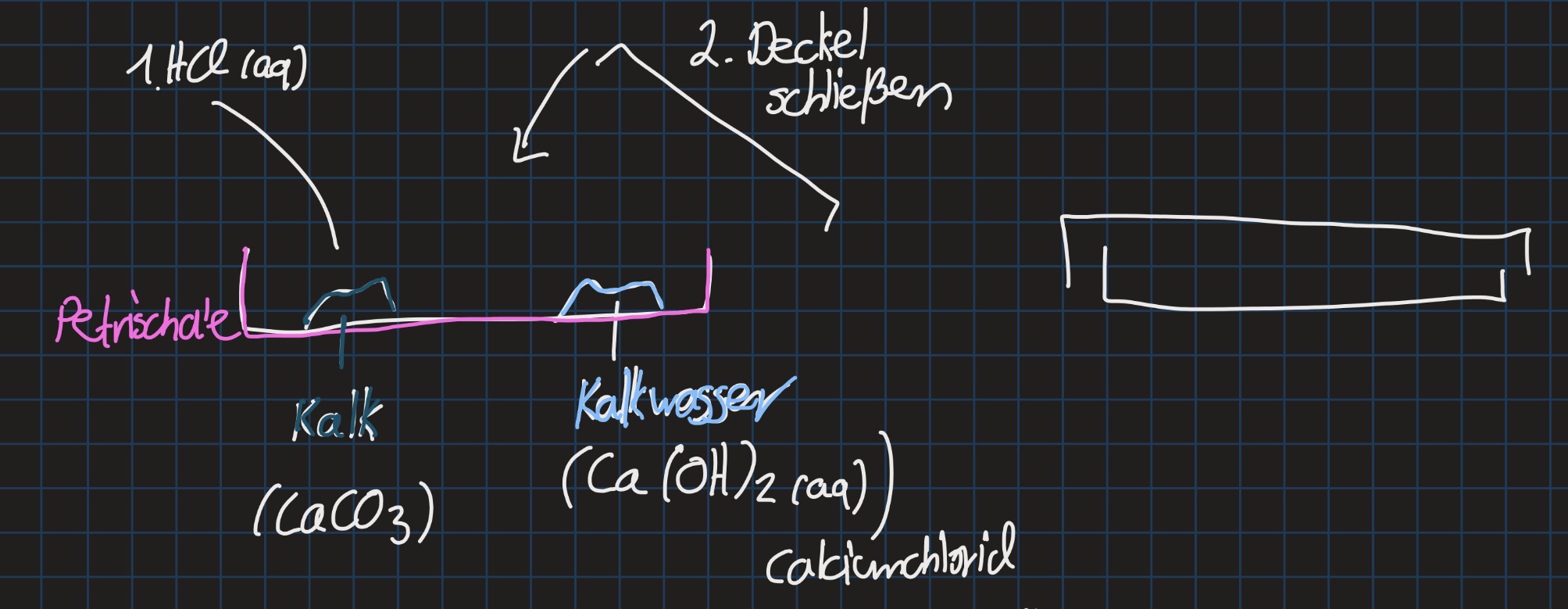
Nachweis von Carbonat.-Ionen in Kalk mit petrischale
Wenn man zu Carbonat saure Lösung hinzugibt, entsteht Kohlensäure → Zerfällt sofort in gasförmiges CO2 und H2O
CO32-+2 H3O+ ←→ CO2 (g) + 3 H2O (l)
CO2/Kohlensäure reagiert mit Kalkwasser zum Calicumcarbonat
Ca2+ + 2OH- + CO2 → CaCO3(s) + H2O (l)
Autoprotolyse des Wassers und ihr Zusammenhang mit dem pH-Wert des Wassers
Wasser reagiert mit sich selbst, folgendes GG:
2 H2O ←→ H3O+ + OH-
Daher Kw = c(H3O+) * c(OH-) = 10-14
Konzentration H3O+ und OH- sind im GG, daher
C(H3O+) = c(OH-) = 10-7 → pH= 7
Was sind Puffersysteme ?
Lösungen schwacher Säuren bzw Basen und ihrer korrespondierenden Basen bzw Säuren
Puffeerlösungen ändern ihren pH-Wert bei Zugabe von Oxonium/Hydroxid-Ionen nur wenig → Da bei schwachen Säure/Basen wegen mangelnder Protolyse GG besteht, kann System Zugabe von H3O+/OH- abfangen
Zugabe von H3O+ → GG links
HAc + H2O ← Ac- + H3O+
Zugabe von OH- - GG rechts
HAc + OH- → H2O + Ac-
Eigenschaften von Puffersystemen
Bei 10-fachen Überschuss an Base/Säure weicht pH-Wert Pufferlösung um +1 bzw -1 vom pKs-Wert ab
Pufferbereich +-1 pKs
Pufferlösung kann nicht beliebig viele H3O+ / OH- -Ionen neutralisieren (Pufferkapazität)
Pufferkapazität erschöpft, wenn Großteil Säure zur konjugierten Base/ Base zu konjugierenden Säure reagiert hat
Wie berechnet man pH Werte von Puffelösungen
Hendeson-Hasselbach-Gleichung
pKs/pKb Wert von Tabelle ablesen
Falls H3O+ oder OH- Ionen zusätzlich eingefügt werden →
c hinzufügen/abziehen
c(H2PO42-) = c(HPO42-) = 0,1 mol/l ; V= 1l
Es wird n= 0,01 mol HCl hinzugegeben
Berechne den pH-Wert
pH= pKs + lg ( c(HPO42-) / c(H2PO4-) )
Säure kommt hinzu ! Verschiebung GG
n(H3O+)= n (HCl) = 0,01 mol
Mehr H3O+, weniger HPO4- → mehr H2PO42-
pH= 7,21 + lg(0,1-0,01 / 0,1+0,01)
Untere → Säure konzentration erhöht sich durch H3O+
Obere → Base wird geringer durch mehr H3O+, um GG zu erhalten
Berechne das benötigte Volumen der Base am ÄP und bestimme, wieviel Volumen insgesamt vorhanden ist
Am ÄP: c(Säure)*V(Säure)=c(Base)*V(Base)
V(Base)= c(Säure)*V(Säure)/c(Base)
Am Ende → V=V0+V(Base)
Titration schwacher Säuren
Anfangs pH-Wert : ½ (pKs-lg(c0(Säure))
HÄP: pH=pKs ; c(OH-) = c(Säure) → Hendersson-Hasselbach-Gleichung / Pufferbrereich +-1pKs
Genau die Häflte der ursprünglich vorhandenen Essigsäure Moelkülen wurde verbraucht
ÄP: nz(OH-) = n0(HAc)
Formel für ausrechnung benötigtes Volumen der Base
V(Lauge) = c(Säure)*V(Säure) / c(Lauge)
V = V0 + VBase
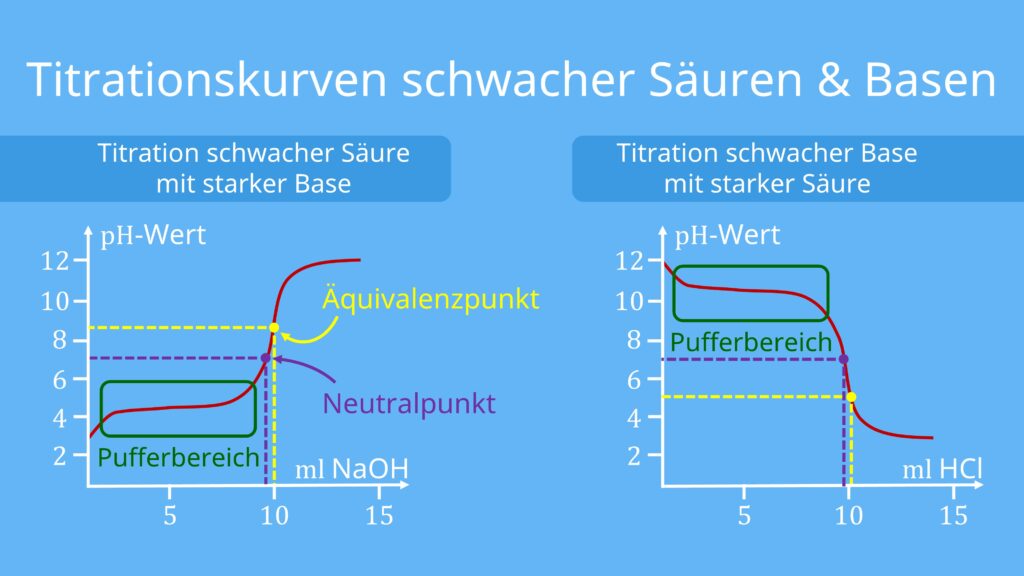
Titration schwacher Basen
pKB Wert 4,75, jedoch pKs = pH wert daher HÄP bei 9,25
HÄP: genau die Hälfte der ursprünglich vorhandenen Ammoniak Moleküle verbraucht
ÄP: nz(H3O+) = n0(NH3) → ph Wert kleiner als 7
PH wert nähert sich der zugegeben starken Säure an
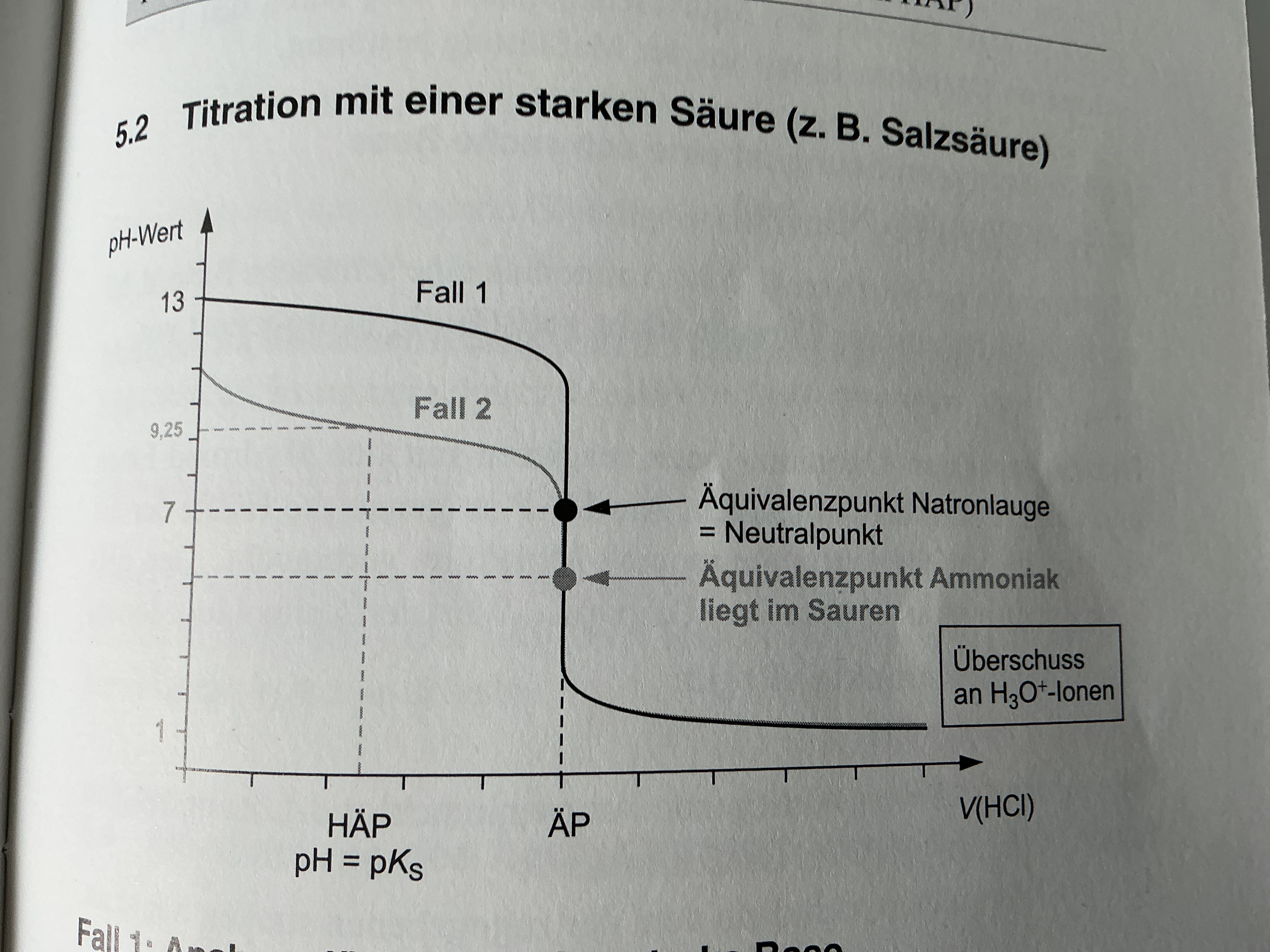
Säure-Base GG auf Indikatoren
Säure-Base-Indikator ist ein schwache, farbige organische Säure, deren korrespondierende Base eine andere Farbe aufweist
GG in wässriger Lösung
HINd+ H2O ←→ Ind- + H3O+
pH= pKs(Ind) + lg(c(Ind-) / c(HInd)
Umschlagbereich eines Indikators ?
pH = pKs(HInd) +-1
Wann ist ein Indikator für eine Titration geeignet?
Wenn innerhalb seines Umschlagbereichs der pH-Wert des ÄP liegt
Prinzip der DC
Ein Gemisch, das in einer mobilen Phase gelöst ist, wird an einer stationären Phase vorbeigeführt
DC-Platte → stationäre Phase, Proben werden auf eine Startlinie gebracht
DC-Platte in Gefäß, mit Fließmittel am Boden → Fließmittel wandert nach oben (mobile Phase) → nimmt Proben mit
Kurz bevor das Fließmittel den oberen Rand der DC-Platte erreicht Versuch beendet

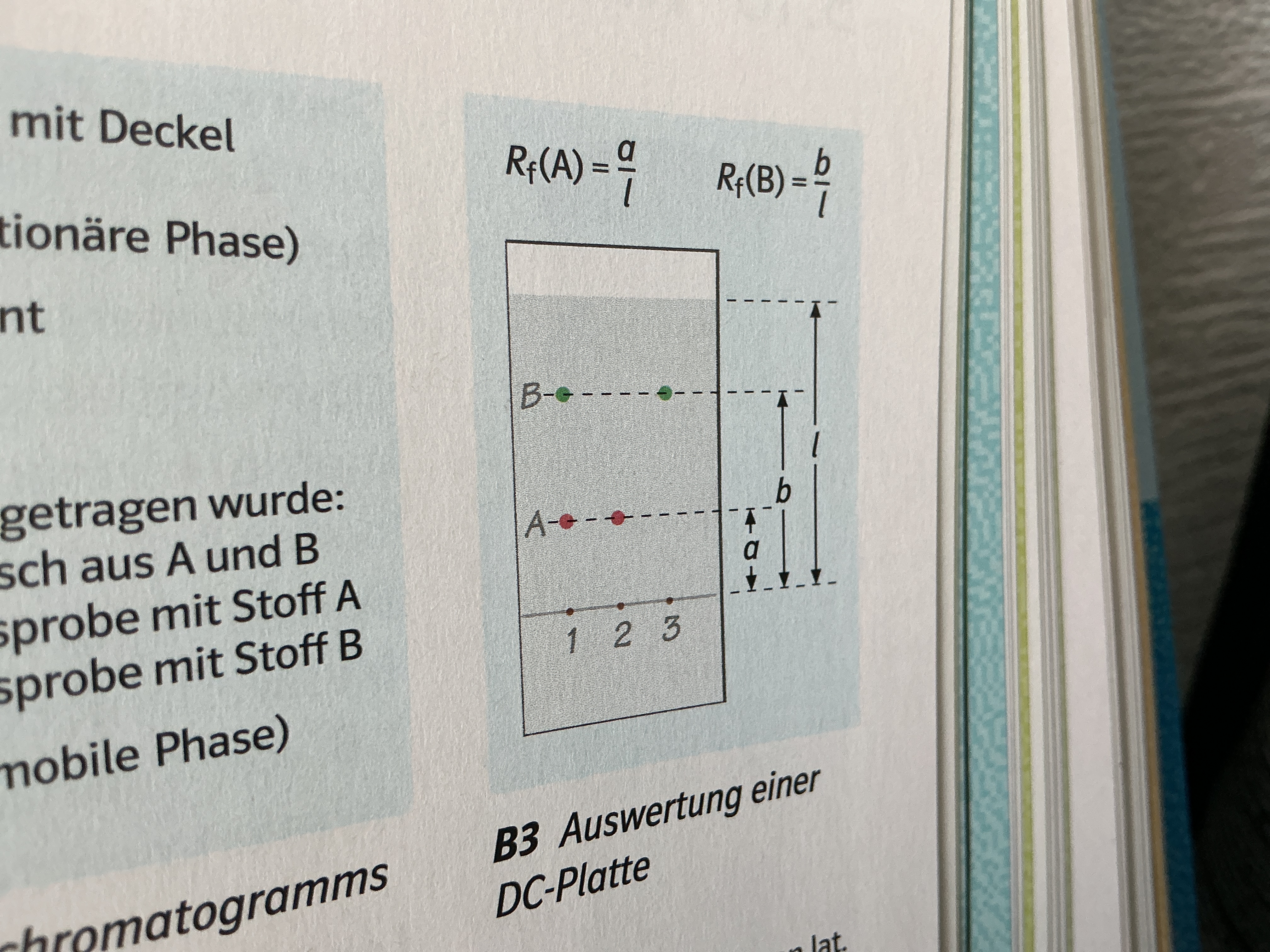
Auswertung von DC-Platten
Bestimmung der Rf-Werte
Rf= Strecke(Startlinie-Substanzfleck) /
Strecke (Startlinie-Fließmittlefront)
Für Farbstoffe wird alkalisches Fließmittel verwendet → Farbe sichtbar
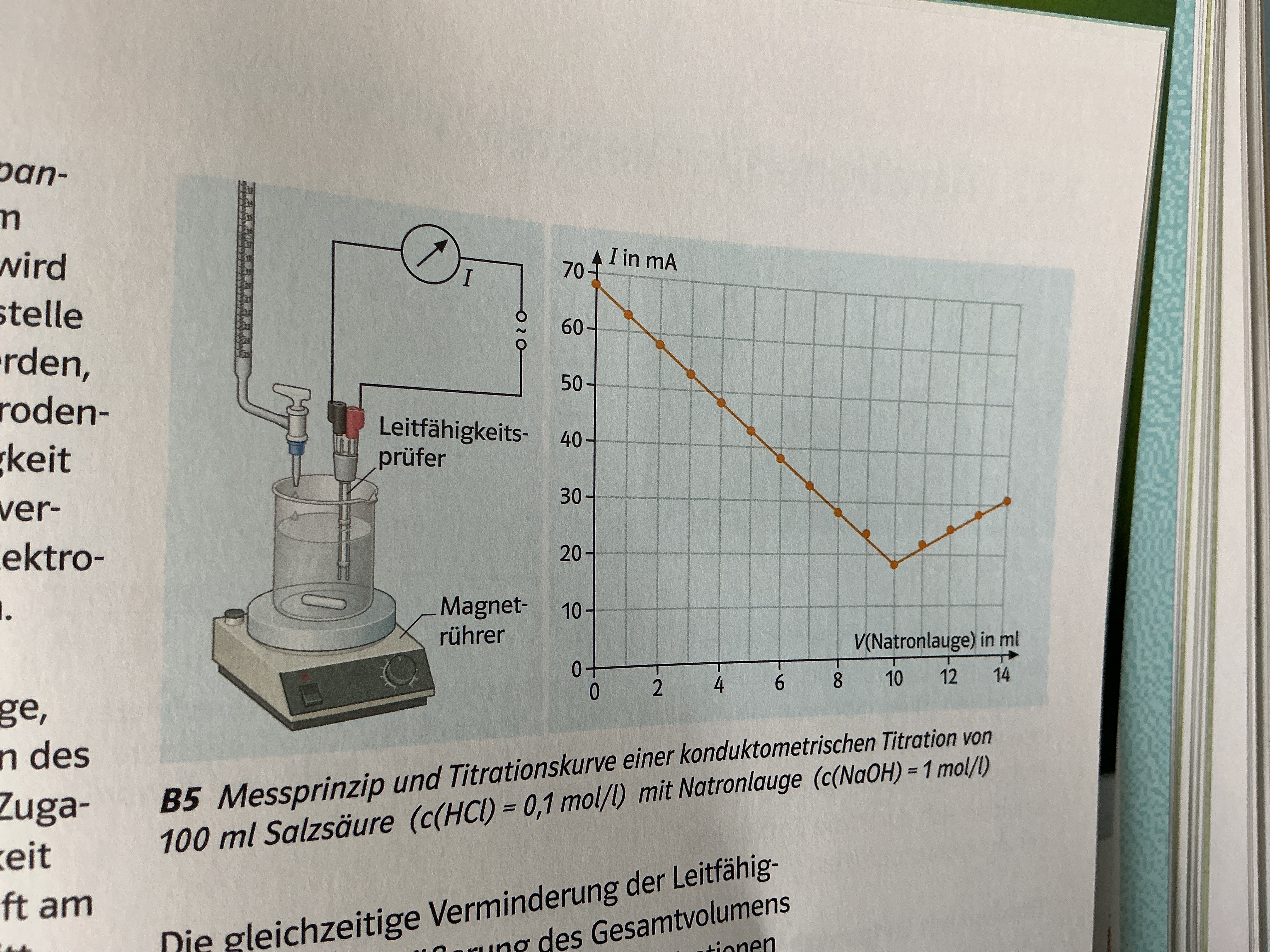
Konduktometrische Titration
Saure/alklaische Lösungen leiten ebenso wie Salzlösungen den elektrischen Strom
An einen leitfähigkeitsprüfer, der in die Lösung taucht, wird Wechselspannung angelegt → Wechselspannung zur Vermeidung Abscheidung von Elektrolysenprodukten
Salzsäure mit NaOH
→ Leitfähigkeit nimmt bis ÄP ab , da H3O+ mit OH- zu H2O (Ersatz von Na-Ionen)
→ Danach nimmt sie zu (Überschüssige OH- Ionen nehmen zu)
→ Schnittpunkt beider linearen Kurven = Verbrauch an Maßlösung bis zum ÄP