Chapitre 2 : Techniques de biologique moléculaire
1/114
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
115 Terms
Pourquoi utilise-t-on la biologie moléculaire en microbiologie ?
Pour détecter des micro-organismes dans un échantillon, surtout s’ils sont présents en faible quantité
Pour quantifier les virus (quantification spécifique aux virus)
Pour détecter des gènes de résistance aux antimicrobiens :
Présence de gènes de résistance
Mutations sur les gènes cibles de certains antibiotiques
Pour typage moléculaire lors d’épidémies :
Identifier si toutes les souches isolées chez plusieurs patients sont identiques
Suivre la chaîne de transmission
Déterminer le profil génétique d’une souche
Adapter le traitement selon le génotype du patient (mutations de résistance)
Connaître la prévalence d’une souche donnée dans une population
→ technique rapide, sensible et spécifique qui permet une adaptation précoce du traitement.
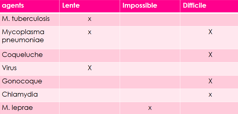
Dans quels cas la biologie moléculaire est-elle préférée à la culture classique ?
Lorsque l’échantillon contient peu de micro-organismes (faible charge)
Lorsque la culture est :
Difficile (ex : Bordetella pertussis, Chlamydia trachomatis)
Trop lente (ex : Mycobacterium tuberculosis, virus)
Impossible en routine (ex : Mycoplasma pneumoniae, M. leprae)
Lorsque le germe est fragile ou que le patient a déjà reçu des antibiotiques
Pourquoi la PCR est-elle utile dans le diagnostic d’une méningite ?
Car les méningites sont souvent bactériennes ou virales, et le temps est crucial
Le LCR prélevé par ponction lombaire contient peu de pathogènes → sensibilité PCR nécessaire
La culture virale est trop lente → la PCR permet une identification rapide
En fonction de l’aspect du LCR, des lympcytes et polynucléaires, le patient reçoit déja un premier traitement
La PCR permet aussi une quantification de la charge virale pour adapter le traitement
Un test multiplex (PCR multiple) peut être réalisé pour rechercher plusieurs pathogènes à la fois
Le traitement est alors ajusté :
Si la PCR détecte une bactérie → antibiotique adapté
Si la PCR détecte un virus → poursuite du traitement antiviral
Que détecte une PCR spécifique d’un germe ?
Elle ne détecte que ce que l’on cherche.
Exemple : si on fait une PCR pour détecter la coqueluche, elle ne montrera pas un autre germe.
Pourquoi la PCR peut-elle détecter un germe alors que la culture est négative ?
Si le patient est déjà sous traitement, les germes ne pousseront pas en culture.
Mais la PCR peut toujours détecter l’ADN du germe, même s’il est mort.
Pourquoi la PCR ne prouve-t-elle pas que le germe est vivant ?
Parce que la PCR détecte de l’ADN, qu’il soit vivant ou mort.
La PCR ne permet pas de conclure sur l’infectiosité.
C’est seulement si la dernière culture est négative que l’on peut confirmer l’efficacité du traitement.
➤ La PCR ne remplacera jamais la culture pour cette raison.
La PCR est-elle utilisée en routine pour la détection des microorganismes ?
Non, la PCR n’est pas systématiquement utilisée en routine pour les bactéries.
Elle est surtout utilisée pour les virus.
Pourquoi la PCR ne remplace-t-elle pas l’antibiogramme ?
Parce que la PCR ne donne pas la CMI (concentration minimale inhibitrice).
L’antibiogramme reste indispensable pour guider le traitement antibiotique.
Dans quels cas la culture est-elle difficile à mettre en œuvre ?
Coqueluche (Borderella pertussis)
Chlamydia trachomatis
Dans quels cas la culture est-elle lente ?
Mycobacterium tuberculosis
Virus (au moins 5 jours pour avoir un résultat)
Dans quels cas la culture est-elle impossible en routine ?
Mycoplasma pneumoniae
Mycobacterium leprae (se cultive uniquement sur animaux, pas en routine)
Pourquoi la quantification par PCR est-elle nécessaire pour les virus ?
Pour suivre l’évolution du traitement.
Pour évaluer la charge virale.
➤ Exemple de virus : CMV, EBV, HIV.
Dans quels cas la PCR est-elle utilisée ?
Méningites : pour détecter rapidement l’agent infectieux dans le LCR.
Quand la culture est difficile, lente ou impossible.
M. tuberculosis : culture possible mais très lente.
M. pneumoniae : culture difficile et lente.
Coqueluche : culture difficile, nécessite des conditions particulières.
Virus : culture très lente (min. 5 jours).
Gonocoque : pousse en 24h mais fragile ; nécessite des conditions de transport précises.
Chlamydia : culture lente (5 jours) et difficile car nécessite entretien cellulaire.
M. leprae : culture impossible en routine, réalisable uniquement sur animaux.
Pourquoi détecte-t-on la résistance avec la biologie moléculaire ?
Pour adapter le traitement au plus vite.
Lorsqu’un germe est déjà connu pour avoir une résistance potentielle, un test de résistance est essentiel.
La détection précoce permet de modifier rapidement le traitement, sans attendre la culture.
➤ Ex : en cas de Staphylococcus aureus résistant à la méthicilline (MRSA).
Quel est l’avantage de la PCR par rapport aux méthodes phénotypiques ?
La PCR est beaucoup plus rapide que les antibiogrammes classiques (tests phénotypiques).
Elle permet de détecter directement les gènes de résistance dans l’ADN du germe.
Pourquoi la PCR est-elle utile en cas d’épidémie ?
Parce que la transmission de la résistance se fait souvent par des plasmides (échange horizontal).
Ce transfert de gènes est rapide entre bactéries.
➤ Exemple : la PCR peut aider à repérer une épidémie liée à un gène de résistance, même si les bactéries sont d’espèces différentes.
Quel gène de résistance est typique du Staphylococcus aureus résistant à la méthicilline ?
Le gène mecA.
Ce gène code une protéine PBP2A, qui remplace les protéines PBP classiques
En condition normale, les bêta-lactamines se lient au PBP et empêche la synthsèe de petidoglycans.
Les bêta-lactamines (ex : pénicilline) ne peuvent plus se fixer, donc elles sont inefficaces. Les peptidoglycans sont malgré tout produits
Quelles sont les conséquences cliniques d’une infection par un S. aureus portant mecA ?
Infection plus grave et plus longue.
Les médecins doivent prescrire de la vancomycine par voie parentérale.
Les MRSA sont plus résistants que les souches classiques.
Comment détecte-t-on le gène mecA ?
Par PCR (plus rapide).
On peut aussi faire une culture avec milieu sélectif, mais cela prend plus de temps (pas de problèmes en clinique, car le médecin peut changer de traitement au bout de deux jours)
➤ En pratique, la PCR est préférée dans les situations urgentes (S. doré)
Quels sont les modes d’acquisition d’un staphylocoque doré résistant ?
Contamination extérieure (ex : hôpital).
Auto-contamination (ex : mauvaise désinfection d’une plaie avec sa propre flore cutanée).
3) Le typage moléculaire, pourquoi ?
En Afrique, la malaria est présente et pourrait être résistante aux traitements donnés.
Actuellement, tous les traitements sont des combinaisons de plusieurs antibiotiques pour éviter que les résistances ne se propagent trop vite.
Comment est organisée un laboratoire de biologie moléculaire ?
On travaille avec :
des filtres
des gants
des blouses
un tablier
des hottes
des PCR
À quoi servent les enceintes de laboratoire ?
Elles permettent d’isoler un espace de travail.
Un tube UV permet de stériliser la hotte.
Combien de hottes utilise-t-on et pour quoi faire ?
Une hotte permet la production du mix PCR.
Une autre hotte sera uniquement utilisée pour l’assemblage.
Les hottes PCR sont utiles pour créer un espace de travail.
Que se passe-t-il dans la salle de pré-PCR ?
On y traite les échantillons après réception au dispatching.
Tous les échantillons arrivent d’abord au dispatching qui les met soit au frigo, soit à -4°C.
Le dispatching attribue les échantillons aux différents laboratoires.
Le technicien prend ensuite les échantillons pour :
extraire l’ADN (ou éventuellement l’ARN)
assembler l’ADN avec le mix PCR (magnésium, dNTP…)
Peut-on associer deux postes de travail différents dans une même pièce ?
Il serait possible d’utiliser une hotte pour faire l’assemblage.
Cela permet de protéger l’environnement et d’éviter les contaminations.
Que se passe-t-il après la pré-PCR ?
On réalise la PCR proprement dite.
Cela se fait dans une pièce distincte remplie de thermocycleurs :
thermocycleurs classiques
thermocycleurs en temps réel
Que peut-on faire après la PCR ? (Post-PCR)
On peut faire deux choses :
La PCR nichée ou la PCR en temps réel
1) Que sont les PCR nichées ?
Ce sont des PCR utilisant deux paires de primers différents.
Les seconds primers sont toujours à l’intérieur.
C’est une technique :
non quantitative
plus complexe
qui prend plus de temps
On réalise deux PCR successives.
Il faut ouvrir les tubes entre les deux manipulations.
Le risque de contamination est donc important.
Quelles sont les précautions à prendre avec les PCR nichées ?
On ne doit pas ouvrir tous les tubes à la fois pour éviter les contaminations par aérosols.
On travaille derrière un plexiglas pour éviter de contaminer les échantillons.
En pratique :
on transfère l’ADN amplifié dans un nouveau mix
on referme le tube
puis on ouvre le suivant, etc.
Quelles sont les règles de circulation dans le laboratoire ?
On ne peut pas retourner en salle de pré-PCR après avoir manipulé en post-PCR.
On peut être contaminé sur les vêtements, cheveux…
Cela risquerait de contaminer les tampons et fausser tous les résultats de PCR.
Les PCR nichées sont donc réalisées en fin de journée.
En principe, on ne peut pas aller en post-PCR après avoir été en pré-PCR.
Comment révèle-t-on les amplicons ?
Via un gel d’agarose.
Il n’y a pas d’avantage à faire cette technique.
2) Qu’est-ce que la PCR en temps réel ?
On extrait l’ADN
On amplifie
On ajoute un marqueur de détection
On peut faire des courbes de quantification
Quels sont les avantages de la PCR en temps réel ?
Plus simple à mettre en œuvre
Plus souple
Permet de refaire facilement plusieurs fois un mix (jusqu’à 10 fois)
Pourquoi chaque prélèvement est-il adapté à l’application souhaitée ?
Parce que selon ce qu’on recherche (virus, bactéries, champignons, etc.), le type de prélèvement et sa préparation doivent être ajustés.
Quels sont les prélèvements dits "à frais" utilisés pour la PCR ?
Sang :
C’est le prélèvement le plus fréquent.
On analyse le sérum, le plasma ou le sang total.
On recherche souvent des virus (ex : CMV).
Urines :
Les bébés nés de mères infectées par le CMV ont de grandes quantités de virus dans les urines.
On peut aussi y détecter le polyomavirus.
Prélèvements respiratoires :
Une PCR est réalisée pour détecter des agents pathogènes.
Biopsies :
Dépendent de la taille du fragment.
Extraction d’un petit morceau.
Techniques utilisées doivent éliminer toutes traces de sang.
Que peut-on utiliser comme prélèvements dans des blocs de paraffine ?
Tissus :
Les PCR peuvent aussi se faire à partir de tissus inclus en blocs de paraffine.
Quels sont les autres types de prélèvements utilisés ?
Cultures bactériennes ou de levures :
Une PCR ciblée ou large est réalisée pour orienter vers bactéries ou champignons.
Échantillons environnementaux :
Sols
Eaux
Murs
Peut-on utiliser du papier buvard pour la PCR ?
Oui, ce n’est pas utilisé en routine mais utile dans certaines études de terrain.
Exemple : un étudiant a recueilli du sang dans des villages africains en déposant une goutte sur un papier buvard.
Dans quels cas faut-il travailler en hotte de type 3 pour la biologie moléculaire ?
En fonction des agents pathogènes comme tuberculose ou brucellose.
Nécessite un laboratoire avec :
2 sas d’entrée
Entrée limitée
Pression négative
Hottes à flux laminaire de type 3
Techniques d’extraction des acides nucléiques
Techniques d’extraction des acides nucléiques
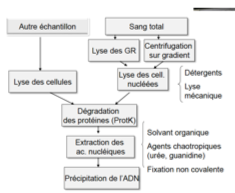
Quel est le principe général de l’extraction ?
On lyse les cellules.
On extrait les acides nucléiques.
Quelles méthodes peut-on utiliser pour purifier l’ADN ?
Manuellement : sur colonnes de silice.
Automatiquement : avec des automates (ou semi-automates).
La plupart des automates fonctionnent avec des billes de silice magnétiques.
Comment fonctionne l’extraction avec des billes de silice magnétiques ?
L’ADN se fixe sur les billes.
On place un aimant pour retenir les billes.
On élue l’ADN avec un tampon à haute force ionique.
On récupère une solution d’ADN pur, sans les billes.
Quels paramètres doivent être pris en compte dans l’extraction ?
La matrice : nature et volume de l’échantillon
L’agent ciblé : bactérie, virus, parasite ou champignon
Le type d’acide nucléique : ADN ou ARN
La concentration finale nécessaire pour la manipulation
Quels types d’échantillons nécessitent quelles techniques de lyse ?
Sang :
Lyse des hématies et leucocytes
Prélèvements respiratoires :
Présence de mucus
Utilisation de N-acétyl-cystéine pour casser les ponts disulfures
Tissus :
Lyse plus longue avec de la protéinase K overnight
Moustiques (ex : Anopheles) :
Téguments riches en chitine
Utilisation de KOH pendant quelques heures
Étape de bead-beating, puis purification sur colonnes (ex : Qiagen)
Champignons :
Paroi riche en sucre et chitine
Bead-beating nécessaire pour casser la paroi
Mycobactéries :
Lyse thermique : 100°C pendant 30 minutes
Comment conserver les échantillons en phase pré-analytique pour l’ADN ?
L’ADN peut être conservé à température ambiante pendant 24 h.
Si le prélèvement n’est pas traité immédiatement :
Conservation à 4 °C pendant quelques jours.
Conservation à -20 °C si stockage pour plusieurs mois.
À -80 °C : idéal pour une meilleure qualité d’analyse.
Pourquoi l’ARN est-il plus fragile que l’ADN ?
Parce qu’il est rapidement dégradé par les RNAses, qui sont omniprésentes (y compris sur la peau humaine).
Quelles sont les conditions de conservation spécifiques pour l’ARN et l’ADN viral ?
ADN viral sous forme de provirus :
Peut être conservé 24 h à 20 °C,
Ou quelques jours à 4 °C.
ARN :
Doit être congelé à -80 °C dans les 3 heures.
Quels cryoprotecteurs sont utilisés pour les acides nucléiques ?
Paxgène : conserve les ARNm.
Tubes de prélèvement spécifiques pour PCR (ex : Chlamydia, Gonorrhée).
L’extraction de l’ADN est-elle toujours purifiée ?
Non, la purification n’est pas obligatoire, mais recommandée.
La concentration de l’échantillon est parfois nécessaire avant extraction
Pourquoi la qualité de conservation de l’ADN dépend-elle de l’objectif ?
Pour des séquençages de longs fragments, l’ADN doit être bien conservé.
Pour des PCR de quelques centaines de paires de bases, un ADN légèrement abîmé peut suffire.
Que doit-on connaître avant d’extraire l’ADN ?
nature de l’ADN.
La source du spécimen (procaryote, eucaryote…).
Pourquoi congèle-t-on souvent les extraits d’ADN ?
Car toutes les étapes d’analyse ne sont pas faites à la suite.
La congélation permet de préserver les résultats pour les étapes ultérieures.
Quel est l’impact d’une mauvaise extraction sur la PCR ?
Une mauvaise extraction compromet la qualité des résultats PCR.
La maîtrise de la technique d’extraction est indispensable en biologie moléculaire.
1) Lyse cellulaire : Quelles sont les techniques utilisées ?
1) Lyse cellulaire : Quelles sont les techniques utilisées ?
Quelles sont les principales méthodes utilisées pour la lyse cellulaire avant extraction d’ADN ou d’ARN ?
Voie mécanique :
Colonnes pré-remplies de billes.
Très utile pour lyser les champignons (ex. Aspergillus, dermatophytes).
Voie physique :
Variation de température (ex. congélation à l’azote).
Très bon rendement, optimal pour cultures fongiques.
Choc hypotonique :
Utilisé pour lyser les hématies (globules rouges).
Quels agents chimiques sont utilisés pour dénaturer les protéines et faciliter la lyse ?
Détergents :
SDS, Tween, Sarcosyl.
Agents chaotropiques :
Thiocyanate de guanidine, iodure de potassium.
Enzymes protéolytiques :
Protéinase K, utilisée pour une pré-lyse à 56 °C pendant 1 heure.
2) Quelles sont les principales techniques d’extraction des acides nucléiques ?
2) Quelles sont les principales techniques d’extraction des acides nucléiques ?
En quoi consiste le relarguage ?
C’est une précipitation des protéines par haute concentration en sels.
Peu utilisée.
Comment fonctionne la chromatographie par échange d’anions ?
Les charges négatives de l’ADN se fixent sur des supports à charges positives.
L’élution se fait avec un tampon à haute force ionique.
Qu’est-ce que la fixation sur silice ?
L’ADN est fixé de façon sélective sur un gel de silice en présence d’agents chaotropiques.
L’élution se fait par un tampon à basse force ionique.
Qu’est-ce que l’extraction sur colonnes ?
L’ADN (chargé -) est fixé sur de la silice en présence d’un tampon à forte concentration en Na⁺.
Les ARN et protéines dénaturés et lysés sont éliminés dans une première fraction. (on fait agir une protéase pour éviter que les nucléases déteriorent l’ADN)
L’ADN est ensuite élué en diminuant la force ionique.
Quels sont les avantages de la fixation sur silice ?
Pas besoin de précipitation à l’alcool.
Automatisable via des billes de silice magnétiques sur automate.
Quels sont les inconvénients des billes de silice ?
Elles peuvent bloquer les automates.
Qu’est-ce que la méthode GeneXpert ?
Système automatisé de biologie moléculaire.
Permet la PCR, nested-PCR, RT-PCR en temps réel.
Flexible, rapide, résultats disponibles à la demande.
Comment fonctionne la cassette GeneXpert ?
Une chambre reçoit l’échantillon après pré-lyse.
Toutes les étapes (lyse, extraction, amplification) se font dans des chambres intégrées.
L’ADN ou ARN se concentre dans une zone en forme de losange où a lieu la PCR.
Les transferts de température sont très rapides grâce à la finesse des structures internes.
Dans quels contextes utilise-t-on la méthode GeneXpert ?
Infections sexuellement transmissibles (IST).
Méningites.
Autres diagnostics rapides nécessitant biologie moléculaire.
Qu’est-ce que l’automate Biofire ?
C’est une PCR miniaturisée.
On y insère une canette contenant les réactifs nécessaires.
Il contient des billes de silice qui réalisent du bead-beating pour briser les cellules.
Les alvéoles internes permettent de purifier les produits PCR.
Il permet de tester des fluides céphalorachidiens (LCR).
Il peut analyser une grande variété de pathogènes : bactéries, virus, levures.
Les résultats sont disponibles en environ 1 heure.
Que se passe-t-il lors de l’extraction de l’ADN ?
On extrait tout l’ADN, y compris l’ADN plasmidique et l’ADN génomique.
Il est utile de les séparer.
On effectue une lyse alcaline en présence de SDS (un détergent).
Ensuite, on réalise une neutralisation rapide.
L’ADN plasmidique reste soluble.
L’ADN génomique devient insoluble.
Il suffit de récupérer le surnageant pour isoler l’un ou l’autre.
Comment évalue-t-on la pureté d’un échantillon d’ADN ?
Grâce à la spectrophotométrie, on mesure l’absorbance :
À 260 nm pour les acides nucléiques.
À 280 nm pour les protéines.
Le rapport 260/280 permet d’estimer la pureté de l’ADN extrait.
Nested-PCR
Nested-PCR
Qu’est-ce que la nested-PCR (PCR nichée) ?
C’est une PCR en deux étapes successives avec deux paires d’amorces :
Amorces externes : utilisées d’abord, pendant environ 10 cycles.
Puis, ajout d’amorces internes, plus spécifiques, pour 25 cycles supplémentaires.
Cette méthode permet d’amplifier très spécifiquement un fragment cible, même au sein d’un ensemble de séquences homologues.
Elle est utile lorsque les amorces externes amplifient plusieurs séquences similaires.
Quel est le rôle essentiel des amorces en PCR ?
Elles déterminent quel fragment est amplifié.
Si les séquences sont trop homologues, la spécificité est réduite.
On utilise alors des amorces internes pour améliorer la spécificité.
Automate Maxwell 16
Automate Maxwell 16
Qu’est-ce que l’automate Maxwell 16 ?
Un automate de purification de l’ADN, ARN et protéines.
Il permet de traiter jusqu’à 16 à 48 échantillons en parallèle.
Il garantit une purification reproductible, sans contamination croisée.
Les acides nucléiques extraits sont propres, sans inhibiteurs, compatibles avec :
PCR en temps réel
Séquençage
Sondes moléculaires, etc.
Quels sont les points clés à retenir sur l’extraction d’acides nucléiques ?
L’extraction est une étape cruciale.
L’ARN est très fragile, nécessite des précautions strictes (gants, eau sans RNases…).
L’automatisation est de plus en plus privilégiée pour :
Gagner du temps
Standardiser les manipulations
Les techniques de laboratoire doivent garantir une matière génétique de qualité et en quantité suffisante.
Principales techniques de biomol appliqués en microbiologie
Principales techniques de biomol appliqués en microbiologie
L’amplification PCR classique
L’amplification PCR classique
Qu’est-ce que la PCR classique utilisée en microbiologie ?
C’est une réaction d’amplification d’un gène cible.
Après amplification, on fait une révélation sur gel d’agarose.
Pas de quantification possible : la PCR classique permet uniquement de déterminer la présence ou l’absence du gène, pas sa quantité.
Quels sont les types de contrôles indispensables lors d’une PCR ?
Les contrôles sont essentiels pour valider la PCR. Ils sont de deux types internes et témoins
Quels sont les contrôles internes à réaliser systématiquement ?
Contrôle | Oui/non | Nature | But |
|---|---|---|---|
Contrôle d’extraction | Toujours | Une autre cible ajoutée au prélèvement avant extraction (ex. : gène de la bêta-globine si ADN humain présent) | Vérifie que l’extraction est optimale → Le seuil de cycle (Ct) doit être < 3,5 |
Contrôle d’amplification | Pas nécessaire si le témoin d’extraction à la 1re étape permet de voir si ça a fonctionné | Ajouté dans le mix PCR (avec amorces/sondes associés) | Contrôle l’absence d’inhibiteurs de l’amplification |
Quels sont les témoins à inclure dans chaque série de PCR ?
Témoin | Oui/non | Nature | But |
|---|---|---|---|
Témoin positif | Toujours | Qualitatif ou quantitatif (qPCR) | Doit être positif. S’il ne l’est pas → recommencer la PCR, le témoin a échoué ou la PCR aussi |
Témoin négatif | Toujours | Eau | Doit être négatif (pas d’amplification). Si positif → contamination → test invalide et à refaire |
Pourquoi les contrôles sont-ils essentiels dans une PCR ?
Si l’ADN viral n’est pas détecté, il faut vérifier si c’est un échec de l’extraction.
On peut utiliser un gène ubiquitaire (exprimé dans toutes les cellules) comme contrôle d’extraction pour confirmer que l’ADN est bien présent.
Ces contrôles permettent de valider l’ensemble du processus : extraction, amplification, absence de contamination ou d’inhibition.
Quelles sont les applications actuelles de la PCR classique en microbiologie ?
Elles sont moins utilisées aujourd’hui car remplacées par des techniques plus rapides et quantitatives (qPCR).
Néanmoins, elles restent utiles pour certaines infections spécifiques comme la détection des échinocoques.
À quoi sert la PCR ITS ?
ITS = Internal Transcribed Spacer
C’est une PCR de contrôle avant la vraie PCR, principalement utilisée pour l’identification des champignons.
Elle permet, via un séquençage, de déterminer à quel champignon on a affaire.
Si la PCR ITS est positive, cela signifie que l’amplification a fonctionné → on peut envoyer l’échantillon en PCR spécifique.
PCR nichée ou nested-PCR
PCR nichée ou nested-PCR
Qu’est-ce que la PCR nichée (nested ou semi-nested) ?
C’est une méthode reposant sur deux amplifications successives.
1ère amplification : on utilise des amorces forward et reverse universelles.
2e amplification :
Nested : on utilise deux nouvelles amorces internes.
Semi-nested : on utilise le même primer forward et une nouvelle amorce reverse.
Les fragments obtenus sont visualisés sur gel d’agarose.
Cela permet de différencier plusieurs espèces de Plasmodium (diagnostic de paludisme).
PCR classique couplé à une hybridation
PCR classique couplé à une hybridation
Qu’est-ce que la PCR classique couplée à une hybridation ?
C’est une PCR classique avec amorces biotinylées.
L’hybridation se fait ensuite sur bandelette de nitrocellulose contenant des séquences complémentaires.
Une réaction enzymatique colore les bandes selon la présence ou l’absence du produit amplifié.
Applications :
Identification des mycobactéries (ex. : Mycobacterium tuberculosis).
Détection de mutations dans des régions connues de résistance, comme la résistance à la rifampicine.
PCR en temps réel
PCR en temps réel
À quoi sert la PCR en temps réel (qPCR) ?
Elle permet une détection qualitative (présence ou absence d’un pathogène).
Elle permet aussi une quantification précise → mesure de charge virale.
Quel est le principe chimique utilisé dans la qPCR (temps réel) ?
Elle repose sur la chimie TaqMan :
Une sonde est composée d’un fluorophore (extrémité 5’) et d’un quencher (extrémité 3’).
Tant que les deux sont proches, le quencher inhibe la fluorescence.
Lors de l’élongation, l’activité exonucléase 5’–3’ de la Taq polymérase dégrade la sonde.
Le fluorophore est libéré, ce qui permet son émission lumineuse.
Plus il y a de fluorescence détectée, plus il y a d’ADN ciblé → la fluorescence est proportionnelle à la quantité d’ADN.
Comment interprète-t-on les résultats en qPCR ?
La mesure se fait pendant la phase exponentielle de la courbe d’amplification.
Le Ct (Cycle threshold) est le nombre de cycles nécessaires pour que la fluorescence dépasse un seuil.
Plus le Ct est bas, plus la charge virale est élevée.
Le Ct est inversement proportionnel à la quantité d’ADN d’intérêt.
Pourquoi mesure-t-on la charge virale ?
Pour le suivi de l’efficacité du traitement.
Pour détecter une mauvaise observance thérapeutique ou une résistance émergente.
Pour le HIV, cela permet de :
Identifier les zones à haut risque de transmission.
Cibler les actions de santé publique.
Améliorer la qualité des soins et le soutien aux patients.
Séquençage moléculaire
Séquençage moléculaire
Quelles sont les applications principales du séquençage moléculaire en microbiologie ?
Identification d’un micro-organisme inconnu :
Le séquençage est toujours précédé d’une PCR classique, notamment PCR 16S pour les bactéries.
Utilisé si la culture est négative ou l’espèce inconnue.
Le prélèvement doit être monogerme (non contaminé par d’autres bactéries/flore).
Pour les champignons, on cible les régions ITS (Internal Transcribed Spacer).
Recherche de gènes ou de mutations impliquées dans une résistance aux antibiotiques ou antifongiques :
Ex. : mise en évidence d’enzymes produites par des entérobactéries responsables de résistances.
Whole Genome Sequencing
Whole Genome Sequencing
Qu’est-ce que le Whole Genome Sequencing (WGS) ?
Séquençage complet du génome d’un micro-organisme.
Pas utilisé en routine pour le diagnostic, mais utilisé dans les centres de référence.
Il remplace plusieurs PCR → une seule extraction d’ADN est suffisante.
Coût réduit, grande sensibilité, typage très précis, lecture rapide.
Quels sont les inconvénients du séquençage complet du génome ?
Certaines zones peuvent ne pas être couvertes si la couverture n’est pas suffisante → il peut y avoir des gaps.
Il est nécessaire de faire un traitement bio-informatique pour interpréter les données.