PSP T7: Cromatografía
1/47
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
48 Terms
Define cromatografía:
Técnica de fraccionamiento de los solutos debido a la distribucional diferencial de los solutos entre una fase móvil y una estacionaria.
Especialización de la separación por adsorción en columna
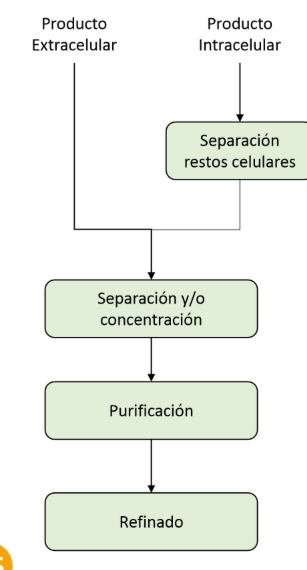
¿En qué momento se encuentra?
Purificación
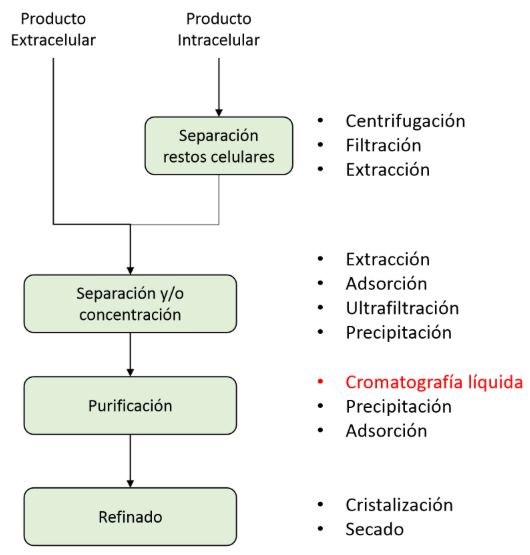
¿Qué dos tipos de utilización tiene la cromatografía?
Cromatografía analítica → finalidad: separación, identificación y cuantificación de las impurezas y el producto (caracterizar productos de las muestras). Aplicaciones:
Análisis biomédicos y medioambientales
Diagnosis
Monitoraje de procesos
Cromatografía preparativa → finalidad: separación de impurezas y recuperación de producto. Aplicaciones:
Purificación de productos biofarmacéuticos (ej: proteínas, lípidos, hormonas, …)
Purificación de productos nutracéuticos y de la industria alimentaria
Compara las características de adsorción con las de una cromatografía:
Adsorción:
Alta capacidad
Selectivo
Etapas iniciales → pre-cleaning: separar productos con diferentes propiedades físio-químicas
Cromatografía:
Baja capacidad
Muy selectivo
Etapas finales del proceso
Equipos más sofisticados
Caro → 70-80% del coste del downstream
¿Qué etapas tiene una cromatografía?
Empacar la columna
Inyección de la muestra
Separación de los solutos dependiendo de su afinidad con la fase estacionaria
Lavado de la columna (Regeneración)
Higienización
Desempacar / Almacenaje
Si un producto tiene — afinidad por la FE, tardará más tiempo en salir de la columna
más
¿Por qué es tan cara la cromatografía?
No solo está la columna, sino que tiene muchos equipos adicionales:
Bomba
Detectores:
Absobancia
UV
Fluorescencia
Conductividad
pH → importante en cromatografía iónica
Diferencial de presión → importante para evitar la colmatación de la columna (obstrucción de la columna)
¿Qué tipos de separación hay en una cromatografía?
Intercambio iónica
Fase reversa / interacciones hidrofóbicas
Exclusión por tamaño
Afinidad
iguales que en adsorción menos la de exclusión por tamaño
¿Qué técnicas hay para separar en una cromatografía? Ordénalas en función de su prevalencia en el sistema de bioseparación
Intercambio iónico
Afinidad
Interacciones hidrofóbicas
Fase reversa
Gel filtración
¿En qué se basa y cuáles so las características de la siguiente técnica?
Intercambio iónico
Separación basada en carga: intercambio catiónico o aniónico
Características:
Alta capacidad
Bajo coste
Fácil manipulación de la carga neta de las proteínas
¿En qué se basa y cuáles so las características de la siguiente técnica?
Afinidad
Separación basada en la interacción específica con un ligando
Características: alta selectividad
¿En qué se basa y cuáles so las características de la siguiente técnica?
Interacciones hidrofóbicas
Separación basada en interacciones hidrofóbicas
Características: fácil manipulación de las interacciones hidrofóbicas con sal
¿En qué se basa y cuáles so las características de la siguiente técnica?
Fase reversa
Separación basada en interacciones hidrofóbicas
Desventaja: uso de solventes orgánicos → desnaturalización de proteínas
¿En qué se basa y cuáles so las características de la siguiente técnica?
Gel filtración
Separación basada en el tamaño de partícula
Desventaja: poca resolución
¿En qué se basa una separación por exclusión por tamaño?
Permite separar partículas de distintos tamaños según su capacidad de entrar en los poros de la resina
Baja resolución
Se necesitan columnas muy largas para separar partículas con tamaños similares
Se puede utilizar a escala lab para cambiar de matriz, pero para eso ya puedes diafiltrar que funciona mejor y es más barato
¿Cuáles son las etapas en una cromatografía de intercambio iónico?
Equilibración: tampón de carga
Carga: se une el producto y algunas impurezas, otras salen
Lavado: se desunen impurezas de unión débil con tampón de carga
Elución: se desune el producto con concentración de NaCl alta
Regeneración: se desunen impurezas residuales con concentración de NaCl muy alta → 2M
Higienización: se eliminan microorganismos con NaOH 0,5M para degradar materia orgánica
Almacenamiento: 20% de EtOH para evitar crecimiento de microorganismos

Resuelve este ejercicio para una cromatografía de intercambio iónico:
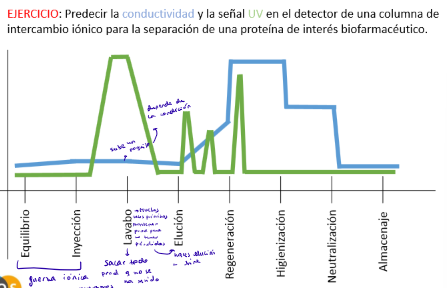
¿Cuáles son las etapas en una cromatografía de interacción hidrofóbica?
Equilibración: buffer con concentración de sal muy alta: la sal expone las regiones hidrofóbicas de las proteínas
Carga: tampón con la muestra y con concentración de sal muy alta
Lavado: mismo tampón de carga
Elución: reducción progresiva de concentración de NaCl, las proteínas salen en orden de hidrofobicidad
Regeneración: tampón sin sal (elimina las proteínas residuales)
Higienización: se eliminan microorganismos con NaOH 0,5M para degradar materia orgánica
Almacenamiento: 20% de EtOH para evitar crecimiento de microorganismos
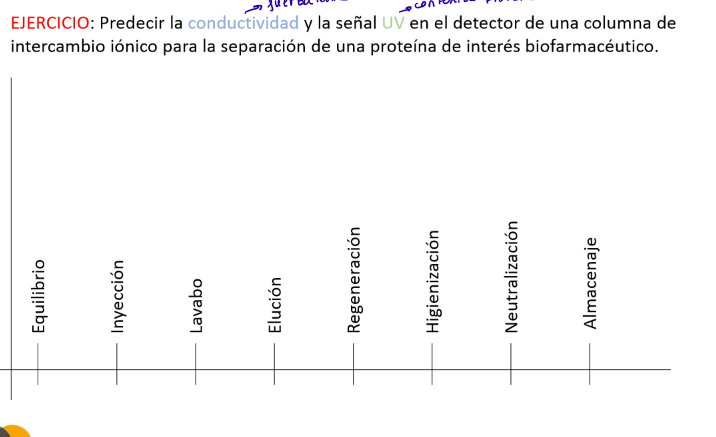
Resuelve este ejercicio para cromatografía de interacciones hidrofóbicas:

¿Qué modos de operación hay en una cromatografía líquido-líquido?
Unión y elución → las más utilizadas
La proteína de interés y algunas impurezas se unen a la columna
La separación se realiza por la acción de un tampón de elución
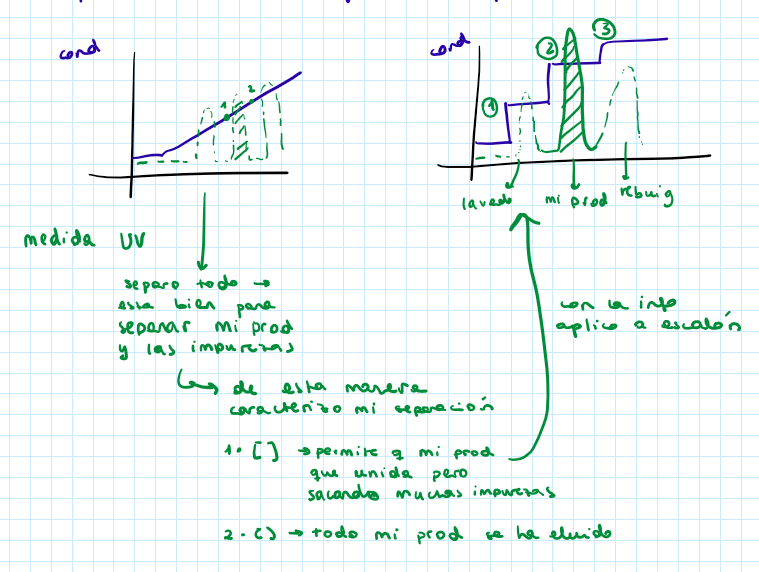
Elución por pasos o etapas → escalón
Elución por gradiente lineal → sirve para caracterizar el sistema, se dan a conocer las concentraciones de sal para usar en escalón
Más resolución y selectividad
Cromatografía isocrática → las que trataremos en este tema
Las impurezas y el producto son retenidas por la resina diferencialmente según su coeficiente de distribución
La fase móvil no cambia
¿Qué es el factor de capacidad? (k’)
Es la medida para cuantificar la interacción de un soluto con la fase estacionaria
¿Qué prefieres que tenga más afinidad por la columna, el producto o las impurezas?
Del que tengas menos
En isocráticas es común la retención de impurezas con k’ elevados comparados con k’ bajos de los productos de interés
¿Qué ocurre si el factor de capacidad (k’) del producto de interés es superior a 10?
No se puede hacer una elución isocrática, sino que se tiene que eluir modo unión-elución (variando la FM)
¿Qué es tm?
Es el tiempo de retención de la fase móvil
¿Qué es tr’?
Es el tiempo de retención ajustado: es el tiempo de retención del producto menos el tiempo de retención de la fase móvil
¿Qué es ε?
ε = la fracción de volumen muerto de la columna → fracción que ocupa la fase móvil
para saber que fracción ocupa la FE = 1 - ε
¿Cómo queremos que sean los picos en un cromatograma?
Picos altos y estrechos
¿Por qué motivos los picos se ensanchan?
Interacciones con la fase estacionaria → si hay interacciones, más lento saldrá el producto por lo que el pico será más amplio
Inyección no ideal → quiero alimentar el producto de manera de que haya la mayor concentración posible
Dispersión radial → la carga debe de ser uniforme en toda la superficie de la columna
Dispersión axial → si hay caminos preferentes, habrán zonas más rápidas y zonas más lentas, por lo que será más amplio el pico (el producto saldrá a tiempos diferentes)
Dispersión difusional ??
¿Qué es la selectividad?
Es la capacidad de diferenciar un compuesto de otro
Debe de ser entre 1,1 < α < 1,5
Es independiente de la concentración
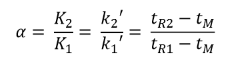
¿Qué es la resolución?
Es lo bien que se separan dos picos
R > 1,5
Es dependiente de la concentración (amplitud)
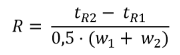
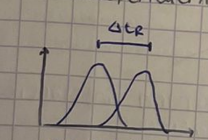
Di si tiene buena selectividad y resolución:
Tiene buena selectividad pero mala resolución
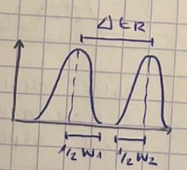
Di si tiene buena selectividad y resolución:
Tiene buena selectividad y buena resolución
Si ½ w1 + ½ w2 > tr2- tr1 → buena separación
¿Qué son HETP? ¿Qué es N?
HETP: altura equivalente de los platos teóricos
N: número de platos teóricos → número de etapas equivalentes en la columna
A — número de platos teóricos, mejor separación
A — HETP, mejor separación
mayor
menor

A — velocidad de la FM (u), se disminuye el efecto de la dispersión axial
mayor
Sin embargo, incrementa la limitación por dispersión difusional
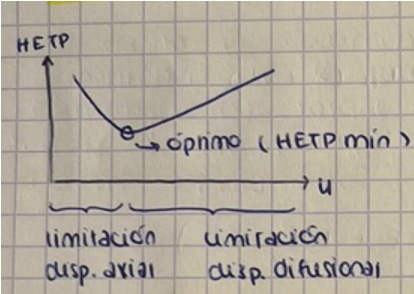
¿Por qué el empacado de la columna es crítico?
El empacado de la columna tiene que ser homogéneo y de alta calidad, ya que si hay irregularidades estas pueden causar caminos preferenciales en el lecho de la columna que impactarán en el rendimiento y la pureza de la separación
¿Qué maneras hay de empacar la columna?
Empacar por gravedad:
La columna sed rellena con la resina y se deja depositar por gravedad para crear el lecho
Se suele hacer en escala lab
Desventajas
Las partículas grandes se depositan más rápido
El lecho sufre compresión al aplicar el flujo de trabajo
Lento
Se pueden crear gradientes, ya que como las partículas caen por sedimentación, las partículas grandes quedan abajo y las pequeñas arriba
Empacar la columna con flujo:
La resina es introducida en la columna juntamente con la fase móvil mediante una bomba a un flujo constante para promover una rápida deposición de las partículas de la resina → FE y FM se ponen a la vez para que la FE deposite rápidamente
¿Cómo se mide la calidad del empacado?
Inyectar un pulso de un trazador que no interactúe con la FE (ej: NaCl)
La concentración del trazador tiene que ser mesurable
El trazador tiene que poder pasar a través de los poros del lecho de la columna
Desplazar el pulso a través de la columna con una FM apropiada en las condiciones de trabajo
Analizar la salida del trazador
Asimetría del pico
HETP
¿Cómo se clacula la asimetría y cuál es su valor esperado?
As = B/A
A = amplitud de la primera mitad del pico a 10% de la altura total
B = amplitud de la segunda mitad del pico a 10% de la altura total
Valor ideal → 1
Rango esperado → 0,8-1,5
Idealmente, los picos de un cromatograma siguen una distribución —
Normal o gaussiana
La amplitud del pico es — veces la desviación estándar si se sigue una distribución gaussiana
4
dispersión estándar = w / 4
Nos movemos desde -2 SD hasta +2 SD
¿Qué es un proceso de normalización?
Convertir todos los picos en curvas normales con media = 0 y dispersión estándar = 1
¿Qué describe la función de densidad?
Describe la concentración a la salida de la columna dependiendo del tiempo de retención y la desviación estándard
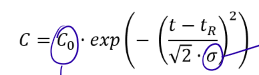
¿Qué es la función de distribución (FDist)?
Sale de integrar la función de la densidad entre los dos tiempos entre los cuales sale el producto
Indica la fracción de área entre dos tiempos y permite calcular la pureza y el rendimiento
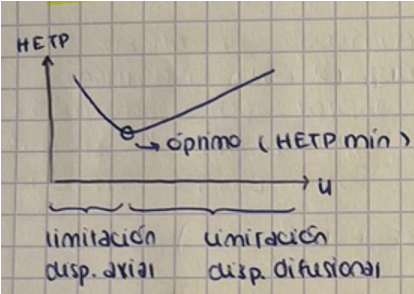
No se puede trabajar a flujos muy alto (u) debido a la limitación por dispersión difusional. ¿Qué tipo de cromatografía se puede hacer para que no afecte la dispersión difusional?
Utilizar una cromatografía de membranas → se utilizan membranas con microporos que tienen un ligando, haciendo que el producto se una en el proceso de filtración
¿Qué características tiene la cromatografía de membranas?
Volumen y tiempos de residencia menores
Transporte del soluto a los sitios de unión por convección (en columna es por difusión)
Caudales mayores (tiempos de residencia menores)
Resolución equivalente a las columnas de cromatografía
Utilizado comúnmente en modo isocrático donde se unen las impurezas
Capacidades de unión menores que en cromatografías convencionales
¿Qué características tiene el escalado?
Se escala el volumen/masa FE, manteniendo constante la resolución y los tiempos de residencia:
mantener cte la altura/longitud de la columna (h) y la velocidad superficial entre escalas (u): h1=h2 y u1=u2 → Q1/A1 = Q2/A2
mantener cte la relación entre gramos de proteínas adicionads y volumen de la columna entre escalas
Columnas más largas: mayor rendimiento
Columnas más anchas: mayor pureza
¿Qué procedimiento se sigue para el escalado de la columna?
Estudios de la capacidad de unión en dinámico a escala laboratorio para obtener los parámetros óptimos (máx capacidad de unión, tipo de resina, caudal, pH, …) utilizando la misma solución que se quiere purificar a escala piloto-industrial
Diseño a escala piloto-industrial utilizando el mismo adsorbente/resina