Antimicrobiële middelen I & II (HC7)
1/22
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
23 Terms
Aan welke criteria moet een medicijn voldoen?
Alleen toxisch voor pathogeen
Geen bijwerkingen (geen effect op humane cel)
Selectieve toxiciteit medicijn: hoog
‘Magic bullet theory’
= Het draait allemaal om het vinden van verschillen. Een goed medicijn valt iets aan dat de bacterie wél heeft, maar de mens niet.
→ Ehrlich stelde voor dat je een chemische verbinding zou kunnen maken die zich als een "magische kogel" door het lichaam beweegt.
De kogel vliegt langs alle gezonde menselijke cellen zonder ze te raken.
De kogel raakt alleen de specifieke ziekteverwekker waarvoor hij gemaakt is.
Resistentie
= het vermogen van een micro-organisme (bacterie, parasiet, virus) om te overleven of te groeien, ondanks de aanwezigheid van een middel dat hem normaal gesproken zou doden.
Ontstaat op 2 manieren:
Mutatie: Een foutje in het DNA van de bacterie zorgt ervoor dat het antibioticum niet meer past op zijn doelwit.
Horizontale genoverdracht: Bacteriën kunnen "recepten" voor resistentie aan elkaar doorgeven via kleine stukjes DNA (plasmiden). Het is alsof ze elkaar een cheat-code sturen via WhatsApp.
Hoe vecht de bacterie tegen medicijnen (resistentie)?
De uitsmijter (Efflux-pomp): De bacterie pompt het medicijn net zo hard weer naar buiten als het naar binnen komt.
Het schild (Enzymatische afbraak): De bacterie maakt een enzym (zoals bèta-lactamase) dat het antibioticum letterlijk in stukken knipt voordat het schade kan aanrichten.
De vermomming (Target modificatie): De plek waar het medicijn normaal gesproken aanhecht, wordt veranderd van vorm. De "sleutel" past niet meer in het "slot".
Klinische resistentie
= wanneer de bacterie niet meer geremd wordt door een concentratie van het medicijn die veilig en haalbaar is in het lichaam van de patiënt.
Verworven resistentie
= een nieuwe eigenschap die een bacterie krijgt die voorheen wél gevoelig was voor een antibioticum.
Je kunt het zien als een bacterie die plotseling een "hack" of een "upgrade" krijgt waardoor het medicijn niet meer werkt. Dit gebeurt vaak door spontane mutaties in het DNA.
Penicilline
semi-synthetisch (dit betekent dat het door mens iets is aangepast om bijwerkingen te verminderen)
-> eerste ‘natuurlijke’ antibioticum (eerste ‘magic bullet’)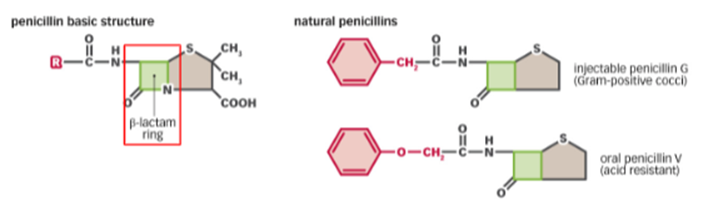
Smal-spectrum vs. breed-spectrum - Penicilline
Smal-spectrum
= Dit is een specialist. Het werkt fantastisch tegen Gram-positieve bacteriën omdat zij die dikke, blootliggende laag peptidoglycaan hebben. Het heeft echter moeite met Gram-negatieve bacteriën, omdat hun extra buitenmembraan (die "plastic zak" waar we het eerder over hadden) de penicilline simpelweg tegenhoudt. (bijv. Penicilline G)Breed-spectrum
= Dit zijn chemisch aangepaste varianten. Ze zijn zo ontworpen dat ze wél door de buitenmembraan van Gram-negatieve bacteriën kunnen glippen. Hierdoor kunnen ze een veel grotere groep verschillende bacteriën aanpakken. (bijv. Amoxicilline)
Werkingsmechanisme - antibioticum

Route van toediening - Penicilline
Niet elke penicilline kan als pilletje worden ingenomen:
→ De vroege penicillines (zoals Penicilline G) vallen uit elkaar door maagzuur, moeten hierdoor via injectie gegeven worden
→ Varianten zoals Penicilline V of Amoxicilline zijn chemisch aangepast zodat het het zuur kan overleven
Half-waarde tijd - Penicilline
"Antibiotica met een lange halfwaardetijd zijn beter voor de therapietrouwheid (1x per dag). Penicilline heeft echter meestal een korte halfwaardetijd, wat de therapietrouwheid lastiger maakt omdat je het vaker per dag moet innemen."
Distributie - Penicilline
→ penicillines verspreiden zich over het algemeen goed in de meeste lichaamsvochten en weefsels, maar komen slecht in CZN of in botweefsel
Chromosomen - resistentie
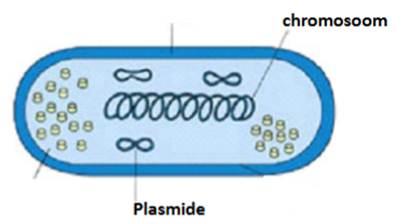
= meestal het gevolg van een toevallige mutatie. Dit beïnvloedt vaak maar één specifieke "aanvalsroute" van een antibioticum.
→ Verspreiding: verticaal
—> overdracht DNA naar volgende generatie
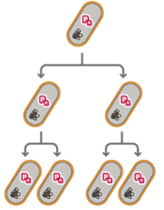
Plasmiden - resistentie
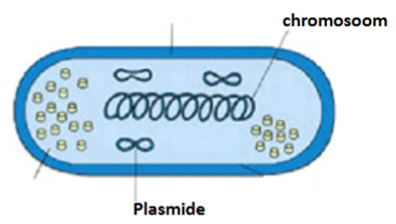
→ resistentie tegen meerdere klasse antibiotica
= de grootste veroorzakers van Multi-Drug Resistance (MDR). Dit komt omdat plasmiden vaak niet één gen bevatten, maar hele pakketjes met genen, ook wel "resistentie-cassettes" genoemd.
Verspreiding: verticaal & horizontaal
→ ook overdracht DNA mogelijk tussen bacteriën
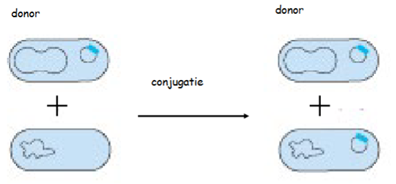
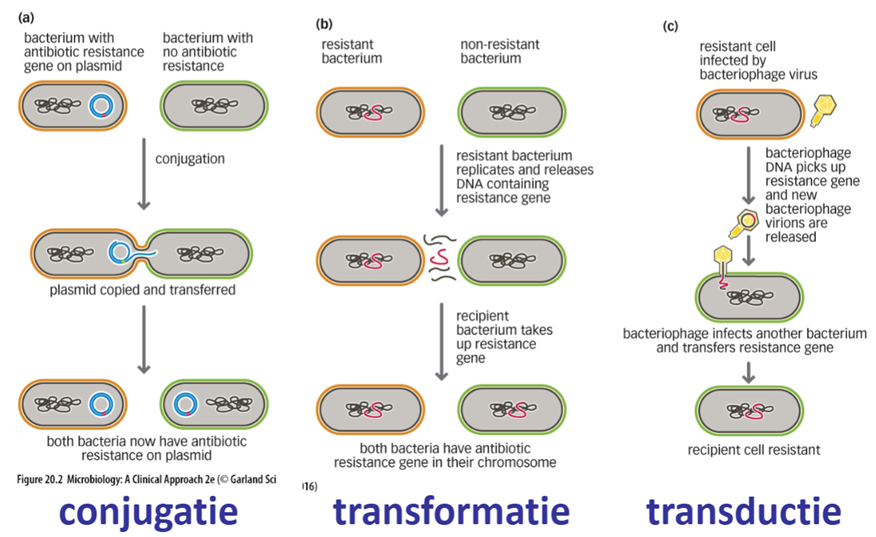
Verschillende manieren van horizontale DNA overdracht (HGT)
Conjugatie
= 2 bacteriën maken fysiek contactTransformatie
= bacterie haalt DNA uit zijn omgeving
→ wanneer een bacterie doodgaat en uit elkaar valt (lyse), komt zijn DNA vrij in de omgevingTransductie
= DNA wordt per ongeluk getransporteerd door een virus dat bacteriën infecteert, een bacteriofaag
→ wanneer een virus een bacterie infecteert, kaapt hij de cel om nieuwe virussen te maken. Soms gaat er iets mis bij het inpakken: virus stopt per ongeluk een stukje bacterieel DNA in zijn kop in plaats van zijn eigen virus-DNA
4 verschillende bacteriële mechanismen - resistentie
= strategieën die bacteriën gebruiken om aanval van antibiotica te overleven:
Inactivatie van het antibioticum
= bacterie produceert specifieke enzymen die antibioticum chemisch veranderen of volledig vernietigen voordat het schade kan aanrichten (bijvoorbeeld B-lactamase)
-> het antibioticum is er nog wel maar doet niets meer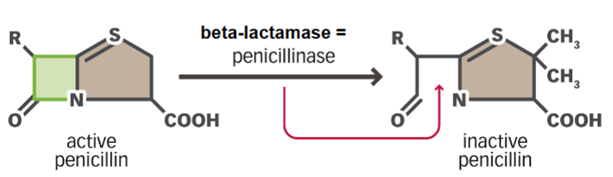
Verandering concentratie antibioticum
= bacterie zorgt ervoor dat de hoeveelheid medicijn binnen de cel te laag blijft om dodelijk te zijn, kan op 2 manieren:
Minder instroom: bacterie sluit de poortjes (porines)
Actieve uitstroom (Efflux-pompen): bacterie gebruikt “pompen” die het antibioticum direct weer naar buiten werkt
Verandering van het antibioticum ‘target’
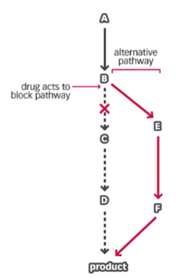
= de bacterie verandert de vorm van het target, waardoor het antibioticum er niet meer op pastMetabolisme ‘switch’
= sommige antibiotica werken door een cruciale stap in de stofwisseling van de bacterie te blokkeren
→ bij de ‘switch’ vindt de bacterie een biologische omweg (bypass) -> hij gaat bijvoorbeeld een ander enzym gebruiken om hetzelfde eindproduct te maken
Factoren die ontwikkelingen van antibioticum resistentie bespoedigen
Overmatig gebruik antibioticagebruik in veeteelt
Kuur niet afmaken
Verouderde antibiotica
Niet de juiste dosis nemen
Overmatig gebruik van breedspectrum-antibiotica
Ziekenhuizen
Soorten antibiotica
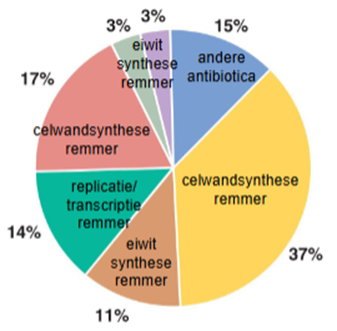
Celwand synthese remmers
Beta-Lactams (penicillines & cefalosporines)
Glycopeptiden
Eiwitsynthese remmers (gericht op ribosoom)
Ribosoom bestaat uit 2 onderdelen:50S: verhinderen van peptide elongatie,
De grote 50S-onderunit is de plek waar de aminozuren aan elkaar worden geknoopt tot een lange ketting (peptide elongatie).
(bijvoorbeeld Macroliden)30S: verhindert binding van tRNA,
De kleine 30S-onderunit is verantwoordelijk voor het "lezen" van de code en het toelaten van tRNA. tRNA is de vrachtwagen die de bouwstenen (aminozuren) aanlevert.
(bijvoorbeeld Tetracyclines)
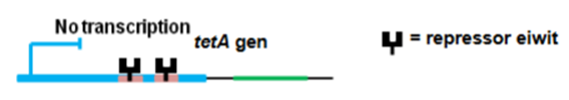
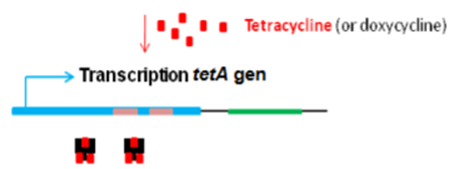
Replicatie- & transcriptie remmers (gericht op chromosoom)
→ bacterie heeft een circulair chromosoomQuinolonen
= DNA replicatieRymfamycines
= transcriptie; DNA afhankelijke RNA polymerase
→ verandering target site (mutatie)
Chromosoom & plasmide
Resistentie van bacteriën (beta-lactamase)
1. beta-lactamase: De "Snoeischaar"
Alle penicillines en cefalosporines hebben één ding gemeen: een chemische structuur die de beta-lactamring heet. Dit is de "actieve kop" van het medicijn die de celwand-bouw blokkeert.
Het mechanisme: Sommige bacteriën maken het enzym $\beta$-lactamase. Dit enzym knipt de beta-lactamring simpelweg doormidden.
Het gevolg: Het antibioticum is kapot nog voordat het de celwand-fabriek kan bereiken. Het medicijn werkt niet meer.
2. ESBL (Extended Spectrum beta-Lactamase)
Dit is de "geüpgradede" versie van de gewone schaar.
Het verschil: Waar een gewone beta-lactamase alleen penicilline sloopt, kan een ESBL bijna alle penicillines én bijna alle cefalosporines (een andere grote groep celwand-remmers) afbreken.
De dader: Vooral de E. coli en Klebsiella bacteriën zijn berucht om het bij zich dragen van ESBL-genen.
Gevolg: Je standaard arsenaal aan antibiotica is in één klap waardeloos.
3. BRMO (Bijzonder Resistente Micro-Organismen)
Dit is een verzamelnaam voor bacteriën die tegen de belangrijkste antibiotica resistent zijn geworden.
Normale flora: Het enge is dat BRMO’s (zoals de ESBL-producerende E. coli) vaak gewoon in je darmen wonen zonder dat je het merkt. Ze horen bij je normale flora.
Opportunistisch: Zolang ze in je darm zitten, is er niets aan de hand. Maar als ze via een katheter in je blaas komen of via een operatiewond in je bloed, veroorzaken ze een opportunistische infectie die extreem moeilijk te behandelen is.
4. De "Reddingsmiddelen": Carbapenems & Monobactams
Als een bacterie ESBL heeft, moeten we overstappen op antibiotica die resistent zijn tegen die "schaar".
Carbapenems (bijv. Meropenem): Dit zijn de zwaargewichten. Ze hebben een beta-lactamring die zo stevig is dat de meeste ESBL-scharen hem niet kunnen doorknippen. Ze werken tegen zowel Gram-positieve als Gram-negatieve bacteriën (breed-spectrum). Dit is vaak ons laatste redmiddel in het ziekenhuis.
Monobactams (bijv. Aztreonam): Deze hebben een unieke, "eenzame" ringstructuur. Ze werken alleen tegen Gram-negatieve bacteriën. Omdat hun structuur anders is, worden ze niet herkend of afgebroken door de meeste standaard beta-lactamases.
MRSA (Staphylococcus aureus, S. aureus)
1. Wat is MRSA precies?
Staphylococcus aureus is een bacterie die bij ongeveer 30% van de mensen gewoon op de huid of in de neus zit. Dat is meestal prima (commensalisme). Meticilline-Resistent betekent dat deze specifieke stam een gen (mecA) heeft opgepikt waardoor hij zijn "sloten" (eiwitten in de celwand) heeft veranderd.
Het gevolg: Gewone penicillines, amoxicilline en zelfs de sterke cefalosporines kunnen zich niet meer aan de bacterie vastmaken. De "sleutel" past niet meer op het "slot".
2. "Op de huid" vs. "Invasief"
Je hebt gelijk: zolang MRSA op je huid zit, merk je er niets van. Je bent dan een drager. De problemen beginnen pas als de bacterie de barrière van de huid doorbreekt.
Dragerschap: De bacterie leeft van je zweet en dode huidcellen. Je bent niet ziek, maar je kunt de bacterie wel verspreiden naar anderen (bijvoorbeeld via een handdruk).
Invasieve infectie: Als de bacterie via een wondje, een operatie-snede of een infuusnaald naar binnen glipt, wordt hij pathogeen. Hij kan dan veroorzaken:
Abcessen (diepe steenpuisten).
Pneumonie (longontsteking).
Sepsis (bloedvergiftiging): de bacterie verspreidt zich door je hele lichaam. Dit is het stadium waarin het dodelijk kan zijn.
3. Waarom de "Ziekenhuisbacterie"?
In een ziekenhuis komen drie gevaarlijke factoren samen:
Kwetsbare gastheren: Mensen met een zwak immuunsysteem of open wonden.
Invasieve poorten: Veel infusen, katheters en operaties (de ideale Port d'entrée).
Selectiedruk: Er worden veel antibiotica gebruikt. De "zwakke" bacteriën gaan dood, waardoor de resistente MRSA alle ruimte krijgt om te groeien.
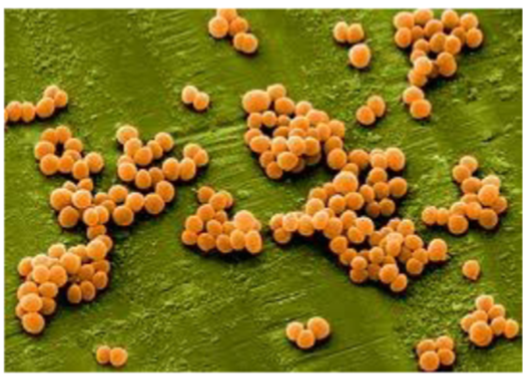
MRSA is voorbeeld van:
1. Horizontal Gene Transfer
2. Meerdere mechanismen van resistentie
S. Aureus - kenmerken en virulentiefactoren
Kenmerken:
gram+, facultatief anaëroob
bevindt zich in normale flora: neus, keel en huid
zoönose
T-route: direct: contact transmissie; indirect: 3 maanden op polyester
Virulentiefactoren:
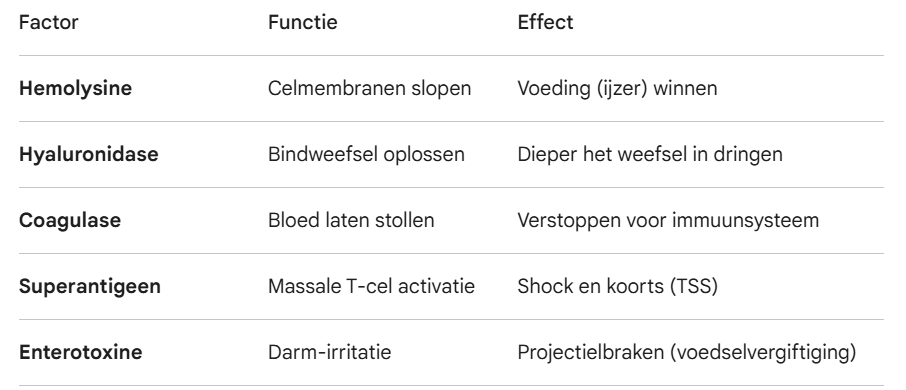
Vancomycine - 1 antibioticum die wel actief was tegen MRSA
Net als penicilline valt vancomycine de celwand aan, maar op een andere manier.
Penicilline blokkeert de "metselaar" (het enzym).
Vancomycine gaat boven op de "bakstenen" (de bouwstenen van de celwand) zitten. Het bindt zich aan het uiteinde van de peptidoglycaan-keten.
Het gevolg: De metselaar kan er niet meer bij. De celwand kan niet worden afgebouwd, de bacterie knapt uit elkaar en gaat dood (bactericide).
Ligase zorgt ervoor dat target site veranderd wordt
→ waardoor vancomycine niet meer kan binden
→ Gevolg is dat celwandsynthese niet meer geremd wordt
→ VRSA = vancomycine resistente S.aureus
→ MRSA, heeft 7% van genoom gewijd aan antibioticum resistentie en is dus ook resistent tegen meerdere antibiotica
Wat deden we tegen MRSA? - Search and Destroy
→ patiënten werden ingedeeld in 1 van de volgende categorieën, hier hoorde isolatie etc. bij:


Heeft veel effect gehad!