5. DERIVATI KARBOKSILNIH KISELINA
1/81
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
82 Terms
Sto su derivati karboksilnih kiselina
Spojevi srodni karboksilnim kiselinama i medusobno srodni
Spojevi s funkcijskim skupinama koje se jednostavnom hidrolizom u kiseloj ili luznatoj sredini mogu pretvoriti u karboksilnu skupinu
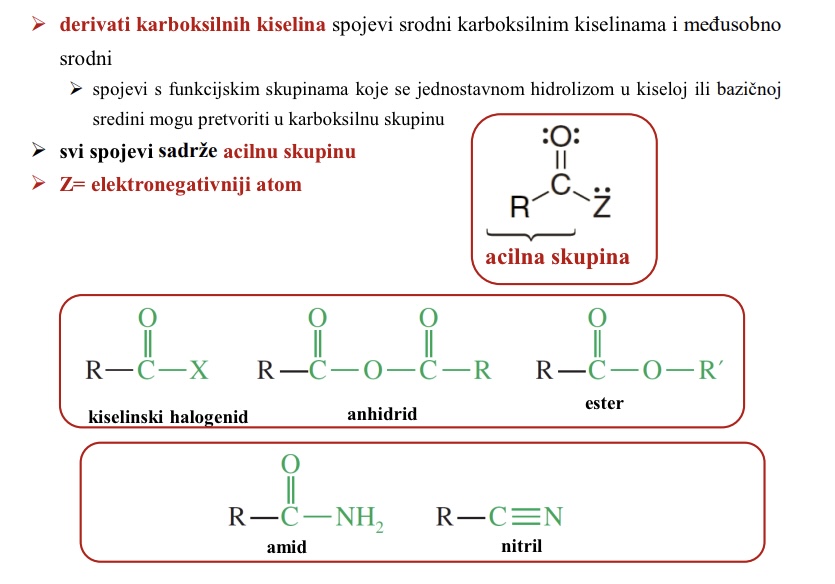
Sto svi derivati karboksilnih kiselina imaju koju skupinu
Acilnu skupinu, Z - elektronegativniji element i karbonilna skupina
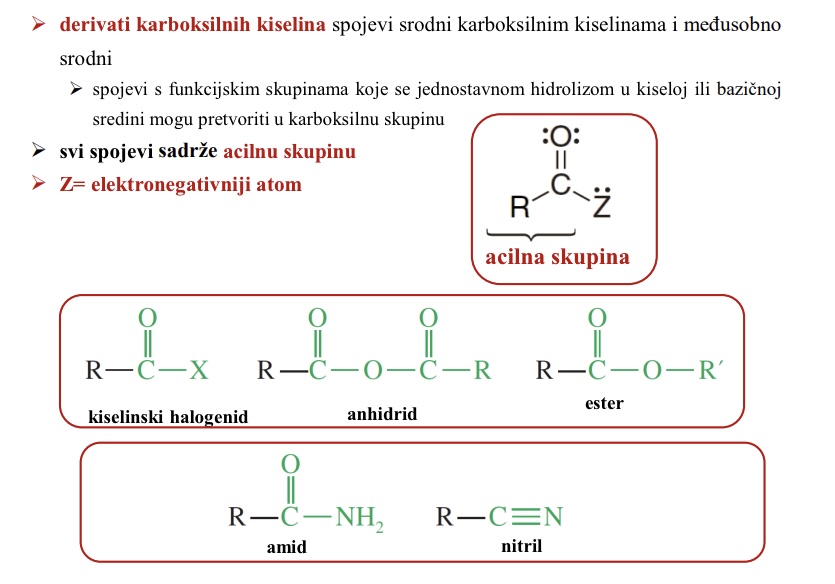
Zasto se nitrili isticu od ostalih derivata karboksilnih kiselina
strukturno razliciti od karboksilnih kiselina i njihovih derivata
Ne sadrze karbonilnu skupinu

Zasto se nitrili svrstavaju u derivate karboksilnih kiselina
Hidrolizom daju kiseline
Koju skupinu sadrze nitrili
Cijano skupinu

Kakav je ugljikov atom cijano skupine u nitrilima
ugljikov atom cijano skupine u istom oksidacijskom stanju kao karbonilni ugljik u derivatima karboksilnih kiselina - slicnost u njihovoj kemiji

Kako se odreduje oksidacijsko stanje ugljika
oksidacijsko se stanje ugljika mijenja za +1 nastajanjem svake veze s elektronegativnim atomom poput heteroatoma
-1 svakom vezom s elektropozitivnijim atomom
Dvostruke i trostruke veze s heteroatomom racunaju se dva odnosno tri puta
Veze ugljik ugljik se ne racunaju

Imaju li derivati karboksilnih kiselina rezonantne strukture
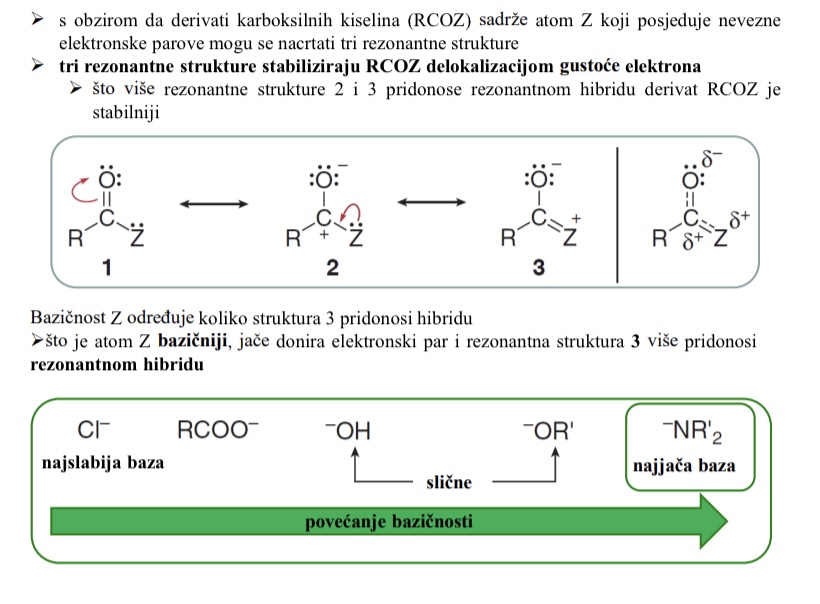
s obzirom da derivati karboksilnih kiselina (RCOZ) sadrze atom Z koji posjeduje nevezne elektronske parove mogu se nacrtati tri rezonantne strukture
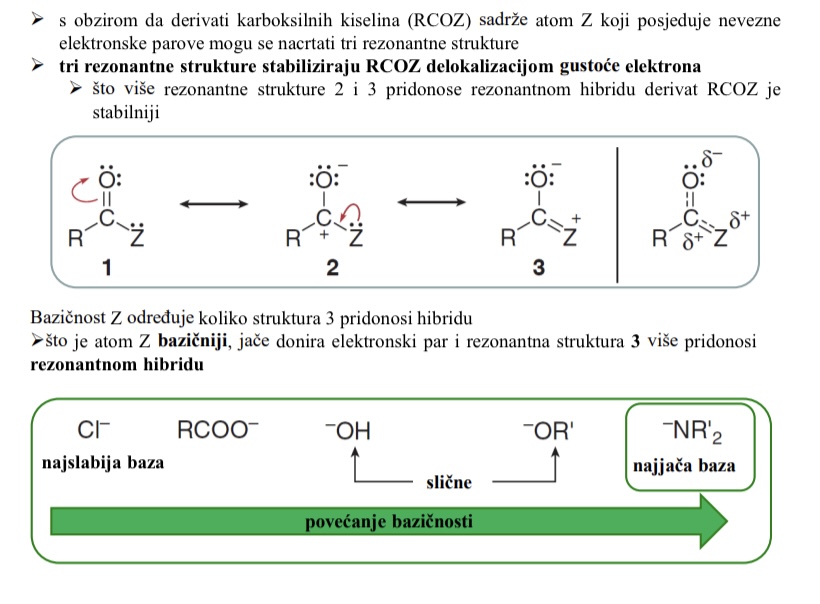
Sto rade rezonantne strukture u derivatima karboksilnih kiselina
tri rezonantne strukture stabiliziraju RCOZ delokalizacijom gustoce elektrona
(sto vise rezonantne strukture 2 i 3 pridonose rezonantnom hibridu derivat RCOZ je stabilniji)
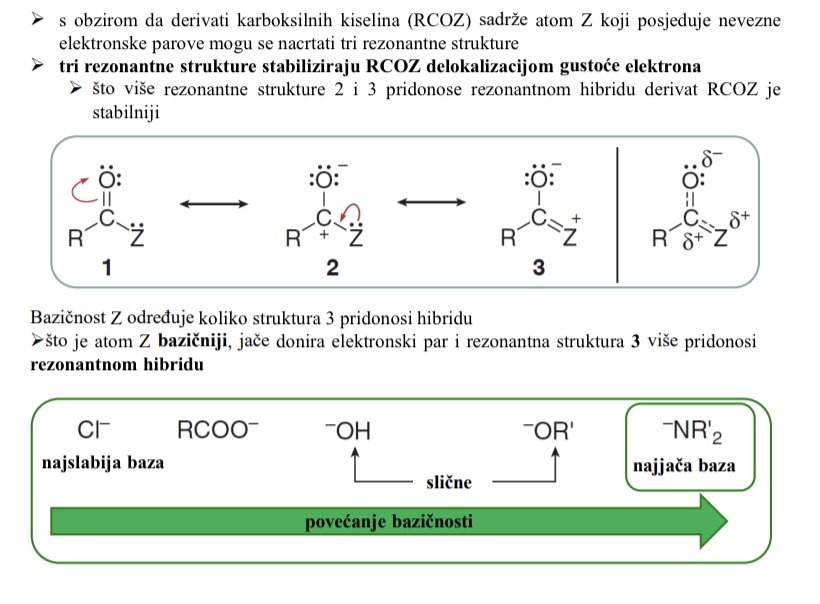
Utjecaj bazicnosti i rezonantnih hibrida RCOZ
Bazicnost Z odreduje koliko struktura 3 prodonosi hibridu
Sto je atom Z bazicniji, jace donira elektronski par i rezonantna struktura 3 vise pridonosi rezonantnom hibridu
Ujtecaj bazicnosti Z na stabilnost RCOZ
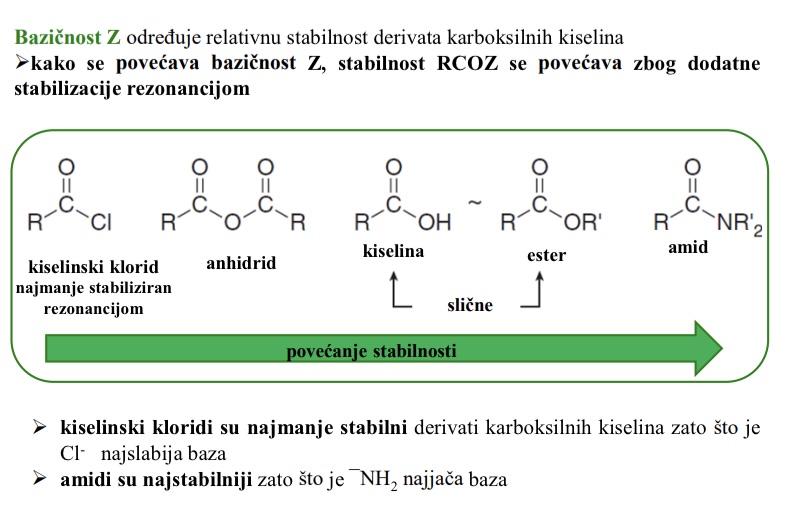
Bazicnost Z odreduje relativnu stabilnost derivata karboksilnih kiselina
kako se povecava bazicnost Z, stabilnost RCOZ se povecava zbog dosatne stabilizacije rezonancijom
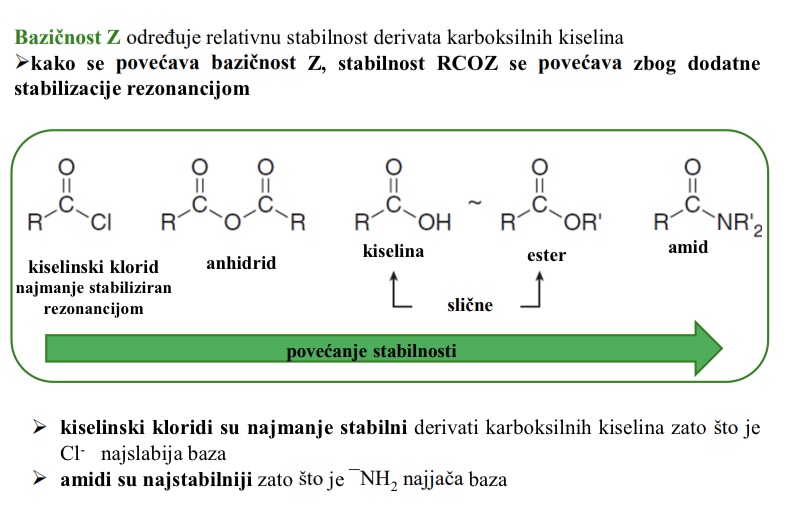
Koji derivati karboksilnih kiselina su najstabilniji a koji najmanje stabilni
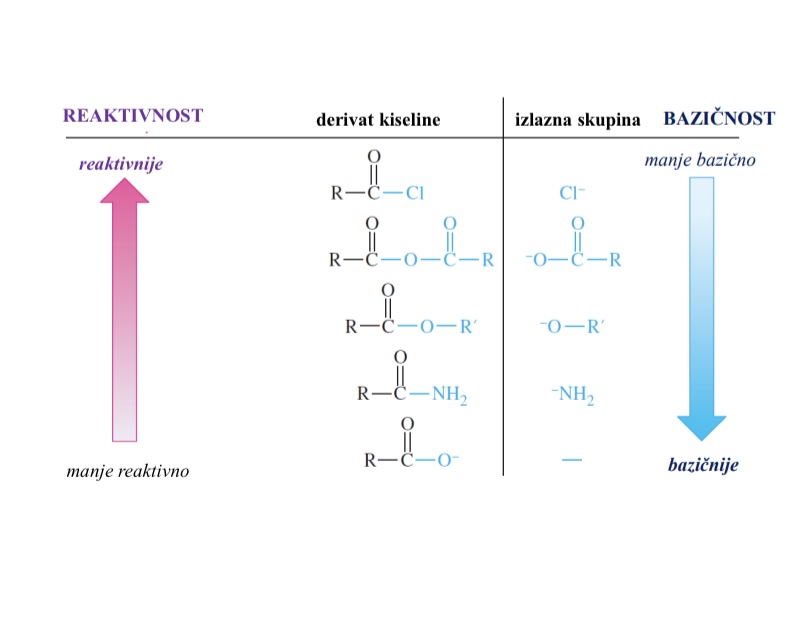
Najmanje stabilni - kiselinski kloridi (Cl- najslabija baza)
Najstabilniji - amidi (-NH2 najjaca baza)
Fizikalna svojstva derivata karboksilnih kiselina
Polarni karakter
Vrelista:
kiselinski i anhidridi priblizno isto kao ketoni i aldehidi odgovarajuce molekularne tezine
amidi najvisa vrelista
Topljivost: topljivi u organskim otapalima
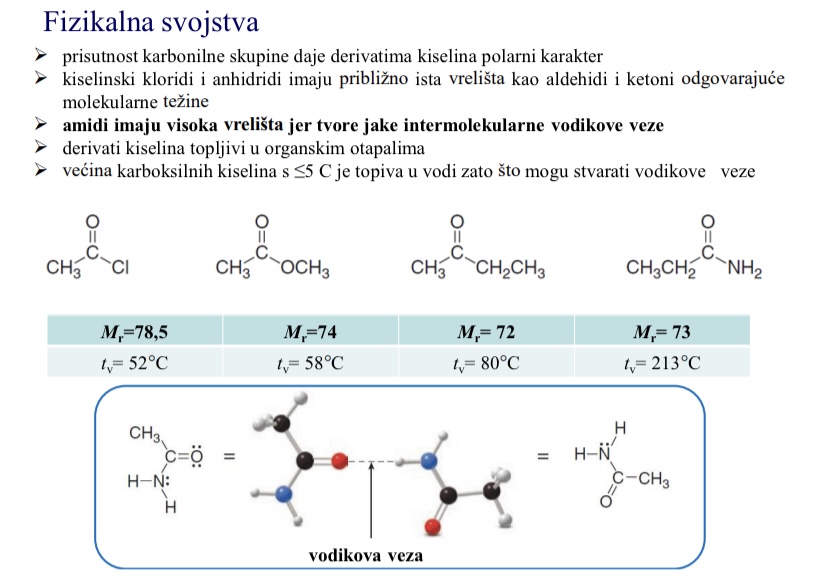
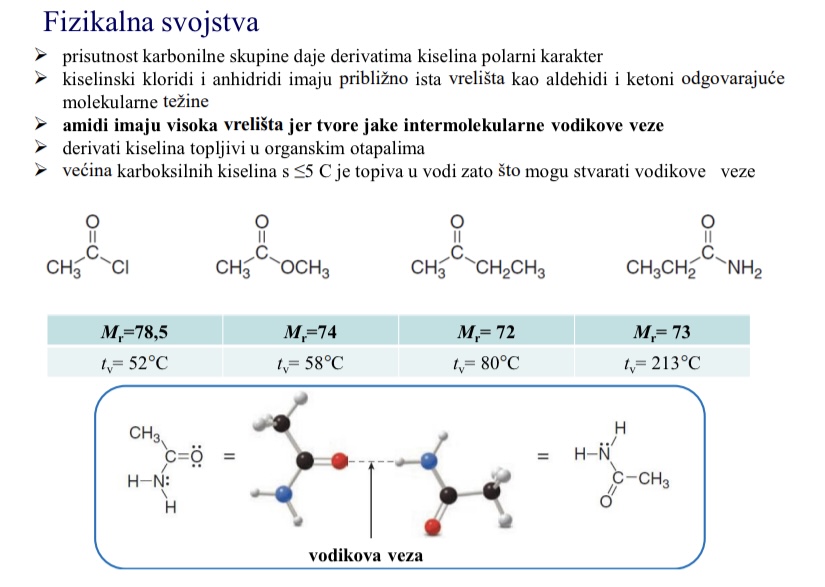
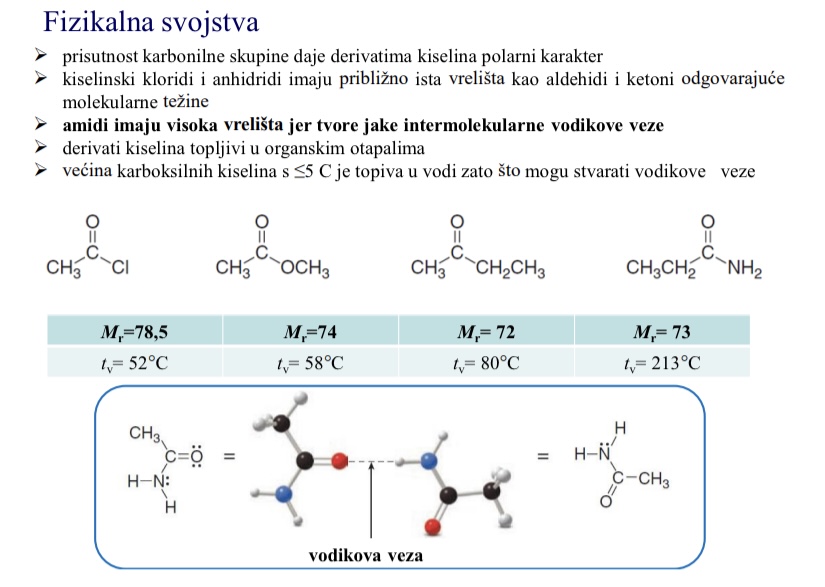
Zasto amidi imaju najvisa vrelista
Tvore jake intermolekularne vodikove veze
Koje su karboksilne kiseline topive u vodi i zasto
Vecina karboksilnih kiselina s 5 ili manje C atoma, mogu stvarati vodikove veze
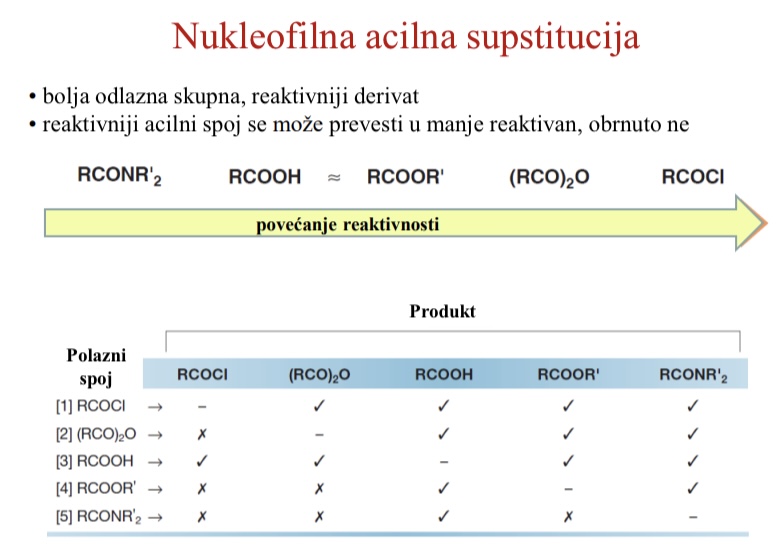
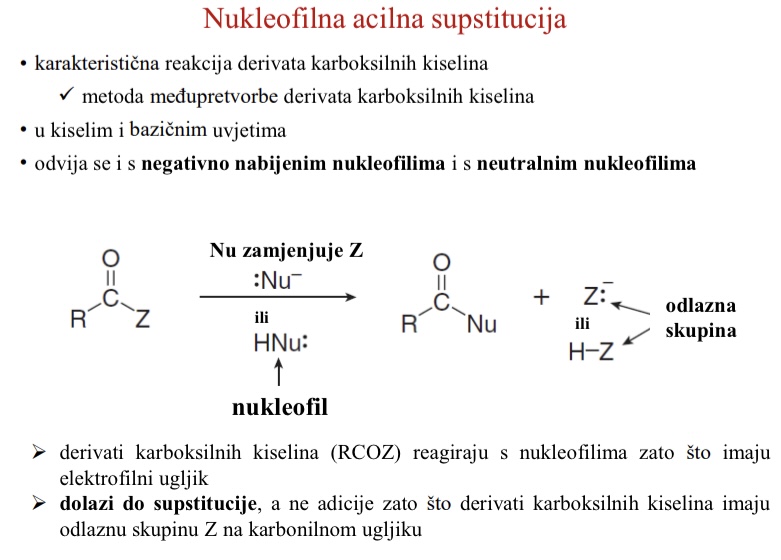
Koja je karakteristicna reakcija derivata karboksilnih kiselina
Nukleofilna acilna supstitucija
/ metoda medupretvorbe derivata karboksilnih kiselina
U kojim se uvjetima odvija nukleofilna acilna supstitucija
U kiselim i bazicnim uvjetima
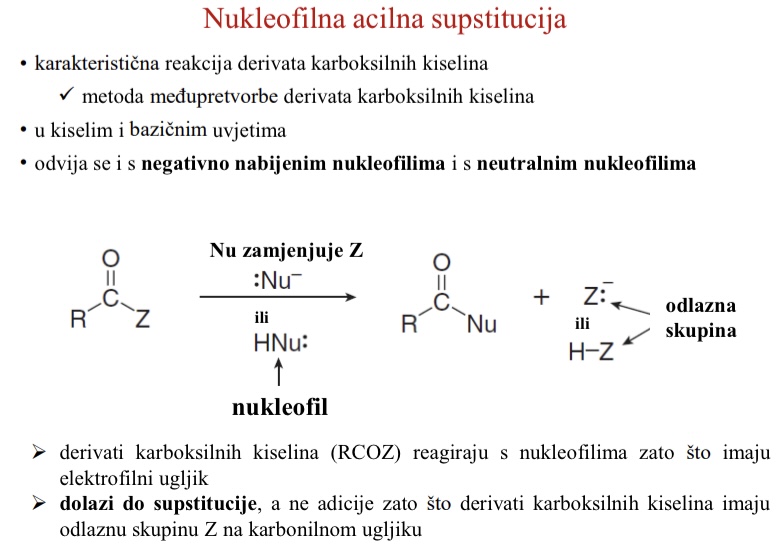
S kojim nukleofilima se moze odvijati nukleofilna acilna supstitucija
I s negativno nabijenim nukleofilima i s neutralnim nukleofilima
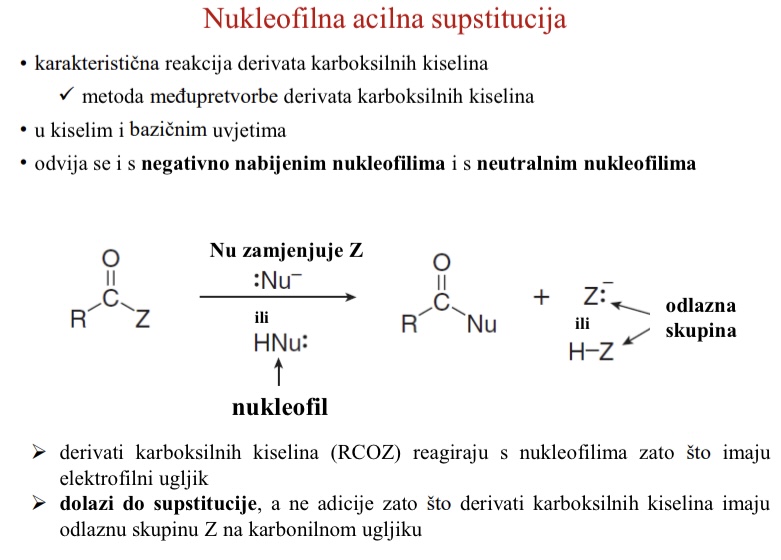
Zasto derivati karboksilnih kiselina RCOZ reagiraju s nukleofilima
Imaju elektrofilni ugljik
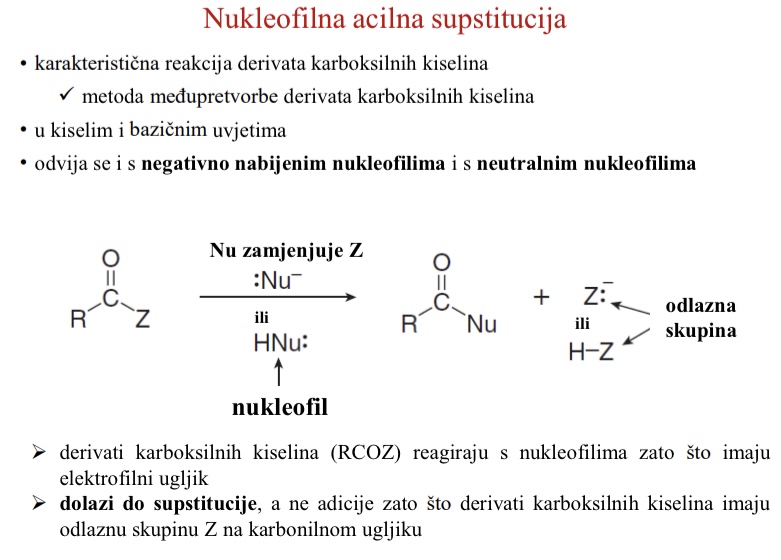
Zasto s RCOZ dolazi do supstitucije a ne do adicije
Derivati karboksilnih kiselina imaju odlaznu skupinu Z na karbonilnom ugljiku
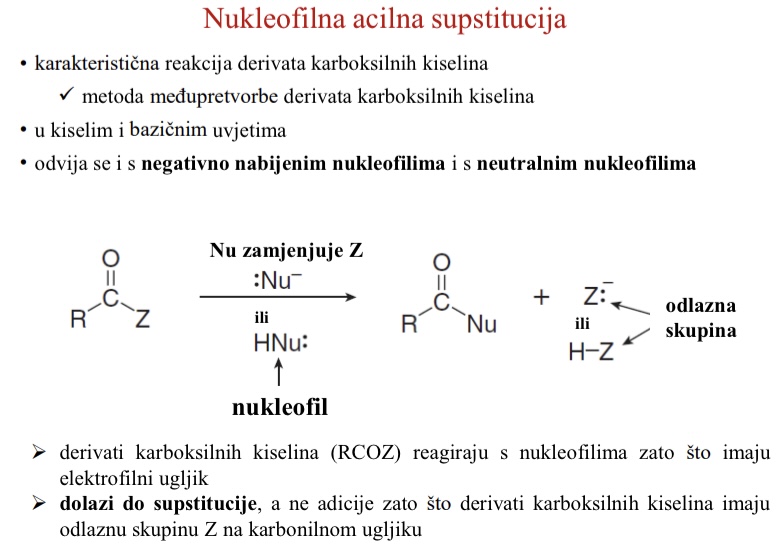
Mehanizam nukleofilne acilne supstitucije
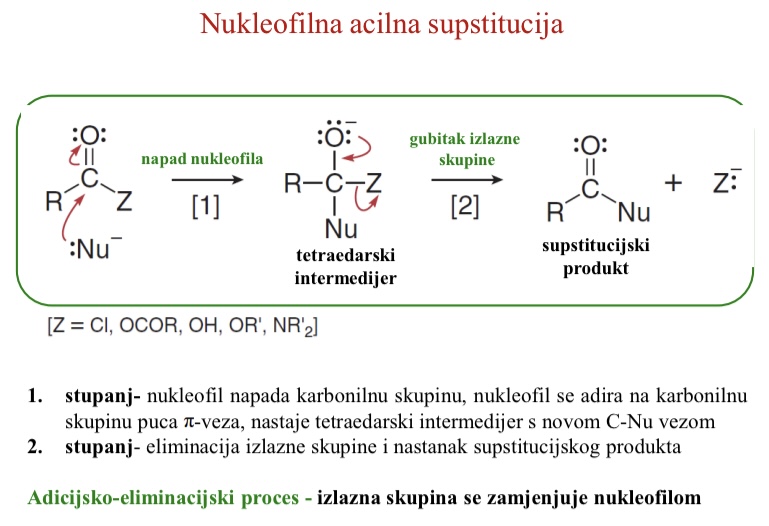
Kako se derivati karboksilnih kiselina mogu prevoditi jedan u drugi
Nukleofilna acilna supstitucija
reaktivniji acilni spojevi (kisleinski kloridi i anhidridi) mogu se prevesti u manje reaktivne (karboksilne kiseline, estere, amide) obrnuto ne
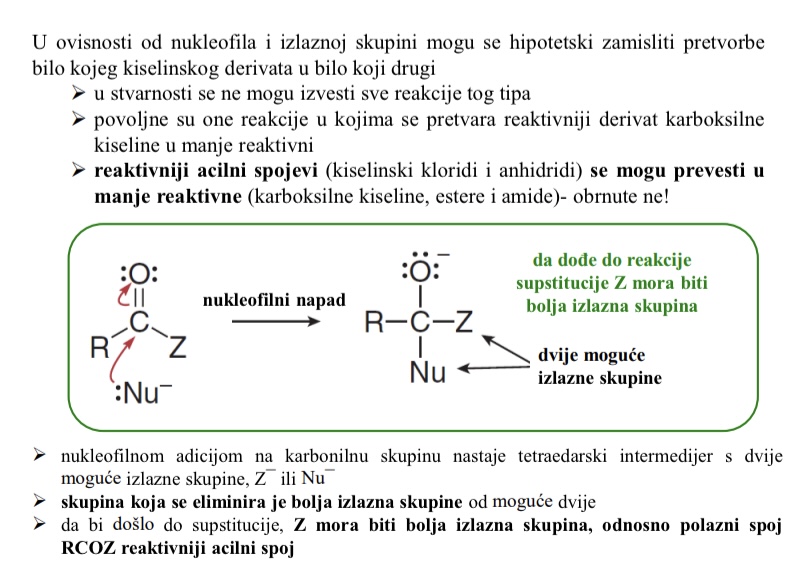
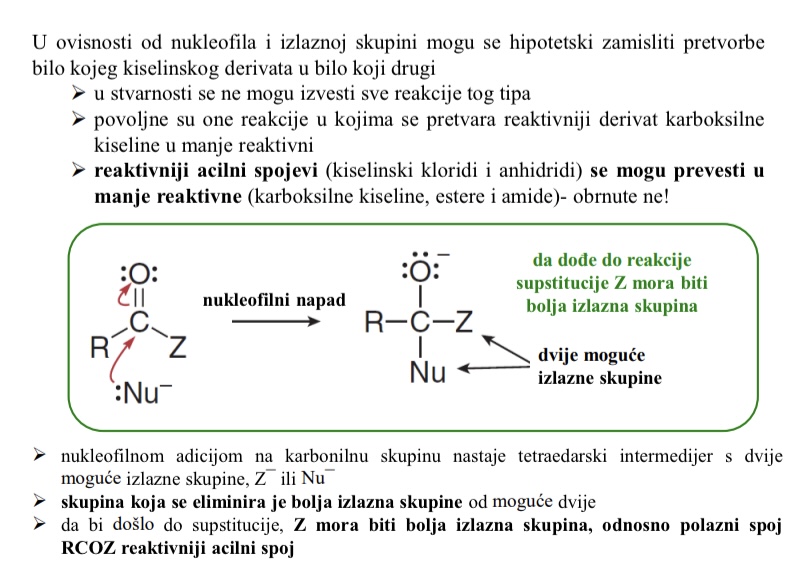
Sto nastaje nukleofilnom adicijom na karbonilnu skupinu
tetraedarski intermedijer s dvije moguce izlazne skupine Z- ili Nu-
Od dviju izlaznih skupina koje nastaju nukleofilnom adicijom na karbonilnu skupinu koja se eliminira (Z- ili Nu-)
Ona koja je bolja izlazna skupina
Da bi doslo do supstitucije koja izlazna skupina mora biti bolja
Z mora biti bolja izlazna skupina, odnosno polazni spoj RCOZ reaktivniji acilni spoj
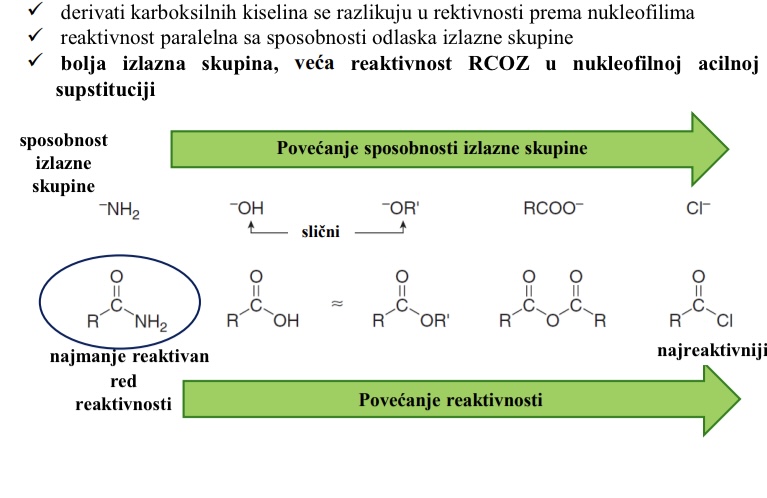
kakvi su po reaktivnosti derivati karboksilnih kiselina
Razlikuju se u reaktivnosti prema nukleofilima
S cime je reaktivnost RCOZ paralelna
Sa sposobnosti odlaska izlazne skupine
bolja izlazna skupina → veca reaktivnost RCOZ u nukleofilnoj acilnoj supstituciji
utjecaj reaktivnosti derivata karboksilnih kiselina i bazicnosti izlazne skupine
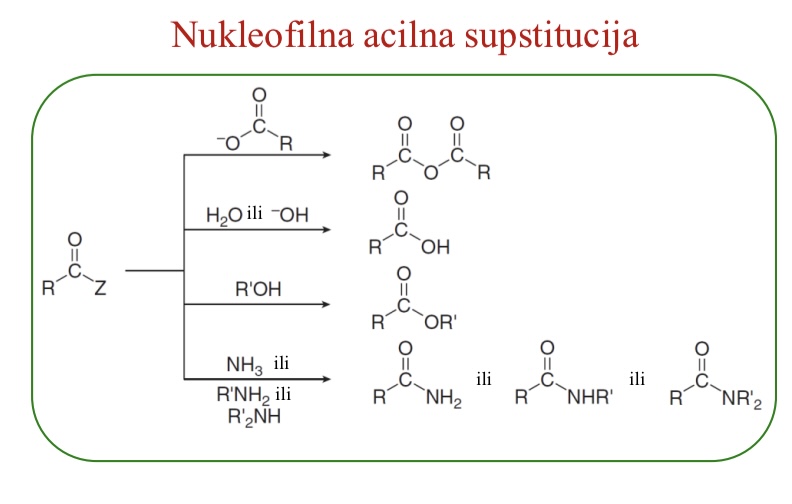
S kojim se sve reagensima moze izvoditi nukleofilna acilna supstitucija
Kako se mogu sintetizirati kiselinski kloridi
djelovanjem razlicitih reagenasa na karboksilne kiseline
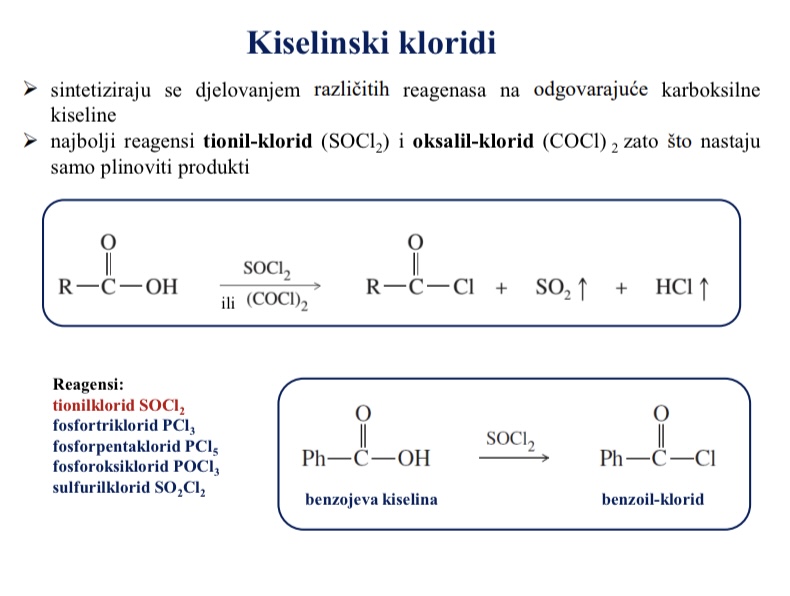
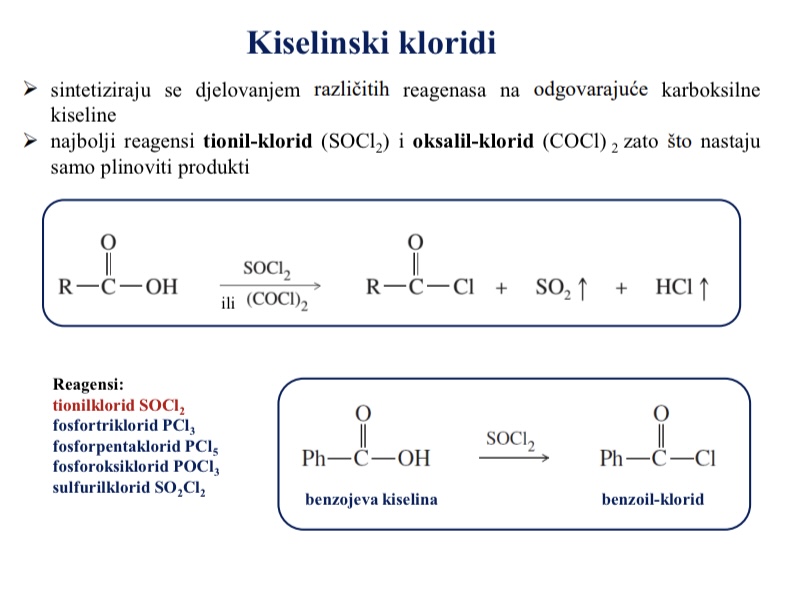
Kojim reagensima se mogu pripraviti kiselinski kloridi - koji su najbolji i zasto
Najbolji reagensi tionil-klorid (SOCl2) i oksalil-klorid (COCl) zato sto nastaju samo plinoviti produkti
Zasto su kiselinski kloridi najreaktivniji derivati kiselina
Mogu se lako pretvoriti u bilo koji kiselinski derivat
lako reagiraju s nukleofilima i daju produkte nukelofilne supstitucije
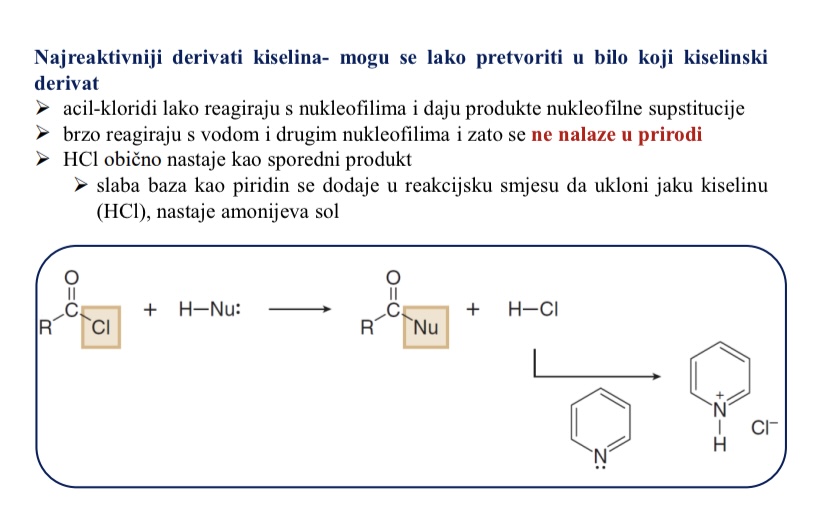
Zasto se kiselinski kloridi ne nalaze u prirodi?
brzo reagiraju s vodom i drugim nukleofilima
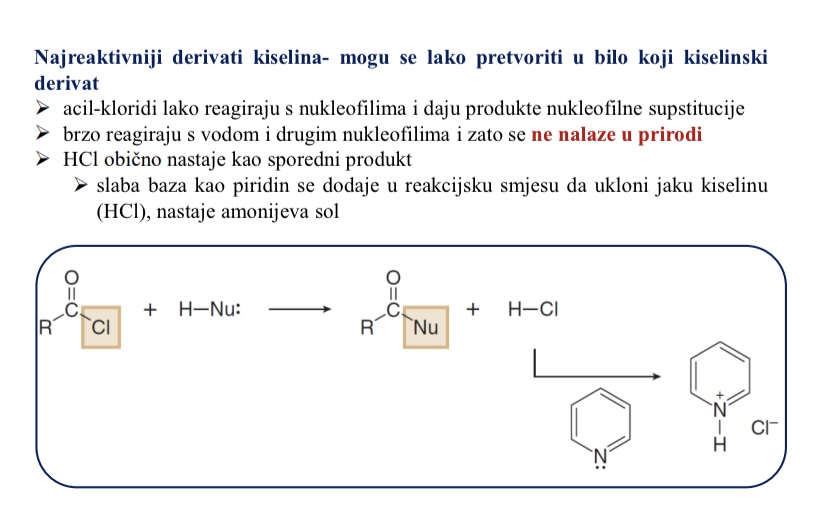
Kada kiselinski kloridi reagiraju sto obicno nastaje kao sporedni produkt
HCl
slaba baza kao piridin se dodaje u reakcijsku smjesu da ukloni jaku kiselinu (HCl) nastaje amonijeva sol
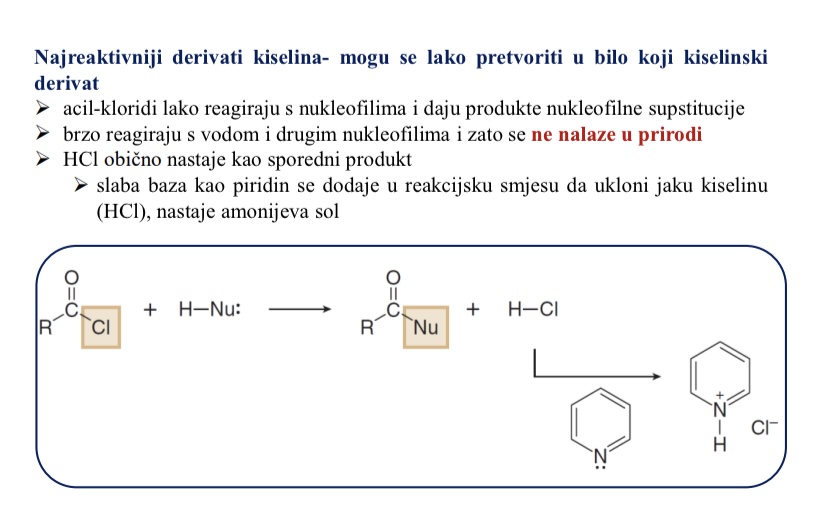
Reakcije kiselinskih klorida
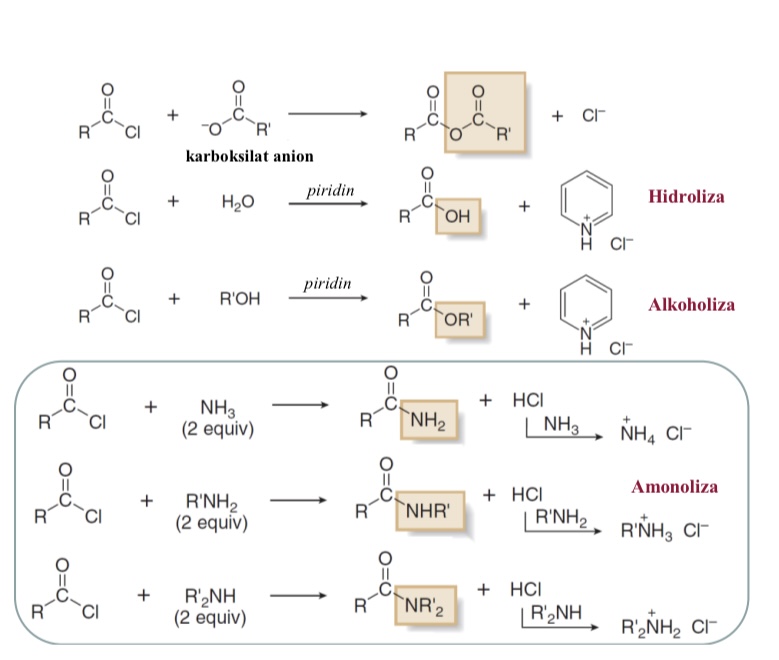
Mehanizmi
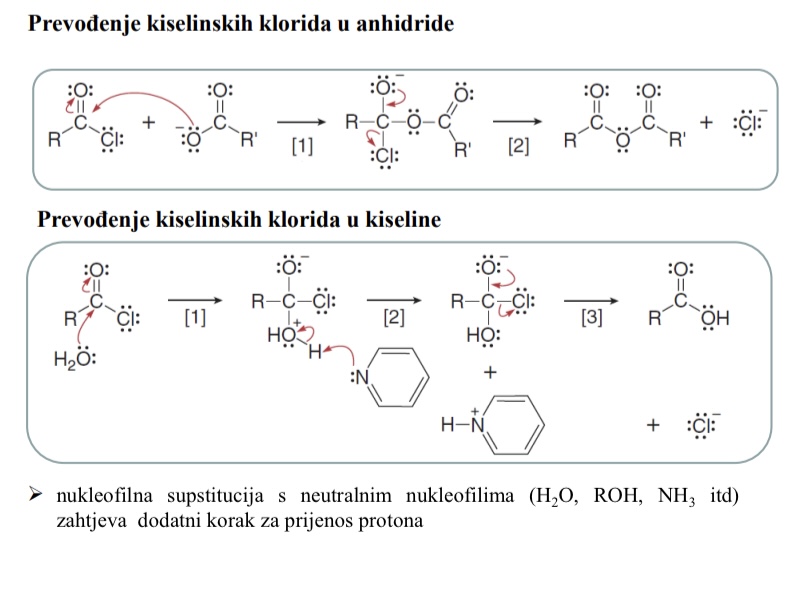
Prevodenje kiselinskih klorida u anhidride
Prevodenje kiselinskih klorida u kiseline
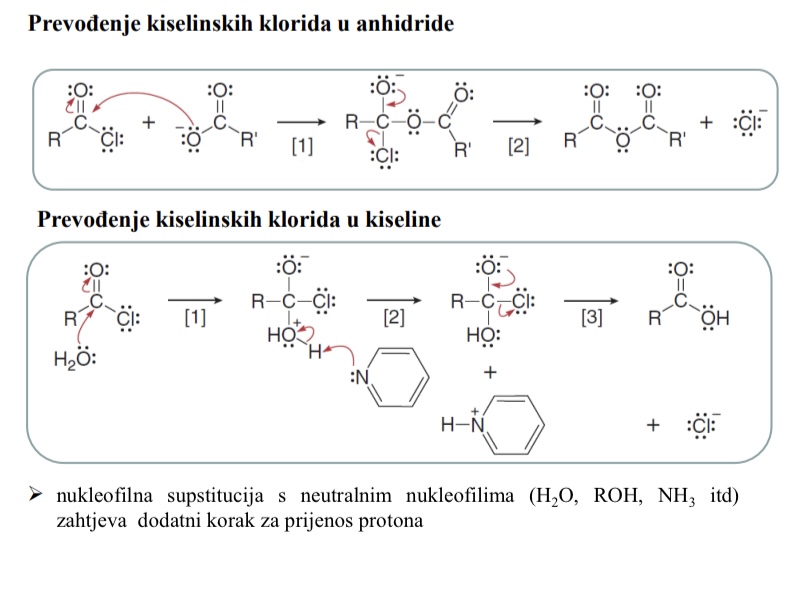
Sto zahtijeva nukleofilna suspstitucija s neutralnim nukleofilima (H2O, ROH, NH3,…)
Dodatni korak za prijenos protona
Anhidridi kiselina
aktivirani kiselinski derivati
Nisu reaktivni kao kiselinski kloridi, mogu se naci u prirodi

Primjer anhidrida kiselina
Kantaridin - otrovni alkaloid dobiven susenjem i mljevenjem kukca - babak, zeleni

Koji je najvazniji anhidrid
Acetanhidrid
Cemu sluzi acetanhidrid
sinteza plastike, smole, lijekova (acetilsalicilna kiselina)
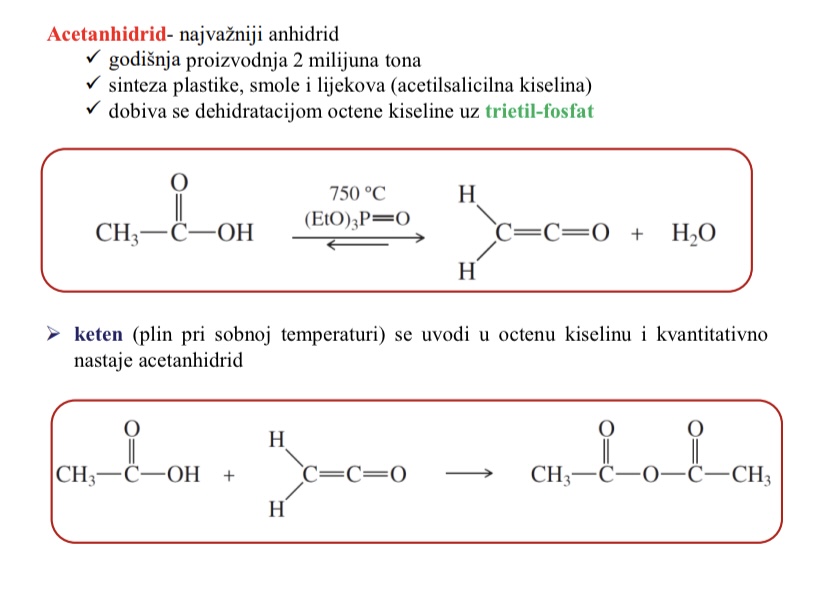
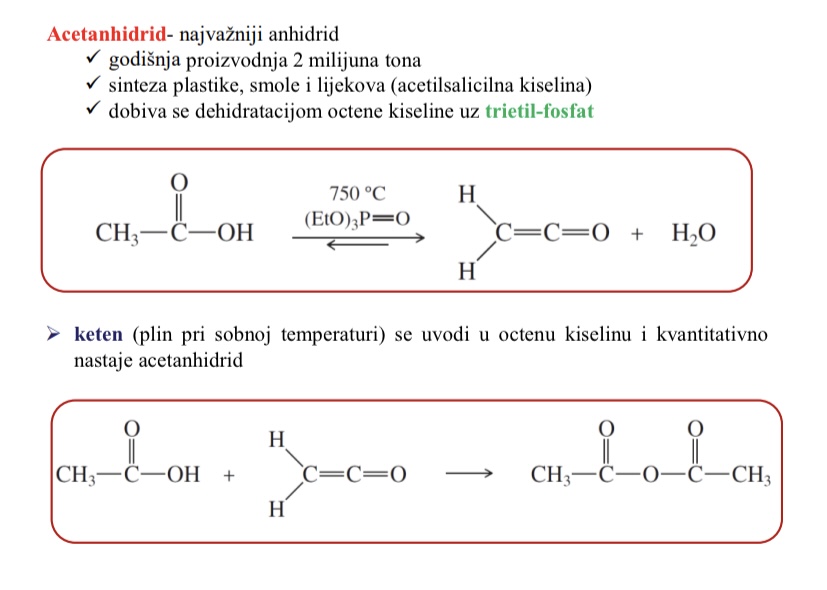
Kako se dobiva acetanhidrid
dehidratacijom octene kiseline uz trietil-fosfat
godisnja proizvodnja 2 milijuna tona
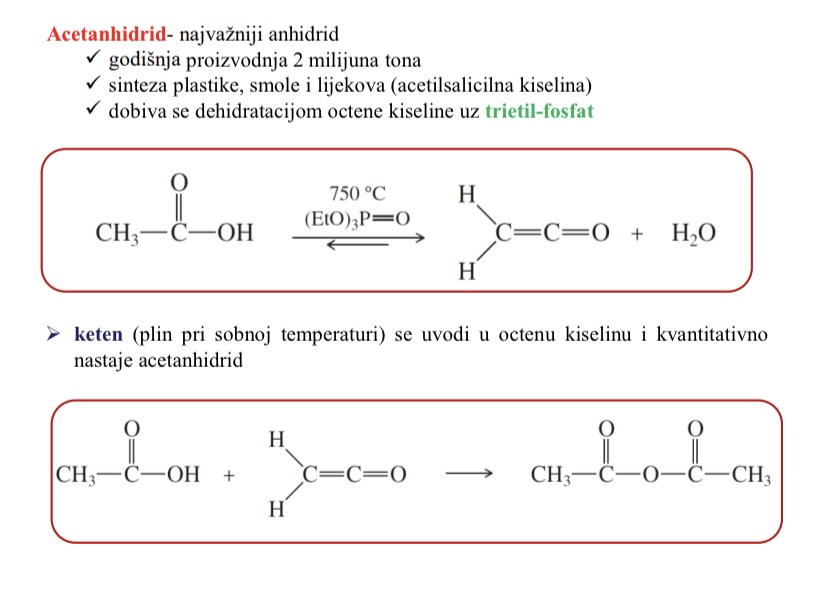
Sto se upotrebljava pri sintezi acetanhidrida
Keten - plin pri sobnoj temperaturi - uvodi se u octenu kiselinu i kvantitativno nastaje acetanhidrid
Kako se najcesce dobivaju kiselinski anhidridi
Reakcijom kiselinskih klorida s karboksilnim kiselinama ili njihovim solima
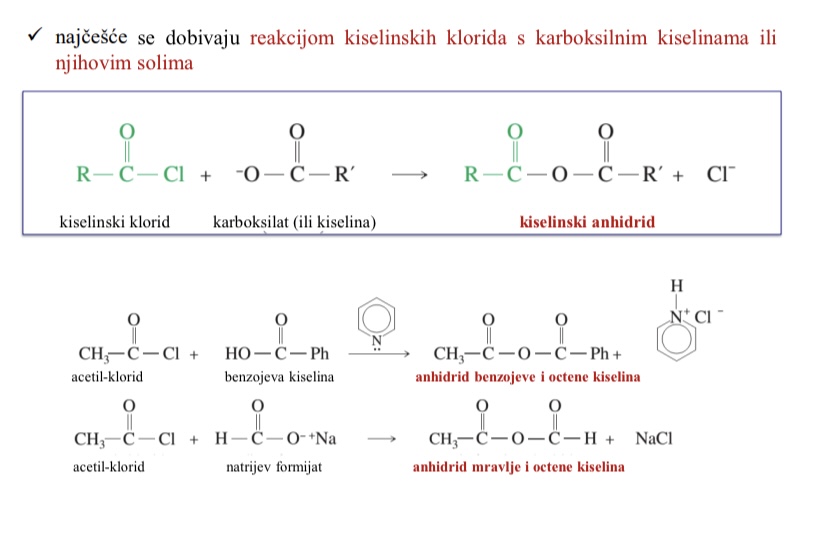
Primjeri dobivanja kiselinskih klorida
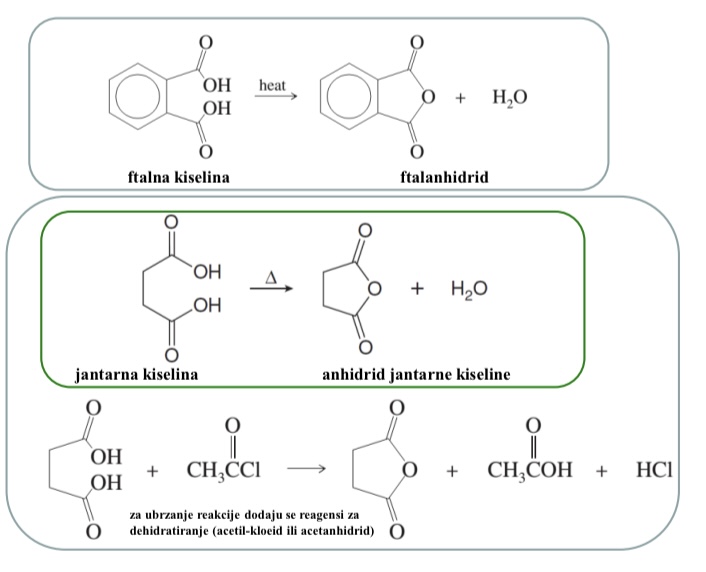
Zasto se anhidridi ne mogu koristiti za pripravu kiselinskih klorida
RCOO- jaca baza i slabija izlazna skupina od Cl-
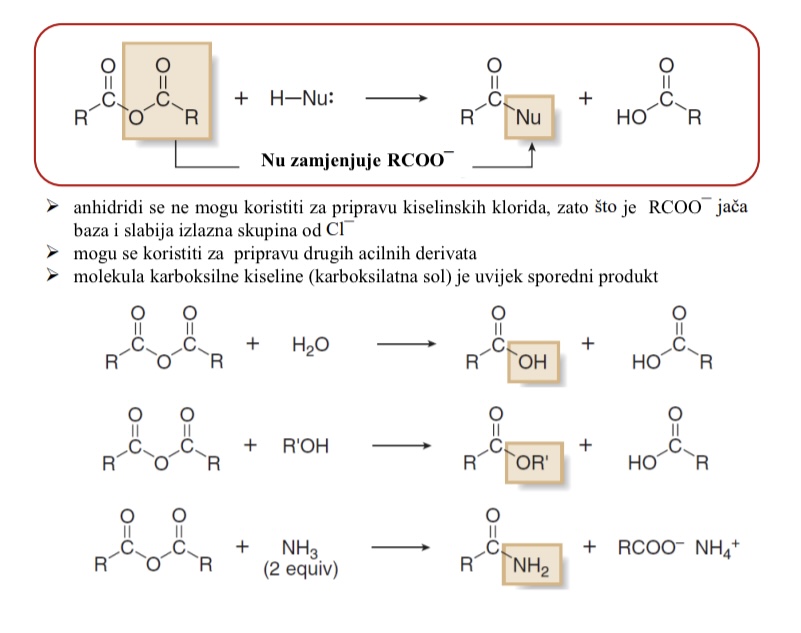
Za sto pripravu cega se mogu koristiti anhidridi kiselina i koji je sporedni produkt
pripravu drugih acilnih derivata
Sporedni produkt: molekula karboksilne kiseline (karboksilna sol)
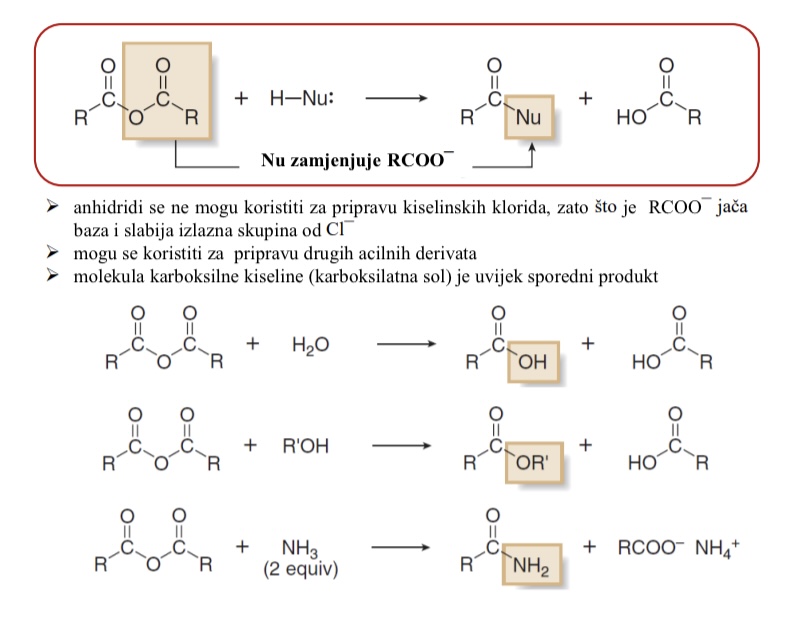
Prevodenje anhidrida u amide
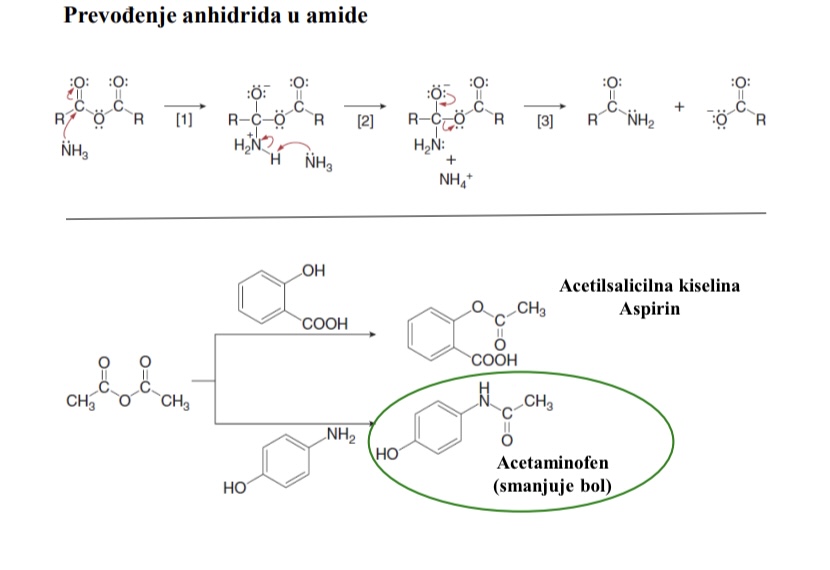
Primjeri iz prirode
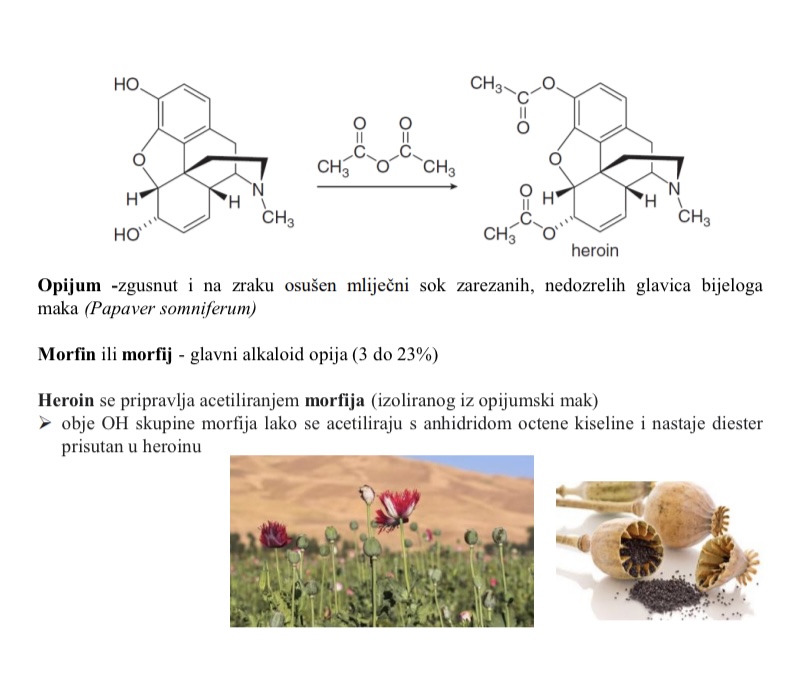
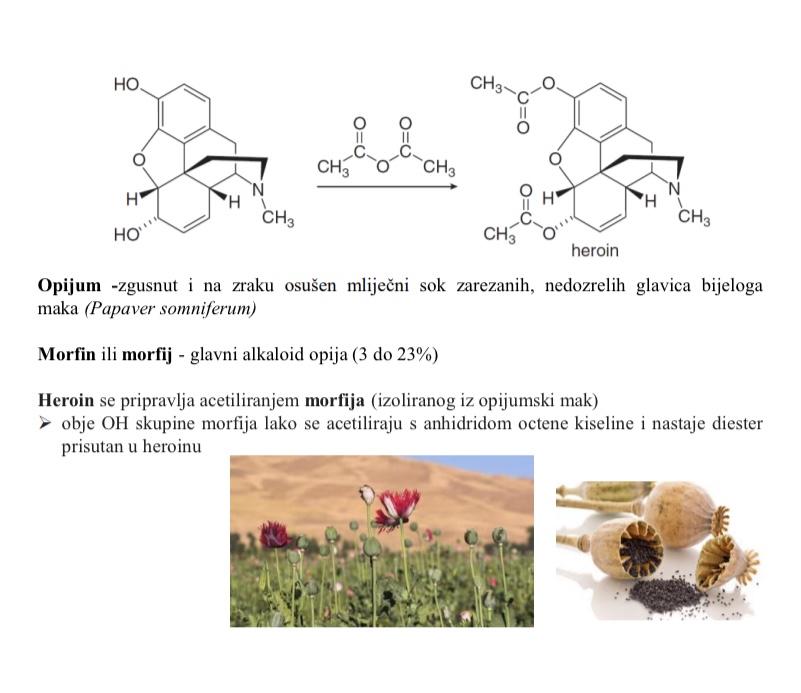
Kako se pripravlja heroin
Acetiliranjem morfija
obje OH skupine morfija lako se acetiliraju a anhidridom octene kiselinei nastaje diester prisutan u heroinu
Kojim reagensima/ reakcijama se mogu dobiti karboksilne kiseline
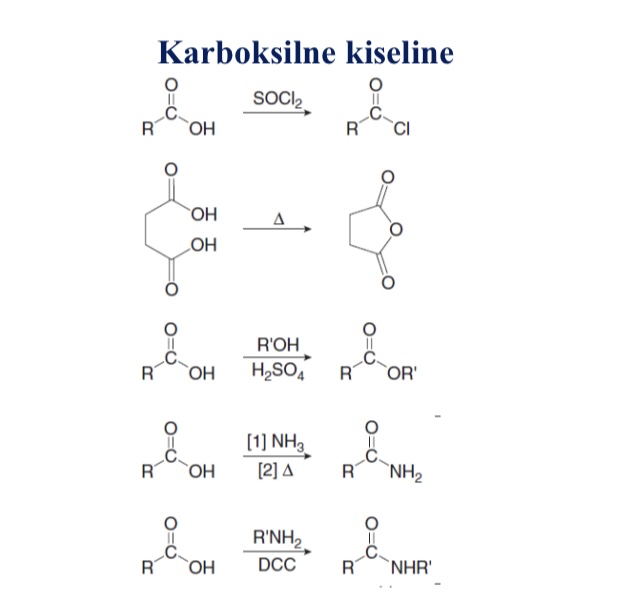
Reakcije kojima nastaju karboksilne kiseline
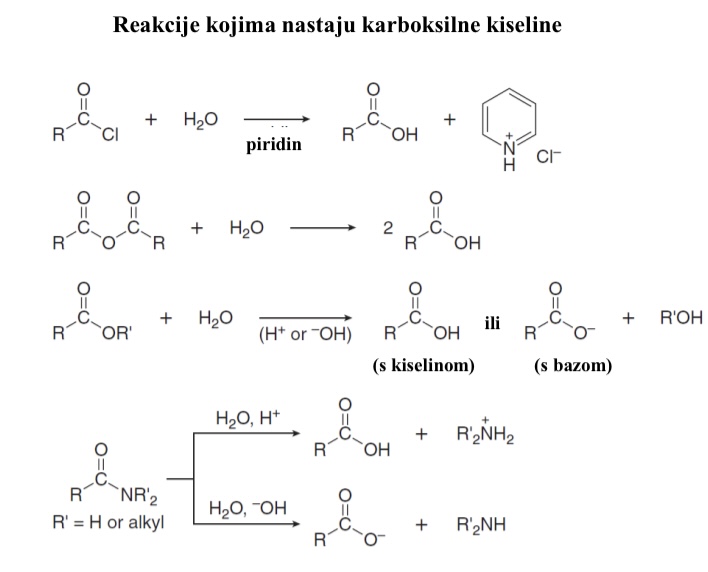
Zasto se karboksilne kiseline ne mogu prevesti u kiselinske kloride uporabom Cl- kao nukleofila
nukleofil koji napada (Cl) slabija baza od izlazne skupine -OH
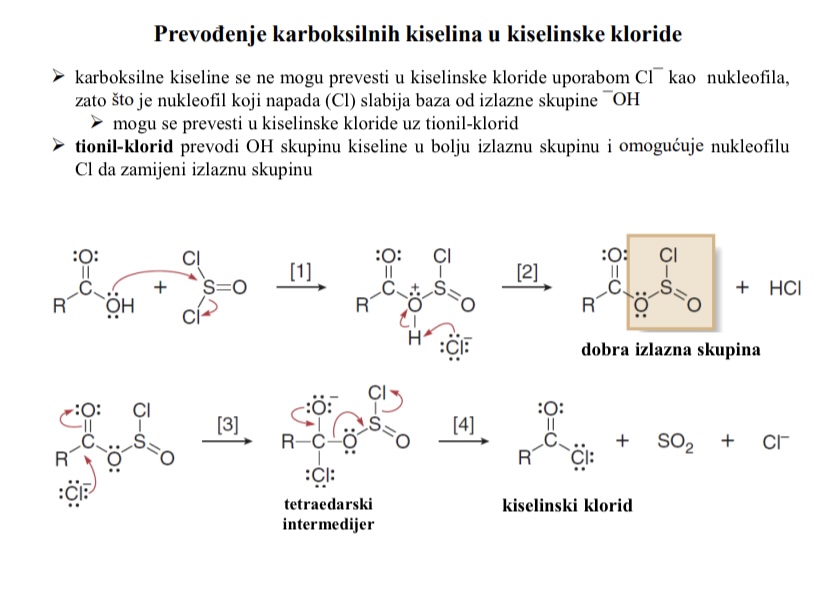
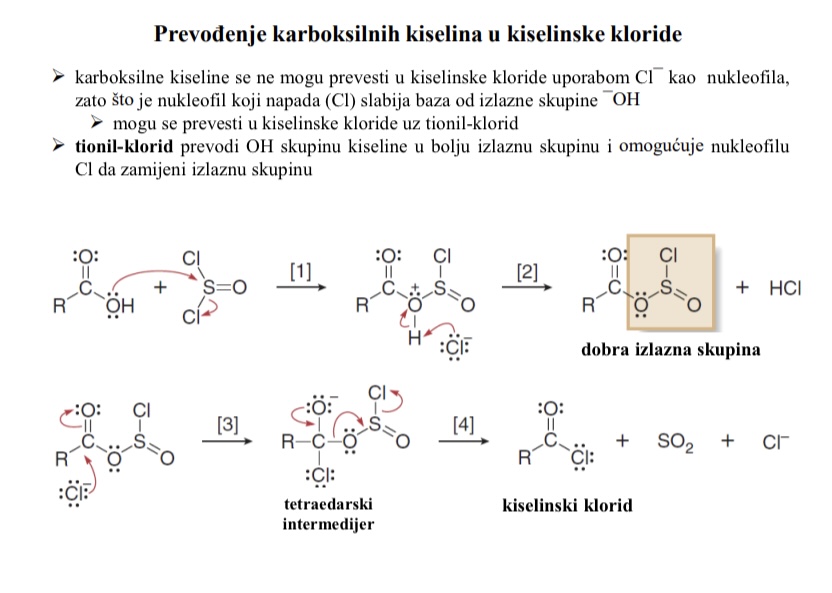
S kojim se reagensom karboksilne kiseline mogu prevesti u kiselinske kloride
Tionil-klorid SOCl2
Prevodi OH skupinu kiseline u bolju izlaznu skupinu i omogucuje nukleofilu Cl da zamijeni izlaznu skupinu
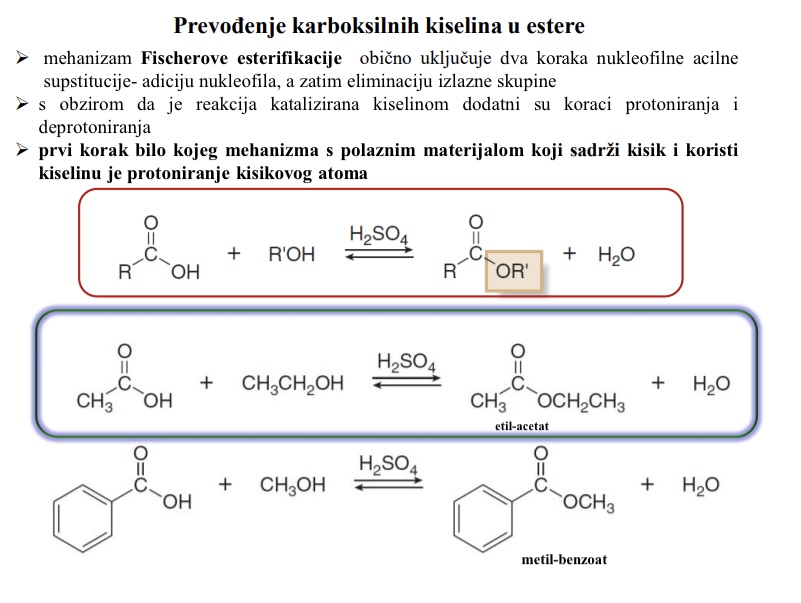
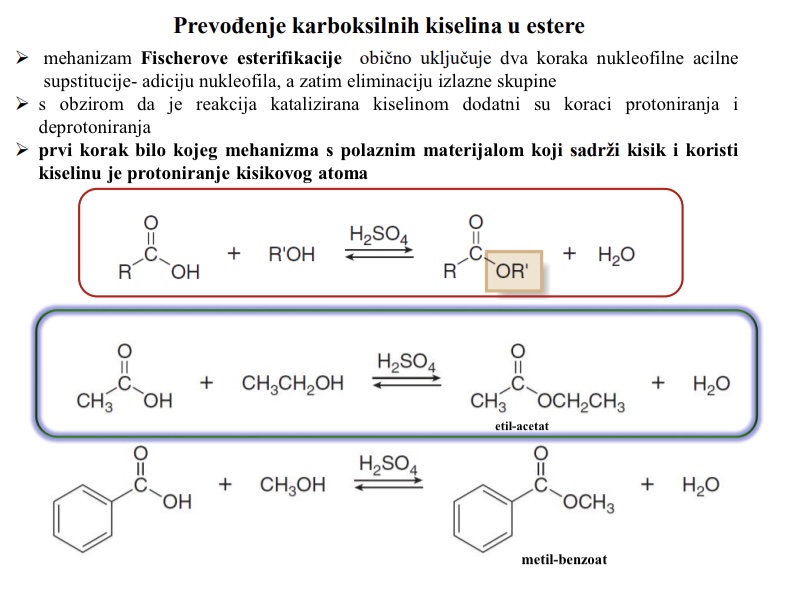
Kojim mehanizmom se karboksilne kiseline prevode u estere
Mehanizam Fischerove esterifikacije
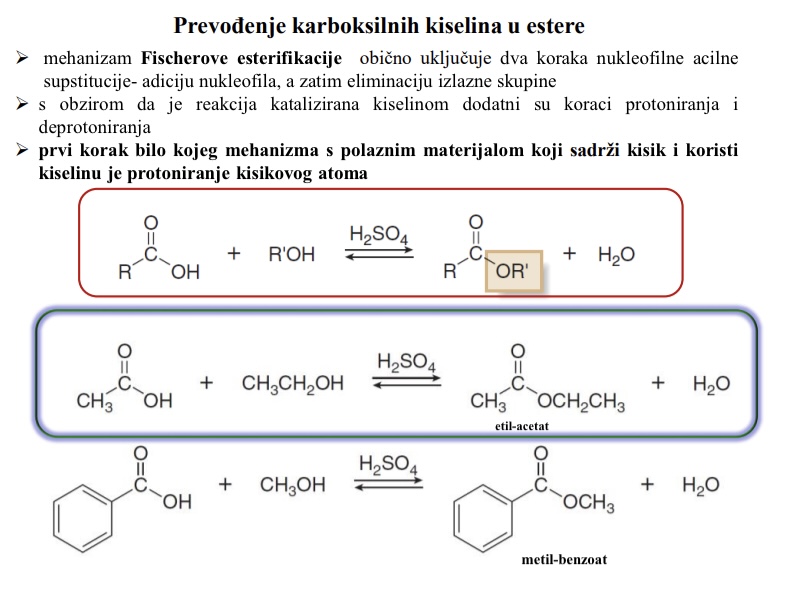
Koje korake obicno ukljucuje mehanizam Fischerove esterifikacije
Ukljucuje dva koraka nukleofilne acilne supstitucije - adiciju nukleofila, a zatim eliminaciju izlazne skupine
S obzirom da je reakcija katalizirana kiselinom dodatni koraci su protoniranje i deprotoniranje
Koji je prvi korak bilo kojeg mehanizma s polaznim materijalom koji sadrzi kisik i koristi kiselinu
Protoniranje kisikovog atoma
Zasto je direktna pretvorba karboksilnih kiselina u amide s NH3 vrlo teska
iako se reaktivniji acilni spoj prevodi u manje reaktivan (stabilniji) - tesko
Problem: karboksilne kiseline su jake organske kiseline i s NH3 aminom bazom reagiraju u kiselo-baznim reakcijama i nastaje amonijeva sol (amonijevi karboksilati) prije nego dode do nukleofilne supstitucije
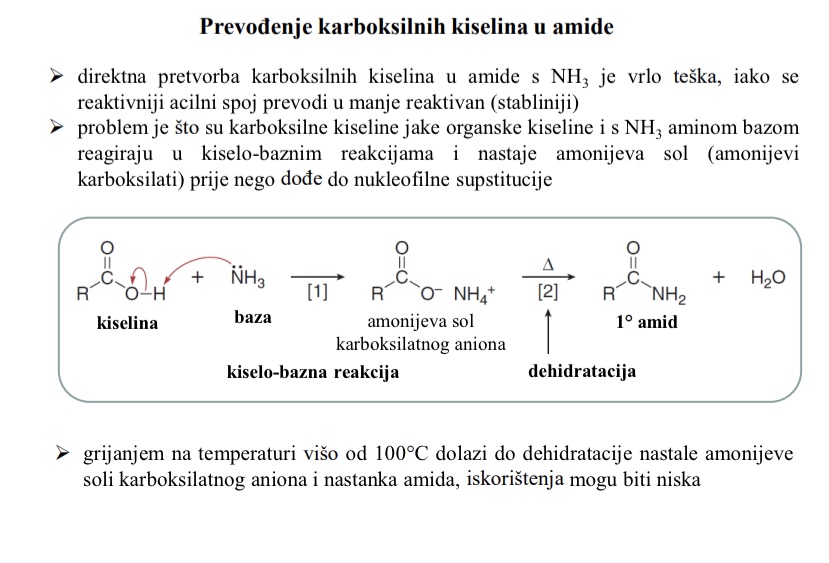
Kako se prevode karboksilne kiseline u amide
grijanjem na temperaturi vise od 100oC dolazi do dehidratacije nastale amonijeve soli karboksilatnog aniona i nastanka amida
Iskoristenja mogu biti niska
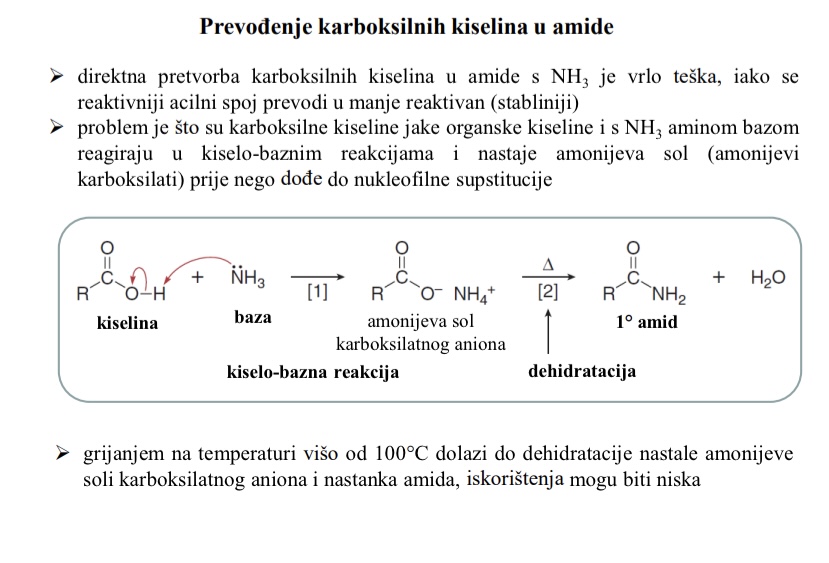
Esteri
najrasprostranjeniji kiselinski derivati
daju miris
nalaze se u biljnim uljima
U industriji se koriste kao otapala
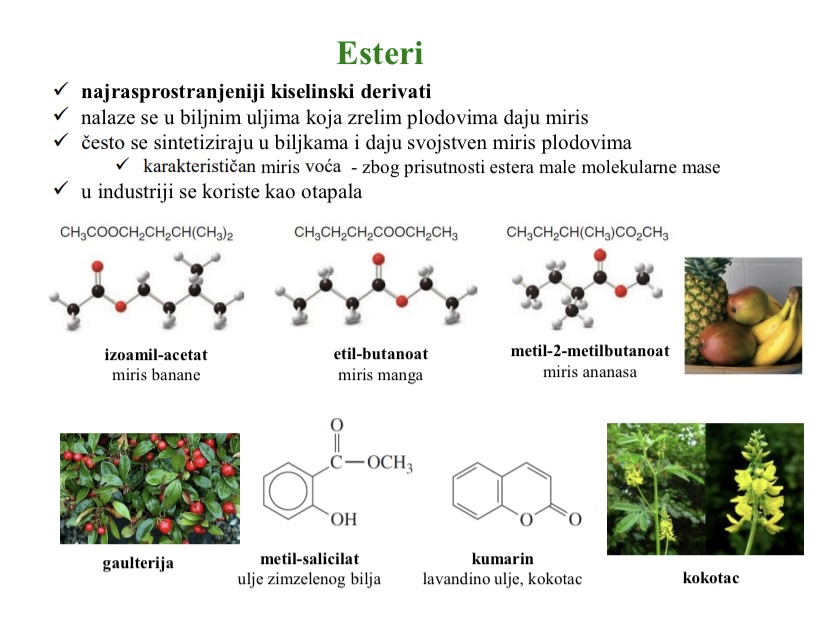
Reakcije kojima nastaju esteri
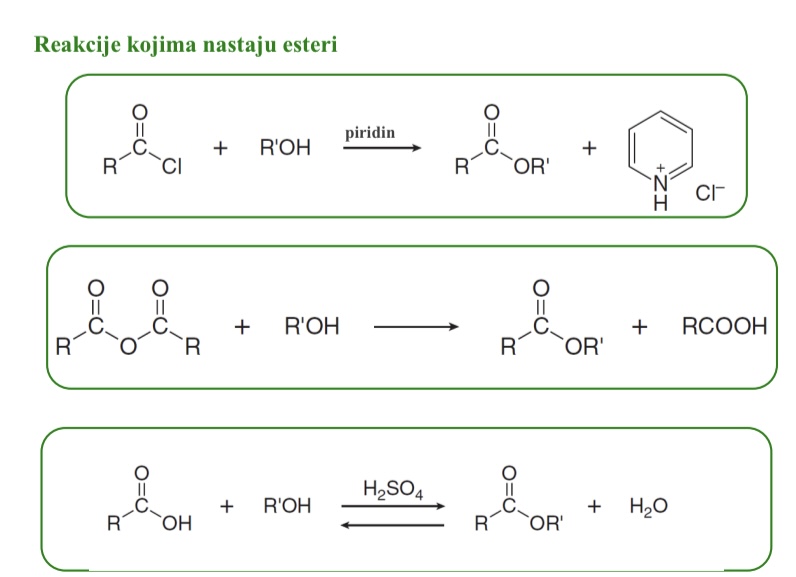
U sto se mogu prevesti esteri
Karboksilne kiseline i amide
Kojom reakcijom iz estera nastaju karboksilne kiseline
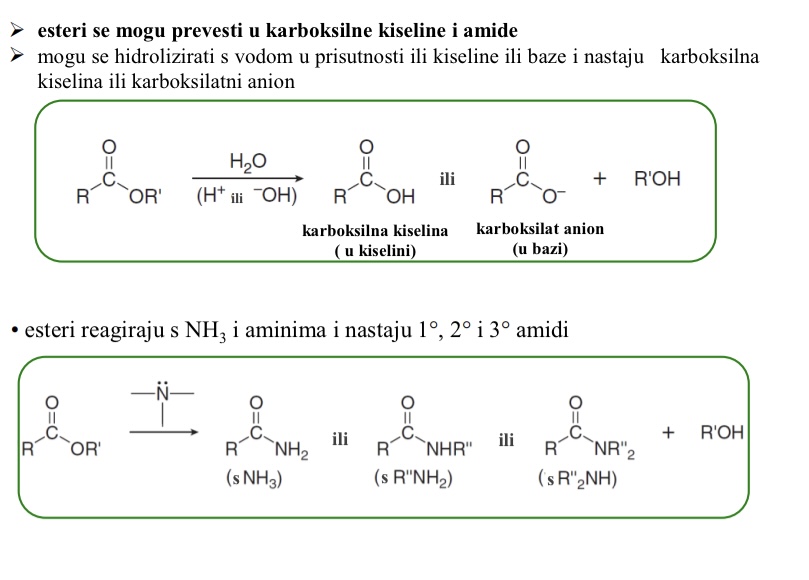
mogu se hidrolizirati s vodom u prisutnosti ili kiseline ili baze i nastaju karboksilna kiselina ili karboksilatni anion
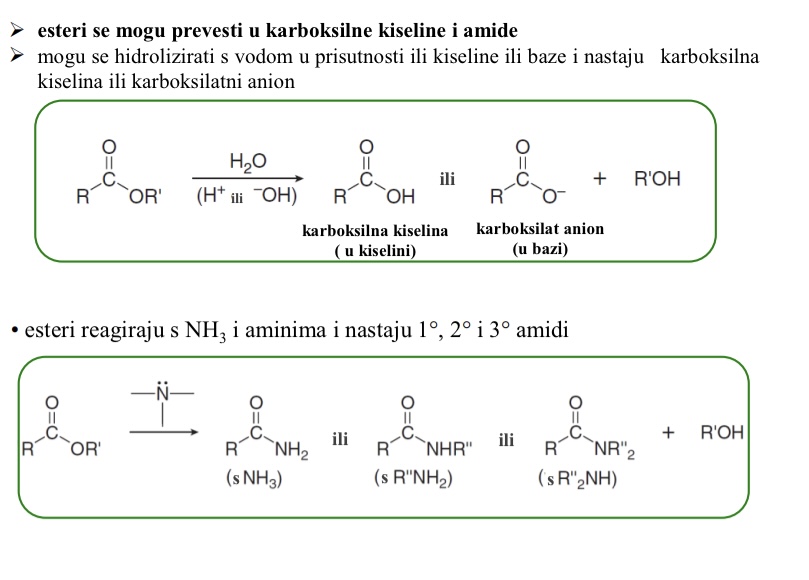
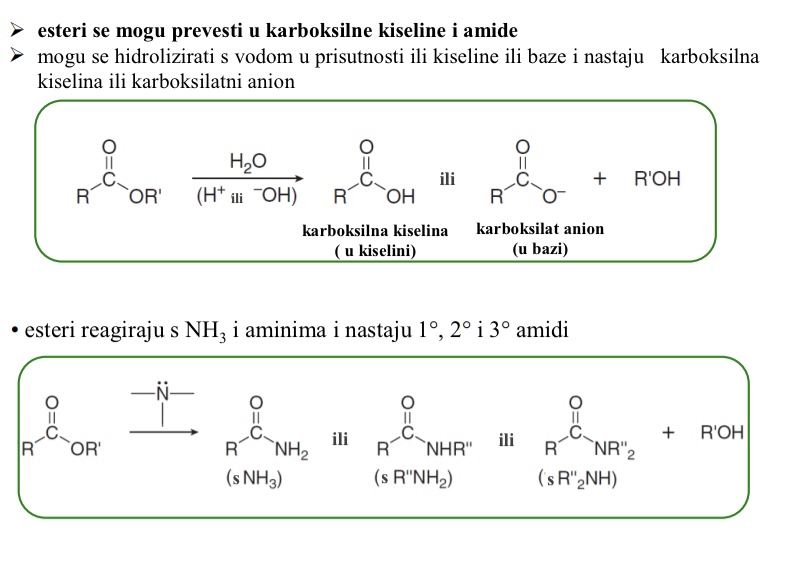
Kojom reakcijom iz estera nastaju amidi
esteri reagiraju s NH3 i aminima i nastaju 1o, 2o i 3o amidi
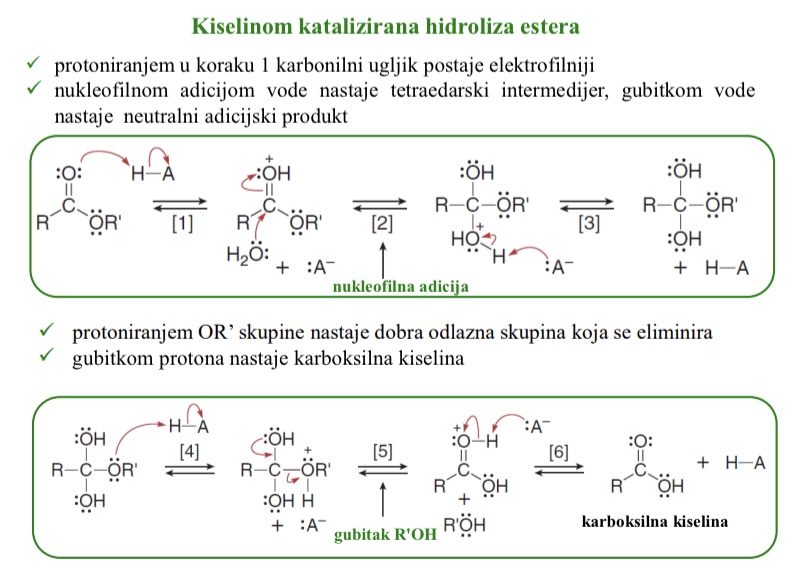
Kiselinom katalizirana hidroliza estera -mehanizam
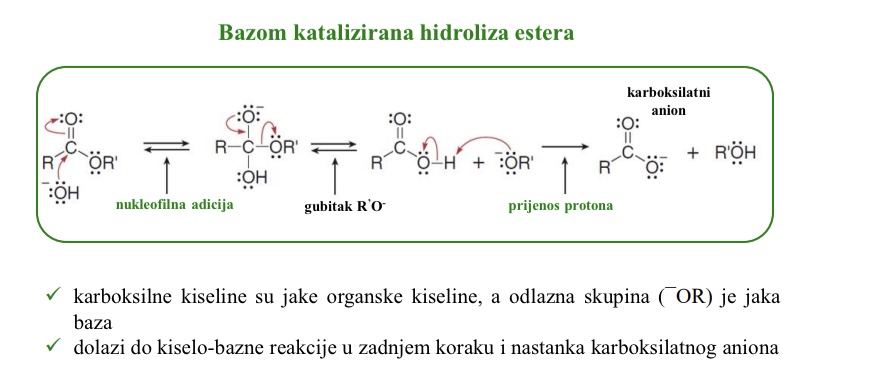
Bazom katalizirana hidroliza estera - mehanizam
Sto su masti i ulja
Esteri trovalentnog alkohola glicerola i visih masnih kiselina s 12-20C atoma
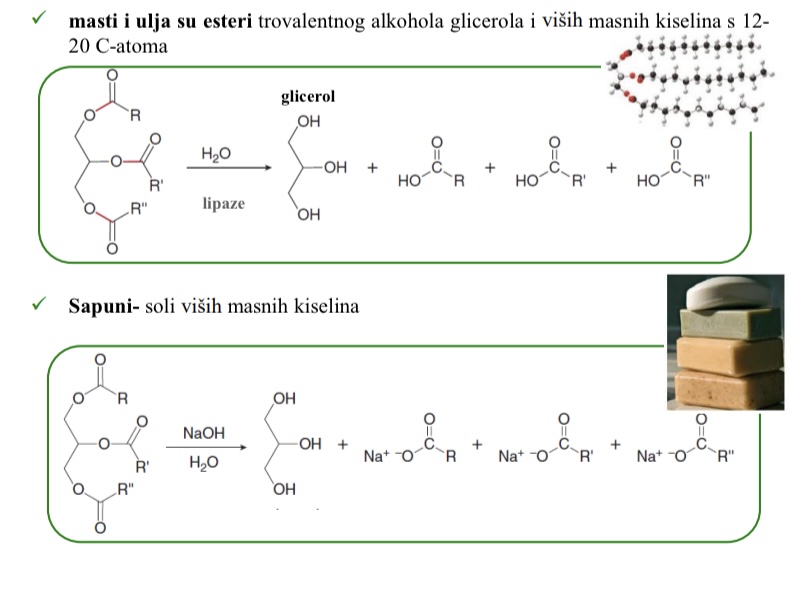
Sto su sapuni
Soli visih masnih kiselina
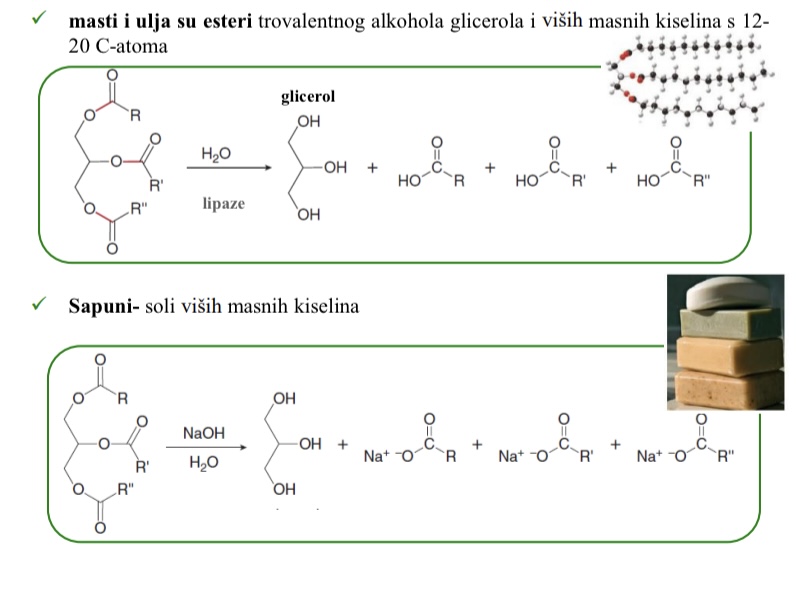
Poliesteri
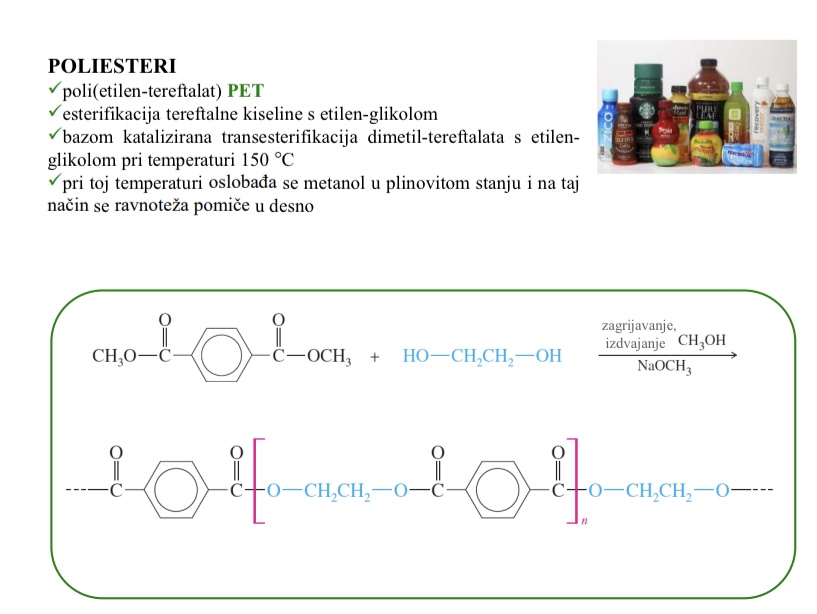
Amidi
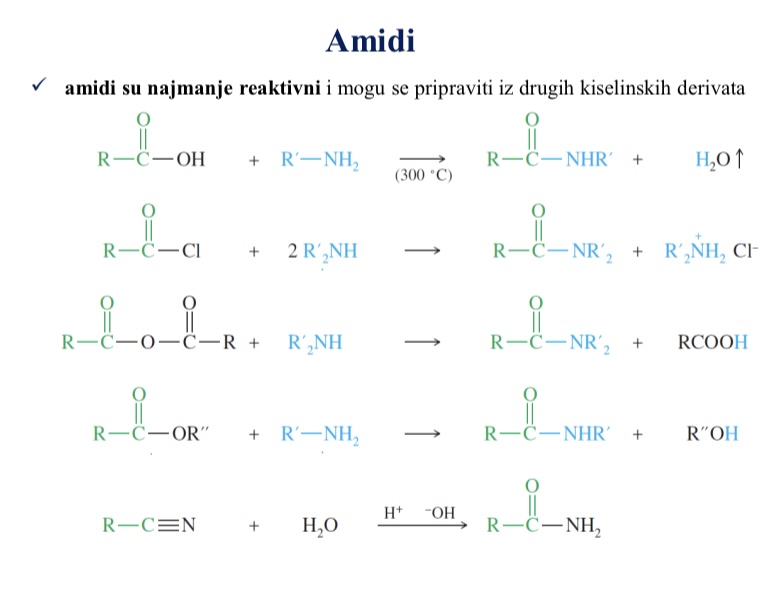
Reakcije kojima nastaju amidi
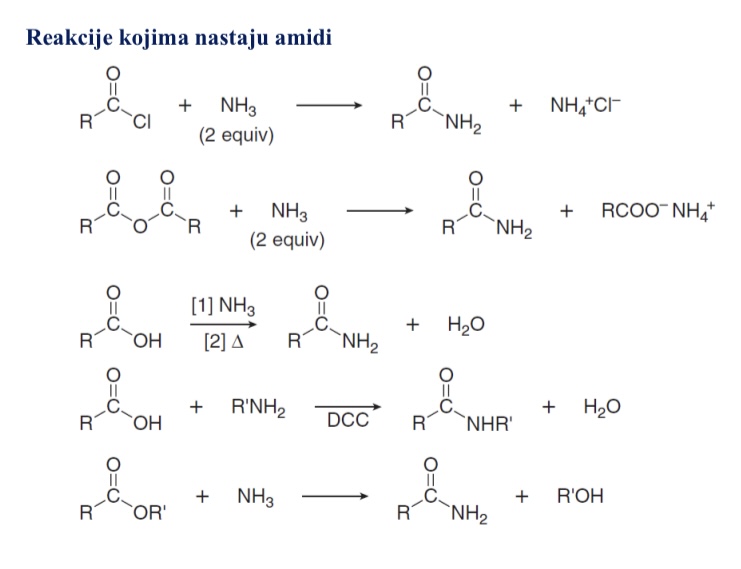
Zasto su amidi najmanje reaktivni
Imaju najslabiju izlaznu skupinu od svih derivata karboksilnih kiselina
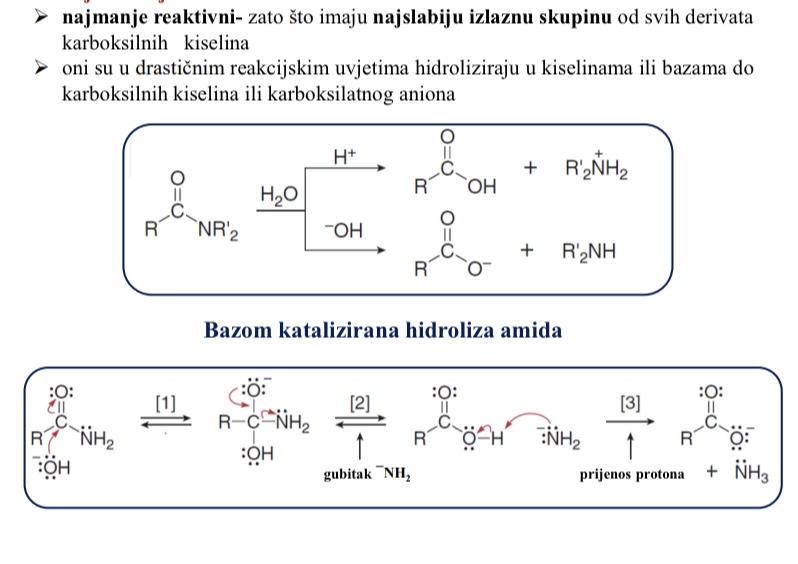
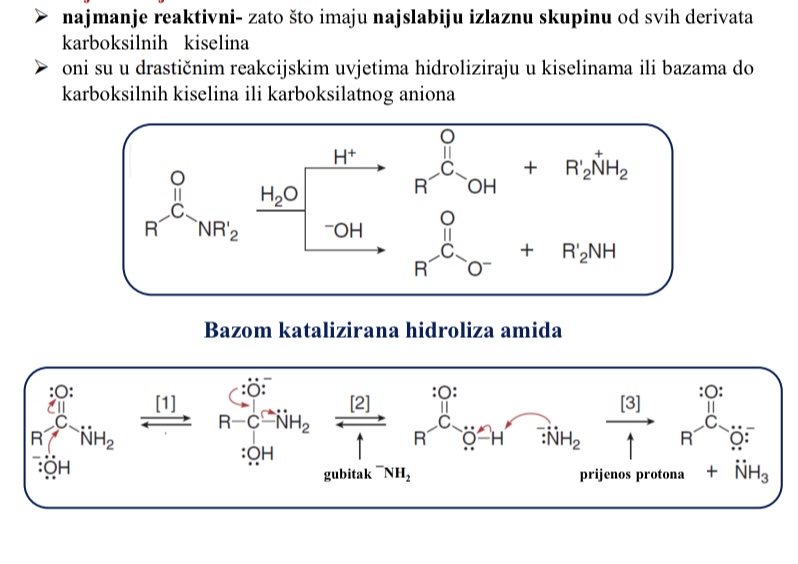
U kakvim se uvjetima amidi hidroliziraju u kiselinama ili bazama do karboksilnih kiselina ili karboksilatnog aniona
Drasticnim
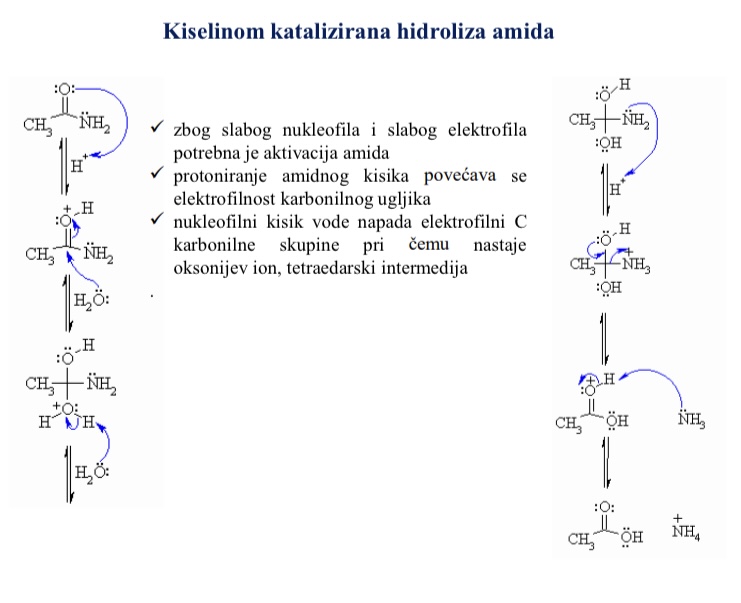
Kiselinom katalizirana hidroliza amida
Redukcija amida
reakcija dobivanja amina

Zasto su amidi vrlo slabe baze u odnosu na amine iako posjeduju nevezni elektronski par na dusikovom atomu
slaba bazicnost posljedica rezonantne strukture amida koji je hibrid dviju rezonancijskih struktura
Protoniranje se ne odvija na dusikovom atomu vec na karbonilnom kisiku
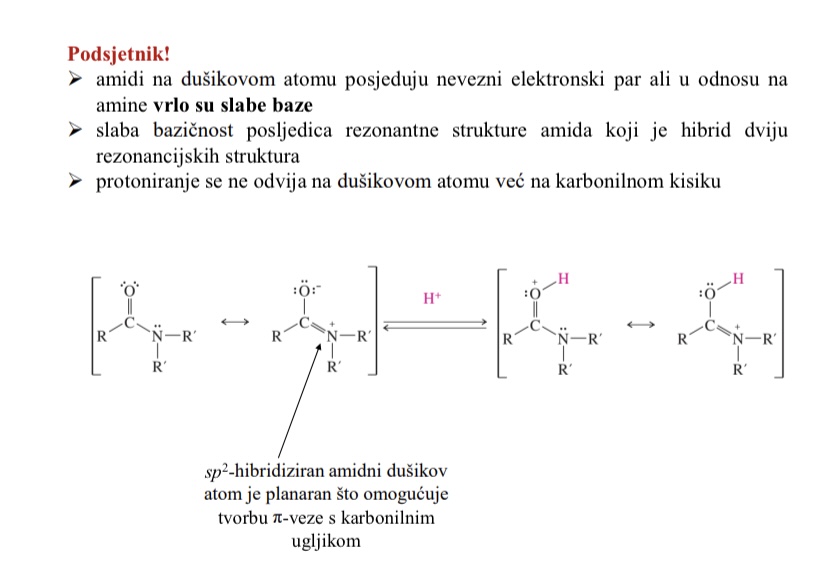
Primjeri amida
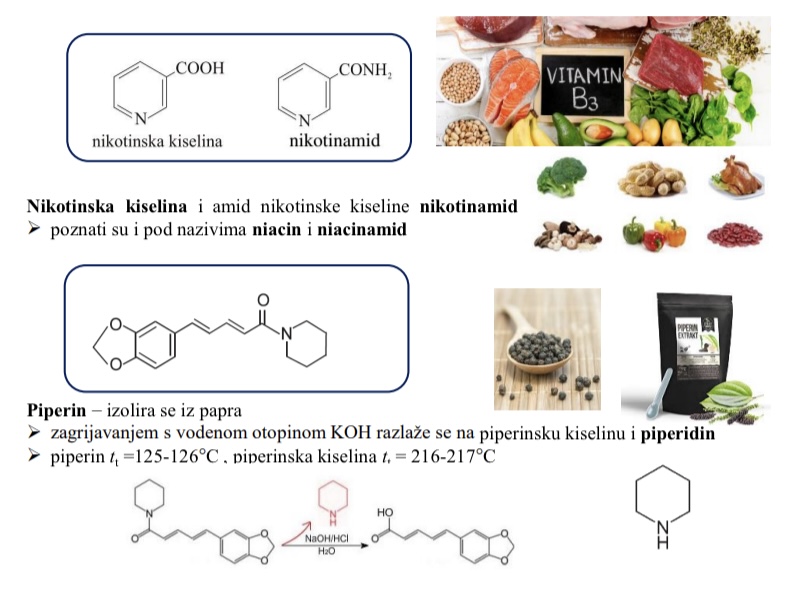
Paracetamol ili acetaminofen
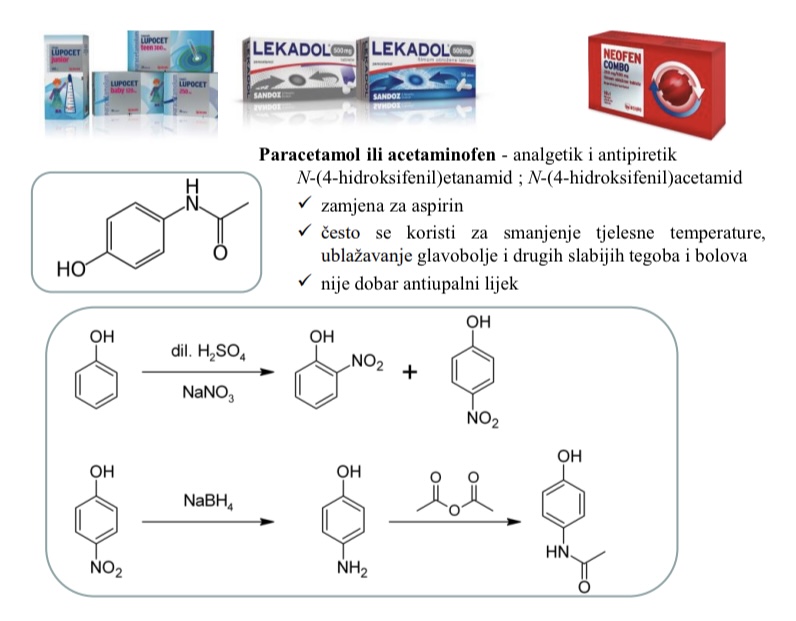
nylon6,6
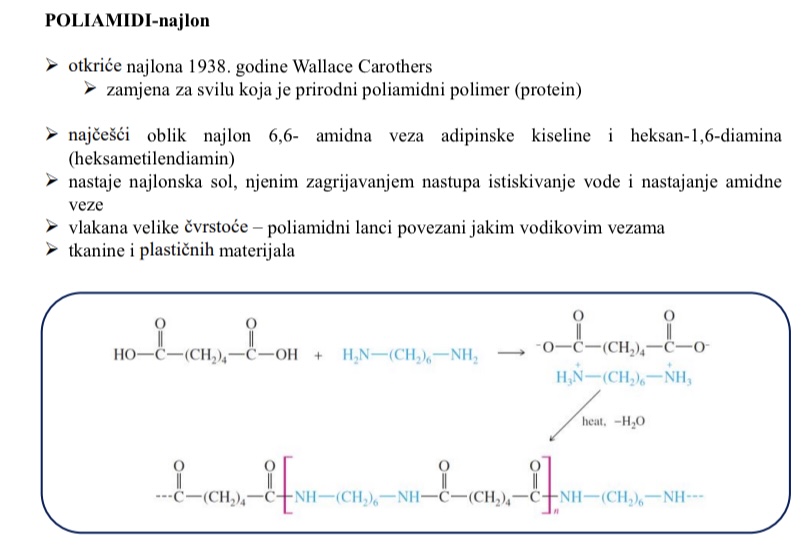
Poliamidi - najlon
Poliamidi - kevlar

Nukleofilna acilna supstitucija pregled