Chemie: Ionenbindungen
0.0(0)
Studied by 3 peopleCard Sorting
1/34
Earn XP
Description and Tags
Bindungstypen, Bildung von Salzen, Verhältnisformeln, Namen der Ionen
Last updated 10:36 PM on 1/1/23
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
35 Terms
1
New cards
Metallbindungen
* zwischen Metallen
* Metall, Legierung
* Beispiel: Na, Fe, NaHg
* Metall, Legierung
* Beispiel: Na, Fe, NaHg
2
New cards
Elektronenpaarbindungen
* zwischen Nichtmetallen
* Überlappung der Elektronenwolken → bindende Elektronenpaare
* in Molekülen
* Beispiele: H2, H2O, CO2
* Überlappung der Elektronenwolken → bindende Elektronenpaare
* in Molekülen
* Beispiele: H2, H2O, CO2
3
New cards
Ionenpaarbindungen
* zwischen Metall und nicht Nichtmetall
* Elektronen vollständig von Metall auf Nichtmetall → geladene Ionen
* in salzartigen Stoffen
* in Salzen
* Beispiele: NaCl, Kl, CaCO3
* Elektronen vollständig von Metall auf Nichtmetall → geladene Ionen
* in salzartigen Stoffen
* in Salzen
* Beispiele: NaCl, Kl, CaCO3
4
New cards
Anion
* negativ geladenes Ion
5
New cards
Kation
* positiv geladenes Ion
* Bei Metallen werden alle Valenzelektronen abgegeben um in einen beständigen Zustand zu kommen → positiv geladene Atomrümpfe
* Bei Metallen werden alle Valenzelektronen abgegeben um in einen beständigen Zustand zu kommen → positiv geladene Atomrümpfe
6
New cards
Anion
* negativ geladenes Ion
* Nichtmetall nehmen so viele Elektronen auf, bis sie die Oktettregel erfüllen
* Nichtmetall nehmen so viele Elektronen auf, bis sie die Oktettregel erfüllen
7
New cards
Atomradius und Ionenradius
* Atomradien sind anders als Ionenradien, da entweder Elektronen aufgenommen oder abgegeben werden
* Anion: grösser als das Atom, da sich die Hülle durch die gegenseitige Abstossung der Elektronen aufbläht.
* Kation: kleiner als das Atom, weil eine Schale weniger
* Anion: grösser als das Atom, da sich die Hülle durch die gegenseitige Abstossung der Elektronen aufbläht.
* Kation: kleiner als das Atom, weil eine Schale weniger
8
New cards
Ionenladung herausfinden
* Metall: Ladung entspricht immer der Hauptgruppennummer, da sie alle Valenzelektronen abgeben, (Magnesium hat 2 VE und gibt diese ab, also gibt es 2 Protonen mehr als Elektronen → Mg2+)
* Nichtmetall: Hauptgruppe - 8, immer soviele, wie aufgenommen werden, (Fluor hat 7 VE und nimmt eins auf, es gibt also ein Elektron mehr als Proton → F-)
* Nichtmetall: Hauptgruppe - 8, immer soviele, wie aufgenommen werden, (Fluor hat 7 VE und nimmt eins auf, es gibt also ein Elektron mehr als Proton → F-)
9
New cards
Bildung von Salzen
* Dabei werden Elektronen vom Metall auf das Nichtmetall übertragen, dass beide Stoffe die Edelgaskonfiguration erreichen.
* Die positiv geladenen und die negativ geladenen Ionen ziehen sich nun an → Ionengitter
* Die positiv geladenen und die negativ geladenen Ionen ziehen sich nun an → Ionengitter
10
New cards
Bildung von Salzen (Schalenmodell)

11
New cards
Bildung von Salzen (Lewis-Formel)

12
New cards
Verhältnisformel
* Die entstandenen Salze sind elektrisch neutral (Ladesumme = 0)
* das kleinste ganzzahlige Verhältnis
* Beispiel: Na+ und Cl- → ==+1==+^^-1^^= 0 → NaCl
* Beispiel: Mg2+ und %%2%% Cl- → ==+2== + %%2%%(^^-1^^) = 0 → MgCl2
* das kleinste ganzzahlige Verhältnis
* Beispiel: Na+ und Cl- → ==+1==+^^-1^^= 0 → NaCl
* Beispiel: Mg2+ und %%2%% Cl- → ==+2== + %%2%%(^^-1^^) = 0 → MgCl2
13
New cards
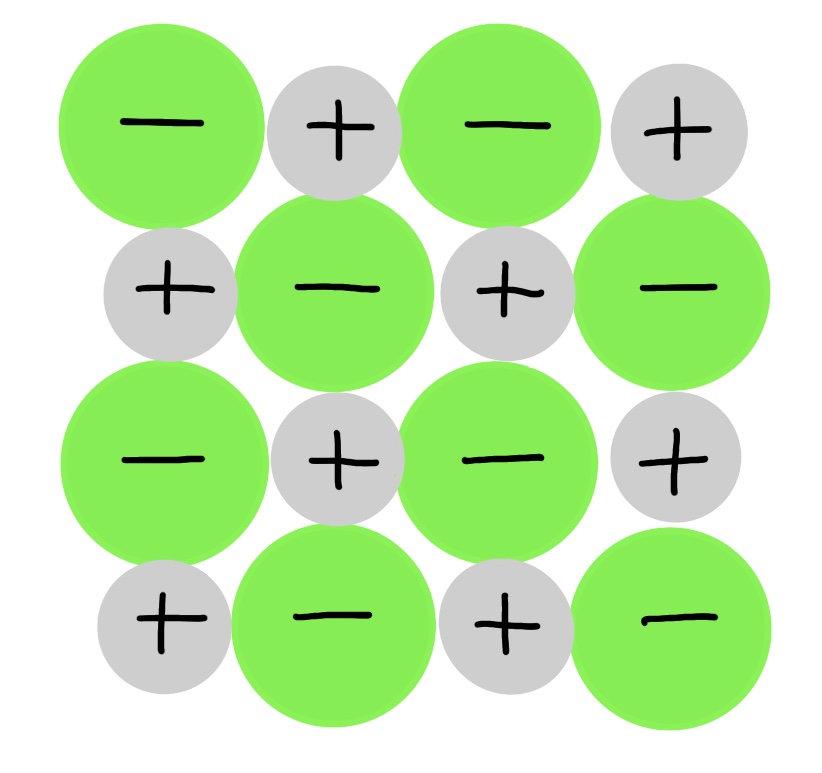
Aufbau der Salze
* Je nach Grösse oder Anzahl der Ionen Form des Ionengitters
* Je nach Verhältnis der Ionenradien von Anion und Kation
* Je nach Verhältnis der Ionenradien von Anion und Kation
14
New cards
Eigenschaften von Salzen (Sprödigkeit)
* Zwischen den verbundenen Kationen und Anionen befinden sich Luft in den Gitterzwischenräumen. Wenn man also bei Salzstruktur daraufschlägt, bricht das Gitter ein durch die Freiräume. Die Gitterstruktur wird zertsört und das Gebilde bricht ein.
15
New cards
Eigenschaften von Salzen (elektrische Leitfähigkeit)
* Sind die Salze in Kristallform vorliegt, sind die Ionen in einem festen Gitter und nicht leitfähig und elektrisch neutral
* Sind sie im Wasser gelöst, gibt es freie geladene Teile → bewegliche Ladungsträger → Stromfluss möglich
* Sind sie im Wasser gelöst, gibt es freie geladene Teile → bewegliche Ladungsträger → Stromfluss möglich
16
New cards
Eigenschaften von Salzen (hohe Schmelzpunkte)
* wegen der starken Anziehungskräfte der Ionen untereinander
* Je höher die Gesamtladung (Q1\*Q2) desto höher die Anziehung
* Je weniger Schalen, desto kleiner der Abstand → höhere Anziehung
* Je höher die Anziehung, desto höher der Schmelzpunkt
* Je höher die Gesamtladung (Q1\*Q2) desto höher die Anziehung
* Je weniger Schalen, desto kleiner der Abstand → höhere Anziehung
* Je höher die Anziehung, desto höher der Schmelzpunkt
17
New cards
Nomenklatur (Hauptgruppenelemente)(einatomig)
Name Metall + Name Nichtmetall + id
18
New cards
O@@2-@@
Oxid
19
New cards
S@@2-@@
Sulfid
20
New cards
N@@3-@@
Nitrid
21
New cards
P@@3-@@
Phosphid
22
New cards
H@@-@@
Hydrid
23
New cards
C@@4-@@
Carbid
24
New cards
Nomenklatur (Nebengruppenmetalle)(einatomig)
Name Metall (inkl. Oxidationsstufe) + Name Nichtmetall + id
25
New cards
Ammonium-Ion
NH4@@+@@
26
New cards
Hydroxid-Ion
OH@@-@@
27
New cards
Phosphat-Ion
PO4@@3-@@
28
New cards
Hydrogenphosphat-Ion
HPO4@@2-@@
29
New cards
Dihydrogenphophat-Ion
H2PO4@@-@@
30
New cards
Sulfat-Ion
SO4@@2-@@
31
New cards
Hydrogensulfat-Ion
HSO4@@-@@
32
New cards
Carbonat-Ion
CO3@@2-@@
33
New cards
Hydrogencarbonat-Ion
HCO3@@-@@
34
New cards
Nitrat-Ion
NO3@@-@@
35
New cards
Nomenklatur (mehratomige Ionen)
Name Kation + Name Anion