équilibre acido basique
1/19
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
20 Terms
définition d’un acide:
= espèce chimique qui, lorsqu'elle se trouve en solution aqueuse, peut céder un ou plusieurs protons (ion hydrogène H+).
Si l'on note AH la formule de l'acide et A- la formule de l'espèce qui a perdu un proton H+, alors la demi équation de réaction s'écrit de la façon suivante :
AH | A- + H+ |
définition d une base
= espèce chimique qui peut, lorsqu'elle se trouve en solution aqueuse, capter un ou plusieurs protons.
Si l'on note B- la base en question, et BH l'espèce qui se forme après avoir capté le proton H+, alors cette réaction peut aussi être décrite par une demi équation se
présentant sous la forme :
B- + H+ | BH |
le PH
permet de mesurer l’activité d un ion hydrogène dans une solution (n a pas d ‘unité)
les tampons
= substances qui, quand elles sont présentes dans une solution, maintiennent celle ci à un pH relativement constant, quand un acide ou une base y sont ajoutés
=mélange acide fort-base faible ou base forte-acide faible
base connue
bicarbonate
acide connu
CO2
tampon extracellulaire
neutralisent les acides en dehors des cellules et les véhiculent vers les organes responsables de leur élimination
Le bicarbonate est le principal tampon extra-cellulaire :
- Sa concentration est élevée
- Système très efficace : il ne se sature pas
- Dans le corps humain, ce système de tampon est dit « ouvert », c’est-à-dire que l’acide généré est éliminé par la respiration , et le bicarbonate régénéré par le rein.
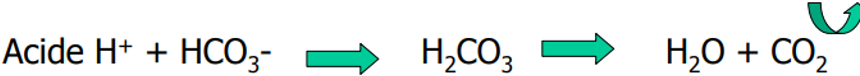
tampons intracellulaires;
neutralisent les acides à l’intérieur des cellules
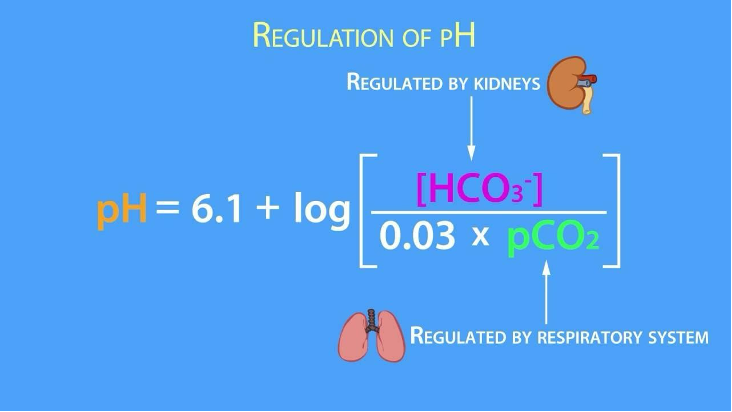
équation d’Henderson - Hasselbach
permet de déterminer le pH
Ainsi, le pH varie quand le rapport entre PCO 2 et HCO3 - est modifié, c’est-à-dire :
Quand il y a une modification primitive de la concentration des ions HCO3 - . Il y a alors alcalose ou acidose métabolique
Quand il y a une modification primitive de la PCO2. Il y a alors alcalose ou acidose respiratoire
role de la ventilation
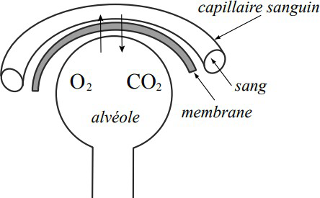
La concentration de CO2 est régulée par variations du volume courant et de la fréquence respiratoire (ventilation-minute).
Le CO2 présent dans les alvéoles quitte l'organisme par les voies aériennes, à chaque respiration.
La PCO2 est fonction de la production tissulaire de CO2 et de son élimination alvéolaire
La ventilation permet une défense semi-retardée : contrairement au processus de tamponnement chimique, qui est immédiat, la régulation pulmonaire se produit au bout de quelques minutes à quelques heures.
PCO2 = ??
capnie
les chémorecepteurs périphériques
Sont situés au niveau des carotides et de l'aorte formant les glomus carotidiens et aortiques.
Sensibles à la variation de la PaO2, PCO2 et du PH
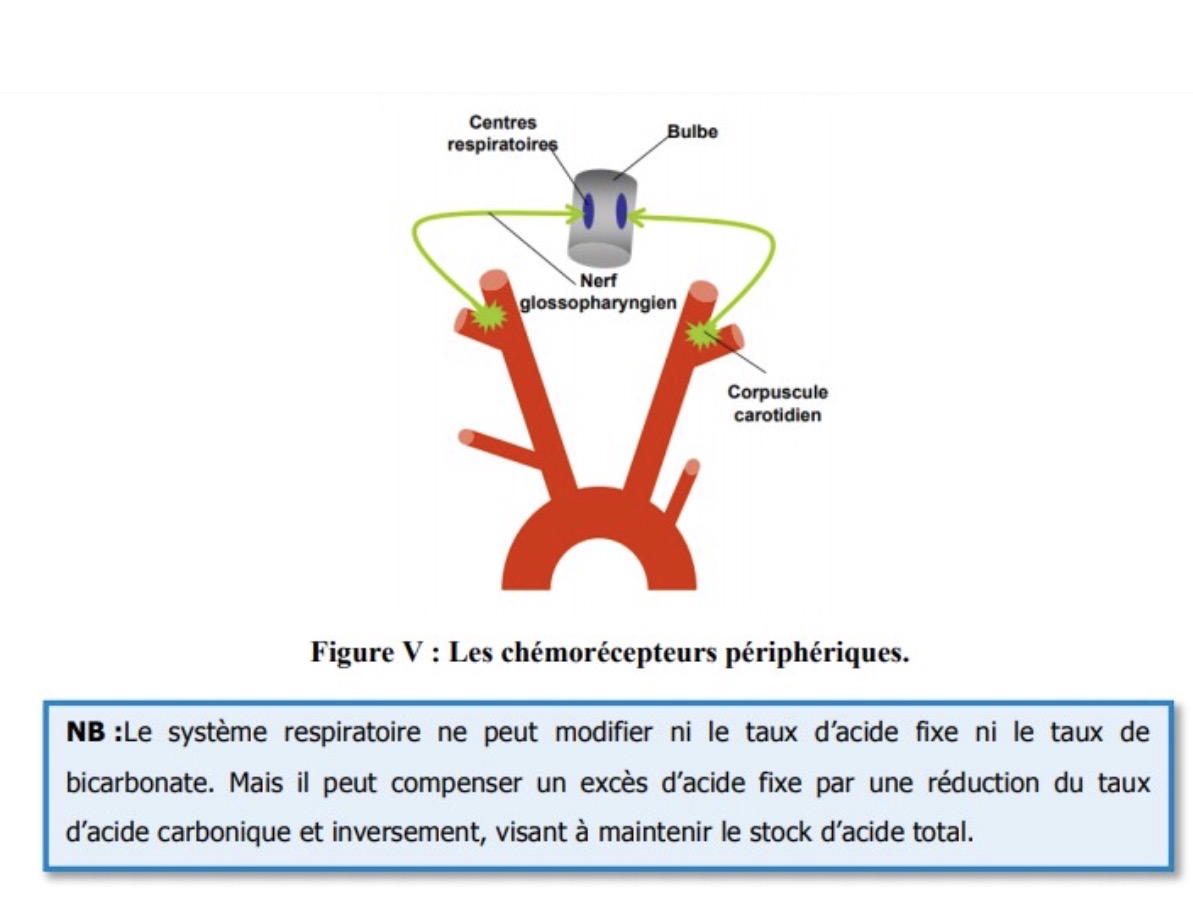
les chémorécepeturs détectent la variation du Ph: PH trop bas=
PH trop bas = acidose respiratoire= charge acide trop élevée → objectif réduire la charge acide => envoyer signal au cerveau => cerveau ordonne aux poumons (et autres effecteurs de la respirations) de fonctionner +++ => hyperventilation => réduction du taux de CO2 dans le sang = HYPOCAPNIE = COMPENSATION RESPIRATOIRE DE L’ACIDOSE
hypoventilation
BPCO
dépression respiratoire
les chémorécepeturs détectent la variation du Ph: PH trop élevé=
PH trop élevé = alcalose respiratoire= charge acide trop basse →objectif augmenter la charge acide → envoyer signal au cerveau => cerveau ordonne aux poumons (et autres effecteurs de la respirations) de fonctionner MOINS pour garder un maximum de charge acide (ICI LE CO2) → HYPOventilation → augmentation du taux de CO2 dans le sang = HYPERCAPNIE = COMPENSATION RESPIRATOIRE DE L’ALCALOSE
crise d’angoisse
hyperventilation
hypoxie
role du rein
Les reins prennent en charge les 25% de compensation que les poumons n'ont pas effectuée.
Le rôle du rein = maintenir constante la bicarbonatémie via
La réabsorption des bicarbonates , librement filtrés ( car non lié aux protéines) au niveau du glomérule : c’est une fonction des parties proximales du tubule rénal = tube contourné proximal.
La régénération des bicarbonates consommés ce qui revient à excréter la charge acide fixe. C’est une fonction des parties distales du néphron (canal collecteur).
→ Les ions HCO3- sont majoritairement réabsorbés au niveau du tubule proximal. Les ions H+ sont excrétés au niveau du canal collecteur.
au niveau du rein: si pH trop bas:
PH trop bas = acidose métabolique = charge acide trop élevée = > objectif réduire la charge acide ou d’augmenter la charge basique => ↑réabsorption de bicarbonate + ↑ sécrétion acide
diarrhée
acidocétose diabétique
acidose lactique
insuffisance rénale
au niveau du rein: si pH trop haut
PH trop élevé = alcalose métabolique= charge acide trop basse → objectif augmenter la charge acide ou diminuer la charge basique → ↓réabsorption acide + ↓ sécrétion acide (sous forme de NH4+)
vomissements
diurétiques
perte d’acide gastrique
valeurs normales des variables de l’équilibre acido basique (apprend js le pH)
Pour PaCO2
PaCO₂ normale ≈ 40 mmHg
PaCO₂ > 40 mmHg → tendance acidifiante
PaCO₂ < 40 mmHg → tendance alcalinisante
Et pour le HCO₃⁻ :
HCO₃⁻ normal ≈ 24 mmol/L
HCO₃⁻ < 24 → tendance acidifiante
HCO₃⁻ > 24 → tendance alcalinisante
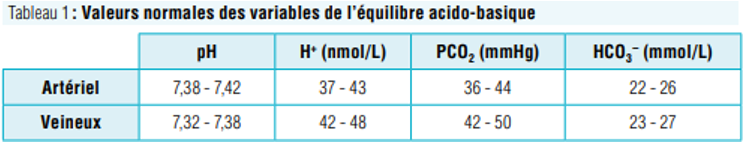
acidose ou alcalose?
étapes pour déterminer alcalose/acidose
Etape 1 = dire si le PH est normal/acide /alcalin
Etape 2 = on évalue si le poumon et le rein réagissent comme on s’attenderait à ce qu’ils réagissent pour compenser c’est-à-dire :
Acidose => on s’attend à ce que :
le poumon hyperventille (hypocapnie)
que le rein augmente la réabsorption de bicarbonates (donc ↑[HCO3-])
Alcalose=> on s’attend à ce que :
le poumon hypoventille (hypercapnie)
que le rein diminue la réabsorption de bicarbonates (donc ↓ [HCO3-])
Etape 3 : quand on voit que le résultat de la réaction du rein/poumon est inadaptée on le pointe du doigt :
EXEMPLE : poumon avec PCO2 trop élevée alors qu’on a une acidose => il y a un problème au niveau du poumon = acidose respiratoire
Etape 4 : donc soit c’est le poumon le problème = acidose/alcalose RESPIRATOIRE
Soit c’est le rein le problème = acidose /alcalose METABOLIQUE
Etape 5 : dire si c’est compensé ou pas : pour dire que c’est compensé (= PH soit normalisé→ c’est pour ça qu’une anomalie de la PCO2 / bicarbonates peut poser l’appellation acidose/alcalose sans anomalie du PH car au final c’est juste que ça a été compensé)
Quand le PH n’est que partiellement corrigé alors que le rein/poumon s’est adapté => on parle de partiellement compensé