Cali
1/48
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
49 Terms
ERCP w ciąży bezpieczeństwo

EGD w ciąży bezpieczeństwo

wzór laboratoryjny cholestazy ciężarnych

cholestazy ciężarnych tableka z ryzykiem
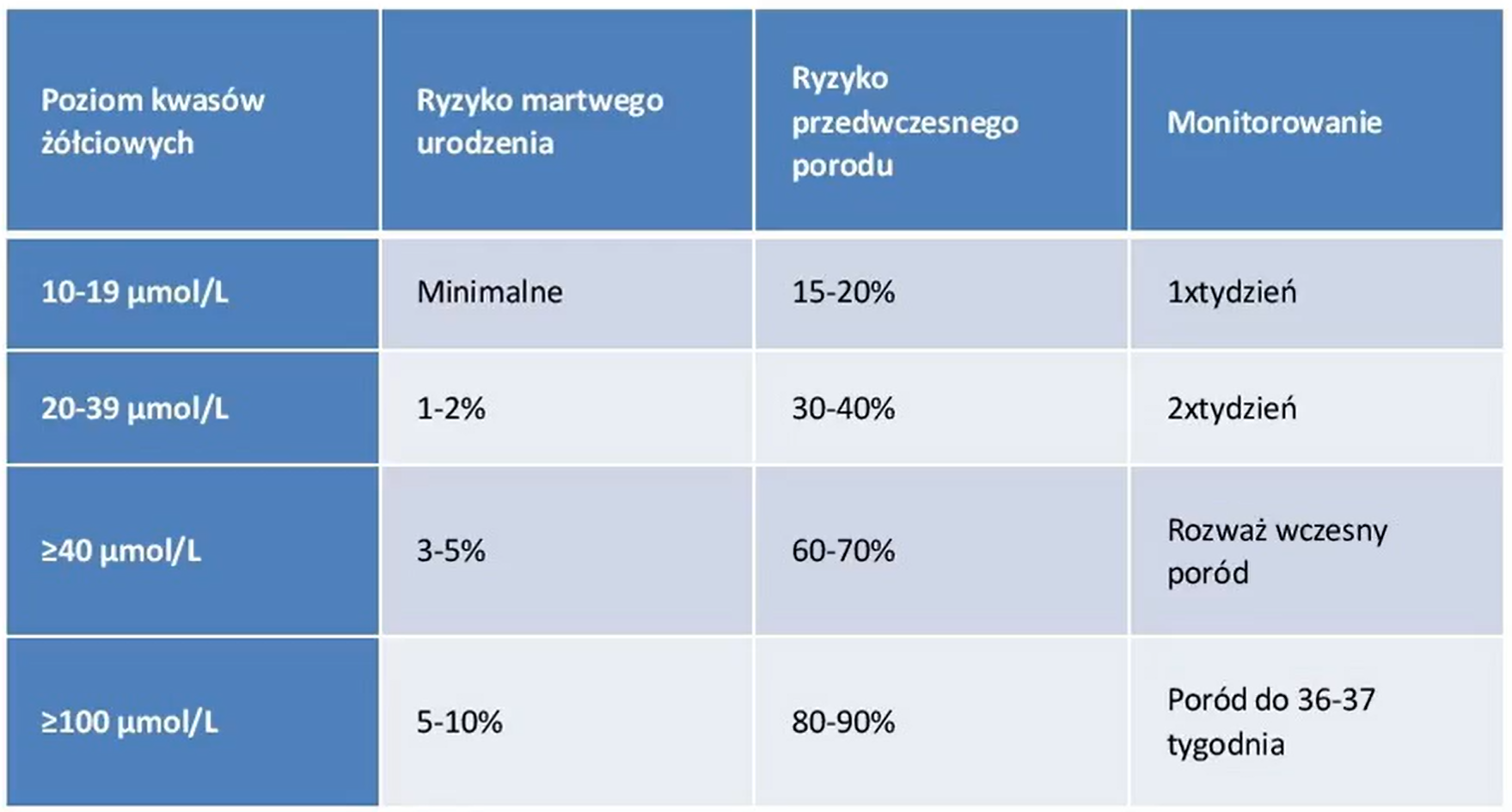
cholestazy ciężarnych leczenie

help rozwinięcie skrótu

help stopnie cieżkości
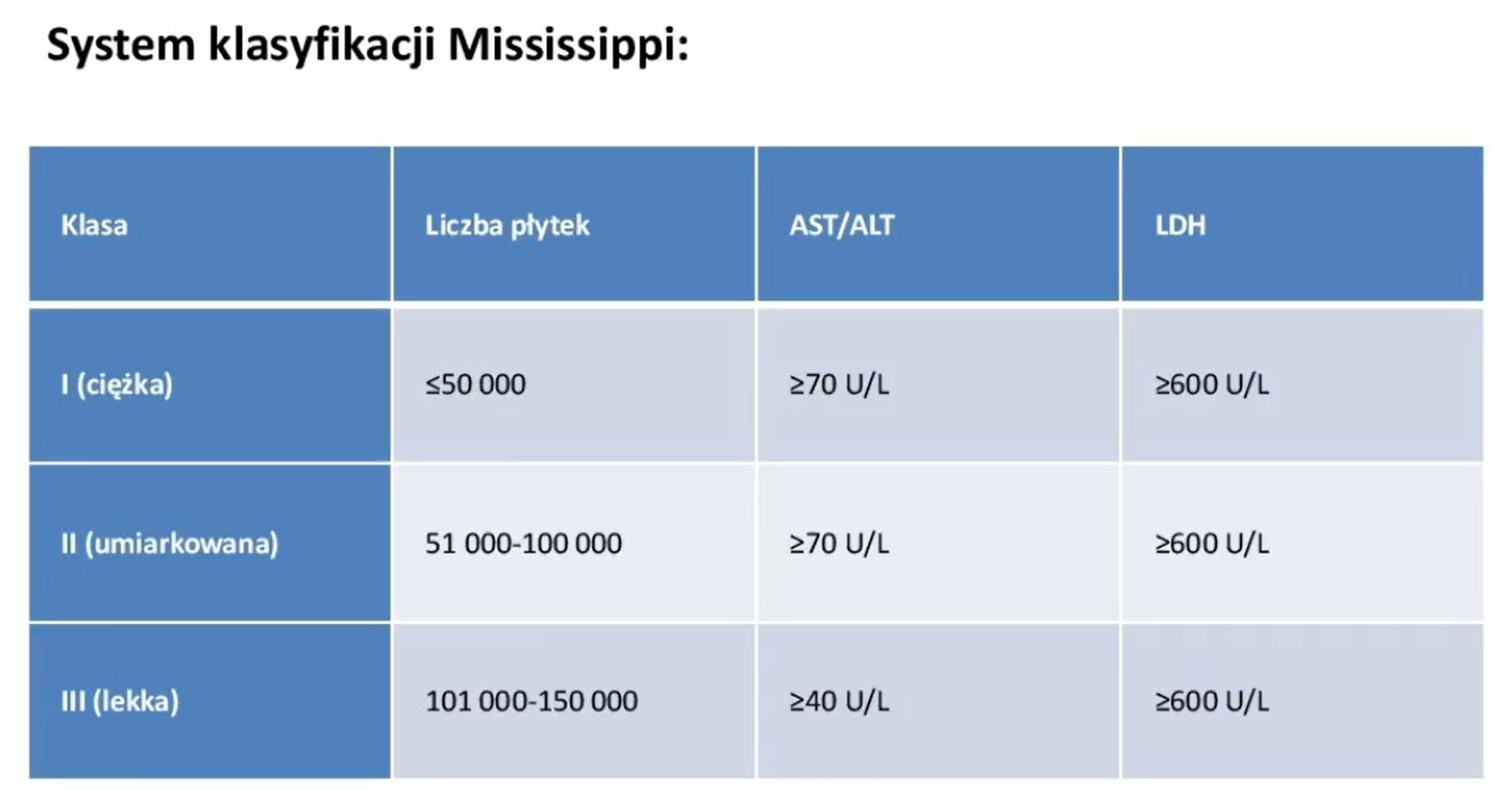
help objawy

help postępowanie

aflp definicja

aflp patogeneza

aflp kryteria swansena
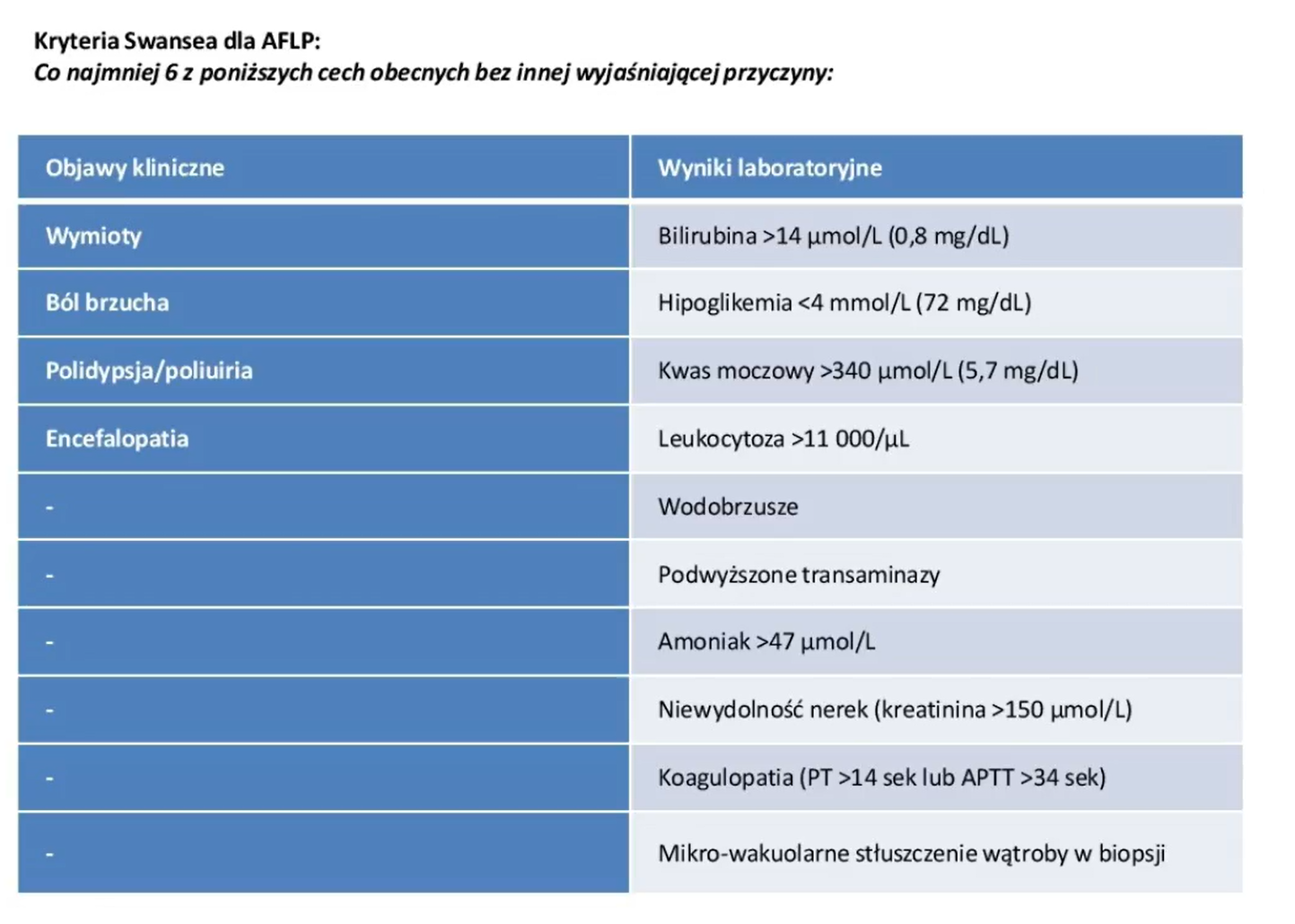
aflp postępowanie

tabelka róznicująca icp aflp hellp
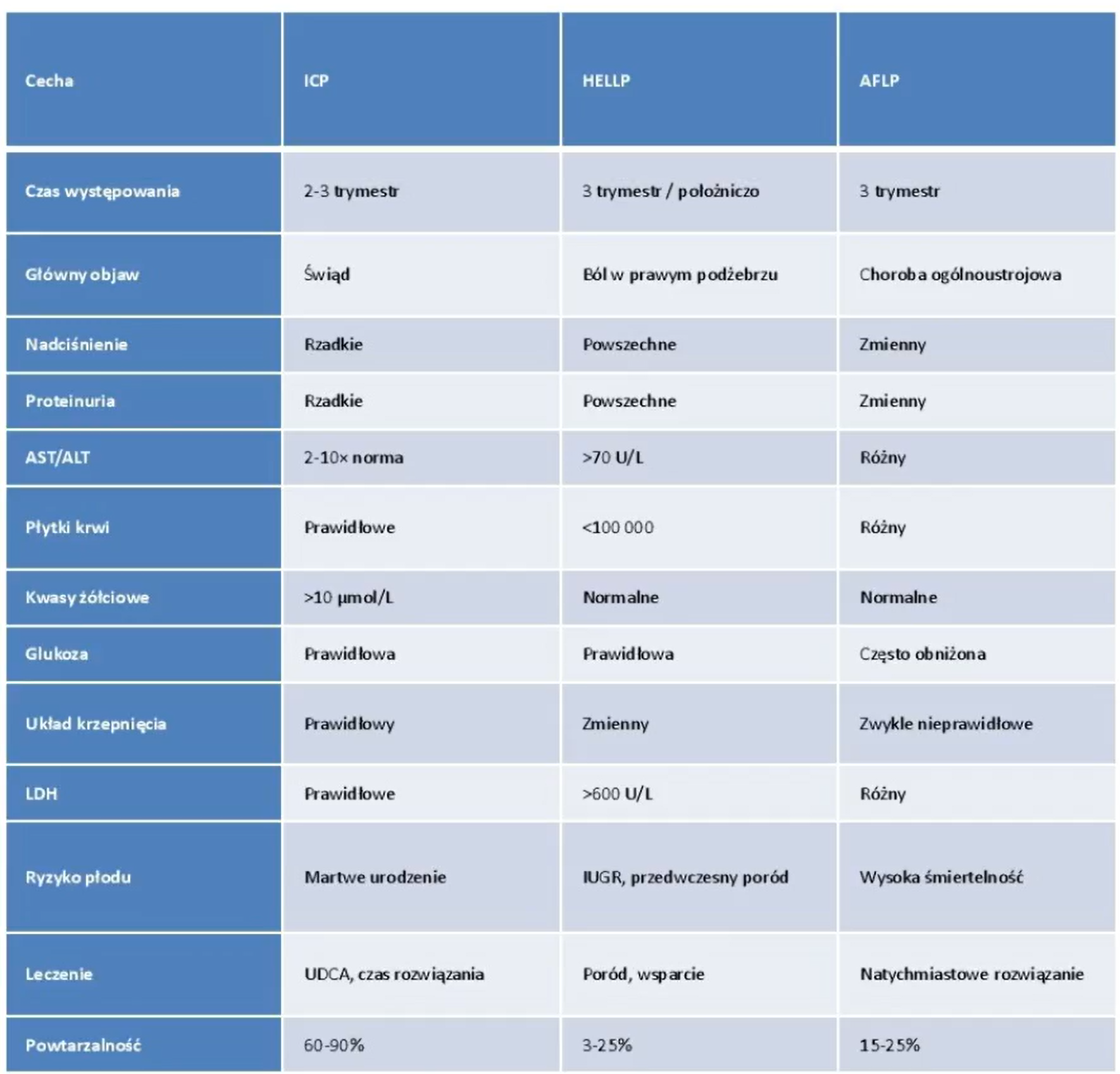
niepowściągliwe wymioty ciężarnych - definicja

niepowściągliwe wymioty ciężarnych -odchylenia w badaniach

niepowściągliwe wymioty ciężarnych - leczenie

Stan przedrzucawkowy rozpoznaje się (wg ISSHP),
jeśli występuje NT wywołane ciążą, do którego rozwoju doszło w ≥20. tyg. ciąży oraz któremu towarzyszy ≥1 z poniższych:
1) białkomocz
2) ostre uszkodzenie nerek (stężenie kreatyniny w surowicy ≥90 μmol/l [1 mg/dl])
3) powikłania wątrobowe (zwiększona aktywność AST lub ALT >40 IU/l), niekiedy z dolegliwościami bólowymi w prawym górnym kwadrancie lub nadbrzuszu
4) powikłania hematologiczne – liczba płytek krwi <150 000/μl, zespół rozsianego krzepnięcia wewnątrznaczyniowego, hemoliza
5) powikłania neurologiczne – np. rzucawka, zaburzenia psychiczne, zaniewidzenie, udar mózgu, skurcz kloniczny, silny ból głowy, utrzymujące się mroczki
6) objawy zagrożenia dobrostanu płodu – wewnątrzmaciczne opóźnienie wzrastania (IUGR), nieprawidłowy przepływ w tętnicy pępowinowej w badaniu doplerowskim lub obumarcie płodu.
Ryzankizumab
Jest to humanizowane przeciwciało monoklonalne IgG1 skierowane przeciwko podjednostce p19 interleukiny 23 (IL-23).
Tofacytynib
hamuje aktywność kinaz JAK1, JAK2, JAK3
reumatologiczne + tylko Wrzodziejące zapalenie jelita grubego
U pacjentów leczonych tofacytynibem zgłaszano przypadki żylnej choroby zakrzepowo-zatorowej o ciężkim przebiegu, w tym zatorowości płucnej
U pacjentów przyjmujących tofacytynib obserwowano ciężkie niepożądane zdarzenia sercowo-naczyniowe.
większą częstość występowania nowotworów złośliwych, zwłaszcza niemelanocytowego nowotworu skóry, raka płuca i chłoniaka, w porównaniu do stosowania z inhibitorami TNF.
U osób leczonych tofacytynibem obserwowano zwiększenie stężenia lipidów we krwi. Maksymalny wpływ obserwowano zazwyczaj w ciągu 6 tyg.
Wpływ na limfopenię i neutropenię oraz ze zmniejszenie stężenia hemoglobiny.
Nie zaleca się rozpoczynania leczenia u osób, u których bezwzględna liczba limfocytów wynosi <750/µl.
Nie zaleca się rozpoczynania leczenia u osób, u których bezwzględna liczba neutrofili <1000/µl (u dzieci <1200/µl).
Nie zaleca się rozpoczynania leczenia u osób, u których stężenie hemoglobiny <9 g/dl (u dzieci <10 g/dl).
ulega metabolizmowi przy udziale CYP3A4
10 mg 2 ×/d przez 8 tyg. (leczenie indukujące), następnie 5 mg 2 ×/d
oportunistycznych zakażeń przewodu pokarmowego Najczęstszymi przyczynami są
mykobakterie (przede wszystkim Mycobacterium avium complex – MAC),
kryptosporidia,
wirus cytomegalii
i mikrosporidia
Biegunka, u chorych na AIDS diagnostyka ; w tym zależna od poziomów cd4+ i ew. gorączki
Do ustalenia przyczyny przewlekłej biegunki konieczne jest ≥3‑krotne badanie kału (posiewy, badania wirusologiczne i parazytologiczne).
U chorego ze znacznym niedoborem odporności (limfocyty CD4+ <200/µl) wskazane jest badanie w kierunku mikrosporydiozy i kryptosporidiozy.
U chorego z gorączką i liczbą limfocytów CD4+ <100/µl należy wykonać posiew krwi w kierunku mykobakterii.
Ryzyko zakażenia CMV jest duże, gdy CD4+ <100/µl; w tych przypadkach wskazana jest endoskopia z pobraniem wycinków błony śluzowej w celu badania morfologicznego i badań wirusologicznych.
CMV infekcja PP - patogeneza ; lokalizacja ; obraz
W przewodzie pokarmowym zmiany – w postaci nadżerek i owrzodzeń błony śluzowej (znacznych rozmiarów w zaawansowanym ) i pogrubienia ściany – są zlokalizowane najczęściej w jelicie grubym i przełyku.
Owrzodzenia są następstwem zapalenia śródbłonka naczyniowego oraz zmian niedokrwiennych błony śluzowej.
CMV diag - HP i krew
HP - Metodami immunohistochemicznymi oraz hybrydyzacją in situ można wykazać CMV w obrębie jądra komórkowego w zmienionej chorobowo tkance oraz charakterystyczne wirusowe ciałka wtrętowe otoczone intensywnym odczynem zapalnym.
KREW identyfikacja wirusa w hodowli, badania serologiczne potwierdzające swoiste przeciwciała anty‑CMV badanie materiału genetycznego metodą PCR .
HSV - obraz diag
zapalenie błony śluzowej przełyku z licznymi, niewielkimi owrzodzeniami,
przyczyną uporczywego, przewlekłego zapalenia odbytu i odbytnicy z bolesnymi owrzodzeniami (także skóry w okolicy odbytowej)
Rozpoznanie: badanie endoskopowe z pobraniem wycinków i badaniem histologicznym, które wykazuje typowe wielojądrowe komórki oraz wtręty jądrowe. Rozpoznanie potwierdza wykrycie przeciwciał anty‑HSV w surowicy
salmonella shigiella i campylobacter w AIDS
najczęściej Salmonella enteritidis, rzadziej Salmonella typhimurium oraz Shigella flexneri. Powodują ostry nieżyt żołądkowo‑jelitowy
Campylobacter jejuni dość często (<30% przypadków) jest przyczyną przewlekłych, wielotygodniowych biegunek.
Sporadycznie zakażenie Salmonella, a dość często Campylobacter jejuni prowadzą u chorych z głębokim niedoborem odporności do bakteriemii i sepsy.
prątki niegruźlicze należące do MAC - jakie układu , jakie obajwy
Okres wylęgania wynosi od 4–6 tyg. do kilku lat.
U chorych na ADIS zakażenie MAC przebiega w postaci uogólnionej z zajęciem szpiku kostnego i węzłów chłonnych, zazwyczaj przy spadku liczby limfocytów CD4+ <50/µl. Najczęstsze objawy to gorączka i niedokrwistość.
W obrębie błony śluzowej jelita, najczęściej (~90%) w dwunastnicy, występuje pogrubienie fałdów i zmiany w postaci białych grudek o średnicy 1–3 mm (wynik gromadzenia się makrofagów w blaszce właściwej błony śluzowej). Zmiany przypominają obraz histologiczny choroby Whipple’a.
Kryptosporydioza - obraz kliniczny
najczęstsza przyczyna przewlekłej biegunki u chorych na AIDS. Pierwotniak C. parvum żyje wewnątrzkomórkowo, najczęściej w enterocytach (zwłaszcza jelita czczego).
gdy liczba limfocytów CD4+ wynosi <100/µl, rozwija się przewlekła biegunka z dużą utratą wody i elektrolitów
Kryptosporydioza diag

Mikrosporydioza obraz kliniczny diag
wewnątrzkomórkowych pasożytów, najczęściej przez Enterocytozoon bieneusi, Encephalitozoon intestinalis i Septala intestinalis.
Powodują biegunkę u 30–50% chorych, u których liczba limfocytów CD4+ wynosi <200/µl.
Rozpoznanie: wykrycie pierwotniaka w badaniu histologicznym wycinków błony śluzowej jelita (najlepiej w mikroskopie elektronowym); badanie kału na obecność spor (małe, 1–2 µm, trudne do odróżnienia od bakterii).
Cystoizosporoza: obraz kliniczny diag
zarażenia u ludzi powoduje Cystoisospora belli.
Namnaża się w enterocytach jelita cienkiego, powoduje zniszczenie nabłonka i kosmków jelitowych. Objawy kliniczne są podobne jak w przypadku kryptosporydiozy.
Rozpoznanie: kilkakrotne badanie mikroskopowe stolca na obecność pasożytów (rozmaz bezpośredni lub wybarwiony zielenią brylantową)
Kandydoza
występuje u 75–90% chorych na ADIS.
Zmiany w kandydozie mogą obejmować błony śluzowe jamy ustnej, gardła i przełyku. Kandydoza jamy ustnej przebiega pod 4 postaciami:
ostra rzekomobłoniasta (zwana pleśniawkami jamy ustnej)
ostra zanikowa
przewlekła przerostowa
przewlekła zanikowa.
Prawie połowa chorych nie ma objawów, u pozostałych występują dysfagia i ból zamostkowy.
Rozpoznanie: ustalane jest podczas badania endoskopowego.
Wymaz szczoteczkowy z następowym badaniem mikrobiologicznym (hodowla i antymykogram) pozwalają na identyfikację grzyba.
Ze względu na szerokie rozpowszechnienie gatunków z rodzaju Candida samo wyhodowanie grzyba z materiału biologicznego (bez objawów chorobowych) nie może być podstawą rozpoznania grzybicy i wdrażania terapii.
kryptokokoza (Cryptococcus neoformans)
jest najczęstszym uogólnionym zakażeniem grzybiczym w zaawansowanym (CD4+ <100/µl).
Zakażenie drogą oddechową prowadzi do zapalenia opon mózgowo‑rdzeniowych i mózgu.
Histoplazmoza może prowadzić również do zajęcia wątroby, na co wskazują nieprawidłowe wyniki biochemicznych wskaźników czynności wątroby.
Rozpoznanie: bezpośrednie badanie mikroskopowe materiału z miejsca podejrzanego oraz posiew i identyfikacja mykologiczna.
Salmonella spp. Lecz
cyprofloksacyna lewofloksacyna
Campylobacter jejuni – leczenie
azytromycyna
MAC leczenie
leczenie skojarzone ≥2‑lekowe: klarytromycyna albo azytromycyna oraz etambutol
Kryptosporydioza leczenie
nitazoksanid lub paromomycyna
Mikrosporydioza: leczenie
albendazol
lub w przypadku zarażenia Trachipleistophora lub Anncaliia leczenie skojarzone – itrakonazol i albendazol
Cystoizosporoza: leczenie
kotrimoksazol
kwestia wchłaniania się zbiorników po OZT (czyyniki ryzyka pozostania)

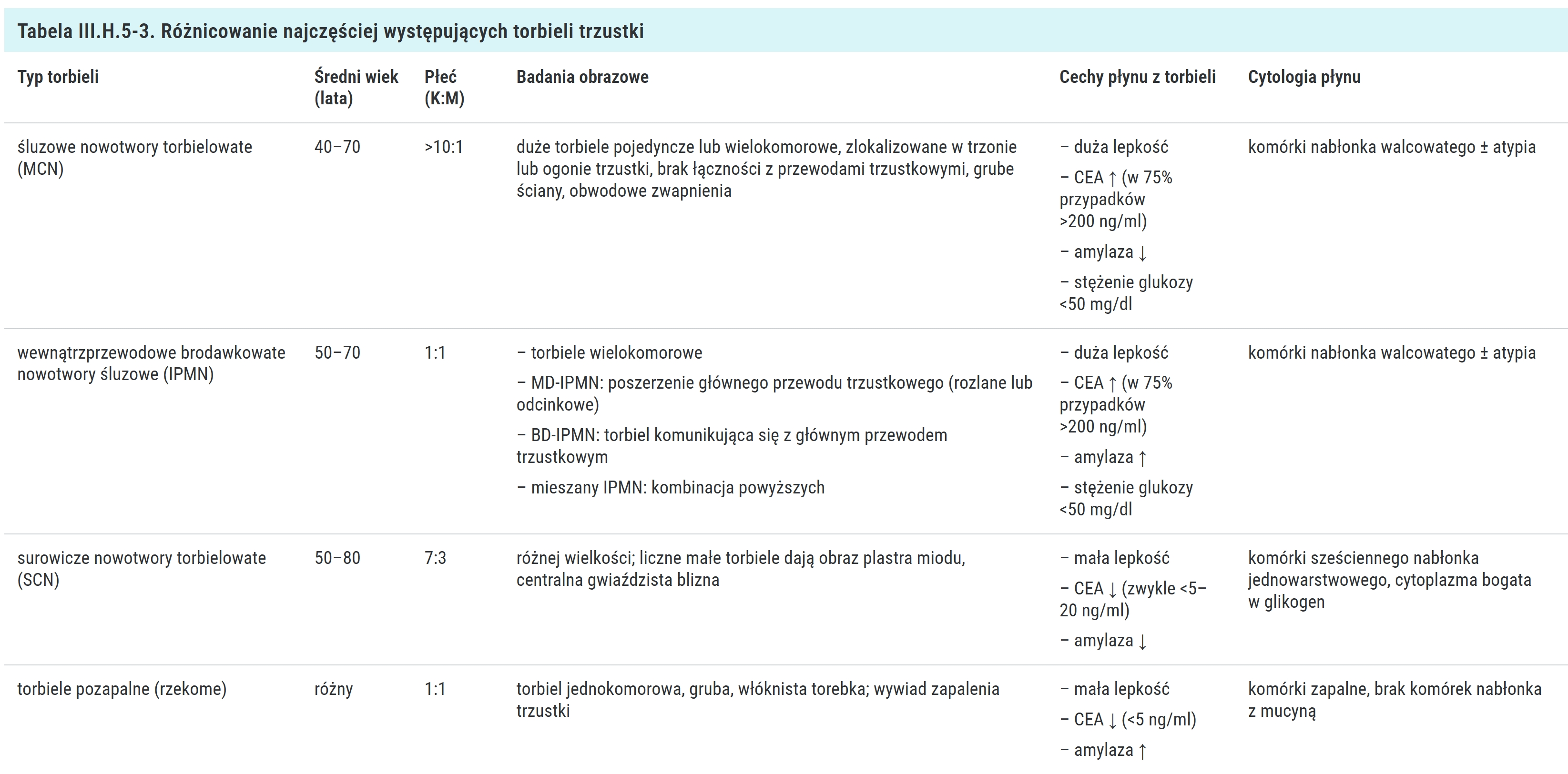
tabelka różnicowanie torbieli
Leczenie farmakologiczne trobieli pozapalnych
W leczeniu przetrwałych objawowych torbieli pozapalnych komunikujących się z przewodem trzustkowym można rozważyć zastosowanie oktreotydu (analogu somatostatyny o przedłużonym działaniu) przed lub razem z drenażem endoskopowym (100–250 mg s.c. co 8–12 h) w celu zmniejszenia wydzielania soku trzustkowego
tętniak rzekomy torbieli pozapalnyc
– powstaje wskutek uszkodzenia tętnic okołotrzustkowych (śledzionowej, żołądkowo‑dwunastniczej, trzustkowo‑dwunastniczych, wątrobowych) z utrzymaniem drożności pomiędzy tętnicą a światłem torbieli. W badaniu doplerowskim można uwidocznić przepływ wewnątrz torbieli. Pęknięcie tętniaka rzekomego może powodować krwawienie (w zależności od lokalizacji) do jamy otrzewnej lub przestrzeni zaotrzewnowej; rzadkim powikłaniem tętniaka jest krwawienie do dwunastnicy przez przewód trzustkowy.
torbiele npl trzustki %
wewnątrzprzewodowe brodawkowate nowotwory śluzowe (intraductal papillary mucinous neoplasms – IPMN) – stanowią ~40%
śluzowe nowotwory torbielowate (mucinous cystic neoplasms – MCN) – stanowią ~25%;
surowicze nowotwory torbielowate (serous cystic neoplasms – SCN) – stanowią ~20%;
lite nowotwory rzekomobrodawczakowate (<10%
torbielowate nowotwory endokrynne (<10%)
gruczolakorak przewodowy ze zwyrodnieniem torbielowatym <1%
torbielakogruczolakorak z komórek pęcherzykowych (<1%).
W przypadku IPMN według międzynarodowych wytycznych z Kyoto z 2024 r. cechami wysokiego ryzyka występowania dysplazji dużego stopnia lub raka są:
żółtaczka u chorego z torbielą w głowie trzustki
wzmacniające guzki o średnicy ≥5 mm w ścianie
lita struktura w świetle torbieli
poszerzenie głównego przewodu trzustkowego ≥10 mm
dodatni lub podejrzany wynik badania cytologicznego
W przypadku IPMN według międzynarodowych wytycznych z Kyoto z 2024 r. cechy niepokojące to:
ostre zapalenie trzustki (OZT) w wywiadzie
zwiększone stężenie CA 19‑9 w surowicy
pojawienie się lub zaostrzenie cukrzycy w ostatnim roku
średnica torbieli ≥30 mm
wzmacniające guzki o średnicy <5 mm w ścianie torbieli
pogrubiałe lub wzmacniające ściany torbieli
nagła zmiana średnicy przewodu trzustkowego z dystalnym zanikiem miąższu trzustki
poszerzenie głównego przewodu trzustkowego do 5–9,9 mm
powiększanie się torbieli o ≥2,5 mm/rok
powiększenie sąsiednich węzłów chłonnych
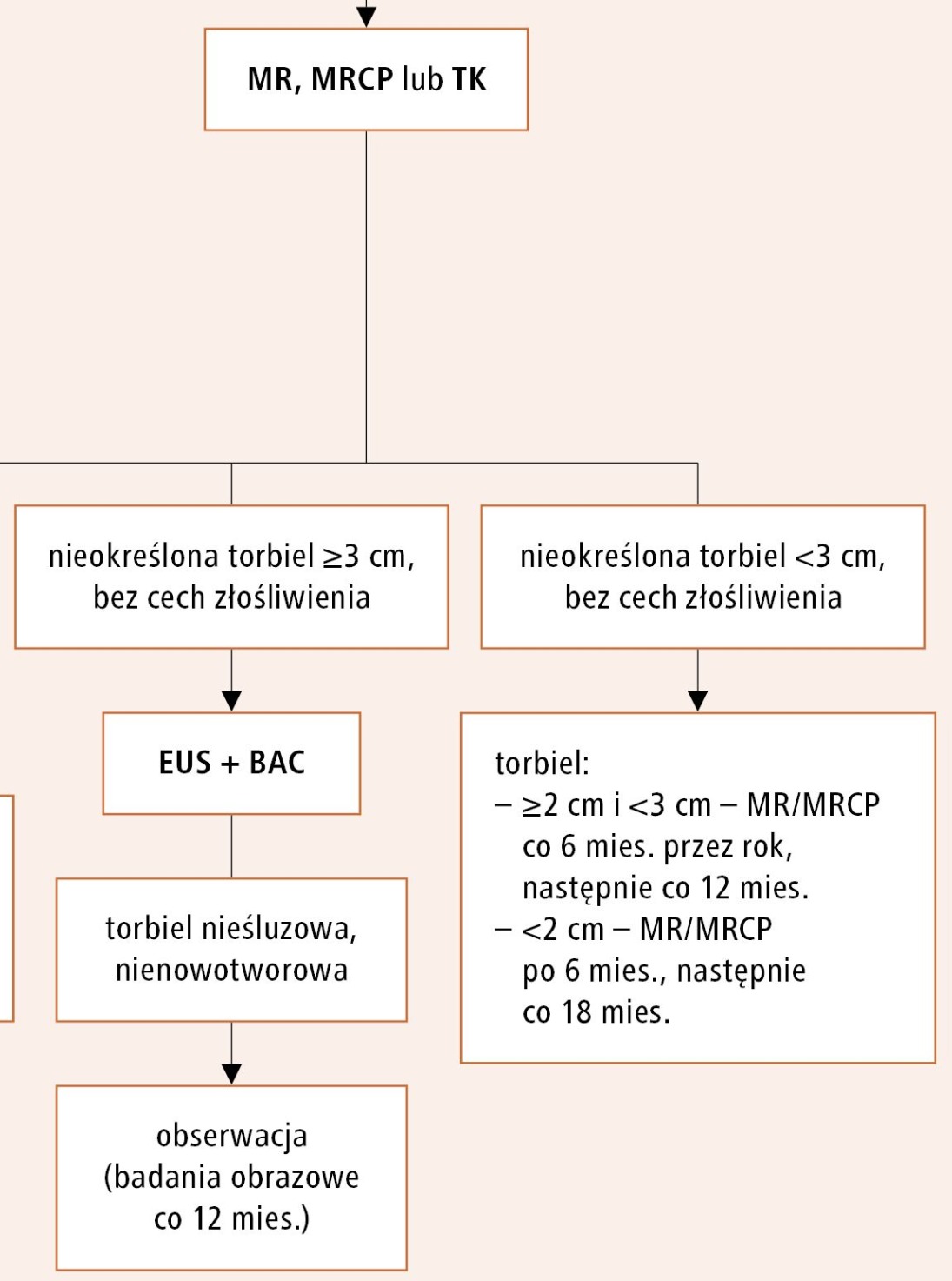
Algorytm postępowania z nieokreśloną torbielą po MR
Według wytycznych z Kyoto leczenie operacyjne IPMN należy rozważyć, jeśli
występuje ≥1 z cech wysokiego ryzyka dysplazji dużego stopnia lub raka
W pozostałych przypadkach leczenie operacyjne rozważyć, jeśli występuje ≥1 z cech niepokojących i ≥1 z poniższych:
nawraca OZT (co pogarsza jakość życia chorego)
występują liczne cechy niepokojące (co zwiększa prawdopodobieństwo dysplazji dużego stopnia lub raka)
u młodych chorych (dobrych kandydatów do operacji).
Sam wymiar torbieli ≥30 mm, bez innych objawów, nie jest wystarczającym wskazaniem do leczenia operacyjnego.
Nadzór IPMN po operacji
w razie raka lub dysplazji dużego stopnia – co 6 mies. przez 5 lat
w przypadku dysplazji małego stopnia – co 12 mies. przez 5 lat