CM8: Utilisation du gras (lipolyse / β-ox / lipogenèse)
1/10
There's no tags or description
Looks like no tags are added yet.
Name | Mastery | Learn | Test | Matching | Spaced | Call with Kai |
|---|
No analytics yet
Send a link to your students to track their progress
11 Terms
Lipolyse et β-oxydation
Thème 1 — Nature et composition
Que sont les TG exogènes et quelle est leur composition chimique ?
Quelle est la source de ces TG exogènes ?
Thème 2 — Dégradation enzymatique
Où et par quelles enzymes les TG exogènes sont-ils hydrolysés ?
Quel est le rôle des sels biliaires dans cette lipolyse ?
Quelles sont les étapes successives d’hydrolyse des TG jusqu’aux produits finaux ?
Thème 3 — Absorption et devenir métabolique
Quels sont les produits finaux absorbés au niveau intestinal ?
Par quel mécanisme ces produits sont-ils absorbés ?
Quel est le sort métabolique du glycérol et des acides gras après absorption ?
Sous quelle forme de transport les acides gras sont envoyés vers les tissus périphériques ?
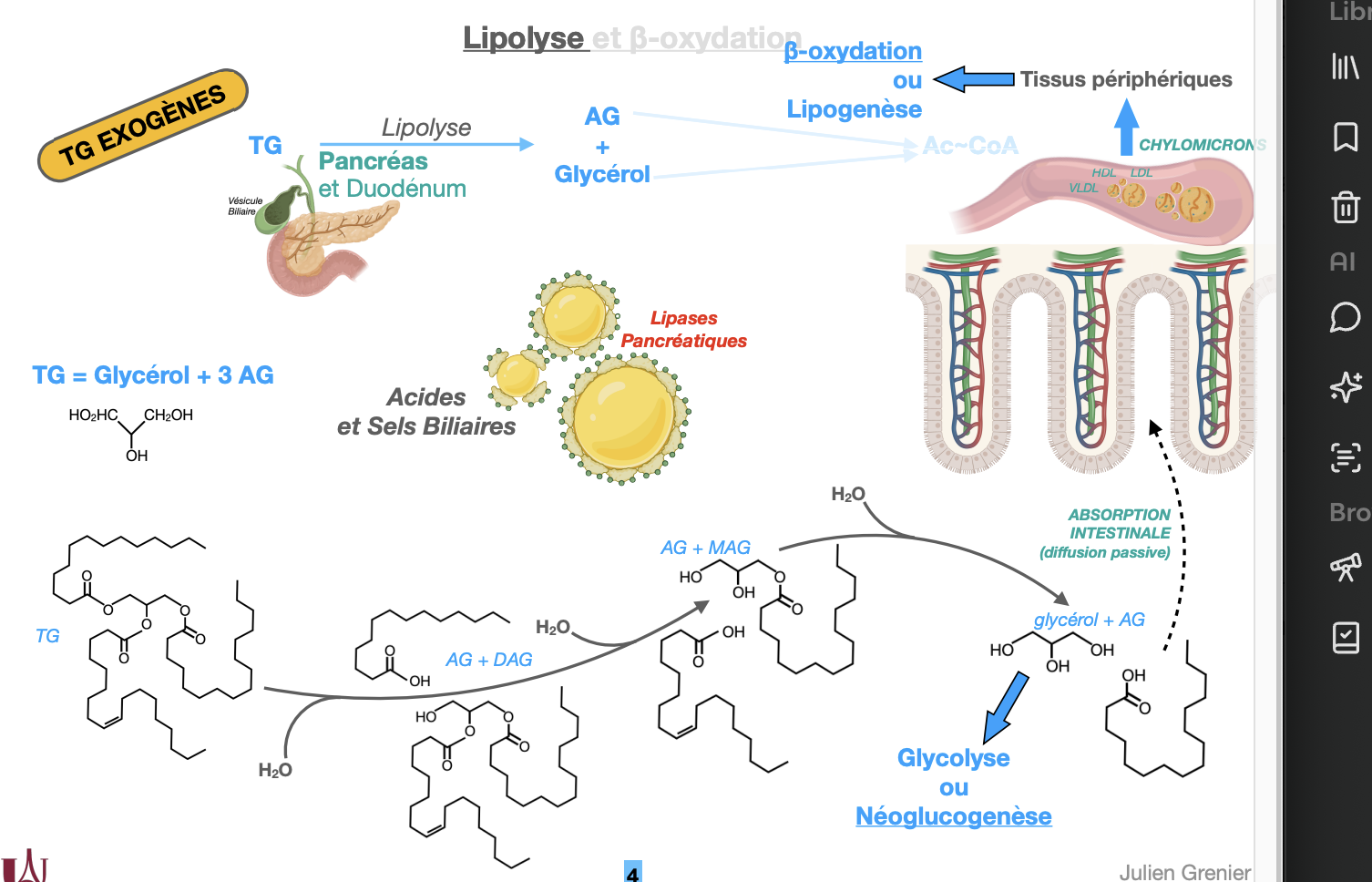
Thème 1 — Nature et composition
Les triglycérides (TG) sont des esters formés d’un glycérol lié à trois acides gras (AG).
Les TG exogènes proviennent de l’alimentation et sont émulsionnés dans le duodénum avant d’être hydrolysés.
Thème 2 — Dégradation enzymatique
L’hydrolyse des TG se déroule dans la lumière intestinale, sous l’action des lipases pancréatiques (sécrétées par le pancréas).
Les sels biliaires, produits par le foie et stockés dans la vésicule biliaire, émulsionnent les lipides en petites gouttelettes → augmentent la surface d’action des lipases.
L’hydrolyse se fait en plusieurs étapes :
TG → AG + DAG (diacylglycérol)
DAG → AG + MAG (monoacylglycérol)
MAG → glycérol + AG
➜ catalysée par les lipases pancréatiques et l’eau (H₂O).
Thème 3 — Absorption et devenir métabolique
Les produits finaux absorbés sont les acides gras libres (AG) et le glycérol.
L’absorption se fait par diffusion passive à travers la membrane des entérocytes de l’intestin grêle.
Le glycérol rejoint le foie, où il peut entrer dans la glycolyse (si besoin d’énergie) ou la néoglucogenèse (production de glucose).
Les acides gras, eux, sont soit oxydés (β-oxydation) pour produire de l’énergie, soit réestérifiés pour la lipogenèse.Les AG et le glycérol sont reformés en TG dans les entérocytes, puis emballés dans des chylomicrons qui passent dans la circulation lymphatique avant d’atteindre les tissus périphériques.
Thème 1 — Localisation et rôle
Où a lieu la lipolyse des TG endogènes ?
Quel est le rôle principal de cette lipolyse dans l’organisme ?
Dans quelles conditions physiologiques cette voie est-elle activée ?
Thème 2 — Mécanisme enzymatique
Quelles sont les enzymes successives intervenant dans la lipolyse des TG endogènes ?
Quel est le rôle de la PKA dans ce processus ?
Quel est le rôle de la périlipine et comment est-elle impliquée dans la régulation ?
Quelles sont les étapes chimiques successives de l’hydrolyse du TG ?
Thème 3 — Produits et devenir métabolique
Quels sont les produits finaux de la lipolyse ?
Que devient le glycérol libéré ?
Que deviennent les acides gras libérés ?
Sous quelle forme de transport les acides gras circulent-ils dans le sang ?
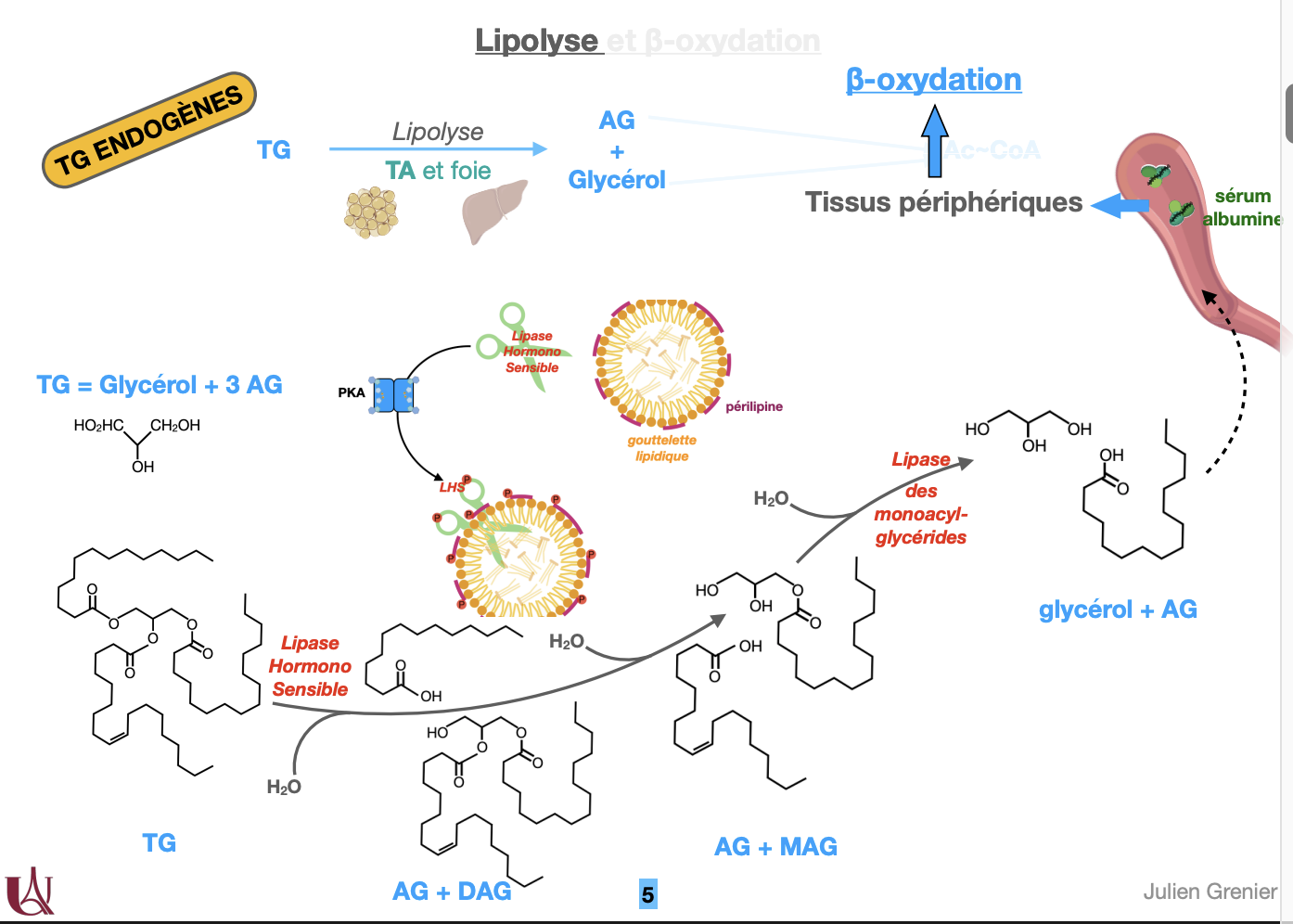
Thème 1 — Localisation et rôle
La lipolyse des TG endogènes se déroule principalement dans le tissu adipeux (TA) et dans une moindre mesure dans le foie.
Elle a pour but de mobiliser les réserves énergétiques sous forme de triglycérides stockés dans les adipocytes afin de fournir des acides gras libres aux tissus énergétiques.
Elle est activée en situation de jeûne, stress ou exercice physique, sous l’action d’hormones comme l’adrénaline, la noradrénaline, le glucagon ou la cortisolémie élevée.
Thème 2 — Mécanisme enzymatique
Les enzymes impliquées sont :
Lipase Hormono-Sensible (LHS) → hydrolyse le TG en DAG + AG ;
Lipase des Diacylglycérols (DAG lipase) → hydrolyse le DAG en MAG + AG ;
Lipase des Monoacylglycérols (MAG lipase) → hydrolyse le MAG en glycérol + AG.
La PKA (protéine kinase A), activée par l’AMPc, phosphoryle la LHS et la périlipine, ce qui active la lipolyse.
La périlipine entoure les gouttelettes lipidiques et empêche l’accès des lipases à leurs substrats. Sa phosphorylation par la PKA provoque un repliement qui rend les TG accessibles à la LHS.
Les étapes d’hydrolyse successives sont :
TG + H₂O → AG + DAG
DAG + H₂O → AG + MAG
MAG + H₂O → AG + glycérol
Thème 3 — Produits et devenir métabolique
Les produits finaux sont le glycérol et les acides gras libres (AG).
Le glycérol rejoint le foie, où il entre dans la néoglucogenèse ou la glycolyse selon l’état énergétique.
Les acides gras sont libérés dans la circulation, transportés vers les tissus périphériques (muscle, cœur, foie) où ils subissent la β-oxydation pour produire de l’acétyl-CoA et donc de l’énergie.
Les AG circulent liés à la sérum-albumine, protéine plasmatique qui les stabilise et transporte dans le sang.
Lipolyse
🔹 PARTIE QUESTIONS
Quelles sont les étapes enzymatiques principales du devenir du glycérol libéré lors de la lipolyse ?
Sous quelle forme le glycérol entre-t-il dans les voies métaboliques centrales, et quelles voies peut-il emprunter ?
Le glycérol est d’abord phosphorylé par la glycérol kinase (dans le foie et le rein) pour former du glycérol-3-phosphate (G3P) en consommant 1 ATP.
Le glycérol-3-phosphate déshydrogénase (glycérol 3-P DH) oxyde ensuite le G3P en DHAP (dihydroxyacétone phosphate) en réduisant un NAD⁺ en NADH,H⁺.Le DHAP est la forme métabolique intégrée dans les voies énergétiques.
→ Il peut entrer dans la glycolyse (converti en GA3P puis en pyruvate → Acétyl-CoA) ou dans la néoglucogenèse (retransformé en glucose dans le foie et le rein).Le foie et les reins sont les organes principaux utilisant le glycérol pour la néoglucogenèse, car ce sont les seuls à exprimer la glycérol kinase et les enzymes complètes de la voie néoglucogénique.
β-oxydation: devenir des AG
Quelles étapes permettent à un acide gras cytosolique d’entrer en β-oxydation mitochondriale ?
Quelles sont les 4 réactions d’un cycle de β-oxydation et leurs cofacteurs ?
Quels sont les produits énergétiques formés par cycle et le bilan pour un AG saturé à n carbones (exemple palmitate C16) ?
Activation + navette carnitine :
Activation (cytosol/face externe mitochondrie) par acyl-CoA synthétase : AG + CoA-SH + ATP → Acyl-CoA + AMP + PPi.
Transport par la carnitine (CPT-I → translocase → CPT-II) : passage de l’acyl-carnitine à travers la membrane interne puis régénération de l’acyl-CoA dans la matrice.
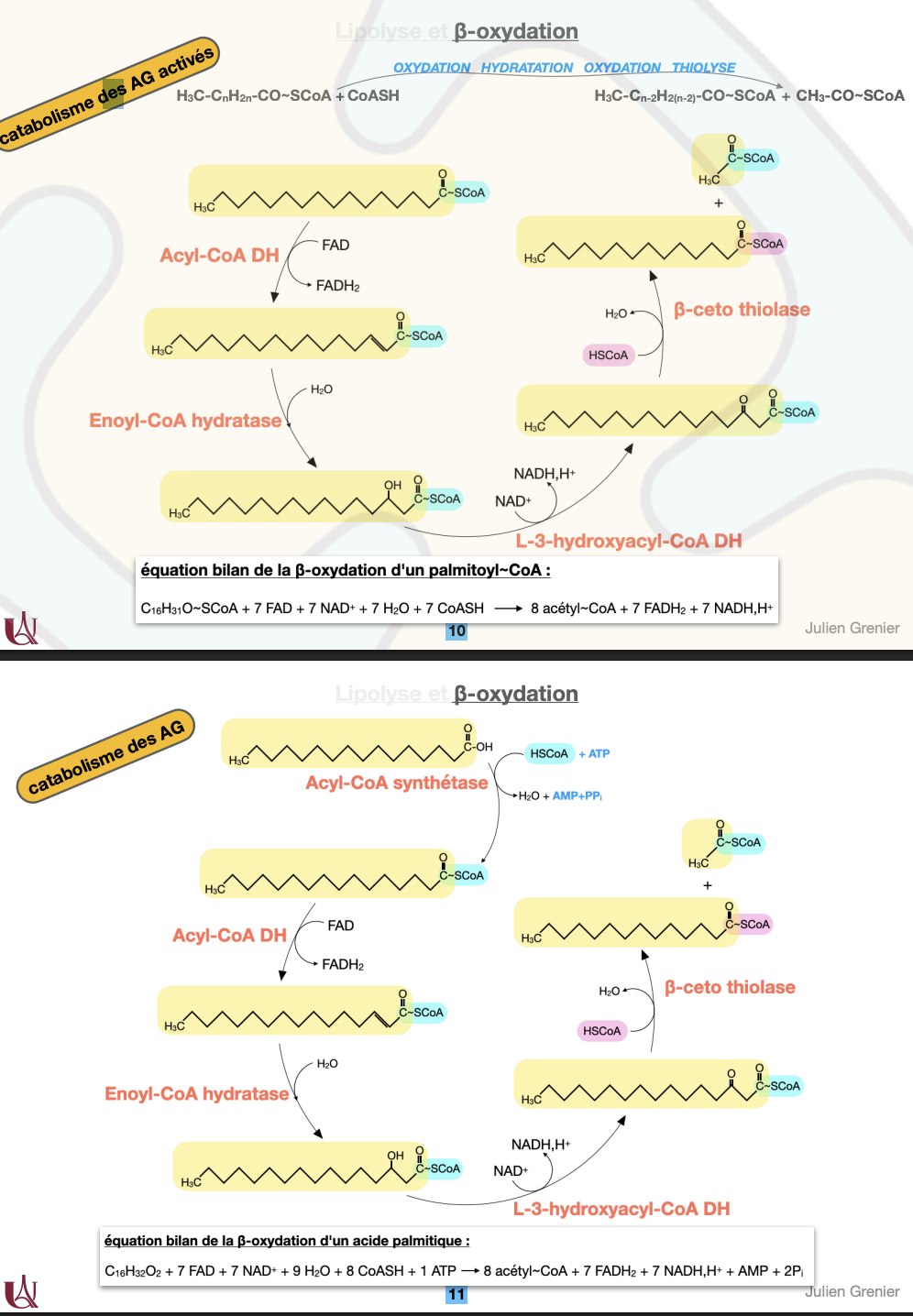
Cycle de β-oxydation (matrice) :
Acyl-CoA déshydrogénase : oxydation → trans-Δ²-énoyl-CoA, FAD → FADH₂.
Énoyl-CoA hydratase : hydratation → L-3-hydroxyacyl-CoA.
L-3-hydroxyacyl-CoA déshydrogénase : oxydation, NAD⁺ → NADH,H⁺, produit 3-cétoacyl-CoA.
β-céto-thiolase : thiolyse par CoA-SH → acyl-CoA raccourci de 2C + acétyl-CoA.
Produits par cycle : 1 acétyl-CoA + 1 FADH₂ + 1 NADH (et un acyl-CoA –2C).
Bilan pour un AG saturé Cₙ :Nombre de cycles = (n/2) – 1, acétyl-CoA = n/2.
Ex. palmitate (C16) : 7 cycles → 8 acétyl-CoA, 7 FADH₂, 7 NADH (grand rendement énergétique après TCA + OXPHOS).
β-oxydation: activation des AG et dressage des AG activés
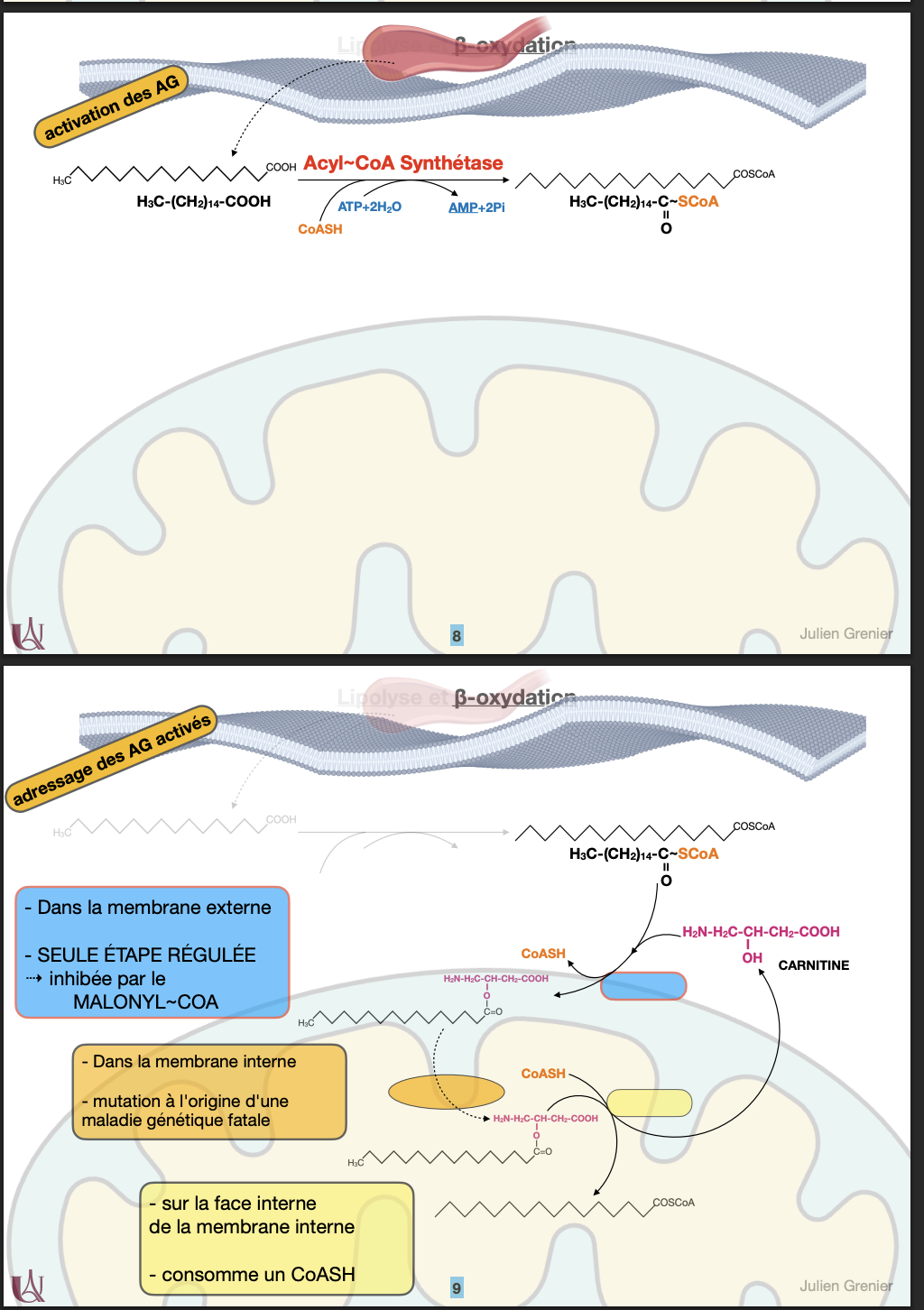
β-oxydation: catabolisme des AG activés
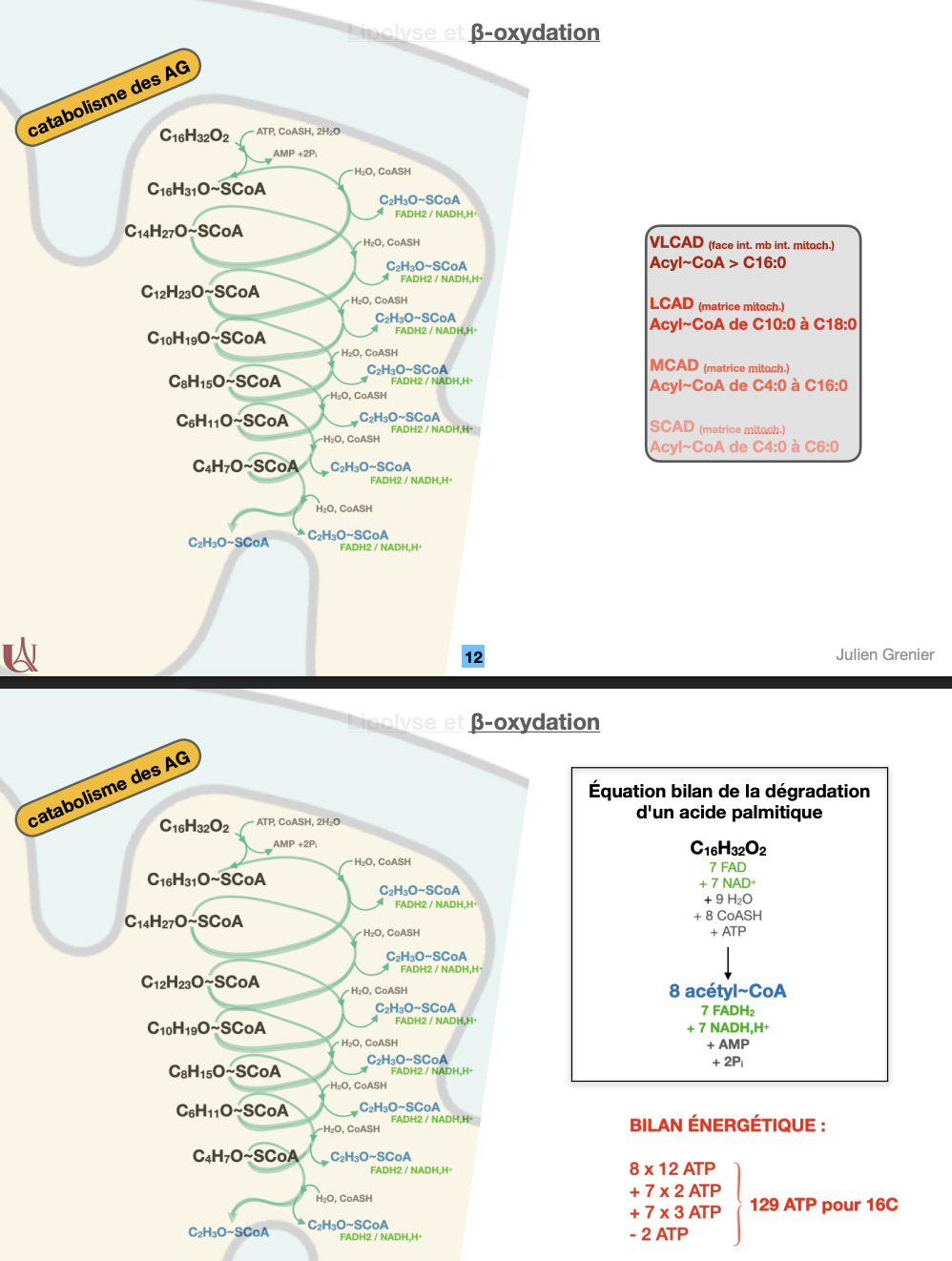
β-oxydation: régulation
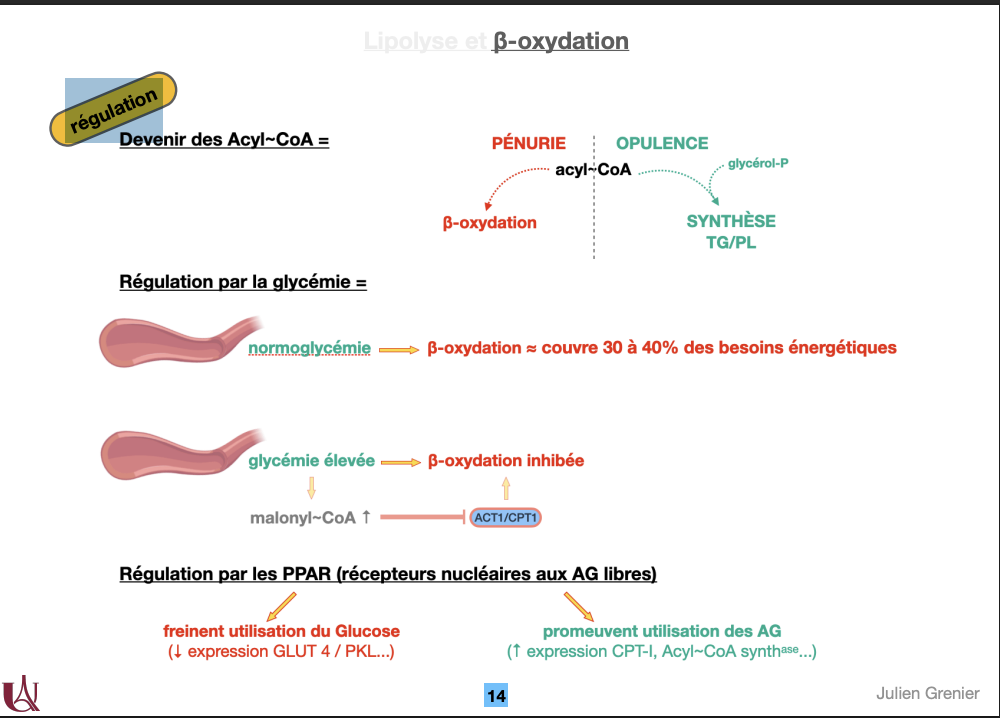
Synthèse des acides gras et lipogenèse
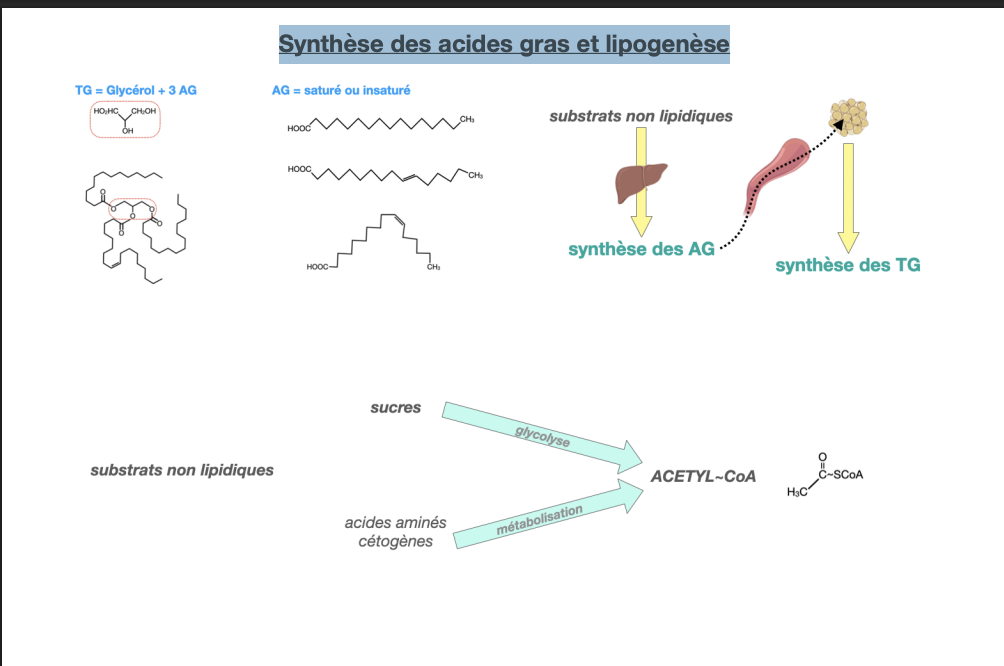
Synthèse des acides gras
🔹 PARTIE QUESTIONS
Quelles sont les trois grandes étapes de la synthèse des acides gras à partir du glucose, et quelles enzymes-clés y participent ?
Quelle est la réaction catalysée par l’acétyl-CoA carboxylase (ACC), et comment cette enzyme est-elle régulée ?
Quelles sont les réactions successives catalysées par le complexe acide gras synthase (AGS), et quel est le bilan global d’élongation d’un acide gras ?
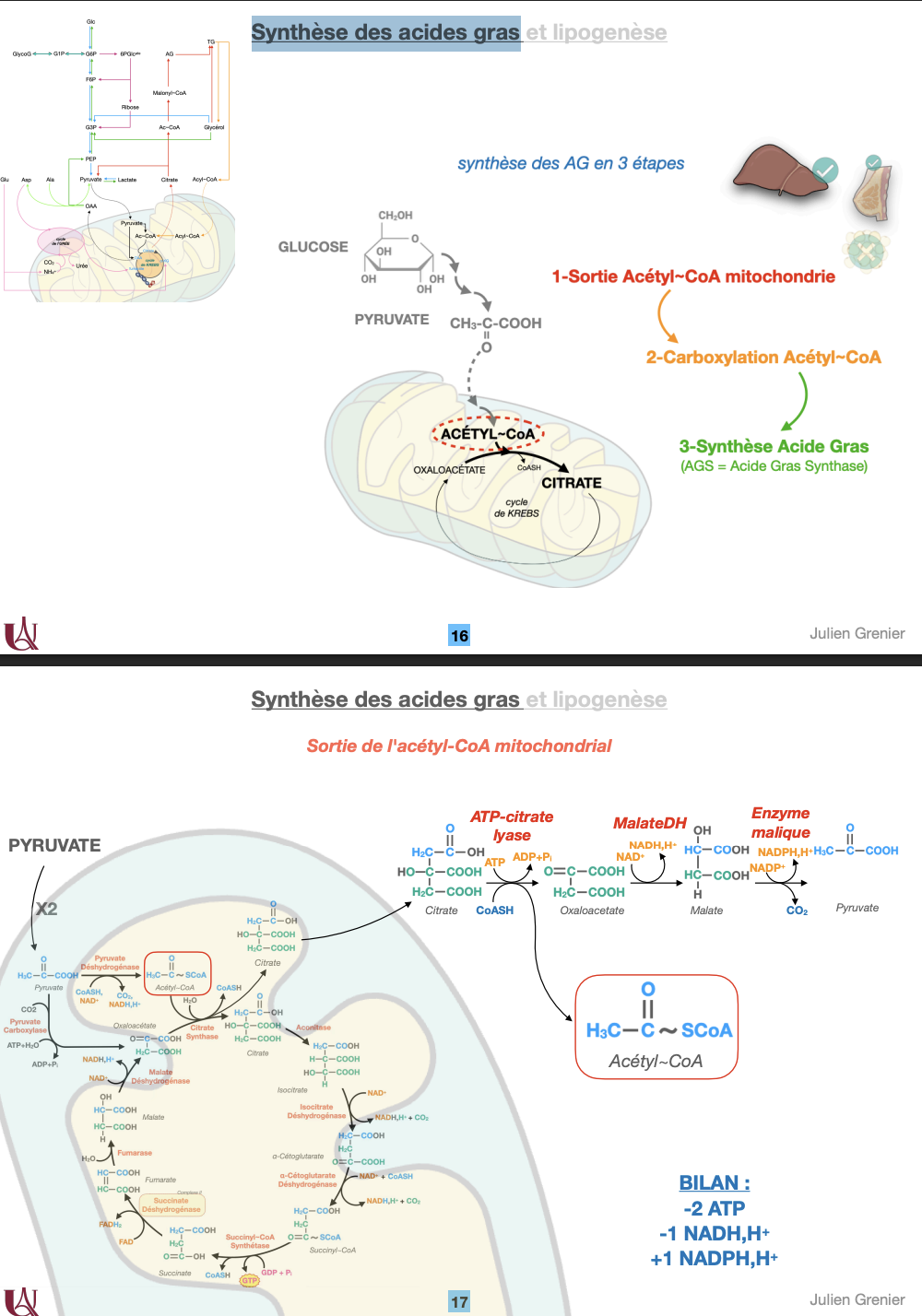
Étape 1 : Sortie de l’acétyl-CoA mitochondrial.
→ L’acétyl-CoA est transformé en citrate (acétyl-CoA + oxaloacétate) qui diffuse vers le cytosol, puis reconverti en acétyl-CoA par l’ATP-citrate lyase (consomme 1 ATP).
→ L’oxaloacétate est réduit en malate par la malate déshydrogénase, puis le malate est décarboxylé en pyruvate par l’enzyme malique, libérant un NADPH,H⁺ nécessaire à la synthèse.Étape 2 : Carboxylation de l’acétyl-CoA en malonyl-CoA.
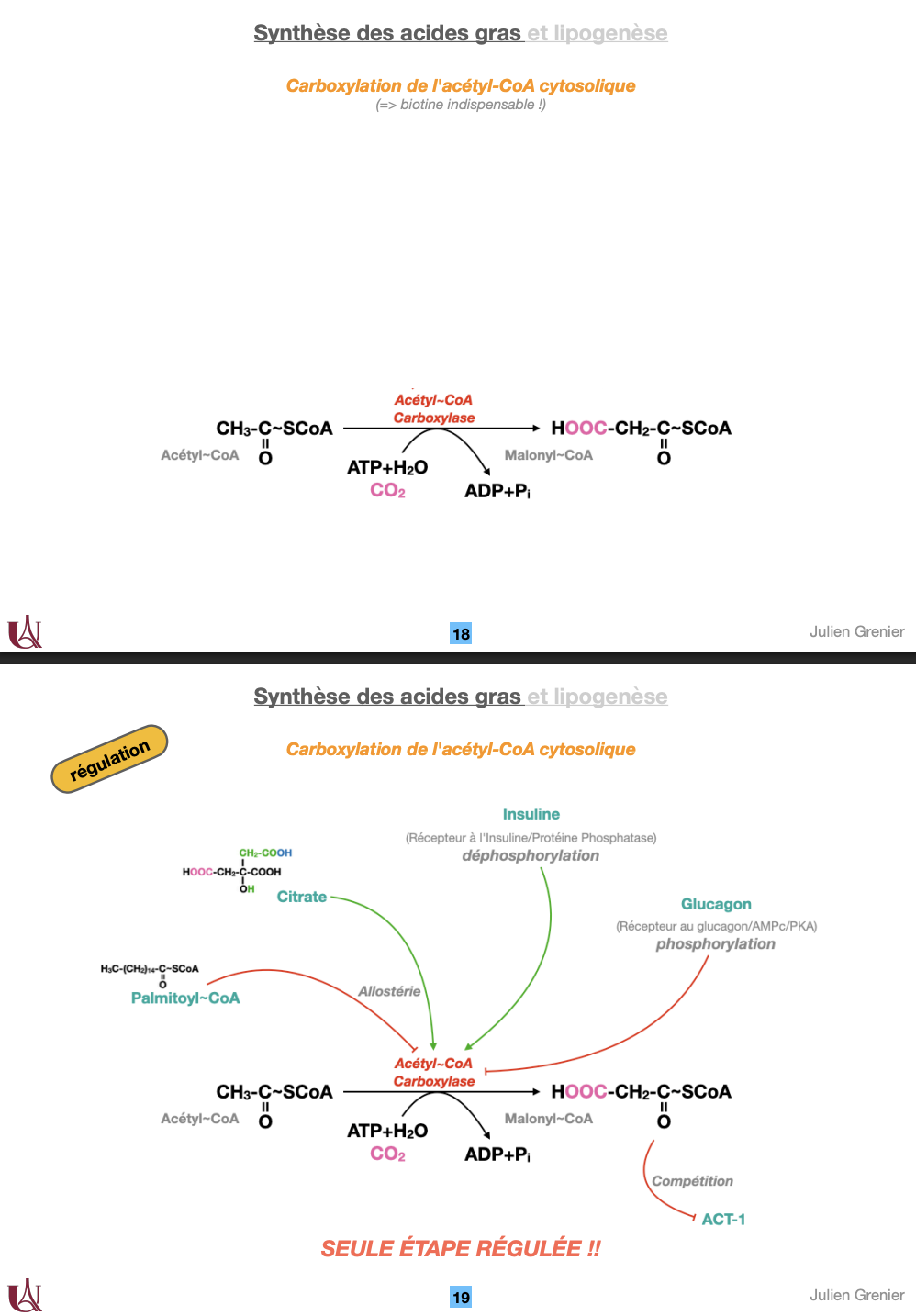
→ Catalysée par l’acétyl-CoA carboxylase (ACC), nécessitant ATP, CO₂ et biotine.
→ Produit : malonyl-CoA, donneur de 2C pour la synthèse.**Étape 3 : Synthèse des acides gras par l’acide gras synthase (AGS) dans le cytosol.
→ L’AGS assemble l’acétyl-CoA et le malonyl-CoA pour former un acide gras saturé (palmitate C16).
Réaction ACC :
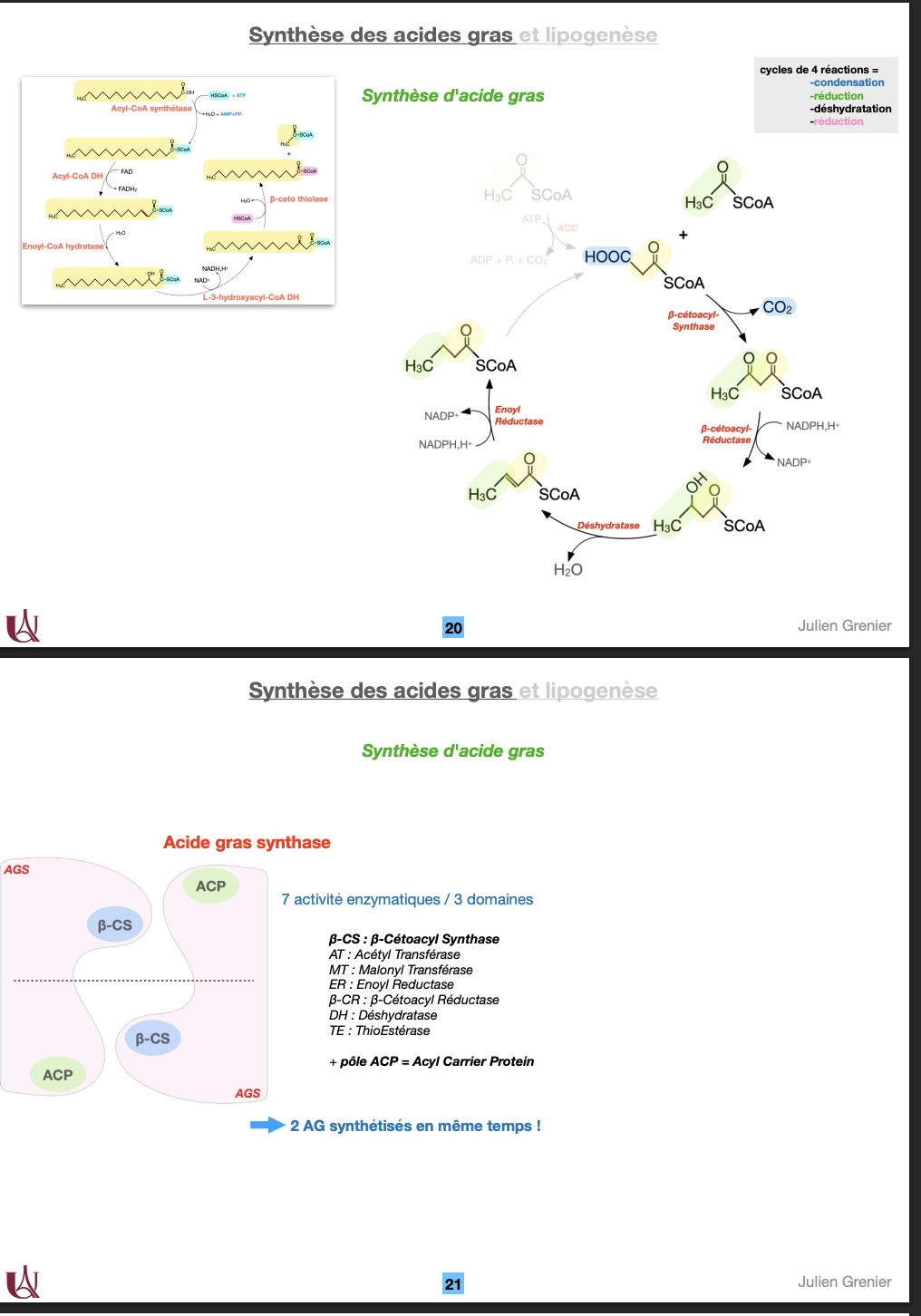
Acétyl-CoA + CO₂ + ATP → Malonyl-CoA + ADP + PiRégulation :
Activation allostérique : par le citrate (signe d’un excès énergétique).
Inhibition allostérique : par le palmitoyl-CoA (produit final).
Régulation hormonale :
Insuline active ACC (déphosphorylation via phosphatase).
Glucagon / adrénaline inhibent ACC (phosphorylation via PKA/AMPK).
→ C’est l’unique étape régulée de la lipogenèse.
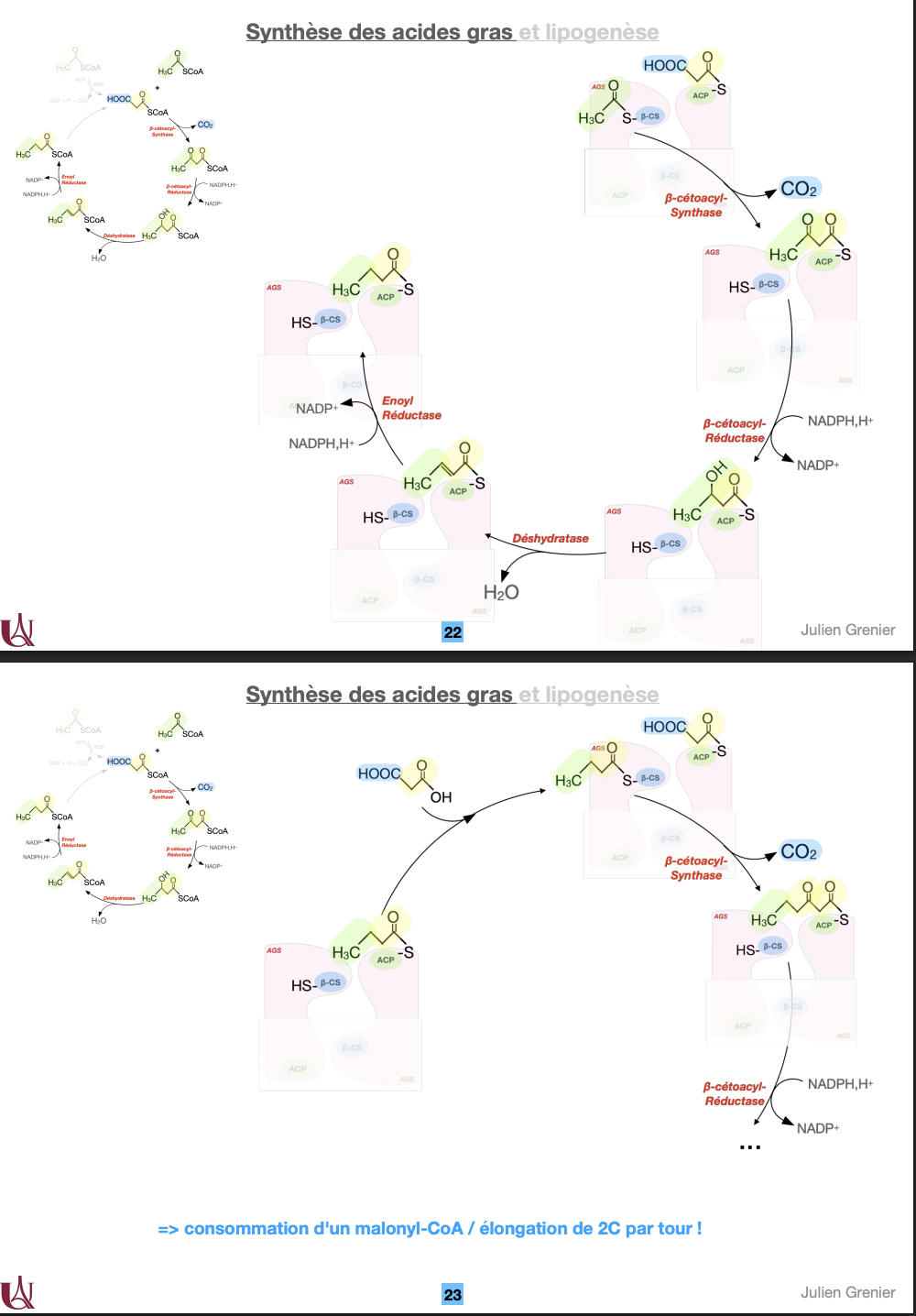
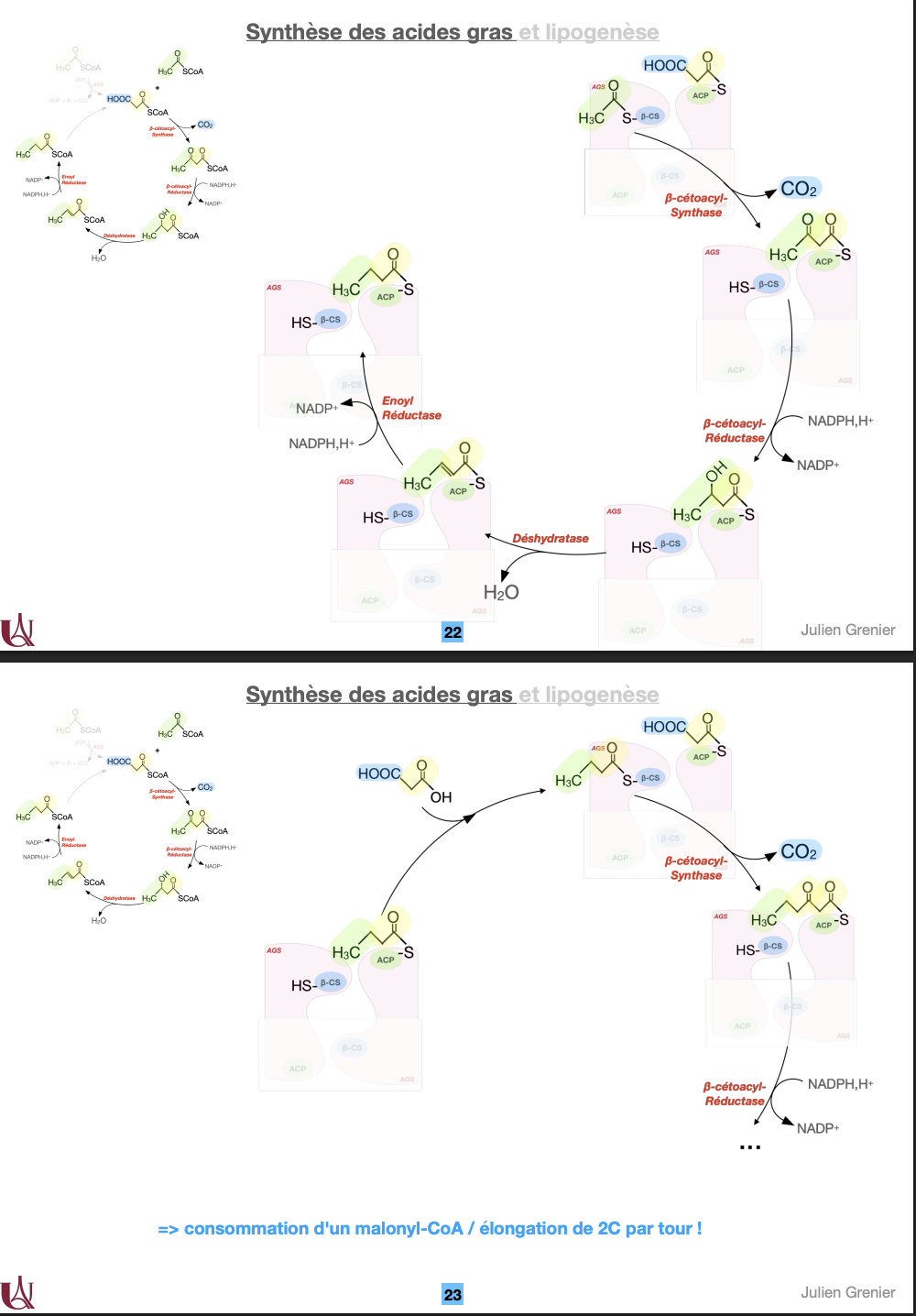
Cycle enzymatique de l’AGS (4 réactions répétées) :
1⃣ Condensation (β-cétoacyl synthase) : acétyl-CoA + malonyl-CoA → β-cétoacyl-ACP + CO₂.
2⃣ Réduction (β-cétoacyl réductase) : NADPH → NADP⁺.
3⃣ Déshydratation (déshydratase) : élimination de H₂O.
4⃣ Réduction finale (énoyl réductase) : NADPH → NADP⁺ → acyl-ACP allongé de 2C.
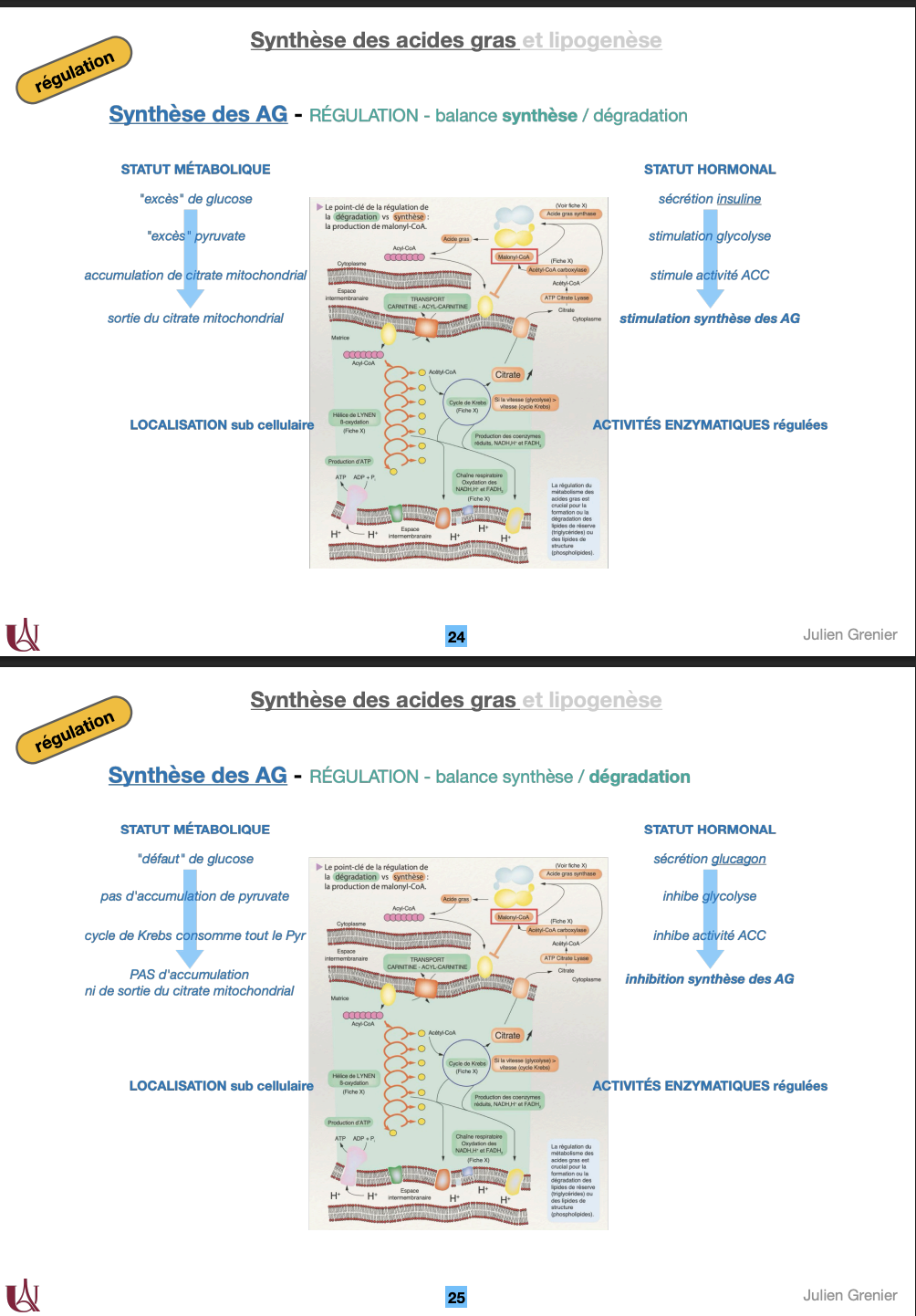
→ Chaque cycle consomme 1 malonyl-CoA et 2 NADPH,H⁺ → élongation de +2 carbones par tour.
→ Le palmitate (C16) est le produit final de la synthèse, ensuite libéré par une thioestérase.
Bilan global :
8 acétyl-CoA + 7 ATP + 14 NADPH → palmitate (C16:0) + 14 NADP⁺ + 8 CoA + 7 ADP + 7 Pi + 6 H₂O.
Lipogenèse
Quelles sont les grandes étapes enzymatiques de la synthèse des triglycérides (TG) à partir du glycérol et des acides gras activés ?
Comment la lipogenèse et la lipolyse sont-elles régulées par les hormones insuline et adrénaline ?
Quelle est la différence fonctionnelle entre le tissu adipeux profond et le tissu adipeux sous-cutané vis-à-vis de la régulation de la lipolyse ?
La synthèse des triglycérides se déroule principalement dans le foie, les intestins et le tissu adipeux.
Le glycérol est phosphorylé en glycérol-3-phosphate (G3P) par la glycérol kinase (foie) ou par la glycérol-3-phosphate déshydrogénase (à partir du DHAP, dans les tissus adipeux).
Les acides gras sont activés en acyl-CoA par l’acyl-CoA synthétase (ATP + CoA → AMP + PPi).
Les étapes successives catalysées par des acyl-transférases ajoutent deux chaînes acyles au G3P pour former un acide phosphatidique, ensuite déphosphorylé en diacylglycérol (DAG) par une phosphatase, puis estérifié une troisième fois → triacylglycérol (TG).
Les TG sont ensuite incorporés dans les VLDL (foie) ou stockés dans des gouttelettes lipidiques (tissu adipeux).
Insuline → favorise la lipogenèse :
Stimule la translocation de GLUT4 (entrée du glucose).
Active la synthèse de glycérol-3-phosphate et l’expression des enzymes lipogéniques (lipoprotéine lipase, acyl-CoA transférase).
Active des phosphatases qui déphosphorylent et inhibent la lipase hormono-sensible (LHS), réduisant la lipolyse.
Adrénaline → stimule la lipolyse via récepteurs β₁/β₂ adrénergiques (activation de la PKA → phosphorylation de la LHS et de la périlipine).
Inversement, l’activation des récepteurs α₂ adrénergiques inhibe la lipolyse (frein sur l’AMPc et la PKA).
Le tissu adipeux profond (viscéral) possède une densité élevée de récepteurs β → favorise la lipolyse sous l’effet de l’adrénaline.
Le tissu adipeux sous-cutané contient davantage de récepteurs α₂ → inhibe la lipolyse.
→ Ainsi, la répartition du tissu adipeux détermine la sensibilité hormonale et l’équilibre entre stockage (lipogenèse) et mobilisation (lipolyse) des graisses.